KONSTRUKSI VEKTOR EKSPRESI GEN UNWK
MENGELIMINASI GEN PENYELEKSI
ANTIBIOTIK
PADA
TANAMAN PAD1 (Ovza
sativaL.)
TRANSGENIK
AGUS RACHMAT
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN
SUMBER INFORMASIDengan ini saya menyatakan bahwa tesis Konstruksi Vektor Ekspresi
Gen untuk Mengeliminasi Gen Penyeleksi Antibiotik pada Tanaman Padi (@a
sativa L.) Transgenik adalah karya saya sendiri dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Surnber informasi yang berasal atau
dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain
telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian
akhir tesis ini.
Bogor, Mei 2006
Agus Rachmat
ABSTRAK
AGUS RACHMAT. Konstruksi Vektor Ekspresi Gen untuk Mengeliminasi Gen Penyeleksi Antibiotik pada Tanaman Padi (Oryza sativa L.) Transgenik. Dibimbing oleh SUHARSONO dan INEZ H.S. LOEDIN.
Gen penanda seleksi diperlukan untuk proses seleksi tanaman transgenik, tetapi tidak diperlukan setelah tanaman transgenik d i i i l k a n . E l i i i gen ini dapat dilakukan dengan memisahkan gen ini dari gen sasaran pada saat integrasi ke dalam genom tanaman. Penelitian ini bertujuan
untuk
mengkonstruksi vektor ekspresi gen yang dapat m e n g e l i i a s i gen penanda seleksi resistensi terhadap antibiotika pada tanaman padi transgenik. Ada dua pendekatan yang dilakukan pertama dengan menggunakan double T-DNA dalam satu vektor biner clan kedua menggunakan dua hang yang membawa gen sasaran dan gen penanda seleksi secara terpisah. Vektor biner dengan double T-DNA yang masing-masing mengandung gen cryIAb dan gen hpt (p2TDNAqIAb), dan vektor b i e r yang mengandung gen penyandi biosintesis asam salisilat (pC12SA) dan vektor biner lain yang membawa gen hpt (pC1300 hpt intron) telah berhasil dikonstruksi. Vektor-vektor ini telah digunakan untuk melakukan transformasi genetik kalus melalui A. tumefaciens. Transformasi genetik kalus menghasilkan 16 tanaman transgenik yang te& dari 1 tanaman transgenik yang ditransformasi dengan p2TDNAcryIAb, 10 tanaman transgenik hasil transformasi dengan pC12SA) danpC1300 hpt intron), dan 5 tanaman trausgenik yang ditransformasi dengan pC1300 hpt intron sebagai kontrol. Hasil analisis tanaman transgenik dengan PCR menunjukan bahwa kedua T-DNA pada plasmid (p2TDNAcTyIAb) dan
plasmid pC12SA telah terintegrasi ke dalam genom tanaman. Perlu dilakukan analisis lebih lanjut untuk melihat pola integrasi gen dalam genom tanaman dan
ABSTRACT
AGUS RACHMAT. Construction of Gene Expression Vector for Selectable Marker Gene Elimination in Rice (Oryza saliva L.) Transgenic Plant. Under the direction of SUHARSONO and INEZ H.S. LOEDIN.
Selectable marker genes are widely used for the efficient transformation of crop plant, but they are not required after transgenic plants were produced. Transformation technic using double T-DNA has been developed to facilitate the removal of the marker gene from plant genome after selection. The aim of reseach was to contruct a gene expression vector for gene elimination of antibiotic resistance gene in transgenic rice plant. In this system
a
marker gene and gene of interest were placed on separate T-DNA molecules. Two approaches were performed. The first was by the construction of a binary vectors containing two separate T-DNA's. The vector that carried two separate T-DNAs was constructed, one T-DNA contained a drug resistance, selection marker gene (hpt)KONSTRUKSI VEKTOR EKSPRESI GEN UNTUK
MENGELIMINASI GEN PENYELEKSI ANTIBIOTIK PADA
TANAMAN PAD1
(Oryza
sativa
L.) TRANSGENIK
AGUS RACHMAT
Tesis
sebagai salah satui syarat untuk memperoleh gelar
Magister Sains pada Program Studi Biologi
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Nama NIM
: Konstruksi Vektor Ekspresi Gen untuk Mengeliminasi
Gen Penyeleksi Antibiotik pada Tanarnan Padi (Oryza
sativa L.) Transgenik
: Agus Rachrnat
: G351020101
Dr. Suharsono. DEA Ketua
Disetujui
Komisi Pembimbing
Dr. 1 d z H. Slamet-Loedin Anggota
Diketahui
Ketua Program Studi Biologi
Dr. Dedi Duryadi, DEA
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT, karena atas berkah dan izin-Nya penulis mampu menyelesaikan penelitian dan penulisan tesis dengan judul Konstruksi Vektor Ekspresi Gen untuk Mengeliminasi Gen Penyeleksi Antibiotik pada Tanaman Padi (Oryza sativa L.) Transgenik.
Selesainya pendidikan dan penelitian ini tidak luput dari bantuan dan
dukungan berbagai pihak. Oleh karena itu pada kesempatan ini penulis mengucapkan terima kasih yang sebesar-besarnya kepada Dr. Suharsono, DEA clan Dr. Inez H. Slamet-Loedin sebagai pembimbing yang selalu mendorong dan
men- untuk dapat menyelesiakan penelitian ini, Ketua Program Studi Biologi beserta staf, Direktur
Program
Pascasarjana IF'B beserta staf yang telah memberikan pelayanan selama penulis menempuh p e n d i d h , Kepala Puslit Bioteknologi LIP1 dan staf yang telah memberikan izin belajar dan penggunaan fasilitas penelitian. Kepada Dr. Inez H. Slamet-bedin dan Sigit Purwantomo penulis mengucapkan terimakasih atas masukan serta bantuan dana yang sangat berarti melaluiRUT
XII. Penulis juga berterimakasih kepada Wulansih Dwi Astuti, keluarga Sasmita, rekan-rekan mahasiswa Pascasarjana khususnyaProgram
Strldi Biologi 2002, rekan-rekan di Lab. Biologi Molekuler Tanaman Padi dan Rumah Kaca Bioteknologi LIP1 dan semua pihak atas bantuan yang diberikan &lam pelaksanaan penelitian dan penyusunan tesis. Kepada Ibunda R. Hj Djulaeha dan keluarga yang telah mendampingi dengan doa, kesabaran dan ketulusan sampai detik ini penulis mengucapkan terimakasih.Semoga Allah SWT senantiasa memberikan limpahan taufik dan
hidayah-Nya atas segala kebaikan yang diberikan dan mohon maaf atas segala kesalahan. Akhir kata semoga karya ilmiah ini dapat bermanfaat bagi dunia ilmu pengetahuan.
Bogor, Mei 2006
RIWAYAT HIDUP
Penulis dilahirkan di Bogor, Jawa Barat pada tanggal 26 Agustus 1970 merupakan putra ke enam dari delapan bersaudara dari pasangan Bapak H. E. Padma (alm) dan Ibu R. Hj. Djulaeha.
Penulis menyelesaikan pendidikan formal di SD Negeri 1 Jonggol, S M P
DAFTAR IS1
Halaman
DAFTAR TABEL
...
ixDAFTAR GAMBAR
...
xDAFTAR LAMPIRAN
...
xiPENDAHULUAN
...
1Latar Belakang
...
1Tujuan
...
4...
TINJAUAN PUSTAKA 5 DNA Vektor (DNA Pembawa)...
5Konstruksi DNA Rekombiian
...
6...
Gen Penyandi Higromisin Fosfotransferase 8...
Strategi Eliminasi Gen Penyeleksi Antibiotik 9...
Gen Penyandi Biosintesis Asam Salisilat 1 1 Gen cry Penyandi 6 Endotoksin...
12Transfomasi Genetik Tanaman Padi melalui Agrobacterium
...
15Regenerasi in vitro Tanaman Padi
...
19Analisis PCR
...
20BAHAN DAN METODE
...
22Waktu dan Tempat
...
22Bahan
...
22Metodologi
...
23Konstruksi Vektor yang Mengandung Double T-DNA
...
25...
Konstruksi Vektor di Dua Inang yang Berbeda 25...
KO-kultivasi dan Kultur Tanaman 29 Analisis Tanaman Transgenik...
31HASIL DAN PEMBAHASAN
...
33...
Konstruksi Plasmid DoubleT-DNA 33 Kontruksi Plasmid Dtla T-DNA Berbeda Inang...
35Transformasi dan Regenerasi Tanarnan
...
38Analisis PCR Tanaman Transgenik
...
40KESIMF'UCAN DAN SARAN
...
43Kesimpulan
...
43Saran
...
:...
43DAFTAR TABEL
Halaman
1 Jumlah koloni E. coli hasil transformasi
... ..
....
...
.
. ....
...
. ...
...
33DAFTAR GAMBAR
Halaman
1 Proses transfer T-DNA dari Agrobacterium tumefaciens ke dalam
sel tanaman
...
172 Plasmid pCAMBIA
...
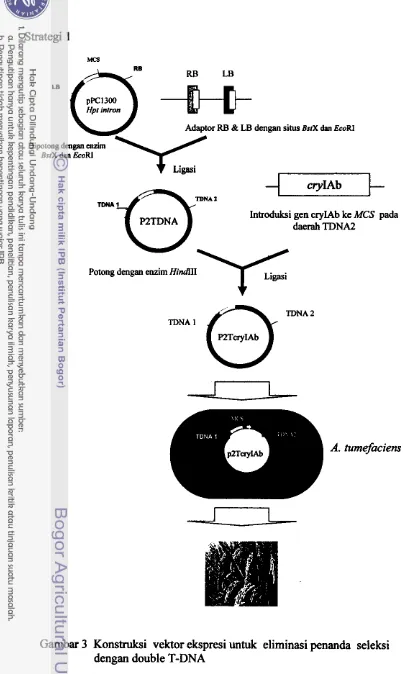
223 Konstruksi vektor ekspresi untuk eliminasi penanda seleksi
dengan double T-DNA
...
244 Lokasi kaset cryIAb dan hpt intron pa& T-DNA
...
255 Konstruksi vektor ekspresi untuk eliminasi penanda seleksi
melalui dua inang
...
266 LokasipmsB dan gen e n s pada T-DNA dari plasmid pC12SA
...
277 Hasil elektroforesis p2TDNA yang dipotong dengan
Ncol dan BglII dan utuh
...
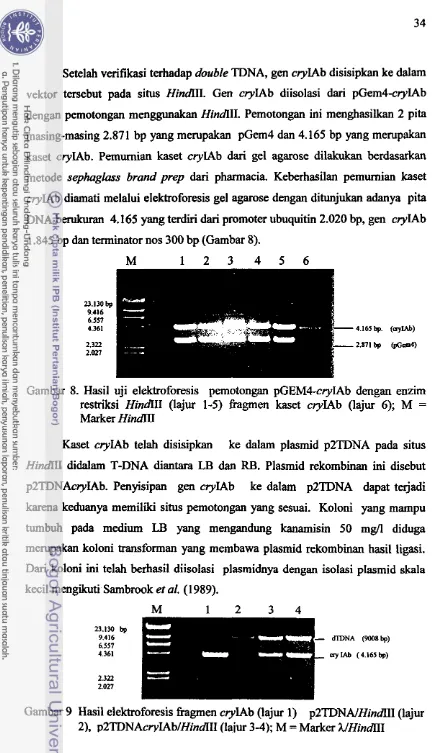
338 Hasil elektroforesis h g m e n cryIAb dengan
...
enzim restriksi H i n m 34
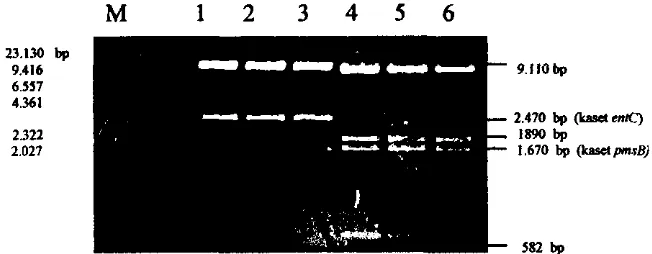
9 Hasil elektroforesis h g m e n cryIAb (lajur 1) pemotongan
p2T-DNA cryIAb dengan enzim restriksi H i d 1 1
...
3410 Hasil elektroforesis pSA yang dipotong dengan
enzim restriksi XbaI; XbaI & EcoRI
...
361 1 Hasil elektroforesis pC12hpt yang mengandung
genpmsB yang dipotong dengan XbaI & EcoRl
...
3612 Hasil elektroforesis DNA pC12hptSA yang dipotong
dengan enzim XbaI dan EcoRI
...
3713 Hasil elektroforesis gen penyandi biosintesis asam
salisilat yang dipotong dengan EcoRl
...
37...
14 Planlet yang ditanam pada media MS yang mengandung higromisin 39
15 Hasil analisis PCR gen hpt
...
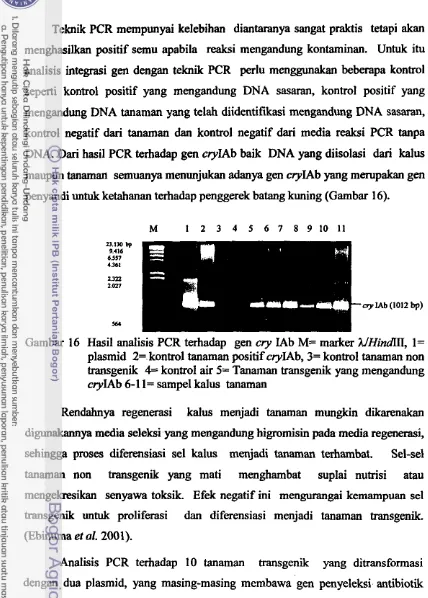
4016 Hasil analisis PCR gen cryIAb
...
41DAFTAR LAMPIRAN
Halaman
1
.
Media untuk ko-kultivasi dan regenerasi...
49...
2
.
Media untuk pertumbuhan bakteri 50...
PENDAHULUAN
Latar Belakang
Padi merupakan komoditas pertanian yang banyak diusahakan oleh petani
di dunia. Bagi sebagian besar petani, padi mempakan pilihan utama untuk diusahakan dalam upaya memenuhi kebutuhan pangan. Sejalan dengan makin
bertambahnya jurnlah penduduk, permintaan terhadap beras pun semakin
meningkat. Pada akhir-akhir ini produksi beras nasional mengalami p e n m a n
yang sangat berarti. Pada tahun 2000 produksi beras Indonesia sebesar 32.8 juta
ton sedangkan pada tahm 2001 produksi berm Indonesia sebesar 31.7 juta ton
(BPS & Ditjen BPTP 2002).
Konsep penggunaan Agrobacterium tumefaciem sebagai vektor untuk merakit tanaman transgenik mempunyai prospek dan harapan. Beberapa tanaman
agronomi dan holtikultura yang memiliki nilai penting secara rutin ditransformasi
menggunakan bakteri hi. Sistem transformasi dengan Agrobacterium secara luas telah digunakan untuk introduksi gen asing kedalam genom tanaman (Gelvin SB
1998). Introduksi gen asing ke dalam sel tanaman melalui proses transformasi
merupakan ide dari perakitan tanaman transgenik.
Keberadaan gen penyeleksi antibiotik atau resistensi herbisida yang
kondisinya terus menerus diekspresikan telah menimbulkan beberapa masalah (Granger 2002). Pertama, munculnya kekhawatiran publik tentang terjadinya
resistensi dari organisme penggangu. Hal ini terjadi karena produk yang
diekspresikan terus menerus dapat berfungsi sebagai agen seleksi sehingga dapat
meningkatkan ketahanan bakteri terhadap antibiotik tertentu (dari penggunaan gen penyeleksi antibiotik) dan gulma terhadap herbisida tertentu (dari penggunaan gen penyeleksi herbisida). Kedua, ekpresi gen penyeleksi yang terus menerus mungkin
dapat mengganggu produksi karena surnber asam amino dipakai untuk
menghasilkan protein yang disandi oleh gen penyeleksi. Ketiga, keterbatasan agen
seleksi pada sistem seleksi yang efektif menjadi hambatan jika akan dilakukan
penyisipan gen lain dengan menggunakan gen seleksi sebagai penanda
seleksinya. Adanya sistem seleksi positif, misalnya dengan menggunakan manosa
Gen penyeleksi antibiotik selalu digunakan dalam sistim transformasi,
tetapi gen tersebut biasanya tidak dibutuhkan apabila tanaman transgenik telah
dihasilkan Gen penyeleksi antibiotik pada tanaman transgenik yang telah didapat
bukan hanya tidak dibutuhkan lagi, tetapi juga dapat menimbulkan masalah baru.
Sebagai contoh, gen resistensi antibiotik yang berbeda hams digunakan bila a&
penambahan gen wing ke dalam tanaman transgenik, tetapi sejumlah gen
penyeleksi antibiotik yang ada terbatas. Keamanan dari gen penyeleksi antibiotik me~pakaIl masalah dalam pemasaran produk rekayasa genetik.
Keberadaan gen penyeleksi antibiotik pada tanaman transgenik telah
menimbulkan keberatan antara lain berupa kekhawatiran terjadinya transfer gen
tersebut ke milcroorganisme dan kemunglunan terganggunya ekspresi gen yang memillki peran penting, serta kesulitan untuk mengintroduksi gen lain karena
terbatasnya gen penyeleksi antibiotik yang dapat digunakan. Gen penyeleksi
dapat dieliminasi dari tanaman transgenik melalui seleksi pada generasi
berikutnya setelah proses segregasi. Gen penyeleksi &pat berpisah dari gen
sasaran bila kedua gen tersebut terletak pada kromosom yang berbeda atau
keduanya bebas. Terdapat beberapa metode yang dapat mengeliminasi keberadaan
gen penyeleksi antibiotik, antara lain melalui, ko-transfonnasi baik dengan
particle bombardment maupun dengan double T-DNA, site-specrfc
recombination (Mom & Hooykaas 1992, Zuo JR et al. 2001), dan inm-
genomic translocation via transposable elements (Cotsafis et al. 2002). Pada
sistem ketransformasi, gen sasaran dipisahkan
dari
gen penyeleksi antibiotik.Teknik ini dapat menjadi suatu teknik generik yang dapat diterapkan untuk semua
sistem transformasi tanaman dalam mengeliminasi gen penyeleksi antibiotik.
Secara alami, beberapa isolat Agrobacterium memiliki lebih dari satu T-DNA, dan tumor crown gall seringkali disebabkan karena ko-transformasi oleh beberapa T-DNA (Hooykaas & Schilperoort 1992).
Selain gen sasaran yang diintroduksikan, T-DNA tidak mengintroduksi
DNA lain kecuali right border dan leji border dari Agrobacterium itu sendiri ke dalam genom. Teknik ini dapat menjadi suatu teknik generik yang &pat
diterapkan untuk semua sistem transformasi tanaman dalam mengeliminasi gen
dengan memisahkan gen sasaran dan gen penyeleksi antibiotik pada T-DNA yang
berbeda. T-DNA adalah daerah DNA yang akan ditransfer dan telah diketahui dibatasi oleh 25 pasangan basa pada masing-masing ujungnya yang dikenal sebagai batas kiri (leji border) dan batas kanan (right border) (Hooykaas &
Schilperoort 1992). KO-transformasi dengan menggunakan Agrobacterium
melalui double T-DNA memungkinkan dihasilkannya tanaman transgenik tanpa gen penyeleksi antibiotik setelah segregasi (Komari et al. 1996; Matthews et al.
2001; Zhou et al. 2003). Kegiatan transformasi gen melalui perantara alami
Agrobacterium tumefaciens telah menjadi kegiatan rutin pada banyak
laboratorium di Indonesia. Akan tetapi tanaman transgenik yang dihasilkan dari
sistem transformasi ini akan selalu mengandung gen penyeleksi antibiotik.
Introduksi gen asing kedalam tanaman tingkat tingg menggunakan teknik
Agrobacterium tumefaciens merupakan teknik yang sering digunakan &lam
biofogi molekuler dan rekayasa genetik tanaman. Walaupun metode ini pada
awalnya digunakan pada tanaman dikotiledon, tetapi sekarang telah dikembangkan pada beberapa tanaman sereal seperti padi, jagung (Hiei et al.
1994). Salah satu keuntungan transfer gen dengan A. tumefaciens adalah efisiensi
transformasi yang tinggi.
Pada penelitian ini strategi yang dilakukan untuk mengintegrasikan gen
penyeleksi yang dapat bersegregasi dengan gen sasaran adalah: 1 ) double
T-DNA yang masing-masing membawa gen penyeleksi dan gen sasaran secara terpisah, dan gen sasaran yang digunakan adalah gen cryIAb. 2 ) Dua T-DNA berbeda inang, T-DNA yang satu membawa gen penyeleksi dan T-DNA lainnya membawa gen sasaran pada masing-masing plasmid Gen sasaran yang digunakan
adalah gen penyandi asam salisilat yang dibawa oleh plasmid pCambia 1200 yang telah dibuang gen penyeleksinya. Asam salisilat dipilih karena memililu potensi
dapat mempertinggi ketahanan tanaman terhadap stres biotik maupun abiotik.
Asam salisilat secara alami terdapat dalam tanaman dan terlibat dalam
beberapa fungsi fisiologis, seperti pembukaan stomata, induksi pembungaan, dan
memiliki peran penting &lam mengatasi serangan patogen (Verbeme et al.
2000). Penelitian yang dilakukan Verbeme et al. (2000) pada tanaman tembakau
e n C ) yang berhasil disisipkan temyata dapat meningkatkan daya resistensi tanaman tersebut terhadap patogen, namun tidak mempengamhi fenotip tanaman tersebut. Kandungan asam salisilat pada tanaman padi berkorelasi positif dengan tingkat ketahanan padi terhadap Pyricularia grisea (Silverman et al. 1995). Gen- gen yang bertanggung jawab dalam biosintesis asam salisilat dihasilkan oleh
Pseudomonm fluorescens (gen pmsB) dan Escherichia coli (gen enlC). Gen-gen tersebut terlibat dalam jalur biosintesis asam salisilat yang dimulai dari
isochorismate sinthase oleh gen entC dan isochorismate pyruvate lyase oleh gen
pmsB untuk meningkatkan resistensi terhadap penyakit yang disebabkan oleh cendawan (Mercado et al. 1989).
Penggerek batang m e ~ p d c a n salah satu hama utama tanaman padi yang kuantitas serangannya semakin meningkat. Penggerek batang me~p&aII salah
satu hama utama padi di Asia yang mengakibatkan kehilangan produksi sebesar
5 1 0 % (Pathak & Khan 1994) bahkan sampai 60-95% (Wunn et al. 1996). Penanganan hama penggerek batang sampai saat ini masih tergantung pada
penggunaan pestisida. Gen cry adalah penyandi protein aktif anti serangga yang
diisolasi dari BaciIlw thuringiemis, yaitu bakteri yang menghasilkan suatu kristal protein yang bersifat racun jika terhidrolisis dalam jaringan usus serangga (Dekeyser et al. 1990). Ekspresi gen yang diisolasi dari B. thuringiensis ini pada kultivar IR58 dan Basmati dapat meningkatkan ketahanan terhadap penggerek batang kuning dan bergaris (Wunn et d. 1996; Nayak et al. 1997). Wunn et al.
(1996) melaporkan tanaman padi yang mengekspresikan gen cyMb dapat
meningkatkan ketahanan terhadap hama penggerek batang sampai 100%.
Tujuan
Penelitian ini bertujuan untuk mengkonsbuksi vektor ekspresi gen yang
dapat mengeliminasi gen penyeleksi antibiotik dengan menggunakan Olyza sativa
TINJAUAN PUSTAKA
DNA Vektor (DNA Pembawa)
Vektor DNA adalah molekul DNA yang dipergunakan
untuk untuk
membawa dan memperbanyak fragmen DNA yang dibawanya. Vektor hams
mampu mengadakan replikasi dalam sel inang sehingga banyak salinan molekul
DNA yang dihasilkan. Vektor yang sering digunakan adalah plasmid bakteri.
Plasmid adalah bahan genetik ektrakromosom yang diwariskan secara tetap.
Ciri-ciri plasmid antara lain berukuran kecil dan hanya mengandung beberapa
gen, pembawa informasi genetika, terlepas dari DNA kromosom atau kadang- kadang &pat terintegrasi dengan DNA kromosom dan dapat diisolasi dengan
mudah dari sel bakteri (Lehninger 1994).
Pada penelitian ini digunakan vektor pCambia 1300 dan pCambia 1200,
yang memiliki beberapa kelebihan seperti memiliki multple cloning site (MCS), bersifat stabil di Agrobacterium, ukurannya relatif kecil dan jumlah salinannya tinggi dalam E coli. pCambia memiliki pBR322 origin of replication
untuk
replikasi dalamE
coli clan Agrobacterium, pBR322 mob siteuntuk
mobilisasidari E. coli ke Agrobacterium, membawa gen hpr penyandi ketahnan terhadap
higromisin, gen nptll untuk ketahanan terhadap kanamisin, gen gusA serta &pat diuji dengan seleksi biru putih karena membawa gen lacZ(Brown 1996).
T-DNA yang ada di dalam vektor pCambia mengandung gen nptZI, gen
hpt dan gen gusA. Gen nprII penyandi enzim neomycin phosphotransfrase yang
digunakan sebagai penyeleksi pada bakteri. Enzim tersebut mendetoksifikasi senyawa aminoglukosida melalui fosforilasi. Gen hpt menyandikan enzim
hygromycin phosphotranferase yang digunakan sebagai penyeleksi untuk
mengetahui terintegrasinya T-DNA Agrobacrer~um ke dalam genom tanaman, sehingga hanya tanaman transgenik yang dapat hidup di media tumbuh yang
mengandung antibiotik higromisin. Gen hpt umum digunakan
untuk
transformasi genetika sel tumbuhan karena antibiotik higromisin pada konsentrasi tertentu mampu menekan pertumbuhan sel tersbut (Christou et al. 1991).Beberapa jenis vektor &pat digunakan sebagai vektor rekombinan
sitoplasma bakteri secara bebas. Plasmid juga membawa gen-gen ketahanan
terhadap antibiotik yang berguna sebagai penyeleksi sel-sel bakteri yang
mengandung plasmid rekombinan, 2) Virus atau bacteriofage DNA yang &pat
membawa DNA sisipan sekitar 15 kb, 3) Cosmid yaitu DNA plasmid yang juga memiliki situs kohesif dari fage. Cosmid memiliki satu atau lebih gen penyeleksi
antibiotik dan membawa sisi cos dari fage A. Cosmid dapat membawa DNA sisipan relatif besar (40-45 kb), 4) Shuttle vector ialah molekul DNA yang
mampu bereplikasi di dalam dua jensi sel berbeda atau lebih. Beberapa jenis
shuttle vector yang banyak digunakan adalah molekul DNA yang mampu
bereplikasi dalam sitoplasma bakteri atau khamir (Kleinsmith & Kish 1995).
Plasmid dapat diklasifikasikan berdasarkan sifat-sifat utama yang disandi
oleh gen-gen dalam plasmid. Klasifikasi tersebut adalah: 1) plasmid fertilitas
atau plamid F yang hanya membawa gen tra untuk melakukan transfer plasmid dengan cam konjugasi, 2) plasmid resistensi atau plasmid R, membawa gen yang
menyebabkan resistensi tuan rumah terhadap satu atau lebih gen antibakteri, 3)
plasmid col, mengkode kolisin, protein yang dapat membunuh bakteri lain, 4)
plasmid degadatif memungkinkan bakteri untuk mengadakan metabolisme
molekul yang tidak biasa seperti toluen, dan 5) plasmid virulensi, menyebabkan
patogenitas pada bakteri inang, misalnya plasmid Ti pada Agrobacterium yang
menimbulkan penyakit crown gall pada tanaman dikotil (Brown 1991).
Konstruksi
DNA
RekombinanTeknik DNA rekombinan m e ~ p a k a n teknik pembentukan kombinasi baru dan DNA dengan cara melakukan penylsipan molekul-molekul DNA yang
dikerjakan di luar sel dalam suatu vektor dan dintroduksikan ke dalam sel inang sehingga berkembang biak dalam sel inang tersebut. Teknologi DNA
rekombinan atau rekayasa genetika pada intinya adalah proses kloning gen
(Davis et a[. 1995; Freifelder 1995). Gen merupakan sekuen nukleotida yang
menyandi RNA yang dibatasi oleh promoter dan terminator. Teknologi DNA
rekombinan memungkinkan sejumlah gen dari sumber berbeda disatukan untuk membentuk DNA rekombinan weinsmith & Kish 1995). Tahapan dalam
dalam molekul DNA vektor, vektor rekombinan dimasukan kedalam sel inang,
vektor dalam sel inang diperbanyak seiring dengan pembelahan sel inang dan
sekaligus memperbanyak gen yang dibawa.
Komponen penting dalam rekombinasi DNA adalah enzim-enzim
manipulasi DNA serta QNA vektor. Brown (1991) membagi enzim manipulasi
berdasarkan jenis dan reaksi yang dikatalisnya menjadi lima golongan yaitu: a)
nuklease yaitu enzim yang mampu memotong molekul asam nukleat, b) ligase
adalah enzim yang berfhgsi menyatukan molekul asam nukleat, c) polimerase
adalah enzim yang &pat mensintesis DNA, d) enzim modifikasi yang mampu
mengh~langkan atau menambahkan gugus kimia, dan e) topoisomerase adalah
enzim yang mengubah DNA tertutup secara kovalen menjadi DNA supercoil.
Pa& kegiatan pengklonan gen hanya dua jenis enzim yang berperan yaitu enzim
restriksi endonuklease clan enzim ligase. Enzim yang mampu memotong ruas
DNA secara tepat dan konsisten digolongkan kedalam tipe 11 endonuklease restriksi. Enzim ini mendegradasi DNA dengan memecah ikatan posfodiester
yang menghubungkan satu nukleotida dengan nukleotida lainnya pada untaian
DNA.
Salah satu komponen yang diperlukan dalam teknologi DNA rekombinan
adalah adanya vektor DNA, yaitu molekul DNA yang diperlukan untuk
membawa dan memperbanyak fragmen DNA. Vektor yang sering dipergunakan
adalah plasmid bakteri yang merupakan materi genetik ekstra luomosom yang
diwariskan secara tetap. Plasmid yang dipergunakan sebagai vektor sebaiknya
berukuran kecil dan terbesar adalah 15 kb. Ukuran kecil sangat penting agar dapat memuat fragmen DNA asing yang besar, mudah dikenali dengan peta
restriksi, dan menghasilkan jumlah salinan relatif lebih banyak dibandingkan dengan yang berukuran besar (Sambrook 1989).
Plasmid yang digunakan untuk rekombinasi DNA berukuran antara
1.0-250 kb. Plasmid yang berukuran besar biasanya mempunyai jumlah salinan
yang rendah yaitu 1-2 salinan per sel. Sebaliknya plasmid yang berukuran kecil
mempunyai jumlah salinan tinggi, jumlahnya dapat mencapai 100 salinan per sel
Gen Penyandi Higromisin Fosfotransferase
Modifikasi tanaman secara potensid memberikan peningkatan substansid
dalam praktek pertanian, kualitas makanan dan kesehatan manusia Kesuksesan ha1 ini tergantung pada kemampuan mengintegrasikan gen asing ke tanaman inang dan efisiensi regenerasi
dari
sel-sel tertransformasi. Efisiensi transformasi yang rendah memerlukan gen marker penyeleksi untuk mengidentifikasi tanaman transgenik (Hare 2002). Penggunaan gen marker dalam proses transformasibertujuan memberikan keuntungan selektif
untuk
sel-sel tertransfonnasi, sehinggamereka tumbuh lebih cepat dan lebih baik serta membunuh sel-sel non transforman (Brasileiro & Aragao 2001)
Efektifitas sistem ketahanan terhadap antibiotik tergantung temtama pada
bahan seleksinya (selective agent) yang harus sepenuhnya menghambat pertumbuhan sel-sel yang tidak tertransformasi. Konsentrasi terendah
dari
bahantoksik
hams
&pat menekan pertumbuhan sel-sel non transforman, akan tetapi tidak memberikan efek yang merusak pa& sel-sel yang tertransformasi(Rodriguez & Nottemburg 2002)
Gen-gen ketahanan terhadap antibiotik sebagai marka penyeleksi yang
umum digunakan adalah neomicin fosfotransfm I1 (nptIl) dan higromisin fosfotransfm (hpt). Higromisin umumnya lebih toksik dibandingkan kanarnisin
dan membunuh sel-sel sensitif lebih cepat (Rodriguez dan Notternburg 2002) dan
me~pakan penyeleksi yang lebih disukai untuk transformasi pada tanaman monokotiledon terutama gramineae (Bashir et a[. 2004).Higromisin merupakan antibiotik aminoglikosida yang diproduksi oleh Streptomyces hygroscopicus dan mempakan sistem marker penyeleksi yang sesuai
untuk
sistem tanaman dan hewan. Antibiotik ini menghambat sintesis protein dengan cara mengganggutranslokasi dan menyebabkan kesalahan translasi pada ribosom 80s (Bashir et al. 2004).
Gen penyandi higromisin fosfotransferase (hpt) juga dikenal sebagai
aminoglykosida 4
-
fosfotransferase (APH 4) dan dinotasikan dengan hp!, hph atau aphW (Rodriguez dan Notternburg 2002). Enzim higromisinkelompok hydroxyl &lam antibiotik higromisin sehingga membuatnya menjadi
tidak aktif (Brasileiro & Aragao 2001).
Strategi Eliminasi Gen Penyeleksi Antibiotik
KO-transformasi dengan double
T-DNA
Keberadaan gen penyeleksi antibiotik pada tanaman transgenik telah
menimbulkan keberatan antara lain berupa kekhawatiran te jadinya transfer gen
tersebut ke mikroorganisme dan kemunglunan terganggunya ekspresi gen yang
memiliki peran penting, serta kesulitan untuk mengintroduksi gen lain. Terdapat
beberapa metode yang &pat mengeliminasi keberadaan gen penyeleksi antibiotik,
antara lain melalui, ko-transformasi baik dengan parficle bombardment maupun dengan double T-DNA, site-specrfic recombination (Mow dan Hooykaas 1992, Zuo JR et al. 2001), dan intra-genomic translocation via transposable elements
(Cotsafii et al. 2002). Pada sistem ko-transformasi, gen sasaran dipisahkan dari
gen penyeleksi antibiotik. Teknik ini dapat menjadi suatu teknik genenk yang
&pat diterapkan untuk semua sistem transformasi tanaman dalam mengeliminasi
gen penyeleksi antibiotik.
Strategi untuk mendapatkan tanaman transgenik yang hanya mengandung
gen sasaran tetapi tidak mengandung gen penyeleksi antibiotik dapat dilakukan
dengan teknik ko-transformasi. Ko-transformasi &pat diperoleh melalui ko-
kultivasi dengan satu Agrobacterium yang membawa satu plasmid biner mengandung gen penyeleksi dan gen sasaran pada T-DNA yang berbeda.
Depicker et a1 (1985) melakukan kokultivasi pada protoplas tembakau dengan satu Agrobacterim strain C58 yang mengandung dua T-DNA (T-DNA alami
dan gen npt 11) pada plasmid Ti nopalin. Frekuensi kalus transforman dari basil seleksi dengan antibiotik kanamisin (Km) adalah 11% dan hormone independent
growth (HN) 8 %. Frekuensi relatif ko-trasnsformasi Km adalah 67% dan HN
73%. Hasil ini mengindikasikan bahwa satu bakteriurn dapat mentrasfer dan
mengintegrasikan dua T-DNA sekaiigus dalam satu tahap infeksi.
Komari et a1 (1996) melakukan ko-kultivasi tembakau dan padi dengan satu Agrobacterium strain LBA 4404 yang mengandung dua T-DNA (satu gen
nptII atau gen hpt sementara yang lain adalah gen p) pada vektor plasmid biner.
yang hidup pada media seleksi higromisin. Dari masing masing transforman yang dihasilkan dari tanaman tembakau 54 dan dari tanaman padi 259 memperlihatkan positif p. Efisiensi trasnformasi adalah 50% untuk tanaman
tembakau dan 47 % untuk tanaman padi. Selanjumya dilakukan penyerbukan sendiri secara acak, dm dari hasil segregasi gen ketahanan higromisin atau
kanarnisisn serta ekspresi p diamati pada k e t m a n berikumya. Anakan yang
hanya mengekpresikan gen p yaitu 56% (519) dari ko-transformasi tanaman tembakau dan 65% (13120) dari hasil ko-transformasi tanaman padi. Hasil ini
mengindikasikan bahwa satu T-DNA yang hanya mengandung gen gus telah terintegrasi sekurang-kurangnya kedalam satu lokus yang berbeda.
Ko-transformasi dengan dua Agrobacterium
Ko-tranforrnasi dilakukan melalui ko-kultivasi dengan dua
Agrobacterium yang mengandung gen penyeleksi antibiotik dan gen s w a n
pada plasmid biner yang berbeda. Tanaman transforman diseleksi dengan
men- penyeleksi antibiotik Untuk mendapatkan tanaman transgenik
yang tidak mengandung gen penyeleksi dilakukan segregasi dari ko-trasnsforman dengan teknik penyilangan Depicker (1985) melakukan ko-kultivasi pada
protoplas tembakau dengan dua Agrobacteriurn yang berbeda menggunakan
strain C58 yang mengandung nopalin plasmid Ti dengan wild T-DNA dan
plasmid vektor biner dengan gen n p n . Frekuensi kalus transforman yang
mengandung ketahanan kanamisin adalah 20% dan
HN
(hormone independent growth) 21%. Frekuensi relatif ko-transformasi sel-sel transformanKm
dan HNmasing-masing adalah 43% dan 42%. Hasil ini menunjukan bahwa masing-
masing sel tanaman mempunyai cukup sisi pelekatan untuk beberapa bakteri dan
transformasi satu sel tanaman oleh dua bakteri berbeda mewakili independent
event (kejadian bebas).
Mc Knight et al. (1987) melakukan kokultivasi daun tembakau dengan dua
strain Agrobacterium LBA4404 yang mengandung gen nos (novalin sintase) dan
gen nptII pada plasmid biner. Dari 16 tanaman yang diperoleh dengan men- seleksi kanamisin, tiga mengandung nopaline. Efisiensi
transformasi ko-kultivasi adaiah 19%. Semua tanaman yang didapat dari ko-
mengindikasikan bahwa dua T-DNA berbeda terintegrasi ke &lam lokus yang
berbeda.
Daley et al. (1998) melakukan ko-kultivasi rapseed dan tembakau dengan satu strain Agrobacterium yang mengandung gen nptII dan gen gus. Dari hail seleksi dengan menggunakan kanamisin diperoleh 34 rapeseed dan 100 tanaman
tembakau yang dpat hidup, 21 dan 52 memperlihatkan aktivitas gus untuk
masing-masing. Frekuensi transfomasi rapeseed adalah 62 % dan tembakau 52
%. Ketunman dari penyerbukan sendiri hanya mengekpresikan satu transgen
yaitu 40% (8120) dari kotrasnsformasi rapeseed dan 58% (24141) untuk tanarnan tembakau. Segregasi nptII dan gen gus setelah penyerbukan sendiri mengindikasikan bahwa dua T-DNA berbeda terintegrasi kedalam lokus yang
berbeda
Gen Penyandi Biosintesis Asam Salisilat
Asam salisilat yang secara alami terdapat dalam tanaman terlibat dalam
beberapa fungsi fisiologis, seperti pembukaan stomata, induksi pembungaan, dan
memiliki peran penting dalam mengatasi serangan patogen (Verbeme et al.
2000). Penelitian Verbeme et al. (2000) pada tanaman tembakau menunjukkan bahwa ekspresi gen-gen yang mendukung peningkatan ekspresi asam salisilat
(gen pmsB dan gen enC) dapat meningkatkan daya resistensi tanaman tersebut terhadap patogen, namun tidak mempengamhi fenotip tanaman tersebut.
Kandungan asam salisilat pada tanaman padi berkorelasi positif dengan tingkat
ketahanan padi terhadap Pyricularia grisea (Silveman et al. 1995).
Jalur biosintesis
asam
salisilat dimulai dari substrat chorismic acid yang dikatalis oleh enzirn isochorismate sinthare menjadi isochorismic yang diubah oleh enzim isochorismatepruvate lyase menjadi asam salisilat. Gen penyandi enzim isochorismate sinthase telah diisolasi dari Pseudomonas jluorescens dandisebut dengan genpmsB.
Dari
Lscherichia coli telah diisolasi gen enC penyandi enzim isochorismatepymate base (Mercado et al. 1989).Penyakit blas
menyerang dan membentuk bercak pada daun, batang, malai, bunga dan biji. Bercak pada pelepah daun jarang ditemukan. Bentuk khas bercak blas adalah elips
yang kedua ujungnya kurang lebih runcing. Bercak yang telah berkembang pada
bagian tepi bemama coklat dan bagian tengah benvama putih keabuan. Dalam
keadaan lembab bercak akan terus membesar terutama pada varietas peka (Amir
& Karden 1991). Pada varietas padi peka, bercak tersebut dapat meluas dan
bersatu sehingga akhimya helai d a m mengering dan mati. Pada padi yang tahan,
gejala serangan hanya berupa bintik kecil b e m a coklat (Ou 1972).
Spora cendawan secara alami menyebar mulai tengah malam karena
adanya embun atau hujan. Penyebaran spora akan bertambah banyak sampai
menjelang pagi hari dan berakhir pada saat terbit matahari. Pelepasan spora di
daemh tropis dapat terjadi pula pada siang hari setelah turun hujan. Embun sangat berpengaruh terhadap pelepasan spora dan infeksi. Jika periode embun lebih lama,
spora yang dilepaskan lebih banyak sehingga infeksi yang terjadi semakin parah
(IRRI 1975). Penyebaran spora dapat terjadi selain oleh embun atau hujan juga
oleh angin, biji dan jerami sakit. Cendawan P. orjnae dapat bertahan dalam sisa jerami sakit dan gabah sakit selama lebih dari satu tahun pada suhu kamar.
Sedangkan dalam bentuk miselia mampu bertahan sampai lebih dari tiga tahun (Amir & Karden 1991).
Gen cry, Penyandi 6 Endotoksin
Bacillus thuringiensis adalah bakteri tanah yang selama proses sporulasi
mampu membentuk laistal protein yang bersifat racun apabila terhidrolisis dalam
usus serangga. Bakteri ini sudah digunakan lebih dari 50 tahun sebagai insektisida biologi (Tu et a[. 2000). Tanaman transgenik menjadi tahan hama karena adanya ekspresi endotoksin yang bersifat seperti insektisida (Insecticidal
CrystaI Protein = ICP) dari Bacillus thuringiensis (Bt toxin) dalam jaringan
tanaman (Nayak et al. 1997; Wu et al. 1997). Aktivitas insektisida Bt sangat spesifik sehingga endotoksin tersebut tidak toksik untuk serangga non target,
burung dan mamalia (Tu et al. 2000).
Gen cry adalah penyandi protein aktif anti serangga yang diisolasi dari
B. thuringiensis yaitu bakteri yang menghasilkan suatu kristal protein yang
1990). Gen cry &pat diklasifikasikan berdasarkan protein yang disandikan dan spesifitasnya terhadap serangga yaitu bersifat racun cryI, cry11 cryIII cryIV cryV
dan c f l . Protein yang disandikan oleh gen cry bersifat racun terhadap
serangga ordo Lepidoptera, Diptera dan Coleoptera (Toenniessen 1991) akan
tetapi aktivitas bioinsektisida Bt tidak toksik terhadap ordo homoptera (Rao et al.
1998).
Pada kondisi normal protein ini sulit larut, tetapi akan larut dalam pH
tinggi (diatas 9.5) yaitu kondisi yang biasa ditemukan pada usus tengah larva
lepidoptera. Karena itulah Bt merupakan bahan insektisida yang sangat spesifik.
Saat larut dalam usus serangga, protoksin dipecah oleh protease usus untuk
menghasilkan toksin aktif yang berukuran sekitar 60 kDa Toksin ini diistilahkan
sebagai Gendotoksin. Toksin tersebut berikatan dengan sel-sel epitelium usus,
membuat lubang-lubang (pori) pada sel membran dan menyebabkan
ketidakseimbangan ion. Sebagai akibatnya kerja usus terhenti dengan cepat, sel-
sel epitelium lisis dan isi usus masuk dalam rongga tubuh. Hal ini akhimya
mengakibatkan keracunan dan matinya larva (Anonim 2000). Penempelan racun
pada usus serangga memerlukan adanya reseptor untuk protein kristal spesifik
sehingga terjadi toksisitas, dan pada satu serangga mungkin saja terdapat reseptor
berbeda untuk protein kristal berbeda
.
Kristal protein ini disandikan oleh gen cry. Gen q y yang telah berhasil diidentifikasi adalah sebanyak lebih dari 140 gen dan telah diklasifikasi ulang menjadi 24 kelompok utama (Criclanore et al. 1998). Toksin yang berbeda mempunyai spesifitas yang berbeda untuk serangga yang berbeda. Cry 1 spesifik
untuk hama-hama dari ordo Lepidoptera, Cry 2 untuk Lepidoprera dan Diptera,
Cry 3 untuk Coleoptera dan Cry 4 untuk Diptera (Maqbool er al. 1998).
Beberapa peneliti telah melakukan introduksi gen cry ke dalam tanaman padi. Gen crylAb dari Bacillus thuringiemis mampu meningkatkan ketahanan padl kultivar Tarom molaii terhadap penggerek batang padi kuning dan bergaris
(Wu et al. 1997; Ghareyazie et a[. 1997). Nayak et al. (1997) telah mentransfer
gen cryIAc ke padi indica varietas IR64 dan dari hasil insect feeding assoy
menunjukkan bahwa galur transgenik mampu mengekspresikan toksin pa& level
2000) menghasilkan galur padi transgenik yang mengandung h i gen crylAc dan
gen crylAb, dan menunjukkan ketahanan terhadap penggulung daun dan penggerek batang kuning.
Penggerek batang
Penggerek batang merupakan salah satu hama utama tanaman padi yang
kuantitas
serangan
dari tahun ketahun semakin meningkat. Penggerek batang merupakan salah satu hama utama padi di Asia yang mengakibatkan kehilanganproduksi sebesar 5-10% (Pathak &
Khan 1994), bahkan bisa sampai 60-95%
(Wunn et al. 1996). Terdapat empat spesies penggerek batang padi yaitu
penggerek batang kuning (Schirphopaga incertulas), penggerek batang putih
(Schirphopaga innotata), penggerek batang bergaris (Chilo supresalis) dan
penggerek batang merah jambu (Sesamia injerens). Tiga jenis pertama tergolong
famili Pyralidae dan yang terakhir tergolong famili Noctuidae dan semua termasuk ordo Lepidoptera. Di Indonesia, dari empat spesies yang ada, hanya dua yang dominan di daerah produksi padi yaitu penggerek batang kuning
(Schirphopaga incertulas), penggerek batang putih (Schirphopaga innotata)
W l i n et al. 1995; Soewito et al. 1995).
Penggerek batang padi menimbulkan gejala kerusakan melalui liang
gerek yang dibuat oleh larva sehingga dapat memutuskan transfort air dan unsur
hara dari akar. Kerusakan yang timbul tergantung pada fase pertumbuhan tanaman. Jika serangan te jadi pada fase vegetatif maka dam tengah atau pucuk
tanaman mati karena titik tumbuhnya dimakan, gejda ini disebut sundep. jika seranga tejadi pada fas generatif maka malai akan mati karena pangkalnya
dikerat oleh larva sehingga bulir padi menjadi hampa. Gejala serangan pada tahap
ini disebut beluk (Soewito et al. 1995).
Penanganan penggerek batang sampai saat ini masih tergantung pada
penggunaan pestisida. Teknik penyisipan gen asing untuk tujuan pemberian
ketahanan terhadap hama telah dikembangkan pada beberapa kultivar padi
Indonesia. Salah satu gen ketahanan yang berhasil disisipkan ke kultivar Rojolele
adalah ciyIAb penyandi ketahanan terhadap hama dari golongan Lepidoptera
dari B. thuringiensis pda kultivar
IR58
dan Basmati dapat meningkatkan ketahanan terhadap penggerek batang kuning dan bergaris (Wunn et al. 1996; Nayak et al. 1997). Wunn et al. (1996) melaporkan bahwa hasil introduksi gencryIAb ke tanaman padi dapat menekan serangan hama penggerek batang
sampai 100%.
Transformasi Genetik Tanaman Padi melalui Agrobacterium
Kemampuan Agrobacterium untuk menjadi mesin genetik alami telah dimanfaatkan sebagai alat genetik yang sangat penting. Kemampuan untuk
melakukan transformasi sel tanaman tersebut berhubungan dengan adanya
plasmid penginduksi tumor. Istilah tanaman transgenik dalam pengertian luas
dipakai untuk tanaman yang memiliki gen asing yang terintegrasi ke dalam genom
tanaman dan gen tersebut berfungsi (Uchimiya et al. 1989). Berbagai metode saat ini telah dikembangkan dan digunakan untuk menghasilkan tanaman transgenik baik melalui transformasi langsung maupun tidak langsung (Herman 1999).
Transformasi secara langsung antara lain dengan elektroporasi, fusi dengan PEG
@oliethylene glycol), mikro injeksi dan penembakan DNA. Transformasi gen
secara tidak langsung ialah melalui vektor A. tumefaciens.
Bakteri A. tumefaciens merupakan patogen tanaman. Secara alami melalui mekanisme yang komplek, Agrobacterum mampu memindahkan suatu vektor plasmid yaitu Ti (Tumor inducing) yang terdapat di dalam genom tanaman. Pada plasrnid Ti terdapat bagian-bagian penting yang terkait dalam mekanisme transfer
gen. Bagian-bagian tersebut ialah daerah T-DNA dan daerah virulence (vir) pada plasmid Ti. Gen target yang akan diintroduksikan ke dalam T-DNA untuk
selanjutnya dipindahkan ke dalam genom tanaman. Gen vir berperan penting dalam rnekanisme pemindahan daerah T-DNA ke dalam genom tanaman. Selain
plasmid Ti, ada gen lain yang berperan dalam transfomasi yaitu gen cromosomal
virulence (chv). Gen-gen ini berperan dalam pelekatan bakteri ke dalam sel
tanaman (Sheng & Citovsky 1996). Mekanisme transfer DNA dari plasmid Ti ke
dalam genom tanaman disajikan pada gambar 2 (Gelvin 1993).
Salah satu ha1 penting dalam keberhasilan transformasi melalui
ganda (biner) me~pi3kan cara yang umum dilakukan. Pada sistim vektor ganda
diperlukan dua plasmid dalam Agrobacterium. Plasmid tersebut adalah plasmid
vektor yang mengandung fragmen DNA dan plasmid helper Ti yang
menyediakan gen vir sebagai fasilitator transfer gen ke dalam sel tanaman
(Slamet-Loedin 1994). Disamping itu efisiensi transformasi melalui
Agrobacterium sangat dipengaruhi kesesuaian antara galur Agrobacteriwn
dengan jenis maupun varietas tanaman yang akan ditransformasi. Varietas
tanaman yang berbeda memiliki respon berbeda pula terhadap galur
Agrobacterium yang dipakai &lam proses transformasi genetik.
Keberhasilan Hiei et al. (1994) mentrasnformasi tanaman padi dengan
A. tumefaciens menunjukan keberhasilan penerapan sistem transformasi
A. tumefaciens pada monokotil. Secara alami bakteri patogen tanah ini hanya
menginfeksi tanaman dikotil dengan cara mengintroduksi T-DNA dari plasmid Ti bakteri ke dalam inti sel tanaman (Smith & Hood 1995). Dong et al. (1996) menggunakan A. tumefaciens LBA4404 dengan pTok 233 untuk transformasi padi
javanica kultivar Gulhont, tetapi efisiensi transformasinya masih sangat rendah.
Kemudian Rashid et al. (1996) berhasil mentransformasi tanaman padi Indica-
India kultivar Basmati menggunakan A. tumefaciens EHA 101 dengan PIG 121
Hm. Diantara berbagai jenis tanaman pangan utama, padi m e ~ p a k a n spesies pertama yang menghasilkan tanaman transgenik fertil. Metode transformasi
genetik pada tanaman padi semakin berkembang termasuk pengetahuan tentang berbagai promoter (Terada & Shimamoto 1993). Untuk meningkatkan efisiensi transformasi melalui Agrobacferium pada tanaman monokotil temtama untuk spesies yang rekalsitran seringkali diperlukan berbagai modifikasi dalam metode
transformasi melalui Agrobacferium (Smith & Hood 1995). Transformasi terhadap kecambah kedelai menggunaka Agmbacterium juga telah berhasil
dilakukan oleh Chee et al. (1989).
Menurut Sheng dan Citovky (1996) terdapat tiga komponen dalam
A. tumefaciens yang berperan dalam transfer DNA ke dalam sel tanaman, yaitu: 1. Daerah T-DNA
T-DNA yaitu bagian dari tumor inducing plasmid (Ti) yang dimiliki
bagian DNA yang memiliki ciri khusus yang berada pada 200 kb Ti
plasmid Agrobacterium yang diapit oleh sekuen berulang DNA (25)
sebagai batas T-DNA.
2. Daerah virulence (vir)
Gen vir ini mempunyai ukuran 35 kb dan terbagi atas 7 macam, yaitu vir A, B, C, D, E, F, G, dan vir H. Gen-gen vir mensistesis protein
virulence. Protein vir ini berperan di dalam menginduksi terjadiiya
trasfer T-DNA dan integrasinya ke tanaman. Ekspresi gen-gen diinduksi oleh adanya senyawa fenolik seperti asetoseringon, monosakarida
spesifk (glukosa, arabinosa, galaktosa, fruktosa, dan xilosa), dan kondisi
pH juga mempengaruhi ekspresi gen vir. Tanaman yang terluka
mengeluarkan cairan dengan keasaman yang khas antara pH 5,O-5,s
(Sheng & Citovsky 1996). Senyawa fenolik dan monosakarida terbentuk
pa& saat tanaman dikotil luka dengan mengeluarkan getah dan proses ini jarang terjadi pada tanaman monokotil yang perlu penyesuaian
kondisi infeksi. Penyesuaian kondisi dapat berupa penambahan fenolik,
penambahan monosakarida, dan pengurangan pH.
3. Gen chromosomal virulence (chv)
Komponen ini terletak pada kromosom Agrobacterium, yang terdiri atas
chv A, chv B, psc A dan art. Gen chv digunakan untuk pelekatan bakteri ke dalam sel tanaman dengan membentuk senyawa 8-1,2 glukan (Sheng
& Citovsky, 1996).
Kemampuan Agrobacterium menyebabkan tumor disebabkan karena adanya plasmid Ti (tumor inducing) di dalam bakteri yang
akan
menginfeksi tanaman dikotil. Daerah T-DNA dari plasmid Ti ditransfer dan diintegrasikan ke dalam sel tanaman target. Daerah T-DNA mengandung gen-gen penyandi hormon perbmbuhan dan opine. Terintegrasinya T-DNA menyebabkan ekspresigen-gen
untuk
mensintesis hormon pertumbuhan dan opin. Opin digunakan sebagai sumber karbon dan nitrogen bagi Agrobacterium (Sheng & Citovsky 1996).Plasmid Ti dapat diadaptasikan sebagai vektor yang berguna
untuk
transfer gen ke dalam sel tanaman. T-DNA ditentukan oleh adanya sekuensberulang (terdiri dari 25 bp) yang mengapitnya dari bagian kin dan kanan. Sekuens ini diperlukan secara in cis
untuk
trasnfer T-DNA dan merupakan sekuens pengenalanuntuk
situs spesifik endonuklease yang disandi oleh gen virD.Hasil pemotongan adalah molekul utas tunggal linier yang diduga sebagai
intermediet untuk transfer T-DNA ke sel tanaman. Hal ini penting untuk merancang vektor bahwa sekuens pembatas harus mengapit DNA dasar yang akan ditransfer dan m e ~ p a k a n elemen yang beraksi in cis
untuk
transfer T- DNA.Penambahan senyawa fenolik asetosyringone pada tahap kekultivasi bertujuan untuk mengakhpkan gen-gen vir pada Ti plasmid. Proses transfer T-
DNA diawali dengan dideteksinya senyawa fen01 dan te jadinya pengaktifan gen vir. Protein
dari
gen vir A ini akan mengnduksi fosforilasi dari gen vir G yang selanjutnya mengaktifkan gen vir lainnya. Beberapa gen vir berperan &am pemotongan fragmen T-DNA dan pengintegrasian T-DNA ke dalam kromosomsel inang. Integrasi T-DNA
akan
mengalami sedikit pengaturan kembali secara intra dan inter molekuler,untuk
memulihkan system transkripsi dan translasiasetosiringon merupakan kunci keberhasilan transformasi melalui
Agrobacterium pada tanaman padi. Penambahan glukosa, pH media 5.2 serta
suhu ko-kultivasi antara 22-28 "C juga merupakan kondisi optimum yang
diperlukan bagi transformasi padi melalui Agrobacferium (Hiei er al. 1994)
A. tumefaciens mempunyai kemampuan untuk mentransfer potongan
DNA (T-DNA) dari Ti plasmid kedalam nukleus sel-sel yang diinfeksi sehingga
terintegrasi kedalam genom tanaman dan akan menyebabkan crown gall (Nester
er al. 1984).
T-DNA
mengandung dua tipe gen yaitu gen onkogenik yangmengodekan enzim yang dilibatkan dalam sintesis auksin dan sitokonin serta berperan dalam pembentukan tumor, gen kedua berperan mengodekan sintesis
opin. Senyawa ini dihasilkan karena kondensasi antara asam amino dan gula juga
disintesis dan dielaesikan oleh sel-sel crown gall yang kemudian digunakan oleh
Agrobacterium sebagai sumber karbon dan nitrogen. Disamping itu T-DNA
ditempatkan pada gen-gen yang berperan dalam katabolisme opin, gen tersebut
dilibatkan dalam proses transfer T-DNA dari bakteri ke sel tanaman dan
transfer plasmid bakteri konjugatif (Hooykass & Schilperoort 1992).
Regenerasi in virro Tanaman Padi
Tanaman merupakan organisme multiseluler yang kompleks dengan
organ-organ yang memiliki fungsi berbeda. Dengan kemajuan ilmu fisioilogi
tanaman memungkinkan bagian tertentu dari organisme multiseluler tersebut
ditumbuhkan secara terpisah dalam keadaan in vitro. Melalui manipulasi lingkungan tumbuh, bagian-bagian tanaman tersebut dapat diregenersiskan
menjadi tanaman lengkap p i x o n 1985). Regenerasi tanaman merupakan suatu proses perkembangan yang sangat kompleks. Gunawan (1992) menyatakan
bahwa regenerasi Mtur in vitro te rjadi melalui pembentukan organ langsung
dari eksplan, pembentukan embrio langsung dari eksplan, pembentukan organ
melalui kalus serta pembentukan embrio melalui kalus.
Kalus yang diinduksi dari skutelum merupakan bahan awal yang sangat
baik untuk Mtur in vitro padi (Hiei el al. 1994). Chauhan dan Shing (1995) menggunakan media LS + 2mgA2.4-D + 1 mgA kinetin untuk induksi kalus padi
kalus 65.0%96.5% dan kondisi kalus yang kompak, warna putih kekuningan,
bentuk nodular dan sebagian besar embriogenik.
Pemakaian pengatur zat tumbuh yang tepat sangat berpengaruh dalam
keberhasilan regenerasi dalam kultur in vitro padi terutama bagi kelompok rekalsitran. Datta et al. (2001) menggunakan media regenerasi N6 dengan 2 mg4
kinetin dan 1 mg4 NAA pada padi Indica cv. IR72, IR64, IR68899B dan MH63.
Nayak et al. (1997) Menggunakan media MS
+
3mgA BAP+
1 mgA NAA untuk regenerasi padi Indica IR64, sedangkan Alam et a1 (1998) menggunakan mediaregenerasi MS
+
2 mg.1 kinetin + 0.1 mg/l NAA pada pad^ Indica cv. Vaidehi.Hatsillah (1998) menggunakan media regenerasi LS
+
0.3 mg/l BAP+
0.5 mg/lIAA
pada padl lndica cv. Membramo akan tetapi sebagian besarkalus
yang tahanterhadap higromisin tidak berhasil membentuk tunas bahkan kalus didominasi
oleh akar.
Analisis PCR
PCR merupakan teknik analisis tingkat DNA yang dipakai untuk
penggandaan urutan basa DNA spesifik secara in vitro dengan memanfaatkan
cara replikasi DNA dengan bantuan enzim polimerase (Davis et al. 1994). Keuntungan teknik PCR diantaranya adalah analisanya cepat, tidak diperlukan
DNA &lam jumlah banyak, dapat dilakukan pada fase awal pertumbuhan dan
metoda ekstraksi DNAnya relatif sederhana. PCR &pat dipergunakan untuk
mengamplifikasi gen yang telah diintroduksikan ke sel tanaman target untuk
membuktikan keberadaannya. Teknik PCR memunglankan analisis sampel &lam
jurnlah banyak dan waktu singkat untuk mengetahui keberadaan gen yang diintroduksikan (Cha & Thilly 1993; Casas et al. 1995).
PCR te jadi melalui reaksi yang berlangsung secara berseri
dan
berulangdari denaturasi, penempelan primer dan ekstensi atau sintesis yang berlangsung
secara otomatis. Pada tahap pertama, molekul DNA didenaturasi dengan
meningkatkan suhu sampai 95°C selama 30 detik. Tahap selanjutnya suhu reaksi
diturunkan berkisar antara 50 sampai 60°C atau tergantung pada panjang primer
dan tahap terakhir suhu dinaikan lagi sampai 72°C untuk mengaktifkan tag
PCR merupakan metode yang sangat sensitif sehingga dengan satu
molekul DNA dapat memperbanyak DNA menjadi jutaan kali lipat setelah 30-40
siklus PCR. Adapun komponen yang dibutuhkan dalam reaksi PCR adalah DNA
target, primer, deoksynukleoside rriphosphat (dNTP), Taq DNA polymerase,
bufer PCR (Muladno 2002). Sekuen primer yang tepat memunglunkan amplifikasi
hanya terjadi pada fragmen spesifik dan tepat. Primer untuk PCR sebaiknya terdiri
dari 18-28 nukleotida, tidak terdapat duplikat antara k e 2 primer untuk mendeteksi
gen target.
Primer harus bersifat komplemen terhadap DNA target. Semakin pendek
ukuran primer (8-mer), maka semakin tidak spesifik fragmen yang dihasilkan.
Sebaliknya semakin panjang primer (20-mer) maka akan semakin spesifik
fragmen yang dihasilkan. Ukuran primer yang lebih besar dari 30-mer sangat
jarang digunakan. DNA target yang diamplifikasi hendaknya tidak lebih dari 3 kb
dan sebaiknya kurang dari 1 kb (Brown 1996). Spesifisitas primer harus tinggi
dan persen kandungan G + C antara 50-60 % serta mempunyai Tm (OC) kedua primer sebaiknya sama. Zat lain yang penting adalah dNTF' yang merupakan
material utama untuk sintesis DNA baru dalam proses PCR, yang stabil pada
-20°C
untuk
beberapa bulan. dNTP terdiri dari empat senyawa, yaitu dATP,dTTP, dGTP, dan dCTP. Ketidakseimbangan konsentrasi keempat komponen
akan mengurangi kemampuan kinerja enzim Tuq DNA polimerase. Konsentrasi dNTP sebaiknya antara 20-200
pM
(Innis & Gelfand 1990).Enzim polimerase yang digunakan dalam teknik PCR adalah enzim yang
tahan panas supaya pada waktu denaturasi (suhu tinggi) enzimnya tidak rusak. Enzim ini dikenal dengan Tuq DNA polimerase yang diisolasi dari bakteri termofilik Termus aquaticus dan dapat aktif pada suhu 9495°C. Suhu annealing merupakan faktor penting yang menentukan spesifitas suatu PCR. Dengan demikian suhu dan waktu yang digunakan bergantung pada urutan DNA yang akan diamplifikasi. Suhu annealing &pat diduga berdasarkan suhu melting (Tm)
antara primer dengan DNA cetakan. Suhu annealing biasanya lebih rendah 3-5°C
BAHAN DAN METODE
Waktu dan Ternpat
Penelitian dilaksanakan di Laboratorium Biologi Molekuler Puslit
Bioteknologi LIP1 Cibinong, Bogor, pada bulan Pebruari -November 2005.
Bahan
Plasmid pC1300 hpr intron (P. Ouwerkerk, Leiden University, The
Netherlands) digunakan sebagai vektor untuk konstruksi vektor ekspresi dengan
double T-DNA, sedangkan plasmid $1200 @ Jefferson, CAMBIA, Canberra, Australia) digunakan sebagai vektor ekspresi dengan dua sel inang. Gen cryIAb
diisolasi dari plasmid pGem4 cryIAb dan digunakan sebagai gen sasaran pada
vektor ekspresi dengan double T-DNA. Gen ciyIAb dibawah kendali promoter
ubiquitin dan terminator nos dari Bt. Gen SA yang terdii dari pmsB dan entC
diisolasi dari pSA (Verberne 2000) dan digunakan sebagai gen sasaran untuk vektor ekspresi dengan dua sel inang. Gen e& yang berasal dari E. coli dan
pmsB dari P 35s masing-masing dibawah kendali promoter dan terminator pit.
Gen hpr yang terletak pada T-DNA dari pC1300 hpt intron digunakan sebagai
penanda seleksi baik pada vektor dengan double T-DNA maupun pada vektor
ekspresi dengan dua sel inang. Plasmid pC1300 hpt intron diturunkan dari
$1300 dan $1200 Ahp diturunkan dari pC1200. Peta fisik pCl2OO dan
$1300 diijikan pada Gambar 2.
[image:37.530.73.454.147.726.2]Adaptor oligonukleotida yang mengandung LB dan
RB
digunakan untuk merakitplasmid double TDNA. Adaptor tersebut adalah oligonukletida utas 1:
5"ITGGGTAAACCTAAGAGAAAAGAGCGmAAGATCTTGGCAGGATA
TA'ITGTGGTGTAAACAG 3', sedangkan utas 2 adalah 5' CATGCTGTITAC
ACCACAATATATCCTGCAAGATCTTAAACGCTCTTTTCTC'ITAGGTITA
CCCAACAT G 3'.A. tumefaciem galw Agl-1 digunakan sebagai perantara transfer gen yang
terdapat pada T-DNA ke dalam genom tanaman padi. E. coli DHSa digunakan
sebagai inang dalam rekayasa DNA dan pRK2013 digunakan sebagai plasmid
helper. Padi kultivar Rojolele digunakan sebagai bahan untuk hansformasi
genetik dengan vektor ekspresi. Media untuk ko-kultivasi dan regenerasi
tanaman padi disajikan pada Lampiran 1 dan media untuk biakan bakteri
disajikan pada Lampiran 2.
Primer untuk mendeteksi gen cryIAb mempunyai urutan basa sebagai
berikut :forward (5'- CATTGTGTCTCTCTXCC-3') dan reverse (5'-CCGlT
AGAGAAGTTGAAAGG-3'). Untuk mendeteksi keberadaan gen pmsB
digunakan primer dengan: forward 5'ATGCTGCCGCTAAAACCGCCACAA 3'
dan reverse 5' TGACTTGGCCTGCGCCGAGTACGT-3'. Untuk gen hpt
dideteksi dengan primer forward
(5'-GATGCCTCCGCTCGAAGTAGCG-3')
dan reverse (5'-GCATCTCCCGCC GTGCAC-3').
Metodologi
Untuk merakit vektor ekspresi sehiigga penanda seleksi &pat
tereliminasi dilakukan melalui dua strategi yaitu :
1. Menggunakan double T-DNA dalarn satu vektor biner yang mengandung
gen penanda seleksi antibiotik dan gen sasaran cryIAb.
2. Menggunakan dua inang Agrobacterium tumefaciens yang mengandung gen penanda seleksi resisten higromisin pada satu inang dan gen sasaran SA yang terdiri daripmsB dan en& pada inang yang lain.
Kedua vektor ekspresi tersebut kemudian diintroduksikan ke dalam tanaman padi
Strategi 1
MCS
v
Adaptor RB & LB 0RIdengan situs BsrX dan EeoRl
cryIAb
PZTDNA Introduksi daerah gen cryIAb TDNA2 ke MCS pada
Potong dengan enzim H i d 1
[image:39.523.27.430.36.710.2]Ligasi
Konstruksi Vektor yang Mengandung Double T-DNA
Strategi untuk konstmksi vektor ekspresi yang mengandung double
T-DNA dilakukan seperti Gambar 3. Double T-DNA dibuat dengan
menyisipkan adaptor oligonukleotida yang mengandung right border dan l e j border (RB dan LB) pada situs BstXI dan EcoRl dari pC1300 hpt intron. Adaptor
ini mengandung situs BglII dan vektor ini selanjutnya disebut dengan p2TDNA
[image:40.523.83.456.94.559.2]pada situs H i d I I . Kaset cry JAb dibawah promoter ubikuitin dan terminator nos disisipkan kedalam p2TDNA yang kemudian dinamakan dengan p2TDNAcryIAb. Lokasi kaset cryIAb dan kaset hpt intron pada dua T-DNA disajikan pada Gambar 4.
Gambar 4 Lokasi kaset cryIAb dan hpt intron pada T-DNA
Konstruksi Vektor di Dna Inang yang Berbeda
Strategi untuk konstruksi dua vektor ekspresi di dua inang yang berbeda
dilakukan seperti Gambar 5. Pada penelitian ini gen penanda seleksi resistensi
terhadap higromisin sudah diionstruksi di dalam pC1300 hpt intron
(P. Ouwerkerk, Leiden University, The Netherlands) sehingga hanya pC12SA
yang harus diionstruksi.
Gen p m B dan gen entC masing-masing dibawah kendali promotor 35s
CaMV dan terminator pit disisipkan ke &lam situs XbaI dan EcoRl pada
pC1200 yang telah dibuang gen hpr nya yang menjadi pC12SA. Lokasi kaset
p m B dan gen entC pada T-DNA dapat dilihat pada Gambar 6. Vektor ini
selanjutnya dimasukkan ke dalam A. tumefaciens galur AGL-I melalui
Strategi 2
MCS
LB
1
enfl
Gen penyandi biosintesis asam salisilat
MCS
A. tumefaciens A. tumefaciens
[image:41.523.49.429.45.736.2]"
p m s ~ K35.s entc
K
35s7
\J
[image:42.523.53.447.85.751.2]Pit right border
Gambar 6 Lokasi p m B dan gen enrC pada T-DNA dari plasmid pC12SApmB :
penyandi enzim isochorismat gmtthare dari Pseudomonas$uorescenr;
enrC: penyandi enzim i s o p a t lyase dari ficherichia coli; Pit: potato proteinase inhibitor.
Isolasi DNA Plasmid pC1300 hpt inbon dan pC1200
lsolasi DNA plasmid dilakukan dengan prosedur Mini Preps (Sambrook et a1.1989). Sebanyak 1,5 ml kultur bakteri hasil perbanyakan di LB cair, dimasukkan ke tabung ependorf 1,s ml, lalu disentrifus pada 12.000 rpm selama 1 menit Supematan dibuang dan pelet ditambah dengan 100 pl larutan I (Tris HCI
pH 8.0 25 mM, EDTA 10 mM, glukosa 10 mM dan lisozime 2 mglml) lalu
divortex hi~~gga suspensi homogen. Kemudian ditambahkan 200 pl larutan I1
(NaOH 0,s M, SDS I%), dan divortex. Selanjutnya ditambahkan 150 pl larutan
III
(CH3COONa 3 M pH 4,s) dan divortex lalu d i i i b a s i di es selama 15 menit Kemudian disentrifus pada 12.000 rpm selama 15 menit. Supematan ditambah dengan 1 ml etanol absolut kemudian disentrifus pada 12.000 rpm selama 15 menit. Pelet DNA dicuci dengan 1 ml etanol 70% kemudian disentrifus pada12.000 rpm selama 15 menit Supematan dibuang dan pelet diieringkan di suhu
ruang. Setelah kering pelet ditambah dengan 50 p1
TE
(Tris HCI 10 mM pH 8.0EDTA 1mM ) dan dishpan pada suhu -20°C.
Pemotongan pC1300, pCl2OO dan pSA
kembali. Plasmid pC12hpt dipotong dengan enzim Xbal dan EcoRI sedangkan
untuk plasmid pSA yang mengandung gen entC dan pmsB dipotong dengan
menggunakan enzim Xbol, Xbal dan EcoRl dan masing-masing tiagmen
diisolasi.
Isolasi fragmen
Pemurnian fragmen cryIAb dan gen-gen penyandi asam salisilat dari gel
dilakukan dengan menggunakan sephoglass brondprep (BP) kit dari Pharmacia.
Gel yang mengandung DNA sasaran ditimbang kemudian ditambahkan larutan
gel solubilizer (1 pVmg gel) lalu divortex. Selanjutnya campuran diinkubasi pada suhu 60°C selama 10 menit (hingga gel larut). Campuran ini ditambah dengan sephaglass BP 20% lalu divortex d m diinkubasi selama 5 menit pada suhu ruang. Selanjutnya disentrifugasi pada kecepatan 12.000 rpm selama 2 menit. Pelet
dicuci dengan wmh buffer (16 x volume sephaglas BP yang ditambahkan) dan
dipipet naik turun lalu disentrifugasi pada 10.000 rpm selama 30 detik (dilakukan 3x). Pelet dikeringkan dan dilarutkan dalam elution buffer.
Ligasi Oligonukleotida yang mengandung right dan leff border dengan pCl300 hpt intron
Proses ligasi dilakukan sesuai dengan prosedur Promega (1996). Reaksi ligasi terdiri atas DNA pC1300 hpt inhon (100 ng) dan oligonukleotida (300 ng) sebagai sisipan, bufer T4-DNA ligase, enzim T4-DNA ligase