ABSTRAK
RINA SRI RAHAYU. Pengujian Sitotoksisitas
Biphasic Calcium Phosphate
dan
Amorphous Calcium Phosphate
Di dalam
Cell Line
Fibroblas
.
Dibimbing oleh
KIAGUS DAHLAN dan BOY M. BACHTIAR.
Biphasic calcium phosphate
(BCP) dan
amorphous calcium phosphate
(ACP) digunakan sebagai bahan implan karena sifat biokompatibilitasnya. BCP
banyak digunakan sebagai implan tulang sedangkan ACP banyak digunakan
sebagai implan pada gigi. Biokompatibilitas juga dapat diamati melalui pelekatan
antara sel dan bahan implan menggunakan mikroskop elektron. Pengujian
toksisitas dilakukan dengan perlakuan perendaman BCP dan ACP di dalam
cell
line
fibroblas (NHDF) selama 1, 2, dan 3 hari. Hasil penelitian menunjukkan
bahwa BCP dan ACP bersifat tidak toksik dan menginduksi sel-sel untuk tumbuh.
Hasil pengujian sitotoksisitas ini sesuai dengan hasil karakterisasi
scanning
electron microscope
(SEM) yang menunjukkan terjadinya pelekatan antara BCP
atau ACP dengan sel fibroblas setelah 1 hari perendaman. Foto SEM sampel
setelah inkubasi selama 3 hari menunjukkan bahwa sel mulai mengalami polifersi
dan mensekresikan protein kolagen. Sekresi protein kolagen semakin nyata
setelah perendaman selama 14 hari. Jadi, BCP dan ACP yang diperoleh dari
cangkang telur ayam bersifat tidak toksik dan memiliki biokompatibilitas yang
baik dengan sel secara
in vitro
.
Kata kunci
:
Biphasic calcium phosphate, amorphous calcium phosphate, in vitro,
sitotoksisitas.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Kasus kerusakan gigi di Indonesia sering terjadi baik akibat kecelakaan maupun kerusakan akibat gigi berlubang. Kasus kerusakan gigi ini dapat diatasi dengan penggunaan gigi palsu atau penambalan gigi. Sejauh ini belum ditemukan material penambal gigi yang diproduksi dari dalam negeri sehingga material penambal gigi yang biasa digunakan oleh para dokter gigi merupakan produk impor. Peningkatan kasus kerusakan gigi meningkatkan riset pengembangan material penambal gigi di dunia. Riset ini berkembang sejak tahun 1920 dengan bahan penambal seperti emas, perak, titanium, kayu, dan berbagai material komposit gigi.1
Riset pengembangan material penambal ini terus diteliti untuk memperoleh karakteristik yang tepat dan nilai estetik yang tinggi. Emas dan perak merupakan material yang pada mulanya digunakan sebagai bahan pengganti atau penambal gigi, namun kini telah berkembang pesat material dalam bentuk komposit mineral apatit. Penggunaan mineral apatit dirasakan lebih baik karena berkesuaian dengan komponen utama gigi dan warna gigi.2
Tulang dan gigi termasuk jaringan keras yang merupakan organ biologi dinamik yang tersusun atas sel aktif metabiologi yang terintegrasi ke dalam.3 Gigi tersusun atas beberapa mineral antara lain adalah 36% kalsium, 17,7% fosfor, 0,5% natrium, 0,44% flour dan sejumlah kecil ion lainnya.4 Senyawa kalsium fosfat merupakan senyawa yang sesuai dengan komponen penyusun gigi sehingga dapat digunakan sebagai pengisi atau penambal gigi.
Senyawa kalsium fosfat diharapkan mampu menjadi material penambal gigi yang lebih biocompatible.5 Secara terminologi, biocompatibilities dapat
diartikan sebagai kemampuan suatu bahan untuk berkesesuaian dengan jaringan
tubuh, antara lain bersifat tahan terhadap korosi dan tidak menimbulkan reaksi penolakan terhadap jaringan tubuh.
Pengujian biocompatibilities dapat dilakukan dengan uji sitotoksisitasnya. Uji sitotoksisitas ini merupakan salah satu syarat minimum sebagai material komposit (sintetik) yang dapat diimplan ke dalam tubuh makhluk hidup.6
Riset mengenai mineral apatit yang digunakan dalam bidang kedokteran gigi antara lain adalah amorphous calcium phosphate (ACP) dan biphasic calcium phosphate (BCP). ACP mempunyai zat yang digunakan untuk remineralisasi gigi,7 sedangkan BCP terdiri dari dua fase
yaitu hydroxyapatite (HA) dan
β–tricalcium phosphate (β-TCP) yang efektif dalam memperbaiki tulang dan regenerasi terbukti secara in vitro dan in vivo.8
Penelitian ini menggunakan cangkang telur sebagai sumber kalsium dan (NH4)2HPO4 sebagai sumber natrium dan fosfat. Cangkang telur digunakan sebagai prekursor kalsium karena memiliki kandungan kalsium karbonat (CaCO3) sebanyak 94-97%9 dan dapat membentuk karbon monoksida (CaO) dengan proses kalsinasi.10 Pengujian toksisitas pada material BCP dan ACP ini dilakukan dengan perendaman dalam larutan cell line normal human dermal fibroblast (NHDF).
1.2 Tujuan Penelitian
1. Menganalisis efek pemberian material BCP dan ACP dengan cara in vitro terhadap viabilitas sel fibroblas.
2. Menganalisis morfologi dari BCP dan ACP dalam sel fibroblas.
1.3 Perumusan Masalah
1. Apakah pemberian material BCP dan ACP dapat mengakibatkan toksik dan mempengaruhi viabilitas sel fibroblas?
1.4 Hipotesis
1. Material BCP dan ACP tidak bersifat toksik dan dapat mempengaruhi viabilitas sel, ditunjukkan dengan persentase sel kontrol lebih rendah dari sel yang sudah ditambahkan dengan material sampel.
2. Terjadi interaksi berupa perlekatan antara sel fibroblas dengan material BCP maupun ACP.
BAB II
TINJAUAN PUSTAKA
2.1 Biphasic Calcium Phosphate
(BCP)
Biphasic calcium phosphate (BCP), merupakan senyawa apatit yang terdiri dari dua fase yaitu hydroxyapatite ((HA), Ca10(PO4)6(OH)2), dan β-tricalcium phosohate (β-TCP, Ca3(PO4)2), walaupun mempunyai komposisi kimia yang mirip, keduanya memiliki kemampuan penyerapan biologis yang berbeda. HA padat keramik dapat digunakan sebagai implan tulang karena hampir restorable dan bio-inert. Sedangkan β-TCP berpori yang mampu terdegradasi secara biologis dengan laju yang lebih tinggi, bioresorbable dan bioaktif.11
Tingkat kelarutan TCP lebih tinggi dibanding HA dapat digambarkan bahwa HA < β-TCP < α-TCP.4 Oleh karena itu, keramik kalsium fosfat merupakan pilihan yang baik untuk rekonstruksi bedah, ortopedi, kedokteran gigi, dan pembedahan kraniofasial, tulang belakang, dan bedah saraf. Sifat kelarutan BCP tergantung pada rasio β-TCP/HA. Semakin tinggi nilai rasio dan porositasnya maka semakin mudah larut material tersebut.11 BCP dapat terbentuk dari HA yang dipanaskan (sintering) pada 1200°C selama 6 jam. Persamaan reaksi pembentukan TCP adalah sebagai berikut:
Ca10(PO4)6(OH)2→ 3β-Ca3(PO4)2+ CaO + H2O(1)
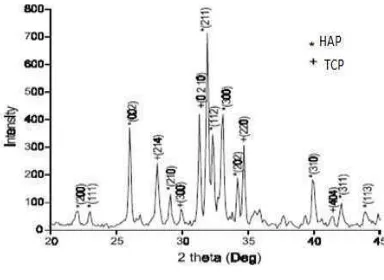
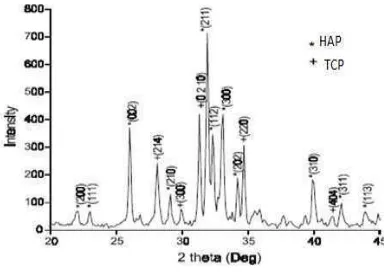
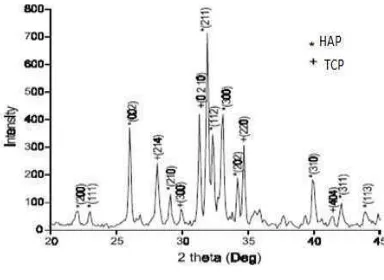
Kumar et al.12 berhasil mensintesis BCP dari proses sintering. Butiran BCP disintesis dari senyawa kalsium hidroksida dan diammonium hydrogen ortho phosphate (DAP) dengan menggunakan microwave. Jumlah reaktan yang digunakan untuk reaksi dihitung berdasarkan perbandingan molar Ca/P sebesar 1,58. Larutan hasil reaksi tersebut kemudian dikeringkan pada suhu 900°C dalam microwave selama 20 menit. Gambar 1 memperlihatkan hasil pola XRD BCP berdasarkan penelitian Kumar et al.12
Gambar 1 Pola Difraksi XRD BCP pada suhu
sintering 900oC.
2.2 Amorphous Calcium Phosphate
(ACP)
Senyawa kalsium fosfat hasil presipitasi dapat berada dalam fase kristalin maupun fase amorf. Fase kristal stabil senyawa kalsium fosfat dikenal sebagai hydroxyapatite (Ca10(PO4)6(OH)2). Fase amorf kalsium fosfat disebut amorphous calcium phosphate (ACP) yang dapat terbentuk pada awal presipitasi. Penggunaan ACP pada email dapat membentuk kristal hydroxyapatite. Mineral yang digunakan ini tentu saja harus tahan terhadap larutan tubuh, tidak mudah terdegradasi, memiliki kekuatan mekanik yang tinggi dan tidak toksik.13
1.4 Hipotesis
1. Material BCP dan ACP tidak bersifat toksik dan dapat mempengaruhi viabilitas sel, ditunjukkan dengan persentase sel kontrol lebih rendah dari sel yang sudah ditambahkan dengan material sampel.
2. Terjadi interaksi berupa perlekatan antara sel fibroblas dengan material BCP maupun ACP.
BAB II
TINJAUAN PUSTAKA
2.1 Biphasic Calcium Phosphate
(BCP)
Biphasic calcium phosphate (BCP), merupakan senyawa apatit yang terdiri dari dua fase yaitu hydroxyapatite ((HA), Ca10(PO4)6(OH)2), dan β-tricalcium phosohate (β-TCP, Ca3(PO4)2), walaupun mempunyai komposisi kimia yang mirip, keduanya memiliki kemampuan penyerapan biologis yang berbeda. HA padat keramik dapat digunakan sebagai implan tulang karena hampir restorable dan bio-inert. Sedangkan β-TCP berpori yang mampu terdegradasi secara biologis dengan laju yang lebih tinggi, bioresorbable dan bioaktif.11
Tingkat kelarutan TCP lebih tinggi dibanding HA dapat digambarkan bahwa HA < β-TCP < α-TCP.4 Oleh karena itu, keramik kalsium fosfat merupakan pilihan yang baik untuk rekonstruksi bedah, ortopedi, kedokteran gigi, dan pembedahan kraniofasial, tulang belakang, dan bedah saraf. Sifat kelarutan BCP tergantung pada rasio β-TCP/HA. Semakin tinggi nilai rasio dan porositasnya maka semakin mudah larut material tersebut.11 BCP dapat terbentuk dari HA yang dipanaskan (sintering) pada 1200°C selama 6 jam. Persamaan reaksi pembentukan TCP adalah sebagai berikut:
Ca10(PO4)6(OH)2→ 3β-Ca3(PO4)2+ CaO + H2O(1)
Kumar et al.12 berhasil mensintesis BCP dari proses sintering. Butiran BCP disintesis dari senyawa kalsium hidroksida dan diammonium hydrogen ortho phosphate (DAP) dengan menggunakan microwave. Jumlah reaktan yang digunakan untuk reaksi dihitung berdasarkan perbandingan molar Ca/P sebesar 1,58. Larutan hasil reaksi tersebut kemudian dikeringkan pada suhu 900°C dalam microwave selama 20 menit. Gambar 1 memperlihatkan hasil pola XRD BCP berdasarkan penelitian Kumar et al.12
Gambar 1 Pola Difraksi XRD BCP pada suhu
sintering 900oC.
2.2 Amorphous Calcium Phosphate
(ACP)
Senyawa kalsium fosfat hasil presipitasi dapat berada dalam fase kristalin maupun fase amorf. Fase kristal stabil senyawa kalsium fosfat dikenal sebagai hydroxyapatite (Ca10(PO4)6(OH)2). Fase amorf kalsium fosfat disebut amorphous calcium phosphate (ACP) yang dapat terbentuk pada awal presipitasi. Penggunaan ACP pada email dapat membentuk kristal hydroxyapatite. Mineral yang digunakan ini tentu saja harus tahan terhadap larutan tubuh, tidak mudah terdegradasi, memiliki kekuatan mekanik yang tinggi dan tidak toksik.13
3
untuk memulihkan 71% dari kerusakan gigi akibat kehilangan mineral. Pada pH rendah, ACP dapat menjadi rusak dan tingkat pelepasan Ca-2 dan PO
4 supersaturating ion. Selain itu, ACP bersifat tidak stabil dan dalam lingkungan air ACP bertransformasi menjadi HA. Kondisi tersebut kondusif untuk remineralisasi gigi.14
Komposisi ACP tidak hanya terdiri atas ion kalsium dan fosfat terdapat ion-ion lain dalam senyawa ACP. Sebagai contoh ion karbonat (CO32-) dengan konsentrasi tinggi ternyata sebagai penghambat proses transformasi dengan menggantikan posisi ion hidroksil dan ion fosfat sehingga membentuk kristal apatit karbonat tipe A dan tipe B, sehingga dapat menghambat proses transformasi dari kalsium fosfat amorf menjadi hydroxyapatite.14
2.3 Fibroblas
Fibroblas adalah sel predominal pulpa yang dapat berasal dari sel mesenkimal pulpa yang tidak berkembang. Fibroblas berbentuk stelat, dengan nuklei ovoid dan prosesus sitoplasmik. Bila bertambah tua menjadi lebih bulat, dengan nuklei bulat dan prosesus sitoplasmik pendek. Perubahan bentuk disebabkan oleh pengurangan aktivitas sel karena bertambah tua.15
Fungsi fibroblas adalah sebagai pembuatan substansi dasar dan serabut kolagen, yang merupakan matriks pulpa. Fibroblas juga berperan dalam degradasi kolagen, deposisi jaringan yang mengapur, membentuk dentine, dan dapat berkembang untuk menggantikan odontoblas yang mati karena memiliki kemampuan untuk memperbaiki dentin. Fibroblas dapat dijumpai pada daerah yang kaya sel pulpa terutama pada daerah coronal.15
Sel-sel fibroblas dermis memainkan peran penting dalam memperbaharui sistem dan untuk mempertahapnkan integritas kulit.16 Sel fibroblas yang akan digunakan dalam pengujian in vitro ini adalah sel fibroblas dermal normal pada manusia (Gambar 2). Para peneliti
mengatakan bahwa meningkatnya jumlah fibroblas akan dapat membantu merevitalisasi pulpa gigi dan mengurangi kemungkinan jaringan pulpa gigi tersebut untuk dibuang.17
Gambar 2 Sel NHDF mikroskopik.18
2.4 In Vitro BCP
Pengujian biocompatibilities secara in vitro dilakukan dengan mendeteksi kerusakan dan kematian sel yang disebut sitotoksitas.19 Uji toksisitas salah satunya dilakukan dengan metodeMTT assay. Uji MTT assay merupakan metode kolorimetrik, dimana larutan pereaksi
[3-(4,5-dimetillthiazol-2-yl)-2,5-difeniltetrazolium bromide] ini yang disebut larutan MTT merupakan garam tetrazolium yang dapat dipecah menjadi kristal formazan oleh sistem suksinat tetrazolium reduktase yang terdapat dalam jalur respirasi sel pada mitokondria yang aktif pada sel yang masih hidup. Kristal formazan ini memberi warna ungu yang dapat dibaca absorbansinya dengan menggunakan mikroplatereader.20
Riberio et al.21 Pada terlihat adanya ikatan material implan.
Gambar 3 Morfologi sel material impla
perendaman) in
dengan mengg
2.5 X-Ray Diffraction
Karakterisasi X (XRD) merupakan tekni untuk mengetahui perubahan fasa, dan de XRD dapat digunakan kualitas kristal suatu ba jenis-jenis unsur dan terkandung dalam kualitatif. Informas diperoleh dari uji struk menggunakan XRD sudut hamburan (2θ) sepanjang sumbu horizont (I) sebagai sumbu vertik material tersebut tersus struktur yang teratur. maksimum dan minim menunjukkan bahwa struktur kristal.
Pada proses te (Gambar 4) yaitu saat be pada bidang P1 dan sejauh d, maka akan terhadap bidang yang dan B. Sementara itu k mencapai maksimum a fasa yang sama. Pada dilihat luas AOC sama karena AC sama denga pantul di 2’ dan 1’ me
a Gambar 3 dapat n antara sel dengan
l osteoblas pada
lan BCP ( 2 hari
in vitro dilihat
ggunakan SEM.21
action (XRD)
X-ray diffraction knik yang digunakan
struktur kristal, n derajat kristalinitas. n untuk mengetahui u bahan, mengetahui dan senyawa yang material secara asi langsung yang ruktur kristal dengan adalah spektrum θ) yang digambarkan izontal dan intensitas rtikal. Atom di dalam rsusun dalam suatu . Adanya intensitas nimum pada difraksi material memiliki terjadinya difraksi t berkas sinar-x jatuh n P2 yang terpisah n terbentuk sudut θ g menumbuk titik A u kedua berkas akan apabila mempunyai da Gambar 4 dapat a dengan luas BOC ngan BC serta sudut empunyai fasa yang
sama jika AC ditambah 2 AC dan merupakan yang dinyatakan denga dengan n adalah bilang sama dengan AC/d se persamaan hukum Bragg n λ = 2d sinθ
Gambar 4 Pola difraksi p memenuhi huk
XRD paling banyak mengidentifikasi minera mineral karena sangat dan hasilnya cepat dan a XRD dihasilkan dan di sebuah alat yang disebut Data yang dikum difraktometer yaitu berupa tunggal.22 Pola XRD memberikan informasi s kuantitatif maupun k komposisi fasa-fasa (mis Pada metode ini ada tig diperhatikan. Pertama maksimum, kedua inten ketiga adalah distribusi fungsi dari sudut difrak memilki pola difraksi y sidik jari manusia. P sinar-X berbagai dikumpulkan dalam da Committee of Pow Standard). Hasil anal sampel yang akan dian fasanya dapat dibanding XRD terukur pada JCPD Perangkat difraktom terdiri atas beberapa ba
4
h BC sama dengan n kelipatan dari λ
ngan 2 AC = n λ
ngan bulat. Sin θ sehingga diperoleh gg sebagai berikut:
(2)
pada bidang kristal ukum Bragg.
ak digunakan untuk ral atau campuran t mudah dilakukan n akurat. Data hasil n dikumpulkan dari ebut difraktometer. umpulkan oleh rupa fragmen kristal RD juga dapat i secara umum baik kualitatif tentang isalnya campuran). tiga hal yang perlu a posisi difraksi ensitas puncak dan usi intersitas sebagai raksi. Setiap bahan yang khas seperti Pola-pola difraksi bahan telah data JCPDS (Joint ower Difraction nalisis pola XRD dianalisis komposisi ngkan dengan pola
DS.
adalah tabung x-ray sebagai sumber biasanya menggunakan sumber CuK atau CoK , direct beam slit, wadah sampel, dan detektor.
Gambar 5 Perangkat difraktrometer.23
2.6 Scanning Electron Microscopy
(SEM)
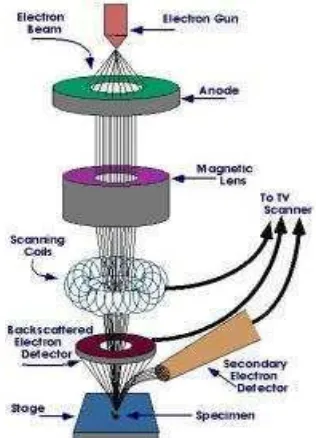
Scanning electron microscopy (SEM) adalah salah satu jenis mikroskop elektron yang menggunakan berkas elektron untuk menggambar profil permukaan benda. Prinsip kerja SEM adalah menembakkan permukaan benda dengan berkas elektron berenergi tinggi. Elektron ini dihasikan oleh sebuah sumber yang disebut electron gun, disejajarkan oleh anoda dan magnetic lens dan difokuskan scanning coil dan detektor. Perangkat mikroskop dapat dilihat pada Gambar 6. Permukaan benda yang dikenai berkas akan memantulkan kembali berkas tersebut atau menghasilkan elektron sekunder ke segala arah. Dari hasil pantulan tersebut ada satu arah dengan intensitas paling tinggi. Pada saat dilakukan pengamatan, lokasi permukaan benda yang ditembak dengan berkas elektron di-scan ke seluruh area daerah pengamatan.24
Elektron sekunder atau elektron pantul yang terdeteksi selanjutnya akan diperkuat sinyalnya. Besarnya amplitudo akan ditampilkan dalam gradasi gelap-terang pada layar monitor cathode ray tube (CRT). Layar CRT ini juga berperan dalam menampilkan gambar struktur
sampel yang sudah diperbesar sehingga bisa dilihat. Hasil karakterisasi SEM menunjukkan morfologi dari sampel uji seperti pada Gambar 3.
Gambar 6 Skema Prinsip Kerja SEM.25
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biofisika Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor dan Laboratorium Fakultas Kedokteran Gigi (FKG) Universitas Indonesia sejak bulan Juli 2010 sampai dengan bulan Mei 2011. 3.2 Bahan dan Alat
3.2.1 Bahan
adalah tabung x-ray sebagai sumber biasanya menggunakan sumber CuK atau CoK , direct beam slit, wadah sampel, dan detektor.
Gambar 5 Perangkat difraktrometer.23
2.6 Scanning Electron Microscopy
(SEM)
Scanning electron microscopy (SEM) adalah salah satu jenis mikroskop elektron yang menggunakan berkas elektron untuk menggambar profil permukaan benda. Prinsip kerja SEM adalah menembakkan permukaan benda dengan berkas elektron berenergi tinggi. Elektron ini dihasikan oleh sebuah sumber yang disebut electron gun, disejajarkan oleh anoda dan magnetic lens dan difokuskan scanning coil dan detektor. Perangkat mikroskop dapat dilihat pada Gambar 6. Permukaan benda yang dikenai berkas akan memantulkan kembali berkas tersebut atau menghasilkan elektron sekunder ke segala arah. Dari hasil pantulan tersebut ada satu arah dengan intensitas paling tinggi. Pada saat dilakukan pengamatan, lokasi permukaan benda yang ditembak dengan berkas elektron di-scan ke seluruh area daerah pengamatan.24
Elektron sekunder atau elektron pantul yang terdeteksi selanjutnya akan diperkuat sinyalnya. Besarnya amplitudo akan ditampilkan dalam gradasi gelap-terang pada layar monitor cathode ray tube (CRT). Layar CRT ini juga berperan dalam menampilkan gambar struktur
sampel yang sudah diperbesar sehingga bisa dilihat. Hasil karakterisasi SEM menunjukkan morfologi dari sampel uji seperti pada Gambar 3.
Gambar 6 Skema Prinsip Kerja SEM.25
BAB III
METODE PENELITIAN
3.1 Tempat dan Waktu Penelitian Penelitian dilakukan di Laboratorium Biofisika Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor dan Laboratorium Fakultas Kedokteran Gigi (FKG) Universitas Indonesia sejak bulan Juli 2010 sampai dengan bulan Mei 2011. 3.2 Bahan dan Alat
3.2.1 Bahan
6
dulbecco’s modified eagle’s medium (DMEM), fetal bovine serum (FBS), penicillin streptomycin, fungizone, trypsin EDTA, trypan blue, phosphate buffered saline (PBS), MTT [3-(4,5-dimethyl thiazol-2-yl)-2-5-diphenyltetrazolium bromide], acidified isopropanol, larutan NaCl, 8% glutaraldehyde, dan ethanol. 3.2.2 Alat
Alat-alat yang digunakan dalam penelitian ini adalah neraca analitik, furnace, heating plate, reaktor hidrotermal, buret, vacum, pH meter digital, beaker glass, crucible, mortar, kertas saring, magnetic stirrer, aluminium foil, gelas ukur, erlenmeyer, gamma radiation sterilization dengan sumber radiasi cobalt-60 (Lampiran 6), 0.2 µ
m-sterile syiringe filter (Corning, Germany), 50 mL-syringe (Terumo, Japan), tube 15 mL and 50 mL (Falcon, USA), scrapper, mikropipet (Eppendorf, Germany), tips micropipette, tube eppendorf (Axygen, USA), hemocytometer, inkubator (Memert), cell culture dish (35 mm×10 mm), 96-well plates (NUNC, Denmark ), mikroskop (Nikon Elipse 80i), biohazard safety cabinet (ESCO Micro PTE Ltd.), water bath, centrifugasi (Sorvall), vortexer (Bio-rad BR 2000), shaker (Certomat), scanning electron microscope (SEM), dan bio-rad microplate reader benchmark visible spectrophotometer. 3.3 Prosedur Penelitian
Prosedur penelitian yang dilakukan terdiri atas 4 tahap yaitu sintesis BCP, sintesis ACP, uji sitotoksisitas, dan karakterisasi. Penelitian ini diawali dengan kalsinasi cangkang telur selama 5 jam pada suhu 1000oC untuk menghasikan CaO yang akan digunakan pada sintesis BCP dan ACP.
3.3.1 Sintesis BCP
Sintesis BCP dilakukan dengan metode hidrotermal. Larutan (NH4)2HPO4 0,67 M sebanyak 100 ml ditambahkan setetes demi setetes kedalam 100 ml larutan CaO 1 M. Reaksi ini dilakukan
pada suhu 300oC selama 8 jam dan diaduk dengan magnetic stirrer dengan kecepatan putaran 300 rpm. Selanjutnya, hasil hidrotermal diendapkan selama 12 jam pada suhu kamar dan disaring di dalam vakum. Sampel basah yang telah disaring kemudian dikeringkan dalam furnace pada suhu 110°C selama 5 jam. Bubuk kering yang diperoleh dihaluskan dengan mortar dan sintering pada 1000°C selama 6 jam.
3.3.2 Sintesis ACP
Sintesis ACP akan dilakukan dengan metode presipitasi suhu rendah. Seratus mililiter (NH4)2HPO4 0,06 M akan ditambahkan setetes demi setetes ke dalam 100 ml larutan CaO 0,1 M. Reaksi ini akan dilakukan selama 8 jam sambil diaduk dengan magnetic stirrer pada kecepatan 300 rpm. Hasil presipitasi akan disaring menggunakan vakum dan dikeringkan menggunakan freeze dryer selama 2 x 24 jam.
3.3.3 Analisis Sitotoksisitas
Persiapan in vitro diawali dengan sterilisasi BCP dan ACP. Material disimpan dalam botol kaca dan setiap botol terisi 2 mg lalu disterilisasi menggunakan radiasi sinar gamma pada dosis 25 kGy. Sebelum melakukan analisis in vitro seluruh alat dan bahan yang akan digunakan diseterilisasi dengan menggunakan sinar ultraviolet (UV) selama 15 menit, dan seluruh prosedur kerja dilakukan dalam biohazard cabinet. 3.3.3.1 Kultur Sel
PBS dan ditambah de EDTA agar pelekatan cawan lepas. Tryps waktu agar dapat be diinkubasi kembali s sebelum dilakukan pr dipindahkan ke tub ditambahkan medium da kemudian disentrifugas 2000 rpm selama 10 me terkonsentrasi menjadi supernatant hasil sentri ditambahkan 5 ml me proses homogenisasi beberapa kali agar terbe
Hasil homogenisa kedalam cawan petri medium kultur lengkap cawan petri mencapai tersebut dimasukan dal suhu 37oC selama 48 bertambah banyak, m tersebut siap dipanen (har 3.3.3.2 Menghitung K
Larutan sel seba 10 µl, dan 10 µl trypa dalam 1,5 ml tabung epp
dengan 1 ml trypsin tan sel pada dasar psin membutuhkan bekerja maka sel selama 10 menit proses scrapping, ube 15 ml, dan dasar. Tube tersebut asi dengan kecepatan menit (24°C) agar sel njadi pellet. Cairan ntrifugasi dibuang dan edium dasar untuk i dengan pippeting
bentuk larutan sel. nisasi sel dipindahkan
ri dan ditambahkan ap hingga volum di i 7 ml. Cawan perti dalam incubator pada 48 jam. Setelah sel maka sel fibroblas
harvesting). ng Konsentrasi Sel
banyak 80 µl, FBS ypan blue dicampur eppendorf. 10 µl dari
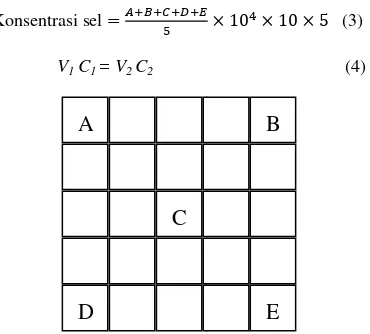
larutan dalam tabu dipindahkan pada papa glass (Gambar 7). Perhi dilakukan dalam papan glass dibawah mikrosk perbesaran 40x. Hemo mempunyai bagian-menghitung sel seperti pa B, C, D, dan E adalah dihitung secara di ba optik. Perhitungan kons digunakan memenuhi per
Konsentrasi sel
V1 C1 = V2 C2
Gambar 7 Skema pembagi
hemocytometer g
Gambar 8 Skema 96-well plates MTT assay.
D
C A
7
abung eppendorf pan hemocytometer
rhitungan sel akan pan hemocytometer oskop optik dengan mocytometer glass
-bagian untuk pada Gambar 7. A, lah letak sel yang bawah mikroskop onsentrasi sel yang persamaan 3 dan 4:
10 10 5 (3)
(4)
gian pada papan
8
Suspensi sel disiapkan dengan konsentrasi 2×105 sel/ml dan dipindahkan pada 96 well plates sebanyak 1 ml setiap wellplate. Gambar 8 menunjukkan skema percobaan sampel pengujian toksisitas. Serbuk BCP danACP dibubuhkan pada well plates dan diinkubasi selama 1, 2, dan 3 hari pada setiap sampel sebagaimana skema yang ditunjukkan pada Gambar 8. Tahap inkubasi dilanjutkan dengan pemberian larutan MTT pada setiap well plate sebanyak 1 µl yang langsung diinkubasi kembali selama 3 jam. Serbuk MTT dilarutkan dengan menggunakan larutan NaCl. Tahap selanjutnya adalah pemberian larutan isopropanol dan pengocokan dengan menggunakan alat shaker selama 1 jam. Kode sampel A adalah sampel blank yang hanya mengandung medium dasar, kode sampel B adalah sel dalam medium (kontrol), kode sampel C adalah sampel BCP yang dibubuhkan pada sel, kode sampel D adalah sampel ACP yang dibubuhkan pada sel. Volum larutan sel yang dipersiapkan, yaitu 5 ml. Konsentrasi sel yang diperoleh dari Persamaan 3 (C1) disetarakan dengan konsentrasi dan volum yang diinginkan (V2, C2) menggunakan Persamaan 4 untuk memperoleh volume V1 yang harus diambil dari 5 ml larutan sel.
Uji MTT assay menunjukkan nilai presentase perbandingan nilai absorbansi dari sampel (BCP dan ACP) terhadap kontrol sebagai viabilitas fibroblas cell line dengan menggunakan persamaan In vitro Technologies sebagai berikut:
!"
# $ "% 100% (5)
Jika presentase viabilitas sel jauh lebih kecil dari viabilitas sel kontrol, maka material yang dipaparkan pada sel tersebut dinyatakan bersifat toksik.24
3.3.3.3 Preparasi Sampel untuk Karakterisasi SEM
Prepapasi sampel ini diawali dengan kultur sel seperti pada analisis sitotoksisitas. Untuk karakterisasi ini sampel dipanen dari media kultur kemudian sampel dicuci dalam PBS, lalu sampel difiksasi dengan menambahkan 2,5% glutaraldehid, setelah itu dibilas dua kali dengan PBS dan dehidrasi etanol secara berurutan (seri). Sampel kemudian dikeringkan pada suhu kamar (27oC) dan dilapisi dengan logam emas sebelum analisis SEM.
3.3.4 Pengujian Sampel
3.3.4.1 Karakterisasi XRD
Karakterisasi XRD menggunakan Shimadzu XRD610 diffractrometer dengan sumber Co-60. Pola XRD ditunjukkan oleh grafik intensitas terhadap sudut 2θ, dengan kisaran 10o-
80° dengan laju 0,02o/sekon. 3.3.4.2 Analisis Sitotoksisitas
dengan Metode MTT Assay
Absorbansi sel dianalisis mengunakan visible spectrophotometer (Bio-Rad Microplate Reader Benchmark) pada panjang gelombang 655 nm. Hasil akhir yang diperoleh dari nilai absorbansi dapat menggambarkan kemampuan viabilitas sel terhadap sampel.
3.3.4.3 Karakterisasi SEM
BAB IV
HASIL DAN PEMBAHASAN
4.1 Sintesis BCP dan ACP
Sintesis BCP dan ACP dilakukan dengan metode yang berbeda, dengan bahan dasar yang sama yaitu CaO dan (NH4)2HPO4. CaO bersumber dari cangkang telur ayam yang telah dikalsinasi 1000o C selama 5 jam berdasarkan penelitian Nurleila et al.10 Proses kalsinasi bertujuan untuk menghilangkan fase karbonat (CO3) dalam cangkang telur yang memiliki kandungan CaCO3 sebesar 94-97% sehingga menjadi CaO.
Penentuan fase pada pola XRD yang diperoleh dibandingkan dengan data JCPDS (Joint Committee on Powder Diffraction Standards) dengan nomor 09-0432 untuk HA, nomor 09-0169 untuk TCP, dan nomor 35-0180 untuk apatit karbonat tipe A (AKA) (Lampiran 7). Pendekatan HA dan TCP digunakan untuk penentuan fase sampel BCP karena BCP mempunyai dua fase yaitu HA dan TCP sedangkan AKA untuk penentuan pola XRD hasil dari sampel ACP.
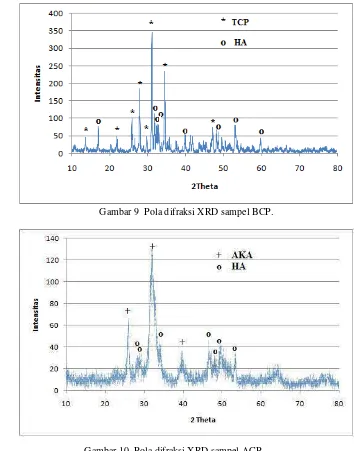
Sintesis BCP menggunakan metode hidrotermal mengacu pada penelitian Fajriyah27 dengan perbandingan molaritas Ca/P 1,67, 1 M CaO dan 0,6 M (NH4)2HPO4. Hasil karakterisasi XRD pada sampel BCP menunjukkan kedua fase dari HA dan TCP sudah terbentuk dengan derajat kristalinitas yang dimiliki sampel BCP ini sebesar 77,90% (Lampiran 13). Tabel 1 dan Tabel 2 merupakan nilai sudut 2θ yang dimiliki oleh fase BCP dan ACP berturut-turut dengan pola XRD ditunjukkan pada Gambar 9 dan Gambar 10.
Tabel 1 Nilai 2θ pada fase BCP
Puncak fase TCP terletak pada 2θ
Puncak fase HA terletak pada 2θ
13,70 31,78
17,09 32,24
25,85 32,90
27,91 39,83
31,11 48,13
32,57 53,04
47,12
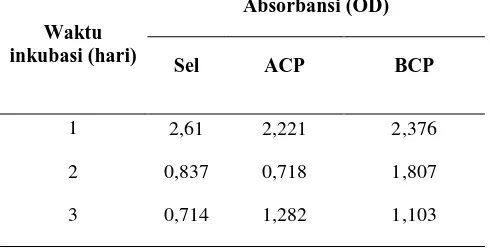
Tabel 2 Nilai 2θ pada fase ACP
Puncak fase AKA terletak pada 2θ
Puncak fase HA terletak pada 2θ
25,93 28,24
32,19 28,88
39,65 34,15
46,67 49,55
ACP merupakan fase amorf dari kristal apatit HA. Sintesis ACP menggunakan metode presipitasi suhu rendah mengacu pada penelitian Laeny28 dengan perbandingan Ca/P sebesar 1,67. Laeny menggunakan beberapa perbandingan molaritas yaitu 1:0,6, 0,5:0,3, dan 0,1:0,06. Perbandingan molaritas yang digunakan pada penelitian ini adalah 0,1 M CaO dan 0,06 M (NH4)2HPO4. Perbandingan molaritas ini digunakan karena pada penelitian Laeny menghasilkan derajat kristalinitas yang paling rendah yaitu sebesar 14,39%.
10
Gambar 9 Pola difraksi XRD sampel BCP.
Gambar 10 Pola difraksi XRD sampel ACP
Hal ini menyebabkan fase amorf dari ACP bertransformasi menjadi fase kristal. Kristal yang terbentuk di antaranya adalah fase kristal HA dan fase apatit karbonat tipe A (AKA). AKA dapat terbentuk karena ion hidroksil (OH) digantikan oleh CO3. Hal ini dapat terjadi karena ACP masih memiliki pengotor seperti CO3 yang dapat mengganggu struktur dari ACP.14
Analisis sitotoksisitas bahan penambal gigi dilakukan melalui pengujian terhadap viabilitas sel fibroblas dengan metode MTT assay. BCP dan
11
yang diambil dari larutan sel adalah 1,73 ml dan penambahan medium sebesar 16,27 ml (Tabel 1). Medium dasar berfungsi sebagai media hidup dan nutrisi untuk sel.29
4.2 Pengujian Sitotoksisitas
Analisis sitotoksisitas bahan penambal gigi dilakukan melalui pengujian terhadap viabilitas sel fibroblas dengan metode MTT assay. BCP dan ACP serbuk diuji dalam cell line NHDF yang merupakan prototype dari sel fibroblas pada pulpa gigi manusia.15 Sel yang telah dikultur kemudian dihitung konsentrasinya untuk membuktikan bahwa sel siap untuk dipanen. Konsentrasi sel hasil pengkulturan sel setelah 2 hari adalah 20,8×105 sel/ml diperoleh dari persamaan 3 dengan nilai A, B, C, D, dan E sebesar 11, 12, 11, 7, dan 11. Konsentrasi tersebut mencukupi untuk tahap inkubasi analisis MTT karena melebihi konsentrasi yang diinginkan yaitu 2×105 sel/ml (Tabel 1). Volume sel yang diambil dari larutan sel adalah 1,73 mL dan penambahan medium adalah 16,27 ml (Tabel 1). Medium dasar berfungsi sebagai media hidup dan nutrisi untuk sel.27
Tabel 3 Konsentrasi dan volume kultur sel.
C2 (sel/ml) C1 (sel/ml) V2 (ml) V1 (ml) medium (ml)
2×105 20,8×105 18 1,73 16,27
Analisis sitotoksisitas menggunakan larutan MTT yang bersifat toksik dan berwarna kuning. Reaksi larutan MTT terhadap sel diindikasikan dengan perubahan warna yang menjadi hitam pekat, sedangkan pemberian larutan MTT pada blank tidak menyebabkan perubahan warna (tetap berwarna kuning seperti larutan MTT). Perubahan warna menjadi hitam merupakan terjadinya reduksi MTT menjadi formazan.20 Derajat kepekatan warna hitam sampel setelah pemberian MTT diukur dengan memanfaatkan prinsip absorbansi. Cahaya yang digunakan adalah warna merah 655 nm agar cahaya diteruskan pada sampel berwarna kuning (sampel blank) dan diserap pada sampel yang berwarna hitam (sampel yang mengandung sel). Tabel 2 menunjukkan data hasil pengukuran absorbansi dari spektrofotometer yang merupakan rata-rata dari 3 kali pengulangan untuk tiap hari waktu inkubasi.
Tabel 4 Absorbansi sel pada sel kontrol, sel dengan implan ACP, dan sel dengan implan BCP.
Waktu inkubasi (hari)
Absorbansi (OD)
Sel ACP BCP
1 2,61 2,221 2,376
2 0,837 0,718 1,807
Gam
Tabel 5 Viabilitas
Waktu inku
0 0.5 1 1.5 2 2.5 3
N
il
ai
A
b
so
rb
an
si
ambar 11 Viabilitas sel bedasarkan nilai absorbansi.
tas sel pada sampel dengan perlakuan waktu inkubasi ya
nkubasi (hari) Sampel Viabilitas sel (%
1
Sel (kontrol) 100,00
Sel+ACP 85,11
Sel+BCP 91,06
2
Sel (kontrol) 100,00
Sel+ACP 85,76
Sel+BCP 215,76
3
Sel (kontrol) 100,00
Sel+ACP 179,61
Sel+BCP 154,53
1 2 3
Waktu inkubasi (Hari)
sel (ko
ACP
BCP
12
yang berbeda.
%)
0 50 100 150 200 250 P e rs e n tas e ( % )
Gambar 12 Persentase via inkubasi 1, 2,
Hasil pengamatan memperlihatkan ada berdasarkan hasil absor kontrol dan sel yang t (persamaan 5). Hal ini medium yang tersedia s sehingga nutrisi untuk juga berkurang. Pada pertama penambahan BCP tidak mempenga Pada hari kedua inkuba mempertahankan viabi lipat dibandingkan de sedangkan ACP mempengaruhi viabilit ketiga kedua mempertahankan viab baik karena lebih dari bertahan dibandingkan de Hal ini membuktikan ba dan BCP bersifat tidak mempertahankan viabil 4.3 Karakterisasi SEM
Karakterisasi SEM mengetahui morfologi 13a, 13b, dan 13c mer pada sel NHDF tanpa pe implan dengan waktu ink hari. Sel NHDF me seperti bulatan kecil saling merekat satu de sehingga membentuk butiran yang saling mel 14 inkubasi tampak sel
1 2 3
Waktu Inkubasi (Hari)
sel (kon
ACP
BCP
viabilitas sel pada kontrol, sampel ACP, dan sampel BC 2, dan 3 hari.
tan viabilitas sel ini danya penurunan orbansi MTT dari sel telah diberi implan ni disebabkan karena a semakin berkurang uk sel bertahan hidup ada inkubasi hari n sampel ACP dan ngaruhi viabilitas sel. ubasi, BCP mampu bilitas sel dua kali dengan sel kontrol, masih belum bilitas sel. Pada hari sampel dapat abilitas sel dengan ari 50% sel mampu n dengan sel kontrol. n bahwa sampel ACP k toksik dan mampu bilitas sel.
EM
M digunakan untuk ogi sampel. Gambar erupakan foto SEM npa penambahan bahan u inkubasi 1, 3 dan 14 mempunyai struktur il yang teratur dan dengan yang lainnya uk seperti tumpukan elekat. Hari ke 3 dan sel mulai berpolifersi
dan memproduksi matrik sehingga bentuk sel s terlihat. Sel fibroblas me jaringan ikat sehi membentuk kolagen.15 terbentuk dalam pene memiliki derajat kris 62.57% sehingga sudah kristal yang teratur seper BCP memiliki kristalin tinggi sehingga memili lebih teratur.
Gambar 14 dan 15 SEM sel dengan pen yaitu BCP (Gambar (Gambar 15). Pada hari bentuk butiran kristal masih jelas terlihat dan sel juga sudah dapat ter dengan perlekatan yang seluruh struktur AC Morfologi sel dengan pe ACP dan BCP pada ha menunjukkan hasil yang hari ke-3 inkubasi belum perubahan morfologi s dengan implan BCP. Hal bahwa BCP lebih muda dengan sel dibandingk ditunjukkan pula dengan pada analisis sitotoksisita ke-2 inkubasi dapat viabilitas sel dua kali lipa pada sel kontrol dan se ACP. Selain itu, ACP da tingkat kelarutan yang
13
kontrol)
CP setelah waktu
triks ekstra seluler29 sudah tidak jelas merupakan sel pada ehingga mampu 15 ACP yang nelitian ini sudah ristalinitas sebesar h memiliki struktur perti HA sedangkan linitas yang lebih iliki struktur yang 15 merupakan foto penambahan implan r 14) dan ACP ri pertama inkubasi l BCP dan ACP dan interaksi dengan erlihat, ditunjukkan ng hampir menutupi CP dan BCP. penambahan implan
(a)
(a)
memiliki fase TCP kelarutannya lebih t sehingga lebih cepat berpolifersi dan mens kolagen atau mem ekstraseluler.30 Se membutuhkan waktu
Gambar 13 Foto SEM dengan 20.000
Gambar 14 Foto SEM hari, dan (c
Gambar 15 Foto SEM (b) 3 hari (a)
(b)
(b) CP yang tingkat
tinggi dari HA4 pat berinteraksi dan
sekresikan protein embentuk makriks Sedangkan ACP u yang lebih lama
dibandingkan BCP untuk dan memproduksi matrik
Foto SEM setelah baik pada BCP maupun memperlihatkan terja kolagen dan interaksiny implan (Gambar 14c dan
M sel NHDF setelah inkubasi (a) 1 hari, (b) 3 har 20.000 kali perbesaran.
M sel NHDF dengan implan BCP setelah inkubas c) 14 hari dengan 20.000 kali perbesaran.
EM sel NHDF dengan implan ACP setelah ink ri, dan (c) 14 hari dengan 20.000 kali perbesaran.
(b)
14
(c)
(c)
untuk berpoliferasi sel riks kolagen.
inkubasi 14 hari upun ACP semakin rjadinya matriks inya dengan bahan dan 15c).
ri, dan (c) 14 hari
ubasi (a) 1 hari, (b) 3
BAB V
KESIMPULAN
5.1 Kesimpulan
Sintesis BCP dan ACP pada penelitian ini menggunakan sumber kalsium dari cangkang telur ayam. Fase BCP yang dihasilkan terdiri dari dua fase, TCP dan HA dengan 3 puncak tertinggi dimiliki oleh fase TCP. Sedangkan sintesis ACP menghasilkan fase AKA dan HA dengan derajat kristalinitas sebesar 62,57% hal ini dapat disebabkan oleh faktor pengeringan menggunakan frezee drying lebih dari 1x24 jam.
Berdasarkan analisis secara in vitro dibuktikan bahwa bahan implan BCP dan ACP bersifat tidak toksik terbukti dengan pengujian toksisitas yang dilakukan dengan perlakuan perendaman BCP dan ACP di dalam cell line fibroblas (NHDF) selama 1, 2, dan 3 hari. Viabilitas sel yang direndam dengan BCP dan ACP hari ke-1 perendaman, tidak mempengaruhi viabilitas sel, sedangkan hari ke-2 dan hari ke-3 perendaman viabilitas selnya lebih dari sel kontrol. BCP menginduksi sel lebih cepat dari pada ACP. Hari kedua
perendaman BCP mampu
mempertahankan sel 2 kali lipat lebih banyak dibandingkan sel kontrol sedangkan ACP di hari ketiga perendaman mampu mempertahankan sel 57% lebih besar dari sel kontrol. Hasil ini menunjukkan bahwa BCP dan ACP bersifat tidak toksik dan menginduksi sel-sel untuk tumbuh.
Hasil pengujian MTT ini sesuai dengan hasil karakterisasi scanning electron microscope (SEM) yang menunjukkan terjadinya pelekatan antara BCP atau ACP dengan sel fibroblas setelah 1 hari perendaman. Foto SEM sampel setelah inkubasi selama 3 hari menunjukkan bahwa sel mulai mengalami poliferasi dan mensekresikan protein kolagen. Sekresi protein kolagen semakin terlihat setelah perendaman selama 14 hari. Jadi, BCP dan ACP yang diperoleh dari cangkang telur bersifat tidak toksik dan memiliki biokompatibilitas yang baik
dengan sel secara in vitro dan memungkinkan untuk selanjutnya bahan implan dianalisis secara in vivo.
5.2 Saran
Sintesis ACP pada suhu rendah sebaiknya dilakukan frezee drying selama 1 x 24 jam karena proses frezee drying yang lebih lama akan timbul pembentukan fase kristal yang lebih banyak. Prosedur analisis in vitro memerlukan keahlian dan ketelitian agar tidak terjadi kontaminasi terhadap sel dan selanjutnya dapat dilakukan pula analisis MTT dengan sel odontoblas atau stem cell karena untuk menjadi bahan penambal yang baik sampel juga harus dapat berinteraksi dengan sel odontoblas, karena sel odontoblas merupakan sel pembentuk dentin30 dan stem cell merupakan sel induk atau sel yang belum matang yang belum berdiferensiasi menjadi sel atau jaringan tertentu.31
Berdasarkan hasil in vitro dapat dilakukan pula penelitian lanjutan secara in vivo untuk menguji sitotoksisitas dalam kondisi tubuh makhluk hidup yang sesungguhnya. Pengujian poliferasi sel dan sekresi protein perlu dibuktikan dengan dilakukan tes kuantifikasi sehingga banyaknya kolagen yang terbentuk oleh sel fibroblas dapat dihitung.
DAFTAR PUSTAKA
1. Oliveira M, Mansur HS. Synthetic tooth enamel: SEM characterization of a fluoride hydroxyapatite coating for dentistry applications. Mat. Res 2007; 2:10.
2. LeGeros RZ. Calcium phosphate in oral biology and medicine. Monograph in Oral Sciences 1991; Vol 15.
PENGUJIAN S
PHOSPHA
PHOSPHATE
FAKULTAS MA
AN SITOTOKSISITAS BIPHASIC C
HATE DAN AMORPHOUS CALC
TE DI DALAM CELL LINE FIBR
RINA SRI RAHAYU
DEPARTEMEN FISIKA
ATEMATIKA DAN ILMU PENGETAHU
INSTITUT PERTANIAN BOGOR
BOGOR
2011
IC CALCIUM
LCIUM
IBROBLAS
16
4. Shi D. Biomaterials and Tissue Engineering. New York: Springer; 2003.
5. Betts F, Blumenthal NC, Posner AS. Bone mineralization. J. Crys. Growth 1981; 53:63-73.
6. Zhang, M. Biomaterials and tissue engineering. Springer-Verlag Berlin Heidelberg 2004; 83-143.
7. Fostera JA, Berzinsb DW, Bradleyc TG. Bond strength of an amorphous calcium phosphate-containing orthodontic adhesive. Angel Orthodontist 2008; 78:2.
8. Ramay HRR, Zhang M. Biphasic calcium phosphate nanocomposite porous scaffolds for load-bearing bine tissue engineering. Biomaterials 2004; 25: 5171-5180.
9. Prabakaran K, Balamurugan A, Rajeswari S. Development of calcium phosphate based apatite from hen’s eggshell. Bull. Mater. Sci 2005; 28: 115-119.
10. Nurlaela A, Dewi SU, Dahlan K, Soejoko DS. The use of eggshells as calcium sources for synthesis of bone mineral. Proceeding of the 1st International Seminar on Science and Technology; 24-25 Jan 2009. 11. Lobo SE, Arinzeh TL. Biphasic
calcium phosphate ceramics for bone regeneration and tissue engineering applications. Materials 2010; 3:815-826.
12. Kumar, K L. Kumar T.S.S., Sunder M., Babu N. R., Victor S. P. Biphasic calcium phosphates for antibiotic release. Trends biomater. Artif. Organ 2005; 18: 2.
13. Uysal T, Amasyali M, Koyuturk
AE, Sagdic D. Efficiency of
amorphous calcium phosphate–
containing orthodontic composite and resin modified glass ionomer on
demineralization evaluated by a new
laser fluorescence device. Eur J Dent
2009;3(2): 127–134.
14. Sinyaev VA, Le Geros R, Levchenko LV, Shustikova ES, Karzhaubaeva RA. State of water in amorphous calcium and calcium– magnesium phosphates. Russian Journal of General Chemistry 2008; 78(5): 864–867.
15. Grossman L I, Seymour Oliet, Carlos E Del Rio. Ilmu Endodontik dalam Praktek. Abyon R, Penerjemah; Suryo S, editor. Jakarta: Penerbit buku kedokteran EGC. Terjemahan dari: Endodoctic Practice Eleventh edition; 1995. 16. Patlolla A, Knighten B, Tchounwou
P. Multi-walled carbon nanotubes induce cytotoxicity, genotoxicity and apoptosis in normal human dermal
fibroblast cells. Ethn Dis 2010;
20(1): 65-72.
17. Hamsafir E. Pusat kesehatan gigi dan mulut. [Terhubung Berkala] www.Infogigi.com [30 Juni 2010]. 18. [Anonim1]. Normal human dermal
fibroblast. [Terhubung Berkala] http://www.invitrogen.com [ 4 Juni 2010].
19. Coelho MJ, Cabral AT, Fernandes MH. Human bone cell cultures in biocompatibility testing. Part I: Osteoblastic differentialtion of serially passaged human bone marrow cell cultured in a-MEM adan in DMEM. Biomaterials 2000; 21: 1087-1094.
17
21. Ribeiro C, Rojas-Cabrera WI, Marques M, Bressiani JC, Bressiani AHA. In vitro characterization of porous ceramic based calcium phosphate processing with albumin. Key Engineering Materials 2009; 396-398: 27-30.
22. Rakovan J. X-ray diffraction (XRD). Rocks & Minerals 2004; 79: 351-353.
23. Connolly J. Introduction to X-ray powder diffraction. Spring 2007; 1-9.
24. Abdullah M, Khairurrijal. Review: Karakterisasi nanomaterial. J Nano Saintek 2009; 2 (1):1-9.
25. Harsas NA. Efek pemberian graf tulang berbentuk pasta dengan berbagai komposisi dan kosentrasi terhadap viabilitas sel osteoblas, In Vitro. [skripsi] Jakarta: Fakultas Kedokteran Gigi, Unifersitas Indonesia; 2008.
26. [Anonim2]. Perangkat scaning elektron microscopy. [terhubung berkala]
http://mse.iastate.edu/microscopy/col lege.html. [20 Juli 2010].
27. Fajriyah HI. Hydrothermal synthesis of biphasic calcium phosphate [tesis]. Bogor: Program Pascasarjana, Insitut Pertanian Bogor; 2010.
28. Laeny AN. Synthesis of amorphous calcium phosephate by low temperature-precipitation methode from eggshell [Skripsi]. Bogor: Department of Physics Mathematics and Natural Sciences Faculty Bogor Agricultural University; 2008. 29. Lin FH, Liao CJ, Liu HC, Chen KS,
Sun JS. Behavior of fetal rat osteoblasts cultured in vitro on the DP-bioactive glass substratum. Materials Chemist and Physics 1997; 49: 270-276.
30. Mozartha M. A-Z gigi dan mulut. [Terhubung Berkala] http://www.klikdokter.com/gigimulu t/read/2010/07/05/49/pulpa. 2010; [2 April 2011]
31. Mozartha M. Terapi stem cell harapan masa depan. [Terhubung Berkala]
PENGUJIAN S
PHOSPHA
PHOSPHATE
FAKULTAS MA
AN SITOTOKSISITAS BIPHASIC C
HATE DAN AMORPHOUS CALC
TE DI DALAM CELL LINE FIBR
RINA SRI RAHAYU
DEPARTEMEN FISIKA
ATEMATIKA DAN ILMU PENGETAHU
INSTITUT PERTANIAN BOGOR
BOGOR
2011
IC CALCIUM
LCIUM
IBROBLAS
PENGUJIAN S
PHOSPHA
PHOSPHATE
FAKULTAS MA
AN SITOTOKSISITAS BIPHASIC C
HATE DAN AMORPHOUS CALC
TE DI DALAM CELL LINE FIBR
RINA SRI RAHAYU
DEPARTEMEN FISIKA
ATEMATIKA DAN ILMU PENGETAHU
INSTITUT PERTANIAN BOGOR
BOGOR
2011
IC CALCIUM
LCIUM
IBROBLAS
ABSTRAK
RINA SRI RAHAYU. Pengujian Sitotoksisitas
Biphasic Calcium Phosphate
dan
Amorphous Calcium Phosphate
Di dalam
Cell Line
Fibroblas
.
Dibimbing oleh
KIAGUS DAHLAN dan BOY M. BACHTIAR.
Biphasic calcium phosphate
(BCP) dan
amorphous calcium phosphate
(ACP) digunakan sebagai bahan implan karena sifat biokompatibilitasnya. BCP
banyak digunakan sebagai implan tulang sedangkan ACP banyak digunakan
sebagai implan pada gigi. Biokompatibilitas juga dapat diamati melalui pelekatan
antara sel dan bahan implan menggunakan mikroskop elektron. Pengujian
toksisitas dilakukan dengan perlakuan perendaman BCP dan ACP di dalam
cell
line
fibroblas (NHDF) selama 1, 2, dan 3 hari. Hasil penelitian menunjukkan
bahwa BCP dan ACP bersifat tidak toksik dan menginduksi sel-sel untuk tumbuh.
Hasil pengujian sitotoksisitas ini sesuai dengan hasil karakterisasi
scanning
electron microscope
(SEM) yang menunjukkan terjadinya pelekatan antara BCP
atau ACP dengan sel fibroblas setelah 1 hari perendaman. Foto SEM sampel
setelah inkubasi selama 3 hari menunjukkan bahwa sel mulai mengalami polifersi
dan mensekresikan protein kolagen. Sekresi protein kolagen semakin nyata
setelah perendaman selama 14 hari. Jadi, BCP dan ACP yang diperoleh dari
cangkang telur ayam bersifat tidak toksik dan memiliki biokompatibilitas yang
baik dengan sel secara
in vitro
.
Kata kunci
:
Biphasic calcium phosphate, amorphous calcium phosphate, in vitro,
sitotoksisitas.
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi yang berjudul
Pengujian
Sitotoksisitas Biphasic Calcium Phosphate dan Amorphous Calcium
Phosphate Di dalam Cell Line Fibroblas
adalah benar-benar hasil karya saya
sendiri di bawah bimbingan Dr. Kiagus Dahlan dan Prof. drg. Boy M Bachtiar,
MS, PhD. dan belum pernah dipublikasikan sebagai karya ilmiah pada perguruan
tinggi atau lembaga manapun. Sumber informasi yang berasal atau dikutip dari
karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan
dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Bogor, Mei 2011
Judul :
Pengujian Sitotoksisitas
Biphasic Calcium Phosphate
dan
Amorphous Calcium Phosphate
Di dalam
Cell Line
Fibroblas.
Nama :
Rina Sri Rahayu
NIM :
G74070003
Disetujui,
Dr. Kiagus Dahlan
Pembimbing I
Prof. drg. Boy M Bachtiar, MS, PhD
Pembimbing II
Diketahui:
Dr.Ir. Irzaman, M.Si
Ketua Departemen Fisika
PENGUJIAN SITOTOKSISITAS BIPHASIC CALCIUM
PHOSPHATE DAN AMORPHOUS CALCIUM
PHOSPHATE DI DALAM CELL LINE FIBROBLAS
RINA SRI RAHAYU
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Fisika
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
RIWAYAT HIDUP
Penulis dilahirkan di Sukabumi, 13 Agustus
1989 dari pasangan Asep Sulaeman dan Rustiyati.
Penulis merupakan anak ke dua dari empat bersaudara.
Penulis menyelesaikan pendidikan Sekolah Dasar
hingga Sekolah Menengah Atas di Sukabumi yaitu SD
Negeri 1 Sukaraja, SMP Negeri 1 Sukaraja, dan SMA
Negeri 5 Sukabumi.
KATA PENGANTAR
Puji syukur kepada Allah Subhanahu wa Ta’ala, atas segala rahmat, nikmat
kesehatan, kekuatan, karunia, dan hidayah-Nya sehingga penelitian untuk tugas
akhir yang berjudul “Pengujian Sitotoksisitas
Biphasic Calcium Phosphate
dan
Amorphous Calcium Phosphate
Di dalam
Cell Line
Fibroblas” dapat
diselesaikan
.
Tugas akhir ini disusun sebagai salah satu syarat kelulusan program
sarjana di Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam,
Institut Pertanian Bogor.
Pada kesempatan ini penulis mengucapkan terima kasih kepada:
1.
Bapak Dr. Kiagus Dahlan dan Bapak Prof. drg. Boy M Bachtiar, MS, PhD.
selaku pembimbing yang telah memberikan bimbingan, masukan, dan
koreksi yang sangat berarti dalam penulisan skripsi ini.
2.
Bapak Abd. Djamil Husin, M.Si dan Bapak Ardian Arif, M.Si selaku
penguji yang telah banyak memberikan masukan dan saran demi perbaikan
skripsi ini.
3.
Ibu Setia Utami Dewi, M.Si dan Mba Nur Aisyah Nuzulia, S.Si yang telah
membantu dalam pengolahan data serta atas waktu yang diluangkan untuk
berdiskusi.
4.
Mba May dan Mba Desi yang bersedia meluangkan waktunya dan
membantu dalam proses penelitian di laboratorium Oral Biologi FKG UI.
5.
Orang tua, adik, dan kakak penulis yang selalu memberikan do’a, dukungan,
cinta dan kasih sayang yang tidak terhitung.
6.
Teman-teman seperjuangan Fisika 44 dan sahabat liqo tercinta yang saling
mendukung dan memberikan semangat dalam penyelesaian skripsi ini.
Penulis menyadari bahwa penelitian tugas akhir ini jauh dari sempurna, oleh
karena itu, saran dan kritik yang bersifat membangun sangat penulis harapkan
demi kemajuan dari aplikasi material yang dikembangkan ini dan semoga tugas
akhir ini bermanfaat bagi semuanya.
Bogor, Mei 2011
DAFTAR ISI
halaman
DAFTAR TABEL ...
iv
DAFTAR GAMBAR ...
v
DAFTAR LAMPIRAN ...
vi
BAB 1 PENDAHULUAN ...
1
1.1 Latar Belakang ...
1
1.2 Tujuan Penelitian ...
1
1.3 Perumusan Masalah ...
1
1.4 Hipotesis ...
2
BAB 2 TINJAUAN PUSTAKA ...
2
2.1
Biphasic Calcium Phosphate
(BCP) ...
2
2.2
Amorphous Calcium Phosphate
(ACP) ...
2
2.3 Fibroblas ...
3
2.4
In Vitro
BCP ...
3
2.5
X-Ray Diffaction
(XRD) ...
4
2.6
Scanning Electron Microscopy
(SEM) ...
5
BAB 3 METODE PENELITIAN...
5
3.1 Waktu dan Tempat Penelitian ...
5
3.2 Bahan dan Alat ...
5
3.2.1 Bahan ...
5
3.2.1 Alat ...
6
3.3 Prosedur Penelitian ...
6
3.3.1 Sintesis BCP ...
6
3.3.2 Sintesis ACP...
6
3.3.3 Analisis Sitotoksisitas ...
6
3.3.3.1 Kultur Sel ...
6
3.3.3.2 Menghitung Konsentrasi Sel ...
7
3.3.3.3 Preparasi Sampel untuk Karakterisasi SEM` ...
8
3.3.4 Pengujian Sampel ...
8
3.3.4.1 Karakterisasi XRD ...
8
3.3.4.2 Analisis Sitotoksisitas dengan Metode MTT
Assay ...
8
iii
DAFTAR TABEL
halaman
Tabel 1 Nilai 2
θ
pada fase BCP………... 9
Tabel 2 Nilai 2
θ
pada fase ACP ... 9
Tabel 3 Konsentrasi dan volume kultur sel ... 11
Tabel 4 Absorbansi sel pada sel kontrol, sel dengan implan ACP, dan sel
DAFTAR GAMBAR
[image:33.595.84.517.94.764.2]halaman
Gambar 1 Pola difraksi XRD BCP pada suhu sintering 900
oC ...
2
Gambar 2 Sel NHDF secara mikroskopik ...
3
Gambar 3 Morfologi sel osteoblas dilihat pada material implan BCP
(2 hari perendaman)
in vitro
dilihat dengan menggunakan SEM .
4
Gambar 4 Pola difraksi pada bidang kristal memenuhi hukum Bragg ...
4
Gambar 5 Perangkat difraktometer ...
5
Gambar 6 Skema prinsip kerja SEM ...
5
Gambar 7 Skema pembagian pada papan
hemocytometer glass
...
7
Gambar 8 Skema 96-
well plates
MTT
assay
...
7
Gambar 9 Pola difraksi XRD sampel BCP ... 10
Gambar 10 Pola difraksi XRD sampel ACP ... 10
Gambar 11 Grafik viabilitas sel berdasarkan nilai absorbansi... 12
Gambar 12 Persentase viabilitas sel pada kontrol, sampel ACP, dan sampel
BCP setelah waktu inkubasi 1, 2, dan 3 hari ... 13
Gambar 13 Foto SEM sel NHDF setelah inkubasi (a) 1 hari, (b) 3 hari, dan
(c) 14 hari ... 14
Gambar 14 Foto SEM sel NHDF dengan implan BCP setelah inkubasi
(a) 1 hari, (b) 3 hari, dan (c) 14 hari ... 14
Gambar 15 Foto SEM sel NHDF dengan implan ACP setelah inkubasi
(a) 1 hari,(b) 3 hari, dan (c) 14 hari ... 14
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Diagram alir penelitian ...
19
Lampiran 2 Peralatan yang digunakan untuk sintesis ACP dan BCP ..
21
Lampiran 3 Peralatan yang digunakan untuk kultur sel dan uji
sitotoksisitas ...
22
Lampiran 4 Alat yang digunakan untuk sterilisasi ...
23
Lampiran 5 Database JCPDS fase (a) AKA, (b) HA, dan (c) TCP ...
24
Lampiran 6 Hasil pengolahan data ACP ...
25
Lampiran 7 Hasil pengolahan data BCP ...
26
Lampiran 8 Perhitungan parameter kisi untuk fase HA dari sampel
ACP ...
28
Lampiran 9 Perhitungan parameter kisi untuk fase HA dari sampel
BCP ...
29
Lampiran 10 Perhitungan parameter kisi untuk fase TCP dari sampel
BCP ...
30
Lampiran 11 Derajat kristalinitas BCP ...
32
Lampiran 12 Derajat kristalinitas ACP...
33
Lampiran 13 Foto SEM sel NHDF dengan beberapa variasi perbesaran
34
Lampiran 14 Foto SEM sel dengan implan BCP pada beberapa variasi
perbesaran ...
35
Lampiran 15 Foto SEM sel dengan implan ACP pada beberapa variasi
BAB I
PENDAHULUAN
1.1 Latar Belakang
Kasus kerusakan gigi di Indonesia sering terjadi baik akibat kecelakaan maupun kerusakan akibat gigi berlubang. Kasus kerusakan gigi ini dapat diatasi dengan penggunaan gigi palsu atau penambalan gigi. Sejauh ini belum ditemukan material penambal gigi yang diproduksi dari dalam negeri sehingga material penambal gigi yang biasa digunakan oleh para dokter gigi merupakan produk impor. Peningkatan kasus kerusakan gigi meningkatkan riset pengembangan material penambal gigi di dunia. Riset ini berkembang sejak tahun 1920 dengan bahan penambal seperti emas, perak, titanium, kayu, dan berbagai material komposit gigi.1
Riset pengembangan material penambal ini terus diteliti untuk memperoleh karakteristik yang tepat dan nilai estetik yang tinggi. Emas dan perak merupakan material yang pada mulanya digunakan sebagai bahan pengganti atau penambal gigi, namun kini telah berkembang pesat material dalam bentuk komposit mineral apatit. Penggunaan mineral apatit dirasakan lebih baik karena berkesuaian dengan komponen utama gigi dan warna gigi.2
Tulang dan gigi termasuk jaringan keras yang merupakan organ biologi dinamik yang tersusun atas sel aktif metabiologi yang terintegrasi ke dalam.3 Gigi tersusun atas beberapa mineral antara lain adalah 36% kalsium, 17,7% fosfor, 0,5% natrium, 0,44% flour dan sejumlah kecil ion lainnya.4 Senyawa kalsium fosfat merupakan senyawa yang sesuai dengan komponen penyusun gigi sehingga dapat digunakan sebagai pengisi atau penambal gigi.
Senyawa kalsium fosfat diharapkan mampu menjadi material penambal gigi yang lebih biocompatible.5 Secara terminologi, biocompatibilities dapat
diartikan sebagai kemampuan suatu bahan untuk berkesesuaian dengan jaringan
tubuh, antara lain bersifat tahan terhadap korosi dan tidak menimbulkan reaksi penolakan terhadap jaringan tubuh.
Pengujian biocompatibilities dapat dilakukan dengan uji sitotoksisitasnya. Uji sitotoksisitas ini merupakan salah satu syarat minimum sebagai material komposit (sintetik) yang dapat diimplan ke dalam tubuh makhluk hidup.6
Riset mengenai mineral apatit yang digunakan dalam bidang kedokteran gigi antara lain adalah amorphous calcium phosphate (ACP) dan biphasic calcium phosphate (BCP). ACP mempunyai zat yang digunakan untuk remineralisasi gigi,7 sedangkan BCP terdiri dari dua fase
yaitu hydroxyapatite (HA) dan
β–tricalcium phosphate (β-TCP) yang efektif dalam memperbaiki tulang dan regenerasi terbukti secara in vitro dan in vivo.8
Penelitian ini menggunakan cangkang telur sebagai sumber kalsium dan (NH4)2HPO4 sebagai sumber natrium dan fosfat. Cangkang telur digunakan sebagai prekursor kalsium karena memiliki kandungan kalsium karbonat (CaCO3) sebanyak 94-97%9 dan dapat membentuk karbon monoksida (CaO) dengan proses kalsinasi.10 Pengujian toksisitas pada material BCP dan ACP ini dilakukan dengan perendaman dalam larutan cell line normal human dermal fibroblast (NHDF).
1.2 Tujuan Penelitian
1. Menganalisis efek pemberian material BCP dan ACP dengan cara in vitro terhadap viabilitas sel fibroblas.
2. Menganalisis morfologi dari BCP dan ACP dalam sel fibroblas.
1.3 Perumusan Masalah
1. Apakah pemberian material BCP dan ACP dapat mengakibatkan toksik dan mempengaruhi viabilitas sel fibroblas?
1.4 Hipotesis
1. Material BCP dan ACP tidak bersifat toksik dan dapat mempengaruhi viabilitas sel, ditunjukkan dengan persentase sel kontrol lebih rendah dari sel yang sudah ditambahkan dengan material sampel.
2. Terjadi interaksi berupa perlekatan antara sel fibroblas dengan material BCP maupun ACP.
BAB II
TINJAUAN PUSTAKA
2.1 Biphasic Calcium Phosphate
(BCP)
Biphasic calcium phosphate (BCP), merupakan senyawa apatit yang terdiri dari dua fase yaitu hydroxyapatite ((HA), Ca10(PO4)6(OH)2), dan β-tricalcium phosohate (β-TCP, Ca3(PO4)2), walaupun mempunyai komposisi kimia yang mirip, keduanya memiliki kemampuan penyerapan biologis yang berbeda. HA padat keramik dapat digunakan sebagai implan tulang karena hampir restorable dan bio-inert. Sedangkan β-TCP berpori yang mampu terdegradasi secara biologis dengan laju yang lebih tinggi, bioresorbable dan bioaktif.11
Tingkat kelarutan TCP lebih tinggi dibanding HA dapat digambarkan bahwa HA < β-TCP < α-TCP.4 Oleh karena itu, keramik kalsium fosfat merupakan pilihan yang baik untuk rekonstruksi bedah, ortopedi, kedokteran gigi, dan pembedahan kraniofasial, tulang belakang, dan bedah saraf. Sifat kelarutan BCP tergantung pada rasio β-TCP/HA. Semakin tinggi nilai rasio dan porositasnya maka semakin mudah larut material tersebut.11 BCP dapat terbentuk dari HA yang dipanaskan (sintering) pada 1200°C selama 6 jam. Persamaan reaksi pembentukan TCP adalah sebagai berikut:
Ca10(PO4)6(OH)2→ 3β-Ca3(PO4)2+ CaO + H2O(1)
[image:36.595.316.508.279.419.2]Kumar et al.12 berhasil mensintesis BCP dari proses sintering. Butiran BCP disintesis dari senyawa kalsium hidroksida dan diammonium hydrogen ortho phosphate (DAP) dengan menggunakan microwave. Jumlah reaktan yang digunakan untuk reaksi dihitung berdasarkan perbandingan molar Ca/P sebesar 1,58. Larutan hasil reaksi tersebut kemudian dikeringkan pada suhu 900°C dalam microwave selama 20 menit. Gambar 1 memperlihatkan hasil pola XRD BCP berdasarkan penelitian Kumar et al.12
Gambar 1 Pola Difraksi XRD BCP pada suhu
sintering 900oC.
2.2 Amorphous Calcium Phosphate
(ACP)
Senyawa kalsium fosfat hasil presipitasi dapat berada dalam fase kristalin maupun fase amorf. Fase kristal stabil senyawa kalsium fosfat dikenal sebagai hydroxyapatite (Ca10(PO4)6(OH)2). Fase amorf kalsium fosfat disebut amorphous calcium phosphate (ACP) yang dapat terbentuk pada awal presipitasi. Penggunaan ACP pada email dapat membentuk kristal hydroxyapatite. Mineral yang digunakan ini tentu saja harus tahan terhadap larutan tubuh, tidak mudah terdegradasi, memiliki kekuatan mekanik yang tinggi dan tidak toksik.13
3
untuk memulihkan 71% dari kerusakan gigi akibat kehilangan mineral. Pada pH rendah, ACP dapat menjadi rusak dan tingkat pelepasan Ca-2 dan PO
4 supersaturating ion. Selain itu, ACP bersifat tidak stabil dan dalam lingkungan air ACP bertransformasi menjadi HA. Kondisi tersebut kondusif untuk remineralisasi gigi.14
Komposisi ACP tidak hanya terdiri atas ion kalsium dan fosfat terdapat ion-ion lain dalam senyawa ACP. Sebagai contoh ion karbonat (CO32-) dengan konsentrasi tinggi ternyata sebagai penghambat proses transformasi dengan menggantikan posisi ion hidroksil dan ion fosfat sehingga membentuk kristal apatit karbonat tipe A dan tipe B, sehingga dapat menghambat proses transformasi dari kalsium fosfat amorf menjadi hydroxyapatite.14
2.3 Fibroblas
Fibroblas adalah sel predominal pulpa yang dapat berasal dari sel mesenkimal pulpa yang tidak berkembang. Fibroblas berbentuk stelat, dengan nuklei ovoid dan prosesus sitoplasmik. Bila bertambah tua menjadi lebih bulat, dengan nuklei bulat dan prosesus sitoplasmik pendek. Perubahan bentuk disebabkan oleh pengurangan aktivitas sel karena bertambah tua.15
Fungsi fibroblas adalah sebagai pembuatan substansi dasar dan serabut kolagen, yang merupakan matriks pulpa. Fibroblas juga berperan dalam degradasi kolagen, deposisi jaringan yang mengapur, membentuk dentine, dan dapat berkembang untuk menggantikan odontoblas yang mati karena memiliki kemampuan untuk memperbaiki dentin. Fibroblas dapat dijumpai pada daerah yang kaya sel pulpa terutama pada daerah coronal.15
Sel-sel fibroblas dermis memainkan peran penting dalam memperbaharui sistem dan untuk mempertahapnkan integritas kulit.16 Sel fibroblas yang akan digunakan dalam pengujian in vitro ini adalah sel fibroblas dermal normal pada manusia (Gambar 2). Para peneliti
[image:37.595.336.491.166.284.2]mengatakan bahwa meningkatnya jumlah fibroblas akan dapat membantu merevitalisasi pulpa gigi dan mengurangi kemungkinan jaringan pulpa gigi tersebut untuk dibuang.17
Gambar 2 Sel NHDF mikroskopik.18
2.4 In Vitro BCP
Pengujian biocompatibilities secara in vitro dilakukan dengan mendeteksi kerusakan dan kematian sel yang disebut sitotoksitas.19 Uji toksisitas salah satunya dilakukan dengan metodeMTT assay. Uji MTT assay merupakan metode kolorimetrik, dimana larutan pereaksi
[3-(4,5-dimetillthiazol-2-yl)-2,5-difeniltetrazolium bromide] ini yang disebut larutan MTT merupakan garam tetrazolium yang dapat dipecah menjadi kristal formazan oleh sistem suksinat tetrazolium reduktase yang terdapat dalam jalur respirasi sel pada mitokondria yang aktif pada sel yang masih hidup. Kristal formazan ini memberi warna ungu yang dapat dibaca absorbansinya dengan menggunakan mikroplatereader.20
Riberio et al.21 Pada ter