ISOLASI DAN IDENTIFIKASI SAPOGENIN DARI TERIPANG Actinopyga sp.
SKRIPSI
OLEH:
RADOTI MERLIN SAGALA 060824029
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
ISOLASI DAN IDENTIFIKASI SAPOGENIN DARI TERIPANG Actinopyga sp.
SKRIPSI
Diajukan Untuk Melengkapi Salah Satu Syarat Untuk Mencapai Gelar Sarjana Farmasi
Pada Fakultas Farmasi Universitas Sumatera Utara
OLEH:
RADOTI MERLIN SAGALA 060824029
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
Pengesahan Skripsi
Judul:
ISOLASI DAN IDENTIFIKASI SAPOGENIN DARI TERIPANG
Actinopyga sp.
Oleh:
RADOTI MERLIN SAGALA NIM : 060824029
Dipertahankan di Hadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal: Desember 2008
Pembimbing I, Panitia Penguji,
KATA PENGANTAR
Puji dan syukur penulis ucapkan kepada Bapa Maha Kuasa atas kasih setia dan kemurahanNya yang telah memberikan pengetahuan, kekuatan, dan kebijaksanaan dalam penyelesaian skripsi ini untuk memenuhi syarat guna mencapai gelar sarjana Farmasi pada Fakultas Farmasi Universitas Sumatera Utara Medan.
Penulis juga mengucapkan banyak terima kasih kepada orang tua tercinta Ayahanda W. Sagala dan Ibunda H. br. Sinaga, atas kasih sayang dan doa yang selalu mengiringi yang tidak terbalas dengan apapun juga.
Penulis menyadari bahwa skrpsi ini tidak akan terwujud tanpa adanya bantuan dari berbagai pihak, untuk itu penulis menyampaikan rasa terima kasih yang tulus kepada :
1. Ibu Dra. Aswita Hafni Lubis, M.Si, Apt., sebagai pembimbing I yang telah banyak memberikan waktunya untuk membimbing dengan penuh kesabaran, tulus dan ikhlas selama penelitian dan penulisan skripsi ini. 2. Ibu Dra. Suwarti Aris, M.Si, Apt., sebagai pembimbing II yang telah
banyak memberikan waktunya untuk membimbing dengan penuh kesabaran, tulus dan ikhlas selama penelitian dan penulisan skripsi ini. 3. Bapak Prof. Dr .rer.nat. Effendi De Lux Putra SU, Apt., sebagai dosen
wali yang telah membimbing penulis selama masa pendidikan.
Awaluddin Saragih M.Si, Apt., sebagai tim penguji yang sangat banyak memberikan masukan dan saran atas skripsi ini.
5. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas Farmasi yang telah memberikan bantuan dan fasilitas selama masa pendidikan.
6. Bapak Kepala Laboratorium Farmakognosi Fakultas Farmasi Drs. Panal Sitorus, M.Si, Apt yang juga banyak membimbing saya.
7. Teman-teman senasib seperjuangan Dani, Een, Ratih, Faisal, , dan teman-teman stambuk 2003 lainnya serta semua pihak terkait yang tidak dapat penulis sebutkan satu persatu yang telah memberi motivasi dan bantuan langsung maupun tidak langsung kepada penulis selama penelitian hingga selesainya penulisan skrpsi ini.
Medan, Desember 2008 Penulis,
ABSTRAK
Telah dilakukan isolasi dan identifikasi senyawa sapogenin dari teripang Actinopyga sp. Hasil uji pendahuluan terhadap senyawa kimia menunjukkan adanya senyawa saponin dan steroid/triterpenoid.
ABSTRACT
Phytochemical screening, isolation and identification of sapogenin compounds of the sea cucumber of Actinopyga Sp, have been carried out by ultraviolet, infrared spectrofotometri, and mass spectra. Phytochemical screening has done to the presence of saponin and triterpene/steroid.
DAFTAR ISI
Halaman
JUDUL………... ... i
HALAMAN PENGESAHAN……… ... iii
KATA PENGANTAR ... iv
ABSTRAK………. ... vi
ABSTRACT……… ... vii
DAFTAR ISI……….. ... viii
DAFTAL TABEL……….. ... x
DAFTAR GAMBAR………... ... xi
DAFTAR LAMPIRAN……….. ... xii
BAB I. PENDAHULUAN……….. ... 1
1.1Latar Belakang………... ... 1
1.2Perumusan Masalah……… ... 3
1.3Hipotesis……….. ... 3
1.4Tujuan Penelitian ………. ... 3
BAB II. TINJAUAN PUSTAKA... ... .. 4
2.1 Uraian Hewan... 4
2.2 Habitat dan Penyebaran... . 4
2.3 Sistematika... ... .. 6
2.4 Morfologi... ... 7
2.5 Uraian Kimia... ... 8
2.6Triterpen/steroid... 9
2.8 Ekstraksi... ... 13
2.9 Kromatografi ... ... 14
2.10 Kromatografi lapis tipis... ..15
BAB III. METODOLOGI……… . ……16
2.1 Bahan-bahan……… .. ….16
2.2 Alat-alat……… . ….16
2.3 Pengumpulan dan pengolahan sampel……… ... 16
2.3.1 Pengumpulan sampel ... 16
2.3.2 pengolahan sampel ... 16
2.4 Pemeriksaan karakteristik ... …...16
2.4.1 pemeriksaan mkroskopik ... 16
2.4.2 penetapan kadar air ... 16
2.5 Pembuatan larutan pereaksi ... 16
2.6 Pemeriksaan senyawa saponin 2.6.1 Uji busa ... ………..19
2.6.2 Uji hemolisis darah ... ……….19
2.7 Pemeriksaan senyawa steroid/triterpenoid ... ...20
2.8 Pembuatan ekstrak .... ………21
2.9 Isolasi senyawa sapogenin dari ekstrak etanol... 21
2.10 Analisis ekstrak kloroform dengan cara KLT………23
2.11 Pemisahan senyawa sapogenin teripang dengan KLT Preparatif ... 23
2.12Uji kemurnian senyawa hasil isolasi dengan KLT ... 23
2.13Uji kemurnian senyawa hasil isolasi dengan KLT dua arah ... 23
2.14.1 identifikasi isolat dengan spektrofotometri UV ... 23
2.14.2 identifikasi isolat dengan spektrofotometri inframerah ... 23
2.14.3 identifikasi isolat dengan spektrometri massa... 23
BAB IV. HASIL DAN PEMBAHASAN ... ……….25
BAB V. KESIMPULAN DAN SARAN ... ………30
4.1 Kesimpulan ... ………30
4.2 Saran ... ……….30
DAFTAR PUSTAKA ... ………..31
DAFTAR GAMBAR
Gambar Halaman
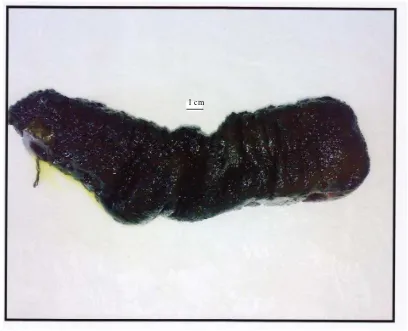
1. Hewan teripang segar... ...21
2. Simplisia teripag...22
3. Bagan ekstraksi simplisia...23
4. Kromatogram hasil KLT ekstrak etanol...24
5. Kromatogram hasil KLT ekstrak kloroform dengan fase gerak n-hexan-etilasetat...24
6. Kromatogram hasil KLT ekstrak kloroform dengan fase gerak kloroform-toluen...25
7. Kromtogram ekstrak kloroform secara KLT Preparatif...26
8. Kromatogram hasil KLT isolat 1...27
9. Kromatogram hasil KLT dua arah...28
10.Spektrum ultraviolet...29
11.Spektrum inframerah...30
DAFTAR LAMPIRAN
lampiran Halaman
1. hasil identifikasi hewan laut teripang ... ...33
2. gambar hewan teripag segar ... . 48
3. gambar simplisia teripang ... 44
4. bagan ekstraksi simplisia... 44
5. gambar kromatogram hasil KLT ekstrak etanol... 34
6. gambar kromatogram hasil KLT ekstrak kloroform dengan fase gerak n-hexan-etil asetat ... 44
7. Kromatogram hasil KLT ekstrak kloroform dengan fase gerak kloroform-toluen ... 33
8. Kromtogram ekstrak kloroform secara KLT Preparatif...55
9. Kromatogram hasil KLT isolat 1...55
10.Kromatogram hasil KLT dua arah...28
11.Spektrum ultraviolet...29
12.Spektrum inframerah...30
ABSTRAK
Telah dilakukan isolasi dan identifikasi senyawa sapogenin dari teripang Actinopyga sp. Hasil uji pendahuluan terhadap senyawa kimia menunjukkan adanya senyawa saponin dan steroid/triterpenoid.
ABSTRACT
Phytochemical screening, isolation and identification of sapogenin compounds of the sea cucumber of Actinopyga Sp, have been carried out by ultraviolet, infrared spectrofotometri, and mass spectra. Phytochemical screening has done to the presence of saponin and triterpene/steroid.
BAB I PENDAHULUAN
1.1Latar Belakang
Sejak jaman dahulu, teripang atau nama lainnya gamat/sea cucumber dikenal berkhasiat obat. Teripang mampu menyembuhkan berbagai penyakit . kemampunanya dalam regenerasi sel jadi alasan utama teripang dipakai menyembuhkan penyakit . selain mampu meregenerasi sel, teripang kaya akan nutrisi, senyawa aktif terbanyak berupa antioksidan yang baik untuk perbaikan sel tubuh manusia. teripang digunakan sebagai obat luka ringan, teripang mempercepat penyembuhan luka dalam setelah persalinan normal dan caesar/pembedahan, sakit sendi, paru-paru, hipertensi, kencing manis, dan sebagai sumber protein. khasiat teripang juga didukung kandungan EPA (eikosa pentaenoic acid) dan DHA (dokosa hexaenoic acid), keduanya termasuk asam lemak omega 3. faedahnya dapat menghabat proses penuaan, menurunkan kolesterol jahat LDL (low density lipid) dan VLDL (very low density lipid) dalam tubuh sehingga mengurangi resiko penyakit jantung. (Anonim, 2007)
indonesia merupakan penghasil teripang terbesar didunia, sayangnya tidak ada yang mengolahnya, hampir semua diekspor, teripang dekspor dalam beberapa bentuk produk, diantaranya produk setengah jadi yaitu teripang kering, usus asin, gonad kering, otot kering, teripang kaleng, kerupuk teripang, serta beragam produk lainnya. pasaran utama dari teripang tersebut diantaranya beberapa negara Eropa, Jepang, Malaysia, Amerika.
Teripang mempunyai niai ekonomis penting karena kandungan atau kadar nutrisinya yang tinggi. dari hasil penelitian, kandungan nutrisi teripang dalam kondisi kering terdiri dari protein sebanyak 82%, lemak 1,7%, kadar air 8,9%, kadar abu 8,6%, da karbohidrat 4,8%. (
saponin merupakan komponen toksik dari filum Echinodermata. diantara fium Echinodermata yang dibagi dalam 5 kelas, diantaranya Crinoidea (sea lilies), Asteroidea (bintang laut), Ophiuroidea (brittle star), Echinoidea (sea urchin), Holothuroidea (sea cucumber), hanya bintang laut, timun laut dan sejenisnya yang mengandung saponin. (Yashimoto, )
saponin, senyawa komplek dari gula dengan steroida/triterpenoida, terdistribusi luas pada tanaman tetapi jarang terdapat pada hewan, saponin dapat menghambat pertumbuhan kanker kolon dan membantu kadar kolesterol menjadi normal.
1.2 Perumusan Masalah
a. Apakah teripang Actinopyga sp mengandung senyawa sapogenin?
b. Bagaimana cara mengisolasi dan mengidentifikasi senyawa sapogenin dari teripang Actinopyga sp?
1.3 Hipotesis
a. Teripang Actinopyga sp. mengandung senyawa sapogenin
b. Senyawa sapogenin dalam teripang Actinopyga sp. dapat diisolasi dengan cara KLT dan diidentifikasi isolatnya dengan spektrofotometri UV, IR dan MS.
1.4 Tujuan Penelitian
a. Untuk mengetahui seyawa sapogenin yang terdapat dalam teripang Actinopyga sp.
BAB II
TINJAUAN PUSTAKA 2.1. Uraian Hewan
Teripang merupakan hewan berkulit duri (Echinodermata). Namun tidak semua teripang mempunyai duri pada kulitnya. Ada beberapa jenis teripang yang tidak berduri. Tubuh teripang lunak, berdaging dan berbentuk silindris memanjang seperti buah ketimun. Oleh karena itu hewan ini disebut ketimun laut. Gerakan teripang sangat lamban sehingga hampir seluruh hidupanya berada didasar laut. Warna tubuh teripang bermacam-macam, mulai dari hitam, abu-abu, kecoklat-coklatan, kemerah-merahan, kekuning-kuningan, sampai putih.
Ukuran tubuh tiap jenis teripang berbeda-beda. Teripang termasuk jenis hewan dioecious yang berarti hewan berkelamin jantan terpisah dengan hewan berkelamin betina.(Martoyo, 2006)
2.1.1. Habitat dan Penyebaran
2.1.2. Sistematika
Filum : Echinodermata Sub-filum : Echinozoa Kelas : Holothuroidea Sub-kelas : Aspidochirotaceae Ordo : Aspidochirotda Famili : Holothuridae Genus : Actinopyga 2.1.3. Morfologi
Badan teripang hitam berbentuk bulat panjang dan akan segera mengkerut bila diangkat dari permukaan air. Di seluruh permukaan badan teripang hitam terdapat bintil-bintil halus. Teripang hitam mudah dikenali karena warnanya indah. Bagian punggungnya berwarna hitam keungu-unguan atau kebiru-biruan. Sementara bagian perut, sisi sekitar mulut, dan duburnya kemerah-merahan. Teripang hitam hidup di daerah perairan berkarang atau berpasir yang ditumbuhi ilalang (sea grass) (Martoyo, 2006).
2.1.4. Reproduksi
Perkawinan teripang biasanya berlangsung secara eksternal atau diluar tubuh. Sel telur dan sperma masing-masing dihasilkan oleh individu betina dan jantan dengan cara disemprotkan. Setelah itu larva hidup didasar perairan sampai menjadi juvenil (teripang muda) (Martoyo, 2006)
2.2. Uraian Kimia
serta dapat dideteksi berdasarkan kemampuannya membentuk busa dan menghemolisa sel darah merah. Pola glikosida saponin kadang-kadang rumit, banyak saponin yang mempunyai satuan gula sampai lima dan komponen yang umum adalah asam glukoronat. (Harborne, 1996)
Senyawa saponin dapat pula diidentifikasi dari warna yang dihasilkannya dengan pereaksi Liebermann-Burchard. Warna biru hijau menunjukkan saponin steroid, warna merah, merah muda, atau ungu menunjukkan saponin triterpenoida (Fransworth, 1966)
2.2.1 Triterpenoid/Steroid Triterpenoid
Triterpenoid adalah senyawa yang kerangka karbonnya berasal dari enam satuan isopren dan secara biosintesis diturunkan dari hidrokarbon C30 asiklik yaitu skualen yang merupakan senyawa yang tidak berwarna, berbentuk kristal, biasanya bertitik leleh tinggi dan optis aktif (Harborne, 1987).
Pada tumbuhan, senyawa terpenoida terdapat bebas, tidak terikat dengan senyawa lain tetapi banyak juga yang terdapat sebagai glikosida atau ester (Harborne, 1987;Robinson, 1995).
Triterpenoid merupakan komponen aktif dalam tumbuhan yang digunakan untuk beberapa penyakit seperti diabetes, gangguan kulit, antibakteri dan antivirus (Robinson, 1995).
CH3
CH2 C CH CH2
Steroida
Steroida adalah senyawa triterpenoida yang kerangka dasarnya sistem cincin siklopentana perhidrofenantren.Senyawa ini tersebar luas dialam dan mempunyai fungsi biologis yang sangat penting, misalnya kontrasepsi, insektisida, analgesik dan antiinflamasi (Brunetton, 1995; Harborne, 1987).
Inti steroida dasar sama dengan inti lanosterol dan triterpenoida tetrasiklik lain, tetapi hanya pada 2 gugus metil yang terikat pada sistem cincin pada posisi 10 dan 13 (Robinson, 1995).
Sistem Penomoran Senyawa Steroida
2.2.2 Saponin
Saponin merupakan suatu glikosida yang aglikonnya berupa sapogenin.Sapogenin dapat diperoleh dengan hidrolisis dalam suasana asam atu hidrolisis memakai enzim.Berdasarkan sturktur kimianya, sapogenin dibedakan menjadi sapogenin steroida dan sapogenin triterpenoida (Farnsworth, 1966).
Sapogenin steroida ditemukan dalam tumbuhan monokotil atau dikotil.Sapogenin triterpenoida jarang terdapat dalam tumbuhan monokotil, tetapi banyak terkandung pada suku dikotil(Gunawan, 2004).
2.3. Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut tertentu (Depkes, 2000)
Proses ekstraksi akan menghasilkan ekstrak, merupakan sediaan kental yang diperoleh dengan mengekstraksi senyawa aktif dari simplisia menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Depkes, 2000)
Beberapa metode ekstraksi dengan menggunakan pelarut yaitu (Depkes, 2000):
A. Cara Dingin 1. Maserasi
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna (exhaustive extraction) yang umumnya dilakukan pada temperatur ruangan. Proses terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/ penampungan ekstrak), terus-menerus sampai diperoleh ekstrak (perkolat) yang jumlahnya 1-5 kali bahan.
B. Cara Panas 1. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses eksatraksi sempurna.
2. Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
3. Digesti
Digesti adalah maserasi kinetik (dengan pengadukan kontinu) pada temperatur yang lebih tinggi dari temperatur ruangan (kamar), yaitu secara umum dilakukan pada temperatur 40-50°C.
4. Infus
5. Dekok
Dekok adalah infus pada waktu yang lebih lama (≥30°C) dan temperatur sampai titik didih air. (Depkes, 2000)
2.4. Kromatografi
Kromatografi didefenisikan sebagai pemisahan campuran dua atau lebih senyawa yang berbeda dengan distribusi antara dua fase, yaitu fase diam dan fase gerak (Pavia,et al, 1988). Fase gerak dapat berupa zat cair atau gas dan ada 4 macam sistem kromatografi (Sastrohamidjojo, 1991), yaitu:
1. Fase garak zat cair-fase diam padat (kromatografi serapan) - Kromatografi Lapis Tipis
2. Fase gerak gas-fase diam padat - Kromatografi gas padat
3. Fase cair-fase diam cair (kromatografi partisi) - Kromatografi Kertas
4. Fase gerak gas-fase diam cair - Kromatografi gas cair
2.4.1. Kromatografi Lapis Tipis
Kromatografi Lapis Tipis adalah pemisahan memakai fase gerak cair yang bergerak karena gaya kapiler melalui fase diam padat yang disaputkan pada permukaan penyangga datar dengan ketebalan seragam. (Gritter, 1991)
a. tipe penjerap dan metode pengaktivan; jika tidak dinyatakan lain, dipanaskan pada suhu 110 ºC selama 30 menit
b. metode persiapan dan konsentrasi dari sampel dan petunjuk pelarut c. volume larutan ditempatkan diatas plat
d. fase gerak, temperatur dan waktu pengembwngan; jarak dari perpindahan fase gerak.
e. Metode pengeringan dan temperatur yang digunakan dan cara mendeteksi (WHO Geneva, 1979)
Kromatografi lapis tipis merupakan kromatografi serapan dimana fase diam berupa zat padat yang disebut adsorbent (penyerap) berupa lapisan tipis dan fase gerak berupa zat cair yang disebut larutan pengembang. KLT dapat dipakai untuk dua tujuan, yaitu (Gritter,1991):
1) sebagai metode untuk mendapatkan hasil kualitatif, kuantitatif dan preparatif.
2) Dipakai untuk mengetahui sistem pelarut yang akan dipakai dalam kromatografi kolom.
Fase diam (penyerap) dapat dibagi dua, jenis polar dan non polar. Penyerap polar meliputi berbagai oksida organik seperti silika, alumina, magnesia, magnesia silikat. Penyerap non polar yang biasa digunakan adalah arang. Fasa cocok (fasa gerak), pemisahan terjadi selama pengembangan. Selanjutnya senyawayang tidak berwarna harus ditempatkan/ dideteksi (Gritter, 1991)
memuaskan dan salah satu alasan untuk menaikkan hasil pemisahan adalah menggunakan penyerap yang butirannya halus. Beberapa contoh penyerap yang biasa digunakan untuk pemisahan dalam KLT adalah silika gel, alumina, selulosa, dan pati (Sastrohamidjo, 1990).
Pada umumnya dipakai larutan 0,1-1 %. Pelarut yang terbaik untuk melarutkan campuran adalah pelarut yang bertitik didih antara 50-100°C karena pelarut yang demikian mudah menguap dari lapisan (Gritter, 1991).
Dalam mengidentifikasi noda-noda dalam kromatografi digunakan harga Rf yang didefenisikan sebagai berikut (Sastrohamidjojo,1990):
Rf = jarak yang ditempuh oleh senyawa dari titik penotolan Jarak yang ditempuh oleh pelarut dari titik penotolan Faktor-faktor yang dapat mempengaruhi harga Rf (Sastrohamidjojo, 1990):
1. Struktur kimia 2. sifat dari penyerap
3. tebal dan kerataan dari lapisan penyerap 4. pelarut dan derajat kemurniannya 5. derajat kejenuhan bejana pengembang 6. teknik percobaan
7. jumlah cuplikan yang digunakan 8. suhu
9. kesetimbangan
2.5. Spektrofotometri Ultraviolet (UV)
biasanya digunakan lampu hidrogen. Panjang gelombang dari sumber cahaya akan dibagi oleh pemisah panjang gelombang seperti prisma atau monokromator. Ketika suatu atom atau molekul menyerap cahaya maka energi tersebut akan menyebabkan elektron terluarnya tereksitasi ketingkat energi yang lebih tinggi (Dachriyanus, 2004).
Spektrofotometri ultraviolet merupakan sautu metode analisis berdasarkan atas pengukuran serapan suatu larutan yang dilalui radiasi monokromatis ultraviolet. Apabila suatu molekul menyerap menyerap radiasi ultraviolet, didalam molekul tersebut terjadi perpindahan tingkat energi elektron-elektron ikatan diorbital molekul paling luar, dari tingkat energi paling rendah ketingkat energi ysng lebih tinggi.
Panjang gelombang cahaya ultraviolet tergantung pada mudahnya promosi elektron akan menyerap radiasi ultraviolet pada panjang gelombang yang lebih pendek. Molekul yang memerlukan energi lebih sedikit akan menyerap pada panjang gelombang yang lebih panjang (Fessenden dan Fessenden, 1995)
2.6. Spektrofotometri Inframerah
Sinar inframerah bila dilewatkan melalui cuplikan senyawa organik maka sejumlah frekwensi akan diserap sedangkan frekwensi yang lain diteruskan tanpa diserap. Daerah inframerah terletak antara spektrum elektromagnetik cahaya tampak dan spectrum radio, yakni antara 4000-400cmˉ¹.(Noerdin,
1985;Sastrohamidjojo, 1985).
untuk menentukan struktur senyawa yang belim diketahui yaitu dengan cara membandingkannya terhadap senyawa yang sudah diketahui. Sangat jarang dua senyawa organik memiliki spektrum inframerah yang identik baik dalam posisi maupun intensitas puncak-puncaknya(Wingrove and Caret, 1981).
Cara menganalisis spektrum inframerah dari senyawa yang tidak diketahui adalah pertama harus ditentukan ada atau tidaknya beberapa gugus fungsional utama, seperti C-O, O-H, N-H, C-O, C=C, C≡C, C=N, C≡N, dan NO2. Langkah-langkah umum untuk memeriksa gugus yang penting pada spektrum inframerah (Pavia, et al.1988) adalah:
1. apakah terdapat gugus karbonil?
Gugus C=O memberikan puncak pada daerah 1820-1660 cm-1. puncak ini biasanya merupakan yang terkuat dengan lebar medium pada spektrum. 2. jika gugus C=O ada, periksalah gugus berikut. Jika C=O tidak ada,
langsung kenomor 3.
Asam : apakah ada gugus O-H?
Serapan melebar didaerah 3300-2500 cm-1. (biasanya tumpang tindih dengan C-H)
Amida : apakah ada N-H
Serapan medium didekat 3500 cm -1, kadang-kadang dengan puncak rangkap.
Ester : apakah ada C-O?
Serapan dengan intensitas medium didaerah 1300-1000c-1. Anhidrida : mempunyai dua serapan C=O didaerah 1810 dan 1760
Aldehid : apakah ada C-H aldehid?
Dua serapan lemah didekat 2850-2750 cm-1 yaitu disebelah kanan serapan C-H.
Keton : jika kelima kemungkinan diatas tidak ada. 3. Jika gugus C-O tidak ada
Alkohol/fenol : periksalah gugus O-H, merupakan serapan melebar didaerah 3600-3300cm-1 yang diperkuat adanya serapan C-O didaerah 1300-1000cm-1.
Amina : periksalah gugus N-H, yaitu serapan medium didaerah 3500cm-1.
Eter : periksalah gugus C-O (dan tidak adanya O-H), yaitu serapan medium didaerah 1300-1000cm-1.
4. Ikatan rangkap dua atau cincin aromatik
- C=C mempunyai serapan lemah didaerah1650cm-1.
- Serapan medium sampai kuat pada daerah 1650-1450cm-1 sering menunjukkan adanya cincin aromatik.
- Buktikan kemungkinan diatas dengan memperhatikan serapan pada daerah C-H aromatik disebelah kiri 3000 cm-1, sedangkan C-H alifatis terjadi disebelah kanan daerah tersebut.
5. Ikatan rangkap tiga
- C≡N mempunyai serapan medium dan tajam didaerah 2250 cm-1. - C≡C mempunyai serapan lemah tapi tajam didaerah 2150 cm-1.
6. Gugus nitro
Dua serapan kuat didaerah 1600-1500 cm-1 dan 1390-1300cm-1 7. Hidrokarbon
- apabila keenam kemungkinan diatas tidak ada. - Serapan utama didaerah CH dekat 3000cm-1.
- Spektrum sangat sederhana, hanya terdapat serapan lain didaerah 1450-1375cm-1.
2.7. Spektrometri Massa
Spektrometri massa adalah suatu teknik analisis berdasarkan pemisahanberkas ion-ion yang sesuai dengan perbandingan massa dengan muatan pengukuran intensitas dari berkas ion-ion tersebut.
Pada spektrometri massa, molekul-molekul organik ditembak dengan berkas-berkas elektron dan diubah menjadi ion-ion yang bermuatan positif bertenaga tinggi yang dapat dipecah menjadi ion-ion yang lebih kecil. Lepasnya elektron dari molekul menghasilkan radikal kation, dan proses ini dapat dinyatakan sebagai M→M+ . Ion molekul M+ biasanya terurai menjadi sepasang pecahan / fragmen, yang dapat berupa radikal dan ion, atau molekul yang lebih kecil dan radikal kation (Sastrohamidjojo, 1985).
(tertinggi)pada spektrum, disebut puncak dasar (base peak), dinyatakan dengan nilai 100% dan kekuatan puncak lain, termasuk puncak ion molekulnya dinyatakan sebagai persentase puncak dasar tersebut (Silverstein, 1986; Willard et
al, 1981).
BAB III
HASIL DAN PEMBAHASAN
Hasil identifikasi yang telah dilakukan oleh pusat penelitian Oseanopgrafi LIPI Jakarta adalah termasuk hewan teripang filum Echinodermata, kelas Holothuroidea, jenis Actinopyga.
Hasil makroskopik teripang, yaitu berukuran panjang 37,5 cm, lebar 8 cm, dengan berat 100 g, berwarna hitam, dan berbau spesifik. Hasil penetapan kadar air terhadap simplisia hewan adalah 8%
Ekstraksi teripang dilakukan dengan cara maserasi menggunakan pelarut etanol 96% dimana semua senyawa yang terdapat dalam teripang tersari secara sempurna. Ekstrak etanol setelah dipekatkan diperoleh sebanyak 6 g yang berasal dari 700 g serbuk simplisia.
Analisis KLT dari ekstrak etanol digunakan fase diam silika gel GF254, fase gerak n-hexan-etil asetat dengan berbagai perbandingan, sebagai penampak bercak adalah Liebermann-Burchard. Diperoleh 1 bercak senyawa saponin setelah disemprot dengan penampak bercak Liebermann-Burchard. Pemutusan ikatan glikosida dilakukan dengan cara Refluks diatas waterbath dengan penambahan HCl 2N, hasil Refluks kemudian diuapkan dan sisanya dipartisi dengan CHCl3, dan diperoleh ekstrak kloroform yang kemudian diuapkan dan diperoleh ekstrak kental kloroform.
yang paling baik adalah kloroform-toluen (80:20) diperoleh 2 bercak senyawa sapogenin setelah disemprot dengan penampak bercak Liebermann-Burchard dengan harga Rf berturut-turut 0,52 (ungu), 0,89 (merah coklat). Adapun pengembang yang dipakai untuk KLT preparatife adalah Kloroform-toluen, karena pemisahan yang terjadi lebih baik dibandingkan dengan n-hexan-etil asetat dimana, pada pengambang n-hexan-etil asetat diperoleh noda yang berdekatan dan
tidak seluruhnya naik melainkan masih ada tertinggal pada titik penotolan. Isolasi senyawa sapogenin yang dilakukan terhadap ekstrak kloroform
secara kromatografi lapis tipis preparatif diperoleh 2 isolat, isolat yang diperoleh kemudian diidentifikasi dengan spektrofotometri ultraviolet, spektrofotometri inframerah dan spektrometri massa, dimana isolat yang diambil untuk diidentifikasi adalah isolat I.
Hasil spektrofotometri ultraviolet dari isolat memberikan panjang gelombang maksimum (λ) 229nm. Hasil spektrofotometri Inframerah menunjukkan adanya ikatan O-H yang ditunjukkan oleh dua puncak berdekatan pada bilangan gelombang 3448,72 adanya C-H alifatis yang ditunjukkan gugus metilen (CH2) 2924,09 dan 2854,65 ini diperkuat oleh puncak pada bilangan gelombang 1373,32 menunjukkan adanya gugus metil (CH3), sedangkan hasil spektrometri massa dengan SI 88 maka diduga senyawa tersebut adalah cholestan-3-ol (C27H48O). Spektrum massa tersebut memberikan puncak-puncak sebagai berikut:
1. m/z 388 (M+) merupakan puncak ion molekul yang berarti sama dengan berat molekul senyawa.
3. m/z 355 (M+- 18) adalah akibat terlepasnya gugus H2O.
4. m/z 215 (M+- 140) menunjukkan adanya pemecahan fragmentasi pada cincin C.
BAB IV
KESIMPULAN DAN SARAN 4.1. Kesimpulan
Hasil identifikasi oleh Pusat Penelitian Oseanografi LIPI adalah termasuk hewan teripang filum Echinodermata, kelas Holothuroidea, jenis Actinopyga.
Hasil pemeriksaan identifikasi senyawa bioaktif terhadap serbuk simplisia teripang menunjukkan adanya golongan senyawa saponin.
Sapogenin dalam teripang dapat diisolasi dengan cara KLT menggunakan fase diam plat pra lapis GF 254 dan fasee gerak kloroform-toluen (80:20).
Hasil isolasi ekstrak kental kloroform secara Kromatografi Lapis Tipis (KLT) preparatif terhadap teripang diperoleh 2 isolat senyawa sapogenin dengan harga Rf 0,52 dan 0,86.
Hasil analisis isolat secara spektrofotometri ultraviolet memberikan absorbansi maksimum pada panjang gelombang (λ)229 nm, Hasil
spektrofotometri Inframerah menunjukkan adanya ikatan O-H yang ditunjukkan oleh dua puncak berdekatan pada bilangan gelombang 3448,72 adanya C-H alifatis yang ditunjukkan gugus metilen (CH2) 2924,09 dan 2854,65 ini diperkuat oleh puncak pada bilangan gelombang 1373,32 menunjukkan adanya gugus metil (CH3), sedangkan hasil spektrometri massa dengan SI 88 maka diduga senyawa tersebut adalah cholestan-3-ol (C27H48O).
4.2. Saran
DAFTAR PUSTAKA
Dachriyanus. (2004). Analisis struktur senyawa Organik secara Spektroskopi. Padang : Universitas andalas press. Hal. 1-6.
Depkes. (1979). Farmakope indonesia. Edisi III Jakarta: Kesehatan RI. Hal 8-13,21
Ditjen POM. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Hal 1, 10-11
Fransworth, N.R. (1966). Biological and Phytochemical Screening Of Plants. Journal Of Pharmaceutical Sciences. Volume 55. no 3. Chicago: Reheis Chemical Company. P.
Fessenden, R.J., dan Fessenden, J.S. (1995). Kimia Organik. Terjemahan: Padmawinata, K.Jilid 2. edisi III. Jakarta: Penerbit Erlangga. Hal 436-456 Gritter, R.J., Bobitt, J.M, dan Schwarting. A.E. (1991). Pengantar Kromatografi.
Terjemahan Padmawinata, K. Edisi II. Bandung : Penerbit ITB. Hal107-146.
Harborne, J.B.(1987). Metode Fitokimia, penuntun cara moderen menganalisa tumbuhan. Penerjemah : K. padmawinata,. Edisi II. Bandung: ITB.Hal 6-8. Hostettmann, K., Hostettmann, M., Marston, A., (1995). Cara Kromatografi
Preparatif: Penggunaan Pada Isolasi Senyawa Alam. Terjemahan Padmawinata, K. Bandung: Penerbit ITB. Hal .9-11
Pavia, D.L., Lampman, G.M., and Kriz, G.S. (1988). Introduction to Organic Laboratory Techniques. Third edition. USA: Saunders Collage Publishing. P:597, 607, 700-712.
Sastrohamidjojo, H. (1996). Sintesis Bahan Alam. Yogyakarta : Gadjah Mada University Press. Hal …
Silverstein, R. M, Bessler, G. C, dan Morrill, T. C. (1986). Penyidikan Spektrometrik Senyawa Organik. Alih bahasa Hartono, dkk. Jakarta : Erlangga. Hal. 305-308
Stahl, E. (1985). Analisis Obat Secara Kromatografi dan Mikroskopi. Terjemahan :Padmawinata, K dan SudiroI. Bandung : Penerbit ITB. Hal. 3-13.
Yashimoto,Yashiro(2000).Marine Toxins and Other Bioactive Marine Metabolites.
Lampiran 1
Lampiran 2
1 cm
Lampiran 3
Lampiran 4
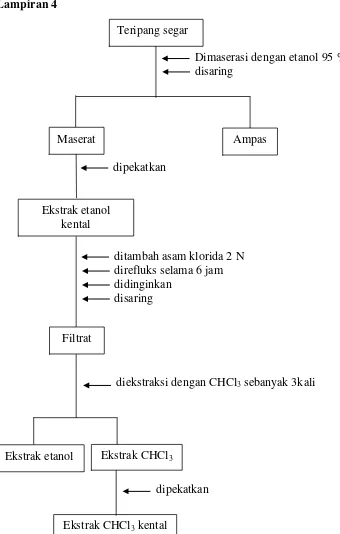
Gambar 3. Bagan Ekstraksi Senyawa Sapogenin dari Teripang Keterangan :
CHCl3 : kloroform
Dimaserasi dengan etanol 95 % disaring
Ekstrak etanol kental
ditambah asam klorida 2 N direfluks selama 6 jam didinginkan
diekstraksi dengan CHCl3 sebanyak 3kali
Ekstrak CHCl3
dipekatkan
Lampiran 4 (lanjutan)
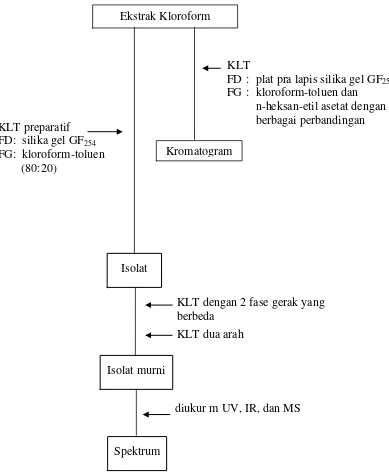
Gambar 4. Bagan Isolasi Senyawa Sapogenin dari Ekstrak Kloroform
Keterangan :
KLT dengan 2 fase gerak yang berbeda
Isolat murni
diukur m UV, IR, dan MS
Spektrum
Lampiran 5
bp bp bp bp bp
tp tp tp tp tp
I II III IV V
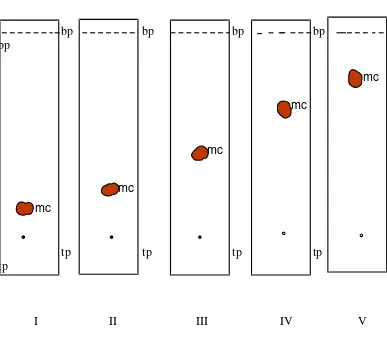
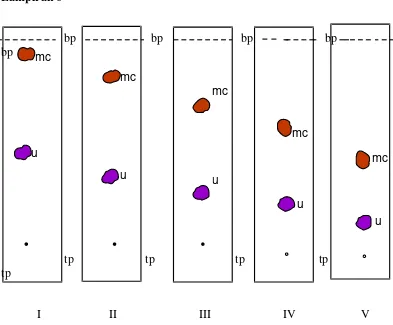
Gambar 5. Kromatogram hasil KLT ekstrak etanol
Keterangan: Fase diam silica gel GF 254, fase gerak n-hexan-etil asetat, penampak bercak Liebermann-Burchard, mc= merah coklat, bp=batas penotolan, tp=titik penotolan
I=90:10, II=80:20, III=70:30, IV=60:40, V=50:50, VI=40:60 mc
mc
mc
mc
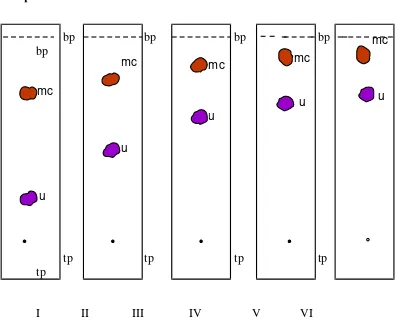
Lampiran 6 Gambar 6. Kromatogram hasil KLT ekstrak kloroform
Keterangan: Keterangan: Fase diam silica gel GF 254, fase gerak kloroform-toluen, penampak bercak Liebermann-Burchard, u=ungu, mc= merah coklat, bp=batas penotolan, tp=titik penotolan
Lampiran 7
Gambar 7. Kromatogram KLT ekstrak kloroform
Keterangan: Keterangan: Fase diam silica gel GF 254, fase gerak n-hexan-etil asetat, penampak bercak Liebermann-Burchard, u=ungu, mc= merah coklat, bp=batas penotolan, tp=titik penotolan
Lampiran 8
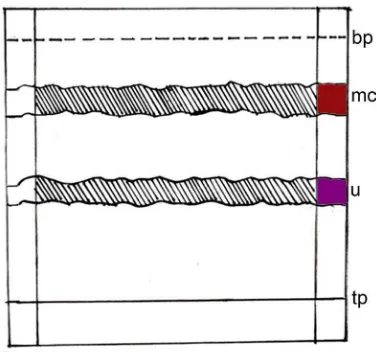
Gambar 8. Kromatogram KLT preparatif
Lampiran 9
bp
tp
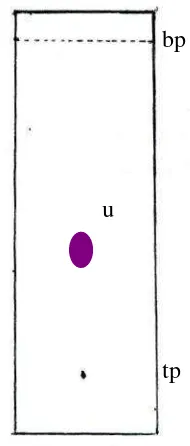
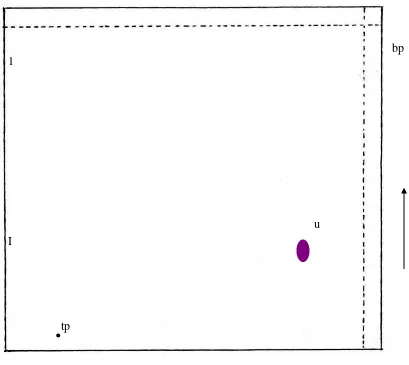
Gambar 9. Kromatogram hasil KLT isolat 1
Keterangan: Fase diam silica gel GF 254, fase gerak kloroform-toluen, penampak bercak Liebermann-Burchard, u=ungu, bp=batas penotolan, tp=titik penotolan
Lampiran 10
bp 1
I
bp 2 II
Gambar 10. Kromatogram hasil KLT dua arah
Keterangan: Fase diam silica gel GF 254, fase gerak 1= kloroform-toluen (80:20) fase gerak 2=kloroform-metanol (30:70), penampak bercak
Liebermann-Burchard, u=ungu, bp 1=batas penotolan 1, bp 2=batas penotolan 2, tp=titik penotolan
u
Lampiran 11
Lampiran 11
Lampiran 13