PENETAPAN KADAR BESI PADA BUAH ANGGUR MERAH
DAN ANGGUR HIJAU (
Vitis vinifera
) SECARA
KOLORIMETRI
SKRIPSI
OLEH:
SANDRY LUMBAN TOBING NIM 050804048
FAKULTAS FARMASI
PENETAPAN KADAR BESI PADA BUAH ANGGUR MERAH
DAN ANGGUR HIJAU (
Vitis vinifera
) SECARA
KOLORIMETRI
SKRIPSI
Diajukan untuk Melengkapi Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
SANDRY LUMBAN TOBING NIM 050804048
FAKULTAS FARMASI
PENGESAHAN SKRIPSI
PENETAPAN KADAR BESI PADA BUAH ANGGUR MERAH
DAN ANGGUR HIJAU (
Vitis vinifera
) SECARA KOLORIMETRI
OLEH:
SANDRY LUMBAN TOBING NIM: 050804048
Dipertahankan dihadapan Panitia Penguji Skripsi Fakultas Farmasi Universitas Sumatera Utara
Pada Tanggal : 06 Desember 2010
Pembimbing I Panitia Penguji
(Dra. Siti Nurbaya,Apt.) (Dra. Nurmadjuzita,M.Si.,Apt.) NIP. 195008261974122001 NIP. 194809041974122001
Pembimbing II
(Drs.Muchlisyam,M.Si.,Apt.) (Dra. Saleha Salbi,M.Si.,Apt.) NIP 195006221980021001 NIP. 194909061980032001
(Drs. Immanuel S.Meliala,M.Si.,Apt.) NIP 195001261983031002
(Dra. Siti Nurbaya,Apt.) NIP. 195008261974122001
Medan, Desember 2010 Fakultas Farmasi UniversitasSumatera Utara
Dekan
KATA PENGANTAR Salam damai sejahtera,
Puji syukur pada Tuhan Yesus Kristus atas berkat anugerah dan kasih
setia-Nya, hingga penulis dapat menjalani masa perkuliahan dan penelitian hingga
akhirnya menyelesaikan penyusunan skripsi ini untuk mencapai gelar Sarjana
Farmasi di Fakultas Farmasi di Fakultas Farmasi Universitas Sumatera Utara.
Ucapan terima kasih yang tulus tiada terhingga penulis sampaikan kepada
kedua orangtua tercinta, Ayahanda S.M Lumban Tobing dan Ibunda I.M Siahaan,
juga kepada Abangku Roy Dedy Lumban Tobing, dan adik-adikku Charlie, Indra,
Juanda, Mona, Seri dewi Lumban Tobing dan Juniar Sianipar, beserta seluruh
keluarga besar yang senantiasa memberikan motivasi, dukungan, perhatian,
semangat, dan doa kepada penulis selama perkuliahan hingga penyelesaian skripsi
ini.
Penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada Ibu
Dra.Siti Nurbaya,Apt dan Bapak Drs. Muchlisyam,M.Si.,Apt., selaku dosen
pembimbing yang telah membimbing penulis dengan penuh kesabaran, ketulusan,
dan keikhlasan selama melakukan penelitian hingga selesainya penulisan skripsi
ini.
Ucapan terimakasih juga disampaikan kepada:
1. Dekan Fakultas Farmasi USU, Prof. Dr. Sumadio Hadisahputra, Apt., yang
telah memberikan bantuan dan fasilitas selama masa pendidikan.
2. Ibu Dra.Nurmadjuzita,M.Si.,Apt., Ibu Dra. Saleha Salbi, M.Si., Apt., dan
Bapak Drs. Immanuel S. Meliala, M.Si., Apt., sebagai tim penguji yang sangat
3. Bapak Drs. Suryadi Achmad, M.Si, Apt., selaku dosen wali serta seluruh dosen
staf pengajar Fakultas Farmasi yang telah banyak membimbing dan mendidik
penulis selama masa perkuliahan hingga selesai.
4. Ibu Dra. Masfria, M.S., Apt., selaku Kepala Laboratorium Kimia Farmasi
Kualitatif dan Bapak Drs. Maralaut Batubara, M.Phill., Apt., selaku Kepala
Laboratorium Kimia Bahan Makanan yang telah membantu dan menyediakan
fasilitas kepada penulis selama melakukan penelitian.
5. Sahabat-sahabat terbaikku, “Christian Pharmacy ’05”, yaitu Andi, Intan, Riris,
Victor, Januar, Harri, Iwanto, Tagor, Rianti, Yes Olo, Hermin, Siska dan Ernita
dan abang senior Farmasi, adik-adik junior Farmasi, serta semua pihak yang
tidak dapat disebutkan satu persatu yang telah banyak membantu penulis
hingga selesainya penulisan skripsi ini.
Semoga Tuhan Yesus memberikan balasan yang berlipat ganda atas segala
kebaikan dan bantuan yang telah diberikan kepada penulis.
Akhir kata penulis menyadari bahwa tulisan ini masih belum sempurna.
Untuk itu penulis mengharapkan kritik dan saran yang membangun. Semoga skripsi
ini dapat memberikan sumbangan yang bermanfaat bagi ilmu pengetahuan
khususnya bidang farmasi.
Medan, 18 Desember 2010
Penulis,
ABSTRAK
Anggur merupakan tumbuhan merambat yang termasuk kedalam keluarga
Vitaceae. Buah ini mengandung banyak gizi termasuk besi. Besi merupakan
mineral yang dibutuhkan oleh tubuh kurang dari 100 mg perhari. Kekurangan besi
akan mengakibatkan anemia, pusing, kurang nafsu makan dan menurunnya
kekebalan tubuh.
Penetapan kadar besi dilakukan secara spektrofotometri sinar tampak
dengan pereaksi warna ammonium tiosianat yang diukur pada panjang gelombang
maksimum 458 nm. Larutan besi tiosianat memberikan warna merah yang stabil
dengan persamaan regresi Y= 0,1778X – 0,0018 dan nilai koefisien korelasi (r)
= 0,9998.
Dari hasil analisis diperoleh kadar besi pada buah anggur merah dan
anggur hijau dengan terlebih dahulu dilakukan destruksi basah yaitu : anggur merah
berbiji tanpa dikupas = 2,770 ± 0,08 mcg/g, anggur hijau berbiji tanpa dikupas
= 2,574 ± 0,05 mcg/g, anggur merah tanpa biji yang dikupas = 3,323 ± 0,02 mcg/g,
anggur hijau tanpa biji yang dikupas = 2,420 ± 0,02 mcg/g, anggur merah tanpa biji
dan tanpa dikupas = 2,689 ±0,015 mcg/g, anggur hijau tanpa biji dan tanpa dikupas
= 2,388 ± 0,05 mcg/g, anggur merah berbiji yang dikupas = 2,619 ± 0,018 mcg/g,
anggur hijau berbiji yang dikupas = 2,618 ± 0,018 mcg/g.
Kadar besi pada buah anggur merah dan anggur hijau secara destruksi
kering yaitu : anggur merah berbiji tanpa dikupas = 2,277 ± 0,069 mcg/g, anggur
hijau berbiji tanpa dikupas = 2,279 ± 0,043 mcg/g, anggur merah tanpa biji yang
dikupas = 1,779 ± 0,019 mcg/g, anggur hijau tanpa biji yang dikupas = 2,361 ±
anggur hijau tanpa biji dan tanpa dikupas = 2,348 ± 0,008 mcg/g, anggur merah
berbiji yang dikupas = 1,883 ± 0,078 mcg/g, anggur hijau berbiji yang dikupas
ABSTRACT
Wine is a creeping plant belonging to the family Vitaceae. This fruit
contains many nutrients including iron. Iron is a mineral needed by the body less
than 100 mg a day. Iron deficiency will cause anemia, dizziness, loss of appetite
and decreased immunity.
Determination of iron content carried by visible spectrophotometry with
ammonium thiocyanate reagent color is measured at maximum wavelength of
458 nm. Iron thiocyanate solution gives a stable red color with the regression
equation Y = 0.1778X - 0.0018 and correlation coefficient (r) = 0.9998.
From the results obtained by analysis of iron content in red grapes and green
grapes with the first conducted wet destruction, namely: red grapes have seeds
without shelled = 2.770 ± 0.08 mcg/g, green grapes have seeds without shelled
= 2,574 ± 0.05 mcg/g, seedless red grapes are peeled = 3.323 ± 0.02 mcg/g,
seedless green grapes are peeled = 2.420 ± 0.02 mcg/g, red wine and without a
peeled seedless = 2.689 ± 0.015 mcg/g, green grapes without seeds and without
shelled = 2.388 ± 0.05 mcg/g, red wine seeds are shelled = 2.619 ± 0.018 mcg/g,
which peeled seeded green grapes = 2.618 ± 0.018 mcg/g.
Iron content in red grapes and green grapes are dried destruction: red grapes
have seeds without shelled = 2.277 ± 0.069 mcg/g, green grapes have seeds without
shelled = 2.279 ± 0.043 mcg / g, seedless red grapes are peeled = 1.779 ± 0.019
mcg/g, seedless green grapes are peeled = 2.361 ± 0.026 mcg/g, red wine and
without a peeled seedless = 2.740 ± 0.025 mcg/g, seedless green grapes and without
shelled = 2.348 ± 0.008 mcg/g, red wine seeds are shelled = 1.883 ± 0.078
DAFTAR ISI
Halaman
JUDUL
HALAMAN PENGESAHAN
KATA PENGANTAR
ABSTRAK ... i
ABSTRACT ... iii
DAFTAR ISI ... iv
DAFTAR TABEL ... xiii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Perumusan Masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan Penelitian ... 4
BAB II TINJAUAN PUSTAKA ... 5
2.1 Buah Anggur ... 5
2.2 Besi ... 8
2.2.1 Daur Ulang Besi ... 8
2.2.2 Angka Kecukupan Besi yang Dianjurkan ... 9
2.2.3 Sumber Besi ... 9
2.3 Destruksi ... 10
2.3.2 Destruksi Kering ... 10
2.4 Spektrofotometri ... 11
2.5 Validasi Metode Analisis ... 11
2.6 Kecermatan (Accuracy) ... 12
2.7 Batas Deteksi ... 12
2.8 Batas Kuantitasi ... 13
BAB III METODOLOGI PENELITIAN... 14
3.1 Alat dan Bahan Penelitian ... 14
3.1.1Alat-alat Penelitian ... 14
3.1.2 Bahan ... 14
3.2 Metode Pengambilan Sampel ... 14
3.3 Pembuatan Pereaksi ... 14
3.4 Penetapan Kadar Besi ... . 15
3.4.1 Proses Destruksi ... 15
3.4.1.1 Dekstruksi Kering ... 15
3.4.1.2 Destruksi Basah ... 15
3.4.2 Pemeriksaan Kuantitatif Besi secara Spektrofotometri Sinar Tampak Menggunakan Amonium Tiosianat 0,1N ... 16
3.4.2.1 Pembuatan Larutan Induk Baku... 16
3.4.2.2 Pembuatan Kurva Serapan Larutan FeCl3 ... 16
3.4.2.3 Penentuan Waktu Kerja ... 17
3.4.2.4 Penentuan Kurva Kalibrasi Larutan Baku FeCl3 ... 17
3.4.3 Pemeriksaan Kuantitatif Besi Pada Sampel Anggur Merah Berbiji dan Tanpa Biji yang Dikupas Menggunakan Pereaksi Warna Amonium Tiosianat ... 17
3.6 Penetuan batas deteksi dan batas kuantitasi ... 22
BAB IV HASIL DAN PEMBAHASAN ... 23
4.1 hasil Uji Kuantitatif ... 23
4.1.1 Kurva Serapan Larutan Besi Tiosianat ... 23
4.1.2 Penentuan waktu Kerja larutan Besi tiosianat pada Panjang Gelombang Maksimum 458 nm ... 24
4.1.3 Kurva Kalibrasi Larutan Besi Tiosianat ... 25
4.1.4 Analisis Kadar Besi Pada Buah Anggur ... 27
4.1.4.1 Kadar besi pada anggur berbiji secara destruksi basah ... 27
4.1.4.2 Kadar besi pada anggur tanpa berbiji secara destruksi basah ... 27
4.1.4.3 Kadar besi pada anggur berbiji secara destruksi kering ... 28
4.1.4.4 Kadar besi pada anggur tanpa berbiji secara destruksi kering ... 28
4.1.4.5Kadar besi anggur merah hasil destruksi basah dibandingkan dengan destruksi kering ... 29
4.1.4.6 Kadar besi anggur hijau hasil destruksi basah dibandingkan dengan destruksi kering ... 30
BAB V KESIMPULAN DAN SARAN ... 31
5.1 Kesimpulan ... 31
5.2 Saran ... 32
DAFTAR PUSTAKA ... 33
DAFTAR TABEL
Tabel 1. Panjang Gelombang Maksimum Larutan Besi Tiosianat ... .. 24
Tabel 2. Data Penentuan Waktu Kerja Larutan Besi Tiosianat
DAFTAR GAMBAR
Gambar 1. Kurva Serapan Larutan Besi Tiosianat ... 23
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Perhitungan Persamaan Regresi Besi ... 34
Lampiran 2. Perhitungan Batas Deteksi dan Batas Kuantitasi ... 36
Lampiran 3. Data Berat Sampel,Absorbansi, dan Kadar Besi pada
Anggur Merah dengan Destruksi Basah ... 37
Lampiran 4. Data Berat Sampel,Absorbansi, dan Kadar Besi pada
Anggur Merah dengan Cara Destruksi Kering ... 38
Lampiran 5. Data Berat Sampel,Absorbansi, dan Kadar Besi pada
Anggur Hijau dengan Destruksi Basah ... 39
Lampiran 6. Data Berat Sampel,Absorbansi, dan Kadar Besi pada
Anggur Hijau dengan Cara Destruksi Kering ... 40
Lampiran 7. Perhitungan Kadar Besi sebenarnya dalam Buah Anggur Merah Berbiji Tanpa Dikupas dengan Metode Destruksi
Basah ... 41
Lampiran 8. Perhitungan Kadar Besi sebenarnya dalam Buah Anggur Merah Berbiji Tanpa Dikupas dengan Metode Destruksi
Kering ... 43
Lampiran 9. Perhitungan Kadar Besi sebenarnya dalam Buah Anggur Hijau Berbiji Tanpa Dikupas dengan Metode Destruksi
Basah ... 45 Lampiran 10. Perhitungan Kadar Besi sebenarnya dalam Buah Anggur
Hijau Berbiji Tanpa Dikupas dengan Metode Destruksi
Kering ... 47
Lampiran 11. Data Uji Perolehan Kembali Anggur Merah Tanpa Biji
Dan Tanpa Dikupas Secara Destruksi Basah ... 49
Lampiran 12. Data Uji Perolehan Kembali Anggur Merah Berbiji
Yang Dikupas Secara Destruksi Kering ... 50
Lampiran 13. Contoh Perhitungan Kadar Besi pada Buah Anggur Merah
Berbiji tanpa Dikupas secara Destruksi Basah ... 51
Lampiran 14. Contoh Perhitungan Kadar Besi pada Buah Anggur Merah
Berbiji tanpa Dikupas secara Destruksi Kering ... 53
ABSTRAK
Anggur merupakan tumbuhan merambat yang termasuk kedalam keluarga
Vitaceae. Buah ini mengandung banyak gizi termasuk besi. Besi merupakan
mineral yang dibutuhkan oleh tubuh kurang dari 100 mg perhari. Kekurangan besi
akan mengakibatkan anemia, pusing, kurang nafsu makan dan menurunnya
kekebalan tubuh.
Penetapan kadar besi dilakukan secara spektrofotometri sinar tampak
dengan pereaksi warna ammonium tiosianat yang diukur pada panjang gelombang
maksimum 458 nm. Larutan besi tiosianat memberikan warna merah yang stabil
dengan persamaan regresi Y= 0,1778X – 0,0018 dan nilai koefisien korelasi (r)
= 0,9998.
Dari hasil analisis diperoleh kadar besi pada buah anggur merah dan
anggur hijau dengan terlebih dahulu dilakukan destruksi basah yaitu : anggur merah
berbiji tanpa dikupas = 2,770 ± 0,08 mcg/g, anggur hijau berbiji tanpa dikupas
= 2,574 ± 0,05 mcg/g, anggur merah tanpa biji yang dikupas = 3,323 ± 0,02 mcg/g,
anggur hijau tanpa biji yang dikupas = 2,420 ± 0,02 mcg/g, anggur merah tanpa biji
dan tanpa dikupas = 2,689 ±0,015 mcg/g, anggur hijau tanpa biji dan tanpa dikupas
= 2,388 ± 0,05 mcg/g, anggur merah berbiji yang dikupas = 2,619 ± 0,018 mcg/g,
anggur hijau berbiji yang dikupas = 2,618 ± 0,018 mcg/g.
Kadar besi pada buah anggur merah dan anggur hijau secara destruksi
kering yaitu : anggur merah berbiji tanpa dikupas = 2,277 ± 0,069 mcg/g, anggur
hijau berbiji tanpa dikupas = 2,279 ± 0,043 mcg/g, anggur merah tanpa biji yang
dikupas = 1,779 ± 0,019 mcg/g, anggur hijau tanpa biji yang dikupas = 2,361 ±
anggur hijau tanpa biji dan tanpa dikupas = 2,348 ± 0,008 mcg/g, anggur merah
berbiji yang dikupas = 1,883 ± 0,078 mcg/g, anggur hijau berbiji yang dikupas
ABSTRACT
Wine is a creeping plant belonging to the family Vitaceae. This fruit
contains many nutrients including iron. Iron is a mineral needed by the body less
than 100 mg a day. Iron deficiency will cause anemia, dizziness, loss of appetite
and decreased immunity.
Determination of iron content carried by visible spectrophotometry with
ammonium thiocyanate reagent color is measured at maximum wavelength of
458 nm. Iron thiocyanate solution gives a stable red color with the regression
equation Y = 0.1778X - 0.0018 and correlation coefficient (r) = 0.9998.
From the results obtained by analysis of iron content in red grapes and green
grapes with the first conducted wet destruction, namely: red grapes have seeds
without shelled = 2.770 ± 0.08 mcg/g, green grapes have seeds without shelled
= 2,574 ± 0.05 mcg/g, seedless red grapes are peeled = 3.323 ± 0.02 mcg/g,
seedless green grapes are peeled = 2.420 ± 0.02 mcg/g, red wine and without a
peeled seedless = 2.689 ± 0.015 mcg/g, green grapes without seeds and without
shelled = 2.388 ± 0.05 mcg/g, red wine seeds are shelled = 2.619 ± 0.018 mcg/g,
which peeled seeded green grapes = 2.618 ± 0.018 mcg/g.
Iron content in red grapes and green grapes are dried destruction: red grapes
have seeds without shelled = 2.277 ± 0.069 mcg/g, green grapes have seeds without
shelled = 2.279 ± 0.043 mcg / g, seedless red grapes are peeled = 1.779 ± 0.019
mcg/g, seedless green grapes are peeled = 2.361 ± 0.026 mcg/g, red wine and
without a peeled seedless = 2.740 ± 0.025 mcg/g, seedless green grapes and without
shelled = 2.348 ± 0.008 mcg/g, red wine seeds are shelled = 1.883 ± 0.078
BAB I PENDAHULUAN 1.1 Latar Belakang
Mineral merupakan kebutuhan tubuh manusia yang mempunyai peranan
penting dalam pemeliharaan fungsi tubuh, antara lain untuk pengaturan kerja
enzim-enzim, pemeliharaan keseimbangan elektrolit, membantu pembentukan
ikatan yang memerlukan mineral misalnya proses pembentukan haemoglobin.
Mineral digolongkan atas mineral makro dan mineral mikro. Mineral makro adalah
mineral yang dibutuhkan tubuh dalam jumlah lebih dari 100 mg sehari, sedangkan
mineral mikro dibutuhkan tubuh kurang dari 100 mg sehari. Yang termasuk mineral
makro antara lain natrium, klorida, kalium, kalsium, fosfor, magnesium, dan sulfur.
Sedangkan yang termasuk mineral mikro antara lain besi, seng, mangan dan
tembaga (Almatsier, 2004).
Unsur besi yang tergolong mineral mikro merupakan komponen utama dari
haemoglobin (Hb), sehingga kekurangan besi dalam tubuh akan mempengaruhi
pembentukan Hb. Sel darah merah yang masih muda(korpuskula), mengandung Hb
yang diproduksi dalam sumsum tulang untuk mengganti sel darah merah yang
rusak. Jumlah normal zat besi pada usia 13-19 tahun yaitu 19-25 mg (perempuan)
dan 17-23 mg (laki-laki), jumlah normal zat besi pada 20 – 45 tahun yaitu 25-26 mg
(perempuan), 23–25 mg (laki-laki). Kekurangan zat besi merupakan penyebab
utama dari pada anemia atau kadar haemoglobin di bawah normal yaitu pada pria
kurang dari 14-18 gr/100ml, pada perempuan 12-16 gr/100ml (wanita). Disamping
itu kekurangan zat besi juga dapat disebabkan oleh gangguan penyerapan besi
Beberapa jenis warna buah anggur yang beredar dipasaran kota Medan
antara lain anggur warna merah dan anggur warna hijau dan buah anggur ini ada
yang berbiji dan tanpa biji. Untuk menentukan besi dari bahan nabati dapat
dilakukan penetapan kadar dengan terlebih dahulu dilakukan destruksi basah dan
destruksi kering.
Zat besi dalam anggur dapat ditetapkan kadarnya dengan beberapa cara
antara lain: metode kolorimetri menggunakan spektrofotometri visibel
(Vogel,1994), metode titrasi, dan metode spektrofotometri serapan atom. Zat besi
diukur menggunakan spektrofotometri visibel dengan menggunakan pereaksi warna
amonium tiosianat yang menghasilkan besi tiosianat yang berwarna merah tua yang
dapat diukur pada panjang gelombang maksimum 458 nm. Digunakan metode
spektrofotometri visibel untuk pengukuran kadar besi pada buah anggur karena
metode spektrofotometri visibel sangat baik digunakan untuk mengukur larutan
yang berwarna pada konsentrasi kecil (ppm).
Berdasarkan hal tersebut di atas, penulis memilih meneliti buah anggur.
Kandungan besi buah anggur yang diteliti yaitu anggur merah dan anggur hijau,
yang berbiji dan tanpa biji, anggur merah dan anggur hijau yang dikupas dan tanpa
dikupas dengan terlebih dahulu didestruksi basah dan didestruksi kering, setelah itu
dilakukan penetapan kadar besi dengan cara mengukur absorbansi larutan besi
tiosianat secara spektrofotometri visibel pada panjang gelombang maksimum 458
1.2 Perumusan Masalah
a. Apakah terdapat perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau yang berbiji tanpa dikupas dan yang dikupas
secara destruksi basah
b. Apakah terdapat perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau tanpa biji tanpa dikupas dan yang dikupas
secara destruksi basah
c. Apakah terdapat perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau yang berbiji tanpa dikupas dan yang dikupas
secara destruksi kering
d. Apakah terdapat perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau tanpa biji tanpa dikupas dan yang dikupas
secara destruksi kering
1.3 Hipotesa
a. Terdapat perbedaan kadar besi yang terdapat pada buah anggur merah dan
buah anggur hijau yang berbiji tanpa dikupas dan yang dikupas secara
destruksi basah
b. Terdapat perbedaan kadar besi yang terdapat pada buah anggur merah dan
buah anggur hijau tanpa biji tanpa dikupas dan yang dikupas secara
destruksi basah
c. Terdapat perbedaan kadar besi yang terdapat pada buah anggur merah dan
buah anggur hijau yang berbiji tanpa dikupas dan yang dikupas secara
d. Terdapat perbedaan kadar besi yang terdapat pada buah anggur merah dan
buah anggur hijau tanpa biji tanpa dikupas dan yang dikupas secara
destruksi kering
1.4Tujuan
a. Untuk mengetahui perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau yang berbiji tanpa dikupas dan yang dikupas
secara destruksi basah
b. Untuk mengetahui perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau tanpa biji tanpa dikupas dan yang dikupas
secara destruksi basah
c. Untuk mengetahui perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau yang berbiji tanpa dikupas dan yang dikupas
secara destruksi kering
d. Untuk mengetahui perbedaan kadar besi yang terdapat pada buah anggur
merah dan buah anggur hijau tanpa biji tanpa dikupas dan yang dikupas
BAB II
TINJAUAN PUSTAKA 2.1 Buah Anggur
Taksonomi buah anggur sebagai berikut :
Kingdom : Plantae
Divisio : Magnoliophyta
Class : Magnoliopsida
Ordo : Vitales
Family : Vitaceae
Genus : Vitis L
Species : VitisVinifera
Anggur merupakan salah satu tanaman yang hidup pada daerah dataran
rendah. Tidak seperti kebanyakan tanaman lainnya, tanaman anggur justru
membutuhkan musim kemarau panjang berkisar 4-7 bulan agar dapat tumbuh
dengan baik dan intensitas cahaya matahari yang cukup tinggi.
Buah anggur memiliki banyak spesies, antara lain:
- Vitis vinifera
- Vitis labrusca
- Vitis riparia
- Vitis rotundifolia
- Vitis aestivalis
Ada 75 macam varietas anggur yang terdapat di Indonesia antara lain
Groscolman, Probolinggo biru, Probolinggo 81, Sultana ( Thompson seedless),
Golden champion, Briliant 4, beacon, banjar sari dan lain-lain.
Anggur bermanfaat karena mengandung berbagai jenis senyawa metabolit
sekunder, terutama golongan flavonoid dan antosianin, serta resveratol. Anggur
mampu memperlancar aliran darah dalam arteri terkait dengan aktivitasnya
terhadap sel-sel otot halus sehingga dapat mengurangi serangan jantung.
Kandungan gizi anggur merah dan anggur hijau per 100 g yaitu:
Tenaga 70 kkal 290 kJ
Karbohidrat 18.1 g
- Gula 15.48 g
- Serat pangan 0.9 g
Lemak 0.16 g
Protein 0.72 g
Tiamina (Vit. B1) 0.069 mg 5%
Riboflavin (Vit. B2) 0.07 mg 5%
Niasin (Vit. B3) 0.188 mg 1%
Asam pantotenat (B5) 0.05 mg 1%
Vitamin B6 0.086 mg 7%
Asam folat (Vit. B9) 2 µg 1%
Vitamin B12 0 µg 0%
Vitamin C 10.8 mg 18%
Vitamin K 22 µg 21%
Fosforus 20 mg 3%
Kalium 191 mg 4%
Kalsium 10 mg 1%
Magnesium 7 mg 2%
Natrium 3.02 mg 0%
Seng 0.07 mg 1%
Rajin mengkonsumsi anggur atau jus anggur bisa membangkitkan
semangat, menghilangkan rasa lelah, dan meningkatkan kekebalan tubuh. Secara
alami, buah anggur merupakan makanan pembentuk basa (alkaline forming). Sifat
membentuk basa dengan kandungan air berlimpah dalam anggur menjadikan
pembuluh darah memiliki kemampuan lebih besar untuk mengurangi timbunan
toksin dan lemak dalam pembuluh darah. Kondisi ini mencegah terjadinya
penyempitan/penyumbatan pembuluh darah.
Anggur juga mengandung enzim yang bersifat tonik penggiat fungsi
empedu. Peningkatan fungsi empedu akan meningkatkan efisiensi pengubahan
lemak mejadi asam empedu, yang akan dibuang ke luar tubuh, sehingga mencegah
terjadinya lonjakan kadar lemak darah (hiperlipidemia). Karena itu, rajin
menyantap anggur dan mengosumsi jus anggur amat disarankan bagi pengidap
hipertensi, serta kadar kolesterol/trigleserida darah berlebihan.
Tanaman anggur paling rentan terhadap serangan kapang atau jamur.
Kapang mengganggu perkembangan optimal buah-buah anggur. Tetapi serangan
kapang justru mendatangkan keuntungan. Secara alami tanaman anggur akan
membentuk antibodi 3,5,4-trihidroksi-trans-stibena, yang populer dengan nama
2.2 Besi
Besi merupakan mineral mikro yang paling banyak terdapat di dalam tubuh
manusia dan hewan yaitu sebanyak 3-5 g di dalam tubuh manusia. Besi mempunyai
beberapa fungsi esensial di dalam tubuh : sebagai alat angkut oksigen dari
paru-paru ke jaringan tubuh, sebagai alat angkut elektron di dalam sel, dan sebagai
bagian terpadu berbagai reaksi enzim di dalam jaringan tubuh.
Tubuh sangat efisien dalam penggunaan besi. Sebelum diabsorpsi, didalam
lambung besi dibebaskan dari ikatan organik seperti protein. Sebagian besar besi
dalam bentuk feri direduksi menjadi bentuk fero. Hal ini terjadi dalam suasana
asam di dalam lambung dengan adanya HCl dan vitamin C yang terdapat di dalam
makanan. Absorpsi terutama terjadi di bagian atas usus halus (duodenum) dengan
alat angkut protein khusus (Almatsier, 2004).
2.2.1 Proses daur ulang besi
Sel darah merah rata-rata berumur kurang lebih empat bulan. Sel-sel hati
dan limpa akan mengambilnya dari darah, memecahnya dan menyiapkan
produk-produk pemecahan tersebut untuk dikeluarkan dari tubuh atau di daur ulang. Zat
besi sebagian besar mengalami proses daur ulang. Hati mengikatkannya ke
transferin darah, yang mengangkutnya kembali ke sumsum tulang untuk digunakan
kembali membuat sel darah merah baru. Hanya sedikit sekali besi dikeluarkan dari
tubuh, terutama melalui urin, keringat, dan kulit yang mengelupas. Hanya bila
terjadi perdarahan, tubuh bisa lebih banyak kehilangan besi. Kehilangan besi pada
2.2.2 Angka kecukupan besi yang dianjurkan
Widya karya pangan dan gizi tahun 1998 menetapkan angka kecukupan besi untuk
Indonesia sebagai berikut :
- bayi : 3-5 mg
- balita : 8-9 mg
- anak sekolah : 10 mg
- remaja laki-laki : 14-17 mg
- remaja perempuan : 14-25 mg
- dewasa laki-laki : 13 mg
- dewasa perempuan : 14-26 mg
- ibu hamil : + 20 mg
- ibu menyusui : + 2 mg (Almatsier, 2004).
2.2.3 Sumber besi
Nilai besi berbagai bahan makanan ( mg/100g)
Bahan Makanan Nilai Fe
Tempe kacang kedelai 10,0
Kacang merah 5,0
Kelapa tua 2,0
Udang segar 8,0
Anggur 0,36
Tepung terigu 0,25
Telur bebek 2,8
Ikan segar 2,0
Pisang ambon 0,5
2.3.1 Destruksi basah
Penentuan kandungan mineral dalam bahan makanan dapat dilakukan
dengan metode destruksi yaitu destruksi kering, destruksi basah dan homogenat
asam. Pemilihan cara tersebut tergantung pada sifat zat organik dan anorganik yang
ada dalam bahan mineral yang akan dianalisis.
Metode destruksi basah untuk penentuan unsur-unsur mineral di dalam
bahan makanan merupakan metode yang paling baik. Prinsip pengabuan basah
adalah penggunaan HNO3 untuk mendestruksi zat organik pada suhu rendah agar
kehilangan mineral akibat penguapan dapat dihindari.
Pada umumnya metode ini digunakan untuk menganalisis Fe, As, Cu, Pb,
Sn dan Zn. Keuntungan pengabuan basah adalah: suhu yang digunakan tidak dapat
melebihi titik didih larutan dan pada umumnya karbon lebih cepat hancur. Cara
pengabuan basah yang dapat dilakukan ada 3 cara, yaitu:
1. Pengabuan menggunakan HNO3
2. Pengabuan menggunakan HNO3 (p), H2SO4 (p) dan HClO4 (p).
3. Pengabuan menggunakan HNO3 (p), H2SO4 (p) dan H2O2 (p).
2.3.2 Destruksi kering
Destruksi kering merupakan metode dimana sampel yang telah diketahui
beratnya diletakkan pada sebuah krus, dan mengalami proses pengabuan dalam
tanur yang dipanaskan pada suhu tinggi. Krus umumya terbuat dari platinum dan
juga tersedia krus yang terbuat dari perselen, silika, besi, dan nikel.
Perhatian harus diberikan pada saat melakukan destruksi kering karena ada
- Kehilangan mekanis pada saat pengeringan sampel, misalnya jika sampel
dikeringkan dengan sangat cepat, tejadi kehilangan zat dari krus. Dengan
demikian untuk mencegah hal ini terjadi, diperlukan proses pengeringan yang
relatif lambat
- Kehilangan zat pada saat penguapan sampel dalam tanur. Logam yang memiliki
titik lebur yang rendah seperti Sb, Cr, Mo, Fe, Mg, Al kemungkinan akan mudah
rusak saat pengabuan pada suhu 750o C.
- Penyerapan zat ke dalam krus dapat saja terjadi, kecuali pada wadah platinum.
Hal terburuk dapat terjadi apabila sampel mengandung logam halida atau
senyawa phospat.
2.4 Spektrofotometri
Spektrofotometri merupakan suatu metoda analisa yang didasarkan pada
pengukuran serapan sinar monokromatis oleh suatu lajur larutan berwarna pada
panjang gelombamg spesifik dengan menggunakan monokromator prisma atau kisi
difraksi dengan detektorfototube.
Spektrofotometri dapat dianggap sebagai perluasan suatu pemeriksaan
visual dengan studi yang lebih mendalam dari absorbsi energi. Absorbsi radiasi
oleh suatu sampel diukur pada berbagai panjang gelombangdan dialirkan oleh suatu
perkam untuk menghasilkan spektrum tertentu yang khas untuk komponen yang
berbeda.
2.5 Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter
tertentu berdasarkan percobaan laboratorium untuk membuktikan bahwa parameter
yang harus dipertimbangkan dalam validasi metode analisis diuraikan dan
didefinisikan sebagaimana cara penentuannya (Harmita, 2004). Beberapa parameter
validasi diuraikan di bawah ini:
2.6 Kecermatan (accuracy)
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis
dengan kadar analit yang sebenarnya. Kecermatan dapat dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan. (Harmita, 2004).
Perolehan kembali dapat dihitung dengan rumus berikut (Harmita, 2004):
Keterangan:
Cr = konsentrasi sampel yang diperoleh setelah penambahan larutan baku
Ca = konssentrasi sampel sebelum penambahan larutan baku
C = konsentrasi larutan baku yg ditambahkan
2.10.2 Keseksamaan (precision)
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara
hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika
prosedur diterapkan secara berulang pada sampel-sampel yang diambil dari
campuran yang homogen (Harmita, 2004).
2.7 Batas Deteksi
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat
dideteksi yang masih memberikan respon signifikan. Batas ini dapat diperoleh dari
kalibrasi standar yang diukur sebanyak 6 sampai 10 kali. Batas deteksi dapat
dihitung dengan rumus sebagai berikut (Harmita, 2004):
Keterangan: SB = simpangan baku
2.7 Batas Kuantitasi
Batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang
masih dapat memenuhi kriteria cermat dan seksama. Batas ini dapat diperoleh dari
kalibrasi standar yang diukur sebanyak 6 sampai 10 kali. Batas kuantitasi dapat
dihitung dengan rumus sebagai berikut (Harmita, 2004):
Batas kuantitasi =
BAB III
METODOLOGI PENELITIAN
Penelitian dilaksanakan di Laboratorium Kimia Farmasi Kualitatif dan
Laboratorium Sintesa Bahan Obat Fakultas Farmasi Universitas Sumatera Utara.
3.1 Alat dan Bahan Penelitian 3.1.1 Alat-alat Penelitian
Alat-alat yang digunakan antara lain : spektrofotometri UV/Visible (UV
mini 1240 Shimadzu), tanur, desikator, hot plate, neraca listrik (AND GF-200),
kertas saring dan alat gelas.
3.1.2 Bahan
Bahan-bahan yang digunakan dalam penelitian ini jika tidak dinyatakan lain
mempunyai kualitas pro analis yaitu Ferri klorida, asam nitrat 5N, ammonium
tiosianat 0,1N dan aquadest (Laboratorium Kimia Farmasi Kuantitatif Fakultas
Farmasi Universitas Sumatera Utara).
3.2Metode Pengambilan Sampel
Pengambilan sampel dilakukan secara purposif yaitu sampel yang berasal
dari Brastagi Supermarket tanpa membandingkan anggur dari supermarket lain
yang ada di kota Medan.
3.3Pembuatan Pereaksi
3.3.1Larutan amonium tiosianat 0,1N
Dilarutkan 8 g amonium tiosianat dalam air hingga 100 ml (Farmakope
3.3.2 Larutan asam nitrat 5N
Larutan HNO3 65% v/v sebanyak 349 ml diencerkan dengan air suling
hingga 1000 ml (Farmakope Indonesia Edisi III,1979)
3.4 Prosedur Penetapan Kadar besi 3.4.1 Proses destruksi
Sebelum dilakukan penetapan kadar besi terlebih dahulu buah anggur
didestruksi yaitu dengan cara destruksi kering dan destruksi basah.
3.4.1.1Destruksi kering
Buah anggur dicuci bersih sebanyak ± 500 gr, lalu dibiarkan mengering
diudara bebas diruang laboratorium. Kemudian diblender dan ditimbang seksama
50 gr buah anggur dalam krus porselen. Dipanaskan diatas hot plate untuk
menghilangkan air. Diabukan di tanur dengan temperatur awal 1000C dan
perlahan-lahan temperatur dinaikkan menjadi 7000C dengan interval 250C setiap 5 menit.
Destruksi dilakukan selama 16 jam dan dibiarkan dingin pada desikator. Hasil
destruksi dilarutkan dalam 5 ml HNO3 5N kemudian dipanaskan di atas penangas
air selama 5 menit. Pada residu ditambahkan 5 ml HNO3 5N sampai residu larut.
Disaring dan ditampung dalam labu tentukur 100 ml. kemudian sisa pada krus
porselen dibilas dengan aquades sebanyak 3 kali. Prosedur diatas dilakukan untuk
anggur merah dan anggur hijau berbiji dan tanpa biji maupun yang dikupas ataupun
tidak dikupas.
3.4.1.2 Destruksi basah
Buah anggur dicuci bersih sebanyak ± 500 g, lalu dibiarkan mengering di
udara bebas diruang laboratorium. Kemudian diblender, selanjutnya ditimbang
dipanaskan di atas hotplate hingga larutan bening. Kemudian disaring
menggunakan kertas saring. Ditampung dalam labu tentukur 100 ml. Sisa pada
kertas saring dibilas dengan aquadest. Prosedur dilakukan untuk anggur merah dan
anggur hijau yang berbiji dan tanpa biji yang dikupas maupun tidak dikupas.
3.4.2Pemeriksaan Kuantitatif Besi secara Spektrofotometri Sinar Tampak menggunakan Amonium Tiosianat 0,1N
3.4.2.1 Pembuatan Larutan Induk Baku
FeCl3 ditimbang teliti 0,343 g kemudian dimasukkan kedalam labu tentukur
100 ml, dan dilarutkan dengan aquadest sampai garis tanda.
Kadar besi = % FeCl3X
3.4.2.2 Pembuatan Kurva Serapan Larutan Besi
Larutan Induk Baku dipipet 2,3 ml dimasukkan kedalam labu tentukur 100
ml kemudian ditambahkan 5 ml larutan amonium tiosianat 0,1N, kemudian
diencerkan dengan aquadest hingga garis tanda (C = 2,713 mcg/ml). Dikocok
sampai homogen larutan tersebut dan diukur serapannya pada panjang gelombang
3.4.2.3 Penentuan Waktu Kerja
Larutan Induk Baku dipipet 2,3 ml dimasukkan kedalam labu tentukur 100
ml kemudian ditambahkan 5 ml larutan amonium tiosianat 0,1N, kemudian
diencerkan dengan aquadest hingga garis tanda (C = 2,713 mcg/ml). Dikocok
sampai homogen larutan tersebut dan diukur serapannya pada panjang gelombang
400-800 nm mulai menit ke-5 hingga menit ke-35.
3.4.2.4 Penentuan Kurva Kalibrasi Larutan Baku Besi
Larutan Induk Baku tersebut dipipet 0; 1,8; 2,1; 2,4; 2,7; dan 3,0 ml dan
masing masing dimasukkan ke dalam labu tentukur 100 ml, ditambahkan 5 ml
larutan amonium tiosianat 0,1N, kemudian diencerkan dengan aquadest hingga
garis tanda. Dikocok sampai homogen larutan tersebut dan diukur setelah menit
ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458 nm.
3.4.3 Pemeriksaan Kuantitatif Besi pada Anggur Berbiji dan Tanpa Biji yang Dikupas maupun Tanpa Dikupas menggunakan Pereaksi Warna Amonium Tiosianat 0,1N
3.4.3.1 Pada anggur merah berbiji tanpa dikupas secara destruksi kering Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
Kadar (mcg/gr) = B CxVxFp
C = Konsentrasi Larutan Sampel (mcg/ml)
V = Volume Larutan (ml)
B = Berat Sampel (gr)
3.4.3.2 Pada anggur merah berbiji tanpa dikupas secara destruksi basah
Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.3 Pada anggur merah berbiji yang dikupas secara destruksi kering
Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.4 Pada anggur merah berbiji yang dikupas secara destruksi basah
Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.5 Pada anggur merah tanpa biji tanpa dikupas secara destruksi kering Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.6 Pada anggur merah tanpa biji tanpa dikupas secara destruksi basah Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.7 Pada anggur merah tanpa biji yang dikupas secara destruksi kering Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.8 Pada anggur merah tanpa biji yang dikupas secara destruksi basah Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.9 Pada anggur hijau berbiji tanpa dikupas secara destruksi kering
Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.10 Pada anggur hijau berbiji tanpa dikupas secara destruksi basah
Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.11 Pada anggur hijau berbiji yang dikupas secara destruksi kering
Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.12 Pada anggur hijau berbiji yang dikupas secara destruksi basah
Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.13 Pada anggur hijau tanpa biji tanpa dikupas secara destruksi kering Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.14 Pada anggur hijau tanpa biji tanpa dikupas secara destruksi basah Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.15 Pada anggur hijau tanpa biji yang dikupas secara destruksi kering Larutan uji hasil destruksi kering dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.4.3.16 Pada anggur hijau tanpa biji yang dikupas secara destruksi basah Larutan uji hasil destruksi basah dimasukkan kedalam labu tentukur 100 ml
kemudian ditambahkan 5 ml amonium tiosianat 0,1N dan diencerkan dengan
aquadest hingga garis tanda. Dikocok sampai homogen larutan tersebut dan diukur
setelah menit ke-18 hingga menit ke-20 pada penjang gelombang maksimum 458
nm.
3.5 Prosedur Uji Ketetapan
Buah anggur ditimbang seksama sebanyak 50 g, dimasukkan ke dalam
yang sama seperti 2.4.2, lalu dihitung persentase uji perolehan kembali (uji
recovery) dengan rumus :
% recovery = x100%
3.6 Penentuan Batas Deteksi dan Batas Kuantitasi
Penentuan batas deteksi dapat dihitung berdasarkan pada standar deviasi
(SD) respon dan kemiringan (slope) linieritas baku dengan rumus :
(SD) =
Sedangkan untuk penentuan batas kuantitasi dapat dipergunakan rumus :
Batas Kuantitasi = Slope
SD
10
BAB IV
HASIL DAN PEMBAHASAN 4.1 Hasil Uji Kuantitatif
4.1.1 Kurva Serapan Larutan Besi Tiosianat
Sebelum dilakukan penetapan kadar besi pada buah anggur, terlebih dahulu
dilakukan pengukuran kurva serapan larutan baku besi, yaitu larutan FeCl3 dengan
menambahkan pereaksi warna amonium tiosianat 0,1N, menghasilkan warna merah
yang diukur pada range panjang gelombang 400-800 nm . Diperoleh kurva serapan
larutan besi seperti Gambar 1.
Gambar 1. Kurva Serapan Larutan Besi Tiosianat pada panjang gelombang 400-800 nm
Dari kurva diatas menunjukkan bahwa larutan besi tiosianat dapat diukur
dengan spektrofotometri visibel, karena warna merah larutan besi tiosianat
Puncak serapan larutan besi tiosianat dengan pereaksi warna amonium tiosianat
0,1N dalam pelarut aquadest, terbentuk warna merah darah yang mempunyai pada
panjang gelombang maksimum 458 nm. Dapat dilihat pada Tabel 1.
Tabel 1. Panjang Gelombang Maksimum Larutan Besi Tiosianat yaitu 458 nm 4.1.2 Penentuan Waktu Kerja Larutan Besi Tiosianat pada Panjang Gelombang Maksimum 458 nm
Untuk menentukan waktu kerja larutan besi tiosianat, digunakan larutan
baku besi yang diukur absorbansinya pada λ 458 nm pada menit ke-5 sampai menit
Tabel 2. Data penentuan waktu kerja larutan besi tiosianat (C=2,713 mcg/ml) Pada λ= 458 nm
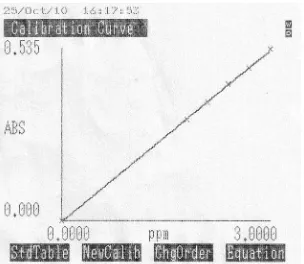
4.1.3 Kurva Kalibrasi Larutan Besi tiosianat
Kurva kalibrasi larutan besi diperoleh dengan cara mengukur absorbansi
dari larutan besi tiosianat. Dari pengukuran kurva kalibrasi untuk besi diperoleh
persamaan garis regresi yaitu: Y = 0,1778X – 0,0018. Kurva kalibrasi larutan baku
Gambar 2. Kurva Kalibrasi Larutan Induk Baku Besi
Berdasarkan kurva diatas diperoleh hubungan yang linier antara konsentrasi
dengan serapan (absorbansi) dengan nilai koefisien korelasi (r) sebesar 0,9998.
Nilai r ini menunjukkan hubungan korelasi yang positif antara konsentrasi dan
absorbansi (Rohman, 2007). Koefisien korelasi (r) dapat kita lihat pada persamaan
4.1.4 Analisis Kadar Besi pada Buah anggur
Penentuan kadar besi dilakukan secara Spektrofotometri visibel. Konsentrasi
besi pada buah anggur ditentukan berdasarkan persamaan garis regresi linier kurva
kalibrasi larutan standar FeCl3.
4.1.4.1 Kadar besi pada anggur berbiji secara destruksi basah
Dari lampiran 3 dapat dilihat bahwa kadar besi anggur merah berbiji tanpa
dikupas yaitu 2,770 ± 0,08 mcg/g dan kadar besi anggur merah berbiji yang dikupas
yaitu 2,619 ± 0,018 mcg/g. Dari kadar diatas disimpulkan bahwa seharusnya kadar
besi anggur merah berbiji yang dikupas lebih besar dibandingkan kadar anggur
merah berbiji yang dikupas, karena pada kulit banyak terdapat lebih banyak
flavonoid dan resveratrol, dibandingkan besi. Besi tersebut lebih banyak terdapat
pada daging buah (Anonim,2009).
Dari lampiran 5, kadar anggur hijau berbiji tanpa dikupas yaitu 2,574 ± 0,05
mcg/g dan kadar besi anggur hijau berbiji yang dikupas yaitu 2,618 ± 0,018 mcg/g.
Kadar anggur hijau berbiji yang dikupas 0,044 lebih besar dibandingkan kadar
anggur hijau berbiji tanpa dikupas.
4.1.4.2 Kadar besi pada anggur tanpa biji secara destruksi basah
Dari lampiran 3 dapat dilihat bahwa kadar besi anggur merah tanpa biji
tanpa dikupas yaitu 2,689 ±0,015 mcg/g dan kadar besi anggur merah tanpa biji
yang dikupas yaitu 3,323 ± 0,02 mcg/g. Dari kedua kadar besi diatas disimpulkan
bahwa kadar besi anggur merah tanpa biji yang dikupas 0,634 lebih besar
dibandingkan dengan kadar besi anggur merah tanpa biji dan tanpa dikupas.
Dari lampiran 5, kadar anggur hijau tanpa biji tanpa dikupas yaitu 2,388 ±
mcg/g. Kadar anggur hijau tanpa biji yang dikupas 0,23 lebih besar dibandingkan
kadar anggur hijau tanpa biji tanpa dikupas.
Dari data diatas, kadar anggur tanpa biji dan yang dikupas lebih besar
dibandingkan kadar anggur berbiji dan tanpa dikupas karena pada kulit dan biji
buah anggur sangat sedikit terdapat besi.
4.1.4.3 Kadar besi pada anggur berbiji secara destruksi kering
Dari lampiran 4 dapat dilihat bahwa kadar besi anggur merah berbiji tanpa
dikupas yaitu 2,277 ± 0,069 mcg/g dan kadar besi anggur merah berbiji yang
dikupas yaitu 1,883 ± 0,078 mcg/g. Dari kedua kadar besi diatas disimpulkan
bahwa kadar besi anggur merah berbiji yang dikupas 0,394 lebih besar
dibandingkan dengan kadar besi anggur merah berbiji yang dikupas.
Dari lampiran 6, kadar anggur hijau berbiji tanpa dikupas yaitu 2,279 ±
0,043 mcg/g dan kadar besi anggur hijau berbiji yang dikupas yaitu 1,883 ± 0,078
mcg/g. Kadar anggur hijau berbiji yang dikupas 0,396 lebih besar dibandingkan
kadar anggur hijau berbiji tanpa dikupas.
4.1.4.4 Kadar besi pada anggur tanpa biji secara destruksi kering
Dari lampiran 4 dapat dilihat bahwa kadar besi anggur merah tanpa biji
tanpa dikupas yaitu 2,740 ± 0,025 mcg/g dan kadar besi anggur merah tanpa biji
yang dikupas yaitu 1,779 ± 0,019 mcg/g. Dari kedua kadar besi diatas disimpulkan
bahwa kadar besi anggur merah tanpa biji yang dikupas 0,961 lebih besar
dibandingkan dengan kadar besi anggur merah tanpa biji dan tanpa dikupas.
Dari lampiran 6, kadar anggur hijau tanpa biji tanpa dikupas yaitu 2,348 ±
mcg/g. Kadar anggur hijau tanpa biji yang dikupas 0,156 lebih besar dibandingkan
kadar anggur hijau tanpa biji tanpa dikupas.
Dari data diatas, kadar anggur tanpa biji dan yang dikupas lebih besar
dibandingkan kadar anggur berbiji dan tanpa dikupas karena pada kulit dan biji
buah anggur sangat sedikit terdapat besi.
4.1.4.5 Kadar besi anggur merah hasil destruksi basah dibandingkan dengan destruksi kering
a. Kadar besi anggur merah berbiji tanpa dikupas hasil destruksi basah (2,770
mcg/g) 0,493 lebih besar dibandingkan kadar besi anggur merah berbiji
tanpa dikupas hasil destruksi kering (2,277 mcg/g)
b. Kadar besi anggur merah berbiji yang dikupas hasil destruksi basah (2,619
mcg/g) 0,736 lebih besar dibandingkan kadar besi anggur merah berbiji
yang dikupas hasil destruksi kering (1,883 mcg/g)
c. Kadar besi anggur merah tanpa biji tanpa dikupas hasil destruksi basah
(2,689 mcg/g) 0,051 lebih kecil dibandingkan kadar besi anggur merah
tanpa biji dan tanpa dikupas hasil destruksi kering (2,740 mcg/g)
d. Kadar besi anggur merah tanpa biji yang dikupas hasil destruksi basah
(3,323 mcg/g) 1,544 lebih besar dibandingkan kadar besi anggur merah
berbiji tanpa dikupas hasil destruksi kering (1,779 mcg/g).
Karena pada proses destruksi kering, keseluruhan serat, biji dan kulit buah hancur
menjadi abu dan besi terpisah membentuk oksidanya Fe2O3 dan terlarut seluruhnya
dengan HNO3 5N. Sedangkan pada proses destruksi basah, serat tidak larut dalam
4.1.4.6 Kadar besi anggur hijau hasil destruksi basah dibandingkan dengan destruksi kering
a. Kadar besi anggur hijau berbiji tanpa dikupas hasil destruksi basah (2,574
mcg/g) 0,295 lebih besar dibandingkan kadar besi anggur hijau berbiji tanpa
dikupas hasil destruksi kering (2,279 mcg/g)
b. Kadar besi anggur hijau berbiji yang dikupas hasil destruksi basah (2,619
mcg/g) 0,115 lebih besar dibandingkan kadar besi anggur hijau berbiji yang
dikupas hasil destruksi kering (2,504 mcg/g)
c. Kadar besi anggur hijau tanpa biji tanpa dikupas hasil destruksi basah
(2,388 mcg/g) 0,04 lebih besar dibandingkan kadar besi hijau merah tanpa
biji dan tanpa dikupas hasil destruksi kering (2,348 mcg/g)
d. Kadar besi anggur hijau tanpa biji yang dikupas hasil destruksi basah
(2,420 mcg/g) 0,059 lebih besar dibandingkan kadar besi anggur hijau
berbiji tanpa dikupas hasil destruksi kering (2,361 mcg/g).
Seharusnya kadar besi hasil destruksi basah lebih kecil dibandingkan kadar besi
hasil destruksi kering karena serat tidak larut dalam basa sehingga banyak besi yang
BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
a. Dari hasil penelitian yang telah dilakukan diperoleh kadar zat besi pada
buah anggur merah dan buah anggur hijau berbiji tanpa dikupas yang
terlebih dahulu dilakukan destruksi basah, masing – masing adalah 2,770 ±
0,08 mcg/g dan 2,574 ± 0,05 mcg/g ; pada buah anggur merah dan buah
anggur hijau berbiji yang dikupas, masing – masing adalah 2,619 ± 0,018
mcg/g dan 2,618 ± 0,018 mcg/g ; pada buah anggur merah dan buah anggur
hijau tanpa biji dan tanpa dikupas, masing–masing adalah 2,689 ±0,015
mcg/g dan 2,388 ± 0,05 mcg/g ; pada buah anggur merah dan buah anggur
hijau tanpa biji yang dikupas, masing -masing adalah 3,323 ± 0,02 mcg/g
dan 2,420 ± 0,02 mcg/g.
b. Kadar zat besi pada buah anggur merah dan buah anggur hijau berbiji tanpa
dikupas yang dilakukan secara destruksi kering, masing – masing adalah
2,277 ± 0,069 mcg/g dan 2,279 ± 0,043 mcg/g ; pada buah anggur merah
dan buah anggur hijau berbiji yang dikupas, masing – masing adalah 1,883
± 0,078 mcg/g dan 2,504 ± 0,014 mcg/g ; pada buah anggur merah dan buah
anggur hijau tanpa biji dan tanpa dikupas yang dilakukan secara destruksi
kering, masing – masing adalah 2,740 ± 0,025 mcg/g dan 2,348 ± 0,008
mcg/g ; pada buah anggur merah dan buah anggur hijau tanpa biji yang
dikupas, masing–masing adalah 1,779 ± 0,019 mcg/g dan 2,361 ± 0,026
5.2Saran
Disarankan kepada peneliti selanjutnya agar dapat meneliti kadar besi pada
DAFTAR PUSTAKA
Anonim. (2009). Anggur.
Anonim. (2010). Besi
Almatsier, Sunita. 2003. Prinsip Dasar Ilmu Gizi. PT. Gramedia Pustaka Utama. Jakarta
Apriantono. (1989). Petunjuk Laboratorium: Analisis Pangan. Depdikbud, Direktorat Jendral Pendidikan Tinggi Pusat Antar Universitas Pangan dan Gizi. IPB. Hal. 16-19.
Ditjen POM. (1979). Farmakope Indonesia. Edisi ke III. Jakarta: Departemen Kesehatan RI. Hal. 643, 651.
Ditjen POM. (1995). Farmakope Indonesia. Edisi ke IV. Jakarta: Departemen Kesehatan RI. Hal. 1126.
Hartono. (2008). SPSS 16.0 Analisa Data Statistika dan Penelitian. Edisi Kedua.
Cetakan I. Yogyakarta: Pustaka Pelajar. Hal. 146-153, 161-195.
Harmita. (2004). Petunjuk Pelaksanaan Validasi, Metode dan Cara
Perhitungannya. Majalah Ilmu Kefarmasian. Vol. I No.3. Hal.117, 119,
121, 130-131.
Khopkar, S.M. (1990). Konsep Dasar Kimia Analitik. Penerjemah: A. Saptorahardjo. Jakarta: Universitas Indonesia Press. Hal. 275.
Pudjiadi, S. (2000). Ilmu Gizi Klinis pada Anak. Edisi Keempat. Jakarta: Gaya Baru. Hal. 254.
Rohman, A. (2007). Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Hal. 22, 31, 298, 463.
Sudjana. (2005). Metode Statistika. Edisi Keenam. Bandung: Penerbit Tarsito. Hal. 168.
Lampiran 1. Perhitungan Persamaan Regresi Besi
Maka persamaan regresinya adalah : Y= 0,1778X – 0,0018
Lampiran 2. Perhitungan Batas Deteksi dan Batas Kuantitasi
Simpangan Baku (SB) =
Lampiran 3. Data Berat Sampel, Absorbansi dan Kadar Besi pada Anggur Merah Dengan Destruksi Basah
sampel Berat anggur
Lampiran 4. Data Berat Sampel, Absorbansi dan Kadar Besi pada Anggur Merah Dengan Cara Destruksi Kering
sampel Berat anggur
Lampiran 5. Data Berat Sampel, Absorbansi dan Kadar Besi pada Anggur Hijau Dengan Cara Destruksi Basah
sampel Berat anggur
Lampiran 6. Data Berat Sampel, Absorbansi dan Kadar Besi pada Anggur Hijau Dengan Cara Destruksi kering
sampel Berat
anggur (gr) absorbansi
Kadar sebenarnya terletak antara :
µ = x ±(t xSD/ n )
= 2,770 ± (2,5706 x 0,013 / 6 )
Kadar sebenarnya terletak antara :
µ = x ±(t xSD/ n )
= 2,277± (2,5706 x 0,011 / 6 )
Kadar sebenarnya terletak antara :
µ = x ±(t xSD/ n )
= 2,574 ± (2,5706 x 0,008 / 6 )
Lampiran 10. Perhitungan Kadar Besi sebenarnya dalam Buah Anggur Hijau
Kadar sebenarnya terletak antara :
µ = x ±(t xSD/ n )
= 2,279 ± (2,5706 x 0,007 / 6 )
Lampiran 11. Data Uji Perolehan Kembali Anggur Merah Tanpa Biji dan Tanpa
Kadar Kadar Rata-rata
Anggur merah tanpa biji dan tanpa dikupas secara
destruksi kering
Perhitungan Uji Perolehan Kembali
% recovery = x100%
Lampiran 12. Data Uji Perolehan Kembali Anggur Merah Berbiji yang Dikupas
Kadar Kadar Rata-rata
Anggur hijau tanpa biji dan tanpa dikupas secara
destruksi basah
Perhitungan Uji Perolehan Kembali
% recovery = x100%
Lampiran 13. Contoh Perhitungan Kadar Besi pada Buah Anggur Merah Berbiji Tanpa Dikupas secara Destruksi Basah
Berat buah anggur merah yang ditimbang :
B1 = 50,263 gram
X = konsentrasi (mcg/ml)
Lanjutan lampiran 13...
Cara ini dilakukan terhadap :
1. anggur merah berbiji yang dikupas
2. anggur merah tanpa biji dan tanpa dikupas
3. anggur merah tanpa biji yang dikupas
4. anggur hijau berbiji tanpa dikupas
5. anggur hijau berbiji yang dikupas
6. anggur hijau tanpa biji yang dikupas
Lampiran 14. Contoh Perhitungan Kadar Besi pada Buah Anggur Merah Berbiji Tanpa Dikupas secara Destruksi Kering
Berat buah anggur merah yang ditimbang :
B1 = 50,124 gram
X = konsentrasi (mcg/ml)
Lanjutan lampiran 14...
Cara ini dilakukan terhadap :
1. anggur merah berbiji yang dikupas
2. anggur merah tanpa biji dan tanpa dikupas
3. anggur merah tanpa biji yang dikupas
4. anggur hijau berbiji tanpa dikupas
5. anggur hijau berbiji yang dikupas
6. anggur hijau tanpa biji yang dikupas
Lampiran 15. Larutan sampel setelah penyaringan