PENGARUH KONSENTRASI H2SO4 DAN HCl PADA ZEOLIT
ALAM TERAKTIVASI SERTA pH LARUTAN TERHADAP
ADSORPSI LOGAM KOBAL (Co) DAN NIKEL (Ni)
DALAM LARUTAN STANDAR DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
RIVAN
050802035
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH KONSENTRASI H2SO4 DAN HCl
PADA ZEOLIT ALAM TERAKTIVASI SERTA pH LARUTAN TERHADAP ADSORBSI LOGAM KOBAL (Co) DAN NIKEL (Ni) DALAM LARUTAN STANDAR DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM.
Kategori : SKRIPSI Nama : RIVAN Nomor Induk Mahasiswa : 050802035
Program Studi : SARJANA (S1) KIMIA Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Desember 2011
Komisi Pembimbing :
Pembimbing 2 Pembimbing 1
Prof.Dr.Harry Agusnar.M.Sc.,M.Phill Prof.Dr.Zul Alfian.M.Sc NIP. 195308171983031002 NIP.195504051983031002
Diketahui/Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
PENGARUH KONSENTRASI H2SO4 DAN HCl PADA ZEOLIT
ALAM TERAKTIVASI SERTA pH LARUTAN TERHADAP
ADSORPSI LOGAM KOBAL (Co) DAN NIKEL (Ni)
DALAM LARUTAN STANDAR DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
RIVAN
050802035
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERNYATAAN
PENGARUH KONSENTRASI H
2SO
4DAN HCl PADA ZEOLIT
ALAM TERAKTIVASI SERTA pH LARUTAN TERHADAP
ADSORBSI LOGAM KOBAL (Co) DAN NIKEL (Ni)
DALAM LARUTAN STANDAR DENGAN
METODE SPEKTROFOTOMETRI
SERAPAN ATOM
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, Desember 2011
PENGHARGAAN
Bismillahirrahmanirrahim.
Puji dan syukur penulis panjatkan kepada Sang Pencipta Allah SWT yang memberikan rahmat dan karunianya kepada penulis sehingga dapat menyelesaikan penelitian dan skripsi ini yang berjudul: “PENGARUH KONSENTRASI H2SO4 DAN
HCl PADA ZEOLIT ALAM TERAKTIVASI SERTA pH LARUTAN TERHADAP ADSORBSI LOGAM KOBAL (Co) DAN NIKEL (Ni) DALAM LARUTAN STANDAR DENGAN METODE SPEKTROFOTOMETRI SERAPAN ATOM”
Skripsi ini merupakan tugas akhir untuk melengkapi salah satu syarat untuk memperoleh gelar sarjana Kimia pada Fakultas MIPA-USU Medan.
Penulis mengucapkan terima kasih kepada orang tua saya yang sangat saya sayangi, ayahanda Himsar dan ibunda Mery Desna yang telah memberikan dukungan moral dan material, serta kepada adik-adik saya tersayang: Ruri, Restu, dan Rian atas semangat dan doa yang selalu diberikan kepada saya. Kepada (alm) Kakek dan Nenek, serta semua keluarga yang selalu mendoakan dan memotivasi penulis.
Dengan segala kerendahan hati penulis juga mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Bapak Prof. Dr. Zul Alfian. M.Sc selaku dosen pembimbing I dan Bapak Prof. Dr. Harry Agusnar, M.Sc., M.Phill selaku dosen pembimbing II yang telah dengan sabar meluangkan waktu, tenaga, dan pikirannya serta saran dan petunjuk kepada penulis dalam melakukan penelitian dan penyusunan skripsi ini.
2. Ibu Dr. Marpongahtun, M.Sc selaku dosen pembimbing akademik yang telah memberikan bimbingannya kepada penulis selama mengikuti kegiatan akademik.
3. Bapak dan Ibu staf pengajar Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara terutama Jurusan Kimia yang telah membantu penulis selama mengikuti perkuliahan.
4. Ibu Dr.Rumondang Bulan, MS dan Bapak Dr. Albert Pasaribu, M.Sc selaku ketua dan sekretaris Departemen Kimia yang telah memberikan pengarahan dan mensahkan skripsi ini.
5. Seluruh staf Laboratorium Kimia Dasar LIDA USU : Mas Gun, Kak Ayu dan juga rekan-rekan asisten laboratorium Kimia Dasar LIDA USU : Sony, Novrida, Ando, Via, Hendi, Yani, Widya, Afrima, Fatma, Eko, Reni, Deasy, Ani, Andreas, Novi, Arifin, Desy, Salmi, Nurul, Ilman, Irwanto, Dwi, Icha, Indah, Rina, Ayu.
6. Sahabat-sahabatku : Dwi, Rina, Mega, Albinur, Misbah, Rafles, Mail, Surnog, Verroez, Bayu, Egy.
7. Teman-teman stambuk 2005 dan adik-adik stambuk 2006, 2007, 2008, 2009, dan 2010 yang telah berbagi ilmu yang bermanfaat.
8. Rekan-rekan staf pengajar SSC Medan, terutama Departemen Kimia : Bang Darmas, Kak Frida, Kak Mellany, Pahotton, Stephanus, Arman, dan Ali.
Penulis hanya dapat mengucapkan terima kasih, semoga Allah SWT membalas segala kebaikan yang telah diberikan kepada penulis. Penulis berharap Allah melimpahkan Rahmat dan Berkah-Nya kepada kita semua, amin ya Rabbalalamin.
Medan, Desember 2011 Penulis
ABSTRAK
Telah dilakukan penelitian tentang pengaruh variasi konsentrasi H2SO4 dan HCl
terhadap daya serap zeolit alam teraktivasi pada logam kobal (Co) dan nikel (Ni) dalam larutan standar dengan metode Spektrofotometri Serapan Atom. Pada proses aktivasi zeolit alam dikaji pengaruh konsentrasi H2SO4 dan HCl yaitu 1,0; 2,0; 3,0;
4,0; dan 5,0 N untuk masing – masing asam. Ke dalam larutan standar kobal (Co) dan nikel (Ni) ditambahkan 5 gram zeolit alam yang telah diaktivasi dengan H2SO4 dan
zeolit alam yang telah diaktivasi dengan HCl, pada pH larutan 4; 5; 6; dan 7, diaduk selama 6 jam, disaring dan diukur konsentrasi logam kobal (Co) dan nikel (Ni) dengan Spektrofotometer Serapan Atom melalui kurva kalibrasi. Hasil penelitian menunjukkan bahwa zeolit alam dengan konsentrasi aktivasi H2SO4 2 N dengan pH
larutan 6 yang paling baik dengan menyerap logam kobal (Co) sebesar 95,02% dan logam nikel (Ni) sebesar 96,18%. Zeolit alam dengan konsentrasi aktivasi H2SO4 2 N
THE CONCENTRATE EFFECT’S H2SO4 AND HCl OF NATURAL ZEOLITE
MOST ACTIVATION WELL AS pH SOLUTION ON ADSORPTION OF THE METAL COBALT (Co) AND NICKEL (Ni) IN STANDARD
SOLUTION USING ATOMIC ABSORPTION SPECTROPHOTOMETRIC METHOD
ABSTRACT
The influence of variations in concentrate H2SO4 and HCl of natural zeolite most
activated on adsorbtion of the metal cobalt (Co) and nickel (Ni) in the standard solution by Atomic Absorption Spectrophotometric method has been studied. In the activation process of natural zeolites assessed by concentrate effect’s of H2SO4 and
HCl which is 1.0, 2.0, 3.0, 4.0, and 5.0 N for each one. Into a standard solution of cobalt (Co) and nickel (Ni) was added 5 grams of natural zeolites that have been activated with H2SO4 and natural zeolites that have been activated with HCl, at pH 4, 5, 6, and 7, stirred for 6 hours, filtered and measured the concentration of cobalt metal (Co) and nickel (Ni) by Atomic Absorption Spectrophotometer with a calibration curve. The results showed that activation concentrate H2SO4 2 N with pH 6 which is
best by adsorbing metallic cobalt (Co) of 95.02% and the metals nickel (Ni) of 96.18%. Natural zeolite with a concentration H2SO4 2 N activation can absorb metal
DAFTAR ISI 2.2.3 Pengaktifan mineral zeolit 10 2.2.4 Pengaktifan dengan pemanasan 11 2.2.5 Pengaktifan dengan pengasaman 11
2.3 Adsorbsi 13
2.4 Kobal (Co) 14
2.4.1 Penggunaan Co dalam bidang industri 14
2.4.2 Efek toksik 14
2.5 Nikel (Ni) 14
2.5.1 Efek Toksik 15
2.6 Spektrofotometri Serapan Atom 15 2.6.1 Prinsip Dasar Spektrofotometri Serapan Atom 15 2.6.2 Instrumentasi Spektrofotometri Serapan Atom 16
Bab 3 Metodologi Penelitian 18
3.1 Alat dan Bahan 18
3.1.1 Alat-alat 18
3.1.2 Bahan-bahan 18
3.2 Prosedur Penelitian 19 3.2.1 Pembuatan Pereaksi H2SO4 19
3.2.4 Aktivasi Zeolit Alam dengan H2SO4 21
3.2.5 Aktivasi Zeolit Alam dengan HCl 21 3.2.6 Pembuatan Larutan Standar Kobal (Co) 100 mg/L 21 3.2.7 Pembuatan Larutan Standar Kobal (Co) 10 mg/L 21 3.2.8 Pembuatan Larutan Seri Standar Kobal (Co) 0,10; 0,50;
1,00; 2,00; dan 3,00 mg/L 22 3.2.9 Pembuatan Larutan Standar Nikel (Ni) 100 mg/L 22 3.2.10 Pembuatan Larutan Standar Nikel (Ni) 10 mg/L 22 3.2.11 Pembuatan Larutan Seri Standar Nikel (Ni) 0,10; 0,50;
1,00; 2,00; dan 3,00 mg/L 22 3.2.12 Pembuatan Kurva Kalibrasi Logam Kobal 22 3.2.13 Pembuatan Kurva Kalibrasi Logam Nikel 23 3.2.14 Penyerapan Larutan Standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi 23 3.2.1.4.1 Penyerapan Larutan Standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan
variasi konsentrasi H2SO4 23
3.2.14.2 Penyerapan Larutan Standar Kobal dan Nikel dengan menggunakan zeolit alam yang telah diaktivasi dengan
variasi konsentrasi HCl 23 3.2.14.3 Penyerapan Larutan Standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan
H2SO4 2 N dengan variasi pH 24
3.2.14.4 Penyerapan Larutan Standar Kobal dan Nikel dengan menggunakan zeolit alam yang telah diaktivasi dengan
HCl 4 N dengan variasi pH 24
3.3 Bagan Penelitian 25
3.3.1 Aktivasi Zeolit Alam dengan H2SO4 25
3.3.2 Aktivasi Zeolit Alam dengan HCl 26 3.3.3 Penyerapan larutan standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan
variasi konsentrasi H2SO4 27
3.3.4 Penyerapan larutan standar Kobal dan Nikel dengan menggunakan zeolit alam yang telah diaktivasi dengan
variasi konsentrasi HCl 28 3.3.5 Penyerapan larutan standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan
H2SO4 2 N dengan variasi pH 29
3.3.6 Penyerapan larutan standar Kobal dan Nikel dengan menggunakan zeolit alam yang telah diaktivasi dengan
HCl N dengan variasi pH 30 3.3.7 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi
Nikel 31
3.3.8 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi
Kobal 32
Bab 4 Hasil dan Pembahasan 33
4.1 Hasil Penelitian 33
4.1.2 Pengolahan Data Logam Kobal (Co) 34 4.1.2.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 34 4.1.2.2 Koefisien Korelasi 35 4.1.2.3 Persentasi (%) Penurunan Konsentrasi Logam
Kobal (Co) 36
4.1.3 Logam Nikel 39
4.1.4 Pengolahan Data Logam Nikel (Ni) 40 4.1.4.1 Penurunan Persamaan Garis Regresi dengan
Metode Least Square 40 4.1.4.2 Koefisien Korelasi 42 4.1.4.3 Persentasi (%) Penurunan Konsentrasi Logam
Nikel (Ni) 42
4.2 Pembahasan 45
Bab 5 Kesimpulan dan Saran 48
5.1 Kesimpulan 48
5.2 Saran 48
DAFTAR TABEL
Halaman Tabel 2.1 Nama mineral zeolit dan rumus kimianya 9 Tabel 4.1 Kondisi alat SSA merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Kobal (Co) 33 Tabel 4.2 Data absorbansi larutan standar Kobal (Co) 33 Tabel 4.3 Penentuan persamaan garis regresi untuk penentuan konsentrasi
logam Kobal (Co) berdasarkan pengukuran absorbansi larutan
standar Kobal (Co) 34
Tabel 4.4 Data persentase (%) penurunan konsentrasi logam kobal (Co) dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan variasi konsentrasi H2SO4 37
Tabel 4.5 Data persentase (%) penurunan konsentrasi logam kobal (Co) dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan variasi konsentrasi HCl 37 Tabel 4.6 Data persentase (%) penurunan konsentrasi logam kobal (Co)
dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan konsentrasi H2SO4 2 N dengan variasi pH larutan 38
Tabel 4.7 Data persentase (%) penurunan konsentrasi logam kobal (Co) dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan konsentrasi HCl 4 N dengan variasi pH larutan 38 Tabel 4.8 Kondisi alat SSA merek Shimadzu tipe AA-6300 pada
pengukuran konsentrasi logam Nikel (Ni) 39 Tabel 4.9 Data Absorbansi larutan standar Nikel (Ni) 39 Tabel 4.10 Penentuan persamaan garis regresi untuk penentuan konsentrasi
logam Nikel (Ni) berdasarkan pengukuran absorbansi larutan
standar Nikel (Ni) 40
Tabel 4.11 Data persentase (%) penurunan konsentrasi logam Nikel (Ni) dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan variasi konsentrasi H2SO4 43
Tabel 4.12 Data persentase (%) penurunan konsentrasi logam Nikel (Ni) dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan variasi konsentrasi HCl 43 Tabel 4.13 Data persentase (%) penurunan konsentrasi logam Nikel (Ni)
dalam larutan standar setelah penambahan zeolit alam teaktivasi dengan konsentrasi H2SO4 2 N dengan variasi pH larutan 44
DAFTAR GAMBAR
ABSTRAK
Telah dilakukan penelitian tentang pengaruh variasi konsentrasi H2SO4 dan HCl
terhadap daya serap zeolit alam teraktivasi pada logam kobal (Co) dan nikel (Ni) dalam larutan standar dengan metode Spektrofotometri Serapan Atom. Pada proses aktivasi zeolit alam dikaji pengaruh konsentrasi H2SO4 dan HCl yaitu 1,0; 2,0; 3,0;
4,0; dan 5,0 N untuk masing – masing asam. Ke dalam larutan standar kobal (Co) dan nikel (Ni) ditambahkan 5 gram zeolit alam yang telah diaktivasi dengan H2SO4 dan
zeolit alam yang telah diaktivasi dengan HCl, pada pH larutan 4; 5; 6; dan 7, diaduk selama 6 jam, disaring dan diukur konsentrasi logam kobal (Co) dan nikel (Ni) dengan Spektrofotometer Serapan Atom melalui kurva kalibrasi. Hasil penelitian menunjukkan bahwa zeolit alam dengan konsentrasi aktivasi H2SO4 2 N dengan pH
larutan 6 yang paling baik dengan menyerap logam kobal (Co) sebesar 95,02% dan logam nikel (Ni) sebesar 96,18%. Zeolit alam dengan konsentrasi aktivasi H2SO4 2 N
THE CONCENTRATE EFFECT’S H2SO4 AND HCl OF NATURAL ZEOLITE
MOST ACTIVATION WELL AS pH SOLUTION ON ADSORPTION OF THE METAL COBALT (Co) AND NICKEL (Ni) IN STANDARD
SOLUTION USING ATOMIC ABSORPTION SPECTROPHOTOMETRIC METHOD
ABSTRACT
The influence of variations in concentrate H2SO4 and HCl of natural zeolite most
activated on adsorbtion of the metal cobalt (Co) and nickel (Ni) in the standard solution by Atomic Absorption Spectrophotometric method has been studied. In the activation process of natural zeolites assessed by concentrate effect’s of H2SO4 and
HCl which is 1.0, 2.0, 3.0, 4.0, and 5.0 N for each one. Into a standard solution of cobalt (Co) and nickel (Ni) was added 5 grams of natural zeolites that have been activated with H2SO4 and natural zeolites that have been activated with HCl, at pH 4, 5, 6, and 7, stirred for 6 hours, filtered and measured the concentration of cobalt metal (Co) and nickel (Ni) by Atomic Absorption Spectrophotometer with a calibration curve. The results showed that activation concentrate H2SO4 2 N with pH 6 which is
best by adsorbing metallic cobalt (Co) of 95.02% and the metals nickel (Ni) of 96.18%. Natural zeolite with a concentration H2SO4 2 N activation can absorb metal
BAB 1
PENDAHULUAN
1.1Latar Belakang
Zeolit merupakan senyawa alumino-silikat hidrat terhidrasi dengan unsur
utama yang terdiri dari kation alkali dan alkali tanah terutama Ca, K dan Na, dengan
rumus umum (LaAlbSic O2.nH2O) dimana L adalah logam. Sifat umum dari zeolit
adalah kristal yang agak lunak dengan warna putih coklat atau kebiru-biruan.
Senyawaan kristalnya berwujud dalam sruktur tiga dimensi yang tak terbatas dan
memiliki rongga-rongga yang saling berhubungan membentuk saluran ke segala arah
dengan ukuran saluran tergantung dari garis tengah logam alkali ataupun alkali tanah
yang terdapat pada srukturnya. Dimana rongga-rongga tersebut akan terisi oleh air
yang disebut air kristal.
Aktivasi asam pada zeolit menyebabkan terjadinya dekationisasi yang
menyebabkan bertambahnya luas permukaan zeolit karena berkurangnya pengotor
yang menutupi pori-pori zeolit. Luas permukaan yang bertambah diharapkan
meningkatkan kemampuan zeolit dalam proses penyerapan (Weitkamp, 1999).
Situs dari rangka zeolit perlu diubah menjadi situs yang mudah
disubstitusi oleh logam yaitu dengan jalan memodifikasi zeolit menjadi zeolit-H
(Pearson, 1963). Peningkatan daya guna atau optimalisasi zeolit sebagai adsorben
(penyerap) dapat dilakukan melalui aktivasi secara fisis maupun kimia (Priatna et al.,
1985). Proses aktivasi secara fisis dilakukan dengan pemanasan yang bertujuan
untuk menguapkan air yang terperangkap dalam pori-pori kristal zeolit sehingga
jumlah pori dan luas permukaan spesifiknya bertambah. Aktivasi secara kimia dapat
dilakukan dengan menggunakan larutan HCl atau H2SO4 yang bertujuan untuk
membersihkan permukaan pori, membuang senyawa pengganggu dan menata kembali
Banyak penelitian yang telah dilakukan tentang zeolit alam yang digunakan
sebagai adsorben logam berat. Pengaktivan merupakan salah satu faktor yang
mempengaruhi kemampuan zeolit alam dalam menyerap logam berat. Asam yang
sering digunakan sebagai aktivator adalah HCl. Penambahan HCl bertujuan untuk
mengeluarkan logam-logam Fe, Mg, dan zat lain yang terikat di sekitar kristal
zeolit. Reaksi yang terjadi adalah sebagai berikut:
Fe2+ + 2HCl → FeCl2 + H2
Mg2+ + 2HCl → MgCl2 + H2
M3+ + 2HCl → 2MCl3 + H2
Proses selanjutnya adalah penyaringan dan pencucian. Proses pencucian dengan
HF harus menggunakan wadah dan pengaduk yang terbuat dari bahan plastik.
Hal ini bertujuan untuk mencegah terjadinya korosi, akibat penggunaan larutan
yang bersifat asam. Kemudian zeolit yang bersifat asam dicuci dengan aquades
sampai bebas asam (pH filtrat = pH aquades). Pencucian dengan aquades
membutuhkan waktu sekitar 3 hari. Zeolit mempunyai sifat asam, karena
mempunyai situs asam lewis. Situs asam Lewis dapat diperoleh dari
dehidroksilasi gugus hidroksil dengan perlakuan panas (T>750K) (Oudejans,
1984).
1.2Permasalahan
1. Pada konsentrasi H2SO4 dan HCl berapakah zeolit alam teraktivasi dapat
mengadsorbsi logam Kobal (Co) dan Nikel (Ni) pada larutan standar secara
optimum.
2. Apakah perbedaan asam sebagai aktivator yang digunakan mempengaruhi
kemampuan zeolit alam teraktivasi dalam mengadsorpsi kadar logam pada
larutan standar.
3. Apakah perbedaan pH dari larutan akan mempengaruhi kemampuan zeolit
alam teraktivasi dalam mengadsorpsi kadar logam pada larutan standar.
Penelitian ini dibatasi pada penentuan kadar logam Kobal (Co) dan Nikel (Ni) pada
larutan standar dengan menggunakan instrumen SSA tipe nyala merek Shimadzu seri
AA-6300 sebelum dan sesudah penambahan zeolit alam teraktivasi dengan pH
larutan tertentu.
1.4Tujuan Penelitian
1. Penelitian ini bertujuan untuk menentukan konsentrasi H2SO4 dan HCl yang
optimum dan persentase (%) penurunan kadar logam Kobal (Co) dan Nikel
(Ni) pada larutan standar setelah penambahan zeolit alam teraktivasi.
2. Penelitian ini bertujuan untuk menentukan pH larutan yang optimum dalam
penyerapan kadar logam Kobal (Co) dan Nikel (Ni) oleh zeolit alam yang
telah diaktivasi dengan HCl dan H2SO4.
1.5Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat memberikan informasi kepada
masyarakat mengenai aktivasi zeolit dengan menggunakan H2SO4 dan HCl dan
penggunaannya sebagai adsorben yang digunakan untuk menurunkan kadar ion
Nikel dan Kobalt dalam larutan standar. Serta pengaruh pH larutan terhadap
kemampuan zeolit alam dalam mengadsorpsi ion logam Nikel dan Kobalt dalam
larutan standar.
1.6Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Dasar LIDA Universitas
Sumatera Utara dan analisis Spektrofotometri Serapan Atom dilakukan di
Laboratorium Kimia Analitik Fakultas Matematika dan Ilmu Pengetahuan Alam
(FMIPA) Universitas Sumatera Utara.
1.7Metodologi Penelitian
1. Penelitian ini merupakan eksperimen laboratorium.
2. Sampel yang digunakan adalah larutan standar.
3. Aktivator yang digunakan adalah H2SO4 dam HCl
4. Metode pengaktivan yang digunakan adalah pemanasan dan pengasaman.
6. Konsentrasi HCl yang digunakan adalah 1; 2; 3; 4; dan 5 N.
7. pH larutan standar pada saat penyerapan adalah pH 7; 6; 5; dan 4.
8. Lamanya penyerapan larutan standar oleh zeolit alam teraktivasi selama 6 jam.
9. Zeolit alam yang digunakan adalah zeolit alam Sarulla dari kabupaten
Tapanuli Utara.
10.Penentuan kadar ion Nikel dan Kobalt dilakukan dengan metode Spektrofotometri Serapan Atom pada λspesifik 232 nm untuk Nikel dan 240 nm
untuk Kobalt.
11.Kadar ion Nikel dan Kobalt dalam larutan standar dihitung dengan
menggunakan data analisis Spektrofotometri Serapan Atom dan dengan
BAB 2
TINJAUAN PUSTAKA
2.1. Logam
Dalam kehidupan sehari-hari, kita tidak terpisah dari benda-benda yang bersifat
logam. Benda ini kita gunakan sebagai alat perlengkapan rumah tangga seperti
sendok, garpu, pisau dan lain-lain, sampai pada tingkat perhiasan mewah yang tidak
dapat dimiliki oleh semua orang seperti emas, perak dan lain-lain. Secara gamblang,
dalam konotasi keseharian kita beranggapan bahwa logam diidentikkan dengan besi.
Padat, keras, berat dan sulit dibentuk. (Palar, 2008).
Logam berat ini dapat menimbulkan efek kesehatan bagi manusia tergantung
pada bagian mana logam berat tersebut terikat dalam tubuh. Daya racun yang dimiliki
akan bekerja sebagai penghalang kerja enzim, sehingga proses metabolisme tubuh
terputus. Lebih jauh lagi, logam berat ini akan bertindak sebagai penyebab alergi,
karsinogen bagi manusia. Jalur masuknya adalah melalui kulit, pernapasan dan
pencernaan.
Logam berat jika sudah terserap ke dalam tubuh maka tidak dapat dihancurkan
tetapi akan tetap tinggal di dalamnya hingga nantinya dibuang melalui proses ekskresi.
Hal serupa juga terjadi apabila suatu lingkungan terutama di perairan telah
terkontaminasi (tercemar) logam berat maka proses pembersihannya akan sulit sekali
dilakukan. Kontaminasi logam berat ini dapat berasal dari faktor alam seperti kegiatan
gunung berapi dan kebakaran hutan atau faktor manusia seperti pembakaran minyak
bumi, pertambangan, peleburan, proses industri, kegiatan pertanian, peternakan dan
kehutanan, serta limbah buangan dan termasuk sampah rumah tangga.
Di dalam air biasanya logam berikatan dalam senyawa kimia atau dalam
bentuk logam ion, bergantung pada kompartemen tempat logam tersebut berada.
Tingkat kandungan logam pada setiap kompartemen sangat bervariasi, bergantung
pada lokasi, jenis kompartemen dan tingkat pencemarannya. Biasanya tingkat
konsentrasi logam berat dalam air dibedakan menurut tingkat pencemarannya, yaitu
polusi berat, polusi sedang, dan nonpolusi.
Tujuan utama untuk mengetahui konsentrasi logam dalam lingkungan perairan
adalah :
a. Mengetahui konsentrasi logam yang tinggi dalam hewan air, baik ikan air
laut maupun air tawar, yang dapat digunakan sebagai pedoman untuk
mencegah terjadinya toksisitas kronis maupun akut pada orang yang
memakannya.
b. Mengetahui konsentrasi logam yang tinggi dalam air dan sedimen, yang
dapat digunakan sebagai pedomanuntuk memonitor kualitas air yang
mungkin digunakan sebagai irigasi ataupun air minum, yang akhirnya
berakibat buruk bagi orang yang mengonsumsinya.
Hart dan Lake (1987) mengatakan bahwa ada empat kompartemen yang
terlihat dalam siklus biogeokimiawi logam dalam air, yaitu sebagai berikut :
a. Kompartemen logam yang terlarut adalah ion logam bebas, kompleks, dan
koloidal ikatan senyawanya.
b. Kompartemen partikel abiotik, terdiri dari bahan kimia inorganic dan
organic.
c. Kompartemen partikel biotik, terdiri dri fitoplankton dan bacteria di dalam
laut dangkal dan laut dalam, daerah pantai, serta muara sungai yang
menempel pada tanaman.
d. Kompartemen sedimen di dasar air, merupakan kompartemen terbesar dari
Untuk mengetahui proses perpindahan logam berat yang melibatkan transformasi dan
transport dari kompartemen satu ke lainnya di dalam suatu lingkungan perairan, perlu
mempelajari hal sebagai berikut :
a. Bentuk fisika-kimia dari logam yang terdapat dalam setiap kompartemen.
b. Proses yang menstimuli terjadinya transportasi logam dalam sistem tersebut.
c. Suatu proses perpindahan logam dalam suatu kompartemen ke kompartemen
lainnya.
d. Suatu kejadian logam berat berinteraksi dengan biota air (Darmono, 2001).
2.2 Zeolit
Zeolit merupakan senyawa alumino-silikat hidrat terhidrasi dengan unsur utama yang
terdiri dari kation alkali dan alkali tanah terutama Ca, K dan Na, dengan rumus umum
(LaAlbSic O2.nH2O) dimana L adalah logam. Sifat umum dari zeolit adalah kristal
yang agak lunak dengan warna putih coklat atau kebiru-biruan. Senyawaan kristalnya
berwujud dalam sruktur tiga dimensi yang tak terbatas dan memiliki rongga-rongga
yang saling berhubungan membentuk saluran ke segala arah dengan ukuran saluran
tergantung dari garis tengah logam alkali ataupun alkali tanah yang terdapat pada
srukturnya. Dimana rongga-rongga tersebut akan terisi oleh air yang disebut air
kristal.
Mineral zeolit yang paling umum dijumpai adalah (Na,K)2O, Al2O3. 10 SiO2.
8H2O. Perbandingan antara atom Si dan Al yang bervariasi akan menghasilkan banyak
jenis atau spesies zeolit yang terdapat di alam.
2.2.1Komposisi mineral zeolit
Mineral zeolit merupakan sekelompok mineral yang terdiri dari beberapa jenis
(species) mineral. Secara umum mineral zelolit mempunyai rumus kimia sebagai
berikut : Mx/n(AlO2)x(SiO2)y.H2O
dimana : n = valensi dari kation logam
w = bilangan molekul air per unit cell zeolit
x dan y = bilangan total tetrahedral per unit cell dan perbandingan x /y
Berdasarkan hasil analisa kimia total, kandungan unsur-unsur zeolit
dinyatakan sebagai oksida SiO2, Al2O3, CaO, MgO, Na2O, K2O dan Fe2O3. Akan
tetapi di alam tergantung pada komponen bahan induk dan keadaan lingkungannya,
maka perbandingan Si/Al dapat bervariasi, dan juga unsur Na, Al, Si, sebahagian
dapat disubstitusikan oleh unsur lain.(Dana,D.James,1951)
Parameter kimia yang penting dari zeolit adalah perbandingan Si/Al, yang
menunjukkan persentase Si yang mengisi di dalam tetrahedral, jumlah kation
monovalen dan divalent, serta molekul air yang terdapat didalam saluran kristal.
Perbedaan kandungan atau perbandingan Si/Al akan berpengaruh terhadap ketahanan
zeolit terhadap asam atau pemanasan. Ikatan ion Al-Si-O adalah pembentuk struktur
kristal sedangkan logam alkali adalah kation yang mudah tertukar (“exchangeable
cation”). Jumlah molekul air menunjukkan jumlah pori-pori atau volume ruang
kosong yang terbentuk bila unit sel kristal tersebut dipanaskan.(Sastiano,A.1991)
Hingga kini sudah 40 jenis (species) mineral zeolit yang telah diketahui. Dari
jumlah tersebut, hanya 20 jenis saja yang diketahui terdapat dalam bentuk sedimen,
terutama dalam bentuk piroklastik. Nama dan rumus kimia mineral zeolit yang
Tabel 2.1. Nama mineral zeolit dan rumus kimia nya
NO Nama Mineral Rumus kimia unit sel
1 Analsim Na16(Al16Si16O96).16H2O
2.2.2 Sifat fisik Mineral Zeolit
Seperti halnya mineral kwarsa dan felspar, maka mineral zeolit mempunyai
struktur kristal 3 dimensi tetrahedra silikat (SiO4-4) yang biasa disebut tectosilicate.
Dalam struktur ini sebagian silikon (tidak bermuatan atau netral) kadang-kadang
diganti oleh aluminium bermuatan listrik, sehingga muatan listrik kristal zeolit
tersebut bertambah. Kelebihan muatan ini biasanya diimbangi oleh kation-kation
logam K, Na, dan Ca yang menduduki tempat tersebar dalam struktur zeolit alam yang
bersangkutan. Dalam susunan kristal zeolit terdapat dua jenis molekul air, yaitu
molekul air yang terikat kuat dan molekul air yang bebas. Berbeda dengan struktur
kisi kristal kwarsa yang kuat dan pejal, maka struktur kisi kristal zeolit terbuka dan
mudah terlepas. Volume ruang hampa dalam struktur zeolit cukup besar
kadang-kadang mencapai 50 Angstrom, sedangkan garis tengah ruang hampa tersebut
mineral zeolit yang bersangkutan. Dibawah ini struktur stereotip clinoptilolit yang
menjadi precursor dalam penelitian ini.
Gambar2.1 Kerangka utama zeolit
Volume dan ukuran garis tengah ruang hampa dalam kisi-kisi kristal inilah
yang menjadi dasar penggunaan mineral zeolit sebagai bahan penyaring (molecular
sieving). Molekul zat yang disaring yang ukurannya lebih kecil dari ukuran garis
tengah ruang hampa mineral zeolit dapat melintas, sedangkan yang berukuran lebih
besar akan tertahan atau ditolak. Kapasitas atau daya saring mineral zeolit tergantung
dari volume dan jumlah ruang hampanya. Makin besar jumlah ruang hampa, maka
makin besar pula daya saring zeolit alam yang bersangkutan. Mineral zeolit
mempunyai struktur tiga dimensi tetrahedral (SiO4-4) yang biasa disebut “
tektosilikat”, dimana masing-masing berhubungan dengan ion silicon sebagai
pusatnya, sehingga masing-masing atom oksigen terdapat diantara atom silicon dan
aluminium. Setiap atom terikat oleh dua struktur yang tetrahedral. Struktur yang
hanya terdiri dari silicon dan oksigen ini bersifat netral. Dalam struktur zeolit terdapat
pergantian silicon bervalensi empat dengan aluminium bervalensi tiga. Dalam struktur
ini sebahagian silicon ( tidak bermuatan listrik atau netral ) dapat diganti oleh
aluminium (bermuatan listrik) sehingga muatan listrik zeolit tersebut bertambah.
Kelebihan muatan ini biasanya diimbangi oleh kation logam, seperti K, Na, Ca, yang
menduduki tempat-tempat tersebar dalam struktur Kristal mineral zeolit.
2.2.3 Pengaktifan mineral zeolit
Zeolit alam perlu diaktifkan terlebih dahulu sebelum digunakan, untuk mempertinggi
daya kerjanya. Pengaktifan zeolit dapat dilakukan melalui beberapa cara antara lain :
1. Pemanasan dalam jangka waktu dan suhu tertentu
2. Mengubah atau mempertukarkan kation yang dapat dipertukarkan
2.2.4 Pengaktifan dengan Pemanasan
Pemanasan terhadap zeolit alam bertujuan untuk mengeluarkan air atau garam
pengotor dari dalam rongga-rongga kristal zeolit. Kemampuan atau sifat pertukaran
kation zeolit teruatama selektifitas dan kapasitas pertukarannya akan sangat
ditentukan oleh struktur kristalnya. Pemakaian panas terlalu tinggi menyebabkan
terjadinya pelepasan aluminium dari struktur kerangka tetrahedral zeolit. Menurut
Barrer (1982) aktifasi pemanasan yang terlalu tinggi akan menyebabkan terjadinya
dehidroksilasi gugus OH pada struktur zeolit. Akibat terjadinya pemutusan ikatan
Si-O-Al, menyebabkan pembentukan gugus siloksan (Si-O-Al) dan aluminium yang
miskin gugus hidroksil. Akibatnya bila terjadi kerusakan pada struktur zeolit tersebut
maka kemempuan mempertukarkan kation dan adsorbsinya berkurang/menurun.
Kestabilan zeolit terhadap temperatur tergantung pada jenis kandungan mineral
zeolitnya (perbandingan Si dengan Al, dan kation yang terdapat dalam zeolit).
Umumnya zeolit dengan silika lebih banyak mempunyai kestabilan yang lebih besar.
Clinoptilolit alam yang kaya akan kalsium rusak pada temperature 5000C, jika
kationnya diganti dengan kalium, maka akan tetap utuh pada temperature 8000C.
komposisi kation yang berbeda dan perbandingan Si dan Al yang berbeda dan
perbandingan Si dengan Al yang berbeda pada beberapa zeolit alam menyebabkan
kestabilannya pada temperature yang berbeda-beda. Seperti modernit yang stabil pada
800-10000C sedangkan philipsit stabil pada 360-4000(Saputra.,R 2006)
2.2.5 Pengaktifan dengan Pengasaman
Yang kedua aktivasi zeolit secara kimia dengan tujuan untuk membersihkan
permukaan pori, membuang senyawa pengotor dan mengatur kembali letak atom yang
dapat dipertukarkan. Proses aktivasi zeolit dengan perlakuan asam HCl pada
konsentrasi 0,1 N hingga 1 N menyebabkan zeolit mengalami dealuminasi dan
dekationisasi yaitu keluarnya Al dan kation-kation dalam kerangka zeolit. Aktivasi
asam menyebabkan terjadinya dekationisasi yang menyebabkan bertambahnya luas
permukaan zeolit karena berkurangnya pengotor yang menutupi pori-pori zeolit. Luas
permukaan yang bertambah diharapkan meningkatkan kemampuan zeolit dalam
Tingginya kandungan Al dalam kerangka zeolit menyebabkan kerangka zeolit
sangat hidrofilik. Sifat hidrofilik dan polar dari zeolit ini merupakan hambatan dalam
kemampuan penjerapannya.
Proses aktivasi dengan asam dapat meningkatkan kristalinitas, keasaman dan
luas permukaan (Shrihapsari,D 2006)
Setiap oksigen dalam ikatan ini cenderung akan mengikat H+ membentuk OH
atau gugus silanol yang bersifat polar.
Ion hidrogen pada gugus hidroksilini siap dipertukarkan dengan kation lain.
Pada keadaan netral atau agak asam, dapat terjadi hidrolisis akan menyebabkan
kenaikan pada pH dengan reaksi :
SiO2- + H2O → SiOH + OH-+
Keadaan yang demikian akan menyebabkan kapasitas pertukarannya meningkat.
Pada harga konsentrasi tertentu, asam juga menghidrolisa aluminium dari
kerangka zeolit yang menyebabkan struktur menjadi rusak. Bila proses dealuminasi
dilakukan berlebihan maka akhirnya Si(OH)4 mudah berpolimerisasi dan terjadi
pemisahan gugus OH (dehidroksilasi), membentuk Si –O-Si yang merupakan ikatan
yang kuat. Hasil dari proses dealuminasi zeolit ini berbentuk silica gel, seperti pada
pemanasan yang terlalu tinggi dan terbentuk bahan amorf sebagai bahan
akhir.(Bambang.P.,dkk.1995)
Secara umum konsentrasi larutan asam serta jenis asam yang dipergunakan di
dalam aktivasi akan mempengaruhi sifat pertukaran dan struktur Kristal dari mineral
zeolit.
Berdasarkan kelarutan di dalam Asam Klorida (HCl), Bogdanova dan Belitsky
(1968) membagi zeolit dalam empat kelompok :sangat resisten, resisten, sedikit
resisten, sedang klinoptilolit resisten. Keadaan ini merupakan sifat dari struktur Kristal
dan ratio Si/Al yang dimiliki oleh masing-masing jenis zeolit tersebut.(Sarno,H.,1983
2.3 Adsorpsi
Adsorpsi secara umum adalah suatu proses pemisahan bahan dari campuran gas atau
cair, bahan yang harus dipisahkan ditarik oleh permukaan sorben padat dan diikat oleh
gaya-gaya yang bekerja pada permukaan tersebut
Sesuai dengan jenis ikatan yang terdapat antara bahan yang diadsorpsi dan
adsorbennya, maka adsorbsi dibedakan antara adsorpsi fisik dan adsorpsi kimia.
adsorpsi kimia berada dalam orde panas reaksi. Sedangkan panas adsorpsi fisik,
khususnya pada campuran gas, lebih besar dan seringkali besarnya 2-3 kali panas
kondensasi dari bahan yang di adsorpsi. Kecepatan adsorpsi tidak hanya bergantung
pada perbedaan konsentrasi dan pada luas permukaan adsorben, melainkan juga pada
suhu, tekanan (untuk gas), ukuran partikel dan porositas adsorben.
Adsorben adalah bahan padat dengan luas permukaan dalam yang sangat
besar. Permukaan yang luas ini terbentuk karena banyaknya pori yang halus pada
ikatab tersebut. Biasanya luasnya berada dalam orde 200 – 1000 m2/g adsorben,
dengan diameter pori sebesar 0,0003 – 0,02 µm.
Adsorben yang sering dikenal ialah karbon aktif, silika gel, tapis molekuler
(molecular sieve), tanah kelantang (bleaching earth) dan aluminium oksida.
(Bernasconi, G., 1995)
2.4 Kobal
Kobal (Co) merupakan logam transisi, memiliki berat molekul 58,93 g/mol, berbentuk
padat pada suhu kamar, berwarna abu-abu perak, memiliki titik didih 2.870-2927 oC.
Cobalt dan senyawanya terdapat di alam melalui sumber alam dan aktivitas manusia.
Kobal secara alami terdapat di bebatuan, tanah, air tanaman dan hewan. Sumber alami
Co di lingkungan adalah tanah, debu, air laut, lava gunung berapi, dan kebakaran
hutan. Co juga bias berasal dari limbah yang berasal dari pembakaran minyak,
pembakaran batu bara, sisa pembakaran kendaraan bermotor, pesawat, serta limbah
dari industri logam keras.
2.4.1 Penggunaan Co dalam Bidang Industri
Kobalt digunakan sebagai :
1. Bahan campuran berbagai jenis superalloy sehingga menghasilkan logam yang
lebih keras.
2. Bahan magnet, sebagai katalisator petroleum dan berbagai industri seperti
tinta, pengering cat.
3. Menstabilisasi buih pada minuman bir.
4. Kobal radioaktif digunakan sebagai sterilisasi peralatan medis. 60Co digunakan untuk memproduksi radioisotop dan sinar γ.
5. Pada industri plastik serta iradiasi pada industri pangan untuk membunuh
2.4.2 Efek Toksik
Co tidak berbahaya bagi kesehatan manusia apabila dikonsumsi dalam dosis rendah.
Namun, konsumsi dalam dosis besar akan berbahaya bagi kesehatan, terutama pada
organ paru-paru dan jantung. Anak-anak lebih sensitif terhadap toksisitas Co
dibandingkan orang dewasa. Co dan garam Co relative tidak toksik bila melalui
paparan pencernaan. Sebagian besar kasus toksik Co terjadi melalui kontak kulit,
terutama bagi penduduk atau pekerja yang tinggal di wilayah industri Co. Inahalasi
udara dengan kadar Co cukup tinggi bias mengakibatkan gangguan paru-paru beruap
asma dan pneumonia. Batas aman kadar Co dalam tubuh adalah sebesar 1,1 mg. Kadar
Co tertinggi disimpan dalam lemak, lalu dalam otot. Kadar Co lebih tinggi terdapat
dalam organ hati, jantung, serta rambut. Pada manusia, kadar Co normal dalam urin
adalah sebesar 98 µg/L, sedangkan kadar Co normal dalam darah sebesar 0,18 µg/L.
(Widowati, W, 2008)
2.5 Nikel
Nikel adalah logam berwarna putih perak dngan berat jenis 8,5 dan berat atom 58,71
g/mol. Ni merupakan logam yang tahan terhadap korosi dan oksidasi pada temperature
tinggi sehingga bias digunakan untuk memproduksi stainless steel. Logam Ni
memiliki sifat kuat, dapat ditempa, serta tahan terhadap karat dan oksidasi.
2.5.1 Efek Toksik
Paparan Nikel (Ni) bisa terjadi melalui inhalasi, oral, dan kontak kulit. Paparan akut
Ni melalu inhalasi bias mengakibatkan kerusakan berat pada paru-paru dan ginjal
serta gangguan gastrointestinal berupa mual, muntah, dan diare. Berdasarkan uji
toksisitas, senyawa larut seperti nikel asetat lebih toksik disbanding dengan senyawa
Ni yang tidak larut.
Paparan Ni lewat kulit secara kronis bias menimbulkan gejala, antara lain
dermatitis nikel berupa kulit kemerahan pada jari-jari tangan serta tangan. Paparan
inhalasi nikel oksida, nikel subsulfida, nikel sulfat heptahidrat dapat mengakibatkan
munculnya gangguan paru-paru. Tingginya kadar Ni dalam jaringan tubuh manusia
bias mengakibatkan munculnya berbagai efek samping, yaitu akumulasi Ni pada
kelenjar pituitari yang bias mengakibatkan depresi sehingga mengurangi sekresi
hormon prolaktin dibawah normal. Akumulasi Ni pada pankreas bias menghambat
2.6 Spektrofotometri Serapan Atom
2.6.1 Prinsip Dasar Spektrofotometri Serapan Atom
Spektroskopi serapan atom adalah spektroskopi atomik yang disertai penyerapan
sebagai suatu emisi atau pancaran. Di dalam beberapa dekade spektroskopi serapan
atom menjadi salah satu dari cara yang yang paling luas digunakan untuk teknik
analisa.(Kennedy, J.H.1984).
Spektroskopi serapan atom digunakan untuk analisis kuantitatif unsur-unsur
logam dalam jumlah sekelumit dan sangat kelumit. Cara analisis ini memberikan
kadar total unsur logam dalam suatu sampel dan tidak tergantung pada bentuk molekul
dari logam dalam sampel tersebut.
Spektroskopi serapan atom didasarkan pada penyerapan energi sinar oleh
atom-atom netral, dan sinar yang diserap biasanya sinar tampak atau ultraviolet.
Metode spektroskopi serapan atom berdasarkan pada prinsip absorbsi cahaya oleh
atom. Atom-atom akan menyerap cahaya pada panjang gelombang tertentu,
tergantung pada sifat unsurnya. Cahaya pada panjang gelombang ini mempunyai
cukup energi untuk mengubah tingkat elektronik suatu atom yang mana transisi
elektronik suatu atom bersifat spesifik. Dengan menyerap suatu energi, maka atom
akan memperoleh energi sehingga suatu atom pada keadaan dasar dapat ditimgkatkan
energinya ke tingkat eksitasi(Rohman,A.2007).
Spektrofotometri serapan atom kegunaannya lebih ditentukan untuk analisis
kuantitatif logam-logam alkali dan alkali tanah. Untuk maksud ini ada beberapa hal
yang perlu diperhatikan antara lain :
- Larutan sampel diusahakan seencer mungkin kadar unsur yang dianalisis tidak
lebih dari 5% dalam pelarut yang sesuai. Larutan yang dianalisis lebih disukai
diasamkan atau kalau dilebur dengan alkali tanah terakhir harus diasamkan
lagi.
- Hindari pemakaian pelarut aromatik atau halogenida. Hendaklah dipakai
2.6.2 Instrumentasi Spektrofotometri Serapan Atom
Gambar 2.2 Sistem peralatan spektrofotometer serapan atom (Rohman, A. 2007)
1. Sumber sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga. Lampu ini
terdiri atas tabung kaca tertutup yang mengandung suatu katoda dan anoda.
Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau
dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon
atau argon) dengan tekanan rendah. Neon biasanya lebih disukai karena
memberikan intensitas pancaran lampu yang lebih rendah.
2. Tempat Sampel
Dalam analisis dengan spektrofotometri serapan atom, sampel yang akan
dianalisis harus diuraikan menjadi atom-atom netral yang masih dalam
keadaan asas. Ada berbagai macam alat yang dapat digunakan untuk
mengubah suatu sampel menjadi uap atom-atom yaitu dengan nyala dan tanpa
nyala
a. Nyala (flame)
Nyala digunakan untuk mengubah sampel yang berupa padatan atau cairan
menjadi bentuk uap atomnya, dan juga berfungsi untuk atomisasi.
b. Tanpa nyala (flameless)
Teknik atomisasi dengan nyala dinilai kurang peka karena atom gagal
mencapai nyala, tetesan sampel yang masuk kedalam nyala terlalu besar,
dan proses atomisasi kurang sempurna. Oleh karena itu muncullah suatu
teknik atomisasi yang baru yakni atomisasi tanpa nyala. Pengatoman dapat
dilakukan dalam tungku dari grafit. Sampel diletakkan dalam tabung grafit,
melewatkan arus listrik grafit. Akibat pemanasan ini, maka zat yang akan
dianalisis berubah menjadi atom-atom netral(Rohman, A. 2007).
3. Monokromator
Monokromator memisahkan, mengisolasi dan mengontrol intensitas dari
radiasi energi yang mencapai detektor. Pada hakekatnya mungkin saja dapat
dianggap sebagai suatu saringan yang dapat disesuaikan dengan suatu daerah
yang spesifik, yang mana spectrum transmisi yang tidak sesuai akan ditolak.
Idealnya monokromator harus mampu memisahkan garis resonansi. Karena
ada beberapa unsur yang mudah dan ada beberapa unsur yang
sulit(Haswell,S.J.1991).
4. Detektor
Detektor dapat diatur sedemikian rupa pada nilai frekuensi tertentu, sehingga
tidak memberikan respon terhadap emisi yang berasal dari eksitasi
termal(Khopkar,S.M.2003).
5. Readout
Readout merupakan suatu alat penunjuk atau dapat juga diartikan sebagai
BAB 3
METODOLOGI PERCOBAAN
3.1 Alat dan Bahan
3.1.1 Alat-alat
- Alu dan Lumpang
- Gelas Beaker Pyrex 1000 mL
- Gelas Erlenmeyer Pyrex 250 mL
- Gelas Beaker Pyrex 250 mL
- LabuTakar Pyrex 100 mL
- Pipet Tetes
- Spatula
- Hotplate Cimarec
- Tungku Pemanas ShinShaeng
- Magnetic Bar
- Oven
- Kertas Saring Whatman No 40
- Neraca Analitis AND
- Ayakan Mesh
- Spektrofotometer Serapan Atom (SSA) Shimadzu AA-6300
- Corong
- Statif dan Klem
3.1.2 Bahan-bahan
- Zeolit Alam Sarulla
- HCl(p) p.a (E.Merck)
- HNO3(p) p.a (E.Merck)
- Akuades
- Larutan standar Ni 1000 mg/L
- Larutan standar Co 1000 mg/L
3.2Prosedur Penelitian
3.2.1 Pembuatan Pereaksi H2SO4
1. Pembuatan H2SO4 1 N
Sebanyak 2,7 mL H2SO4(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
2. Pembuatan H2SO4 2 N
Sebanyak 5,4 mL H2SO4(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelahdingin, kemudian dihomogenkan.
3. Pembuatan H2SO4 3 N
Sebanyak 8,1 mL H2SO4(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
4. Pembuatan H2SO4 4 N
Sebanyak 10,8 mL H2SO4(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
5. Pembuatan H2SO4 5 N
Sebanyak 13,5 mL H2SO4(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda.Di tunggu
3.2.2 Pembuatan Pereaksi HCl
1. Pembuatan HCl 1 N
Sebanyak 8,3 mL HCl(p) dimasukkan kedalam labutakar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
2. Pembuatan HCl 2 N
Sebanyak 16,6 mL HCl(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda.Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3. Pembuatan HCl 3 N
Sebanyak 24,9 mL HCl(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
4. Pembuatan HCl 4 N
Sebanyak 33,2 mL HCl(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
5. Pembuatan HCl 5 N
Sebanyak 41,5 mL HCl(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
sampai larutan benar-benar dingin. Setelah dingin, kemudian dihomogenkan.
3.2.3 Pembuatan Pereaksi HNO3 4 N
Sebanyak 28,1 mL HCl(p) dimasukkan kedalam labu takar 100 mL secara
perlahan-lahan. Ditambahkan aquadest secara perlahan-lahan sampai garis tanda. Di tunggu
3.2.4 Aktivasi Zeolit Alam Dengan H2SO4
Sebanyak 25 gram zeolit alam 120 mesh dimasukkan kedalam gelas beaker yang
berisi 100 mL H2SO4 1 N. Di aduk dengan menggunakan magnetic stirrer selama 2
jam dengan kecepatan 80 rpm sambil dipanaskan pada suhu 100oC. Disaring dengan
menggunakan kertas saring. Kemudian dibilas dengan menggunakan aquadest sampai
pH netral. Dipanaskan di dalam oven pada suhu 105oC. Kemudian di haluskan
kembali. Hal yang sama dilakukan untuk aktivasi zeolit alam dengan menggunakan
H2SO4 2N, H2SO4 3N, H2SO4 4N, dan H2SO4 5N.
3.2.5 Aktivasi zeolit alam dengan HCl
Sebanyak 25 gram zeolit alam 120 mesh dimasukkan kedalam gelas beaker yang
berisi 100 mL HCl 1 N. Di aduk dengan menggunakan magnetic stirrer selama 2 jam
dengan kecepatan 80 rpm sambil dipanaskan pada suhu 100oC. Disaring dengan
menggunakan kertas saring. Kemudian dibilas dengan menggunakan aquadest sampai
pH netral. Dipanaskan di dalam oven pada suhu 105oC. Kemudian di haluskan
kembali. Hal yang sama dilakukan untuk aktivasi zeolit alam dengan menggunakan
HCl 2N, HCl 3N, HCl 4N, dan HCl 5N.
3.2.6 Pembuatan Larutan Standar Kobal 100 mg/L
Sebanyak 10 ml larutan induk logam kobal 1000 mg/L dimasukkan kedalam labu
takar 100 ml lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.7 Pembuatan Larutan Standar Kobal 10 mg/L
Sebanyak 25 ml larutan standar kobal 100 mg/L dimasukkan kedalam labu takar 250
ml lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk sampai
3.2.8 Pembuatan Larutan Seri Standar Kobal 0,10; 0,50; 1,00; 2,00; dan 3,00;
mg/L
Sebanyak 0,5; 2,5; 5,0; 10,0; dan 15,0 ml larutan standar Kobal 10 mg/L dimasukkan
kedalam labu takar 50 ml lalu diencerkan dengan larutan pengencer sampai garis
tanda dan diaduk sampai homogen. (SNI 06-6989.7-2004)
3.2.9 Pembuatan Larutan Standar Nikel 100 mg/L
Sebanyak 10 ml larutan induk logam Nikel 1000 mg/L dimasukkan kedalam labu
takar 100 ml lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk
sampai homogen.
3.2.10 Pembuatan Larutan Standar Nikel 10 mg/L
Sebanyak 25 ml larutan standar Nikel 100 mg/L dimasukkan kedalam labu takar 250
ml lalu diencerkan dengan larutan pengencer sampai garis tanda dan diaduk sampai
homogen.
3.2.11 Pembuatan Larutan Seri Standar logam Nikel 0,1; 0,50; 1,00; 2,00; dan
3,00 mg/L
Sebanyak 0,5; 2,5; 5,0; 10,0; dan 15,0 ml larutan standar Nikel 10 mg/L dimasukkan
kedalam labu takar 50 ml lalu diencerkan dengan larutan pengencer sampai garis
tanda dan diaduk sampai homogen. . (SNI 06-6989.6-2004)
3.2.12 Pembuatan kurva kalibrasi Logam Kobal
Larutan seri standar logam Kobal 0,10 mg/L kemudian diukur absorbansinya dengan spektrofotometer serapan atom pada λspesifik = nm. Perlakuan dilakukan sebanyak 3
kali dan dilakukan hal yang sama untuk larutan seri standar 0,50; 1,00; 2,00; dan 3,00
3.2.13 Pembuatan kurva kalibrasi Logam Nikel
Larutan seri standar logam nikel 0,10 mg/L kemudian diukur absorbansinya dengan spektrofotometer serapan atom pada λspesifik = nm. Perlakuan dilakukan sebanyak 3
kali dan dilakukan hal yang sama untuk larutan seri standar 0,50; 1,00; 2,00; dan 3,00
mg/L.
3.2.14 Penyerapan larutan standar Kobal dan Nikel dengan menggunakan
zeolit alam yang telah diaktivasi
3.2.14.1 Penyerapan larutan standar Kobal dan Nikel dengan
mengggunakan zeolit alam yang telah diaktivasi dengan variasi
konsentrasi H2SO4
Sebanyak 25 ml larutan seri standart Kobal 3 mg/L dimasukkan kedalam gelas beaker
250 ml. Ditambahkan 5 gram zeolit yang telah diaktivasi dengan H2SO4 1 N. Diaduk
dengan menggunakan magnetik bar selama 6 jam. Disaring, dan filtrat yang
mengandung ion logam Kobal diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada λspesifik 240 nm. Diulangi perlakuan yang sama untuk konsentrasi
H2SO4 2; 3; 4; dan 5 N. Diulangi perlakuan yang sama untuk larutan seri standart
Nikel 3 mg/L.
3.2.14.2 Penyerapan larutan standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan variasi
konsentrasi HCl
Sebanyak 25 ml larutan seri standart Kobal 3 mg/L dimasukkan kedalam gelas beaker
250 ml. Ditambahkan 5 gram zeolit yang telah diaktivasi dengan HCl 1 N. Diaduk
dengan menggunakan magnetik bar selama 6 jam. Disaring, dan filtrat yang
mengandung ion logam Kobal diukur absorbansinya dengan Spektrofotometer
Serapan Atom pada λspesifik 240 nm. Diulangi perlakuan yang sama untuk konsentrasi
HCl 2; 3; 4; dan 5 N. Diulangi perlakuan yang sama untuk larutan seri standart Nikel
3.2.14.3 Penyerapan larutan standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan H2SO4 2 N dengan
variasi pH
Sebanyak 25 ml larutan seri standart Kobal 3 mg/L dimasukkan kedalam gelas beaker
250 ml. Ditambahkan HNO3 4 N hingga pH 4. Ditambahkan 5 gram zeolit yang telah
diaktivasi dengan H2SO4 N. Diaduk dengan menggunakan magnetik bar selama 6 jam.
Disaring, dan filtrat yang mengandung ion logam Kobal diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 240 nm. Diulangi perlakuan yang
sama untuk variasi pH 5, dan 6. Diulangi perlakuan yang sama untuk larutan seri
standart Nikel 3 mg/L.
3.2.14.4 Penyerapan larutan standar Kobal dan Nikel dengan
menggunakan zeolit alam yang telah diaktivasi dengan HCl 4 N dengan
variasi pH
Sebanyak 25 ml larutan seri standart Kobal 3 mg/L dimasukkan kedalam gelas beaker
250 ml. Ditambahkan HNO3 4 N hingga pH 4. Ditambahkan 5 gram zeolit yang telah
diaktivasi dengan HCl 4 N. Diaduk dengan menggunakan magnetik bar selama 6 jam.
Disaring, dan filtrat yang mengandung ion logam Kobal diukur absorbansinya dengan Spektrofotometer SerapanAtom pada λspesifik 240 nm. Diulangi perlakuan yang sama
untuk variasi pH 5, dan 6. Diulangi perlakuan yang sama untuk larutan seri standart
Zeolit Alam
Serbuk
Zeolit Bebas Air
Zeolit Berwarna Kehijauan
Endapan Filtrat
Zeolit Alam Teraktivasi
3.3 Bagan Penelitian
3.3.1 Aktivasi Zeolit Alam Dengan H2SO4
Dihaluskan
Diayak 180 Mesh
Ditimbang sebanyak 25 gram
Dimasukkan kedalam beaker glass
Dipanaskan didalam tanur pada suhu 300 oC
Dibiarkan hingga suhunya turun
Ditambahkan 100 mL H2SO4 1, 2, 3, 4 dan 5 N
Dipanaskan diatas hotplate pada suhu 100 oC sambil diaduk
dengan magnetik stirer selama 2 jam
Disaring
Dibilas sampai mencapai pH 7
Dipanaskan dalam oven pada suhu 100 oC sampai benar-benar
Zeolit Alam Zeolit Alam
Serbuk
Zeolit Bebas Air
Zeolit Berwarna Kehijauan
Endapan Filtrat
Zeolit Alam Teraktivasi
3.3.2 Aktivasi Zeolit Alam Dengan H
Dihaluskan
Diayak 180 Mesh
Ditimbang sebanyak 25 gram
Dimasukkan kedalam beaker glass
Dipanaskan didalam tanur pada suhu 300 oC
Dibiarkan hingga suhunya turun
Ditambahkan 100 mL HCl 1, 2, 3, 4 dan 5 N
Dipanaskan diatas hotplate pada suhu 100 oC sambil diaduk
dengan magnetik stirer selama 2 jam
Disaring
Dibilas sampai mencapai pH 7
Dipanaskan dalam oven pada suhu 100 oC sampai benar-benar
25 mL larutan seri standar Kobal 3 mg/L
Filtrat Endapan
Hasil
3.3.3 Penyerapan larutan standar Kobal dan Nikel dengan mengggunakan
zeolit alam yang telah diaktivasi dengan variasi konsentrasi H2SO4
Dimasukkan kedalam gelas Beaker
Ditambahkan 5 gram Zeolit Alam yang telah diaktivasi dengan
H2SO4 1, 2, 3, 4, dan 5 N
Diaduk dengan menggunakan magnetik stirer selama 6 jam
Disaring dengan menggunakan kertas saring Whatman No 40
Diukur absorbansinya dengan menggunakan Spektrofotometer
Serapan Atom dengan λspesifik 240 nm
Catatan : Perlakuan yang sama dilakukan untuk logam Nikel dengan λspesifik 232
25 mL larutan seri standar Kobal 3 mg/L
Endapan Filtrat
Hasil
3.3.4 Penyerapan larutan standar Kobal dan Nikel dengan mengggunakan
zeolit alam yang telah diaktivasi dengan variasi konsentrasi HCl
Dimasukkan kedalam gelas Beaker
Ditambahkan 5 gram Zeolit Alam yang telah diaktivasi dengan
HCl 1, 2, 3, 4, dan 5 N
Diaduk dengan menggunakan magnetik stirer selama 6 jam
Disaring dengan menggunakan kertas saring Whatman No 40
Diukur absorbansinya dengan menggunakan Spektrofotometer
Serapan Atom dengan λspesifik 240 nm
Catatan : Perlakuan yang sama dilakukan untuk logam Nikel dengan λspesifik 232
25 mL larutan seri standar Kobal 3 mg/L
Filtrat Endapan
Hasil
3.3.5 Penyerapan larutan standar Kobal dan Nikel dengan menggunakan zeolit
alam yang telah diaktivasi dengan H2SO4 2 N dengan variasi pH
Dimasukkan kedalam gelas Beaker
Ditambahkan 5 gram Zeolit Alam yang telah diaktivasi dengan
H2SO4 2 N
Ditambahkan HNO3 4 N hingga pH larutan menjadi 7, 6, 5, dan 4
Diaduk dengan menggunakan magnetik stirer selama 6 jam
Disaring dengan menggunakan kertas saring Whatman No 40
Diukur absorbansinya dengan menggunakan Spektrofotometer
Serapan Atom dengan λspesifik 240 nm
Catatan : Perlakuan yang sama dilakukan untuk logam Nikel dengan λspesifik 232
25 mL larutan seri standar Kobal 3 mg/L
Filtrat Endapan
Hasil
3.3.6 Penyerapan larutan standar Kobalt dan Nikel dengan menggunakan
zeolit alam yang telah diaktivasi dengan HCl4 N dengan variasi pH
Dimasukkan kedalam gelas Beaker
Ditambahkan 5 gram Zeolit Alam yang telah diaktivasi dengan
HCl 4 N
Ditambahkan HNO3 4 N hingga pH larutan menjadi 7, 6, 5, dan 4
Diaduk dengan menggunakan magnetik stirer selama 6 jam
Disaring dengan menggunakan kertas saring Whatman No 40
Diukur absorbansinya dengan menggunakan Spektrofotometer
Serapan Atom dengan λspesifik 240 nm
Catatan : Perlakuan yang sama dilakukan untuk logam Nikel dengan λspesifik 232
3.3.7 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi Nikel (Ni)
Dipipet sebanyak 5 ml larutan standar Nikel dan
dimasukkan kedalam labu takar 50 ml
Diencerkan dengan larutan pengencer sampai garis
tanda
Diaduk hingga homogen
Dipipet sebanyak 10 ml larutan standar Nikel dan
dimasukkan kedalam labu takar 100 ml
Diencerkan dengan larutan pengencer sampai garis
tanda
Diaduk hingga homogen
Dipipet sebanyak 0,5; 2,5; 5; 10;dan 15 ml larutan
standar Nikel dan dimasukkan kedalam labu takar 50 ml
Diencerkan dengan larutan pengencer sampai garis
tanda
Diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada λspesifik 232 nm
Larutan standar Nikel 1000 mg/L
Larutan standar Nikel 100 mg/L
Larutan standar Nikel 10 mg/L
Larutan seri standar Nikel 0,1; 0,5; 1; 2; dan 3 mg/L
3.3.8 Pembuatan Larutan Seri Standar dan Kurva Kalibrasi Kobal (Co)
Dipipet sebanyak 5 ml larutan standar Kobal dan
dimasukkan kedalam labu takar 50 ml
Diencerkan dengan larutan pengencer sampai garis
tanda
Diaduk hingga homogen
Dipipet sebanyak 10 ml larutan standar Kobal dan
dimasukkan kedalam labu takar 100 ml
Diencerkan dengan larutan pengencer sampai garis
tanda
Diaduk hingga homogen
Dipipet sebanyak 0,5; 2,5; 5; 10; dan 15 ml larutan
standar Kobal dan dimasukkan kedalam labu takar 50
ml
Diencerkan dengan larutan pengencer sampai garis
tanda
Diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan Atom pada λspesifik 240 nm
Larutan standar Kobal 1000 mg/L
Larutan standar Kobal 100 mg/L
Larutan standar Kobal 10 mg/L
Larutan seri standar Kobal 0,1; 0,5; 1; 2; dan 3 mg/L
BAB 4
HASIL DAN PEMBAHASAN
4.1. Hasil Penelitian
4.1.1. Logam Kobal (Co)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi
logam Kobal (Co) dapat dilihat pada tabel 4.1.
Tabel 4.1. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam Kobal (Co).
No Parameter Logam Kobal (Co)
Kecepatan aliran gas pembakar (L/min)
Kecepatan aliran Udara (L/min)
Lebar Celah (nm)
Tabel 4.2. Data absorbansi larutan standar Kobal (Co)
Konsentrasi (mg/L) Absorbansi Rata-rata
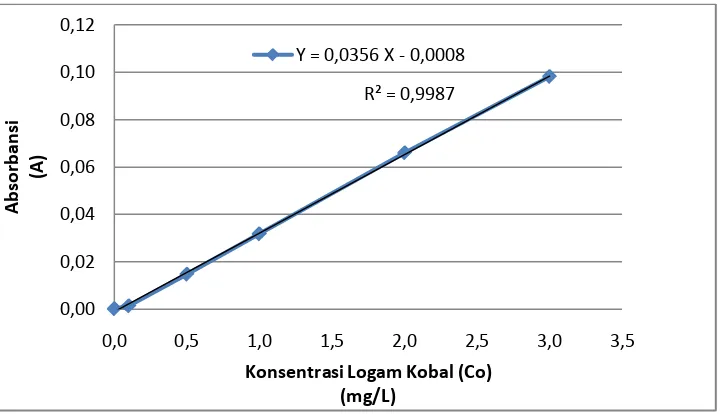
Gambar 4.1. Kurva kalibrasi larutan standar Kobal (Co).
4.1.2. Pengolahan Data Logam Kobal (Co)
4.1.2.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Kobal (Co) pada tabel 4.2.
diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada tabel 4.3.
Tabel 4.3. Penurunan persamaan garis regresi untuk penentuan konsentrasi logam Kobal (Co) berdasarkan pengukuran absorbansi larutan standar Kobal (Co).
No X Y Xi-X Yi-Y (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
1 0,0000 0,0002 -1,1000 -0,0354 1,2100 0,0013 0,0389
2 0,1000 0,0011 -1,0000 -0,0345 1,0000 0,0012 0,0345
3 0,5000 0,0162 -0,6000 -0,0194 0,3600 0,0003 0,0116
4 1,0000 0,0317 -0,1000 -0,0039 0,0100 0,0001 0,0004
5 2,0000 0,0660 0,9000 0,0304 0,8100 0,0009 0,0274
6 3,0000 0,0982 1,9000 0,0626 3,6100 0,0039 0,1190
∑ 6,6000 0,2134 0 0 7,0000 0,0077 0,2318
X = = 1,1
Y = = 0,0356
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
dimana :
Selanjutnya harga slope dapat ditentukan dengan mengunakan metode least square
sebagai berikut :
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.3. pada persamaan
ini maka diperoleh :
a =
a = 0,0331
b = 0,0356 – (0,0331)(1,1)
b = 0,0356 – 0,0364
b = -0,0008
Maka pesamaan garis yang diperoleh adalah :
4.1.2.2. Koefisien Korelasi
r =
Koefisien korelasi untuk logam Kobal (Co) adalah:
r =
r =
r = 0,9987
4.1.2.3. Persentasi (%) penurunan konsentrasi logam Kobal (Co)
Dari data di atas dapat ditentukan persentase (%) penurunan konsentrasi logam Kobal
(Co) dengan menggunakan rumus :
x 100%
Maka persentasi (%) penurunan konsentrasi logam Kobal (Co) dalam larutan standar
setelah penambahan zeolit alam teraktivasi adalah :
x 100% = 95,02%
Dengan cara yang sama dapat dihitung persentasi (%) penurunan konsentrasi logam
Kobal (Co) dalam larutan standar setelah penambahan zeolit alam teraktivasi. Data
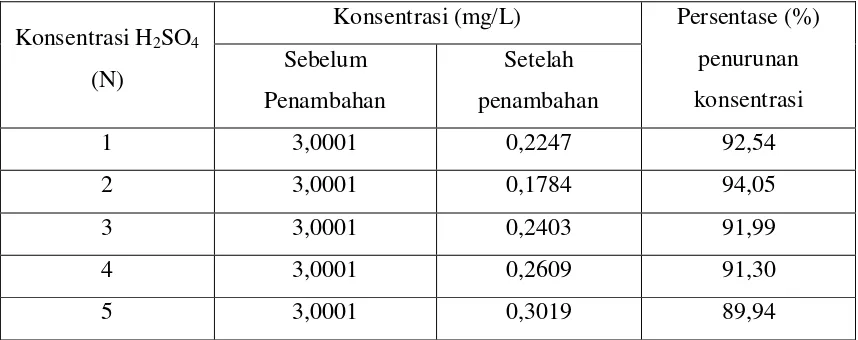
Tabel 4.4. Data persentase (%) penurunan konsentrasi logam Kobal (Co) dalam larutan standar setelah penambahan zeolit alam tearktivasi dengan variasi konsentrasi H2SO4.
Konsentrasi H2SO4
(N)
Konsentrasi (mg/L) Persentase (%)
penurunan
Tabel 4.5. Data persentase (%) penurunan konsentrasi logam Kobal (Co) dalam larutan standar setelah penambahan zeolit alam teraktivasi dengan variasi konsentrasi HCl.
Konsentrasi HCl
(N)
Konsentrasi (mg/L) Persentase (%)
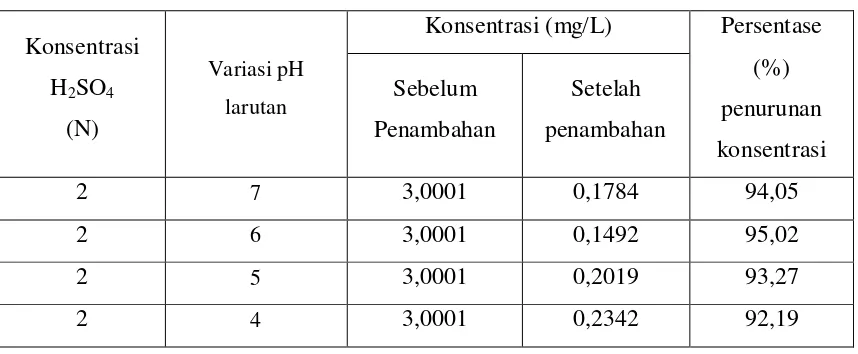
Tabel 4.6. Data persentase (%) penurunan konsentrasi logam Kobal (Co) dalam larutan standar setelah penambahan zeolit alam teraktivasi konsentrasi H2SO4 2 N dengan variasi pH larutan.
Konsentrasi
H2SO4
(N)
Variasi pH
larutan
Konsentrasi (mg/L) Persentase
(%)
Tabel 4.7. Data persentase (%) penurunan konsentrasi logam Kobal (Co) dalam larutan standar setelah penambahan zeolit alam teraktivasi konsentrasi HCl 4 N dengan variasi pH larutan.
Konsentrasi
HCl
(N)
Variasi pH
larutan
Konsentrasi (mg/L) Persentase
4.1.3. Logam Nikel (Ni)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi
logam Nikel (Ni) dapat dilihat pada tabel 4.8.
Tabel 4.8. Kondisi alat SSA Merek Shimadzu tipe AA-6300 pada pengukuran konsentrasi logam Nikel (Ni).
No Parameter Logam Nikel (Ni)
Kecepatan aliran gas pembakar (L/min)
Kecepatan aliran Udara (L/min)
Lebar Celah (nm)
Tabel 4.9. Data absorbansi larutan standar Nikel (Ni).
Konsentrasi (mg/L) Absorbansi Rata-rata
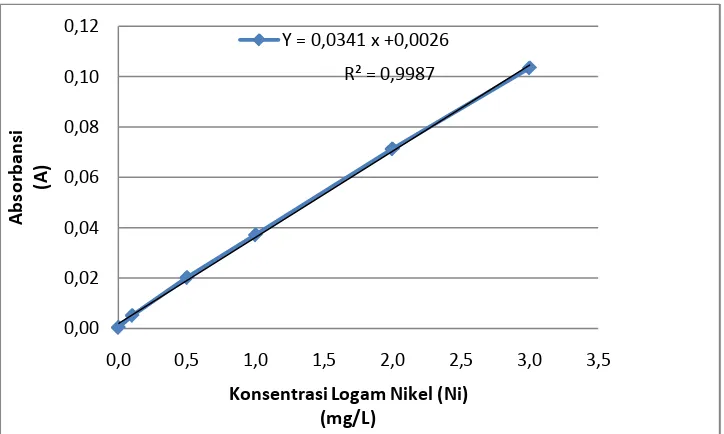
Gambar 4.2. Kurva kalibrasi larutan standar Nikel (Ni).
4.1.4. Pengolahan Data Logam Nikel (Ni)
4.1.4.1. Penurunan Persamaan Garis Regresi dengan Metode Least Square
Hasil pengukuran absorbansi larutan seri standar logam Nikel (Ni) pada Tabel 4.9.
diplotkan terhadap konsentrasi sehingga diperoleh kurva kalibrasi berupa garis linier.
Persamaan garis regresi untuk kurva kalibrasi ini dapat diturunkan dengan metode
least square dengan data pada Tabel 4.10
Tabel 4.10. Penurunan persamaan garis regresi untuk penentuan konsentrasi logam Nikel (Ni) berdasarkan pengukuran absorbansi larutan standar Nikel (Ni).
2 0,1000 0,0047 -1,0000 -0,0354 1,0000 0,0013 0,0354
3 0,5000 0,0228 -0,6000 -0,0173 0,3600 0,0003 0,0104
4 1,0000 0,0371 -0,1000 -0,0029 0,0100 0,0001 0,0003
5 2,0000 0,0722 0,9000 0,0321 0,8100 0,0013 0,0289
6 3,0000 0,1034 1,9000 0,0633 3,6100 0,0040 0,1203
X = = 1,1
Y = = 0,0401
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis :
dimana :
Selanjutnya harga slope dapat ditentukan dengan mengunakan metode least square
sebagai berikut :
Dengan mensubstitusikan harga-harga yang tercantum pada tabel 4.11. pada
persamaan ini maka diperoleh :
a =
a = 0,0341
b = 0,0401 – (0,0341)(1,1)
b = 0,0401 – 0,0375
b = 0,0026
4.1.4.2. Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
r =
Koefisien korelasi untuk logam Nikel (Ni) adalah:
r =
r =
r = 0,9987
4.1.4.3. Persentasi (%) penurunan konsentrasi logam Nikel (Ni)
Dari data di atas dapat ditentukan persentase (%) penurunan konsentrasi logam Nikel
(Ni) dengan menggunakan rumus :
x 100%
Maka persentasi (%) penurunan konsentrasi logam Nikel (Ni) dalam larutan standar
setelah penambahan zeolit alam teraktivasi.
x 100% = 96,18 %
Dengan cara yang sama dapat dihitung persentasi (%) penurunan konsentrasi logam
Nikel (Ni) dalam larutan standar setelah penambahan zeolit alam. Data selengkapnya
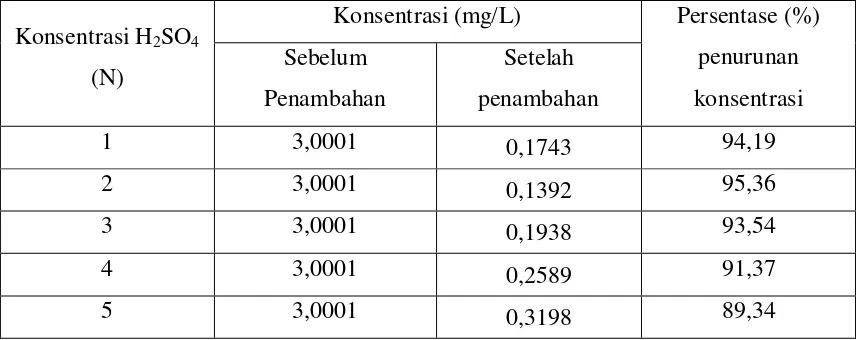
Tabel 4.11. Data persentase (%) penurunan konsentrasi logam Nikel (Ni) dalam larutan standar setelah penambahan zeolit alam teraktivasi dengan variasi konsentrasi H2SO4.
Konsentrasi H2SO4
(N)
Konsentrasi (mg/L) Persentase (%)
penurunan
Tabel 4.12. Data persentase (%) penurunan konsentrasi logam Nikel (Ni) dalam larutan standar setelah penambahan zeolit alam teraktivasi dengan variasi konsentrasi HCl.
Konsentrasi HCl
(N)
Konsentrasi (mg/L) Persentase (%)
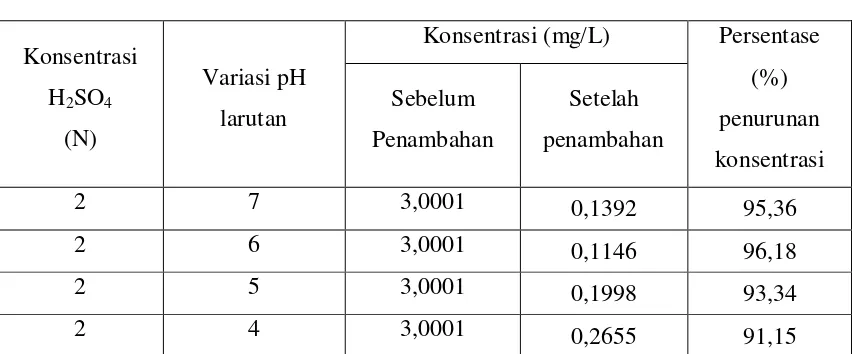
Tabel 4.13. Data persentase (%) penurunan konsentrasi logam Nikel (Ni)) dalam larutan standar setelah penambahan zeolit alam teraktivasi konsentrasi H2SO4 2 N dengan variasi pH larutan.
Konsentrasi
H2SO4
(N)
Variasi pH
larutan
Konsentrasi (mg/L) Persentase
(%)
Tabel 4.14. Data persentase (%) penurunan konsentrasi logam Nikel (Ni) dalam larutan standar setelah penambahan zeolit alam teraktivasi konsentrasi HCl 4 N dengan variasi pH larutan.
Konsentrasi
HCl
(N)
Variasi pH
larutan
Konsentrasi (mg/L) Persentase