BIOSENSOR ARSEN(III) MENGGUNAKAN ELEKTRODE
PASTA KARBON TERMODIFIKASI PARTIKEL
NANOZEOLIT-Fe DAN PENGARUH KEBERADAAN
TIMBAL(II)
MUHAMMAD HAMDANI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Biosensor Arsen(III) Menggunakan Elektrode Pasta Karbon Termodifikasi Partikel Nanozeolit dan Pengaruh Keberadaan Timbal(II) adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juni 2014
Muhammad Hamdani
ABSTRAK
MUHAMMAD HAMDANI. Biosensor Arsen(III) Menggunakan Elektrode Pasta Karbon Termodifikasi Partikel Nanozeolit-Fe dan Pengaruh Keberadaan Timbal(II). Dibimbing oleh HENNY PURWNINGSIH SUYUTI dan DYAH ISWANTINI PRADONO
Pendeteksian ion arsen(III) dengan biosensor menggunakan prinsip penghambatan kerja enzim dapat digunakan sebagai metode untuk pendeteksian ion arsen(III) di perairan. Biosensor dibuat dari elektrode pasta karbon termodifikasi nanopartikel zeolit-Fe dan enzim piruvat dehidrogenase (PDH) sebagai agen pengenal hayati yang aktivitasnya akan dihambat oleh adanya ion arsen(III). Enzim PDH diimmobilisasi pada permukaan elektrode. Kondisi optimum aktivitas enzim adalah suhu 33 °C, pH 7, dan [PDH] 0.0141 U/mL. Aktivitas PDH linear pada rentang konsentrasi ion arsen(III) 0.6-20 ppb dengan nilai R2 = 0.9932. Nilai limit deteksi dan limit kuantisasi didapatkan masing-masing sebesar 2.06 dan 6.99 ppb. Elektrode relatif stabil selama 3 hari, dan menghasilkan keterulangan yang baik dengan nilai %RSD 1.98%. Keberadaan ion pengganggu Pb(II) tidak mengganggu kinerja pengukuran elektrode terhadap ion As(III), karena nilai Ki,j< 1.
Kata kunci: arsen, piruvat dehidrogenase, limit deteksi, limit kuantitasi, ion pengganggu Pb(II)
ABSTRACT
MUHAMMAD HAMDANI. Arsenic-(III) Biosensor Using Modified Carbon Electrodes Pasta of Nanozeolit-Fe particles and the Effect of Lead (II). Supervised by HENNY PURWNINGSIH SUYUTI and DYAH ISWANTINI PRADONO
Ion detection of arsenic(III) with biosensors using enzyme inhibition principle can be used as a method for detecting arsenic(III) ions in waters. Biosensor is made of carbon paste electrode as modified using zeolite-Fe nanoparticles and the enzyme pyruvate dehydrogenase (PDH) as an agent of biological activity identifier that will be inhibited by the presence of arsenic(III) ions. PDH was immobilized on the surface of the electrode. The optimum condition of enzyme activity was at 33 ᵒC , pH 7, and [PDH] 0.0141 U/mL. The activity of PDH was linear in the range of 0.6-20 ppb arsenic(III) ion concentracions with R2 = 0.9932. Detection limit and quantitation limit were 2.06
and 6.99 ppb, respectively. The electrode was relatively stable for 3 days, with good repeatability at %RSD of 1.98%. The existence Pb(II) ion did not interfere the performance of the ion electrode measurements of As-(III), as the value of Ki,j was <1.
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
pada
Departemen Kimia
BIOSENSOR ARSEN(III) MENGGUNAKAN ELEKTRODE
PASTA KARBON TERMODIFIKASI PARTIKEL
NANOZEOLIT-Fe DAN PENGARUH KEBERADAAN
TIMBAL(II)
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM INSTITUT PERTANIAN BOGOR
BOGOR 2014
Judul Skripsi : Biosensor Arsen(III) Menggunakan Elektrode Pasta Karbon Termodifikasi Partikel Nanozeolit-Fe dan Pengaruh Keberadaan Timbal(II)
Nama : Muhammad Hamdani NIM : G44100115
Disetujui oleh
Dr Henny Purwaningsih S, MSi Pembimbing I
Prof Dr Dyah Iswantini Pradono, MSc Agr Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga penilitian dan karya ilmiah ini berhasil diselesaikan. Karya ilmiah ini disusun berdasarkan penelitian dan studi pustaka yang dilakukan pada bulan Januari hingga Juni 2014 bertempat di Laboratorium Kimia Fisik dan Lingkungan, Laboratorium Bersama, dan Laboratorium Terpadu Institut Pertanian Bogor.
Terima kasih penulis ucapkan kepada Ibu Dr Henny Purwaningsih Suyuti, Msi, Ibu Prof Dr Dyah Iswantini Pradono, M Agr selaku pembimbing atas saran, kritikan, dorongan, dan bimbingannya selama penelitian dan penyusunan karya ilmiah ini. Di samping itu, penulis juga berterimakasih kepada staf laboran Kimia Fisik dan Lingkungan, Bapak Mail dan Ibu Ai; staf laboran Laboratorium Bersama, Bapak Wawan dan Mas Eko; serta staf teknisi Laboratorium Terpadu, Mbak Ani, Mas Yono, Mbak Indah, Kak Tari, Kak Denar, Kak Agy dan tak lupa juga terima kasih atas rasa sayang yang tak terkira untuk seluruh keluarga kimia khususnya Kimia 47 yang selalu memberikan dukungan, khususnya teman seperjuangan dalam penelitian Ali Aulia Ghozali.
Ucapan terimakasih yang tak terhingga juga disampaikan kepada Mama tercinta yang senantiasa mendoakan yang terbaik untuk ananda, dan Almarhum Papa tersayang yang selalu hadir dalam hati sanubari. Serta kepada kakak Nurhidayati, Zulfakar Fadhillah, Dzulafifah, Singgih, Maritsa Afni, dan Adik Arif Putra Alhafidz, serta keluarga besar yang selalu memberikan nasihat, motivasi, serta semangat untuk penulis.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juni 2014
DAFTAR ISI
DAFTAR TABEL vi
DAFTAR GAMBAR vi
DAFTAR LAMPIRAN vi
PENDAHULUAN 1
METODE 3
Alat dan Bahan 3
Metode Penelitian 3
HASIL DAN PEMBAHASAN 6
Zeolit Termodifikasi-besi 6
Kadar Fe pada Zeolit Termodifikasi-Besi 6
Pencirian Elektrode Pasta Karbon 7
Optimasi Aktivitas PDH 8
Pencirian Elektrode 11
SIMPULAN DAN SARAN 14
Simpulan 14
Saran 14
DAFTAR PUSTAKA 15
LAMPIRAN 17
DAFTAR GAMBAR
1 Persentase kenaikan kadar Fe pada zeolit. 7
2 Voltamogram siklik K3Fe(CN)6 1 mM dengan menggunakan elektroda
pasta karbon. 8
3 Voltamogram siklik pada suhu 33 ᵒC, pH 7, dan [PDH] 0.0141 U/mL. 9 4 (a) Plot kontur antara suhu dan pH, (b) suhu dan [PDH], (c) serta pH
dan [PDH] terhadap puncak arus oksidasi aktivitas enzim PDH. 11 5 Profil arus puncak oksidasi terhadap konsentrasi arsen. 11 6 Profil linearitas elektrode biosensor arsen. 12
7 Kurva stabilitas aktivitas enzim PDH. 13
DAFTAR LAMPIRAN
1 Bagan alir penelitian. 17
2 Hasil analisis kadar Fe pada zeolit termodifikasi-besi menggunakan
AAS 18
3 Optimasi suhu, pH, konsentrasi PDH, dan arus yang dihasilkan. 19 4 Nilai LOD dan LOQ dari pengukuran aktivitas biosensor arsen. 19 5 Stabilitas biosensor arsen pada suhu 33 ᵒC, pH 7, dan [PDH] 0.0141
U/mL. 20
6 Keterulangan arus puncak oksidasi dari 3 elektrode. 20 7 Nilai koefisien selektivitas biosensor arsen(III) terhadap ion Pb(II). 21 8 Profil hasil pemayaran EPK termodifikasi zeolit-Fe dengan
PENDAHULUAN
Pencemaran lingkungan yang disebabkan oleh kegiatan perindustrian, pertambangan, dan pembuangan limbah yang tidak teratur telah banyak ditemui di dalam kehidupan masyarakat diantaranya disebabkan oleh pencemaran yang berasal dari limbah anorganik seperti logam berat yang bersifat toksik. Konsentrasi logam berat yang melampaui ambang batas dapat mempengaruhi kesehatan makhluk hidup di sekitarnya.
Salah satu logam berat yang bersifat toksik, yaitu senyawaan logam arsen (As). Arsen merupakan unsur yang ditemukan di kerak bumi dengan kadar rata-rata 5 ppm, dan terkonsentrasi di beberapa bagian dunia karena mineralisasi alami (Shen et al. 2013). Logam arsen banyak digunakan dalam bidang pertanian, perindustrian, dan medis, sehingga apabila penggunaannya secara intensif dapat menimbulkan limbah beracun terutama dalam perairan. Keracunan logam As dapat menyebabkan berbagai gejala dan penyakit seperti dapat merusak kulit, gejala gastrointestinal, peripheral neuropathy, diabetes, gangguan ginjal, jantung, dan kanker (Anetor et al. 2007). Keputusan Direktur Jenderal Pengawasan Obat dan Makanan No.03725/B/SK/VII/1989 memberikan kisaran maksimum dari arsen dalam makanan sebesar 0.1-1.0 mg/kg dan dalam peraturan pemerintah no. 82 tahun 2001 pada pasal 8 kandungan arsen yang diizinkan sebagai sumber baku air minum sebesar 0.05 mg/L. Arsen memiliki sifat racun dan dapat menghambat kerja metabolisme dalam tubuh. Dengan demikian, pendeteksian arsen sangat diperlukan untuk memonitor kualitas air di lingkungan.
Banyaknya bahaya kesehatan yang ditimbulkan oleh kontaminasi logam As memicu upaya penanganan yang lebih intensif mengenai bahaya tersebut sehingga diperlukan suatu metode pendeteksian yang cepat, akurat, dan lebih sensitif untuk menentukan kadar arsen pada limbah industri. Beberapa metode yang dikembangkan diantaranya teknik spektrometri (Luong et al. 2007), Hydride Generation Atomic Absorption Spectrometry (HGAAS) (Niedzielski et al. 1999), dan Carbon Nano Tubes (CNTs) (Daud et al. 2012). Namun metode-metode tersebut membutuhkan biaya yang mahal, prosedur yang kompleks, dan membutuhkan sampel khusus untuk mengidentifikasi kompleks warna atau logam toksik seperti arsen (Fajardo 2003 dalam Valle et al. 2013), metode ini juga tidak bisa untuk mengetahui secara langsung garam logam berat dan senyawa organik lainnya yang ada pada suatu limbah perairan. Untuk itu, metode elektrokimia dengan menggunakan elektrode biosensor berpotensi untuk dikembangkan dalam analisis rutin di lapangan.
2
konsentrasi logam arsen dalam sampel. Prinsip inhibisi aktivitas enzim sebelumnya sudah dilakukan pada pengontrolan kualitas makanan, pestisida, insektsida, dan logam berat (Mostafa 2010; Neujahr 1984; Han et al. 2000; Shang
et al. 2011). Sehingga, dalam penelitian ini dilakukan pengembangan metode pendeteksian logam berat dengan perangkat biosensor untuk analisis yang cepat, akurat, dan selektif.
Pengukuran inhibisi aktivitas enzim dilakukan menggunakan voltametri siklik dengan elektrode pasta karbon (EPK) yang terbuat dari grafit dan minyak mineral. EPK banyak digunakan dalam berbagai proses analisis, seperti voltametri, potensiometri, dan amperometri karena memiliki keunggulan mudah dimodifikasi, mudah dibuat, memiliki selang potensial yang cukup luas, arus latar belakang yang rendah, inert, dan cocok untuk berbagai aplikasi deteksi dan pengukuran (Taufik 2013). Berberapa penelitian yang menggunakan EPK adalah parameter kinetika biosensor antioksidan dengan enzim SOD Deinococcus radiodurans
(Trivadilla 2011), Pemanfaatan EPK untuk meningkatkan pengukuran sensor kimia (Zaidi 2013), sensor katekolamina dengan EPK termodifikasi Cu dan Ag (Sanghavi et al. 2013), dan biosensor asam urat dari Lactobacillus Plantarum
(Iswantini et al. 2013). Oleh karena itu, digunakan EPK sebagai elektrode yang ekonomis, mudah dibuat dan mudah dimodifikasi.
Enzim piruvat dehidrogenase (PDH) merupakan komponen pertama pada kompleks piruvat dehidrogenase yang berfungsi mengubah piruvat menjadi asetil-KoA. Enzim PDH berpotensi dikembangkan sebagai agen pengenal hayati logam arsen karena arsen dapat bertindak sebagai inhibitor bagi enzim PDH sehingga aktivitas yang ditimbulkan elektrode yang berbasis PDH berkurang jika terdapat logam arsen (Hughes 2002 dalam Rose 2013).
Untuk menghasilkan biosensor yang stabil dan memiliki kinerja yang baik, dilakukan pengembangan elektrode dengan sebuah matriks sebagai tempat imobilisasi enzim yaitu nanopartikel zeolit, terutama zeolit alam. Penggunaan zeolit sebagai matriks untuk immobilisasi enzim dapat meningkatkan respon arus yang dihasilkan (Balal 2009). Beberapa penelitian yang menggunakan zeolit alam diantaranya biosensor antioksidan (Trivadilla 2011), dan biosensor asam urat (Iswantini et al. 2009). Penggunaan nanopartikel zeolit ini dilakukan untuk meningkatkan luas permukaan dan kapasitas matriks pengimobilisasi, sehingga dihasilkan aktivitas enzim yang tinggi dan arus yang baik.
Penelitian ini menggunakan zeolit alam berukuran nano yang berasal dari Bayah dan dimodifikasi dengan besi sebagai matriks modifikasi EPK. Enzim PDH diimmobilisasi pada permukaan EPK sebagai bioreseptor logam As dengan basis inhibisi. Elektrode dikarakterisasi pada kinerja optimum yang dilihat dari pengaruh masa zeolit-Fe, konsentrasi PDH, pH, dan suhu. Kemudian dilihat pengaruh ion logam timbal (Pb) terhadap arus yang dihasilkan pada pengukuran As(III)
3
METODE
Alat dan Bahan
Bahan-bahan yang digunakan dalam penelitian ini adalah HCl (pH 2, 3 M, 0.2 M), K3[Fe(CN)6] 0.1 mM, FeCl3·6H2O 0.1 M, AgNO3 0.1 M, enzim PDH
(Sigma Aldrich, P7032), larutan substrat piruvat 2.1 mM, larutan stok As(III) 1000 ppb, larutan stok Pb 1000 ppb, larutan dapar fosfat pH 7, zeolit alam Bayah berukuran nano, grafit, dan parafin cair. Alat-alat yang digunakan dalam penelitian adalah kompartemen elektrode, mortar, nilon, membran dialisis, benang paranilon, pipet mikroliter, kertas minyak, gelas piala, AAS Shimadzu P-700, potensiostat/galvanostat eDAQ dan komputer yang telah dipasang program pengolah data Echem v.2.1.0 serta MINITAB 16.
Metode Penelitian
Pembuatan Zeolit Termodifikasi Besi (Balal et al. 2009)
Modifikasi zeolit dilakukan dengan memvariasikan konsentrasi FeCl3, yaitu
0.005, 0.01, 0.03, dan 0.05 M. Zeolit yang sudah diaktivasi sebanyak 1 g direndam dalam 250 mL FeCl3, kemudian diaduk dengan pengaduk magnetik
selama 48 jam. Zeolit selanjutnya disaring dan dicuci dengan air destilasi serta larutan HCl pH 2 sebanyak 3 kali ulangan untuk manghilangkan ion-ion klorida. Kemudian zeolit dikeringkan di dalam desikator hingga kering.
Penenetuan Kadar Fe pada Zeolit Termodifikasi-Besi (Agustina 2012)
Kadar Fe dalam zeolit ditentukan menggunakan AAS. Zeolit sebelum dan setelah dimodifikasi masing-masing ditimbang sebanyak 50 mg, kemudian ditambahkan 10 mL larutan HNO3 5 M dan didiamkan selama 1 jam. Selanjutnya
campuran disaring dan filtrat ditepatkan dengan labu takar menjadi 100 mL. Larutan selanjutnya diukur menggunakan AAS.
Pembuatan Elektrode Pasta Karbon (Balal et al. 2009)
Elektrode dipersiapkan dengan menggerus 55 mg serbuk grafit dengan 35 μL parafin cair di dalam mortar hingga didapatkan campuran yang rata. Kemudian zeolit yang telah termodifikasi Fe dicampurkan dengan grafit lalu ditambahkan 2 mL dietil eter. Campuran diaduk hingga pelarut menguap. Kawat tembaga yang berdiameter 3 mm dimasukkan ke dalam tabung kaca hingga tersisa ruang sepanjang 5 mm pada ujung tabung sebagai tempat pasta karbon. Pasta karbon yang sudah termodifikasi dimasukkan ke dalam elektrode hingga penuh dan padat. Kemudian diratakan dengan menggoreskannya pada kertas minyak.
Karakterisasi Elektrode Pasta Karbon (modifikasi Taufik 2013)
Elektrode yang sudah dibuat dikarakterisasi dengan mengukur respon elektrode dengan larutan K3[Fe(CN)6] 1 mM meggunakan teknik voltametri siklik,
4
Immobilisasi Enzim PDH (Ikeda et al. 1998).
Larutan enzim PDH dengan konsentrasi tertentu diteteskan pada permukaan elektrode pasta karbon, kemudian elektrode dikeringkan hingga pelarutnya menguap. Ujung elektrode ditutup dengan membran dialisis, jaring nilon, dan diikat dengan paranilon. Elektrode direndam dalam larutan penyangga fosfat dan dapat digunakan dalam pengukuran aktivitas PDH dengan metode elektrokimia.
Pengukuran Elektrokimia
Pengukuran elektrokimia dilakukan dengan metode voltametri siklik menggunakan eDAQ potensiostat (Ecorder 410) yang dilengkapi perangkat lunak
Echem v 2.1.0. Elektrode yang digunakan adalah elektrode Ag/AgCl, platina, dan PDH yang berturut-turut sebagai elektrode pembanding, elektrode pembantu (counter), dan elektrode kerja. Parameter pengukuran dibuat dengan mode cyclic,
initial E-100 mV, final E 100 mV, rate 125 mV/s, step W 20 ms upper, E 600 mV,
lower E 50 mV, range 5 V.
Larutan penyangga fosfat sebanyak 1.9 mL dan 100 µL larutan PDH ditambahkan ke dalam sel pengukuran. Puncak arus anode yang diamati ditetapkan sebagai blangko. Kemudian ditambahkan 1 mL substrat piruvat 2.1 mM dan diukur perubahan arus puncak anode. Selanjutnya 1 mL larutan arsen ditambahkan dan dilihat penurunan arus anode akibat penambahan arsen dengan konsentrasi tertentu.
Optimasi Aktivitas Enzim PDH
Optimasi yang dilakukan adalah suhu 20-30 °C, pH 6-8, dan konsentrasi PDH (0.0085-0.0198 U/mL). Metode yang digunakan untuk pengoptimumuan aktivitas PDH adalah Respon Surface Method. Metode ini dilakukan dengan cara memasukkan kombinasi faktor-faktor peubah bebas pada perangkat lunak statistik minitab. Setelah itu, percobaan dilakukan sesuai dengan kombinasi yang dihasilkan untuk mendapatkan nilai aktivitas optimum.
Pencirian Elektrode
Elektrode biosensor pada kondisi optimum dikarakterisasi dengan parameter Linearitas dan limit deteksi, stabilitas, uji keterulangan, dan koefisien selektivitas terhadap logam Pb.
Linearitas, Limit Deteksi (LOD), dan Limit Kuantisasi (LOQ)
Linearitas pengukuran diukur dengan mengukur respon arus terhadap konsentrasi ion arsenat (As2O3). Konsentrasi masing-masing yang digunakan
adalah 0.6, 1.25, 2.5, 5, 10, 15, 20, 30, dan 50 ppb. Data kemudian diplot dalam kurva dengan sumbu-x adalah konsentrasi ion arsenat dan respon arus (mA) pada sumbu-y. Ekstrapolasi garis akan memberikan linearitas, limit deteksi, dan kuantisasi.
Limit deteksi dan kuantisasi ditentukan dengan rumus berikut: LOD = 3 × σ analit
b LOQ =
5 Keterangan:
σanalit = simpangan baku respon analitik analit
b = kemiringan garis pada persamaan garis linear
Stabilitas
Kestabilan biosensor ditentukan dengan mengukur arus yang dihasilkan dalam pengukuran. Seluruh nilai aktivitas yang diperoleh pada pengukuran awal dianggap sebesar 100%. Aktivitas diukur kembali selama 3 hari dengan interval 1 hari. Persen aktivitas biosensor diukur dengan menggunakan rumus:
% Aktivitas = I saat hari ke-n (µA)
I saat awal (µA) × 100%
Uji Presisi
Presisi diukur sebagai simpangan baku atau simpangan baku relatif (koefisien variasi). Presisi dapat dinyatakan sebagai repeatability (keterulangan). Presisi ditentukan dengan menghitung simpangan baku (SD) dari pengujian 3 buah elektrode dan standar deviasi standar (%RSD) dihitung sebagai berikut:
%RSD = SD
X × 100%
Keterangan:
SD : Simpangan baku pengukuran X : Rata-rata pengukuran
Koefisien Selektivitas (Wahab 2006)
Penentuan koefisien selektivitas dilakukan dengan metode tercampur. Larutan arsen dengan konsenrasi terkecil diukur potensialnya. Selanjutnya pengukuran potensial juga dilakukan pada larutan campuran yang mengandung arsen konsentrasi terkecil dan ion pengganggu Pb2+ (0.6, 1, dan 1.25 ppb). Pengukuran dilakukan secara triplo. Koefisien selektivitas dihitung dengan menggunakan persamaan berikut:
Ki,j =
ai �10 E2-E1S �-1
aj
Keterangan:
Ki,j = Koefisiean selektivitas
ai = Konsentrasi ion utama (Arsen)
aj = Konsentrasi ion pengganggu
E1 = Potensial sel pengukuran ion As(III) (mV)
6
HASIL DAN PEMBAHASAN
Zeolit Termodifikasi-besi
Zeolit adalah suatu mineral aluminosilikat terhidrasi yang terdiri atas satuan tetrahedral SiO4 dan AlO4 dengan kerangka struktur berongga yang ditempati oleh
molekul-molekul air dan kation (Agustina 2012).
Beberapa atom Si pada zeolit jika digantikan oleh atom Al akan menghasilkan struktur zeolit yang bermuatan negatif. Hal ini berasal dari perbedaan muatan antara tetrahedron (AlO4)5- dan (SiO4)4-. Adanya perbedaan
muatan ini menyebabkan zeolit memiliki kemampuan yang rendah atau tidak memiliki daya jerap terhadap anion. Untuk meningkatkan karakter permukaan zeolit menjadi lebih positif sebagai tempat immobilisasi enzim, maka zeolit perlu dimodifikasi.
Pada penelitian ini, modifikasi zeolit dilakukan dengan kation besi (Fe3+)
dari larutan FeCl3. Hal ini dilakukan dengan prinsip penukaran kation logam pada
pori-pori zeolit. Menurut Hanafiah (2005) penukaran kation logam pada zeolit tidak akan mengubah struktur kristal tetrahedron zeolit, namun akan mengubah afinitas daya jerap zeolit.
Preparasi nanozeolit-Fe dilakukan dengan penjerapan nanozeolit teraktivasi dalam larutan FeCl3 selama 48 jam (Balal et al 2009). Nanozeolit yang sudah
diaktivasi direndam dengan larutan FeCl3 dengan konsentrasi yang divariasikan.
Setelah nanozeolit diaduk dan didiamkan dalam FeCl3 campuran disaring dan
diambil endapan nanozeolit. Endapan nanozeolit dicuci dengan HCl pH 2, dan kemudian dikeringkan agar didapatkan serbuk kering zeolit-Fe. Hasil modifikasi nanozeolit dengan besi berupa serbuk berwana kuning. Setelah nanozeolit dimodifikasi dengan penambahan ion Fe3+ diharapkan karakter nanozeolit menjadi lebih positif sehingga memudahkan interaksi dengan muatan negatif atau gugus elektronegatif yang terdapat pada enzim dan akan menguatkan interaksi antara enzim dengan permukaan elektrode, sehingga enzim tidak mudah terlepas dari permukaan elektrode.
Kadar Fe pada Zeolit Termodifikasi-Besi
Keberadaan kation besi maksimum pada zeolit termodifikasi dengan berbagai konsentrasi FeCl3 diidentifikasi menggunakan AAS. Sampel zeolit
sebelum dan sesudah modifikasi didestruksi dengan menggunakan HNO3 5 M
selama 1 jam dan kemudian filtrat dari sampel diukur. Kadar Fe dalam zeolit termodifikasi dengan variasi konsentrasi FeCl3 dibandingkan dengan kadar Fe
dalam zeolit yang belum dimodifikasi. Pada Lampiran 2 terlihat bahwa zeolit yang belum dimodifikasi mengandung sedikit ion Fe, yaitu sebesar 6.0292 ppm. Setelah zeolit dimodifikasi dengan FeCl3, kandungan ion Fe yang terdapat pada
zeolit naik secara signifikan.
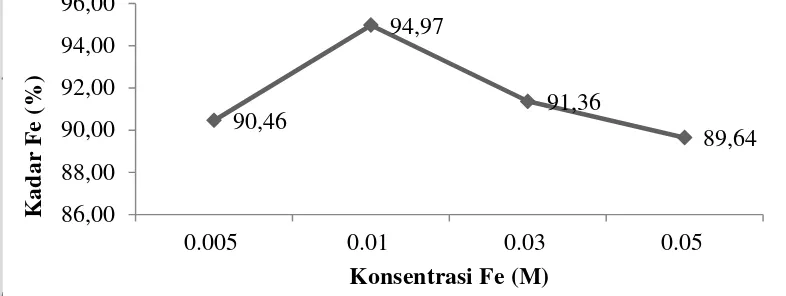
Pada Gambar 1 terlihat peningkatan kadar Fe pada zeolit setelah dimodifikasi dengan FeCl3. Pada konsentrasi 0.005 M FeCl3 penukaran kation
7 konsentrasi FeCl3 0.01 M terjadi proses penukaran kation maksimum hingga
94.97%. Namun, pada konsentrasi FeCl3 0.03 dan 0.05 M terlihat kadar Fe pada
zeolit turun hingga 91.36 dan 89.64%. Hal ini dapat disebabkan oleh proses penukaran kation logam pada pori-pori zeolit sudah melebihi titik maksimumnya yang terjadi pada konsentrasi 0.01 M. Kenaikan kadar Fe yang didapatkan pada FeCl3 0.01 M lebih kecil jika dibandingkan dengan hasil yang didapatkan oleh
Agustina (2012) yang melakukan modifikasi zeolit-Fe dengan mereaksikan Fe(NO3)3 dan NaOH, yaitu sebesar 95.6%, sehingga FeCl3 0.01 M digunakan
untuk pengujian selanjutnya karena menghasilkan bobot Fe yang tinggi dari 6.0292 menjadi 120.0237 ppm. Konsentrasi FeCl3 0.01 M yang digunakan ini
sama dengan yang digunakan oleh Balal (2009), namun dengan menggunakan zeolit sintetik NaY. Dan hal ini memperlihatkan bahwa modifikasi zeolit dengan kation besi berhasil dilakukan karena proses modifikasi zeolit dengan FeCl3
menghasilkan kadar Fe yang tinggi pada zeolit.
Gambar 1 Persentase kenaikan kadar Fe pada zeolit.
Pencirian Elektrode Pasta Karbon
Voltametri siklik adalah teknik yang digunakan untuk memperoleh informasi kualitatif mengenai reaksi elektrokimia dengan prinsip mengukur perubahan arus akibat reaksi redoks. Timbulnya arus disebabkan karena terjadi reaksi oksidasi dan reduksi pada permukaan elektrode dan sebanding dengan konsentrasi analit dalam larutan (Apriliani 2009). Sinyal berupa potensial diaplikasikan pada elektrode kerja, mengubah potensial relatif terhadap potensial tetap dari elektrode rujukan, kemudian arus yang dihasilkan antara elektrode kerja dan pembantu diukur (Harvey 2000).
Elektrode pasta karbon (EPK) dibuat dengan mencampurkan 55 mg grafit dengan 35 µL parafin cair. Kemudian dilakukan modifikasi EPK dengan menambahkan zeolit-Fe dengan variasi bobot 10-25 mg. Elektrode yang sudah dibuat dikarakterisasi dengan menggunakan K3Fe(CN)6 1 mM. Pada Gambar 2
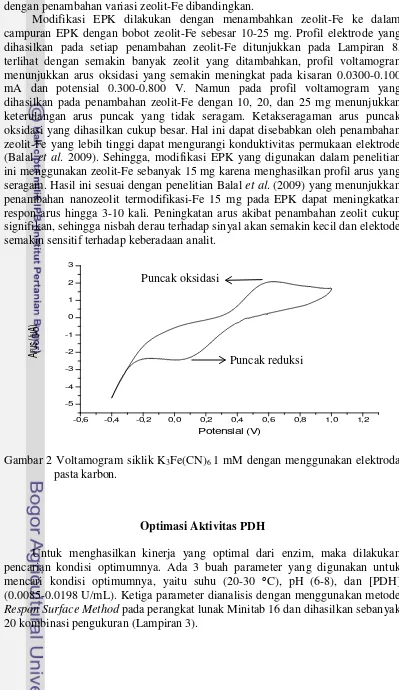
karakterisasi dengan menggunakan K3Fe(CN)6 menghasilkan puncak oksidasi dan
reduksi. Puncak oksidasi terjadi karena oksidasi larutan [Fe(CN)6]4- menjadi
[Fe(CN)6]3- pada potensial 0.5680 V dan arus 2.2010 µA dan puncak reduksi
terjadi karena larutan [Fe(CN) ]3- tereduksi menjadi [Fe(CN) ]4- pada potensial 90,46
0.005 0.01 0.03 0.05
8
0.2460 V dan arus 2.0900 µA. Selanjutnya respon arus yang dihasilkan EPK dengan penambahan variasi zeolit-Fe dibandingkan.
Modifikasi EPK dilakukan dengan menambahkan zeolit-Fe ke dalam campuran EPK dengan bobot zeolit-Fe sebesar 10-25 mg. Profil elektrode yang dihasilkan pada setiap penambahan zeolit-Fe ditunjukkan pada Lampiran 8, terlihat dengan semakin banyak zeolit yang ditambahkan, profil voltamogran menunjukkan arus oksidasi yang semakin meningkat pada kisaran 0.0300-0.100 mA dan potensial 0.300-0.800 V. Namun pada profil voltamogram yang dihasilkan pada penambahan zeolit-Fe dengan 10, 20, dan 25 mg menunjukkan keterulangan arus puncak yang tidak seragam. Ketakseragaman arus puncak oksidasi yang dihasilkan cukup besar. Hal ini dapat disebabkan oleh penambahan zeolit-Fe yang lebih tinggi dapat mengurangi konduktivitas permukaan elektrode (Balal et al. 2009). Sehingga, modifikasi EPK yang digunakan dalam penelitian ini menggunakan zeolit-Fe sebanyak 15 mg karena menghasilkan profil arus yang seragam. Hasil ini sesuai dengan penelitian Balal et al. (2009) yang menunjukkan penambahan nanozeolit termodifikasi-Fe 15 mg pada EPK dapat meningkatkan respon arus hingga 3-10 kali. Peningkatan arus akibat penambahan zeolit cukup signifikan, sehingga nisbah derau terhadap sinyal akan semakin kecil dan elektode semakin sensitif terhadap keberadaan analit.
Gambar 2 Voltamogram siklik K3Fe(CN)6 1 mM dengan menggunakan elektroda
pasta karbon.
Optimasi Aktivitas PDH
Untuk menghasilkan kinerja yang optimal dari enzim, maka dilakukan pencarian kondisi optimumnya. Ada 3 buah parameter yang digunakan untuk mencari kondisi optimumnya, yaitu suhu (20-30 ᵒC), pH (6-8), dan [PDH] (0.0085-0.0198 U/mL). Ketiga parameter dianalisis dengan menggunakan metode
Respon Surface Method pada perangkat lunak Minitab 16 dan dihasilkan sebanyak 20 kombinasi pengukuran (Lampiran 3).
9 Aktivitas enzim PDH ditentukan dengan menggunakan teknik voltametri siklik. Pengukuran dilakukan dengan mengukur larutan penyangga fosfat dan larutan PDH dengan konsentrasi terkecil yang ditetapkan sebagai blangko, kemudian ditambahkan substrat asam piruvat sesuai dengan kombinasi pengukuran. Pada Gambar 3 terlihat bahwa pada blangko terdapat puncak oksidasi dengan arus 0.0422 mA dan potensial -0.0980 V, puncak oksidasi timbul karena adanya penambahan larutan PDH dengan konsentrasi yang kecil pada blangko. Hal ini dilakukan agar di dalam analisis selanjutnya untuk menentukan puncak oksidasi dari PDH tidak sulit. Setelah ditambahkan substrat asam piruvat 2.1 mM terjadi kenaikan arus puncak oksidasi hingga 0.1064 mA dan ketika ditambahkan arsen dengan berbagai konsentrasi terjadi penurunan arus pucak oksidasi. Dengan semakin besar konsentrasi arsen yang ditambahkan maka arus puncak oksidasi akan semakin turun, yaitu pada rentang 0.1044-0.0656 mA dan rentang potensial 0.2600-0.4200 V. Penurunan arus puncak oksidasi ini terjadi karena arsen merupakan suatu inhibitor bagi enzim PDH (Hughes 2002 dalam Rose 2013), sehingga aktivitas yang ditimbulkan elektrode yang berbasis enzim PDH berkurang jika terdapat ion arsen.
Gambar 3 Voltamogram siklik pada suhu 33 ᵒC, pH 7, dan [PDH] 0.0141 U/mL. Respon arus yang dihasilkan dalam pengukuran 20 kombinasi dari 3 parameter (suhu, pH, dan [PDH]) (Lampiran 3) ditentukan kondisi optimumnya dengan menggunakan Response Optimizer pada perangkat lunak Minitab 16. Kondisi optimum aktivitas enzim PDH adalah suhu 33 ᵒC, pH 7, dan [PDH] 0.0141 U/mL, hal ini terlihat pada Gambar 4 yang menunjukkan plot kontur antara (a) suhu dan pH terhadap arus puncak oksidasi, (b) suhu dan [PDH] terhadap arus puncak oksidasi, serta (c) pH dan [PDH] terhadap arus puncak oksidasi. Ketiga plot menunjukkan aktivitas optimum dari enzim yang
10
Gambar 4a dan 4b menunjukkan pengaruh suhu terhadap aktivitas enzim PDH yang ditunjukkan dengan arus puncak oksidasi. Suhu yang terlalu tinggi dapat menyebabkan enzim terdenaturasi sehingga rusak dan tidak dapat berfungsi lagi, sedangkan suhu yang rendah dapat menyebabkan enzim tidak dapat bekerja dengan optimal. Aktivitas enzim PDH optimum pada suhu 33 ᵒC, namun pada rentang suhu 24-26 ᵒC juga dihasilkan arus yang cukup tinggi, sehingga biosensor arsen berpotensi untuk digunakan pada suhu ruang.
Gambar 4b dan 4c menunjukkan pengaruh [PDH], terlihat aktivitas enzim PDH menghasilkan arus yang tinggi pada rentang konsentrasi 0.0125-0.0157 U/mL. Dari gambar 4a dan 4c terlihat aktivitas PDH menghasilkan arus yang tinggi pada rentang pH 6.5-7.5 sehingga optimum pada pH 7. pH yang terlalu tinggi atau terlalu rendah dapat menyebabkan penurunan kinerja enzim yang berakibat pada penurunan arus pengukuran.
11
(c)
Gambar 4 (a) Plot kontur antara suhu dan pH, (b) suhu dan [PDH], (c) serta pH dan [PDH] terhadap puncak arus oksidasi aktivitas enzim PDH.
Pencirian Elektrode `
Linearitas, Limit Deteksi (LOD), dan Limit Kuantitatif (LOQ)
Linearitas, LOD, dan LOQ ditentukan dengan melakukan pengukuran aktivitas dari enzim PDH terhadap ion As (III) pada kondisi optimum suhu 33 ᵒC, pH 7, [PDH] 0.0141 U/mL, dengan menggunakan 1 elektrode dan 3 kali ulangan. Penentuan linearitas diperoleh dari grafik hubungan arus dan konsentrasi ion arsen (III).
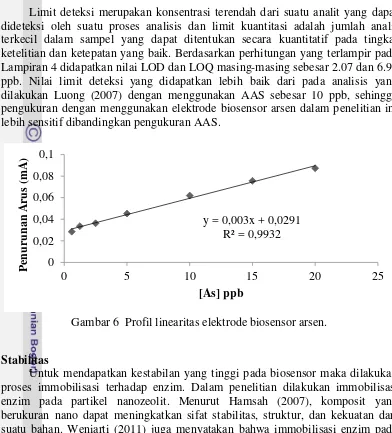
Pengukuran ion As(III) dilakukan pada rentang 0.6-50 ppb (Gambar 5). Pengukuran pada rentang ini bertujuan mengetahui linearitas, limit deteksi, dan limit kuantisasi biosensor arsen yang dibuat. Hasil pengukuran pada elektrode menunjukkan linearitas dari aktivitas enzim PDH terhadap ion As(III) pada rentang konsentrasi 0.6-20 ppb. Rentang linearitas yang dihasilkan cukup panjang sehingga didapatkan keakuratan dan nilai regresi linear yang tinggi, yaitu R2 = 0.9932. Dari persamaan garis y = 0.003x + 0.0291 ditentukan nilai limit deteksi dan limit kuantisasi pengukuran (Gambar 6).
12
Limit deteksi merupakan konsentrasi terendah dari suatu analit yang dapat dideteksi oleh suatu proses analisis dan limit kuantitasi adalah jumlah analit terkecil dalam sampel yang dapat ditentukan secara kuantitatif pada tingkat ketelitian dan ketepatan yang baik. Berdasarkan perhitungan yang terlampir pada Lampiran 4 didapatkan nilai LOD dan LOQ masing-masing sebesar 2.07 dan 6.90 ppb. Nilai limit deteksi yang didapatkan lebih baik dari pada analisis yang dilakukan Luong (2007) dengan menggunakan AAS sebesar 10 ppb, sehingga pengukuran dengan menggunakan elektrode biosensor arsen dalam penelitian ini lebih sensitif dibandingkan pengukuran AAS.
Gambar 6 Profil linearitas elektrode biosensor arsen.
Stabilitas
Untuk mendapatkan kestabilan yang tinggi pada biosensor maka dilakukan proses immobilisasi terhadap enzim. Dalam penelitian dilakukan immobilisasi enzim pada partikel nanozeolit. Menurut Hamsah (2007), komposit yang berukuran nano dapat meningkatkan sifat stabilitas, struktur, dan kekuatan dari suatu bahan. Weniarti (2011) juga menyatakan bahwa immobilisasi enzim pada zeolit akan membuat kestabilan enzim meningkat serta dapat digunakan kembali.
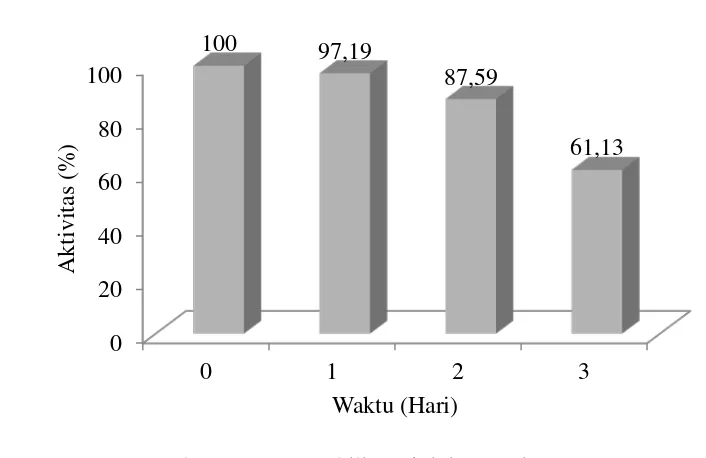
Pengukuran stabilitas aktivitas enzim PDH terhadap ion As(III) dilakukan pada kondisi optimum suhu 33 ᵒC, pH 7, dan [PDH] 0,0141 U/mL dengan waktu pengukuran selama 3 hari. Kurva stabilitas menunjukkan hubungan antara waktu pengukuran dengan aktivitas enzim PDH terhadap As (Gambar 7). Terlihat bahwa stabilitas dari elektrode biosensor arsen mengalami penurunan setiap hari. Pada hari pertama dan kedua stabilitas dari elektrode mengalami penurunan aktivitas yang tidak terlalu besar, namun pada hari ketiga terjadi penurunan aktivitas elektrode secara signifikan hingga mencapai 61.13%. Dari hasil stabilitas elektrode ini, dapat dikatakan bahwa pengukuran atau analisis dengan menggunakan biosensor arsen menghasilkan stabilitas yang cukup baik pada hari pertama dan kedua, sedangkan pada hari ketiga elektrode mempunyai kestabilan yang rendah. Sehingga kestabilan elektrode perlu untuk ditingkatkan.
13
Gambar 7 Kurva stabilitas aktivitas enzim PDH.
Uji presisi
Uji presisi merupakan uji yang digunakan untuk menentukan nilai keterulangan dari suatu elektrode. Keterulangan ditentukan dengan melihat aktivitas 3 buah elektrode yang diukur pada kondisi optimum dan pada konsentrasi ion As(III) 0.6 ppb. Keterulangan berfungsi untuk menentukan keakuratan dari suatu metode yang digunakan berdasarkan nilai standar deviasi (SD) dan standar deviasi relatif (%RSD). Pada Lampiran 6 dihasilkan SD dari pengukuran aktivitas enzim PDH terhadap ion As(III) sebesar 0,0132 dan %RSD sebesar 1.98%. Hasil ini dapat dikatakan bahwa keterulangan dari aktivitas 3 buah elektrode cukup baik karena dihasilkan %RSD yang lebih kecil dari 5% (Yashin 2011).
Selektivitas
Uji selektivitas dari elektrode pasta karbon termodifikasi partikel nanozeolit bertujuan mempelajari pengaruh adanya penambahan ion lain dalam analisis ion As(III). Ion logam pengganggu yang digunakan dalam uji selektivitas elektrode ini adalah ion Pb(II).
Pengaruh dari ion lain terhadap analisis ion As(III) dapat diketahui dengan melihat nilai koefisien selektivitas pengukuran yang dihasilkan. Koefisien selektivitas merupakan faktor yang dapat menurunkan selektivitas dari elektrode (Wahab 2006). Penentuan nilai koefisien selektivitas pada penelitian ini dilakukan dengan membandingkan potensial dari ion utama As(III) dan nilai potensial dari adanya ion pengganggu Pb(II). Sebelum dilakukan pengukuran terhadap ion pengganggu, diukur potensial dari ion utama As(III). Nilai koefisien selektivitas yang dihasilkan dapat dilihat pada Tabel 1.
14
Tabel 1 Koefisien selektivitas ion pengganggu Pb (II) terhadap ion utama As (III). [Pb]
ppb
Koefisien selektivitas (Ki,j)
0,6 -1,7332
1 -0,9904
1,25 -0,7121
Tabel 1 menunjukkan nilai koefisien selektivitas dari ion pengganggu Pb(II) dengan konsentrasi 0.6, 1, dan 1.25 ppb tidak mengganggu kinerja pengukuran elektrode terhadap ion As(III). Hal ini dapat disebabkan oleh nilai koefisien selktivitas yang kecil dari 1 (Wahab 2006). Namun, pada Tabel 1 terlihat bahwa nilai koefisien selektivitas dari ion Pb(II) semakin besar dengan bertambahnya konsentrasi ion pengganggu, sehingga ion Pb(II) akan dapat mengganggu selektivitas dari pengukuran jika berada dalam konsentrasi yang cukup besar.
SIMPULAN DAN SARAN
Simpulan
Elektrode biosensor arsen termodifikasi partikel nanozeolit-Fe menggunakan enzim PDH telah berhasil dibuat. Jumlah nanozeolit-Fe yang ditambahkan ke EPK menghasilkan profil arus yang seragam pada bobot 15 mg. Kinerja biosensor optimum pada pH larutan, suhu, dan konsentrasi enzim PDH sebesar 7.00, 33 ᵒC, dan 0.0141 U/mL. Linearitas pengukuran As dengan biosensor berada pada rentang 0.6-20 ppb. Nilai LOD dan LOQ yang dihasilkan dari pengukuran sebesar 2.07 dan 6.90 ppb. Nilai ini relatif lebih rendah dibanding LOD pengukuran menggunakan metode AAS. Stabilitas pengukuran elektrode cenderung turun setiap harinya sehingga pengukuran lebih baik dilakukan dengan kondisi enzim yang segar dan dihasilkan keterulangan dari aktivitas elektrode yang baik dengan nilai %RSD sebesar 1.98%. Keberadaan ion pengganggu Pb2+
dengan konsentrasi 0.6, 1.00, 1.25 ppb tidak memengaruhi aktivitas pengukuran dari aktivitas biosensor arsen.
Saran
15
DAFTAR PUSTAKA
Anetor I J, Wanibuchi H, dan Fukushima S.2007. Arsenic Exposure and its Health Effects and Risk of Cancer in Developing Countries: Micronutrients as Host Defence. Asian Pacific J Cancer Prev. (8):13-23.
Agustina R I. 2012. Pencirian Elektrode Pasta Karbon Termodifikasi Zeolit-Besi Sebagai Media Deteksi Kromium(VI) [Skripsi]. Bogor (ID). Institut Pertanian Bogor (IPB).
Apriliani R. 2009. Studi Penggunaan Kurkumin Sebagai Modifier Elektroda Pasta Karbon Untuk Analisis Timbal (II) Secara Stripping Voltametry [skripsi]. Surakarta (ID). Universitas Sebelas Maret (UNS).
Balal M, Mohammad H, Bahareh B, Ali B, Maryam H, Mozhgan Z. 2009. Zeolite nanoparticle modified carbon paste electrode as a biosensor for simultanous determination of dopamine and tryptophan. J Chin Chem Soc. 56(4):789-796.
Daud N, Yusof NA, Tee TW, Abdullah AH. 2012. Electrochemical Sensor for As(III) Utilizing CNTZs/leucine/nafion modifiede electrode. Int J Electrochem. 7:175-185.
Hamsah D. 2007. Pembuatan, pencirian, dan uji aplikasi nanokomposit berbasis montmorilonit dan besi oksida. [skripsi]. Bogor: FMIPA, IPB.
Hanafiah KA. 2005. Dasar-Dasar Ilmu Tanah. Jakarta (ID): PT Raja Grafindo Persada.
Han S, Zhu M, Yuan Z, Li X. 2000. A methylene blue-mediated enzyme electrode for the determination of trace mercury(II), mercury(I), methylmercury, and mercury–glutathione complex. Biosensors & Bioelectronics. 16:9-16.
Harvey D. 2000. Modern Analytical Chemistry. Singapore: Mc-Graw Hill.
Ikeda et al. 1998. Electrochemical Monitoring of in vivo Reconstruction of Glucose Dehydrogenase in Escherichia coli Cells With Externally Added Pyrroloquinoline. J Electroanal Chem. 449:219-224.
Iswantini D, Nurhidayat N, Trivadilla, Widiyatmoko O. 2013. Activity and Stability of Uricase from Lactobacillus Plantarum Immobilizated on Natural Zeolite for Uric Acid Biosensor. Pak J Biol Sci. ISSN 1028-8880.doi: 10.3923/pjbs. 2013.
Luong J H T, Majid E, Male K B. 2007. Analytical Tools for Monitoring Arsenic in the Environment. The Open Analytical Chemistry Journal. 1:7-14.
Méndez S S, Renedo O D, dan Martínez M J A. 2010. Immobilization of Acetylcholinesterase on Screen-Printed Electrodes. Application to the Determination of Arsenic(III). Sensors. 10: 2119-2128.
Mostafa G A E. 2010. Electrochemical Biosensors for the Detection of Pesticides.
The Open Electrochemistry Journal. 2:22-42.
Neujahr H Y. 1984. Biosensor for Environmental Control. Biotechnology and Genetic Engineering Reviews. 1:167-186.
Niedzielski P, Siepak J, Kowalczuk Z. 1999. Speciation of Analysis of Arsenic, Antimony, and Selenium in the Surface Waters of Poznari. Polish Journal of Environmental Studies. 8(3):183-187.
16
Sanghavi BJ, Mobin SM, Mathur P, Lahiri GK, Srivastava AK. 2013. Biomimetic sensor for certain catecholamines employing copper(II) complex and silver nanoparticle modified glassy carbon paste electrode. Biosensors and Bioelectronics 39(1):124-132.
Shang Z, Xu Y, Gu Y, Wang Y, Wei D, Zhan L. 2011. A Rapid Detection of Pesticide Recidue Based on Piezoelectric Biosensor. Procedia Engineering. 15:4480-4485.
Shen S, Xing F L, William R, Weinfeld M, dan Chris L. 2013. Arsenic Binding to Proteins. Chem. Rev 113:7769-7792.
Taufik M. 2013. Analisis Cu(II) pada bawang dayak (Eleutherine palmifolia (L.) Merr.) menggunakan elektrode pasta karbon termodifikasi kuersetin. [Skripsi]. Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor. Bogor.
Trivadilla. 2011. Biosensor antioksidan menggunakan superoksida dismutase
Deinococcus radiodurans yang diimobilisasi pada permukaan elektrode pasta karbon dan parameter kinetikanya [Tesis]. Sekolah Pascasarjana,Institut Pertanian Bogor. Bogor.
Valle M A D, et al. 2013. Use of a polymer modified electrode for arsenic determination. International of Science. 2:27-39.
Wahab W A. 2006. Pegaruh Komposisi Membran Berbasis PVC dan Ion Pengganggu Zn (II), Cd(II), dan Pb(II) Terhadap Elektrode Selektif Ion (ESI)-Hg(II) Menggunakan Ionofor DBA218C6. Ind J Chem. 6(1):27-31.
Weniarti. 2011. Biosensor antioksidan berbasis superoksida dismutase
Deinoccocus radiodurans diimobilisasi pada nanokomposit zeolit alam Indonesia [tesis]. Bogor (ID) : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Yashin A, Yashin Y, Nemzer B. 2011. Determination of Antioxidant Activity in Tea Extracts, and Their Total Antioxidant Content. Am J Biomed Sci. 3(4):322-335.
17 Lampiran 1 Bagan alir penelitian.
Nanozeolit
Zeolit termodifikasi
Fe3+ ECP
Grafit + parafin
Campuran grafit+parafin
Pengukuran elektrode
ECP
Biosensor Arsen
1. Linearitas, LOD, dan LOQ 2. Stabilitas
3. Uji presisi
4. Koefisien selektivitas 250 mL FeCl3 0.01 M
Imobilisasi enzim PHD
Optimalisasi aktivitas enzim PDH
18
Lampiran 2 Hasil analisis kadar Fe pada zeolit termodifikasi-besi menggunakan AAS
a. Kurva standar untuk penentuan kadar Fe
Konsentrasi Absorbans Absorbans terkoreksi
standar (ppm)
1 0,0646 0,0000
2 0,1055 0,0409
4 0,1861 0,1215
8 0,3433 0,2787
b. Kadar Fe dalam zeolit termodifikasi-besi Sampel Absorbansi Kadar Fe
Keterangan: ZA = Nanozeolit alami, ZB = Zeolit termodifikasi-besi Contoh perhitungan:
Kadar Fe sebenarnya = ppm kurva ×Volume contoh ×fp
bobot sampel (g)
Kadar Fe sebenarnya = 3.1292 ppm ×0.1 L ×1
0.0519 g = 6.0292 ppm
% peningkatan kadar Fe = Kadar Fe ZB-Kadar Fe ZA
19 = 120.0237 ppm-6.0292 ppm
120.0237 ppm × 100% = 94,97%
Lampiran 3 Optimasi suhu, pH, konsentrasi PDH, dan arus yang dihasilkan.
Suhu pH [PDH] Arus
25,00 7,00 0,0142 0,0045
30,00 8,00 0,0198 -0,0068
25,00 7,00 0,0142 0,0100
25,00 7,00 0,0046 -0,0040
20,00 6,00 0,0085 -0,0027
25,00 7,00 0,0142 0,0011
25,00 5,32 0,0142 -0,0019
25,00 7,00 0,0142 0,0010
20,00 6,00 0,0198 -0,0361
30,00 6,00 0,0198 -0,0072
25,00 7,00 0,0142 0,0034
33,41 7,00 0,0142 0,0131
20,00 8,00 0,0198 -0,0184
25,00 7,00 0,0142 0,0058
30,00 6,00 0,0085 -0,0038
25,00 8,68 0,0142 -0,0078
25,00 7,00 0,0237 -0,0018
30,00 8,00 0,0085 -0,0165
16,59 7,00 0,0142 -0,0012
20,00 8,00 0,0085 -0,0579
Lampiran 4 Nilai LOD dan LOQ dari pengukuran aktivitas biosensor arsen. [As]
20
Contoh perhitungan:
Yi dari persamaan garis y = 0,003x + 0,0291
• Untuk X = 0.6 ppb, maka y = 0.003 (0.6) + 0.0291 = 0.0309
• S2 = ∑�Ȳi-Yi�2
N-2
= 2.15E-05
5 = 4.30E-06
• SD = √4.30E-06 = 2.07E-03
• LOD = 3 SD b⁄
= 3. 2.07E-03 0.003⁄ = 2.07 ppb • LOQ = 10 SD b⁄
= 10. 2.07E-03 0.003⁄ = 6.9 ppb
Lampiran 5 Stabilitas biosensor arsen pada suhu 33 ᵒC, pH 7, dan [PDH] 0.0141 U/mL.
Hari ke-
Persen (%)
Arus total (mA)
0 100 0,8214
1 97,19 0,7984
2 87,59 0,7195
3 61,13 0,5022
Lampiran 6 Keterulangan arus puncak oksidasi dari 3 elektrode. Elektrode Aktivitas
21 Contoh perhitungan:
%RSD = SD
Rerata × 100%
= 0.0132
0.0262 × 100% = 1.9848
Lampiran 7 Nilai koefisien selektivitas biosensor arsen(III) terhadap ion Pb(II). [As]
ppb [Pb] ppb
E rata-rata
(mV) dE (mV) ai aj dE/s Ki,j
0,6 0 1,79E-04 0 0,6 0 0
-0,6 0,6 1,59E-04 -2,00E-05 0,6 0,6 -6,66E-03 -1,7332 0,6 1 1,84E-04 5,00E-06 0,6 1 1,66E-03 -0,9904 0,6 1,25 2,34E-04 5,50E-05 0,6 1,25 0,0183 -0,7121 Contoh Perhitungan:
Pada konsentrasi As 0.6 ppb dan Pb 0.6 ppb • dE = E2-E1
= 1,59E-04 - 1,79E-04 = -2,00E-05 • dE/s = −2,00E−05
0.003 = -6,66E-03
• Ki,j =
ai �10 E2-E1S �-1
aj
= 0.6�10
-2,00E-05 0.003 �-1
0.6
22
Lampiran 8 Profil hasil pemayaran EPK termodifikasi zeolit-Fe dengan K3[Fe(CN)6] 1 mM
1 Profil voltamogram EPK termodifikasi zeolit-Fe 10 mg
2 Profil voltamogram EPK termodifikasi zeolit-Fe 15 mg
23
3 Profil voltamogram EPK termodifikasi zeolit-Fe 20 mg
4 Profil voltamogram EPK termodifikasi zeolit-Fe 25 mg
24
RIWAYAT HIDUP
Penulis dilahirkan di Pekanbaru pada tanggal 2 Januari 1993 dari pasangan Khaidir dan Riauwati. Penulis adalah anak kedua dari tiga bersaudara. Tahun 2010 penulis lulus dari Sekolah Menengah Atas Negeri (SMAN) 1 Lintau Buo Utara dan melanjutkan studi di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor melalui jalur ujian Seleksi Nasional Masuk Perguruan Tinggi Nasional (SNMPTN).
![Gambar 3 Voltamogram siklik pada suhu 33 ᵒC, pH 7, dan [PDH] 0.0141 U/mL.](https://thumb-ap.123doks.com/thumbv2/123dok/403732.418762/23.595.115.494.349.573/gambar-voltamogram-siklik-pada-suhu-c-dan-pdh.webp)
![Gambar 4b dan 4c menunjukkan pengaruh [PDH], terlihat aktivitas enzim](https://thumb-ap.123doks.com/thumbv2/123dok/403732.418762/24.595.95.449.203.811/gambar-dan-menunjukkan-pengaruh-pdh-terlihat-aktivitas-enzim.webp)
![Gambar 4 (a) Plot kontur antara suhu dan pH, (b) suhu dan [PDH], (c) serta pH](https://thumb-ap.123doks.com/thumbv2/123dok/403732.418762/25.595.113.512.62.569/gambar-plot-kontur-antara-suhu-suhu-pdh-serta.webp)