PEMANFAATAN SERBUK KAYU
UNTUK PRODUKSI ETANOL
DENNY IRAWATI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ABSTRAK
DENNY IRAWATI. Pemanfaatan Serbuk Kayu Untuk Produksi Etanol. Dibimbing oleh NORMAN RAZIEF AZW AR, WASRIN SYAFII dan I MADE ARTIKA.
Saat ini di Indonesia tengah terjadi krisis bahan bakar minyak. Salah satu jenis bahan bakar alternatif adalah bioetanol. Bioetanol dapat diproduksi dari berbagai bahan lignoselulosa. Dilain pihak, pada tahun 2003, produksi log Indonesia adalah mencapai 10.086.217,06 m3, dengan jumlah limbah industri perkayuan diperkirakan sekitar 3,03-4,03 juta m3 untuk tahun 2003. Proses pengolahan serbuk kayu menjadi bioetanol dapat dilakukan dengan menggunakan metode sakarifikasi-fermentasi secara simultan. Kendala yang dihadapi dalam hidrolisis serbuk kayu dengan cara enzimatis yang menyebabkan rendahnya laju hidrolisis, salah satunya adalah adanya kandungan lignin dalam serbuk kayu tersebut. Oleh karena itu perlu dilakukan penelitian mengenai perlakuan delignifikasi atau penghilangan lignin dari serbuk kayu sebelum perlakuan sakarifikasi-fermentasi simultan untuk meningkatkan kemampuan hidrolisis dari enzim.
Penelitian ini dilakukan dengan menyerangkan jamur pelapuk putih yaitu
Phanerochaete chrysosporium pada 3 jenis serbuk kayu yaitu jati, meranti dan sengon. Sebelum dan sesudah didegradasi ligninnya menggunakan jamur P. chrysosporium, ketiga jenis serbuk kayu tersebut dianalisis terlebih dahulu kandungan kimianya (ekstraktif, selulosa, holoselulosa, abu dan lignin). Selanjutnya dilakukan proses sakarifikasi-fermentasi secara simultan menggunakan enzim kasar dari Trichoderma viride dan Saccharomyces cerevisiae pada shaker inkubator dengan kecepatan 12 rpm pada suhu 30OC selama 72 jam. Hasilnya berupa etanol dianalisis menggunakan metode kromatografi gas. Rancangan analisis yang digunakan adalah Rancangan Acak Lengkap, menggunakan dua faktor perlakuan, yaitu : jenis kayu (A) dan waktu inkubasi (B).
ABSTRACT
DENNY IRAWATI. The Utilization of Sawdust for Ethanol Production. Under the direction of NORMAN RAZIEF AZWAR, WASRIN SYAFII and I MADE ARTIKA.
Currently, Indonesia is in the middle of petroleum crisis. One of the alternative fuels which can be used as a petroleum substitute is ethanol. Ethanol can be produced from the timber waste (sawdust). Indonesia, in 2003, had timber waste potency of about 3 – 4 millions m3. Process of sawdust manufacturing become an ethanol can be conducted by simultaneous saccharification-fermentation method. However, ethanol production from sawdust has problem due to its lignin content. Therefore, research on bio-delignification treatment of sawdust prior to ethanol making process is required.
The research was done by acted of growing white rot fungi Phanerochaete chrysosporium on three kinds of sawdust i.e. jati, meranti and sengon. The chemical contents (extractive contents, cellulose contents, holocellulose contents, ash contents and lignin contents) of these three of sawdust were analyzed previously. Then simultaneous saccharification-fermentation (SSF) process was done by using crude enzyme from Trichoderma viride and then followed by fermentation with Saccharomyces cerevisiae on shaker incubator with rate 12 rpm at temperature 30oC for 72 hours. The result as an ethanol was analyzed by using gas chromatography method. Analysis design used was completely randomized design using 2 factors of treatment i.e. type of wood (A) and time of incubation (B).
PEMANFAATAN SERBUK KAYU
UNTUK PRODUKSI ETANOL
DENNY IRAWATI
Tesis
Sebagai Salah Satu Syarat Memperoleh Gelar
Magister Sains
Pada
Departemen Biokomia
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis
: Pemanfaatan Serbuk Kayu Untuk Produksi Etanol.
Nama
: Denny Irawati
NRP
: G. 451040011
PS
: Biokimia (BIK)
Disetujui,
Komisi Pembimbing
Prof.Dr.H. Norman Razief Azwar
Ketua
Prof.Dr.Ir. Wasrin Syafii, M.Agr
Dr.Ir. I Made Artika, MApp.Sc
Anggota
Anggota
Diketahui,
Ketua Program Studi S2 Biokimia
Prof.Dr.drh.Maria Bintang, MS
Tanggal Ujian: 22 Agustus 2006 Tanggal Lulus:
Dekan Sekolah Pascasarjana
PRAKATA
Puji syukur ke hadirat Allah swt atas limpahan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini dengan judul Pemanfaatan Serbuk Kayu Untuk Produksi Etanol. Penelitian dilaksanakan dari bulan November 2005 hingga bulan Mei 2006. Karya ilmiah ini disusun guna memenuhi salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Biokimia, Sekolah Pascasarjana, Institut Pertanian Bogor.
Pada kesempatan penulis mengucapkan terima kasih kepada :
1. Bapak Prof.Dr.H.Norman Razief Azwar,M.Sc., Prof.Dr.Ir. Wasrin Syafii,M.Agr. dan Dr.Ir. I Made Artika,Mapp.Sc. sebagai pembimbing dalam penulisan karya ilmiah ini.
2. Teknisi laboratorium Fermentasi Departemen Biokimia, laboratorium Kimia Kayu Jurusan Teknologi Hasil Hutan, Institut Pertanian Bogor, laboratorium Bioteknologi Hutan Jurusan Budidaya Hutan, laboratorium Kimia dan Serat Kayu Jurusan Teknologi Hasil Hutan, Fakultas Kehutanan, Universitas Gadjah Mada atas segala bantuan yang telah diberikan selama pelaksanaan penelitian.
3. Serta semua pihak yang tidak dapat disebutkan satu per satu yang telah berperan dalam proses penulisan karya ilmiah ini.
Disadari sepenuhnya bahwa karya ilmiah ini masih jauh dari sempurna, oleh karena karena itu kritik dan saran yang membangun sangat penulis harapkan. Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Agustus 2006
RIWAYAT HIDUP
Penulis dilahirkan di Cilacap pada tanggal 12 Juli 1978 dari ayah Pudjianto
dan ibu Muryati. Penulis merupakan anak ke tiga dari lima bersaudara. Tahun
1996 penulis lulus dari SMA Negeri 1 Cilacap dan pada tahun yang sama
diterima sebagai mahasiswa jurusan Teknologi Hasil Hutan, Fakultas Kehutanan,
Universitas Gadjah Mada, Jogjakarta.
Sejak tahun 2002 hingga sekarang penulis menjadi staf pengajar di jurusan
Teknologi Hasil Hutan, Fakultas Kehutanan, Universitas Gadjah Mada. Pada
tahun 2004 penulis mengikuti pendidikan program Magister pada Program Studi
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ………. x
DAFTAR LAMPIRAN ……….. xi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 5
Karakteristik Bahan Baku ... 5
Kimia Kayu ... 7
Jamur Phanerochaete chrysosporium Burdsall ... 15
Reaksi Degradasi Lignin Oleh Jamur ... 17
Kapang Trichoderma viride Person and Fries... 20
Yeast Saccharomyces cerevisiae Meyen ex Hansen ………. 21
Sakarifikasi Fermentasi Simultan ..……….. 22
BAHAN DAN METODE ... 25
Waktu dan Tempat ... 25
Bahan dan Alat ... 25
Prosedur Pelaksanaan ... 26
Analisis Hasil ... 34
HASIL DAN PEMBAHASAN ... 35
Pertumbuhan Jamur Phanerochaete chrysosporium Burdsall ... 35
Kandungan Kimia Kayu ... 37
Aktivtas Enzim ... 52
Kadar Etanol ... 54
SIMPULAN ... 58
DAFTAR PUSTAKA ... 60
DAFTAR TABEL
Halaman Tabel 1. Nilai rata-rata kadar ekstraktif, kadar abu dan kadar lignin
kayu (%) ... 37
Tabel 2. Nilai rata-rata kandar holoselulosa, kadar hemiselulosa, dan
kadar selulosa kayu (%) …………..……… 38
Tabel 3. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi terhadap kadar ekstraktif serbuk kayu ...
42
Tabel 4. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar abu serbuk kayu ... 43
Tabel 5. Hasil uji BNJ faktor waktu inkubasi terhadap kadar
holoselulosa serbuk kayu ... 45
Tabel 6. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar selulosa serbuk kayu ... 46
Tabel 7. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar hemiselulosa serbuk kayu ... 48
Tabel 8. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar lignin serbuk kayu ... 51
Tabel 9. Nilai rata-rata kadar etanol (g/l) dan (g/g) ... 53
Tabel 10. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
DAFTAR GAMBAR
Halaman Gambar 1. Skema dinding sel kayu dan hubungan lignin, selulosa
dan hemiselulosa dalam dinding sekunder ... 7
Gambar 2. A. Struktur selulosa dengan pengulangan unit selobiosa.
B. Selulosa kristalin ... 8
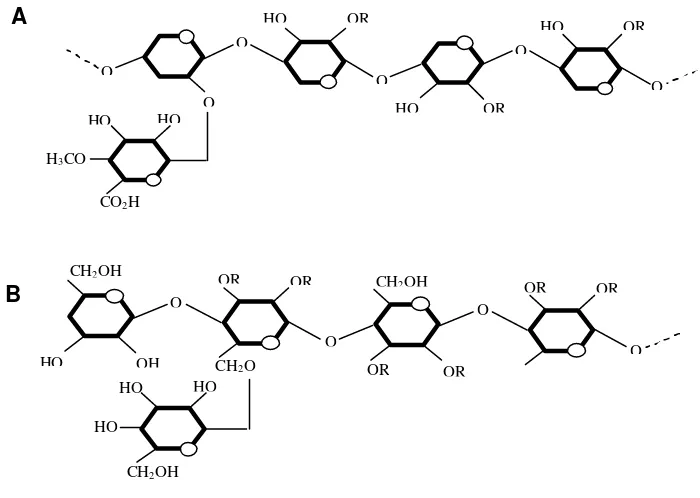
Gambar 3. A. Struktur O-asetil-4-O-metilglukoronoksilan(hemiselulosa utama di kayu daun lebar). B. Struktur O-aselilgalakto
glukomanan (hemiselulosa utama pada kayu daun jarum) . 10
Gambar 4. Model struktur lignin ……….. 11
Gambar 5. Struktur kimia 3 subunit penyusun lignin ... 12
Gambar 6. Ikatan ß-aryl ether pada lignin kayu ... 12
Gambar 7. A. Penggabungan materi lignoselulosa membentuk serat elentari dan mikrofibril. B. Struktur ikatan ester antara lignin dengan arabino-4-O-methilglucomonoxylan pada
Pinus ... 14
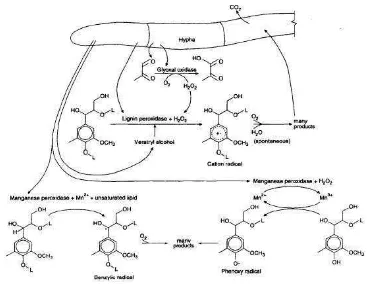
Gambar 8. Skema penyerangan lignin oleh enzim jamur
Phanerochaete chrysosporium ... 17
Gambar 9. Skema lignolitik dari jamur pembusuk putih ……….. 18
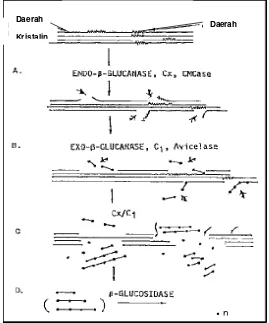
Gambar 10. Mekanisme hidrolisis enzim selulase ... 24
Gambar 11. Isolat P. chrysosporium umur 6 hari pada media PDA ….... 35
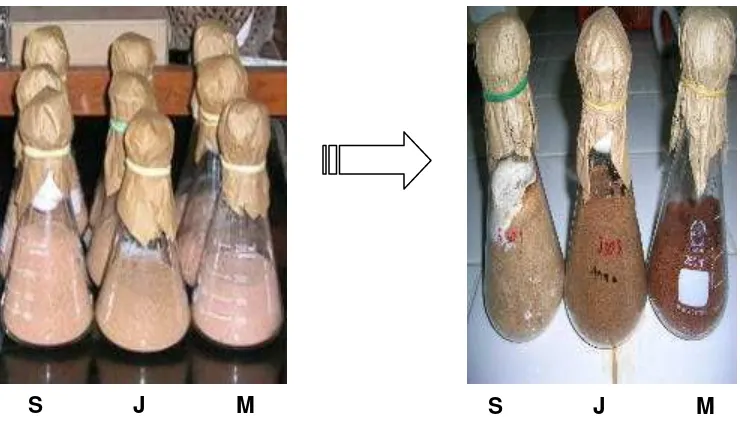
Gambar 12. Kondisi serbuk kayu sebelum diberi perlakuan jamur dan setelah 30 hari waktu inkubasi dengan jamur
P.chrysosporium ………. 36
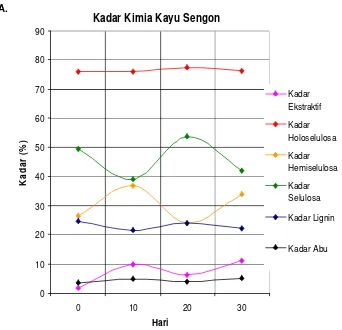
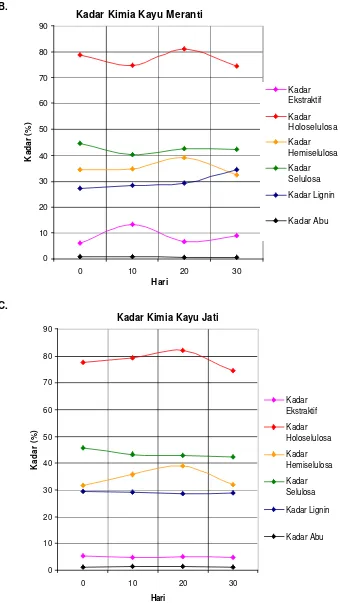
Gambar 13. A. Histogram kadar kimia kayu serbuk kayu sengon. B. Histogram kadar kimia kayu serbuk kayu meranti. C. Histogram kadar kimia kayu serbuk kayu jati ... 39
Gambar 14. A. Isolat T.viride umur 5 hari. B. Spora pada suspensi 10
ml aquades ... 51
Gambar 15. Histogram kadar etanol dari serbuk kayu... 54
PEMANFAATAN SERBUK KAYU
UNTUK PRODUKSI ETANOL
DENNY IRAWATI
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
ABSTRAK
DENNY IRAWATI. Pemanfaatan Serbuk Kayu Untuk Produksi Etanol. Dibimbing oleh NORMAN RAZIEF AZW AR, WASRIN SYAFII dan I MADE ARTIKA.
Saat ini di Indonesia tengah terjadi krisis bahan bakar minyak. Salah satu jenis bahan bakar alternatif adalah bioetanol. Bioetanol dapat diproduksi dari berbagai bahan lignoselulosa. Dilain pihak, pada tahun 2003, produksi log Indonesia adalah mencapai 10.086.217,06 m3, dengan jumlah limbah industri perkayuan diperkirakan sekitar 3,03-4,03 juta m3 untuk tahun 2003. Proses pengolahan serbuk kayu menjadi bioetanol dapat dilakukan dengan menggunakan metode sakarifikasi-fermentasi secara simultan. Kendala yang dihadapi dalam hidrolisis serbuk kayu dengan cara enzimatis yang menyebabkan rendahnya laju hidrolisis, salah satunya adalah adanya kandungan lignin dalam serbuk kayu tersebut. Oleh karena itu perlu dilakukan penelitian mengenai perlakuan delignifikasi atau penghilangan lignin dari serbuk kayu sebelum perlakuan sakarifikasi-fermentasi simultan untuk meningkatkan kemampuan hidrolisis dari enzim.
Penelitian ini dilakukan dengan menyerangkan jamur pelapuk putih yaitu
Phanerochaete chrysosporium pada 3 jenis serbuk kayu yaitu jati, meranti dan sengon. Sebelum dan sesudah didegradasi ligninnya menggunakan jamur P. chrysosporium, ketiga jenis serbuk kayu tersebut dianalisis terlebih dahulu kandungan kimianya (ekstraktif, selulosa, holoselulosa, abu dan lignin). Selanjutnya dilakukan proses sakarifikasi-fermentasi secara simultan menggunakan enzim kasar dari Trichoderma viride dan Saccharomyces cerevisiae pada shaker inkubator dengan kecepatan 12 rpm pada suhu 30OC selama 72 jam. Hasilnya berupa etanol dianalisis menggunakan metode kromatografi gas. Rancangan analisis yang digunakan adalah Rancangan Acak Lengkap, menggunakan dua faktor perlakuan, yaitu : jenis kayu (A) dan waktu inkubasi (B).
ABSTRACT
DENNY IRAWATI. The Utilization of Sawdust for Ethanol Production. Under the direction of NORMAN RAZIEF AZWAR, WASRIN SYAFII and I MADE ARTIKA.
Currently, Indonesia is in the middle of petroleum crisis. One of the alternative fuels which can be used as a petroleum substitute is ethanol. Ethanol can be produced from the timber waste (sawdust). Indonesia, in 2003, had timber waste potency of about 3 – 4 millions m3. Process of sawdust manufacturing become an ethanol can be conducted by simultaneous saccharification-fermentation method. However, ethanol production from sawdust has problem due to its lignin content. Therefore, research on bio-delignification treatment of sawdust prior to ethanol making process is required.
The research was done by acted of growing white rot fungi Phanerochaete chrysosporium on three kinds of sawdust i.e. jati, meranti and sengon. The chemical contents (extractive contents, cellulose contents, holocellulose contents, ash contents and lignin contents) of these three of sawdust were analyzed previously. Then simultaneous saccharification-fermentation (SSF) process was done by using crude enzyme from Trichoderma viride and then followed by fermentation with Saccharomyces cerevisiae on shaker incubator with rate 12 rpm at temperature 30oC for 72 hours. The result as an ethanol was analyzed by using gas chromatography method. Analysis design used was completely randomized design using 2 factors of treatment i.e. type of wood (A) and time of incubation (B).
PEMANFAATAN SERBUK KAYU
UNTUK PRODUKSI ETANOL
DENNY IRAWATI
Tesis
Sebagai Salah Satu Syarat Memperoleh Gelar
Magister Sains
Pada
Departemen Biokomia
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Judul Tesis
: Pemanfaatan Serbuk Kayu Untuk Produksi Etanol.
Nama
: Denny Irawati
NRP
: G. 451040011
PS
: Biokimia (BIK)
Disetujui,
Komisi Pembimbing
Prof.Dr.H. Norman Razief Azwar
Ketua
Prof.Dr.Ir. Wasrin Syafii, M.Agr
Dr.Ir. I Made Artika, MApp.Sc
Anggota
Anggota
Diketahui,
Ketua Program Studi S2 Biokimia
Prof.Dr.drh.Maria Bintang, MS
Tanggal Ujian: 22 Agustus 2006 Tanggal Lulus:
Dekan Sekolah Pascasarjana
PRAKATA
Puji syukur ke hadirat Allah swt atas limpahan rahmat dan hidayah-Nya sehingga penulis dapat menyelesaikan karya ilmiah ini dengan judul Pemanfaatan Serbuk Kayu Untuk Produksi Etanol. Penelitian dilaksanakan dari bulan November 2005 hingga bulan Mei 2006. Karya ilmiah ini disusun guna memenuhi salah satu syarat untuk memperoleh gelar Magister Sains pada Program Studi Biokimia, Sekolah Pascasarjana, Institut Pertanian Bogor.
Pada kesempatan penulis mengucapkan terima kasih kepada :
1. Bapak Prof.Dr.H.Norman Razief Azwar,M.Sc., Prof.Dr.Ir. Wasrin Syafii,M.Agr. dan Dr.Ir. I Made Artika,Mapp.Sc. sebagai pembimbing dalam penulisan karya ilmiah ini.
2. Teknisi laboratorium Fermentasi Departemen Biokimia, laboratorium Kimia Kayu Jurusan Teknologi Hasil Hutan, Institut Pertanian Bogor, laboratorium Bioteknologi Hutan Jurusan Budidaya Hutan, laboratorium Kimia dan Serat Kayu Jurusan Teknologi Hasil Hutan, Fakultas Kehutanan, Universitas Gadjah Mada atas segala bantuan yang telah diberikan selama pelaksanaan penelitian.
3. Serta semua pihak yang tidak dapat disebutkan satu per satu yang telah berperan dalam proses penulisan karya ilmiah ini.
Disadari sepenuhnya bahwa karya ilmiah ini masih jauh dari sempurna, oleh karena karena itu kritik dan saran yang membangun sangat penulis harapkan. Semoga karya ilmiah ini dapat bermanfaat.
Bogor, Agustus 2006
RIWAYAT HIDUP
Penulis dilahirkan di Cilacap pada tanggal 12 Juli 1978 dari ayah Pudjianto
dan ibu Muryati. Penulis merupakan anak ke tiga dari lima bersaudara. Tahun
1996 penulis lulus dari SMA Negeri 1 Cilacap dan pada tahun yang sama
diterima sebagai mahasiswa jurusan Teknologi Hasil Hutan, Fakultas Kehutanan,
Universitas Gadjah Mada, Jogjakarta.
Sejak tahun 2002 hingga sekarang penulis menjadi staf pengajar di jurusan
Teknologi Hasil Hutan, Fakultas Kehutanan, Universitas Gadjah Mada. Pada
tahun 2004 penulis mengikuti pendidikan program Magister pada Program Studi
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ………. x
DAFTAR LAMPIRAN ……….. xi
PENDAHULUAN ... 1
TINJAUAN PUSTAKA ... 5
Karakteristik Bahan Baku ... 5
Kimia Kayu ... 7
Jamur Phanerochaete chrysosporium Burdsall ... 15
Reaksi Degradasi Lignin Oleh Jamur ... 17
Kapang Trichoderma viride Person and Fries... 20
Yeast Saccharomyces cerevisiae Meyen ex Hansen ………. 21
Sakarifikasi Fermentasi Simultan ..……….. 22
BAHAN DAN METODE ... 25
Waktu dan Tempat ... 25
Bahan dan Alat ... 25
Prosedur Pelaksanaan ... 26
Analisis Hasil ... 34
HASIL DAN PEMBAHASAN ... 35
Pertumbuhan Jamur Phanerochaete chrysosporium Burdsall ... 35
Kandungan Kimia Kayu ... 37
Aktivtas Enzim ... 52
Kadar Etanol ... 54
SIMPULAN ... 58
DAFTAR PUSTAKA ... 60
DAFTAR TABEL
Halaman Tabel 1. Nilai rata-rata kadar ekstraktif, kadar abu dan kadar lignin
kayu (%) ... 37
Tabel 2. Nilai rata-rata kandar holoselulosa, kadar hemiselulosa, dan
kadar selulosa kayu (%) …………..……… 38
Tabel 3. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi terhadap kadar ekstraktif serbuk kayu ...
42
Tabel 4. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar abu serbuk kayu ... 43
Tabel 5. Hasil uji BNJ faktor waktu inkubasi terhadap kadar
holoselulosa serbuk kayu ... 45
Tabel 6. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar selulosa serbuk kayu ... 46
Tabel 7. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar hemiselulosa serbuk kayu ... 48
Tabel 8. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
terhadap kadar lignin serbuk kayu ... 51
Tabel 9. Nilai rata-rata kadar etanol (g/l) dan (g/g) ... 53
Tabel 10. Hasil uji BNJ interaksi faktor jenis kayu dan waktu inkubasi
DAFTAR GAMBAR
Halaman Gambar 1. Skema dinding sel kayu dan hubungan lignin, selulosa
dan hemiselulosa dalam dinding sekunder ... 7
Gambar 2. A. Struktur selulosa dengan pengulangan unit selobiosa.
B. Selulosa kristalin ... 8
Gambar 3. A. Struktur O-asetil-4-O-metilglukoronoksilan(hemiselulosa utama di kayu daun lebar). B. Struktur O-aselilgalakto
glukomanan (hemiselulosa utama pada kayu daun jarum) . 10
Gambar 4. Model struktur lignin ……….. 11
Gambar 5. Struktur kimia 3 subunit penyusun lignin ... 12
Gambar 6. Ikatan ß-aryl ether pada lignin kayu ... 12
Gambar 7. A. Penggabungan materi lignoselulosa membentuk serat elentari dan mikrofibril. B. Struktur ikatan ester antara lignin dengan arabino-4-O-methilglucomonoxylan pada
Pinus ... 14
Gambar 8. Skema penyerangan lignin oleh enzim jamur
Phanerochaete chrysosporium ... 17
Gambar 9. Skema lignolitik dari jamur pembusuk putih ……….. 18
Gambar 10. Mekanisme hidrolisis enzim selulase ... 24
Gambar 11. Isolat P. chrysosporium umur 6 hari pada media PDA ….... 35
Gambar 12. Kondisi serbuk kayu sebelum diberi perlakuan jamur dan setelah 30 hari waktu inkubasi dengan jamur
P.chrysosporium ………. 36
Gambar 13. A. Histogram kadar kimia kayu serbuk kayu sengon. B. Histogram kadar kimia kayu serbuk kayu meranti. C. Histogram kadar kimia kayu serbuk kayu jati ... 39
Gambar 14. A. Isolat T.viride umur 5 hari. B. Spora pada suspensi 10
ml aquades ... 51
Gambar 15. Histogram kadar etanol dari serbuk kayu... 54
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Data dan Hasil Analisis Kandungan Kimia Kayu... 64
Lampiran 2. Hasil Analisis Varian Kandungan Kimia Kayu ... 71
Lampiran 3. Hasil dan Analisis S/G Rasio Lignin Kayu Jati ... 73
Lampiran 4. Aktivitas FP-ase Enzim Kasar T.viride ... 77
Lampiran 5. Hasil dan Analisis Kadar Etanol ... 78
Lampiran 6. Hasil Analisis Varian Kadar Etanol ... 79
PENDAHULUAN
Saat ini di Indonesia tengah terjadi krisis bahan bakar minyak. Sejak bulan
Oktober 2005, harga berbagai bahan bakar yang berasal dari minyak bumi
meningkat hingga 2 kali lipat. Ketergantungan akan bahan bakar minyak dapat
merugikan, karena selain potensinya yang akan habis, juga menyebabkan
pencemaran udara yang cukup tinggi. Oleh karena itu perlu dicari bahan bakar
alternatif yang salah satunya adalah bioetanol.
Menurut Bruce dan Palfreyman (1998) etanol dapat diproduksi dari
sumberdaya yang dapat diperbaharui seperti biomasa yang dikategorikan ke
dalam bahan-bahan berbasis gula (gula tebu, gula bit dan sorgum manis), pati
(biji-bijian yaitu: jagung, gandum, beras; serta umbi-umbian yaitu: kentang, ketela
pohon, ubi jalar) dan lignoselulosa (kayu, jerami, bagase, dan sebagainya).
Penggunaan bahan baku berbasis gula dan pati memang lebih mudah pada
proses pembuatan etanol, akan tetapi penggunaan bahan baku tersebut
bersaing dengan pemanfaatannya yang lebih tinggi yaitu sebagai sumber bahan
makanan. Penggunaan bahan baku lignoselulosa, selain harganya lebih murah,
potensinya lebih besar dan tidak bersaing dengan pemanfaatan lain. Hasil
penelitian Itoh et.al. (2003), dengan menggunakan bahan baku kayu beech yang
diberi perlakuan pulping dan tidak diberi perlakuan pulping, menghasilkan etanol
secara berturut-turut sebanyak 0,294 g/g dan 0,176 g/g.
Dilain pihak, Indonesia adalah salah satu negara tropis yang memiliki
kawasan hutan yang luas yang terdiri dari ribuan tumbuhan penghasil kayu
terutama dari jenis daun lebar. Banyaknya bahan baku kayu ini, menyebabkan
berkembangnya industri perkayuan di Indonesia. Kayu dari jenis daun lebar
seperti meranti, jati, mahoni, sengon dan jenis lainnya banyak dimanfaatkan
sebagainya. Hal ini terutama disebabkan karena jenis kayu daun lebar memiliki
sifat pengerjaan yang cukup baik, sifat dekoratif yang lebih indah dan kekuatan
yang tinggi.
Menurut data statistik dari Departemen Kehutanan (2004), pada tahun 2003
produksi log Indonesia adalah mencapai 10.086.217,06 m3 yang berasal dari
hutan alam, hutan tanaman industri dan hutan rakyat. Perkembangan industri
perkayuan yang pesat tentunya juga menimbulkan hasil samping berupa limbah.
Dalam proses pengolahan kayu hanya sekitar 60-70% dari komoditi kayu yang
diolah menjadi produk, dengan limbah sisa kayu dan serbuk gergajiannya
mencapai jumlah kurang lebih 30-40% (Darmaji et al., 1998) atau sekitar
3,03-4,03 juta m3 untuk tahun 2003.
Proses pengolahan serbuk kayu menjadi etanol dapat dilakukan dengan
menggunakan metode sakarifikasi-fermentasi secara simultan. Sakarifikasi
fermentasi secara simultan adalah suatu proses yang dapat dilakukan untuk
mengubah selulosa kayu menjadi etanol dalam 1 tahap fermentasi. Dalam
proses ini selulosa kayu dihidrolisis oleh komplek enzim selulase dan setiap
glukosa yang terbentuk langsung dimanfaatkan oleh yeast untuk diubah menjadi
etanol, sehingga dengan demikian konsentrasi glukosa yang terdapat di dalam
medium selalu rendah dan memberi kemungkinan hasil etanol yang maksimum
(Sjamsuriputra, et al.,1986).
Pada proses sakarifikasi, hidrolisis selulosa dapat dilakukan dengan
menggunakan 2 cara, yaitu hidrolisis menggunakan asam kuat dan
menggunakan enzim. Penggunaan asam kuat pada proses hidrolisis mempunyai
banyak persoalan teknik dan ekonomi misalnya penggunaan peralatan yang
harus tahan terhadap asam, permasalahan pemulihan asam, selain
menghasilkan rendemen yang kecil. Penggunaan bahan kimia juga dapat
enzim (kompleks selulase maupun xilanase), walaupun masih jauh dari
penyelesaian karena laju hidrolisisnya rendah, tetapi lebih disukai karena lebih
ramah lingkungan. Selain itu hidrolisis enzimatis dapat dilakukan pada suhu
ruang dan tekanan rendah, yang artinya tidak memerlukan penggunaan energi,
juga produk yang dihasilkan lebih spesifik.
Terdapat beberapa jenis enzim yang dihasilkan oleh berbagai jamur dan
bakteri yang berperan dalam hidrolisis selulosa. Enari (1983) menyatakan bahwa
ada 3 jenis enzim yang berperan dalam hidrolisis selulosa sec ara sinergi, yaitu
endo-1,4-β-glukanase, exo-1,4-β-glukanase dan β-glukosidase. Enzim yang
berperan dalam hidrolisis hemiselulosa adalah sesuai dengan komponen
monosakarida utama yang terdapat di dalam hemiselulosa, yaitu enzim xylanase,
mannanase dan galaktanase. Penggunaan enzim selulase dipengaruhi oleh
konsentrasi dan kondisi bahan lignoselulosa itu sendiri, antara lain derajat
polimerisasi selulosa, kristalinitas selulosa, aksesibilitas enzim, dan jumlah lignin
(Zhang dan Lynd, 2004).
Fermentasi gula pereduksi menjadi etanol dilakukan dengan menggunakan
yeast yaitu Saccharomyces cerevisiae. Penggunaan yeast pada fermentasi
etanol, lebih disukai jika dibandingkan penggunaan bakteri. Hal ini disebabkan
karena yeast mempunyai sel yang lebih besar dan dinding sel yang lebih padat,
sehingga lebih mudah pada saat pemanenan dan daur ulang yeast. Selain itu
yeast tidak mudah terkontaminasi oleh bakteri maupun virus lain (Jeffries, 2000).
Kendala yang dihadapi dalam hidrolisis serbuk kayu dengan cara enzimatis
yang menyebabkan rendahnya laju hidrolisis, salah satunya adalah adanya
kandungan lignin dalam serbuk kayu tersebut. Hasil penelitian Irawadi (1991),
menunjukkan bahwa hidrolisis dengan menggunakan enzim yang sama pada
mg/g), dibandingkan subtrat serbuk gergaji (40 mg/g). Lignin menyebabkan
aksesibilitas enzim menjadi rendah terhadap polisakarida.
Oleh karena itu perlu dilakukan penelitian mengenai perlakuan delignifikasi
atau penghilangan lignin dari serbuk kayu sebelum perlakuan
sakarifikasi-fermentasi simultan untuk meningkatkan kemampuan hidrolisis dari enzim.
Penghilangan lignin dapat dilakukan secara kimia maupun secara biologi. Cara
biologi (biodelignifikasi) selain lebih murah, juga lebih ramah terhadap
lingkungan, sering dilakukan dengan menggunakan jamur, yaitu jamur pelapuk
putih (white-rot fungi) yang mampu mendegradasi lignin dan memanfaatkan
hasilnya untuk proses metabolisme tubuhnya.
Tujuan dari penelitian ini adalah untuk mengkaji pengaruh berbagai jenis
serbuk kayu terhadap rendemen dan kualitas etanol serta mengkaji pengaruh
kandungan lignin di dalam berbagai jenis serbuk kayu terhadap rendemen dan
kualitas etanol. Penelitian ini diharapkan dapat memberikan informasi mengenai
cara optimalisasi hidrolisis serbuk kayu pada proses sakarifikasi-fermentasi
simultan untuk menghasilkan etanol, sehingga dapat meningkatkan nilai ekonomi
TINJAUAN PUSTAKA
Karakteristik Bahan Baku Kayu Sengon (Paraserianthes falcataria (L.) Nielsen syn.)
Kayu sengon memiliki sifat-sifat yaitu sangat ringan, agak kasar, agak
padat, berwarna putih segar tetapi makin menuju keteras kayu kadang-kadang
berwarna agak kemerah-merahan. Kayu sengon termasuk dalam kelas kuat IV
(Heyne, 1987). Tekstur kayu sengon agak kasar dan merata, arah seratnya lurus,
bergelombang lebar atau berpadu. Permukaan kayunya agak licin dan
mengkilap. Berat jenis kayu sengon berkisar antara 0,24-0,49 dengan rata-rata
0,33. Kayu yang masih segar berbau petai yang lambat laun hilang jika kayunya
menjadi kering.
Kayu sengon termasuk kelas awet IV-V, sehingga daya tahannya
terhadap serangan organisme perusak kayu adalah sangat rendah. Sifat kimia
dari kayu sengon adalah kadar selulosa 49,4%, kadar lignin 26,8%, kadar
pentosan 15,6%, kadar abu 0,6%, kadar silika 0,2% dan kadar ekstraktif larut
alkohol-benzen 3,4% (Martawijaya et al., 1989).
Kayu Meranti (Shorea spp.)
Martawijaya et al. (1989) menyatakan bahwakayu meranti merah memiliki
warna kayu teras bervariasi dari hampir putih, coklat pucat, merah jambu, merah
muda, merah kelabu, merah-coklat muda dan merah sampai merah tua atau
coklat tua. Kayu gubal berwarna lebih muda dan dapat dibedakan dengan jelas
dari kayu teras, berwarna putih, putih kotor, kekuning-kuningan atau
kecoklat-coklatan sangat muda, biasanya kelabu. Memiliki tekstur kayu dari agak kasar
bergelombang atau sangat berpadu. Permukaan kayunya agak licin sampai licin
dan agak mengkilap.
Kayu meranti merah mempunyai gambaran berupa pita pada bidang
radialnya dan juga terdapat gambaran jari-jari yang kurang jelas. Rata-rata berat
jenis kayu meranti merah bervariasi menurut jenisnya dari 0,40-0,77. Kelas kuat
berkisar antara II-IV. Kelas awetnya secara umum termasuk dalam kelas III-IV.
Sifat kimia dari kayu meranti merah adalah kadar selulosa 49,6-56,1%, kadar
pentosan 8,2-24,21%, kadar abu 0,24-0,86%, kadar silika 0,06-0,86% dan kadar
ekstraktif larut alkohol-benzen 0,6-5,39% (Martawijaya et al., 1989). Sedangkan
kadar lignin berkisar antara 24,48-30% (Syafii et al., 1988).
Kayu Jati (Tectona grandis LINN.f.)
Kayu jati termasuk kayu mewah dengan kelas kuat II dan mempunyai nilai
dekoratif yang indah. Lingkaran tahun tampak jelas karena adanya perbedaan
kayu awal dan kayu akhir. Stabilisasi dimensinya baik sehingga sesuai untuk
keperluan bahan baku industri meubel, rangka pintu dan jendela, panel pintu
serta vinir indah (Mandang dan Pandit, 1997).
Warna kayu teras jati adalah coklat muda, kelabu sampai
coklat-merah tua atau coklat-merah coklat. Warna kayu gubalnya adalah putih atau kelabu
kekuning-kuningan. Tekstur kayu agak kasar dan tidak merata. Arah serat lurus
atau kadang-kadang agak terpadu. Permukaan kayu licin atau agak licin, bahkan
terkadang seperti berminyak. Kayu jati berbau bahan penyamak yang mudah
hilang. Berat jenis berkisar antara 0,62-0,75 dengan rata-rata 0,67. Kayu jati
termasuk kelas awet II dan dilaporkan sangat tahan terhadap serangan jamur.
Sifat kimia dari kayu jati adalah kadar selulosa 47,5%, kadar lignin 29,9%, kadar
pentosan 14,4%, kadar abu 1,4%, kadar silika 0,4% dan kadar ekstraktif larut
Kimia Kayu
Komponen kimia utama penyusun kayu adalah selulosa, hemiselulosa, dan
lignin. Gambaran yang disederhanakan menunjukkan bahwa selulosa
membentuk kerangka yang dikelilingi oleh senyawa-senyawa lain yang berfungsi
sebagai matriks (hemiselulosa) dan bahan-bahan yang melapisi (lignin) (Gambar
1) (Kirk dan Cullen,1998). Selain itu pada beberapa spesies terdapat juga
komponen kimia yang lain yang disebut ekstraktif. Ekstraktif terendap pada
rongga sel kayu selama pembentukan kayu teras. Pada spesies kayu yang
berbeda, jenis dan komposisi masing-masing komponen kayu tersebut juga
berbeda.
Gambar 1. Skema dinding sel kayu dan hubungan lignin, selulosa dan hemiselulosa dalam dinding sekunder. M.L: lamella tengah, P: dinding primer, S1: dinding sekunder 1,
S2: dinding sekunder 2, S3: dinding sekunder 3 (Kirk dan Cullen,1998)
Selulosa
Selulosa merupakan konstituen utama kayu. Kurang lebih 40-45% bahan
kering kayu (baik kayu daun jarum maupun kayu daun lebar), terutama di dinding
sekunder terdiri dari selulosa. Dalam dinding sel kayu, selulosa berfungsi untuk
memberikan kekuatan (Sjostrom, 1995).
Selulosa adalah polimer rantai panjang yang tersusun dari monomer β
-1,4-glikosida. Ikatan β menunjukkan bahwa tiap unit glukosa membentuk rotasi 180o.
Perputaran ini menyebabkan selulosa memiliki simetrisitas yang tinggi.
Pasangan antara molekul selulosa yang berdekatan terjadi karena ikatan
hidrogen dan gaya Van der Waals menghasilkan susunan paralel sejajar dan
struktur kristalin (Gambar 2B)(Zhang dan Lynd, 2004). Molekul-molekul selulosa
seluruhnya berbentuk linier dan memiliki kecenderungan membentuk ikatan -OH
intramolekul (antara monomer glukosa dalam 1 rantai selulosa yang sama) dan
intermolekul (antara monomer glukosa dari 2 rantai selulosa yang berdekatan).
Pada kedua ujung rantai selulosa terdapat gugus OH tetapi dengan perilaku yang
berbeda. Gugus C1-OH adalah gugus hidrat aldehida yang mempunyai sifat
pereduksi, sedangkan gugus OH pada akhir C4 merupakan gugus hidroksil
alkohol yang bersifat non pereduksi (Fengel dan Wegener, 1995).
Gambar 2. A. Struktur selulosa dengan pengulangan unit selobiosa (Atalla, 1999). B. Selulosa kristalin (Mosier et al., 1999 dalam Zhang dan Lynd, 2004).
Derajat polimerisasi atau banyaknya monomer β-D-glukosa yang menyusun
1 rantai selulosa pada kayu adalah 7.000-10.000 (Goldstein, 1981). Secara tepat
unit ulangan dari rantai selulosa adalah unit selobiosa dengan ukuran panjang
1,04 nm dan lebar 0,54 nm (Gambar 2A). Ikatan intermolekul menggabungkan
antar rantai selulosa sehingga terbentuk mikrofibril. Gabungan dari mikrofibril
A B
1,04 nm
OH HO
HO HO
O
O
OH HO
HO
OH HO
HO
O
OH
OH OH
membentuk makrofibril dan gabungan dari makrofibril akhirnya membentuk
dinding sel kayu. Mikrofibril selulosa dalam kayu mengandung kurang lebih 40
rantai selulosa dan mempunyai daerah kristalin kurang lebih 100-150 unit
selobiosa yang dipisahkan oleh sedikit daerah amorfous (Atalla, 1999).
Ikatan-ikatan glikosida dalam selulosa terlarut atau amorf mudah dihidrolisis
oleh semua tipe asam dan hidrolisis enzimatis. Tetapi dalam prakteknya terdapat
2 hambatan umum pada hidrolisis selulosa dari serbuk kayu yaitu karena adanya
kandungan lignin di dalam kayu sebagai bahan lignoselulosa dan karena adanya
struktur kristalin dari selulosa (Fengel dan Wegener, 1995). Hubungan antara
struktur selulosa dengan laju hidrolisis enzim telah dipelajari secara ekstensif
tetapi belum terbentuk suatu pemahaman yang menyeluruh. Struktur selulosa
biasanya dipertimbangkan sebagai faktor yang mempengaruhi laju hidrolisis,
antara lain termasuk di dalamnya yaitu: indek kristalinitas, derajat polimerisasi
dan asesibilitas area (Zhang dan Lynd, 2004).
Hemiselulosa
Hemiselulosa adalah rantai polimer bercabang dari berbagai jenis monomer
(monosakarida) yang berbeda atau sering disebut heteropolimer.
Monomer-monomer hemiselulosa antara lain D-glukosa, D-manosa, D-galaktosa, D-xilosa,
L-arabinosa dan sedikit L-ramnosa. Kebanyakan hemiselulosa mempunyai
derajat polimerisasi 100-200 (Sjostrom, 1995).
Goldstein (1981) menyatakan bahwa prosentase hemiselulosa di dalam
kayu daun lebar kurang lebih adalah 30%, sedangkan pada kayu daun jarum
adalah 25%. Komposisi jenis hemiselulosa antara kayu daun lebar dan kayu
daun jarum juga berbeda. Hemiselulosa utama dalam kayu daun lebar adalah
xilan. Xilan merupakan suatu homopolimer yang tersusun dari xilosa sebagai
xilosa, selain itu pada cabang rantai juga terdapat arabinosa (Gambar 3A). Pada
hemiselulosa kayu daun lebar kandungan manan hanya terdapat dalam jumlah
kecil. Galaktoglukomanan merupakan hemiselulosa pokok pada kayu daun jarum
(kurang lebih 20%). Struktur tulang punggungnya tersusun atas glukopiranosa
[image:31.596.134.484.209.458.2]dan manopiranosa dengan ikatan β-1,4-glikosida (Gambar 3B).
Gambar 3. A. Struktur O-asetil-4-O-metilglukoronoksilan (hemiselulosa utama di kayu daun lebar). B. Struktur O-aselilgalaktoglukomanan (hemiselulosa utama pada kayu daun
jarum) (Kirk dan Cullen, 1998)
Hemiselulosa merupakan matriks penggabung antar mikrofibril selulosa
dalam dinding sel kayu. Hemiselulosa juga bersifat tidak mudah larut di dalam
air, akan tetapi dapat larut dalam basa kuat. Hemiselulosa lebih mudah
terhidrolisis dalam asam dibanding selulosa, hal ini karena struktur hemiselulosa
yang amorfous dan derajat polimerisasinya yang lebih rendah dibanding selulosa
(Lewin dan Goldstein, 1991). A
B O
OH HO
CH2OH
OR OR
CH2O
O
HO HO
CH2OH
HO
O
OR OR
CH2OH OR OR
O O O O HO HO
CO2H
H3CO
Lignin
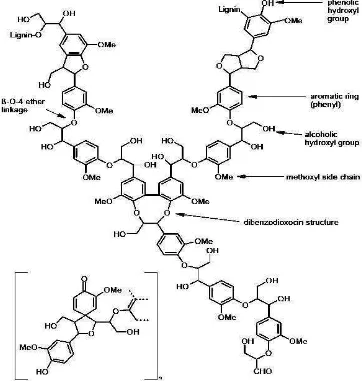
Lignin adalah suatu kompleks polimer 3 dimensi yang diproduksi secara in
vivo oleh enzim penginisiasi polimerisasi dehidrogenatif dari 3 monomer
fenilpropana, yaitu p-hidroksilamin alkohol, koniferil alkohol dan sinapil alkohol.
Polimer lignin terbentuk melalui ikatan eter yang terdiri dari unit-unit fenilpropana
yang saling bergabung (Gambar 4). Biosintesis lignin dari unit fenilpropana
dinyatakan secara umum sebagai polimerisasi dehidrogenatif. Kompleks polimer
lignin berperan sebagai pemberi kekuatan fisik, pertahanan terhadap serangan
mikrobia dan pertahanan terhadap permeabilitas air ke matrik polisakarida
[image:32.596.132.494.339.720.2]dinding sel tumbuhan (Whetten et al., 1998).
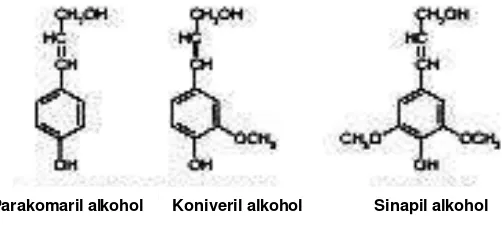
Prekursor lignin yaitu p-coumaryl alkohol, koniferyl alkohol and sinapyl
alkohol tersusun atas sebuah cincin aromatic dan 3 karbon rantai samping.
Prekursor tersebut kemudian membentuk 3 tipe subunit yaitu hydroxyphenol-
(H-type), guaiacyl- (G-type) and syringyl subunits (S-type) (Gambar 5). Suatu hal
yang khas yang ditemukan pada polimer lignin adalah tidak ada ikatan dari satu
jenis subunit penyusun yang berulang. Polimer lignin tersusun atas distribusi
secara acak dari tiap-tiap subunit, dengan kurang lebih membentuk 10 macam
tipe katan yang berbeda. Jenis ikatan yang paling banyak ditemukan adalah
[image:33.596.181.432.334.447.2]ß-aryl ether (ß-O-4) (Gambar 6).
Gambar 5. Struktur kimia 3 subunit penyusun lignin (Lankinen, 2004)
Gambar 6. Ikatan ß-aryl ether pada lignin kayu (Jeffries, 1994)
Lignin tahan terhadap degradasi oleh sebagian besar mikroorganisme.
Meskipun demikian, jamur tertentu mampu menguraikan lignin secara selektif.
Karena strukturnya yang kompleks dan jenis ikatan pada lignin bersifat tahan
terhadap air, maka hal ini menyebabkan lignin menjadi sulit didegradasi. Masa
molekul lignin adalah 100 kDa atau lebih, hal ini dapat mencegah masuknya sel
Koniveril alkohol
[image:33.596.279.383.484.596.2]mikrobial seperti jamur. Oleh karena itu biodegradasi lignin biasanya terjadi
melalui aktivitas enzim ekstraseluler dari organisme pendegradasi lignin.
Menurut Campbell and Sederoff (1996) kandungan struktur dan komposisi
lignin bervariasi pada populasi tanaman spesies tertentu. Gimnospermae
(kelompok kayu daun jarum), mempunyai lignin yang subunit penyusun
utamanya adalah guaiasil (> 90%) dengan sedikit p-hydroxyphenyl yang tidak
termetoksilasi. Tipe lignin dari angiospermae (kelompok kayu daun lebar) adalah
lignin guaiasil-siringil, yang terbentuk dari ko-polymerisasi koniferil and sinapil
alkohol. Lignin rumput-rumputan tersusun atas subunit siringil, guaiasil dan
p-hydroxyphenyl dengan perbandingan komposisi berturut-turut 40% : 40% : 20%
(Stenius, 2000).
Prosentase lignin pada kayu daun lebar kurang lebih adalah 20%, dan lebih
banyak dijumpai jenis lignin guaiasil-siringil dengan nisbah bervariasi dari 4:1
hingga 1:2 (Sjostrom, 1995). Kayu daun lebar dengan kandungan lignin siringil
yang lebih banyak (perbandingan siringi:guaiasil (S/G rasio) yang tinggi)
mempunyai laju delignifikasi yang lebih tinggi jika dibandingkan dengan kayu
daun lebar yang sedikit mengandung lignin siringil (S/G rasio yang rendah). Kayu
sengon mempunyai nilai S/G rasio sebesar 2,03 sedangkan kayu meranti
mempunyai nilai S/G rasio sebesar 1,87 (Syafii, 2001).
Kompleks Lignin Karbohidrat
Lignin umumnya tidak pernah ditemukan dalam bentuk sederhana diantara
polisakarida-polisakarida dinding sel, tetapi selalu tergabung atau berikatan
dengan polisakarida tersebut. Bentuk kompleks lignin karbohidrat (
Lignin-carbohydrate complexes (LCCs)) adalah beraneka ragam berbeda-beda pada
setiap jenis tanaman. Lignin secara langsung ataupun tidak langsung berikatan
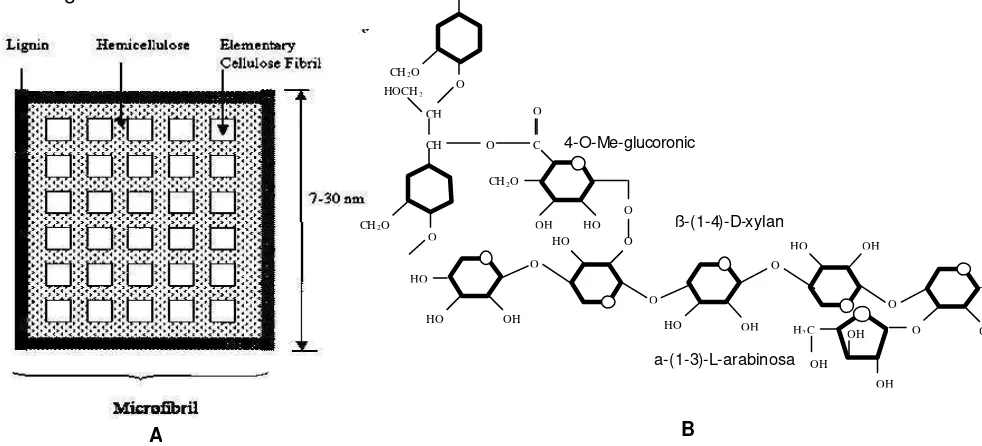
Kurang lebih 100 unit glukan selulosa bergabung menjadi serat elementari
dengan lebar daerah kristalin 4-5 nm, dan sekitar 40 serat elementari ini tertanam
dalam matrik hemiselulosa membentuk mikrofibril dengan ketebalan 7-30 nm.
Selanjutnya proses lignifikasi terjadi pada bagian akhir proses pembentukan
serat alami, sehingga lignin terletak terutama pada bagian luar mikrofibril dengan
ikatan kovalen dengan hemiselulosa (Zhang dan Lynd, 2004).
Interaksi antara lignin dengan polisakarida lebih dipengaruhi oleh ikatan
kimia daripada bentuk-bentuk asosiasi seperti ikatan hidrogen, gaya Van der
Waals dan khemosopsi (Fengel dan Wegener, 1984). Ikatan kimia yang bersifat
stabil yang paling banyak ditemukan pada kompleks lignin karbohidrat adalah
ikatan ester. Ikatan ester terjadi antara gugus karboksil bebas dari asam uronik
pada hemiselulosa dan gugus benzil pada lignin (Jeffries, 1994). Jenis ikatan lain
yang ditemukan pada kompleks lignin karbohidrat adalah ikatan eter dan
[image:35.596.81.572.424.647.2]glikosida.
Gambar 7. A. Penggabungan materi lignoselulosa membentuk struktur mikrofibril (Klein and Snodgrass, 1993 dalam Zhang dan Lynd, 2004). B. Struktur ikatan ester antara lignin dengan arabino-4-O-methilglucomonoxylan pada Pinus (Watanabe dan Koshijima,
1988 dalam Jeffries, 1994b)
Ekstraktif dan Abu
A B
4-O-Me-glucoronic
a-(1-3)-L-arabinosa
HOCH2
CH O
C
CH O
CH2O
O HO O OH HO O HO O OH HO OH HO O OH
H2C OH
OH
OH O
CH2O
HO OH O
CH2O
O O
Zat ekstraktif terdiri dari berbagai jenis komponen senyawa organik seperti
minyak yang mudah menguap, terpen, asam lemak dan esternya, lilin, alkohol
polihidrik, mono dan polisakarida, alkaloid, dan komponen aromatik (asam,
aldehid, alkohol, dimer fenilpropana, stilbene, flavanoid, tannin dan quinon). Zat
ekstraktif adalah komponen diluar dinding sel kayu yang dapat dipisahkan dari
dinding sel yang tidak larut menggunakan pelarut air atau organik (Lewin dan
Goldstein, 1991). Kayu teras secara khas mengandung zat ekstraktif jauh lebih
banyak dari pada kayu gubal. Kandungan zat ekstraktif dalam kayu biasanya
kurang dari 10% (Sjostrom, 1995).
Kandungan dan komposisi zat ekstraktif berubah-ubah diantara spesies
kayu, dan bahkan terdapat juga variasi dalam satu spesies yang sama
tergantung pada tapak geografi dan musim. Sejumlah kayu mengandung
senyawa-senyawa yang dapat diekstraksi yang bersifat racun atau mencegah
bakteri, jamur dan rayap. Selain itu zat ekstraktif juga dapat memberikan warna
dan bau pada kayu (Fengel dan Wegener, 1995).
Kayu juga mengandung komponen-komponen anorganik. Komponen ini
diukur sebagai kadar abu yang jumlahnya jarang melebihi 1% dari berat kering
kayu. Abu ini berasal terutama dari berbagai garam yang diendapkan dalam
dinding sel dan lumen (Sjostrom, 1995). Fengel dan Wegener (1995)
menyatakan bahwa komponen abu utama dalam kayu adalah Ca (hingga 50%),
K dan Mg, yang diikuti oleh Mn, Na, P dan Cl. Selain itu juga masih terdapat
unsur-unsur lain yang disebut sebagai unsur runut dengan konsentrasi di dalam
kayu tidak lebih dari 50 ppm.
Mineral tidak hanya terikat dalam diding sel tetapi juga diendapkan dalam
rongga sel parenkim dan dalam serat libriform. Endapan mineral kebanyakan
terdiri atas kalsium karbonat, kalsium oksalat dan silikat yang mempunyai bentuk
jamur atau bakteri disebabkan oleh hasil metabolik mikroorganisme tersebut
(Fengel dan Wegener, 1995).
Jamur Phanerochaete chrysosporium Burdsall.
Jamur Phanerochaete chrysosporium Burdsall. termasuk dalam kelompok
jamur pelapuk putih (white-rot fungi), dan merupakan jamur kelas Basidiomisetes
yang juga menyerang holoselulosa, namun pilihan utamanya adalah lignin.
Sistematika dari jamur ini selengkapnya adalah kelas Basidiomycetes, sub kelas
Holobasidiomycetes I atau Hymenomycetes I, ordo Aphylophorales, famili
Certiciaceae, genus Phanerochaete dan spesies Phanerochaete chrysosporium
Burdsall (Crawford, 1981).
Jamur ini dapat tumbuh pada suhu optimum 39oC dan maksimum pada
suhu 50oC. Laju pertumbuhan pada media agar ekstrak malt pada suhu 25oC
adalah 15-20 mm per hari, sedangkan pada suhu 40oC adalah 35-42 mm per
hari. Toleransi yang baik terhadap suhu tinggi dan kemampuannya untuk
memproduksi spora dalam jumlah besar dari jenis jamur ini menyebabkan
perlunya perhatian khusus bila digunakan dalam laboratorium. Merupakan jenis
pembusuk putih yang istimewa sehingga banyak dipelajari dan telah digunakan
secara komersial pada proses biopulping (Eaton dan Hale, 1993). Singh dan
Roymoulik (1996) melaporkan bahwa kemampuan P. chrysosporium dalam
mendegradasi lignin dapat mencapai 7% hingga 30% tergantung dari jenis lignin
dan waktu inkubasi. Sedangkan hasil penelitian Widjaja et.al. (2000) adalah
biodelignifikasi menggunakan P chrysosporium pada kayu memberikan derajat
delignifikasi yang lebih tinggi dibanding pinus. Delignifikasi tertinggi 55,02%
diperoleh pada hari ke-30 inkubasi pada sengon menggunakan media okara
Kemampuan jamur dalam mendegradasi lignin disebabkan karena adanya
enzim ekstraseluler yang disekresikan oleh hifa jamur. Menurut Eaton dan Hale
(1993) berbagai enzim yang berperan dalam proses degradasi lignin yang
disekresikan oleh jamur pelapuk putih adalah lignin peroksidase (LiP), mangan
peroksidase (MnP), lakase, demetoksilase, H2O2-generating enzyme dan enzim
pendegradasi monomer seperti selobiosa dehidrogenase, asam vanilat hidrolase
dan trihidroksi benzen dioksigenase. Namun enzim lignolitik yang utama adalah
lignin peroksidase (LiP), mangan peroksidase (MnP) dan lakase. Hasil penelitian
Koker et al. (1998) pada berbagai strains P.chrysosporium, menunjukkan bahwa
P.chrysosporium mempunyai aktivitas MnP bervariasi antara 0,059-0,180 U/g
medium, aktivitas LiP antara 0,019-0,072 U/g medium, dan aktivitas GLOX
[image:38.596.125.492.383.667.2](glyoxal oksidase) antara 0,013-0,042 U/g medium.
Gambar 8. Skema penyerangan lignin oleh enzim jamur Phanerochaete chrysosporium
Reaksi Degradasi Lignin Oleh Jamur
Proses degradasi lignin oleh jamur dapat dibagi menjadi 2 tipe, yaitu tipe
prefensi dan tipe simultan. Jamur tipe prefensi akan mendegradasi lignin terlebih
dahulu sebelum menguraikan hemiselulosa dan selulosa, sedangkan jamur tipe
simultan mampu mendegradasi selulosa, hemiselulosa dan lignin pada waktu
dan kecepatan yang sama (Eaton dan Hale, 1993). Mekanisme reaksi
delignifikasi enzimatik dijelaskan lebih rinci oleh Hattori dan Shimada (2001),
yaitu: ligninase dari Phanerochaete chrysosporium (kemudian disebut
peroxidase) mengkatalis pemutusan ikatan Ca-Cß lignin melalui mekanisme
oksidasi satu elektron menghasilkan produk aldehid aromatik dan phenylglycol.
Pemutusan selanjutnya adalah ikatan Cß-eter, pembelahan cincin aromatik lignin
dan pemutusan ikatan Ca-Cß lignin karbohidrat kompleks. Fengel dan Wegener
(1995) juga menyatakan bahwa reaksi-reaksi pemecahan menghasilkan
senyawa monomer dan dimer yang kebanyakan mengandung gugus karboksil.
Pemecahan cicin aromatik adalah dimaksudkan agar senyawa-senyawa
degradasi lignin tersebut dapat masuk ke dalam metabolisme internal jamur.
Monomer-monomer lain yang ditemukan sebagai hasil degradasi jamur adalah
asam vanilat dan asam veratrat. Skema degradasi lignin oleh jamur pembusuk
Gambar 9. Skema lignolitik dari jamur pembusuk putih (Kirk dan Cullen, 1998) Zabel dan Morrell (1992) menyatakan bahwa hasil analisis dari lignin sisa
degradasi oleh jamur pelapuk putih mengindikasikan hilangnya gugus metoksil
dan peningkatan kadar oksigen dan hidroksil. Perubahan struktur utama dari
lignin meliputi:
1. Demetilasi
2. Oksidasi dari a atom karbon
3. Pembelahan dari rantai samping antara a dan ß karbon dari unit phenyl
propane
C
CH2
OCH3
O
C
CH2
OCH3
O
C
CH2
C
O
O
C
O O
+ C — C
4. Hidroksilasi dan dioksigenasi pembelahan cincin aromatic
5. Pembelahan langsung dari aryl gliserol-ß-aryl ether
Kapang Trichoderma viride Person and Fries.
Trichoderma viride Person and Fries. adalah kapang yang termasuk dalam
genus trichoderma, famili monialiaceae, ordo moniales dan kelas fungi imperfecti.
Kapang trichoderma mempunyai cirri-ciri spesifik antara lain: miselium bersekat,
bercabang banyak, konidiospora berseptat dan cabang paling ujung berfungsi
sebagai sterigma, konidia berwarna hijau cerah dan bergerombol menjadi satu
membentuk bola, serta berkas-berkas hifa berwarna putih terlihat menonjol jelas
diatas konidiospora (Waluyo, 2004).
T.viride merupakan salah satu jamur pelapuk lunak yang memproduksi
komplek enzim selulase yang lengkap yaitu endoselulase dan eksoselulase yang
dapat memutus selulosa kristalin. Penelitian mengenai pemisahan komplek
C = C CH2 OCH O C C C = O
enzim selulase dari T.viride menunjukkan bahwa terdapat bermacam-macan
endoglukanase antara lain EG I dan EG II, dan eksoglukanase yaitu antara lain
selobiohidrolase, CBH I dan CBH II. Hal ini menunjukkan bahwa T.viride memiliki
kemampuan untuk mendegradasi selulosa kristalin dan selulosa non kristalin.
Pada enzim selulase T.viride dapat terjadi sinergisme, bukan hanya antara
endoselulase dengan eksoselulase, melainkan juga antar eksoselulase (Eaton
dan Hale, 1993).
Karakteristik enzim selulase dari T.viride adalah memiliki pH optimum 4 dan
akan tetap stabil pada pH antara 3-7. Suhu optimum adalah 50oC dan
aktivitasnya akan menurun bila suhunya lebih dari 50oC. Berat molekul
endoselulase yang dihasilkan oleh T.viride adalah 42000 dalton, eksoselulase
61000 dalton dan C1 (enzim yang mendegradasi struktur selulosa kristalin)
sebesar 60000 dalton (Fengel dan Wegener, 1995). Aktivitas enzim selulase dari
T.viride tipe QM6a adalah sebesar 2,6 U/mg sedangkan T.viride tipe QM9123
adalah sebesar 5 U/mg (Mandels et al., 1971).
Selain memproduksi enzim selulase, T.viride juga menghasilkan enzim
endo-1,4-β-xilanase yang dapat mendegradasi xilan. Berat molekul enzim
xilanase yang dihasilkan oleh T.viride adalah sebesar 22000 dalton (Ujiie et al.,
1991).
Yeast Saccharomyces cerevisiae Meyen ex Hansen.
Yeast atau khamir Saccharomyces cerevisiae biasa digunakan untuk
membuat roti, anggur dan bir. S. cerevisiae termasuk kedalam kelas
Ascomycetes yang dicirikan dengan pembentukan askus yang merupakan
tempat dihasilkannya askospora. S. cerevisiae memperbanyak diri secara
saccharomyses terdiri dari komponen-komponen glukan, mannan, protein, khitin
dan lemak (Waluyo, 2004). Boyles (1984) menyatakan bahwa untuk setiap mol
glukosa yang dikonsumsi, S. cerevisiae menghasilkan entalpi katabolisme
sebesar –31 Kkal, energi bebas dari hidrolisis ATP (2 mol) sebesar –14,6 Kkal
dan entalpi untuk sintesis selnya hanya 0,23 Kkal. Entalpi dari metabolisme
sebagian besar dihabiskan pada aliran keluar entropy dan hanya sedikit yang
digunakan untuk sintesis materi sel.
Saccharomyces cerevisiae sangat tahan dan toleran terhadap kadar etanol
yang tinggi. Akan tetapi adanya kandungan furaldehid, asam organik dan
komponen fenolik (hasil samping hidrolisis asam selulosa) dapat menghambat
pertumbuhan S. cerevisiae, bahkan kandungan yang tinggi dari furaldehid,
furfural dan 5-hidroksimetil-furfural dapat bersifat meracuni (Brandberg et al.,
2004). Hasil penelitian Samsuri et al. (2005) pada fermentasi bagase yang diberi
perlakuan awal steam dan penjamuran dengan menggunakan S. cerevisiae
dapat menghasilkan etanol sebanyak 15,4 g/l.
Rendemen alkohol dari hexosa dalam fermentasi menggunakan yeast dari
genus Saccharomyces (pada kondisi yang optimal) dapat mencapai 90%
(Boyles, 1984). Hal yang menarik dari proses fermentasi oleh Saccharomyces
adalah pengubahan sebagian besar energi dari gula ke dalam bentuk etanol.
Efisiensi pengubahan energi tersebut dapat mencapai 97% (Cambel, 1983).
Selain yeast S. cerevisiae, bakteri Zymomonas mobilis juga merupakan salah
satu bakteri yang efektif dalam fermentasi etanol, akan tetapi rendemen etanol
yang dihasilkan masih lebih sedikit dibanding yeast karena bakteri tersebut juga
menghasilkan sejumlah produk lain seperti asetat, laktat dan gliserol.
Proses sakarifikasi fermentasi simultan adalah proses kombinasi antara
hidrolisis selulosa secara enzimatik dengan fermentasi gula yang berkelanjutan
sehingga menghasilkan produk akhir berupa etanol. Tahapan-tahapan dalam
proses sakarifikasi fermentasi simultan adalah sama dengan tahapan pada
hidrolisis dan fermentasi secara terpisah, hanya pada proses sakarifikasi
fermentasi simultan ini kedua proses tersebut berlangsung dalam 1 reaktor yang
sama. Yeast secara langsung menfermentasi produk gula yang dihasilkan dari
proses hidrolisis oleh komplek enzim selulolitik, sehingga laju sakarifikasi dan
rendemen etanol yang dihasilkan akan lebih tinggi jika dibanding hasil proses
sakarifikasi dan fermentasi yang terpisah. Keunggulan lain dari proses
sakarifikasi fermentasi simultan adalah penggunaan reaktor tunggal untuk
seluruh proses, sehingga dapat menekan biaya investasi alat. Selain itu adanya
etanol (hasil fermentasi) di dalam media menyebabkan media tidak mudah
terkontaminasi oleh organisme lain yang tidak diinginkan (Ballesteros et al.,
2004).
Proses sakarifikasi selulosa dan hemiselulosa dalam kayu menjadi gula
dapat dilakukan dengan hidrolisis enzimatik atau dengan menggunakan asam.
Jenis enzim yang berperan dalam hidrolisis tersebut adalah komplek selulase
dan hemiselulase (xilanase galaktanase dan mananase). Selulase adalah suatu
komplek enzim yang terdiri dari beberapa enzim yang berkerja secara bertahap
ataupun bersama-sama menguraikan selulosa menjadi glukosa.
Enari (1983) menyatakan bahwa pada proses hidrolisis selulosa ada 3
enzim yang bekerja secara bertahap, yaitu: selobiohidrolase, endoglukonase dan
β-glukosidase dengan tahapan kerja sebagai berikut:
1. Endoglukonase menghidrolisis ikatan glikosidik 1-4 secara acak dan bekerja
2. Selobiohidrolase menyerang ujung rantai selulosa non pereduksi dan
menghasilkan selobiosa. Selain itu enzim ini dapat menghidrolisis
selodekstrin tetapi tidak menyerang selobiosa.
3. β-glukosidase menghidrolisis selobiosa dan selooligomer-selooligiomer
[image:45.596.184.453.213.536.2]pendek lainnya menjadi glukosa.
Gambar 10. Mekanisme hidrolisis enzim selulase (Miyamoto, 1997)
Secara biokimia fermentasi diartikan sebagai pembentukan energi melalui
senyawa organik, sedangkan pengertian dalam bidang industri fermentasi adalah
suatu proses untuk mengubah bahan dasar menjadi suatu produk oleh massa sel
mikrobia. Aplikasi proses fermentasi selalu terdiri dari 6 bagian utama proses,
yaitu: formulasi medium, sterilisasi, produksi starter, pemeliharaan pertumbuhan
mikroorganisme, pemanenan dan pemurnian produk, serta pembuangan limbah
• n Daerah
Kristalin
Daerah
(Wibowo, 1990). Monomer gula dapat diubah secara anaerobik menjadi alkohol
oleh bermacam-macam mikroorganisme. Fermentasi gula sederhana (sukrosa
dan glukosa) menjadi etanol memiliki persamaan stoikiometri, yaitu:
C12H22O11 + H2O 4 C2H5OH + 4 CO2
BAHAN DAN METODOE
Waktu dan Tempat
Penelitian ini dilakukan di Laboratorium Fermentasi Departemen Biokimia
IPB, Laboratorium Bioteknologi Hutan Departemen Budidaya Hutan UGM dan
Laboratorium Kimia dan Serat Kayu Departemen Teknologi Hasil Hutan UGM.
Waktu pelaksanaan penelitian adalah dari bulan Oktober 2005 sampai dengan
bulan Mei 2006.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah serbuk 3 jenis kayu,
yaitu : meranti, jati dan sengon yang diperoleh dari berbagai industri kayu atau
penggergajian kayu di daerah Jogjakarta. Jamur pelapuk putih yaitu spesies
Phanerochaete chrysosporium Burdsall. tipe NRRL 6361 yang diperoleh dari
Laboratorium Mikologi, Fakultas Biologi IPB, kapang Trichoderma viride Person
and Fries tipe CBS 392.92 dan yeast Saccharomyces cerevisiae Meyen ex
Hansen, tipe # 254 (red star) yang diperoleh dari Laboratorium Mikrobiologi, PAU
Pangan dan Gizi UGM. Bahan kimia untuk mengisolasi komponen kimia kayu
antara lain: alkohol, benzene, NaOH, HCl, KOH, CH3COOH, Na2SO3 dan H2SO4 .
Bahan kimia untuk pengujian aktivitas enzim antara lain: reagen somoygi-nelson
dan reagensia arsenomolibdat.
Peralatan yang digunakan dalam penelitian ini meliputi autoklaf, tabung
reaksi atau cawan petri, peralatan pengujian komponen kimia kayu (soxhlett,
penangas air, pompa vacum), oven, timbangan analitik, shaker inkubator,
spektrofotometer, sentrifus, ayakan 40 dan 60 mesh dan kromatografi gas model
Prosedur Pelaksanaan Persiapan penelitian
Serbuk kayu yang akan digunakan terlebih dahulu diayak dengan ukuran
lolos 40 mesh tertahan 60 mesh, dikering udarakan dan dianalisis komponen
kimianya yaitu : selulosa (TAPPI T17 wd-70), holoselulosa, lignin dan ekstraktif
(ASTM D-1102 s.d 1110).
a. Ekstraktif
Sebanyak 2 g sampel serbuk kayu dimasukkan dalam cawan saring.
Selanjutnya cawan saring seisinya dimasukkan dalam soxhlett sedemikian
sehingga ujung cawan saring lebih tinggi dari ujung sifon dan sampel didalamnya
lebih rendah dari titik ini. Cawan saring lalu ditutup dengan sepotong saringan
dari logam agar tidak ada serbuk yang hilang. Ekstraksi dilakukan dengan 200 ml
alkohol benzen (alkohol : benzen = 1 : 2) selama 4-6 jam. Sesudah selesai,
cawan saring itu dikeluarkan dari soxhlett dan dihisap dengan pompa vakum
hingga isinya kering. Kemudian dicuci dengan alkohol untuk menghilangkan
benzen dan dihisap lagi dengan pompa vakum. Selanjutnya cawan saring dan
isinya dikeringkan dalam tanur pada suhu 100-1050C dan ditimbang sampai
beratnya konstan. % 100 tan ker tan ker % = − × ur ing berat ur ing berat awal berat ekstraktif kadar
b. Abu
Sebanyak 2 g (± 0,1 g) serbuk dimasukkan kedalam cawan porselin yang
telah diketahui beratnya. Selanjutnya ditempatkan dalam tanur pada suhu 600ºC
selama 4 jam. Setelah 4 jam, untuk menyempurnakan pembakaran, tutup tanur
dibuka selama kurang lebih 1 menit sehingga sampel berubah menjadi abu
secara sempurna. Setelah itu didinginkan di dalam desikator dan ditimbang
% 100 % = × awal berat abu berat abu kadar
c. Holoselulosa
Sebanyak 0,70 g (± 0,05 g) serbuk bebas ekstraktif dimasukkan ke dalam
erlenmeyer 250 ml. Kemudian ditambahkan 10 ml larutan A (60 ml HCl + 20 g
NaOH, ditambahkan aquades hingga 1000 ml) dan secara hati-hati dimasukkan
pula 1 ml larutan B (200 g NaClO2 dalam 1000 ml aquades). Erlenmeyer
dimasukkan ke dalam penangas air dengan suhu 70 ± 20C dan digoyang setiap
30 menit. Pada menit ke 45, 90, dan 150, ditambahkan 1 ml larutan B dan
erlenmeyer digoyang-goyang setiap penambahan larutan B. Sesudah 4 jam,
erlenmeyer dimasukkan ke dalam penangas air es dan ditambahkan 15 ml
aquades es. Seluruh isi erlenmeyer disaring menggunakan cawan saring yang
sudah diketahui berat kosongnya. Untuk membersihkan seluruh isi erlenmeyer,
dilakukan pencucian dengan 100 ml larutan asam asetat 1%. Cawan saring
dihisap dan dicuci dengan 2-5 ml aseton yang dibiarkan menetes keluar karena
beratnya, kemudian dihisap lagi selama 3 menit. Selanjutnya cawan saring
beserta isinya dikeringkan dalam tanur pada suhu 100-1050C dan ditimbang
sampai beratnya konstan.
% 100 % = × ekstraktif bebas serbuk berat sa holoselulo berat sa holoselulo kadar
d. Selulosa (TAPPI T17 wd-70)
Ke dalam Erlenmeyer 300 ml yang berisi 2 g serbuk bebas ekstraktif
ditambahkan 125 ml HNO3 3,5%. Kemudian diekstrak pada waterbath dengan
suhu 80oC selama 12 jam. Setelah itu serbuk disaring dengan cawan saring dan
dikering udarakan. Cawan saring dimasukkan ke dalam gelas piala 200 ml dan
diekstrak pada suhu 50oC selama 2 jam. Setelah itu serbuk kayu dikeluarkan dari
gelas piala, disaring dan ditambahkan NaClO2 10% sampai berwarna putih.
Setelah serbuk berwarna putih, ditambahkan 100 ml CH3COOH 10% dan dicuci
sampai bebas asam. Terakhir ditambahkan 50 ml etanol (C2H5OH). Kemudian
cawan saring beserta isinya dikeringkan dalam tanur pada suhu 100-1050C dan
timbang sampai beratnya konstan.
% 100 % = × ekstraktif bebas serbuk berat selulosa berat selulosa kadar
e. Lignin
Sebanyak 1 g (± 0,1 g) serbuk bebas ekstraktif dipindahkan ke dalam gelas
piala ukuran 1000 ml dan dicernakan dengan 400 ml air panas di atas penangas
air 1000C selama 3 jam. Setelah itu serbuk disaring dengan cawan saring dan
dibiarkan kering. Setelah kering dipindahkan ke dalam gelas piala dan ditutup
dengan gelas arloji. Dengan perlahan sambil diaduk ditambahkan 15 ml H2SO4
72%, lalu didiamkan selama 2 jam dengan sering diaduk. Setelah 2 jam serbuk
dicuci dan dimasukkan ke dalam erlenmeyer 1000 ml. Selanjutnya konsentrasi
asam dibuat menjadi 3% dengan menambahkan 560 ml aquades. Larutan
tersebut lalu didihkan di bawah pendingin tegak selama 4 jam dan diusahakan
agar volume tetap dengan menambah air panas sewaktu-waktu. Setelah
bahan-bahan yang tidak larut dibiarkan mengendap dan disaring dengan cawan saring,
kemudian cawan saring tersebut dicuci dengan air panas hingga bebas dari
asam. Cawan saring beserta isinya dikeringkan dalam tanur pada suhu
100-1050C dan ditimbang hingga beratnya konstan.
% 100 % = × ekstraktif bebas serbuk berat lignin berat lignin kadar
Selanjutnya dilakukan pula analisis struktur lignin dari ketiga jenis kayu
Meshizuka dalam Syafii et al. (1988) yaitu sebagai berikut: kurang lebih 50 mg
serbuk bebar ekstraktif dioksidasi dengan 0,24 ml nitrobenzene dan 4 ml KOH 2
N pada tabung stainless steel selama 2 jam pada suhu 160oC. Setelah 2 jam
untuk menghentikan oksidasi, tabung stainless steel dengan segera didinginkan
pada air yang mengalir untuk menghentikan reaksi. Selanjutnya isinya disaring.
Produk oksidasi yang masih tersisa di dalam tabung dicuci dengan sedikit KOH
0,1 N. Kemudian unsur nitrogen dihilangkan dari larutan alkali dengan
menggunakan kloroform. pH larutan alkali ditetapkan sebesar 2,5 dengan
menambahkan HCl 1 N. Selanjutnya larutan diekstrak dengan 30 ml kloroform
dan ekstraksi diulang sebanyak 4 kali. Selanjutntya ekstrak dianalisis kuantitatif
dengan kromatografi gas pada kondisi sebagai berikut: detektor FID, kolom
carbowax/PEG, panjang kolom 2 m, diameter 0,4 cm, suhu detektor 200oC, suhu
injektor 20oC, suhu kolom 80-180oC (suhu terprogram 5oC/menit dengan
enahanan 5 menit), kecepatan gas pembawa N2 30 ml/menit, gas pembakar H2
1 kg/cm2 dan udara 1kg/cm2. Range 102 dan attenuasi 8. Recorder : integrator
C-R6A.
Penyerangan jamur Phanerochaete chrysosporium Burdsall.
Isolat jamur diperbanyak dalam 10 ml media PDA dan ditumbuhkan selama
6 hari. Setelah itu ke dalam tabung dimasukkan 10 ml aquades steril dan
suspensi spora tersebut kemudian dimasukkan ke dalam masing-masing serbuk
kayu kering udara ukuran lolos 40 mesh tertahan 60 mesh sebanyak 30 g
(berdasar BKT) yang telah disterilisasi. Selain itu untuk meningkatkan kadar air
serbuk hingga sesuai dengan kondisi pertumbuhan jamur (60-90%) ditambahkan
pula 50 ml aquades steril. Serbuk yang telah diberi suspensi jamur kemudian
dilakukan analisis komponen kimia serbuk kayu (selulosa, hemiselulosa, lignin
dan ekstraktif dan abu).
Produksi enzim.
T.viride digoreskan dalam media PDA yang dibuat miring pada tabung
reaksi dan dibiarkan tumbuh pada suhu kamar selama 5 hari. Setelah itu ke
dalam tabung dimasukkan 10 ml aquades steril sehingga diperoleh suspensi
spora. Sebanyak 10% (v/v) suspensi dipipet dan dimasukkan ke dalam 100 ml
media cair yang terdiri dari quades 1 l, (NH4)2SO4 10%, KH2PO4, urea 70%,
CaCl2 10%, MgSO4.7H2O 10%, larutan mineral 1 ml dan tween 80 dan
ditambahkan selulosa teknis sebanyak 1 g serta 0,1 g proteosa pepton pada
erlenmeyer 100 ml. Erlenmeyer ditutup dengan kapas yang dilapisi kain kasa,
lalu ditempatkan pada shaker inkubator dengan kecepatan 5 rpm pada suhu 28
o
C, dan diinkubasi selama 10 hari (Jeffries, 1987). Pada akhir masa inkubasi,
enzim yang dihasilkan dipanen dengan cara memisahkan miselium dari filtrat
menggunakan penyaring vakum yang dilengkapi pompa vakum. Selanjutnya
dilakukan analisis terhadap aktivitas FP-ase dengan metode Somogyi-Nelson
pada suhu 30oC dan pH 5, yaitu sebagai berikut: sebanyak 0,5 ml filtrat enzim
dan 1 ml buffer dimasukkan dalam tabung reaksi dan ditambahkan 50 mg kertas
saring whatman no 1. Campuran tersebut lalu divorteks dan diinkubasi selama 60
menit pada suhu 30oC. Setelah itu 1 ml larutan dipipet dan dimasukkan ke dalam
tabung reaksi yang bersih. Kedalamnya lalu ditambahkan 1 ml reagensia nelson
dan dipanaskan pada penangas air mendidih selama 20 menit. Setelah 20 menit
tabung segera didinginkan hingga suhu mencapai 25oC. Setelah dingin
ditambahkan 1 ml reagensia arsenomolibdat, lalu digojog sampai semua
endapan Cu2O yang ada larut kembali. Kemudian ditambahkan 7 ml air suling
dencitynya (OD) pada panjang gelombang (λ) 540 nm. Kontrol dibuat dari 50 mg
kertas saring whatman no 1, dalam 1 ml buffer dan 0,5 ml enzim tanpa inkubasi.
Blanko terdiri atas 1,5 ml buffer dan 50 mg kertas saring whatman no 1.
Satu unit (U) aktivitas enzim adalah banyaknya enzim yang memproduksi 1
µmol glukosa dalam 1 menit, yang dihitung berdasarkan persamaan berikut :
(
)
enzim ml glukosa mg
FPase
) (
0925 , 0 )
( ×
=
Persiapan inokulum yeast
Isolat yeast Saccharomyces cerevisiae diperbanyak dalam 10 ml media
PDY dan ditumbuhkan selama 1-2 hari (digunakan sebagai stok kultur). Setelah
itu isolat ditumbuhkan lagi pada 50 ml media yang terdiri dari glukosa 10 g/l,
yeast ekstrak 1 g/l, KH2PO4 0,1 g/l, MgSO4.7H2O 0,1 g/l dan (NH4)2SO4 0,1 g/l, di
dalam erlenmeyer 200 ml. Inkubasi dilakukan pada shaker berkecepatan 12 rpm
dengan suhu 30oC selama 24 jam.
Sakarifikasi Fermentasi Simultan
Kondisi proses sakarifikasi fermentasi secara simultan adalah mengikuti
kondisi optimal hasil penelitian Itoh et al. (2003) yang dimodifikasi. Media
sakarifikasi fermentasi (sebanyak kurang lebih 200 ml) adalah terdiri dari: serbuk
kayu yang telah diberi perlakuan jamur P. chrysosporium (biodelignifikasi)
sebanyak 10 g BKT, media nutrient 50 ml (yang terdiri atas (NH4)2HPO4 1 g/l,
MgSO4.7H2O 0,05 g/l dan yeast ekstrak 2 g/l), enzim selulase 5 FPU, 10% (v/v)
inokulum yeast S.cerevisiae, dan 2 ml buffer Na-sitrat (pH 4,8). Serbuk kayu,
media nutrien dan buffer diautoklaf selama 20 menit pada suhu 121oC. Larutan
enzim selulase dan inokulum yeast ditambahkan tan