UJI AKTIVITAS ANTIBAKTERI EKSTRAK
n
-HEKSAN DAN
ETILASETAT SERTA ETANOL DARI TALUS
Kappaphycus
alvarezii
(Doty) TERHADAP BAKTERI
Escherichia coli
dan
Staphylococcus aureus
SKRIPSI
OLEH:
NISA EPALINA SIMARMATA NIM 101524009
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
UJI AKTIVITAS ANTIBAKTERI EKSTRAK
n
-HEKSAN DAN
ETILASETAT SERTA ETANOL DARI TALUS
Kappaphycus
alvarezii
(Doty) TERHADAP BAKTERI
Escherichia coli
dan
Staphylococcus aureus
SKRIPSI
Diajukan untuk melengkapi salah satu syarat untuk memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi
Universitas Sumatera Utara
OLEH:
NISA EPALINA SIMARMATA NIM 101524009
PROGRAM EKSTENSI SARJANA FARMASI
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA
MEDAN
PENGESAHAN SKRIPSI
UJI AKTIVITAS ANTIBAKTERI EKSTRAK
n
-HEKSAN DAN
ETILASETAT SERTA ETANOL DARI TALUS
Kappaphycus
alvarezii
(Doty) TERHADAP BAKTERI
Escherichia coli
dan
Staphylococcus aureus
OLEH:
NISA EPALINA SIMARMATA NIM 101524009
KATA PENGANTAR
Puji dan syukur kehadirat Tuhan Yang Maha Esa, karena limpahan rahmat,
kasih dan karunianNya, sehingga penulis dapat menyelesaikan skripsi ini.
Penelitian ini bertujuan untuk melakukan uji aktivitas antibakteri ekstrak n-heksana,
etilasetat dan etanol dari talus Kappaphycus alvarezii (Doty) terhadap bakteri
Escherichia coli dan Staphylococcus aureus. Skripsi ini diajukan sebagai salah satu
syarat untuk memperoleh gelar sarjana farmasi pada Fakultas Farmasi Universitas
Sumatera Utara.
Pada kesempatan ini penulis mengucapkan terima kasih yang tulus dan
ikhlas kepada Bapak Prof. Dr. Sumadio Hadisahputra, Apt., selaku Dekan Fakultas
Farmasi USU Medan yang telah memberikan fasilitas sehingga penulis dapat
menyelesaikan pendidikan. Ibu Dra. Aswita Hafni Lubis, M.Si., Apt., dan Ibu Dra.
Suwarti Aris, M.Si., Apt., selaku pembimbing yang telah memberikan waktu,
bimbingan dan nasehat selama penelitian hingga selesainya penyusunan skripsi ini.
Ibu Dra. Masfria, M.Si., Apt., Bapak Drs. Awaluddin Saragih, M.Si., Apt., dan Ibu
Dra. Herawati Ginting, M.Si., Apt.,, selaku dosen penguji yang telah memberikan
kritik, saran dan arahan kepada penulis dalam menyelesaikan skripsi ini. Bapak dan
Ibu staf pengajar Fakultas Farmasi USU Medan yang telah mendidik selama
perkuliahan dan Bapak Drs. Syahrial Yoenoes SU., Apt., selaku penasehat
akademis yang telah memberikan bimbingan kepada penulis. Ibu kepala
Laboratorium Fitokimia dan Mikrobiologi yang telah memberikan bantuan dan
fasilitas selama penulis melakukan penelitian.
Penulis juga mengucapkan terima kasih dan penghargaan yang tiada
tercinta, yang tiada hentinya berkorban dengan tulus ikhlas bagi kesuksesan
penulis, juga kepada abang, kakak dan adikku yang selalu setia memberi doa,
dorongan, dan motivasi selama penulis melakukan penelitian.
Penulis menyadari bahwa penulisan skripsi ini masih belum sempurna,
sehingga penulis mengharapkan kritik dan saran yang membangun untuk
penyempurnaannya. Harapan saya semoga skripsi ini dapat bermanfaat bagi ilmu
pengetahuan kefarmasian.
Medan, Februari 2013 Penulis
Nisa Epalina Simarmata
UJI AKTIFITAS ANTIBAKTERI EKSTRAK n-HEKSAN DAN ETILASETAT SERTA ETANOL DARI TALUS Kappaphycus
alvarezii (Doty) TERHADAP BAKTERI Escherichia coli DANStaphylococcus aureus
ABSTRAK
Upaya menggali potensi laut sangat menarik perhatian, bukan saja terhadap pembudidayaannya tetapi juga penelitian mengenai pemanfaatannya diberbagai bidang kehidupan manusia. Salah satu potensi laut tersebut adalah rumput laut
Kappaphycus alvarezii (Doty). Rumput laut mengandung beberapa jenis senyawa metabolit seperti steroid/triterpenoid, saponin, dan glikosida. Rumput laut ini merupakan sumber karagenan yang banyak di manfaatkan industri farmasi sebagai pengental, pengemulsi, pensuspensi, pembentuk gel dan stabilisator.
Penelitian ini meliputi skrining fitokimia dan menguji aktivitas antibakteri ekstrak n-heksana, etilasetat dan etanol rumput laut Kappaphycus alvarezii (Doty), terhadap bakteri Escherichia coli dan Staphylococcus aureus dengan metode difusi agar dengan pencetak lubang (Punch hole). Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak n-heksana tidak memiliki kemampuan menghambat pertumbuhan bakteri Escherichia coli dan Staphylococcus aureus, sedangkan ekstrak etilasetat dan etanol memiliki kemampuan menghambat pertumbuhan bakteri Escherichia coli dan bakteri Staphylococcus aureus.
Ekstrak etilasetat memiliki kemampuan menghambat pertumbuhan bakteri
Escherichia coli dengan daya hambat pada konsentrasi 300 mg/ml yaitu 14,51 mm dan kadar hambat minimumnya pada konsentrasi 100 mg/ml yaitu 9,52 mm sedangkan untuk bakteri Staphylococcus aureus konsentrasi 400 mg/ml yaitu 14 mm dan kadar hambat minimumnya pada konsentrasi 100 mg/ml yaitu 9 mm. untuk ekstrak etanol daya hambatnya lemah dengan daya hambat pada konsetrasi 500 mg/ml yaitu 10 mm dan kadar hambat minimumnya pada konsentrasi 300 mg/ml yaitu 7,5 mm untuk bakteri Escherichia coli, sedangkan untuk bakteri
Staphylococcus aureus daya hambat pada konsentrasi 500 mg/ml yaitu 10,5 mm dan kadar hambat minimumnya pada konsentrasi 300 mg/ml yaitu 7,31 mm.
Kata kunci: Talus Kappaphycus alvarezii (Doty), antibakteri, Escherichia coli,
TEST ACTIVITY ANTIBACTERIAL EXTRACT n-HEKSAN AND ETHYLACETATE WITH ETHANOL FROM THALLUS
Kappaphycus alvarezii (Doty) AGAINST BACTERIA Staphylococcus aureus AND Escherichia coli
ABSTRACT
Efforts to explore the potential of the sea are very interesting, not only for cultivation but also research on its use in various fields of human life. One potential ocean is seaweed Kappaphycus alvarezii (Doty). Seaweed contains several types of
metabolites compounds such as steroids/triterpenoids, saponins, and glycosides. Seaweed is a source of carrageenan are widely utilized in the pharmaceutical industry as a thickener, emulsifier, suspending agent, forming gels and stabilizers.
Study include screening phytochemical and testing the activity of antibacterial extracts of n-hexane, ethylacetate and ethanol seaweed Kappaphycus alvarezii (Doty). the bacterium Escherichia coli and Staphylococcus aureus by agar diffusion method with the printer hole (hole punch). The test results the activity antibacterial of showed that n-hexane extract did not have the ability to inhibit the growthof bacteria Escherichia coli and Staphylococcus aureus, while extracts ethylacetate and ethanol have the ability to inhibit the growth of bacteria
Escherichia coli and Staphylococcus aureus.
Extract ethylacetate has the ability to inhibit the growth of Escherichia coli
with the inhibition at a concentration of 300 mg/ml is 14,51 mm and the levels inhibitory minimum at a concentration of 100 mg/ml which is 9.52 mm, while for the bacteria Staphylococcus aureus concentration of 400 mg /ml at 14 mm and the levels inhibitory minimum of concentration 100 mg /ml which is 9 mm. Extract ethanol weak inhibition of the inhibition at concentrations of 500 mg/ml which is 10 mm and the minimum inhibitory concentration levels of 300 mg/ml at 7.5 mm for the bacterium Escherichia coli, Staphylococcus aureus while the inhibition at concentrations of 500 mg/ml is 10.5 mm and the minimum inhibitory levels on the concentration of 300 mg/ml which is 7.31 mm.
DAFTAR ISI
Halaman
JUDUL ... i
HALAMAN JUDUL ... ii
PENGESAHAN SKRIPSI ... iii
KATA PENGANTAR ... iv
ABSTRAK ... vi
ABSTRACT ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1
1.1 Latar belakang ... 1
1.2 Perumusan masalah ... 3
1.3 Hipotesis ... 3
1.4 Tujuan penelitian ... 4
1.5 Manfaat penelitian ... 4
1.6 Kerangka konsep penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1 Uraian Tanaman ... 6
2.1.1 Habitat dan sebaran rumput laut ... 6
2.1.2 Perkembangbiakan rumput laut ... 6
2.1.3 Sistematika tumbuhan ... 7
2.1.5. Morfologi tumbuhan ... 8
2.5.2 Fase pertumbuhan bakteri ... 15
2.5.3 Media pertumbuhan bakteri ... 16
2.5.4 Metode isolasi biakan bakteri ... 18
2.5.5 Pengukuran aktifitas antimikroba ... 18
BAB III METODE PENELITIAN ... 20
3.3 Pengumpulan dan Pengolahan Sampel ... 22
3.4.3 Pemeriksaan steroid/triterpenoid ... 24
3.4.4 Pemeriksaan flavonoid ... 25
3.4.5 Pemeriksaan tanin ... 25
3.4.6 Pemeriksaan saponin ... 25
3.4.7 Pemeriksaan antrakinon ... 25
3.5 Pembuatan Ekstrak n-Heksan, Etilasetat, dan Etanol Secara Perkolasi Berkesinambungan ... 26
3.6 Sterilisasi Alat dan Media ... 26
3.8.1.2 Bakteri Staphylococcus aureus ... 28
3.8.2.1 Bakteri Escherichia coli ... 28
3.8.2.2 Bakteri Staphylococcus aureus ... 29
3.9 Pembuatan Larutan Uji Ekstrak n-Heksana, Ekstrak Etilasetat, Ekstrak Etanol Dengan Berbagai Konsentrasi ... 29
3.10 Metode Pengujian Efek Antibakteri Secara Invitro ... 29
3.10.1 Bakteri Escherichia coli ... 29
3.10.2 Bakteri Staphylococcus aureus ... 30
BAB IV HASIL DAN PEMBAHASAN ... 31
4.1 Hasil Identifikasi Tumbuhan ... 31
4.2 Hasil Skrining Fitokimia ... 31
4.3 Hasil Ekstraksi ... 32
4.4 Hasil Uji Aktivitas Antibakteri Ekstrak n-Heksan, Etilasetat, Etanol terhadap Staphylococcus aureus dan Escherichia coli 32 BAB V KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan ... 36
5.2 Saran ... 36
DAFTAR PUSTAKA ... 37
DAFTAR TABEL
Tabel Halaman
4.1 Hasil skrining fitokimia terhadap serbuk simplisia Kappaphycus alvarezii (Doty) ... 31
4.2 Hasil pengukuran diameter daerah hambatan pertumbuhan
Escherichia coli oleh ekstrak etilasetat, ekstrak etanol…………. 32
4.3 Hasil pengukuran diameter daerah hambatan pertumbuhan
DAFTAR LAMPIRAN
7 Bagan uji aktivitas antibakteri ekstrak n-heksan, ekstrak etilasetat, ekstrak etanol rumput laut Kappaphycus alvarezii (Doty) ... 46
8. Hasil pengukuran diameter daerah hambatan pertumbuhan bakteri oleh ekstrak n-heksan ... 47
9 Hasil pengukuran diameter daerah hambatan pertumbuhan bakteri oleh ekstrak etilasetat ... 47
10 Hasil pengukuran diameter daerah hambatan pertumbuhan bakteri oleh ekstrak etanol ... 48
11 Gambar hasil uji aktivitas antibakteri dengan konsentrasi 500mg/ml .. 49
12 Gambar hasil uji aktivitas antibakteri ekstrak etilasetat terhadap Eacherichia coli ... 50
13 Gambar hasil uji aktivitas antibakteri ekstrak etilasetat terhadap bakteri Staphylococcus aureus ... 52
14 Gambar hasil uji aktivitas antibakteri ekstrak etanol terhadap bakteri Escherichia coli ... 54
15 Gambar hasil uji aktivitas antibakteri ekstrak etanol terhadap bakteri Staphylococcus aureus ... 55
UJI AKTIFITAS ANTIBAKTERI EKSTRAK n-HEKSAN DAN ETILASETAT SERTA ETANOL DARI TALUS Kappaphycus
alvarezii (Doty) TERHADAP BAKTERI Escherichia coli DANStaphylococcus aureus
ABSTRAK
Upaya menggali potensi laut sangat menarik perhatian, bukan saja terhadap pembudidayaannya tetapi juga penelitian mengenai pemanfaatannya diberbagai bidang kehidupan manusia. Salah satu potensi laut tersebut adalah rumput laut
Kappaphycus alvarezii (Doty). Rumput laut mengandung beberapa jenis senyawa metabolit seperti steroid/triterpenoid, saponin, dan glikosida. Rumput laut ini merupakan sumber karagenan yang banyak di manfaatkan industri farmasi sebagai pengental, pengemulsi, pensuspensi, pembentuk gel dan stabilisator.
Penelitian ini meliputi skrining fitokimia dan menguji aktivitas antibakteri ekstrak n-heksana, etilasetat dan etanol rumput laut Kappaphycus alvarezii (Doty), terhadap bakteri Escherichia coli dan Staphylococcus aureus dengan metode difusi agar dengan pencetak lubang (Punch hole). Hasil uji aktivitas antibakteri menunjukkan bahwa ekstrak n-heksana tidak memiliki kemampuan menghambat pertumbuhan bakteri Escherichia coli dan Staphylococcus aureus, sedangkan ekstrak etilasetat dan etanol memiliki kemampuan menghambat pertumbuhan bakteri Escherichia coli dan bakteri Staphylococcus aureus.
Ekstrak etilasetat memiliki kemampuan menghambat pertumbuhan bakteri
Escherichia coli dengan daya hambat pada konsentrasi 300 mg/ml yaitu 14,51 mm dan kadar hambat minimumnya pada konsentrasi 100 mg/ml yaitu 9,52 mm sedangkan untuk bakteri Staphylococcus aureus konsentrasi 400 mg/ml yaitu 14 mm dan kadar hambat minimumnya pada konsentrasi 100 mg/ml yaitu 9 mm. untuk ekstrak etanol daya hambatnya lemah dengan daya hambat pada konsetrasi 500 mg/ml yaitu 10 mm dan kadar hambat minimumnya pada konsentrasi 300 mg/ml yaitu 7,5 mm untuk bakteri Escherichia coli, sedangkan untuk bakteri
Staphylococcus aureus daya hambat pada konsentrasi 500 mg/ml yaitu 10,5 mm dan kadar hambat minimumnya pada konsentrasi 300 mg/ml yaitu 7,31 mm.
Kata kunci: Talus Kappaphycus alvarezii (Doty), antibakteri, Escherichia coli,
TEST ACTIVITY ANTIBACTERIAL EXTRACT n-HEKSAN AND ETHYLACETATE WITH ETHANOL FROM THALLUS
Kappaphycus alvarezii (Doty) AGAINST BACTERIA Staphylococcus aureus AND Escherichia coli
ABSTRACT
Efforts to explore the potential of the sea are very interesting, not only for cultivation but also research on its use in various fields of human life. One potential ocean is seaweed Kappaphycus alvarezii (Doty). Seaweed contains several types of
metabolites compounds such as steroids/triterpenoids, saponins, and glycosides. Seaweed is a source of carrageenan are widely utilized in the pharmaceutical industry as a thickener, emulsifier, suspending agent, forming gels and stabilizers.
Study include screening phytochemical and testing the activity of antibacterial extracts of n-hexane, ethylacetate and ethanol seaweed Kappaphycus alvarezii (Doty). the bacterium Escherichia coli and Staphylococcus aureus by agar diffusion method with the printer hole (hole punch). The test results the activity antibacterial of showed that n-hexane extract did not have the ability to inhibit the growthof bacteria Escherichia coli and Staphylococcus aureus, while extracts ethylacetate and ethanol have the ability to inhibit the growth of bacteria
Escherichia coli and Staphylococcus aureus.
Extract ethylacetate has the ability to inhibit the growth of Escherichia coli
with the inhibition at a concentration of 300 mg/ml is 14,51 mm and the levels inhibitory minimum at a concentration of 100 mg/ml which is 9.52 mm, while for the bacteria Staphylococcus aureus concentration of 400 mg /ml at 14 mm and the levels inhibitory minimum of concentration 100 mg /ml which is 9 mm. Extract ethanol weak inhibition of the inhibition at concentrations of 500 mg/ml which is 10 mm and the minimum inhibitory concentration levels of 300 mg/ml at 7.5 mm for the bacterium Escherichia coli, Staphylococcus aureus while the inhibition at concentrations of 500 mg/ml is 10.5 mm and the minimum inhibitory levels on the concentration of 300 mg/ml which is 7.31 mm.
BAB I
PENDAHULUAN
1.1 Latar Belakang
Infeksi merupakan masuknya mikroorganisme ke dalam tubuh, kemudian
berkembang biak dan menimbulkan penyakit (Pratiwi, 2008). Perkembangan
infeksi di Indonesia yang beriklim tropis disebabkan oleh udara yang lembab,
sanitasi yang kurang, lingkungan yang padat penduduk dan tingkat sosial ekonomi
yang rendah. mikroorganisme yaitu bakteri, jamur dan virus (Tjay, 2002). Bakteri
merupakan organisme bersel tunggal yang berkembang biak dengan pembelahan
menjadi dua sel secara terus-menerus (Gibson, 1996).
Rumput laut tergolong tumbuhan tingkat rendah, umumnya tumbuh melekat
pada substrat tertentu, tidak mempunyai akar, batang maupun daun sejati, tetapi
hanya menyerupai batang yang disebut talus. Rumput laut tumbuh dialam dengan
melekatkan dirinya pada karang, lumpur, pasir, batu, dan benda keras lainnya.
Selain benda mati rumput laut dapat melekat pada tumbuhan lain (Anggadiredja,
dkk., 2010).
Algae laut atau rumput laut atau memiliki potensi sebagai antibakteri, salah
satunya yang dilaporkan yaitu ekstrak metanol dari 56 rumput laut yang berasal dari
kelas Chlorophyta (algae hijau), Phaeophyta (algae coklat) dan Rhodophyta (algae
merah). Dari ketiga kelas rumput laut tersebut, yang mempunyai antibakteri paling
tinggi terdapat pada kelas Phaeophyta (Choudhury, et. al.,2005).
Jenis rumput laut Kappaphycus alvarezii dan Eucheuma denticullatum
mempunyai daya antibakteri. Ekstrak metanol Eucheuma denticullatum dan ekstrak
untuk dikembangkan sebagai antibakteri, hal ini ditunjukkan oleh diameter zona
penghambatan, yaitu pada ekstrak Eucheumadenticullatum dengan pelarut metanol
memiliki diameter zona penghambatan sebesar 19,43 mm terhadap bakteri
Aeromonas hydrophila dan 19,85 mm terhadap bakteri Vibrio harveyii. Ekstrak
metanol Kappaphycus alvarezii memiliki diameter zona penghambatan sebesar
16,60 mm terhadap bakteri Aeromonas hydrophila dan 16,33 mm terhadap bakteri
Vibrio harveyii. Senyawa antibakteri dominan yang terdapat pada ekstrak metanol
Eucheuma denticullatum senyawa turunan asam karboksilat yaitu hexadecanoid
acid, 9-octadecanoid acid dan senyawa turunan keton steroid yaitu cholest-5-ene,
3-bromo. Senyawa antibakteri dominan yang terdapat pada ekstrak metanol
Kappaphycus alvarezii senyawa turunan asam karboksilat yaitu hexadecanoid acid,
octadecanoid acid dan senyawa turunan keton steroid yaitu holest-5-ene, 3-bromo,
holest-5-en-3-ol-bromo, holest-5-en-3-ol-beta (Wiyanto, 2010).
Penerapan teknologi memberikan kemungkinan melakukan isolasi metabolit
sekunder dari rumput laut. Rumput laut menghasilkan metabolit sekunder dengan
variasi struktur senyawa biologi aktif. Alga merah mengandung senyawa terpen dan
senyawa asetogenin. Senyawa metabolit sekunder menunjukan aktifitas
antimikroba, bersifat toksik (Anggadiredja, dkk., 2010). Rumput laut Kappaphycus
alvarezii (Doty) memiliki kandungan kimia karagenan (Munthe, 2012).
Berdasarkan uraian di atas, maka dilakukan penelitian mengenai aktivitas
antibakteri terhadap talus Kappaphycus alvarezii (Doty) dengan menggunakan
bakteri Escherichia coli dan Staphylococcus aureus karena bakteri ini masing-masing
mewakili bakteri gram negatif dan gram positif. Penelitian ini meliputi skrining
fitokimia dan pembutan ekstrak rumput laut jenis Kappaphycus alvarezii (Doty)
perkolasi berkesinambungan, selanjutnya masing-masing ekstrak diuji aktivitas
antibakteri dengan metode difusi agar menggunakan punch hole dan diukur dengan
jangka sorong.
1.2 Perumusan Masalah
Perumusan masalah dari peneltian ini adalah:
a. Apakah golongan senyawa kimia yang terdapat dari serbuk simplisia talus
Kappaphycus alvarezii (Doty)?
b. Apakah ekstrak n-heksana, ekstrak etilasetat, dan ekstrak etanol talus
Kappaphycus alvarezii (Doty) mempunyai aktivitas antibakteri terhadap
Escherichia coli, dan Staphylococcus aureus?
1.3 Hipotesis
Hipotesa dari penelitian ini adalah:
a. Golongan senyawa kimia dari simplisia talus Kappaphycus alvarezii (Doty)
dapat diketahui dengan melakukan skrining fitokimia.
b. Ekstrak n-heksana, ekstrak etilasetat, dan ekstrak etanol mempunyai
aktivitas antibakteri terhadap bakteri Escherichia coli dan Staphylococcus
1.4 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
a. Untuk mengetahui golongan senyawa kimia dari serbuk simplisia talus
Kappaphycus alvarezii (Doty).
b. Untuk mengetahui aktivitas antibakteri dari ekstrak n-heksana, ekstrak
etilasetat dan ekstrak etanol talus Kappaphycus alvarezii (Doty), serta
konsentrasi hambat minimumnya terhadap bakteri Escherichia coli dan
Staphylococcus aureus.
1.5 Manfaat
Manfaatdari penelitian ini adalah:
Hasil penelitian ini diharapkan dapat memberikan informasi tentang efek
antibakteri dari ekstrak n-heksana, ekstrak etilasetat, dan ekstrak etanol dari talus
Kappaphycus alvarezii (Doty) serta konsentrasi hambat minimumnya terhadap
1.6 Kerangka Konsep Penelitian
Penelitian dilaksanakan dengan kerangka konsep seperti ditunjukkan dalam
bagan berikut:
Variabel bebas variabel terikat parameter
Serbuk simplisia
Ekstrak n-heksana
Ekstrak etilasetat
Ekstrak etanol
Penentuan golongan senyawa kimia
1. Alkaloida 2. Flavonoida 3. Tanin 4. Saponin
5. Steroida/Triterpenoida 6. Glikosida
Uji aktifitas bakteri
Escherichia coli
dan Staphylococcus
aureus
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tanaman
Rumput laut atau alga termasuk divisi Thallophyta (tumbuhan bertalus)
karena mempunyai struktur kerangka tubuh (morfologi) yang tidak berdaun,
berbatang dan berakar semuanya hanya terdiri dari talus saja (Aslan, 1998).
2.1.1 Habitat dan sebaran rumput laut
Pertumbuhan dan penyebaran rumput laut sangat dipengaruhi oleh factor
lingkungan, seperti substrat, salinitas, temperatur, intensitas cahaya, tekanan dan
nutrisi. Umumnya tumbuh baik didaerah pantai terumbu, karena ditempat inilah
beberapa persyaratan untuk pertumbuhannya banyak terpenuhi, rumput laut ini
lebih menyukai variasi suhu harian yang kecil dan substrat karang mati. Rumput
laut ini tumbuh mengelompok dengan berbagai jenis rumput laut lainya
(Anggadiredja, dkk., 2010).
Kappaphycus alvarezii (Doty) umumnya terdapat didaerah tertentu dengan
persyaratan khusus, kebanyakan tumbuh didaerah pasang surut (intertidal) atau
pada daerah yang selalu terendam air (subtidal) melekat pada substrat didasar
perairan yang berupa karang mati, karang hidup, batu gamping atau cangkang
moluska (Aslan, 1998).
2.1.2 Perkembangbiakan rumput laut
Perkembangbiakan rumput laut dapat terjadi melalui dua cara, yaitu secara
vegetatif dengan talus diploid yang menghasilkan spora. Perbanyakan secara
vegetatif dikembangkan dengan cara stek, yaitu potongan talus yang kemudian
dikembangkan melalui spora baik alami maupun melalui budidaya. Pertemuan dua
gamet membentuk zygot yang selanjutnya berkembang menjadi sporofit, individu
inilah yang mengeluarkan spora dan berkembang melalui pembelahan dalam
sporagenesis menjadi gametofit (Anggadiredja, dkk., 2010; Winarno, 1990).
Faktor biologi utama yang menjadi pembatas produktifitas rumput laut yaitu
faktor persaingan dan pemangsa dari hewan herbifore, selain itu dapat pula
dihambat oleh faktor mobiditas dan mortalitas rumput laut itu sendiri. Morbiditas
dapat disebabkan oleh penyakit akibat infeksi dari mikroorganisme, tekanan
lingkungan perairan (fisika dan kimia perairan) yang buruk, serta tumbuhnya
tanaman menempel (parasit). Mortalitas dapat disebabkan oleh pemangsaan
hewan-hewan herbivora (Aslan, 1998).
2.1.3 Sistematika tumbuhan
Berdasarkan hasil identifikasi LIPI, taksonomi rumpput laut Kappaphycus
alvarezii (Doty) adalah sebagai berikut:
Divisi : Rhodophyta
Kelas : Rhodophyceae
Bangsa : Gigartinales
Suku : Solieriaceae
Marga : Kappaphycus
Spesies : Kappaphycus alvarezii (Doty).
2.1.4 Nama daerah
Nama (dagang) yang lebih dikenal untuk Kappaphycus alvarezii (Doty)
yaitu Eucheuma cottonii dan Eucheuma alvarezii. Nama daerahnya untuk
2.1.5 Morfologi tumbuhan
Dari segi morfologinya, rumput laut tidak memperlihatkan adanya
perbedaan antara akar, batang dan daun. Secara keseluruhan, tanaman ini
mempunyai morfologi yang mirip, walapun sebenarnya berbeda. Bentuk-bentuk
tersebut sebenarnya hanya talus (Aslan, 1998; Winarno, 1990).
Ciri fisik Kappaphycus alvarezii ditandai oleh talus silindris dengan
permukaan licin dan cartilogenous. Warna talus tidak selalu tetap, kadang-kadang
berwarna hijau, kuning, abu-abu atau merah. Perubahan warna sering terjadi karena
pengaruh faktor lingkungan. Kejadian ini merupakan suatu proses adaptasi
kromatik yaitu penyesuaian antara proporsi pigmen dengan berbagai kualitas
pencahayaan. Percabangan talus berujung runcing atau tumpul, ditumbuhi nodulus
(tonjolan-tonjolan) dan duri untuk melindungi gametangia. Percabangan bersifat alternates
(berseling), tidak teratur serta dapat bersifat dichotomus (percabangan dua) atau
trichotomus (system percabangan tiga) (Anggadiredja, dkk.,2010; Largo, et. al.,1995).
2.2 Kandungan kimia
Jenis rumput laut termasuk dalam kelas Rhodophyceae (alga merah)
mengandung saponin, glikosida dan steroid/triterpenoid. Rumput laut ini juga
mengandung pigmen antara lain adalah klorofil a, klorofil d, α dan β karoten, lutein,
zeaxanthin, fikosianin dan fikoeritrin. Fikoeritrin merupakan pigmen yang dominan
yang menyebabkan warna merah pada alga merah (Dawes, 1981).
2.3 Ekstraksi
Ekstraksi adalah suatu proses yang dilakukan untuk memperoleh kandungan
kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani
menurut cara yang cocok, di luar pengaruh cahaya matahari langsung, ekstrak
kering harus mudah digerus menjadi serbuk. Cairan penyari yang digunakan air,
etanol dan campuran air etanol (Depkes, 1979).
Ekstrak adalah sediaan kering, kental atau cair yang dibuat dari simplisia
nabati atau hewani dengan cara yang sesuai diluar pengaruh cahaya matahari
langsung (Ditjen POM, 1979).
2.3.1 Metode ekstraksi
Menurut Ditjen POM (2000), ada beberapa metode ekstraksi:
1. Cara Dingin
a. Maserasi
Maserasi adalah proses pengekstraksian simplisia menggunakan pelarut
dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan.
Maserasi kinetik di lakukan dengan pengadukan yang kontinu (terus-menerus).
Remaserasi dilakukan dengan pengulangan penambahan pelarut setelah di
lakukan penyaringan maserat pertama dan seterusnya.
b. Perkolasi
Perkolasi adalah ekstraksi dengan menggunakan pelarut yang selalu baru
sampai penyarian sempurna, umumnya di lakukan pada temperatur ruangan. Proses
ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara, dan tahap
perkolasi sebenarnya (penetesan/penampungan ekstrak) yang terus menerus sampai
ekstrak yang diinginkan habis tersari. Tahap pengembangan bahan dan maserasi
antara di lakukan dengan maserasi serbuk menggunakan cairan penyari
sekurang-kurangnya 3 jam. hal ini penting terutama untuk serbuk yang keras dan bahan yang
2. Cara Panas
a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut yang relatif konstan dengan adanya
pendingin balik.
b. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, umumnya
dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dan jumlah pelarut
relatif konstan dengan adanya pendingin balik.
c. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang
lebih tinggi dari temperatur ruangan yaitu pada temperature 40-500C.
d. Infudasi
Infudasi adalah ekstraksi dengan pelarut air pada temperatur penangas air
mendidih, temperatur terukur 96-98oC selama waktu tertentu (15-20 menit).
2.4 Sterilisasi
Sterilisasi merupakan proses penghilangan semua jenis organisme hidup,
yang terdapat pada/di dalam suatu benda. Cara-cara sterilisasi yaitu:
a. Sterilisasi dengan bahan kimia, contoh: senyawa fenol dan turunannya.
Desinfektan ini digunakan misalnya untuk membersihkan area tempat
bekerja.
b. Sterilisasi kering digunakan untuk alat-alat gelas misalnya cawan petri,
tabung reaksi waktu sterilisasi selama 2-3 jam dan berdaya penetrasi rendah.
pembakaran dengan api dari Bunsen dengan temperatur sekitar 350oC, dan
dengan udara panas oven yang lebih sederhana dan murah dengan
temperature sekitar 160-170oC.
c. Sterilisasi basah, biasanya menggunakan uap panas bertekanan dalam
autoklaf. Media biakan, larutan dan kapas dapat disterilkan dengan cara ini.
Autoklaf merupakan suatu alat pemanas bertekanan tinggi, dengan
meningkatnya suhu air maka tekanan udara akan bertambah dalam autoklaf
yang tertutup rapat. Sejalan dengan meningkatnya tekanan di atas tekanan
udara normal, titik didih air meningkat. Biasanya pemanasan autoklaf
berada pada suhu 121o C selama 15 menit.
d. Filtrasi bakteri, digunakan untuk mensterilkan bahan-bahan yang terurai
atau tidak tahan panas. Metode ini didasarkan pada proses mekanik yaitu
menyaring semua bakteri dari bahan dengan melewatkan larutan tersebut
melalui lubang saringan yang sangat kecil (Pratiwi, 2008).
2.5 Bakteri
Nama bakteri berasal dari kata “bakterion” (bahasa Yunani) yang berarti
tongkat atau batang, sekarang namanya dipakai untuk menyebutkan sekelompok
mikroorganisme yang bersel satu, berkembang biak dengan pembelahan diri,
berukuran kecilnya sehingga hanya tampak dengan mikroskop (Dwidjoseputro,
1987).
Pertumbuhan dan perkembangan bakteri di pengaruhi oleh:
a. Temperatur
Pertumbuhan bakteri sangat dipengaruhi oleh temperatur. Setiap
kecepatan pertumbuhan optimal dan dihasilkan jumlah sel yang maksimal.
Temperatur yang terlalu tinggi dapat menyebabkan denaturasi protein sedangkan
temperatur yang sangat rendah aktivitas enzim akan terhenti. Berdasarkan batas
temperatur dibagi atas tiga golongan:
1. Psikrofil, tumbuh pada temperatur -5 sampai 30 dengan optimum 10 sampai
20oC.
2. Mesofil, tumbuh pada temperatur 10 sampai 45 dengan optimum 20 sampai
40oC.
3. Termofil, tumbuh pada termperatur 25 sampai 80 dengan optimum 50
sampai 60oC (Pratiwi, 2008).
b. Keasaman dan kebasaan (pH)
PH optimum bagi kebanyakan bakteri terletak antara 6,5 dan 7,5. Namun
ada beberapa mikroorganisme yang dapat tumbuh pada keadaan yang sangat asam
atau alkali (Pratiwi, 2008).
c. Tekanan osmosis
Osmosis merupakan perpindahan air melewati membran semipermeabel
karena ketidak seimbangan material terlarut dalam media. Medium yang baik untuk
pertumbuhan sel adalah medium isotonis terhadap sel tersebut. Dalam larutan
hipotonik air akan masuk ke dalam sel sehingga menyebabkan sel membengkak,
sedangkan dalam larutan hipertonik air akan keluar dari sel sehingga membran
plasma mengerut dan lepas dari dinding sel (plasmolisis) (Pratiwi, 2008; Lay,
1994).
d. Oksigen
Berdasarkan kebutuhan oksigen di kenal mikroorganisme menjadi 5
Anaerob obligat, hidup tanpa oksigen, oksigen toksik terhadap golongan ini.
Anaerob aerotoleran, tidak mati dengan adanya oksigen.
Anaerob fakultatif, mampu tumbuh baik dalam suasana dengan atau tanpa
oksigen.
Aerob obligat, tumbuh subur bila ada oksigen dalam jumlah besar.
Mikroaerofilik, hanya tumbuh baik dalam tekanan oksigen yang rendah
(Pratiwi, 2008).
e. Nutrisi
Nutrisi merupakan substansi yang diperlukan untuk biosintesis dan
pembentukan energi. Berdasarkan kebutuhannya, nutrisi dibedakan menjadi dua
yaitu makroelemen (elemen yang diperlukan dalam jumlah banyak) dan
mikroelemen (trace element yaitu elemen nutrisi yang diperlukan dalam jumlah
sedikit) (Pratiwi, 2008).
2.5.1 Morfologi bakteri
Berdasarkan bentuk morfologinya, maka bakteri dapat di bagi atas tiga
golongan yaitu :
A. Golongan basil
Golongan basil berbentuk serupa tongkat pendek, silindris. Basil dapat
bergandengan dua-dua, atau terlepas satu sama lain, yang bergandeng-gandengan
panjang disebut streptobasil, yang dua-dua disebut diplobasil.
B. Bentuk kokus
Golongan kokus merupakan bakteri yang bentuknya serupa bola-bola kecil.
Golongan ini tidak sebanyak golongan basil. Kokus ada yang
diplokokus, ada yang mengelompok berempat, disebut tetrakokus, kokus yang
mengelompok serupa kubus disebut sarsina.
C. Golongan spiril
Golongan spiril merupakan bakteri yang bengkok atau berbengkok-bengkok
serupa spiral. Bakteri ini tidak banyak terdapat, karena itu merupakan golongan
yang paling kecil, jika dibandingkan dengan golongan kokus maupun golongan
basil (Dwidjoseputro, 1987).
a. Bakteri Escherichia coli
Sistematika bakteri Escherichia coli menurut (Gembong, 1987) adalah
sebagai berikut :
Divisi : Schizophyta
Kelas : Schizomycetes
Bangsa : Eubacteriales
Familia : Enterobacteriaceae
Genus : Escherichia
Species : Escherichia coli
Escherichia coli disebut juga Bacterium coli, merupakan bakteri gram
negatif, aerob atau anaerob fakultatif, panjang 1-4 µm, lebar 0,4-1,7 µm, berbentuk
batang, tidak bergerak. Bakteri ini tumbuh baik pada suhu 370C tetapi dapat tumbuh
pada suhu 8-400C, membentuk koloni yang bundar, cembung, halus dan dengan
tepi rata. Eschericia coli biasanya terdapat dalam saluran cerna sebagai flora
normal. Bakteri ini dapat menjadi patogen bila berada diluar usus atau dilokasi lain
b. Bakteri Staphylococcus aureus
Sistematika bakteri Staphylococcus aureus menurut (Gembong, 1987)
adalah sebagai berikut :
Divisi : Schizophyta
Kelas : Schizomycetes
Bangsa : Eubacteriales
Familia : Micrococcaceae
Genus : Staphylococcus
Species : Staphylococcus aureus
Staphylococcus aureus merupakan bakteri gram positif, aerob atau anaerob
fakultatif berbentuk bola atau kokus berkelompok tidak teratur, diameter 0,8 – 1,0
µm, tidak membentuk spora dan tidak bergerak, koloni berwarna kuning. Bakteri
ini tumbuh cepat pada suhu 370C membentuk pigmen pada suhu 20-250C paling
baik.Koloni pada pembenihan padat berbentuk bulat halus, menonjol dan berkilau
membentuk berbagai pigmen. Bakteri ini terdapat pada kulit, selaput berkembang
biak dan menyebar luas dalam jaringan (Jawetz, dkk., 2001).
2.5.2 Fase pertumbuhan bakteri
Bakteri mengalami pertumbuhan yang dapat dibagi dalam 4 fase menurut
(Pratiwi, 2008; Dwidjoseputro, 1994) yaitu:
1. Fase lag
Pada saat dipindahkan ke media yang baru, bakteri tidak langsung tumbuh
dan membelah, meskipun kondisi media sangat mendukung untuk pertumbuhan.
Bakteri biasanya akan mengalami masa penyesuaian untuk menyeimbangkan
2. Fase log
Selama fase ini, populasi meningkat dua kali pada interval waktu yang
teratur. Jumlah koloni bakteri akan terus bertambah seiring lajunya aktivitas
metabolisme sel.
3. Fase tetap
Pada fase ini terjadi kompetisi antara bakteri untuk memperoleh nutrisi dari
media untuk tetap hidup. Sebagian bakteri mati sedangkan yang lain tumbuh dan
membelah sehingga jumlah sel bakteri yang hidup menjadi tetap.
4. Fase kematian
Pada fase ini, sel bakteri akan mati lebih cepat daripada terbentuknya sel
baru. Laju kematian mengalami percepatan yang eksponensial.
2.5.3 Media pertumbuhan bakteri
Media pertumbuhan bakteri dapat dikelompokkan dalam beberapa kategori,
yaitu:
a. Berdasarkan asalnya, media dibagi atas:
1. Media sintetik yaitu media yang kandungan dan isi bahan yang ditambahkan
diketahui secara terperinci. Contoh: Nutrien agar.
2. Media non-sintetik yaitu media yang kandungan dan isinya tidak diketahui
secara terperinci dan menggunakan bahan yang terdapat di alam. Contohnya:
ekstrak daging, pepton (Lay, 1994).
b. Berdasarkan kegunaannya, dapat dibedakan menjadi:
1. Media selektif
Media selektif adalah media biakan yang mengandung paling sedikit satu
diinginkan dan membolehkan perkembang biakan mikroorganisme tertentu yang
ingin diisolasi.
2. Media diferensial
Media ini digunakan untuk menyeleksi suatu mikroorganisme dari berbagai
jenis dalam suatu lempengan agar.
3. Media diperkaya
Media ini digunakan untuk menumbuhkan mikroorganisme yang diperoleh
dari lingkungan alami karena jumlah mikroorganisme yang ada terdapat dalam
jumlah sedikit (Lay, 1994).
c. Berdasarkan konsistensinya, dibagi atas:
1. Media padat/ solid, diperoleh dengan cara menambahkan agar-agar. Agar
berasal sari ganggang/alga yang berfungsi sebagai bahan pemadat. Alga
digunakan karena bahan ini tidak diuraikan oleh mikroorganisme, dan dapat
membeku pada suhu di atas 45o C. Media padat dapat berupa bahan organik
alamiah, misalnya media yang dibuat dari bahan kentang dan wortel. Media
padat biasanya digunakan untuk mengamati penampilan atau morfologi koloni
dan untuk mengisolasi biakan murni.
2. Media semi solid, dibuat denngan bahan yang sama dengan media padat, akan
tetapi yang berbeda adalah komposisi agarnya. Media ini digunakan untuk
melihat gerak kuman secara mikroskopik dan kemampuan fermentasi.
3. Media cair dapat digunakan untuk berbagai tujuan seperti pembiakan mikroba
dalam jumlah besar, kemampuan fermentasi, dan berbagai macam uji.
Beberapa contoh media cair adalah kaldu nutrient, kaldu glukosa, air pepton,
2.5.4 Metode isolasi biakan bakteri
1. Cara gores
Ose yang telah steril dicelupkan ke dalam suspensi mikroorganisme yang
diencerkan, lalu dibuat serangkaian goresan sejajar yang tidak saling menutupi di
atas permukaan agar yang telah padat.
2. Cara sebar
Suspensi mikroorganisme yang telah diencerkan diinokulasikan secara
merata dengan menggunakan hockey stick pada permukaan media padat.
3 Cara tuang
Pengenceran inokulum yang berturut-turut diletakkan pada cawan petri
steril dan dicampurkan dengan medium agar cair, lalu dibiarkan memadat. Koloni
yang berkembang akan tertanam di dalam media tersebut (Lay, 1994).
2.5.5 Pengukuran aktifitas antimikroba
Penentuan kepekaan bakteri patogen terhadap antimikroba pada dasarnya
dapat dilakukan melalui tiga cara, yaitu:
a. Metode dilusi
Metode ini mengukur kadar hambat minimum (KHM) dan kadar bunuh
minimum (KBM). Metode ini menggunakan antimikroba dengan kadar yang
menurun secara bertahap, dengan media cair dan padat. Bakteri uji diinokulasi ke
dalam media cair dan padat lalu diinkubasi. Dimasukkan larutan antimikroba
dengan kadar yang menghambat atau mematikan. Uji kepekaan cara dilusi
menggunakan 2 cara yaitu dengan menggunakan tabung reaksi dan microdilution
b. Metode difusi
Metode yang paling sering digunakan dan biasanya menggunakan cakram.
Ada beberapa jenis cakram yaitu cakram kertas, cakram silinder dan punch hole.
Cakram tersebut yang berisi sejumlah tertentu obat ditempatkan pada permukaan
medium padat yang sebelumnya telah diinokulasi bakteri uji pada permukaannya.
Setelah diinkubasi, diameter zona hambatan sekitar cakram dipergunakan untuk
mengukur kekuatan hambatan obat terhadap mikroorganisme yang uji (Mudihardi,
2001).
c. Metode turbidimetri
Pada cara ini digunakan media cair. Pertama dilakukan penuangan media
kedalam tabung reaksi, lalu ditambahkan suspensi bakteri, kemudian dilakukan
pemipetan larutan uji, dilakukan inkubasi. Selanjutnya dilakukan pengukuran
kekeruhan, kekeruhan yang disebabkan oleh pertumbuhan bakteri diukur dengan
menggunakan instrumen yang cocok, misalnya nephelometer setelah itu dilakukan
BAB III
METODE PENELITIAN
Penelitian ini dilakukan dilaboratorium Fitokimia dan Mikrobiologi
Fakultas Farmasi Universitas Sumatera Utara Medan. Tahap penelitian yang
dilakukan meliputi penyiapan bahan, skrining fitokimia dan pembuatan ekstrak.
Selanjutnya pengujian aktivitas antibakteri dengan metode difusi agar
menggunakan punch hole Parameter yang dilihat adalah besarnya diameter hambat
pertumbuhan bakteri.
3.1 Alat dan Bahan
3.1.1 Alat–alat
Alat yang digunakan dalam penelitian ini adalah alat-alat gelas
laboratorium, lemari pengering, blender (Philips), desikator, freeze dryer
(Modulio), inkubator (Fiber Scientific), jangka sorong, jarum ose, kamera digital
(Sony), krus porselin, Laminar Air Flow Cabinet (Astec HLF 1200L), lemari
pendingin (Toshiba), mikroskop, neraca kasar (Sun), neraca listrik (Vibra AJ),
oven (Memmert), penangas air (Yenaco), pinset, pipet mikro (Eppendorf), rotary
evaporator(Haake D), seperangkat alat penetapan kadar air, punch hole,
spektrofotometer visible (Dynamica).
3.1.2 Bahan–bahan
Bahan yang digunakan pada penelitian ini adalah talus rumput laut
Kappaphycus alvarezii (Doty), Nutrient Agar (NA), Mueller Hinton Agar (MHA),
bakteri Escherichia coli (ATCC 25922), Staphylococcus aureus (ATCC No 25923)
kecuali dinyatakan lain yaitu alfa naftol, amil alkohol, asam klorida pekat, asam
asetat anhidrida, asam nitrat, asam asetat glasial, asam sulfat pekat, besi (III)
klorida, bismuth (III) nitrat, dimetil sulfoksida (DMSO), etanol 96%, etilasetat, n
-heksana, iodium, isopropanol, kalium iodida, kloralhidrat, kloroform, metanol,
natrium hidroksida, natrium klorida, natrium sulfat anhidrat, raksa (II) klorida,
serbuk magnesium, serbuk zinkum, timbal (II) asetat, dan toluen.
3.2 Pembuatan Larutan Pereaksi
3.2.1 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida dilarutkan dalam air suling secukupnya
kemudian ditambahkan 2 g iodida sedikit demi sedikit, cukupkan dengan air suling
sampai 100 ml (Depkes, 1995).
3.2.2 Pereaksi Dragendorff
Sebanyak 0,8 g bismut (III) nitrat dilarutkan dalam asam nitrat pekat 20 ml
kemudian dicampurkan dengan larutan kalium iodida sebanyak 27,2 g dalam 50 ml
air suling. Campuran didiamkan sampai memisah sempurna. Larutan jernih diambil
dan diencerkan dengan air suling secukupnya hingga 100 ml (Depkes, 1995).
3.2.3 Pereaksi Mayer
Sebanyak 1,36 g raksa (II) klorida, kemudian dilarutkan dalam air suling
hingga 60 ml. Pada wadah lain ditimbang sebanyak 5 g kalium iodida lalu
dilarutkan dalam 20 ml air suling. Kedua larutan dicampurkan dan ditambahkan air
suling hingga diperoleh larutan 100 ml (Depkes, 1995).
3.2.4 Pereaksi besi (III) klorida 1%
Sebanyak 1 g besi (III) klorida dilarutkan dalam air suling sampai 100 ml
3.2.5 Pereaksi Molish
Sebanyak 3 g α-naftol dilarutkan dalam asam nitrat 0,5 N hingga 100 ml
(Depkes, 1995).
3.2.6 Pereaksi timbal (II) asetat 0,4 M
Timbal (II) asetat sebanyak 15,17 g dilarutkan dalam air suling bebas CO2
hingga 100 ml (Depkes, 1995).
3.2.7 Pereaksi asam klorida 2 N
Sebanyak 17 ml asam klorida pekat diencerkan dengan air suling sampai
100 ml (Ditjen POM, 1979).
3.2.8 Pereaksi natrium hidroksida 2 N
Sebanyak 8,002 g pelet natrium hidroksida ditimbang, kemudian dilarutkan
dalam air suling hingga 100 ml (Ditjen POM, 1979).
3.2.9 Pereaksi Liebermann-Burchard
Campur secara perlahan 5 ml asam asetat anhidrida dengan 5 ml asam sulfat
pekat tambahkan etanol hingga 50 ml (Merck, 1978).
3.3 Pengumpulan dan Pengolahan Sampel
3.3.1 Pengambilan sampel
Pengambilan bahan dilakukan secara purposif yaitu tanpa membandingkan
dengan tumbuhan dari daerah lain. Bahan penelitian adalah talus Kappaphycus
alvarezii (Doty) yang diperoleh dari kelompok pembudidayaan rumput laut
masyarakat Beringin-Berjaya, Dusun III, Desa Kuala Tanjung, Kecamatan Sei
3.3.2 Identifikasi tumbuhan
Determinasi tumbuhan dilakukan di Pusat dan Pengembangan Oseanografi
– LIPI, Jakarta. Hasil determinasi menunjukan bahan tumbuhan adalah
Kappaphycus alvarezii (Doty). Hasil identifikasi tumbuhan dapat dilihat pada
lampiran 1, halaman 40.
3.3.3 Pembuatan simplisia
Talus Kappaphycus alvarezii (Doty) yang telah dikumpulkan, direndam
dalam air ledeng dan dibersihkan dari pengotor dan organisme yang melekat serta
sisa-sisa karang yang menempel. Dicuci berkali-kali dengan air ledeng sampai
bersih, kemudian ditiriskan, kemudian disebarkan diatas kertas yang dapat
menyerap air sehingga airnya terserap. Bahan ditimbang sebagai berat basah. Bahan
dikeringkan dilemari pengering hingga kering dimana jika simplisia tersebut
diremas akan hancur. Bahan kering ditimbang dan diperoleh berat kering. Bahan
selanjutnya diserbuk dengan menggunakan blender sampai diperoleh serbuk. Berat
bahan basah adalah 12 kg dan berat kering adalah 1,8 kg.
3.4 Skrining Fitokimia
Penentuan golongan senyawa kimia serbuk simplisia daun Kappaphycus
alvarezii (Doty) meliputi pemeriksaan senyawa golongan alkaloida, glikosida,
antrakinon dan saponin (Depkes , 1995), flavonoida, dan tanin (Farnsworth, 1966),
triterpenoida/steroida (Harborne, 1987).
3.4.1 Pemeriksaan alkaloida
Serbuk simplisia ditimbang 0,5 g kemudian ditambahkan 1 ml asam klorida
2 N dan 9 ml air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan
a. Filtrat sebanyak 3 tetes ditambah 2 tetes larutan pereaksi Mayer, maka akan
terbentuk endapan menggumpal berwarna putih atau putih kekuningan.
b. Filtrat sebanyak 3 tetes ditambah 2 tetes larutan pereaksi Bauchardat, akan
terbentuk endapan berwarna coklat.
c. Filtrat sebanyak 3 tetes ditambah 2 tetes larutan pereaksi Dragendorff
terbentuk endapan warna merah atau jingga.
Alkaloida disebut positif jika endapan atau kekeruhan paling sedikit dua
dari tiga percobaan diatas (Depkes, 1995).
3.4.2 Pemeriksaan glikosida
Ekstrak ditimbang sebanyak 3 g, lalu disari dengan 30 ml campuran etanol
95% dengan air (7:3) dan 10 ml asam klorida 2 N, direfluks selama 2 jam,
didinginkan dan disaring. Diambil 20 ml filrat ditambahkan 25 ml air suling dan 25
ml timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari
dengan 20 ml campuran isopropanol dan kloroform (2:3), dilakukan berulang
sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih
dari 50 C. Sisanya dilarutkan dalam 2 ml metanol. Larutan sisa digunakan untuk
percobaan berikut: 0,1 ml larutan percobaan dimasukan dalam tabung reaksi dan
diuapkan diatas penangas air. Sisa ditambahkan 2 ml air dan 5 tetes pereaksi
Molish, secara perlahan-lahan ditambahkan 2 ml asam sulfat pekat melalui dinding
tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan
adanya ikatan gula (Depkes, 1995).
3.4.3 Pemeriksaan steroida/triterpenoida
Sebanyak 1 g sampel dimaserasi dengan 20 ml n-heksan selama 2 jam, lalu
disaring. Filtrat diuapkan dalam cawan penguap. Pada sisa ditambahkan beberapa
menunjukan adanya steroida, sedangkan warna merah, merah muda atau ungu
menunjukkan adanya triterpenoida (Harborne, 1987).
3.4.4 Pemeriksaan flavonoida
Sebanyak 10 g ekstrak ditambahkan 10 ml air panas, dididihkan selama 5
menit dan disaring dalam keadaan panas, ke dalam 5 ml filtrat ditambahkan 0,1 g
serbuk magnesium dan 1 ml asam klorida pekat dan 2 ml amil alkohol, dikocok dan
dibiarkan memisah. Flavonoida positif jika terjadi warna merah atau kuning atau
jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.4.5 Pemeriksaan tanin
Ekstrak ditimbang sebanyak 1 g, dididihkan selama 3 menit dalam 100 ml
air suling lalu didinginkan dan disaring. Pada filtrat ditambahkan 1-2 tetes peraksi
besi (III) klorida 1%. Jika terjadi warna biru kehitaman atau hijau kehitaman
3.4.7 Pemeriksaan antrakuinon
Ekstrak ditimbang sebanyak 0,2 g, kemudian ditambahkan 5 ml asam sulfat
2 N, dipanaskan sebentar, setelah dingin ditambahkan 10 ml benzena, dikocok dan
didiamkan. Lapisan benzena dipisahkan dan disaring, kocok lapisan benzena
dengan 2 ml NaOH 2 N, didiamkan. Lapisan air berwarna merah dan lapisan
3.5 Pembuatan Ekstrak n-heksana, Ekstrak Etilasetat dan Ekstrak Etanol Secara Perkolasi Berkesinambungan
Pembuatan ekstrak dilakukan secara perkolasi berkesinambungan
menggunakan tiga pelarut. Cara kerja: sebanyak 400 g serbuk simplisia dimasukkan
ke dalam bejana tertutup, dituangi cairan penyari n-heksana sampai semua simplisia
terendam sempurna dan dibiarkan sekurang-kurangnya selama 3 jam. Pindahkan
massa sedikit demi sedikit ke dalam perkolator sambil tiap kali ditekan hati-hati,
dituangi cairan penyari secukupnya sampai cairan mulai menetes dan di atas
simplisia masih terdapat selapis cairan penyari, tutup perkolator dan biarkan selama
24 jam. Biarkan cairan menetes dengan kecepatan 1 ml per menit, ditambahkan
berulang-ulang cairan penyari secukupnya hingga selalu terdapat selapis cairan
penyari di atas simplisia. Perkolasi dihentikan jika 500 mg perkolat yang keluar
terakhir diuapkan, tidak meninggalkan sisa . Ampasnya di keringkan dan
diperkolasi kembali dengan menggunakan cairan penyari etilasetat dengan prosedur
perkolasi yang sama. Perkolat etilasetat di peroleh, ampasnya di perkolasi kembali
dengan menggunakan cairan penyari etanol dengan menggunakan prosedur
perkolasi yang sama. Masing-masing perkolat yang diperoleh dipekatkan dengan
alat penguap rotary evaporator dan dikering bekukan dengan freeze dryer (Depkes,
1995).
3.6 Sterilisasi Alat dan Media
Alat-alat yang digunakan dalam uji aktivitas antibakteri ini, disterilkan
terlebih dahulu sebelum dipakai. Alat-alat gelas disterilkan didalam oven pada suhu
170°C selama 1 jam. Media disterilkan di autoklaf pada suhu 121°C selama 15
3.7 Pembuatan Media
1000 ml, lalu dipanaskan sampai larut sempurna. Media dimasukkan kedalam
erlenmeyer dan disterilkan di dalam autoklaf pada suhu 121°C selama 15 menit
(Oxoid , 2013).
3.7.2 Media Mueller Hinton agar (MHA)
Komposisi: Beef infusion form 300 g
1000 ml, lalu dipanaskan sampai larut sempurna. Media dimasukkan kedalam
erlenmeyer dan disterilkan di dalam autoklaf pada suhu 121°C selama 15 menit
Sebanyak 8 g nutrien broth dilarutkan dalam air suling steril sebanyak 1000
kemudian dimasukkan dalam erlenmeyer. Disterilkan di autoklaf 1210C selama 15
menit (Difco, 1997).
3.7.4 Pembuatan agar miring
Kedalam tabung reaksi dimasukkan 10 ml media Nutrien agar yang sudah
dicairkan, kemudian diletakkan dengan posisi miring dengan kemiringan lebih
kurang 45oC, ditutup mulut tabung reaksi dengan kapas dan dibiarkan memadat.
3.8 Pembiakan Bakteri
3.8.1 Pembuatan stok kultur
3.8.1.1 Bakteri Escherichia coli
Biakan bakteri Escherichia coli dari strain utama diambil dengan jarum ose
steril lalu diinokulasikan pada permukaan media nutrien agar miring, kemudian
diinkubasikan pada suhu 37oC selama 24 jam.
3.8.1.2 Bakteri Staphylococcus aureus
Biakan bakteri Staphylococcus aureus dari strain utama diambil dengan
jarum ose steril lalu diinokulasikan pada permukaan media nutrien agar miring,
kemudian diinkubasikan pada suhu 37oC selama 24 jam.
3.8.2 Penyiapan inokulum
3.8.2.1 Bakteri Escherichia coli
Koloni bakteri Escherichia coli diambil dari stok kultur diambil
menggunakan jarum ose steril kemudian disuspensikan ke dalam 10 ml media
nutrient broth steril lalu diinkubasikan pada suhu 37oC sampai didapat kekeruhan
dengan transmitan 25% menggunakan alat spektrofotometer UV panjang
3.8.2.2 Bakteri Staphylococcus aureus
Koloni bakteri Staphylococcus aureus diambil dari stok kultur diambil
menggunakan jarum ose steril kemudian disuspensikan ke dalam 10 ml media
nutrient broth steril lalu diinkubasikan pada 37oC sampai didapat kekeruhan dengan
transmitan 25% menggunakan alat spektrofotometer UV panjang gelombang 580
nm (Ditjen POM, 1995).
3.9 Pembuatan Larutan Uji (Ekstrak n-heksana, Etilasetat dan Etanol) Dengan Berbagai Konsentrasi.
Sebanyak 5 g masing-masing ekstrak n-heksana, ekstrak etilasetat dan
ekstrak etanol ditimbang seksama dengan neraca analitik, dilarutkan dalam 5 ml
dimetil sulfoksida (DMSO) dan dimasukkan ke dalam labu takar 10 ml. Tambahkan
aquabidest steril hingga garis tanda dan diperoleh konsentrasi ekstrak 500 mg/ml.
Larutan tersebut diencerkan kembali dengan dimetil sulfoksida (DMSO) dan
aquabidest steril hingga didapat ekstrak dimetil sulfoksida (DMSO) dan aquabidest
steril dengan konsentrasi 500 mg/ml, 400 mg/ml, 300 mg/ml, 200 mg/ml, 100
mg/ml, 90 mg/ml, 80 mg/ml, 70 mg/ml, 60 mg/ml,50 mg/ml, 40 mg/ml, 30 mg/ml,
20 mg/ml, 10 mg/ml.
3.10 Metode Pengujian Efek Antibakteri Secara In Vitro
3.10.1 Bakteri Escherichia coli
Kedalam cawan petri dimasukkan 0,1 ml inokulum (106) kemudian
ditambahkan 15-20 ml Mediasteril Mueller Hinton Agar yang telah dicairkan
(45-50o
C CFU/ml) dihomogenkan dan dibiarkan sampai media memadat. Permukaan
-heksana sebanyak 0,1 ml dengan berbagai konsentrasi. Kemudian diinkubasi pada
suhu 37oC selama 18-24 jam. Hal yang sama dilakukan terhadap ekstrak etilasetat
dan ekstrak etanol. Diameter daerah hambat di sekitar sumur diukur dengan
menggunakan jangka sorong. Pengujian dilakukan sebanyak 3 kali (Ditjen POM,
1995).
3.10.2 Bakteri Staphylococcus aureus
Kedalam cawan petri dimasukkan 0,1 ml inokulum (106) kemudian
ditambahkan 15-20 ml Mediasteril Mueller Hinton Agar yang telah dicairkan
(45-50oC CFU/ml) dihomogenkan dan dibiarkan sampai media memadat. Permukaan
media dilubangi, kemudian masing-masing kedalam lubang dimasukkan ekstrak n
-heksana sebanyak 0,1 ml dengan berbagai konsentrasi. Kemudian diinkubasi pada
suhu 37oC selama 18-24 jam. Hal yang sama dilakukan terhadap ekstrak etilasetat
dan ekstrak etanol. Diameter daerah hambat di sekitar sumur diukur dengan
menggunakan jangka sorong. Pengujian dilakukan sebanyak 3 kali (Ditjen POM,
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Identifikasi tumbuhan yang dilakukan di Pusat dan Pengembangan
Oseanologi–LIPI, Jakarta, menyatakan bahwa tumbuhan yang digunakan dalam
penelitian ini adalah Rumput Laut Kappaphycus alverezii (Doty). Hasil
identifikasi dapat dilihat pada Lampiran 1, halaman 40.
4.2 Hasil Skrining Fitokimia
Hasil skrining fitokimia terhadap serbuk simplisia Rumput Laut
Kappaphycus alverezii (Doty) terdapat golongan-golongan senyawa kimia yang
memberikan hasil positif. Data dapat dilihat pada Tabel 4.1 berikut:
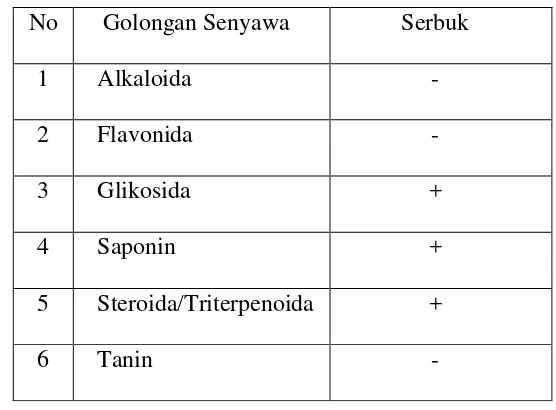
Tabel 4.1 Skrining fitokimia terhadap serbuk simplisia rumput Laut Kappaphycus alverezii (Doty)
Keterangan: (+) = mengandung senyawa (-) = tidak mengandung senyawa
No Golongan Senyawa Serbuk
1 Alkaloida -
2 Flavonida -
3 Glikosida +
4 Saponin +
5 Steroida/Triterpenoida +
Serbuk simplisia Rumput Laut Kappaphycus alverezii (Doty). Skrining
glikosida ditunjukkan dengan penambahan pereaksi Molish dan asam sulfat pekat
dimana terbentuk cincin ungu. Penambahan 10 ml air panas, didinginkan dan
kemudian dikocok kuat-kuat selama 10 detik dengan adanya buih yang mantap
selama tidak kurang dari 10 menit, setinggi 1-10 cm dan tidak hilang dengan
penambahan asam klorida 2 N menunjukkan adanya saponin. Penambahan pereaksi
Liebermann-Burchard memberikan warna ungu menunjukkan adanya senyawa
steroid/triterpenoid.
4.3 Hasil Ekstraksi
Simplisia rumput laut Kappaphycus alvarezii (Doty) 400 g diekstraksi
dengan cara perkolasi menggunakan pelarut n-heksana, etilasetat, dan etanol 96%,
diharapkan senyawa-senyawa aktif yang terkandung di dalamnya dapat tersari
sempurna. Hasilnya diperoleh ekstrak n-heksana 3,5 g, ekstrak etilasetat 4,9 g dan
ekstrak etanol 8 g.
4.4 Hasil Uji Aktivitas Antibakteri Ekstrak n-heksana, Etilasetat, etanol Terhadap Escherichia coli dan Staphylococcus aureus
Hasil uji aktivitas antibakteri dari ekstrak rumput laut jenis Kappaphycus
alvarezii (Doty) menunjukkan bahwa ekstrak n-heksana tidak dapat menghambat
pertumbuhan bakteri Escherichia coli dan Staphylococcus aureus, hal ini ditandai
dengan tidak adanya zona hambat (daerah bening) disekitar daerah sumur. Ekstrak
etilasetat dan etanol dapat menghambat pertumbuhan bakteri Escherichia coli dan
disekitar sumur, semakin tinggi konsentrasi ekstrak etilasetat dan etanol maka akan
menghasilkan diameter daerah hambat yang semakin besar.
Hasil pengukuran diameter daerah hambat ekstrak etilasetat dan ekstrak
etanol Kappaphycus alverezii (Doty) pada Tabel 4.2 dan Tabel 4.3 berikut ini.
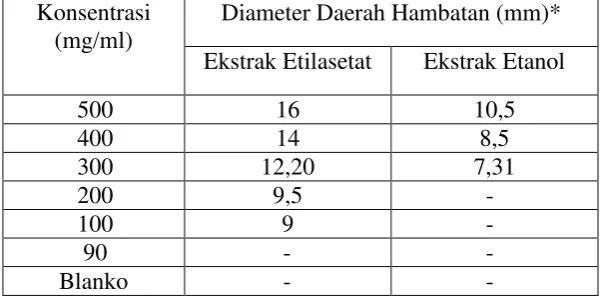
Tabel 4.2 Hasil pengukuran diameter daerah hambatan pertumbuhan Escherichia coli ekstrak etilasetat dan ekstrak etanol.
Konsentrasi
Tabel 4.3 Hasil pengukuran diameter daerah hambatan pertumbuhan Staphylococcus aureus ekstrak etilasetat dan ekstrak etanol.
Berdasarkan Farmakope Indonesia (1995) batas daerah hambatan yang
efektif adalah dengan diameter lebih kurang dari 14 mm sampai 16 mm. Hasil uji
aktivitas antibakteri menunjukkan bahwa ekstrak etilasetat memberikan hasil efektif
untuk bakteri Escherichia coli, pada konsentrasi 300 mg/ml memberikan daya
hamabat 14,51 mm dan KHM 100 mg/ml 9,52 mm pada ekstrak etilasetat rumput
laut jenis Kappaphycus alverezii, dan untuk bakteri Staphylococcus aureus pada
konsentrasi 400 mg/ml memberikan daya hamabat 14 mm dan KHM 100 mg/ml 9
mm.
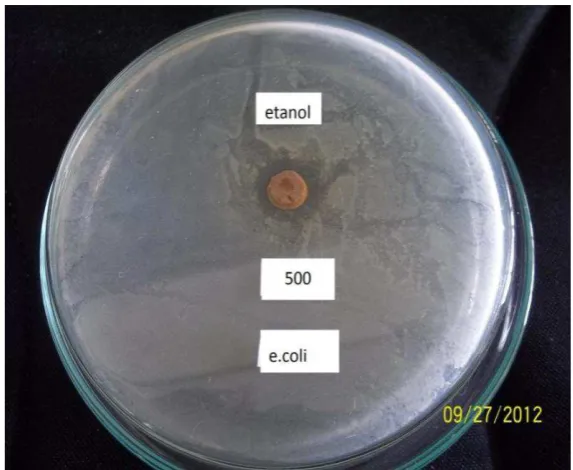
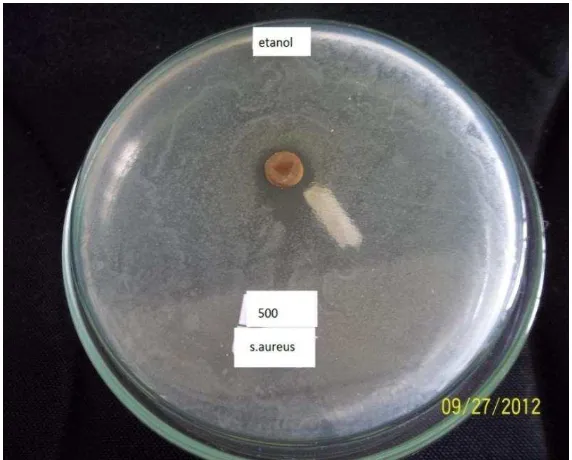
Pengujian pada ekstrak etanol hasil uji aktivitas antibakteri menunjukkan
bahwa ekstrak etanol memberikan hasil untuk bakteri Escherichia coli dan
Staphylococcus aureus, pada konsentrasi 500 mg/ml ekstrak etanol memberikan
daya hamabat pada bakteri Escherichia coli 10 mm dan KHM 300 mg/ml 7,5 mm,
dan pada bakteri Staphylococcus aureus memberikan daya hamabat pada
konsentrasi 500 mg/ml 10,5 mm dan KHM 300 mg/ml 7,31 mm.
Penelitian ini mengunakan DMSO sebagai pelarut ekstrak, dari hasil yang
didapat bahwa DMSO memiliki daya hambat sebagai antibakteri., sehingga dalam
menggunaan sebagai pelarut ekstrak, DMSO diencerkan dengan aquabidest steril.
Hasil skrining fitokimia dari serbuk simplisia Kappaphycus alverezii (Doty)
menunjukkan adanya senyawa golongan saponin, steroid/triterpenoid, glikosida.
Senyawa ini diduga memberikan aktivitas antibakteri (Robinson, 1995).
Senyawa triterpenoid/steroid dan saponin dapat menghambat pertumbuhan
bakteri dengan mekanisme penghambatan terhadap sintesis protein karena
terakumulasi dan menyebabkan perubahan komponen-komponen penyusun sel
Tumbuhan yang mengandung saponin telah digunakan sebagai racun ikan
selama berates-ratus tahun. Saponin digunakan sebagai antimikroba dalam
beberapa tahun terakhir ini ( Robinson, 1995).
Hasil yang tidak efektif pada ekstrak n-heksana, hal ini mungkin disebabkan
karena adanya kerja yang tidak sinergis antara senyawa metabolit sekunder dalam
ekstrak n-heksana dalam peranannya sebagai antibakteri, sedangkan pada ekstrak
etilasetat dan ekstrak etanol kemungkinan disebabkan karena adanya kerja yang
sinergis antara senyawa metabolit sekunder sebagai antibakteri.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
a. Hasil dari penentuan golongan senyawa kimia dijumpai golongan senyawa
steroida/triterpenoida, saponin, dan glikosida.
b. Ekstrak etilasetat memberikan daya hamabat terhadap bakteri Escherichia
coli dan Staphylococcus aureus konsentrasi 300 mg/ml dan 400 mg/ml
yaitu 14,51 mm dan 14 mm, kadar hambat minimum 100 mg/ml 9,52 mm
dan 9 mm. Ekstrak etanol memberikan daya hamabat terhadap bakteri
Escherichia coli dan Staphylococcus aureus konsentrasi 500 mg/ml yaitu
10 mm dan 10,5 mm, kadar hambat minimumnya pada konsentrasi 300
mg/ml yaitu 7,5 mm dan 7,3 mm, sedangkan ekstrak n-heksana tidak
memberikan diameter daerah hambat terhadap bakteri Escherichia coli dan
Staphylococcus aureus.
5.2 Saran
Diharapkan peneliti selanjutnya untuk melakukan isolasi dan identifikasi
senyawa aktif yang terdapat dalam rumput laut Kappaphycus alverezii (Doty) yang
menunjukkan aktivitas antibakteri terhadap bakteri Escherichia coli dan
DAFTAR PUSTAKA
Anggadiredja, J.T., Achmad Z., Heri, P., dan Sri, I. (2010). Rumput Laut. Jakarta: Penebar Swadaya. Halaman 14-19, 26-39, 52-60, 65.
Aslant, L.M. (1998). Budidaya Rumput Laut. Jakarta: Kanisius. Halaman 11-14, 17, 24.
Atmadja, W.S., Kadi A., Sulistijo., dan Safari, R. (1996). Pengenalan Jenis-jenis RumputLaut Indonesia. Jakarta: LIPI PUSLITBANG Oseanologi. . Halaman 95.
Choudhury, S., Sree, A., Mukherjee, S.C., Pattnaik, P., dan Bapuji. M. (2005). In Vitro Antibacterial Activity of Extracts of selected Marine Algae and mangroves Against Fish Pathogens. Journal Asian Fisheries Science. Volume 18. Halaman 185-294.
Dawes, C.J. (1981). Marine Botany. Florida: A Wiley-Interscience Publication. Halaman 41. Microbiology and Clinical Laboratory Procedures. Edisi IX. Detroit Michigan: Difco Laboratories. Halaman 29, 32.
Ditjen POM (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Jakarta: Departemen Kesehatan RI. Halaman 8-11.
Ditjen POM. (1979). Farmakope Indonesia. Edisi ketiga. Jakarta: Depkes RI. Halaman 33, 649, 682.
Ditjen POM. (1995). Farmakope Indonesia. Edisi IV. Jakarta: Direktorat Jenderal Pengawas Obat dan Makanan. Halaman 891-898.
Dwidjoseputro. (1998). Dasar-Dasar Mikrobiologi. Jakarta: D. Jambatan. Halaman 33, 117-133.
Gembong, T. (1994). Toksonomi Tumbuhan. Edisi III. Yogyakarta: Gadjah Mada University Press. Halaman 1-26.