DHIAN EKA WIJAYA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
DHIAN EKA WIJAYA. Pengoptimalan Sintesis Glukosamina Hidroklorida
Berbasis Kitosan. Dibimbing oleh PURWANTININGSIH SUGITA dan
BAMBANG SRIJANTO.
Glukosamina hidroklorida telah disintesis melalui hidrolisis kitosan
menggunakan HCl. Peubah yang diragamkan pada percobaan ini ialah waktu
reaksi, konsentrasi HCl, dan suhu. Rancangan percobaan yang digunakan adalah
rancangan respons permukaan metode Box Behnken. Hasil sintesis glukosamina
hidroklorida dianalisis menggunakan perangkat lunak Minitab 14. Kadar
glukosamina hidroklorida yang diperoleh antara 75.10 dan 99.37%. Interval
peubah yang memberikan kadar glukosamina hidroklorida maksimum adalah pada
konsentrasi HCl 4 N, interval waktu 140 menit, dan suhu 90
°
C.
ABSTRACT
DHIAN EKA WIJAYA. Optimalization Synthesis of Chitosan-Based
Glucosamine Hydrochloride. Supervised by PURWANTININGSIH SUGITA and
BAMBANG SRIJANTO.
DHIAN EKA WIJAYA
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Pengoptimalan Sintesis Glukosamina Hidroklorida Berbasis Kitosan
Nama : Dhian Eka Wijaya
NIM : G44053011
Menyetujui
Pembimbing I,
Pembimbing II,
Prof. Dr. Dra. Purwantiningsih Sugita, MS
Ir. Bambang Srijanto
NIP 196312271988032002
NIP 196605061993121001
Mengetahui
Ketua Departemen,
Prof. Dr. Ir. Tun Tedja Irawadi, MS
NIP 195012271976032002
karunia-Nya, penulis dapat menyelesaikan karya ilmiah. Sholawat dan salam
semoga tercurah kepada Nabi Muhammad SAW beserta keluarga dan para
sahabatnya. Karya ilmiah ini disusun berdasarkan hasil penelitian yang
dilaksanakan pada bulan April sampai November 2009 di Laboratorium Kimia
Organik Departemen Kimia FMIPA IPB.
Penulis mengucapkan terima kasih kepada Prof. Dr. Dra. Purwantiningsih
Sugita, MS dan Ir. Bambang Srijanto selaku pembimbing yang telah banyak
memberikan arahan, motivasi, dan saran dari setiap permasalahan dalam
penelitian dan penulisan karya ilmiah ini. Penghargaan juga penulis sampaikan
kepada Direktur DP3M Direktorat Jenderal Pendidikan Tinggi Depdiknas sebagai
sumber dana penelitian ini melalui Hibah Kompetensi atas nama Prof. Dr. Dra.
Purwantiningsih Sugita, MS tahun 2009. Selain itu, penulis mengucapkan terima
kasih kepada Ibu, Bapak, Rike, Wawan, Nenek, dan keluarga yang telah
memberikan kasih sayang, dorongan, dan doa kepada penulis selama menempuh
studi, penelitian, dan penulisan karya ilmiah ini.
Penulis juga mengucapkan terima kasih kepada Bapak Sabur, Ibu Yenni
Karmilah, dan Ibu Siti Robiah atas fasilitas, bantuan, serta saran yang diberikan.
Tak lupa, ungkapan terima kasih penulis sampaikan kepada seluruh rekan-rekan
peneliti di Laboratorium Kimia Organik Departemen FMIPA IPB Luthfan, Iwan,
Bayu, Akbar, Rita, Dian, Rizki, Aulia, Dwi Agustina, Naftaleni, kakak-kakak
kelas, Kak Tuti Wukirsari, Kak Bekti, Kak Dwi, Kak Miqdad atas diskusi dan
kebersamaan selama penulis menempuh studi dan menjalankan penelitian.
Semoga karya ilmiah ini bermanfaat bagi ilmu pengetahuan dan kehidupan
umat manusia secara umum. Amin.
Bogor, Januari 2010
RIWAYAT HIDUP
Penulis dilahirkan di Tempel Rejo pada tanggal 26 Desember 1987 dari Bapak
Sakip dan Ibu Nemi Laynah. Penulis merupakan anak pertama dari tiga
bersaudara. Penulis menyelesaikan studi di SMU Negeri 1 Curup pada tahun
2005. Pada tahun yang sama penulis diterima di Institut Pertanian Bogor (IPB)
melalui jalur Undangan Seleksi Masuk IPB (USMI).
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... iii
DAFTAR TABEL ... iii
DAFTAR LAMPIRAN ... iii
PENDAHULUAN ...
1
TINJAUAN PUSTAKA ...
1
Kitin dan Kitosan ...
1
Glukosamina Hidroklorida ...
2
BAHAN DAN METODE ...
2
Bahan ...
2
Metode ...
2
HASIL DAN PEMBAHASAN ...
3
Pencirian Kitosan ...
3
Sintesis GlcN-HCl ...
3
Pengaruh konsentrasi HCl, waktu, dan suhu reaksi terhadap kadar
GlcN-HCl ...
3
Pencirian GlcN-HCl sintesis ...
4
SIMPULAN DAN SARAN ...
5
Simpulan ...
5
Saran ...
5
DAFTAR PUSTAKA ...
5
iii
DAFTAR GAMBAR
Halaman
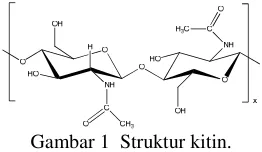
1 Struktur kitin. ...
1
2 Struktur kitosan (x
≥
50%). ...
1
3 Struktur Glukosamina
Hidroklorida
. ...
2
4 Bubur GlcN-HCl hasil sintesis. ...
3
5 GlcN-HCl hasil sintesis. ...
3
6 Kontur hubungan kadar GlcN-HCl terhadap (a) konsentrasi HCl dan suhu, (b)
waktu dan suhu, (c) waktu dan konsentrasi HCl. ...
4
DAFTAR TABEL
Halaman
1 Perbandingan
pencirian
GlcN-HCl sintesis dan standar terhadap literatur ...
4
2 Serapan FTIR GlcN-
HCl
standar dan hasil sintesis terhadap literatur ...
5
DAFTAR LAMPIRAN
Halaman
1 Pencirian kitosan dan
diagram
Alir Penelitian...
8
2 Penentuan kadar air, kadar abu, DD, dan bobot molekul kitosan ...
9
3 Hasil pencirian kitosan ... 11
4 Rancangan percobaan (
keluaran
minitab 14) ... 13
5 Mekanisme reaksi hidrolisis
kitosan
(Solomons dan Fryhle 2004) ... 14
6 Penentuan kurva baku kadar
GlcN
-HCl terhadap konsentrasi NaOH... 16
7 Penentuan kadar GlcN-HCl ... 17
8 Penentuan koefisien regresi
dan
analisis ragam kadar glukosamina ... 18
PENDAHULUAN
Seiring dengan kemajuan teknologi, banyak obat-obatan yang telah dikembangkan dalam rangka meningkatkan kesehatan masyarakat. Obat-obatan ini dapat dihasilkan dari bahan-bahan alami dan sintetik. Beberapa penelitian menyatakan bahwa obat-obatan berbahan baku sintetik banyak menimbulkan ekses negatif, maka penggunaan bahan-bahan alami sebagai bahan baku obat meningkat pesat dan telah menjadi alternatif yang sangat baik. Salah satu obat berbahan baku alami yang banyak dikembangkan adalah glukosa-mina hidroklorida (GlcN-HCl).
GlcN-HCl merupakan salah satu senyawa gula amino yang banyak terkandung dalam tulang rawan. Zat ini sangat penting untuk kesehatan dan kelenturan sendi. GlcN-HCl dapat mencegah dan mengobati osteoporosis, aterosklerosis, hipertensi, dan diabetes. Selain itu, zat ini juga dapat meningkatkan kekebalan tubuh dan memiliki aktivitas antitumor.
Penelitian-penelitian yang berhubungan dengan glukosamina (GlcN) terus dikembang-kan dengan melakudikembang-kan modifikasi-modifikasi terhadap senyawa tersebut. Beberapa contoh modifikasi GlcN diantaranya adalah 2-[N -(7- nitrobenze-2-oksa-1,3-diazol-4-il)amino]-2-deoksi-L-glukosa [2-NBDLG] (Yamamoto et al 2008), N-fenilasetamida-D-glukosamina, N -asetil-D-manosamina, N,N’-diasetilsitobiosa, 2-asetamido-2-deoksi-α-D-glukopirano-sida, dan 2-asetamido-2-deoksi-4,6-O -isopropili-dena-α-D-glukopiranosida (Kuboki et al. 1998).
Salah satu bahan alami yang berpotensi sebagai bahan baku GlcN-HCl adalah kitin. Kitin merupakan suatu bahan alami yang terdiri dari unit-unit N-asetilgukosamina (β(1→4)-2-asetamida-2-deoksi-D -glukopira-nosa atau GlcNAc). Berry (2002) telah berhasil mensintesis GlcN-HCl dari kitin, tetapi kadarnya masih rendah (≤50%). Kitin dapat dihidrolisis dengan basa untuk menda-patkan senyawa yang cukup penting, yaitu kitosan. Kitosan juga dapat dijadikan sebagai bahan baku dalam sintesis GlcN-HCl.
Kitosan memiliki perbandingan kandung-an gugus asetamida (-NHCOCH3) terhadap
gugus amina (-NH2) lebih rendah
dibanding-kan dengan kitin. Oleh karena itu, penelitian ini dilakukan untuk mensintesis GlcN-HCl dengan bahan baku kitosan. Rendemen GlcN-HCl yang dihasilkan dari kitosan adalah 75.10-99.37%.
TINJAUAN PUSTAKA
Kitin dan Kitosan
Kitin adalah suatu produk alami yang terdiri dari unit N-asetilgukosamina yang dihubungkan melalui ikatan glikosidik β(1-4), yaitu β(1→ 4)-2-asetamida-2-deoksi-d-gluko-piranosa, terkandung pada eksoskeleton di Crustacea, kulit insekta, serta dinding sel di fungi dan ragi (Kumirska et al. 2008). Struktur kitin ditampilkan pada Gambar 1.
Gambar 1 Struktur kitin.
Kitin merupakan salah satu polisakarida yang sangat berlimpah di dunia dan biopolimer kedua yang berlimpah di dunia (Chang et al. 2000) dan keberadaannya di alam terikat dengan protein, mineral, dan berbagai macam pigmen.
Kitosan merupakan hasil dari proses deasetilasi yang merupakan kopolimer dari GlcNAc dan β(1→ 4)-2-amino-2-deoksi-d-glukopiranosa (GlcN) dengan kandungan GlcN lebih dari 50% (Sajomsanga et al. 2008). Struktur kitosan ditampilkan pada Gambar 2.
Gambar 2 Struktur kitosan (x≥50%).
Struktur kitosan hampir sama dengan selulosa, perbedaannya yaitu pada gugus rantai C-2, gugus hidroksil pada selulosa digantikan oleh gugus amina.
2
Glukosamina Hidroklorida
GlcN merupakan salah satu senyawa gula amino yang ditemukan secara luas pada tulang rawan dan memiliki peranan yang sangat penting untuk kesehatan dan kelenturan sendi. Secara umum GlcN terbagi menjadi dua golongan utama, yaitu GlcN-HCl dan GlcN sulfat.
GlcN-HCl merupakan bentuk ekstrak asli dari GlcN. Senyawa ini stabil secara kimia dan tidak membutuhkan aditif untuk memper-tahankan aktivitasnya sedangkan GlcN sulfat merupakan bentuk GlcN yang telah ter-modifikasi secara kimia. Karena gugus sulfat mudah terdegradasi, baik natrium maupun kalium klorida perlu ditambahkan untuk mem-pertahankan aktivitasnya. Vitamin C dan kalsium karbonat juga sering ditambahkan sebagai bahan pemantap. Struktur GlcN-HCl ditampilkan pada Gambar 3.
Gambar 3 Struktur Glukosamina Hidroklorida.
Fungsi dari GlcN secara umum berkaitan dengan perawatan kesehatan tulang. Mekanis-me kerja dari GlcN yaitu Mekanis-menghambat sintesis glikosaminoglikan dan mencegah destruksi tulang rawan. GlcN dapat merangsang sel-sel tulang rawan dalam pembentukan proteo-glikan dan kolagen yang merupakan protein esensial untuk memperbaiki fungsi persendian.
BAHAN DAN METODE
Bahan
Bahan-bahan yang digunakan dalam penelitian ini antara lain kitosan niaga dan GlcN-HCl standar.
Metode
Pencirian Kitosan
Kitosan dicirikan dengan pengukuran kadar air, kadar abu, bobot molekul, dan DD. Prosedur-prosedur pencirian tersebut dapat dilihat pada Lampiran 3.
Rancangan Optimalisasi
Peubah yang diragamkan adalah suhu reaksi, konsentrasi HCl, dan waktu reaksi hidrolisis. Batas atas dan bawah masing-masing peubah berturut-turut adalah 70 dan 90 °C, 4.0 dan 7.0 N, serta 60 dan 180 menit. Dengan rancangan respon permukaan (disain Box-Behnken) menggunakan perangkat lunak Minitab 14 didapat ragam masing-masing peubah (Lampiran 4).
Sintesis GlcN-HCl (Modifikasi dari Chang et al. 2000)
Sebanyak 0.1 g kitosan ditimbang, kemu-dian dilarutkan dalam 10 mL asam asetat 0.5 N. Larutan kitosan lalu dimasukan ke dalam labu berleher dua dan ditambahkan 100 mL HCl. Setelah itu, larutan kitosan diberi per-lakuan sesuai dengan rancangan percobaan (Lampiran 4), lalu didinginkan sampai suhu kamar. Larutan kitosan dipusingkan selama 15 menit dengan kecepatan 3500 rpm. Bubur glukosamina yang didapat, dilarutkan dalam 40 mL akuades. Larutan tersebut ditambahkan seujung sudip arang aktif dan diaduk selama 30 menit. Larutan disaring, lalu filtratnya dipanaskan <60 °C sampai terbentuk bubur kembali. Bubur dicuci dengan etanol 96% dan dikeringkan.
Standardisasi NaOH
Ditimbang NaOH sebanyak 1.0192 gram. Dilarutkan dengan akuades yang telah didih-kan terlebih dahulu (±100 mL). Setelah dingin, larutan NaOH dimasukkan ke dalam labu takar 250 mL, encerkan dengan akuades (telah didihkan) sampai tanda tera.
Ditimbang asam oksalat sebanyak 0.3175 gram. Dilarutkan dengan akuades (±25 mL) pada gelas piala dan dimasukan ke labu takar 50 mL. Tambahkan akuades hingga tanda tera. Dipipet 10 mL larutan asam oksalat lalu masukan ke labu erlenmeyer. Ditambahkan 3 tetes indikator fenolftalein dan dititrasi dengan NaOH hingga terjadi perubahan warna menjadi merah muda. Titrasi dilakukan triplo.
Kurva Baku
GlcN-HCl baku yaitu dipipet berturut-turut 0.5; 1; 3; 5; 7; dan 9 mL larutan baku induk ke dalam labu takar 10 mL lalu diencerkan dengan akuades sampai tanda tera. Seri larutan GlcN-HCl baku diukur pH awalnya menggunakan pH-meter. Jumlah NaOH yang ditambahkan pada larutan sampai pH ±9 dicatat.
HASIL DAN PEMBAHASAN
Pencirian Kitosan
Penelitian ini diawali dengan pencirian kitosan yang meliputi kadar air, kadar abu, bobot molekul, dan DD. Kadar air merupakan parameter yang penting untuk diketahui karena berhubungan dengan masa simpan kitosan dan koreksi bobot dalam penimbangan sedangkan kadar abu menggambarkan banyaknya mineral yang terdapat dalam cuplikan yang merupakan suatu oksida logam. Kadar air dan kitosan yang didapat adalah 10.67% dan 0.2706%. Bobot molekul kitosan sangat berkaitan erat dengan DD-nya. Semakin besar DD kitosan maka akan semakin kecil bobot molekul kitosan. Hal ini disebabkan semakin banyaknya gugus asetil yang terlepas dari kitosan. Selain itu, DD kitosan menunjukkan seberapa besar kadar monomer GlcN dalam kitosan. Bobot molekul dan DD kitosan yang didapat adalah sekitar 3.7×105 g.mol-1 dan 73.76%.
Sintesis GlcN-HCl
GlcN-HCl disintesis dengan cara menghidrolisis ikatan glikosidik pada kitosan. Sintesis GlcN-HCl dilakukan dengan meragamkan peubah konsentrasi HCl, suhu reaksi, dan waktu reaksi hidrolisis mengguna-kan rancangan respon permukaan metode Box Behnken. Pada penelitian ini, hidrolisis kitosan menggunakan HCl. Sebelum ditam-bahkan HCl, kitosan dilarutkan terlebih dahulu dalam asam asetat 0.5 N. Hal ini bertujuan agar kontak antara kitosan dengan HCl lebih besar dibandingkan jika kitosan dihidrolisis dalam bentuk padatan.
Proses hidrolisis ini akan menghasilkan bubur GlcN-HCl. Gambar bubur yang dihasilkan ditampilkan pada gambar 4.
Gambar 4 Bubur GlcN-HCl hasil sintesis.
Bubur ini dipusingkan agar didapat padatan GlcN-HCl. Padatan ini dilarutkan dalam akuades agar Cl- yang berlebih dapat dihilangkan. Pada tahap ini juga dilakukan proses penghilangan warna dengan meng-gunakan arang aktif. Padatan glukosamina hidroklorida yang didapat diukur kadarnya dengan penambahan NaOH sampai pH larutan 9. Padatan glukosamina hidroklorida ditampil-kan pada gambar 5.
Gambar 5 GlcN-HCl hasil sintesis.
Pada pH tersebut, Cl- yang berikatan dengan gugus –NH3+ pada glukosamina hidroklorida
telah bereaksi seluruhnya dengan NaOH yang ditambahkan. Sebelumnya NaOH harus distandardisasi menggunakan boraks. Data standardisasi dan kadar glukosamina hidroklorida hasil sintesis dapat dilihat pada Lampiran 7 dan 8.
Pengaruh konsentrasi HCl, waktu, dan
suhu reaksi terhadap kadar GlcN-HCl
Berdasarkan analisis statistika (Lampiran 8) dapat diketahui bahwa terdapat data dengan residual terbakukan yang besar pada pengamatan 17 dengan kadar GlcN-HCl sebesar 76.14%. Pada pengamatan ini, kadar GlcN yang diperoleh berbeda nyata dengan 5 pengamatan lain (pengamatan 3, 7, 17, 19, 25, dan 27) dengan perlakukan yang sama.
4
a
b
c
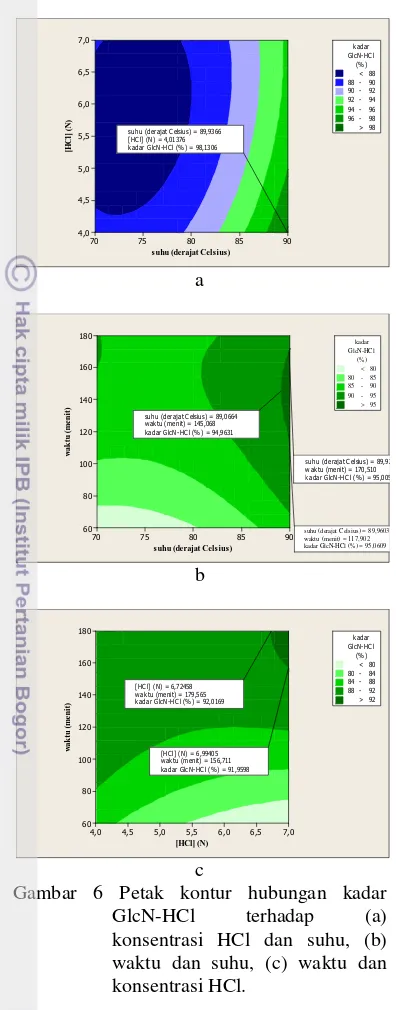
Gambar 6 Petak kontur hubungan kadar GlcN-HCl terhadap (a) konsentrasi HCl dan suhu, (b) waktu dan suhu, (c) waktu dan konsentrasi HCl.
Kadar GlcN-HCl maksimum berada pada konsentrasi HCl 4 N dan suhu 90 °C (Gambar 1a), pada interval waktu 117 sampai 170 menit dan suhu 90 °C (Gambar 1b) serta pada konsentrasi 7 N dan interval waktu 158 sampai 180 menit (Gambar 1c). Dari data diatas, kadar optimum sintesis GlcN-HCl pada konsentrasi HCl 4 N, interval waktu 140 menit, dan suhu 90 °C.
Berry et al (2002) melaporkan bahwa sintesis GlcN-HCl melalui hidrolisis kitin menggunakan HCl menghasilkan kadar yang rendah (≤50%). Nilai ini jauh lebih kecil dibandingkan dengan hasil sintesis glukosa-mina hidroklorida melalui hidrolisis kitosan
(75.10-99.37%). Hal ini disebabkan oleh gugus asetamida pada kitin lebih banyak dibandingkan pada kitosan.
Proses hidrolisis kitosan terjadi pada dua bagian, yaitu gugus asetamida dan ikatan glikosidik. Hidrolisis berlangsung pada gugus asetamida terlebih dahulu kemudian dilanjutkan pada ikatan glikosidik.
Reaksi hidrolisis pada gugus asetamida
Reaksi hidrolisis pada ikatan glikosidik
Hal ini disebabkan ikatan glikosidik (gugus fungsi eter) yang lebih inert dibandingkan gugus asetamida. Mekanisme hidrolisis gugus asetamida dan ikatan glikosidik pada kitosan dapat dilihat pada Lampiran 5.
Pencirian GlcN-HCl sintesis
Pencirian yang dilakukan pada GlcN-HCl sintesis adalah indeks bias, titik leleh, dan FTIR. Hasil ini dibandingkan dengan pencirian GlcN-HCl pada literatur dan standar. Hasil pencirian dapat dilihat pada Tabel 1.
Tabel 1 Perbandingan pencirian GlcN-HCl sintesis dan standar terhadap literatur
Sifat fisik
yang diuji sintesis standar Literatur
Titik leleh (dekomposisi)
184-191°C
188-193°C
190-194°C
Indeks bias 1.3324 1.3327 -
Berdasarkan data dalam Tabel 1, GlcN-HCl sintesis menunjukkan sifat fisik yang mirip dengan GlcN-HCl standar. Hal ini menunjukkan bahwa prosedur sintesis yang digunakan dapat menghasilkan GlcN-HCl yang baik.
Keberhasilan sintesis GlcN-HCl dari kitosan juga dapat ditunjukkan dari hasil analisis spektrofotometer FTIR. Spektrum FTIR kitosan (Lampiran 3) memperlihatkan pita-pita serapan yang kuat pada bilangan gelombang 1649 dan 1561 cm-1. Senyawa-senyawa yang mengandung gugus amida sekunder dicirikan oleh pita serapan karbonil di sekitar 1640 cm-1 (pita amida I) dan serapan tekuk N-H di sekitar 1515-1570 cm-1 (pita s uhu (derajat Celsius)
[H C l] ( N )
! " # $ % " &#
" &#
s uhu (derajat Celsius)
w a k tu ( m e n it ) & & & & & kadar 85
85- 90
90- 95
GlcN-HCl
> 95 (%)
< 80
80-
suhu (derajat Celsius) = 89,9603 waktu (menit) = 117,902 kadar GlcN-HCl (%) = 95,0609
! " ' ( )! " & & " ! "
' ( )! " & " #& [HCl] (N) w a k tu ( m e n it ) & & & &
& $' %( )! " &" && " & $ % " ' ( )! " &
amida II). Selain itu pada daerah 3000-3750 cm-1 terdapat pita serapan ulur NH2 yang lebar
(Silverstein et al. 2005, Fuson et al. 2004). Spektrum FTIR GlcN-HCl sintesis dan standar (Lampiran 9) diringkaskan pada Tabel 2.
Tabel 2 Serapan FTIR GlcN-HCl standar dan hasil sintesis terhadap literatur
Serapan Daerah bilangan gelombang (cm
-1)
Standar Sintesis Literatur
Ulur N-H (NH3+)
Tekuk N-H (NN-H3+)
Ulur C-N Glikosida 3312 dan 3297 (lebar,kuat); 2800 (menengah) 1637 dan 1600 (tajam,kuat); 1537 (tajam, kuat) 1034 (tajam,kuat) 1143 3344 dan 3294 (lebar,kuat); 2837 (menengah) 1617 (tajam,kuat) dan 1600 (tajam, menengah); 1538 (tajam, kuat) 1034 (tajam, kuat) 1143 2800-3000 (lebar,kuat); 2000-2800 (menengah)a 1575-1600; 1504-1550b 1020-1250 (tajam,kuat)a 1140-1175
a Fuson et al . (2004) b Silverstein et al. (2005)
Spektrum GlcN-HCl hasil sintesis menunjukkan pita-pita serapan yang khas untuk senyawa yang mengandung gugus garam amina primer, seperti spektrum FTIR GlcN-HCl standar. Spektrum tersebut memperlihatkan pita-pita serapan tekuk N-H tanpa pita serapan karbonil. Selain itu terlihat juga pita serapan ulur N-H (NH3+) berbentuk
khas pada 3300 cm-1 yang membentuk bahu pada 2800 cm-1. Baik spektrum FTIR GlcN-HCl standar maupun sintesis menunjukkan pita serapan khas ikatan glikosida pada bilangan gelombang 1143 cm-1. Pita tersebut terlihat jauh lebih kuat pada spektrum GlcN-HCl sintesis karena proses hidrolisis yang dilakukan belum cukup kuat untuk memutus sebagian besar ikatan glikosida antar monomer GlcN-HCl.
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil penelitian dapat disimpulkan bahwa metode hidrolisis kitosan dengan menggunakan HCl memberikan kadar GlcN-HCl antara 75.10 dan 99.37%. Kondisi
optimum sintesis GlcN-HCl pada konsentrasi HCl 4 N, interval waktu 140 menit, dan suhu 90°C.
Saran
Perlu dilakukan validasi penetapan kadar GlcN-HCl dan pemurnian lebih lanjut terhadap hasil sintesis GlcN-HCl.
DAFTAR PUSTAKA
AOAC. 1999. Official Methods of Analysis of AOAC International. 5th Revision. Volume 2. Cunnif P (Editor). Maryland: AOAC International.
Berry A, Burlingame RP, Millis JR, penemu; Patent Application Publication. 31 Oct 2002. Process for Production of N-Glucosamine. US patent 0160459 A1
Chang KLB, Lee J, Fu WR. 2000. HPLC Analysis of N-acetyl-oligosaccharides during the Acid Hydrolysis of Chitin. Food Drug Anal 8:75-83.
Fuson RC, Curtin DY, Morrill TC, Hermann CKF, Shriner RL. 2004. The Systematic Identification of Organic Compounds.Ed ke-8. Danvers: J Wiley.
Khan TA, Peh KK, Ch’ng HS. 2002. Reporting degree of deacetylation values of chitosan: the influence of analytical methods. J Pharm Pharmecet Sci 5: 205-212.
Kuboki A et al. 1998. Degradation of Derivatives of N-Acetyl-D-glucosamine by Rhodococcus rhodochrous IFO 15564: Substrate Specificity and Its Application to the Synthesis of Allyl α -N-Acetyl-D-glucosaminide. Biosci Biotechnol Biochem 62 (8): 1581-1585.
Kumirska J et al. 2008. Determination of the pattern of acetylation of low-molecular -weight chitosan used in biomedical
applications. Pharmaceut Biomedical Anal
50: 587-590.
6
Muzzarelli RAA et al. 1986. Methods for the determination of the degree of acetylation of chitin and chitosan. Di dalam Muzarelli RAA & Peter MG (Editor) 1997. Chitin Handbook. Ancona: Eur Chitin Soc. hlm 109-119.
Sajomsanga W et al. 2008. Synthesis and characterization of N-aryl chitosan derivatives. Int Bio Macromolecules 43:79–87.
Silverstein RM, Webster FX, dan Kiemle DJ. 2005. Spectrometric Identification of
Organic Compounds. Ed ke-7. Danvers: J Wiley.
Solomons TWG dan Fryhle CB. 2004. Organic Chemistry. Ed ke-8. Danvers: J Wiley.
8
Lampiran 1 Pencirian kitosan dan diagram Alir Penelitian
waktu : 60-180menit temperatur : 70-90°C [HCl] : 4-7 N Kitosan
Kadar Air (gravimetri) AOAC 1999
Kadar Abu (gravimetri) AOAC 1999
Derajat Deasetilasi (FTIR) Khan et al. 2002 Bobot Molekul (viskometer Ostwald) Tarbojevich & Cosani 1996
transformasi struktur kitosan
HCl
GlcN-HCl
hhjghghjkg
Uji kimia Uji fisik
• Indeks bias
• FTIR
Titik leleh GlcN-HCl
Standar dan literatur
GlcN-HCl optimum Olah data dengan
Lampiran 2
Penentuan kadar air, kadar abu, DD, dan bobot molekul kitosan
Penentuan Kadar Air (AOAC 1999)
Penentuan kadar air kitosan dapat dilakukan dengan metode gravimetri. Sebanyak kira-kira 1.0000 gram kitosan dimasukkan ke dalam cawan porselen yang telah diketahui bobotnya, kemudian cawan beserta isinya dimasukkan ke dalam oven pada suhu 105°C selama 3 jam atau sampai bobotnya konstan. Setelah itu, dimasukkan ke dalam desikator dan ditimbang. Pengeringan dan penimbangan diulang setiap jam sampai diperoleh bobot konstan. Kadar air kitosan dihitung dengan persamaan
Kadar air =
o k o
m
m
m
−
× 100%
Keterangan : mo = bobot sampel awal mk = bobot sampel kering
Penentuan Kadar Abu (AOAC 1999)
Penentuan kadar abu kitosan juga dilakukan dengan metode gravimetri. Cawan porselen dibersihkan dan dipanaskan ke dalam tanur untuk menghilangkan sisa-sisa kotoran yang menempel dalam cawan, kemudian didinginkan dalam eksikator dan ditimbang. Sebanyak kira-kira 0.5000 gram kitosan dimasukkan ke dalam cawan tersebut dan dipanaskan sampai tidak berasap, kemudian dibakar dalam tanur pengabuan dengan suhu 600°C sampai diperoleh abu berwarna putih. Setelah itu, cawan beserta isinya didinginkan dalam eksikator dan ditimbang. Kadar abu kitosan dihitung dengan persamaan:
Kadar abu =
o a
m
m
×100%
Keterangan : mo = bobot sampel awal
ma = bobot abu
Penentuan DD (Khan et al. 2002)
Penentuan yang umum dilakukan menggunakan spektrofotometri inframerah. Penentuan dengan metode ini relatif cepat, dan tidak memerlukan disolusi terhadap sampel kitosan dalam pelarut berair (Khan et al. 2002). Kitosan dibuat pelet dengan KBr 1%, kemudian dilakukan pemindaian pada daerah frekuensi antara 4000 cm-1 dan 400 cm-1. DD ditentukan dengan metode garis dasar.
Puncak tertinggi dicatat dan diukur dari garis dasar yang dipilih. Nilai absorbans dapat dihitung dengan menggunakan rumus
P
P
A
=
log
0P0 = % transmitans pada garis dasar
P = % transmitans pada puncak minimum
Kitosan yang terdeasetilasi sempurna (100%) memiliki nilai A1655 = 1.33. Dengan membandingkan
absorbans pada bilangan gelombang 1655 cm-1 (serapan pita amida I) dengan absorbans pada bilangan gelombang 3450 cm-1 (serapan gugus hidroksil), %DD dapat dihitung dengan persamaan
%
100
33
.
1
1
1
%
3450
1655
×
×
−
=
A
A
DD
10
Penentuan Bobot Molekul Kitosan (Tarbojevich & Cosani 1996)
Bobot molekul kitosan ditentukan dengan menggunakan metode viskometer. Sebanyak ± 0.2500 g kitosan dilarutkan dalam 250 mL asam asetat 0.5 M. Larutan ini dianggap sebagai larutan induk. Kemudian dari larutan tesebut dibuat larutan dengan ragam konsentrasi 0.2; 0.4; 0.6; dan 0.8 M. Diambil sebanyak 5 ml larutan dari pelarut, konsetrasi terendah hingga konsentrasi tertinggi dan dimasukkan ke dalam viskometer untuk ditentukan waktu alirnya.
Viskositas relatif
η
r=
η
η
0≅
t
t
0Viskositas spesifik
η
sp=
η
r−
1
Viskositas intrinsik
[ ]
(
)
0
→
=
η
spc
cη
ln ηsp/c = [η] + k’[η] c; dengan k’ antara 0.3 dan 0.7
[η]= KMa ; dengan K = 3.5 × 10-4 dan a = 0.76 t = waktu alir zat
Lampiran 3
Hasil pencirian kitosan
Penentuan Kadar Air
Sampel Ulangan
Bobot (gram)
Kadar
air (%) Rerata
cawan kitosan (cawan+
kitosan)1
(cawan+ kitosan)2
(cawan+ kitosan)3
Bobot Kering
Kitosan I 1
2 3
20.6820 20.4516 21.0252
1.0032 1.0025 1.0060
21.5797 21.3474 21.9247
21.5760 21.3434 21.9200
21.5760 21.3431 21.9216
0.8940 0.8915 0.8964
10.89 11.07 10.89
10.67% Kitosan
II
1 2 3
17.8787 18.4126 17.7426
1.0027 1.0011 1.0002
18.7782 19.3144 18.6478
18.7704 19.3050 18.6404
18.7740 19.3088 18.6423
0.8953 0.8962 0.8997
10.71 10.48 10.05
Penentuan Kadar Abu Kitosan
Ulangan Bobot (gram) Kadar abu (%)
wadah kitosan wadah+abu abu
1 34.3013 0.5025 34.8025 0.0012 0.24 2 30.1205 0.5020 30.1227 0.0017 0.33 3 23.6557 0.5009 28.6570 0.0013 0.24
Penentuan DD (Khan et al. 2002)
A1649 = log
= log .. = 0.7628 A3439 = log
= log .. = 2.1854
% DD = 1 − × . ×100%
= 1 − .. × . ×100%
= 73.76 %
v (cm-1) % T
Keterangan:
= Po = P
12
Penentuan Bobot Molekul Kitosan (Tarbojevich & Cosani 1996)
Larutan Konsentrasi (% b/v)
Bobot Sampel (gram)
Waktu Alir (detik) Rerata (detik)
Bobot Molekul (g.mol-1)
1 2 3
Pelarut O.5 N - 63 64 64 63.67 -
Kitosan 0.02 0.04 0.06 0.08 0.10 0.2510 69 75 82 90 98 69 75 82 90 98 69 75 82 90 98 69 75 82 90 98 370,163
Larutan Konsentrasi
(% b/v) ηr ηsp ηsp/c ln ηsp/c ln (t/to-1)
Kitosan 0.02 0.04 0.06 0.08 0.10 1.0837 1.1779 1.2879 1.4135 1.5392 0.0837 0.1779 0.2879 0.4135 0.5392 418.56 444.87 479.82 516.92 539.18 6.0368 6.0978 6.1734 6.2478 6.2900 -2.4803 -1.7263 -1.2452 -0.8830 -0.6177
Penentuan Bobot Molekul Kitosan y = 3.29x + 5.9716
R2 = 0.992 Berarti, [η] = 5.9716
M0,76 = 5.9716/3.5 × 10-4 M0,76 = 17062
M = 370,163.3836 g.mol-1
y = 3,29x + 5,9716 R² = 0,9924
6 6,05 6,1 6,15 6,2 6,25 6,3 6,35
0 0,02 0,04 0,06 0,08 0,1 0,12
ln
η
sp
/c
Lampiran 4
Rancangan percobaan (keluaran minitab 14)
Disain Box-Behnken
14
16
Lampiran 6 Penentuan kurva baku kadar GlcN-HCl terhadap konsentrasi NaOH
No Volume GlcN-HCl baku yang ditambahkan (mL) Bobot GlcN-HCl (gram)
pH NaOH (mL) Volume NaOH
(mL)
Mol NaOH (mmol) awal akhir awal akhir
1. 2. 3. 4. 5. 6. 7. 0.50 1.00 3.00 5.00 7.00 9.00 10.00 0.0050 0.0101 0.0302 0.0504 0.0705 0.0906 0.1007 5.93 5.99 5.97 5.87 5.92 5.85 5.82 8.89 8.93 8.97 9.02 8.95 8.92 8.87 0.00 0.24 0.74 2.08 4.23 7.12 10.63 0.24 0.74 2.08 4.23 7.12 10.63 14.64 0.24 0.50 1.34 2.15 2.89 3.51 4.01 0.0216 0.0450 0.1205 0.1933 0.2598 0.3155 0.3605
y = 3,464x + 0,0111 R² = 0,9977
0,0000 0,0500 0,1000 0,1500 0,2000 0,2500 0,3000 0,3500 0,4000
0,0000 0,0200 0,0400 0,0600 0,0800 0,1000 0,1200
Lampiran 7 Penentuan kadar GlcN-HCl
No. Suhu (°C) [HCl]
(N)
Waktu (menit)
Bobot GlcN-HCl sintesis (gram)
pH NaOH (mL) Volume NaOH
(mL) Kadar (% b/b)
awal akhir Meniskus awal Meniskus akhir
18
Lampiran 8 Penentuan koefisien regresi dan analisis ragam kadar GlcN-HCl
Estimated Regression Coefficients for [glukosamina]
Term Coef SE Coef T P Constant 88,2117 2,180 40,455 0,000 suhu 3,9769 1,335 2,978 0,007 [HCl] -1,0281 1,335 -0,770 0,450 waktu 4,7950 1,335 3,591 0,002 suhu*suhu 3,0210 1,965 1,537 0,140 [HCl]*[HCl] 1,1260 1,965 0,573 0,573 waktu*waktu -3,7427 1,965 -1,904 0,071 suhu*[HCl] -0,8738 1,888 -0,463 0,649 suhu*waktu -1,8150 1,888 -0,961 0,348 [HCl]*waktu 3,4825 1,888 1,844 0,080
Analysis of Variance for [glukosamina]
Source DF Seq SS Adj SS Adj MS F P Regression 9 962,5 962,5 106,94 3,75 0,007 Linear 3 637,8 637,8 212,61 7,45 0,002 Square 3 195,1 195,1 65,04 2,28 0,110 Interaction 3 129,5 129,5 43,16 1,51 0,242 Residual Error 20 570,5 570,5 28,53
Lack-of-Fit 3 327,6 327,6 109,19 7,64 0,002 Pure Error 17 243,0 243,0 14,29
Total 29 1533,0
Unusual Observations for [glukosamina]
Obs StdOrder [glukosamina] Fit SE Fit Residual St Resid 17 15 76,140 88,212 2,180 -12,072 -2,48 R
Lampiran 9 Perbandingan spektrum FTIR GlcN-HCl sintesis dengan standar
4000.0 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 600 450.0
3.0 4 6 8 10 12 14 16 18 20 22 24 26 28 30 31.0
cm-1 %T