KARAKTERISASI CENDAWAN Botryodiplodia theobromae
DAN Rhizoctonia solani DARI BERBAGAI TANAMAN INANG
BERDASARKAN MORFOLOGI DAN POLA RAPD-PCR
YAYU SITI NURHASANAH
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
YAYU SITI NURHASANAH. Karakterisasi Cendawan Botryodiplodia theobromae dan Rhizoctonia solani dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola RAPD-PCR. Dibimbing oleh KIKIN HAMZAH MUTAQIN dan SURYO WIYONO.
Cendawan Botryodiplodia theobromae (Pat.) dan Rhizoctonia solani (Kuhn.) masing-masing memiliki kisaran inang yang luas dan gejala yang beragam bergantung inangnya. Morfologi cendawan tersebut dari inang yang berbeda nampak serupa, namun ada kemungkinan bahwa dapat berbeda apabila dianalisis lebih dalam lagi karakteristiknya secara morfologi maupun molekuler. Penelitian ini bertujuan untuk mengkarakterisasi cendawan B. theobromae dan
R. solani dari berbagai tanaman inang berdasarkan morfologi dan pola DNA cendawan dengan teknik RAPD. Berdasarkan pengamatan karakter masing-masing isolat B. theobromae berasal dari lima tanaman inang yaitu, jeruk, kakao, karet, manggis, dan pisang serta R. solani berasal dari lima tanaman inang yaitu, jagung, nanas, padi, sorghum, dan ubi jalar, kedua cendawan tersebut menunjukkan keragaman morfologi. Ukuran konidia B. theobromae asal jeruk, kakao, karet dan pisang menunjukkan perbedaan yang nyata. Konidia isolat
B. theobromae asal manggis tidak terbentuk baik pada media Water Agar (WA) yang diberi jerami maupun pada Potato Dextrose Agar (PDA), hal ini menunjukkan bahwa pembentukan konidia yang optimum membutuhkan kondisi lingkungan tertentu. Hasil analisis menggunakan teknik Random amplified polymorphic-Polymerase chain reaction (RAPD-PCR) terhadap B. theobromae
asal jeruk, karet, kakao, manggis, dan pisang menggunakan primer OPD 06 dan OPN 07 menghasilkan pola pita DNA yang berbeda baik dari jumlah maupun ukuran fragmen DNA. Demikian juga hasil analisis RAPD-PCR terhadap isolat
R. solani asal jagung, nanas, padi, sorghum, dan ubi jalar menggunakan primer OPD 06 dan OPN 07 menghasilkan pola pita DNA yang berbeda. Hasil tersebut menunjukkan bahwa antar isolat B. theobromae maupun R. solani yang berasal dari masing-masing inangnya yang berbeda menunjukkan perbedaan genetik yang nyata.
Kata kunci: Botryodiplodia theobromae, Rhizoctonia solani, karakter morfologi, RAPD-PCR.
YAYU SITI NURHASANAH. Karakterisasi Cendawan Botryodiplodia theobromae dan Rhizoctonia solani dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola RAPD-PCR. Dibimbing oleh KIKIN HAMZAH MUTAQIN dan SURYO WIYONO.
Cendawan Botryodiplodia theobromae (Pat.) dan Rhizoctonia solani (Kuhn.) masing-masing memiliki kisaran inang yang luas dan gejala yang beragam bergantung inangnya. Morfologi cendawan tersebut dari inang yang berbeda nampak serupa, namun ada kemungkinan bahwa dapat berbeda apabila dianalisis lebih dalam lagi karakteristiknya secara morfologi maupun molekuler. Penelitian ini bertujuan untuk mengkarakterisasi cendawan B. theobromae dan R. solani dari berbagai tanaman inang berdasarkan morfologi dan pola DNA cendawan dengan teknik RAPD. Berdasarkan pengamatan karakter masing-masing isolat B. theobromae berasal dari lima tanaman inang yaitu, jeruk, kakao, karet, manggis, dan pisang serta R. solani berasal dari lima tanaman inang yaitu, jagung, nanas, padi, sorghum, dan ubi jalar, kedua cendawan tersebut menunjukkan keragaman morfologi. Ukuran konidia B. theobromae asal jeruk, kakao, karet dan pisang menunjukkan perbedaan yang nyata. Konidia isolat B. theobromae asal manggis tidak terbentuk baik pada media Water Agar (WA) yang diberi jerami maupun pada Potato Dextrose Agar (PDA), hal ini menunjukkan bahwa pembentukan konidia yang optimum membutuhkan kondisi lingkungan tertentu. Hasil analisis menggunakan teknik Random amplified polymorphic-Polymerase chain reaction (RAPD-PCR) terhadap B. theobromae asal jeruk, karet, kakao, manggis, dan pisang menggunakan primer OPD 06 dan OPN 07 menghasilkan pola pita DNA yang berbeda baik dari jumlah maupun ukuran fragmen DNA. Demikian juga hasil analisis RAPD-PCR terhadap isolat R. solani asal jagung, nanas, padi, sorghum, dan ubi jalar menggunakan primer OPD 06 dan OPN 07 menghasilkan pola pita DNA yang berbeda. Hasil tersebut menunjukkan bahwa antar isolat B. theobromae maupun R. solani yang berasal dari masing-masing inangnya yang berbeda menunjukkan perbedaan genetik yang nyata.
KARAKTERISASI CENDAWAN Botryodiplodia theobromae
DAN Rhizoctonia solani DARI BERBAGAI TANAMAN INANG
BERDASARKAN MORFOLOGI DAN POLA RAPD-PCR
YAYU SITI NURHASANAH
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Pertanian pada
Departemen Proteksi Tanaman
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
BOGOR
Judul Skripsi : Karakterisasi Cendawan Botryodiplodia theobromae dan
Rhizoctonia solani dari Berbagai Tanaman Inang
Berdasarkan Morfologi dan Pola RAPD-PCR.
Nama Mahasiswa : Yayu Siti Nurhasanah
NRP : A34070058
Menyetujui,
Pembimbing I Pembimbing II
Dr. Ir. Kikin H. Mutaqin, MSi. Dr. Ir. Suryo Wiyono, MSc.Agr.
NIP 19680602 199303 1003 NIP 19690212 199203 1003
Mengetahui,
Ketua Departemen Proteksi Tanaman
Dr. Ir. Abdjad Asih Nawangsih, M.Si.
NIP 19650621 198910 2001
RIWAYAT HIDUP
Penulis dilahirkan di Bandung pada tanggal 13 Januari 1990 dari pasangan
Abdul Somad Sodikin dan Nenden Nurochmah. Penulis merupakan anak kedua
dari dua bersaudara.
Pada tahun 1995-2001 Penulis menempuh pendidikan di Sekolah Dasar
Assalaam I Bandung, kemudian pada tahun 2001-2004 di Sekolah Menengah
Pertama Negeri 43 Bandung. Pada tahun 2004 penulis melanjutkan pendidikan di
Sekolah Menengah Atas Muhammadiyah I Bandung dan lulus pada tahun 2007.
Pada tahun yang sama penulis diterima di Departemen Proteksi Tanaman,
Fakultas Pertanian, Institut Pertanian Bogor melalui jalur Undangan Seleksi
Masuk IPB (USMI).
Selama masa kuliah penulis memperoleh pengalaman organisasi sebagai
pengurus Himpunan Mahasiswa Proteksi Tanaman (HIMASITA) pada periode
2009/2010 dan periode 2010/2011. Penulis menjadi Asisten mata kuliah
Dasar-Dasar Proteksi Tanaman pada tahun 2010 dan menjadi Asisten mata kuliah Ilmu
Penyakit Tumbuhan Dasar pada tahun 2011. Penulis mengikuti kegiatan magang
di Laboratorium Bakteriologi Tumbuhan, Departemen Proteksi Tanaman, Fakultas
Pertanian, Institut Pertanian Bogor pada tahun 2009, selain itu penulis mengikuti
kegiatan Program Kreatifitas Mahasiswa bidang Penelitian (PKMP) yang didanai
pada periode 2008/2009 dengan judul “Formulasi Bacillus subtilis Pada Tepung
Singkong Sebagai Probiotik Tanaman” dan periode 2009/2010 dengan judul
“Potensi Limbah Air Cucian Beras Sebagai Media Perbanyakan Bakteri Probiotik
PRAKATA
Puji dan syukur penulis panjatkan ke hadirat Allah SWT yang telah
melimpahkan rahmat dan hidayah-Nya, sehingga penulis dapat menyelesaikan
skripsi yang berjudul “Karakterisasi Cendawan Botryodiplodia theobromae dan
Rhizoctonia solani dari Berbagai Tanaman Inang Berdasarkan Morfologi dan Pola
RAPD-PCR”. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh
gelar Sarjana pada Departemen Proteksi Tanaman, Fakultas Pertanian, Institut
Pertanian Bogor.
Penulis mengucapkan terima kasih kepada Dr. Ir. Kikin H. Mutaqin, MSi.
dan Dr. Ir. Suryo Wiyono MSc.Agr. selaku dosen pembimbing tugas akhir
skripsi. Ucapan terima kasih juga disampaikan kepada Dr. Ir. Dhamayanti
Adidharma selaku dosen penguji yang telah memberikan saran dan masukannya.
Terima kasih kepada Dr. Ir. Dadan Hindayana selaku dosen Pembimbing
Akademik, Ibu Tuti (Laboran Laboratorium Virologi), Bapak Dadang (Laboran
Laboratorium Mikologi Tumbuhan), Ibu Ita (Staf Klinik Tanaman) atas seluruh
bantuannya. Terima kasih kepada Dr. Rustam, Ratdiana, SP. MSi. atas semua
masukannya, Agus Eko Prasetyo, SP. MSi., Haliatur Rahma, S.Si, MP, Adeline E
Tanati, SP. MSi., Tita Widjayanti SP. MSi., Tatit, Nelly, Nova, Fathia, Anti,
Annis, Hafidz, Reka, Izza, Nurul, Dewi, Ida, Dolpina, Bapak Fajar, Ariny, Evi,
Helynda, Ibu Dian, dan teman-teman mahasiswa Proteksi Tanaman angkatan 44
atas doa, bantuan, dan dukungannya.
Secara khusus dukungan dan pengertian yang diberikan orang tua serta
kakak kandung Dikdik Mohammad Taufiq kepada penulislah yang menjadi
penyemangat dan dorongan yang sangat berarti dalam penyelesaian skripsi dan
studi di IPB ini.
Bogor, Februari 2012
DAFTAR ISI
Halaman
DAFTAR TABEL ... viii
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN ... x
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 2
Manfaat Penelitian ... 2
TINJAUAN PUSTAKA ... 3
Cendawan Botryodiplodia theobromae ... 3
Taksonomi Cendawan ... 3
Bioekologi dan Nilai Ekonomi ... 3
Gejala Penyakit dan Kisaran Inang ... 4
Cendawan R. solani ... 6
Taksonomi Cendawan ... 6
Bioekologi dan Nilai Ekonomi ... 6
Gejala Penyakit dan Kisaran Inang ... 7
Polymerase Chain Reaction (PCR) ... 8
Random Amplified Polymorphic DNA-Polymerase Chain Reaction (RAPD-PCR) ... 9
BAHAN DAN METODE ... 11
Tempat dan Waktu ... 11
Metode Penelitian ... 11
Penyiapan Isolat Cendawan ... 11
Pengamatan Koloni ... 12
Pengamatan Konidia dan Hifa ... 12
Analisis Data Karakter Morfologi ... 12
Ekstraksi DNA ... 12
RAPD-PCR ... 13
Elektroforesis ... 13
HASIL DAN PEMBAHASAN ... 14
Karakter Morfologi B. theobromae ... 15
Karakter Molekuler Cendawan B. theobromae ... 24
Gejala Penyakit oleh Cendawan R. solani ... 26
Karakter Morfologi R. solani ... 27
Karakter Molekuler Cendawan R. solani ... 31
KESIMPULAN DAN SARAN ... 35
Kesimpulan ... 35
Saran ... 35
DAFTAR PUSTAKA ... 36
DAFTAR TABEL
Halaman
1. Isolat-isolat cendawan yang digunakan dalam penelitian ... 11
2. Pertumbuhan diameter koloni cendawan B. theobromae ... 17
3. Pembentukan konidia muda, konidia matang, dan piknidia B.
theobromae pada media WA dan PDA ... 21
4. Ukuran panjang, lebar, dan tebal dinding konidia muda B.
theobromae ... 22
5. Ukuran panjang, lebar, dan tebal dinding konidia matang B.
theobromae ... 23
6. Ukuran fragmen DNA B. theobromae dengan RAPD menggunakan primer OPD 06 ...
24
7. Ukuran fragmen DNA B. theobromae dengan RAPD menggunakan primer OPN 07 ...
25
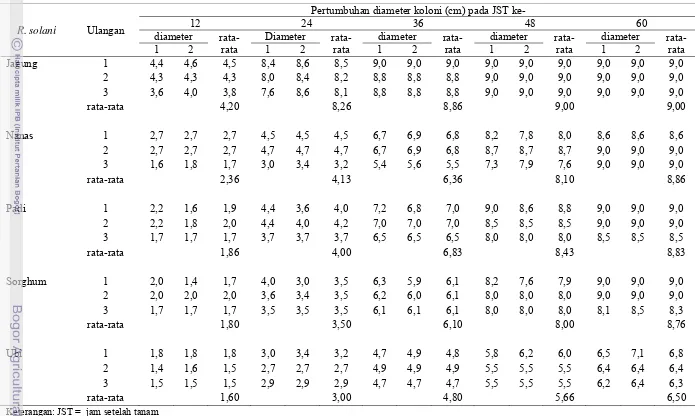
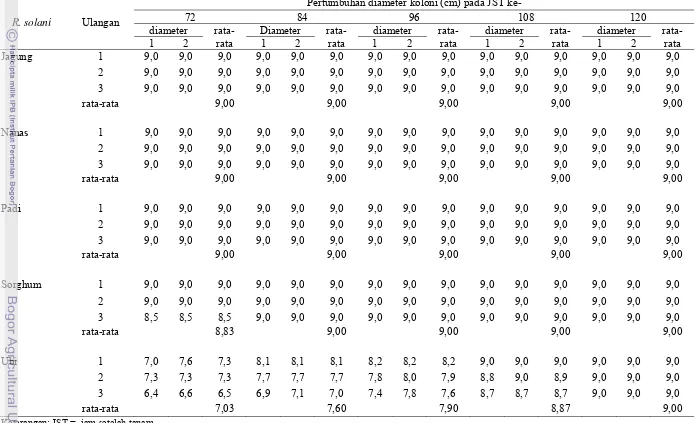
8. Pertumbuhan diameter koloni cendawan R. solani ... 29
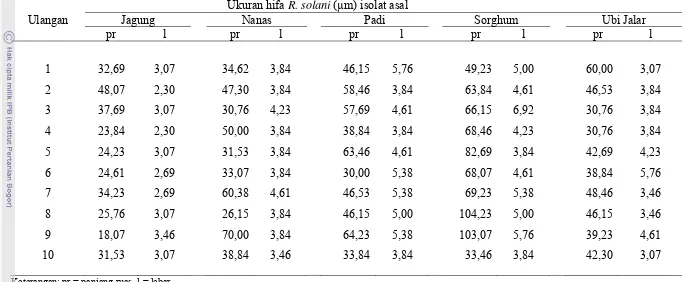
9. Ukuran panjang ruas dan lebar hifa cendawan R. solani ... 30
10. Ukuran fragmen DNA R. solani dengan RAPD menggunakan primer OPD 06 ...
32
11. Ukuran fragmen DNA R. solani dengan RAPD menggunakan primer OPN 07 ...
DAFTAR GAMBAR
Halaman
1. Gejala penyakit yang disebabkan oleh cendawan B. theobromae ………. 14
2. Koloni isolat cendawan B. theobromae umur 3 dan 11 HST (hari setelah tanam) ……… 16
3. Grafik pertumbuhan koloni cendawan B. theobromae ……….. 16
4. Piknidia cendawan B. theobromae dengan perbesaran 40X ……….. 18
5. Piknidia B. theobromae yang pecah mengeluarkan konidia dengan pewarnaan lactophenol blue ……….. 18
6. Konidia cendawan B. theobromae ……… 20
7. Profil DNA lima isolat cendawan B. theobromae dengan RAPD-PCR menggunakan primer OPD 06 ……….. 24
8. Profil DNA lima isolat cendawan B. theobromae dengan RAPD-PCR menggunakan primer OPN 07 ……….. 25
9. Gejala penyakit yang disebabkan oleh cendawan R. solani ………. 27
10. Koloni isolat cendawan R. solani umur 4 dan 8 HST ……….. 28
11. Grafik pertumbuhan koloni cendawan R. solani ……….. 29
12. Hifa R. solani dengan pewarnaan lactophenol blue ………. 30
13. Sklerotia cendawan R. solani ………... 31
14. Profil DNA lima isolat cendawan R. solani dengan RAPD-PCR menggunakan primer OPD 06 ……….. 32
DAFTAR LAMPIRAN
Halaman
1. Pertumbuhan diameter koloni cendawan B. theobromae ……… 40
2. Ukuran panjang, lebar, dan tebal dinding konidia muda cendawan B.
theobromae ………..……….……….. 41
3. Ukuran panjang dan lebar konidia matang cendawan B. theobromae ... 42
4. Pengukuran rasio panjang/lebar konidia muda cendawan B.
theobromae ………. 42
5. Pengukuran rasio panjang/lebar konidia matang cendawan B.
theobromae ………. 43
6. Analisis ragam ukuran panjang, lebar, tebal dinding, dan rasio
panjang/lebar konidia muda B. theobromae ……... 43
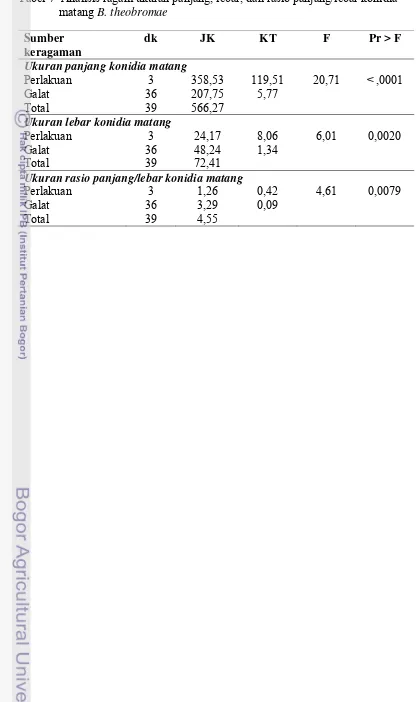
7. Analisis ragam ukuran panjang, lebar, dan rasio panjang/lebar konidia matang B. theobromae ………..
44
8. Pertumbuhan diameter koloni cendawan R. solani ………. 45
9. Ukuran panjang ruas dan lebar hifa cendawan R. solani ……… 47
10. Ukuran sudut percabangan cendawan R. solani ……….. 49
11. Analisis ragam ukuran panjang ruas, lebar, sudut tumpul, dan sudut lancip hifa R. solani ……….
51
PENDAHULUAN
Latar Belakang
Cendawan Botryodiplodia theobromae (Pat.) dan cendawan Rhizoctonia
solani (Kuhn.) termasuk patogen tanaman yang dapat menimbulkan kerugian
secara ekonomi dan masing-masing menginfeksi berbagai jenis tanaman penting.
Cendawan tersebut dapat menurunkan kuantitas dan kualitas produk pertanian
secara langsung maupun secara tidak langsung.
Penyakit yang disebabkan oleh cendawan B. theobromae pada buah jeruk
adalah penyakit kulit diplodia pada batang atau ranting, sedangkan pada pisang
menyebabkan busuk buah. Pada kakao cendawan ini menimbulkan gejala mati
pucuk dan busuk buah (CABI 2007). Pada karet B. theobromae dapat
menyebabkan stem bleeding, mati pucuk, dan puru (Pha et al. 2009).
R. solani dapat menyebabkan penyakit hawar pelepah pada padi, jagung, dan
sorghum, kanker batang pada ubi jalar (CABI 2007), selain itu cendawan tersebut
dapat menyebabkan rebah kecambah, luka akar coklat kemerahan (reddish brown
root lesions), busuk batang, busuk akar, busuk mahkota, hawar daun, hawar
batang dan ranting, kanker rhizoctonia, dan black scurf (Schumann & D’Arcy
2006). R. solani dapat menyerang tanaman padi, juga dapat menginfeksi hampir
50 spesies tanaman lainnya (Zhang et al. 2009).
B. theobromae dan R. solani masing-masing memiliki kisaran inang yang
luas dan gejala yang beragam bergantung inang yang diserangnya. Secara
morfologi cendawan-cendawan tersebut dari inang yang berbeda nampak serupa,
namun ada kemungkinan bahwa cendawan tersebut berbeda bila dianalisis lebih
dalam baik secara morfologi maupun molekuler. Identifikasi cendawan umumnya
dilakukan berdasarkan karakter morfologinya. Identifikasi dan karakterisasi secara
morfologi cendawan B. theobromae dapat dilakukan berdasarkan piknidia dan
konidia, sedangkan untuk cendawan R. solani dapat berdasarkan hifanya
(Watanabe 2002).
Analisis secara molekuler berdasarkan DNA menggunakan teknik
Polymerase Chain Reaction (PCR) saat ini sudah berkembang pesat dalam dua
dasawarsa terakhir. Aplikasi PCR sudah umum diterapkan dalam bidang penyakit
yang dapat digunakan untuk melihat keragaman genetik cendawan adalah teknik
Random Amplified Polymorphic DNA-Polymerase Chain Reaction (RAPD-PCR).
Menurut El-Fadly et al. (2008) ciri-ciri cendawan berdasarkan analisis molekuler
dapat digunakan sebagai alternatif atau pelengkap selain karakterisasi cendawan
secara morfologi. Selain itu RAPD juga merupakan teknik yang sensitif sehingga
dapat digunakan untuk deteksi perbedaan genetik antar individu (Lanfranco et al.
1998).
Tujuan Penelitian
Penelitian ini bertujuan untuk mengkarakterisasi cendawan Botryodiplodia
theobromae dan Rhizoctonia solani dari berbagai tanaman inang berdasarkan
morfologi dan pola DNA dengan teknik RAPD.
Manfaat Penelitian
Manfaat yang diharapkan dari penelitian ini ialah tersedianya informasi
karakter morfologi dan molekuler untuk menunjukkan ada tidaknya perbedaan
TINJAUAN PUSTAKA
Cendawan Botryodiplodia theobromae
Taksonomi Cendawan
Klasifikasi cendawan Botryodiplodia theobromae (Alexopoulos et al. 1996)
adalah sebagai berikut:
Domain : Eukaryota
Kingdom : Fungi
Phylum : Deuteromycota
Kelas : Deuteromycetes
Ordo : Sphaeropsidales
Famili : Sphaeropsidaceae
Genus : Botryodiplodia
Spesies : Botryodiplodia theobromae (Pat.) (anamorph)
Cendawan B. theobromae (Pat.) memiliki nama lain Lasiodiplodia
theobromae (Pat.) Griff. et Maubl., yang dahulu lebih dikenal dengan nama
Diplodia natalensis P. Evans. Cendawan tersebut merupakan cendawan yang
bereproduksi secara aseksual (anamorph), cendawan tersebut memiliki fase
seksual (teleomorph) yaitu sebagai cendawan Botryosphaeria rhodina (CABI
2007).
Bioekologi dan Nilai Ekonomi
B. theobromae merupakan cendawan yang bersifat polifag dan memiliki
kisaran inang yang luas. Patogen ini merupakan parasit lemah yang melakukan
infeksinya melalui luka-luka mekanis seperti akibat pemangkasan atau luka akibat
serangga (Semangun 2007).
Piknidia merupakan tubuh buah yang berbentuk seperti labu yang
didalamnya terdapat konidiofor dan memproduksi konidia (Agrios 2005). Piknidia
B. theobromae berwarna cokelat, berbentuk tabung dan berkumpul. Konidiofor
hialin, sederhana, dan menyatu. Pada konidiofor dibentuk konidia yang berpencar
secara tunggal, hialin, berbentuk jorong atau silinder, pada umumnya terdiri dari
Ukuran piknidia 210 µm X 150 µm (Watanabe 2002). Pada media buatan, waktu
yang dibutuhkan B. theobromae untuk menghasilkan piknidia adalah antara 20-34
hari (Shah et al. 2010). Pada umumnya konidia yang dibentuk oleh B. theobromae
berukuran 10-18 µm X 17-43 µm. Konidia muda hialin, tidak bersekat (satu sel),
dan berbentuk jorong, sedangkan konidia matang memiliki satu sekat (dua sel)
(Timmer et al. 2000).
Cendawan B. theobromae ditemukan terdapat di berbagai belahan dunia
diantaranya, di Amerika bagian utara dan selatan, Eropa, Afrika, Asia, dan
Oceania (Urbez-Torres et al. 2008). Sejak akhir 1980 area perkebunan kakao di
Kamerun mengalami kejadian penyakit mati ujung (dieback) yang luar biasa yang
disebabkan oleh B. theobromae. Di beberapa perkebunan, penyakit ini dapat
merugikan tanaman kakao sampai 100%, hal ini menjadi pembatas produksi
kakao di Kamerun (Mbenoun et al. 2008). Pada tahun 1998 B. theobromae
ditemukan pada pohon karet di Vietnam dan menyebabkan mati pucuk pada
pembibitan, cendawan terus berkembang dan menyebabkan kerusakan yang serius
sehingga menekan produksi perkebunan di Dau Tieng Rubber Company (Pha et
al. 2009). Menurut Rustini (2010) di Denpasar, Bali, hampir 53,24% dari buah
pisang yang dijual mengalami pembusukan akibat cendawan B. theobromae, hal
ini menyebabkan tidak terpenuhinya kebutuhan pasar karena permintaan pisang di
Bali cukup tinggi untuk berbagai upacara keagamaan. Di Kabupaten Magetan,
Jawa Timur, 500 ha pertanaman jeruk besar yaitu sekitar 85% dari jumlah
tanaman telah terserang oleh penyakit diplodia yang disebabkan oleh
B. theobromae dengan tingkat serangan ringan sampai sedang dengan persentase
22-37% (Wiratno & Nurbanah 1997).
Gejala Penyakit dan Kisaran Inang
Cendawan B. theobromae memiliki kisaran inang yang luas, selain dapat
menyerang tanaman jeruk, kakao, karet, manggis, dan pisang, cendawan tersebut
juga dapat menyerang tanaman mangga, nanas, alpukat, melon, kelapa, terong,
paprika, kacang tanah, jagung, tebu dan tembakau (CABI 2007).
Cendawan B. theobromae pada jeruk menyebabkan penyakit kulit diplodia
Miselium muncul di permukaan jaringan pada keadaan lingkungan yang lembab
(Semangun 2007).
Pada tanaman kakao, B. theobromae merupakan parasit lemah atau parasit
sekunder terutama pada bagian cabang dan ranting. Sebagai parasit lemah
cendawan ini hanya dapat menginfeksi jaringan-jaringan lemah, mengikuti
patogen yang kuat atau menginfeksi melalui luka-luka yang diakibatkan oleh
serangga. B. theobromae dapat menyebabkan mati pucuk, busuk buah, dan kanker
batang (Semangun 2000). Pada awalnya, daun yang paling dekat dengan ranting
yang terserang akan berwarna kuning, kemudian kerusakan akan terus meluas
sepanjang cabang dan mencapai batang utama lalu tanaman akan mati dengan
cepat. Bagian dalam ranting dan cabang akan mengalami perubahan warna
menjadi cokelat di bagian pembuluh. Juga terdapat eksudat berwarna putih atau
kekuningan yang keluar dari batang utama (Mbenoun et al. 2008).
Pada tanaman karet, B. theobromae dapat menyebabkan mati pucuk, pustul
yang berukuran 3-5 mm dan kulit menjadi busuk disertai keluarnya lateks atau
getah pada tanaman muda berumur 1-2 tahun. Pada serangan yang berat dapat
menyebabkan retak dan gummosis. Selain itu cendawan ini dapat menekan
pertumbuhan tanaman, menyebabkan produksi lateks rendah, dan untuk varietas
yang rentan seluruh pohon mati dalam waktu 3-4 minggu (Pha et al. 2009).
Serangan B. theobromae menyebabkan busuk buah pada manggis. Pada
awalnya kulit buah manggis akan berubah warna menjadi kehitaman dan
mengkilat, kemudian warnanya menjadi suram karena B. theobromae membentuk
banyak piknidia yang menghasilkan konidium. Biasanya gejala dimulai dari dekat
tangkai, dengan cepat akan meluas ke seluruh buah (Semangun 2007).
Penyakit busuk buah merupakan penyakit pasca panen pada pisang yang
disebabkan oleh B. theobromae. Cendawan ini menyebabkan busuk ujung buah
(tip rot), busuk telapak, dan busuk pangkal. Buah menjadi lunak dan berair, serta
mengeluarkan bau (aroma) yang khas. Biasanya B. theobromae pada pisang hidup
pada bagian tanaman yang membusuk, infeksinya hanya melalui luka-luka. Spora
Cendawan Rhizoctonia solani
Taksonomi Cendawan
Klasifikasi cendawan Rhizoctonia solani (Alexopoulos et al. 1996) adalah sebagai berikut:
Domain : Eukaryota
Kingdom : Fungi
Phylum : Deuteromycota
Kelas : Deuteromycetes
Ordo : Agonomycetales
Genus : Rhizoctonia
Spesies : Rhizoctonia solani
Cendawan R. solani merupakan cendawan yang bereproduksi secara
aseksual (anamorph), cendawan tersebut memiliki fase seksual (teleomorph)
sebagai cendawan Thanatephorus cucumeris.
Bioekologi dan Nilai Ekonomi
Cendawan R. solani biasanya menyerang pada bagian tanaman yang
langsung bersentuhan dengan tanah atau yang berdekatan dengan tanah.
Cendawan ini dapat diidentifikasi dari karakter hifa yang khas, yaitu sudut
percabangan yang tegak lurus yang membedakan dengan cendawan lainnya.
Cendawan ini bertahan di tanah dengan memproduksi sklerotia berwarna cokelat
kemerahan hingga hitam sebagai struktur bertahan. (Schumann & D’Arcy 2006).
Sklerotia merupakan sekumpulan hifa yang memadat, berwarna gelap dan mampu
bertahan dalam kondisi lingkungan yang tidak menguntungkan (Agrios 2005).
Sklerotia R. solani memiliki ukuran dan bentuk yang beragam, umumnya
terbentuk pada permukaan inang dan di dalam jaringan tanaman inang, namun
juga dapat ditemukan pada material sisa-sisa tanaman (Sneh et al. 1998). R. solani
dapat bertahan hidup pada tanaman hidup atau sebagai saprofit pada sisa-sisa
bahan organik.
Penyakit yang disebabkan R. solani diantaranya, damping-off, busuk batang,
hawar daun, hawar batang dan ranting pada kacang tanah, kanker rhizoctonia,
black scurf pada kentang, hawar pelepah pada padi (Schumann & D’Arcy 2006).
Penyakit hawar pelepah pada jagung dilaporkan terdapat di beberapa negara
diantaranya: Georgia, Perancis, dan New Zealand serta dapat menyebabkan
kehilangan hasil hingga 30% (White 2000). Kanker batang pada ubi jalar yang
disebabkan oleh cendawan R. solani dilaporkan menyerang tanaman di seluruh
Amerika Serikat (Clark & Moyer 1988). Menurut Zhang et al. (2009) penyakit
hawar pelepah pada padi di Jepang menyebabkan kehilangan hasil sebesar 20%
dan mempengaruhi sekitar 120.000-190.000 ha pertanaman padi. Saat ini
R. solani menjadi salah satu ancaman utama bagi produksi sorghum di Filipina
(Pascual & Raymundo 1989). Di Indonesia penyakit busuk pelepah pada jagung
mengakibatkan kehilangan hasil pada tanaman jagung hingga 100% (Sudjono
1995).
Gejala Penyakit dan Kisaran Inang
R. solani memiliki kisaran inang yang luas, selain dapat menyerang tanaman
jagung, nanas, padi, sorghum, dan ubi jalar, cendawan tersebut juga dapat
menyerang tanaman kubis, brokoli, paprika, tomat, mentimun, kedelai, gandum,
cengkeh, jeruk dan bunga tulip (CABI 2007).
Gejala awal penyakit hawar pelepah yang disebabkan oleh cendawan
R. solani adalah terdapat bercak berwarna cokelat atau cokelat kemerahan pada
bagian batang yang dekat dengan akar dan pelepah. Bercak dapat meluas ke-
bagian tanaman lainnya hingga pada kejadian penyakit yang cukup parah tanaman
menjadi kering dan mati (White 2000).
Penyakit yang disebabkan oleh cendawan R. solani pada padi disebut
sebagai hawar upih daun dan busuk batang. Pada upih daun dan batang terdapat
bercak-bercak dengan tepian tidak beraturan, berbentuk jorong dengan tepi
berwarna cokelat kemerahan, sedangkan pusat bercak berwarna seperti jerami
atau kuning kehijauan. Bercak sering ditemukan terdapat dekat dengan lidah daun.
Jika keadaan lembab tumbuh benang-benang hifa berwarna putih atau cokelat
muda (Semangun 1991).
Gejala pada tanaman sorghum ditandai dengan adanya bercak-bercak tidak
seperti pita berwarna cokelat atau pada bagian pusat bercak berwarna jerami atau
cokelat kemerahan dan pada bagian pinggir pelepah berwarna cokelat. Dimulai
dari bagian bawah pelepah penyakit akan menyebar ke bagian atas mencapai
setinggi malai dan menyebabkan daun layu. Akibatnya biji akan matang prematur
sehingga biji kecil dan bobotnya ringan. Pada jaringan tanaman yang mati akan
muncul sklerotia (Pascual & Raymundo 1989).
Penyakit busuk batang rhizoctonia atau juga yang dikenal dengan busuk
rhizoctonia termasuk penting untuk ubi jalar. Batang tanaman ubi jalar yang
terserang R. solani akan mengalami pembusukan yang dimulai pada bagian
batang bawah tanaman yang dekat dengan tanah. R. solani menyebabkan gejala
daun menguning sekunder, tanaman menjadi kerdil, dan rebah kecambah. Pada
jaringan tanaman yang bergejala akan terbentuk sklerotia R. solani (Clark &
Moyer 1988).
Polymerase Chain Reaction (PCR)
Polymerase Chain Reaction (PCR) merupakan suatu metode yang memiliki
sensitivitas yang tinggi sehingga secara teoritis dapat mendeteksi satu molekul
dari suatu fragmen DNA tertentu. PCR ini banyak digunakan untuk mempelajari
gen spesifik atau urutan nukleotidanya (Schleif 1993). Teknik PCR didasarkan
pada kemampuan untai ganda DNA untuk menggandakan molekul DNA secara in
vitro melalui reaksi enzimatik untuk ampilifikasi fragmen DNA tertentu dari
sampel DNA yang kompleks dan dapat menghasilkan DNA target dalam jumlah
mikrogram (Edel 1998).
Dalam hitungan jam, PCR memungkinkan untuk dapat membuat salinan
dari fragmen DNA target dalam jumlah yang banyak, sedangkan dengan teknik
amplifikasi lain seperti kloning gen akan membutuhkan waktu berhari-hari atau
berminggu-minggu (Paolella 1998).
Empat komponen utama pada proses PCR adalah (1) DNA cetakan
(template), yaitu fragmen DNA yang akan dilipatgandakan (2) oligonukleotida
primer, yaitu suatu sekuen oligonukleotida pendek (15-25 basa nukleotida) yang
digunakan untuk mengawali sintesis rantai DNA, (3) deoksiribonukleotida
polymerase, yaitu enzim yang melakukan katalisis reaksi sintesis rantai DNA.
Komponen lain yang juga penting adalah senyawa bufer (Yuwono 2006).
Dalam PCR terjadi sintesis DNA target yang melibatkan enzim DNA
polymerase. Enzim ini berasal dari bakteri yang hidup di lingkungan suhu panas
ekstrim misalnya bakteri Thermus aquaticus yang hidup dalam air bersuhu sekitar
75ºC. Enzim dari bakteri tersebut dinamai taq polymerase yang memiliki suhu
optimum untuk aktif pada 72ºC dan tetap stabil pada suhu 94ºC (Paolella 1998).
Random Amplified Polymorphic DNA-Polymerase Chain Reaction (RAPD-PCR)
Random Amplified Polymorphic DNA-Polymerase Chain Reaction
(RAPD-PCR) merupakan salah satu teknik molekuler yang menggunakan penanda
tertentu untuk mempelajari keanekaragaman genetika. Dasar analisis RAPD
adalah menggunakan mesin PCR yang mampu mengamplifikasi sekuen DNA
secara in vitro. Teknik ini melibatkan penempelan primer tertentu yang dirancang
sesuai dengan kebutuhan. Setiap primer dapat berbeda untuk menelaah
keanekaragaman genetik kelompok yang berbeda. Penggunaan teknik RAPD
memungkinkan untuk mendeteksi polimorfisme fragmen DNA yang diseleksi
menggunakan satu primer acak (random), terutama karena amplifikasi DNA
secara in vitro dapat dilakukan dengan baik dan cepat dengan adanya PCR
(Suryanto 2003).
Teknik ini mampu menghasilkan jumlah karakter yang relatif banyak,
sehingga sangat membantu untuk keperluan analisis keanekaragaman organisme
yang tidak diketahui latar belakang genomnya. Teknik RAPD sering digunakan
untuk membedakan organisme tingkat tinggi (eukariot). Namun demikian
beberapa peneliti menggunakan teknik ini untuk membedakan organisme tingkat
rendah (prokariot) atau melihat perbedaan organisme tingkat rendah melalui
piranti organel sel seperti mitokondria (Suryanto 2003).
RAPD menggunakan primer tunggal pendek dengan urutan nukleotida acak,
dilakukan dengan suhu annealing rendah dan menghasilkan beberapa produk PCR
yang menghasilkan pola pita setelah dilakukan pemisahan oleh elektroforesis. Tes
DNA menggunakan RAPD umumnya dilakukan dengan primer non-spesifik
konvensional. Dengan demikian konsentrasi dari semua campuran bahan dalam
reaksi harus akurat. Selain itu kualitas dari template DNA dan Taq polymerase
merupakan faktor yang juga dapat mempengaruhi hasil RAPD (Edel 1998).
Teknik PCR ini telah digunakan juga di berbagai bidang mikologi, termasuk
genetika dan sistematika cendawan, ekologi dan mikrobiologi tanah, patologi
tanaman, mikologi medis, dan bioteknologi cendawan. RAPD-PCR semakin
banyak digunakan dalam menentukan taksonomi dan untuk mengkarakterisasi
populasi cendawan. Keuntungan dari penggunaan teknik RAPD-PCR adalah
sebelumnya tidak perlu mengetahui urutan DNA nya terlebih dahulu, sehingga
setiap primer acak dapat diuji untuk mengamplifikasi setiap DNA cendawan.
Lebih lanjut, RAPD-PCR mengamplifikasi DNA menggunakan primer yang tidak
spesifik, sehingga membutuhkan template DNA yang murni dan tidak dapat
BAHAN DAN METODE
Tempat dan Waktu
Penelitian dilakukan di Laboratorium Bakteriologi Tumbuhan dan
Laboratorium Mikologi Tumbuhan, Departemen Proteksi Tanaman Fakultas
Pertanian, Institut Pertanian Bogor mulai bulan Maret 2011 hingga November
2011.
Metode Penelitian
Penyiapan Isolat Cendawan
Dalam penelitian ini digunakan beberapa isolat cendawan baik
B. theobromae maupun R. solani. Isolat-isolat tersebut diperoleh baik dari koleksi
isolat Klinik Tanaman, maupun diisolasi dari tanaman sakit dari lapangan oleh
penulis, yang disajikan dalam tabel berikut ini:
Tabel 1. Isolat-isolat cendawan B. theobromae dan R. solani yang dikarakterisasi secara morfologi dan molekuler
Isolat B. theobromae Isolat R. solani
Tanaman asal Lokasi Kolektor Tanaman asal Lokasi Kolektor
Jeruk Jember, Jawa
Timur
Dr. Suryo Wiyono
Jagung Leuwi
Kopo, Bogor
Penulis
Kakao TN Lorelindu,
Sulawesi Tengah
Dr. Efi Toding Tondok
Nanas Lampung Dr. Suryo
Wiyono
Karet Pematang
Siantar, Sumatera Utara
Dr. Suryo Wiyono
Padi Cikarawang,
Bogor
Dr. Rustam
Manggis Bukit Tinggi, Sumatera
Barat
Dr. Suryo Wiyono
Sorghum Leuwi
Kopo, Bogor
Penulis
Pisang Ciampea,
Bogor, Jawa Barat
Dr. Suryo Wiyono
Ubi Jalar Kuningan Dr. Suryo Wiyono
Isolasi cendawan R. solani dilakukan dengan melembabkan jaringan
tanaman yang bergejala dalam cawan petri yang berisi kertas tisu lembab dan
diatas sedotan plastik, inkubasi dilakukan hingga sklerotia R. solani muncul,
sklerotia ditanam pada media Potato Dextrose Agar (PDA) untuk pemurnian.
Identifikasi secara morfologi dilakukan dengan kunci identifikasi Watanabe
Pengamatan Koloni
Biakan B. theobromae dan R. solani ditanam pada media Potato Dextrose
Agar (PDA) dengan cara mengambil biakan B. theobromae dan R. solani
menggunakan pelubang gabus (diameter = 5 mm) dan masing-masing ditanam
pada media PDA kemudian dilakukan ulangan sebanyak 3 kali. Pengamatan
diameter pertumbuhan koloni dilakukan 12 jam sekali selama empat hari untuk
B. theobromae dan lima hari untuk R. solani. Warna koloni diamati setiap hari
dimulai dari hari ke-1 hingga ke-18.
Pengamatan Konidia dan Hifa
Dua jenis media disiapkan, yaitu Potato Dextrose Agar (PDA) dan media
Water Agar (WA) yang dimodifikasi dengan diberi potongan jerami steril
digunakan untuk penumbuhan B. theobromae, sedangkan untuk R. solani
ditumbuhkan pada media PDA. Pengamatan dan pemotretan struktur cendawan
dilakukan di bawah mikroskop dengan menyiapkan preparat cendawan yang
diberi pewarna lactophenol blue terlebih dahulu. Koloni B. theobromae diamati
setiap hari untuk mengetahui kapan dibentuknya piknidia, konidia muda, dan
konidia matang. Konidia muda dipotret dan diukur ciri morfologinya yaitu
panjang, lebar, rasio panjang/lebar (bentuk) dan tebal dinding. Cendawan
R. solani diamati morfologi hifanya yaitu panjang ruas dan ketebalan hifa.
Analisis Data Karakter Morfologi
Data kecepatan pertumbuhan koloni, panjang, lebar dan rasio panjang/lebar
konidia B. theobromae serta data kecepatan pertumbuhan koloni, panjang ruas,
lebar dan sudut percabangan hifa R. solani dianalisis ragam menggunakan
program SAS ver. 9.1.3 dan dilanjutkan dengan uji perbandingan nilai tengah
Duncan's Multiple Range Test (DMRT).
Ekstraksi DNA
Ekstraksi DNA dilakukan dengan metode Abd-Elsalam et al. (2003).
Masing-masing miselium B. theobromae dan R. solani ditumbuhkan dalam 500 µl
Potato Dextrose Broth (PDB) pada suhu ruang selama 72 jam. Miselia dipanen
dengan cara sentrifugasi pada 13.000 rpm selama 5 menit. Pelet dicuci dengan
ditambahkan 300 µl bufer ekstraksi (200 mM Tris-HCl [pH 8,5], 250 mM NaCl,
25 mM EDTA dan 0,5% SDS) dan digerus di dalam mortar dingin selama 5
menit. Sebanyak 150 µl sodium asetat (pH 5,2) ditambahkan dan dilanjutkan
dengan inkubasi pada suhu 20 ºC selama 10 menit. Sentrifugasi pada 13000 rpm
selama 5 menit, kemudian supernatan diambil dan dimasukan ke tabung 1,5 ml
dan ditambahkan isopropanol dengan volume yang sama. Presipitasi DNA dengan
sentrifugasi pada 13000 rpm selama 10 menit, DNA dicuci dengan 500 µl 70%
ethanol dingin dan sentrifugasi beberapa menit. DNA dikering-anginkan selama
30 menit dan dilarutkan dalam bufer TE (10 mM Tris-HCl [pH 8], 1 mM EDTA),
kemudian disimpan dalam suhu -20 ºC untuk selanjutnya digunakan dalam proses
RAPD-PCR.
RAPD-PCR
PCR disiapkan terpisah untuk masing-masing penggunaan primer OPD 06
(5’ ACCTGAACGG 3’) dan OPN 07 (5’ CAGCCCAGAG 3’) dalam total volume
25 µl/reaksi. Bahan yang digunakan dalam teknik RAPD-PCR adalah PureTaqTM
Ready-To-GoTM PCR Beads, Aquabidestilata (ddH2O) steril sebanyak 19,5 µl,
MgCl2 25 mM sebanyak 2,5 µl, primer dengan konsentrasi 10 pMol, dan template
DNA 2 µl. Seluruh bahan PCR dimasukan ke dalam tabung PCR.
PCR dilakukan dalam mesin GeneAmp® PCR System 9700 (Applied
BiosystemTM) dengan program: denaturasi awal 94 ºC (1 menit); kemudian 45
siklus pemanasan denaturasi 94 ºC (2,5 menit), annealing 40 ºC (1 menit), sintesis
DNA 72 ºC (1 menit); reaksi diakhiri dengan ekstensi 72 ºC (7 menit).
Elektroforesis
DNA hasil ekstraksi dan RAPD-PCR dielektroforesis untuk melihat pita
DNA yang dihasilkan menggunakan gel agarose 1,5% dalam bufer TAE 2x (80
mM Tris-acetate dan 2 mM EDTA [pH 8.3]) yang mengandung ethidium bromide
(EtBr), pada tegangan listrik 75 V DC selama 35 menit. Hasil elektroforesis
divisualisasikan pada transluminator ultraviolet. Pita DNA yang terbentuk pada
HASIL DAN PEMBAHASAN
Gejala Penyakit oleh B. theobromae
Penyakit yang disebabkan oleh B. theobromae pada lima tanaman inang
menunjukkan gejala yang beragam dan bagian yang terinfeksi berbeda-beda
(Gambar 1). Gejala pada tanaman jeruk adalah kulit batang dan cabang
mengelupas dan kering, pengelupasan kulit batang dan cabang terus meluas
hingga ke seluruh permukaan sehingga terbentuk luka yang terbuka (Wiratno &
Nurbanah 1997). Pada tingkat serangan yang berat batang tanaman jeruk
membusuk dan kemudian mati (1A). Tanaman kakao yang terserang
B. theobromae mengalami penyakit pod rot. Pada buah yang terserang terdapat
bercak cokelat dan menjadi keriput (1B). Menurut CABI (2007) bercak pada buah
kakao yang disebabkan B. theobromae pada awalnya merupakan klorosis yang
kemudian menjadi bercak cokelat yang meluas.
Gambar 1 Gejala penyakit yang disebabkan oleh cendawan B. theobromae pada lima tanaman inang. Jeruk (A); kakao (B); karet (C); manggis (D); pisang (E). Sumber foto: (A,C,D,E) Suryo Wiyono; (B) TNAU 2008
D
E
Permukaan batang tanaman karet muda yang terserang B. theobromae
menjadi berwarna cokelat dan teksturnya menjadi kasar (1C). Menurut Pha et al.
(2009) pada kelembaban yang cukup miselia berwarna putih akan muncul pada
permukaan batang yang retak serta kulit batang dan ranting terkelupas. kulit
batang karet yang terserang menjadi busuk disertai keluarnya lateks atau getah
pada tanaman muda berumur 1-2 tahun. Pada serangan yang berat dapat
menyebabkan retak dan gummosis. Tanaman manggis yang terserang
B. theobromae mengalami mati ujung, ranting menjadi kering dan berwarna
hitam, selain itu kulit terkelupas dan menjadi luka (1D).
Buah pisang yang terserang B. theobromae mengalami busuk buah. Pada
kulit buah terdapat bercak-bercak hitam kecokelatan tidak beraturan yang dapat
meluas (1E). Menurut Raut & Ranade (2004) pada awalnya bercak berwarna
cokelat muda, lama kelamaan bercak berubah warna menjadi cokelat tua hingga
hitam. Bercak meluas dimulai dari bagian ujung atas buah yang kemudian
menyebar hingga ke seluruh bagian buah sehingga daging buah menjadi berwarna
cokelat tua hingga hitam, lembek dan berair. Dalam keadaan yang lembab
miselium dan piknidia berwarna hitam juga dapat terlihat pada jaringan tanaman
yang bergejala.
Karakter Morfologi B. theobromae
Karakter morfologi cendawan B. theobromae berasal dari lima inang
menunjukkan bahwa cendawan-cendawan tersebut memiliki perbedaan dalam
warna koloni (Gambar 2). Koloni pada usia 11 hari (tua) isolat asal jeruk
berwarna abu-abu muda, kakao berwarna cokelat, karet berwarna cokelat tua,
manggis berwarna hitam keabuan, dan pisang berwarna hitam pekat. Perubahan
warna koloni pada karet, kakao, pisang, dan jeruk secara merata di seluruh
miselium pada cawan petri pada awalnya berwarna putih terus bertambah gelap
dengan bertambahnya umur koloni. Sedangkan pada manggis perubahan warna
dimulai dari tengah koloni yang mulai berwarna gelap dan terus menyebar hingga
3 HST
11 HST
Gambar 2 Koloni isolat cendawan B. theobromae dari lima tanaman inang pada media PDA berumur 3 dan 11 hari setelah tanam (HST). Jeruk (A), kakao (B), karet (C), manggis (D), pisang (E).
Koloni mengalami perubahan warna dengan bertambahnya umur koloni.
Pada isolat asal manggis miselium berwarna putih hingga 3 hari setelah tanam
(HST) dan terus bertambah gelap seiring waktu hingga 7 HST. Isolat asal pisang
dan karet berwarna putih hingga 6 HST dan terus bertambah gelap seiring waktu
hingga 8 HST, sedangkan isolat asal kakao dan jeruk miselium masih berwarna
putih hingga 10 HST dan terus bertambah gelap seiring waktu hingga 15 HST.
Gambar 3 Pertumbuhan ukuran koloni cendawan B. theobromae pada media PDA selama 96 jam
0 1 2 3 4 5 6 7 8 9 10
12 24 36 48 60 72 84 96
Diam
eter koloni
(cm
)
Umur biakan (Jam)
Jeruk
Kakao
Karet
Manggis
Pisang
Tabel 2 Pertumbuhan diameter koloni cendawan B. theobromae
B. theobromae Kecepatan pertumbuhan koloni isolat asal (cm)/12 Jam ± SD
Jeruk 1,48 a ± 0,24
Kakao 1,20 ab ± 0,17
Karet 1,45 a ± 0,13
Manggis 0,68 b ± 0,59
Pisang 1,68 a ± 0,15
Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05),
SD = standar deviasi
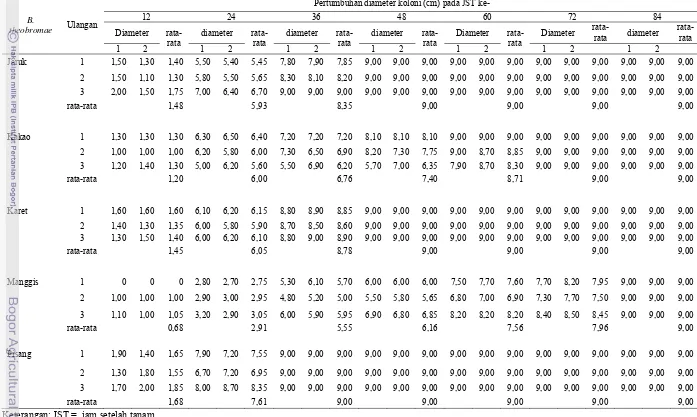
Pertumbuhan koloni B. theobromae pada lima tanaman inang menunjukkan
kecepatan yang berbeda-beda. Koloni isolat asal pisang memiliki kecepatan
tumbuh paling cepat yaitu 1,68 cm per 12 jam, sedangkan isolat asal manggis
menunjukkan kecepatan pertumbuhan paling lambat yaitu 0,68 cm per 12 jam
(Tabel 2). Kecepatan pertumbuhan isolat asal jeruk, karet dan pisang tidak
berbeda nyata, isolat asal kakao tidak berbeda nyata dengan semua isolat lain.
Ukuran maksimum koloni cendawan B. theobromae pada media PDA di
dalam cawan petri dalam penelitian ini adalah 9 cm. Pada umumnya pertumbuhan
miselium mencapai 9 cm pada 36-84 jam setelah tanam (JST). Pada Gambar 3
ditunjukkan bahwa pertumbuhan paling cepat adalah pada isolat B. theobromae
asal pisang yaitu mencapai 9 cm pada 36 JST, miselium isolat asal jeruk dan karet
memiliki kecepatan pertumbuhan yang hampir sama mencapai 9 cm pada 48 HST.
Pada isolat asal kakao pertumbuhan miselium mencapai 9 cm pada 72 JST,
sedangkan pertumbuhan miselium asal manggis adalah yang paling lambat yaitu
mencapai 9 cm pada 84 JST.
Gambar 4 menunjukkan piknidia B. theobromae asal tanaman jeruk, kakao,
karet, manggis dan pisang dengan perbesaran 4 X 10. Piknidia merupakan tubuh
buah yang berbentuk seperti labu yang didalamnya terdapat konidiofor dan
memproduksi konidia (Agrios 2005). Pada umumnya piknidia berwarna cokelat
hingga hitam dan diselimuti oleh miselia. Piknidia terbentuk secara berpencar atau
tidak berkelompok. Pada Gambar 4 A, B, C, dan D piknidia tampak dari atas,
sebagian tubuh piknidia muncul di permukaan, sehingga jika tampak dari atas
putih. Piknidia asal tanaman jeruk, kakao dan manggis berwarna hitam,
sedangkan piknidia asal tanaman karet dan pisang berwarna cokelat tua hingga
cokelat kehitaman.
Gambar 4 Piknidia cendawan B. theobromae dari lima tanaman inang dengan perbesaran 40x. Jeruk (A); kakao (B); karet (C); manggis (D); pisang (E).
Piknidia B. theobromae yang berasal dari tanaman pisang (Gambar 4 E),
tampak dari samping berbentuk jorong atau tabung, berwarna cokelat, dan
piknidia terbentuk diantara miselium cendawan. Tampak samping terlihat bahwa
sebagian tubuh piknidia muncul di atas permukaan koloni cendawan, sedangkan
[image:30.595.100.505.97.804.2]sebagian lainnya berada di dalam miselium.
Gambar 5 Piknidia B. theobromae yang pecah mengeluarkan konidia
A
B
C
Piknidia berwarna hitam yang pecah dan mengeluarkan konidia muda
(Gambar 5). Dengan pewarnaan menggunakan lactophenol blue konidia muda
tampak berwarna biru, konidia keluar dari dalam piknidia yang dipecahkan.
Menurut Masilamani & Muthumar (1996) pada kondisi alami piknidia matang
akan menghasilkan konidia matang yang kemudian konidia matang akan keluar
melalui lubang ostiol pada piknidia dan kemudian menyebar.
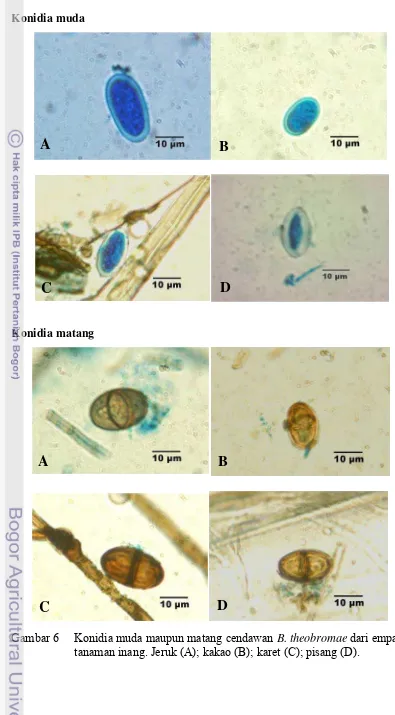
Gambar 6 menunjukkan konidia muda dan konidia matang B. theobromae
yang berasal dari empat tanaman inang dengan perbesaran 10 X 100 dan
pewarnaan dengan lactophenol blue. Konidia muda tidak memiliki sekat (bersel
satu), dinding konidia relatif tebal, dan berwarna hialin sehingga jika diwarnai
dengan lactophenol blue maka konidia akan terlihat berwarna biru. Morfologi
konidia matang memiliki perbedaan dengan konidia muda, yaitu konidia matang
berwarna cokelat tua, memiliki sekat, terdiri dari dua sel dan dinding konidia yang
tidak nampak ketebalannya. Menurut Watanabe (2002) konidia B. theobromae
berpencar secara tunggal, hialin, berbentuk jorong atau silinder, dan pada
umumnya konidia matang terdiri dari dua sel (bersekat satu).
Pada Tabel 3 ditunjukkan bahwa semua isolat B. theobromae asal lima
tanaman inang membentuk piknidia pada media WA+jerami, sedangkan pada
media PDA hanya tiga isolat saja (asal jeruk, karet dan pisang). Konidia muda dan
konidia matang dibentuk oleh isolat asal empat tanaman inang pada media
WA+jerami sedangkan pada media PDA hanya tiga isolat. Pada media PDA,
B. theobromae asal kakao tidak terbentuk piknidia, konidia muda, dan konidia
matang, hal ini karena media PDA termasuk media yang kaya hara seperti glukosa
dan karbohidrat. Menurut Shivas & Beasley (2005), lingkungan yang tidak alami,
seperti media agar-agar yang kaya hara, dapat saja merupakan kondisi yang
kurang cocok untuk sporulasi cendawan patogen tanaman. Sporulasi
B. theobromae dapat ditingkatkan dengan penambahan material asal tanaman
Konidia muda
[image:32.595.102.497.74.789.2]Konidia matang
Gambar 6 Konidia muda maupun matang cendawan B. theobromae dari empat tanaman inang. Jeruk (A); kakao (B); karet (C); pisang (D).
A
B
C
D
A B
Tabel 3 Pembentukan piknidia, konidia muda, dan konidia matang B. theobromae lima tanaman inang pada media WA dan PDA
Tanaman Inang
Waktu (hari) untuk pembentukan
Piknidia Konidia Muda Konidia Matang
WA
+jerami PDA
WA
+jerami PDA
WA
+jerami PDA
Jeruk 13 17 13 17 21 22
Kakao 20 - 20 - 22 -
Karet 13 32 13 39 19 48
Manggis 20 - - - - -
Pisang 17 17 17 18 23 22
Keterangan: WA = water agar, PDA = potato dextrose agar, (-): tidak terbentuk
Pembentukan piknidia, konidia muda, dan konidia matang pada media
WA+jerami cenderung lebih cepat dibanding pada media PDA. B. theobromae
memproduksi piknidia yang menghasilkan konidia pada kondisi lingkungan yang
kurang menguntungkan yaitu kurangnya hara dan media WA+jerami merupakan
media yang miskin hara sehingga piknidia dan konidia terbentuk lebih cepat pada
media tersebut. Piknidia isolat B. theobromae pada media PDA terbentuk antara
17-32 HST. Pada isolat asal jeruk dan pisang piknidia terbentuk paling cepat yaitu
pada 17 HST, sedangkan pembentukan piknidia pada isolat asal karet paling
lambat yaitu terbentuk setelah 32 HST. Pada isolat asal jeruk konidia muda
terbentuk paling cepat diantara isolat lain yaitu pada 17 HST, sedangkan isolat
asal kakao terbentuk paling lambat yaitu setelah 39 HST. Konidia matang pada
media PDA terbentuk antara 22-48 HST. Pada isolat asal jeruk dan pisang konidia
matang terbentuk paling cepat yaitu pada 22 HST, isolat asal karet pembentukan
konidia matang paling lambat yaitu terbentuk setelah 48 HST. Menurut Shah et al.
(2010) waktu yang dibutuhkan B. theobromae untuk menghasilkan piknidia pada
media buatan adalah antara 20-34 hari setelah tanam.
Isolat B. theobromae asal manggis hanya membentuk piknidia pada media
WA+jerami saja, tetapi tidak pada PDA. Konidia muda, dan konidia matang tidak
terbentuk baik pada media WA+jerami maupun media PDA. Sandra (2011)
menyatakan bahwa piknidia dan konidia B. theobromae asal manggis hanya dapat
menunjukkan bahwa dalam pembentukan piknidia dan konidia diperlukan nutrisi
tertentu agar dapat merangsang pembentukannya.
Konidia muda pada isolat B. theobromae asal jeruk berukuran 20-29 µm X
11-14 µm, konidia muda asal kakao berukuran 14-19 µm X 9-11 µm, konidia
muda asal karet berukuran 16-20 µm X 9-12 µm, sedangkan konidia asal pisang
berukuran 16-20 µm X 8-12 µm (Tabel 4). Menurut Watanabe (2002) piknidia
cendawan B. theobromae berukuran 210 µm X 150 µm, dan konidia berukuran
7,5-17,5 µm X 2,2-4,5 µm.
Tabel 4 Ukuran panjang, lebar, dan tebal dinding konidia muda B. theobromae asal empat tanaman inang pada media water agar + jerami
Tanaman Inang
Ukuran konidia muda Panjang (µm) ± SD Lebar (µm) ± SD Rasio panjang/lebar ± SD Tebal dinding (µm) ± SD
Jeruk 22,91 a ± 2,38 12,68 a ± 0,73 1,82 a ± 0,27 1,72 a ± 0,23
Kakao 16,96 b ± 1,64 9,54 c ± 0,52 1,78 a ± 0,19 1,54 ab ± 0,49
Karet 17,44 b ± 1,25 10,56 b ± 1,19 1,67 a ± 0,23 1,86 a ± 0,29
Pisang 17,42 b ± 1,38 10,09 bc ± 1,07 1,75 a ± 0,30 1,32 b ± 0,25
Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05)
SD = standar deviasi
Ukuran panjang, lebar, dan tebal dinding konidia muda B. theobromae
berbeda nyata (Tabel 4). Konidia muda B. theobromae asal jeruk memiliki ukuran
paling besar yaitu rata-rata panjang konidia 22,91 µm dan lebar 12,68 µm,
sedangkan konidia muda isolat asal kakao memiliki ukuran paling kecil, yaitu
rata-rata panjang konidia 16,96 µm dan lebar 9,54 µm. Tebal dinding isolat asal
karet memiliki ukuran yang paling besar yaitu 1,86 µm, sedangkan isolat asal
pisang memiliki tebal dinding yang paling kecil yaitu 1,32 µm.
Rasio panjang/lebar konidia muda B. theobromae asal jeruk, kakao, karet,
dan pisang tidak berbeda nyata (Tabel 5). Konidia muda isolat asal jeruk memiliki
rasio panjang/lebar tertinggi yaitu 1,82 sedangkan konidia isolat asal karet
memiliki rasio panjang/lebar terendah yaitu 1,67. Rasio panjang/lebar konidia
muda dari keempat isolat >1 sehingga konidia berbentuk jorong. Bentuk konidia
Panjang dan lebar konidia matang isolat B. theobromae asal empat tanaman
inang memiliki ukuran panjang dan lebar konidia matang yang berbeda nyata
(Tabel 5). Konidia matang pada isolat B. theobromae asal jeruk berukuran 21-28
µm X 11-14 µm, konidia matang asal kakao berukuran 13-19 µm X 9-12 µm,
konidia matang asal karet berukuran 16-27 µm X 9-13 µm, sedangkan konidia
matang asal pisang berukuran 17-22 µm X 10-13 µm. Berdasarkan pengukuran,
ukuran konidia matang cenderung lebih besar dibandingkan konidia muda, namun
tebal dinding konidia matang tidak dapat diukur karena tebal dinding terlalu kecil.
Tabel 5 Ukuran panjang dan lebar konidia matang cendawa B. theobromae asal empat tanaman inang pada media water agar + jerami
Tanaman Inang
Ukuran konidia matang Panjang (µm)
± SD Lebar (µm) ± SD
Rasio panjang/lebar ± SD
Jeruk 23,63 a ± 2,26 12,83 a ± 1,10 1,86 a ± 0,31
Kakao 15,40 c ± 1,96 10,67 b ± 1,00 1,44 b ± 0,12
Karet 21,08 b ± 3,19 11,39 b ± 1,45 1,89 a ± 0,46
Pisang 19,32 b ± 1,98 11,59 b ± 1,01 1,68 ab ± 0,21
Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05)
SD = standar deviasi
Panjang dan lebar konidia matang isolat B. theobromae asal empat tanaman
inang memiliki ukuran panjang dan lebar konidia matang yang berbeda nyata
(Tabel 5). Konidia matang B. theobromae asal jeruk memiliki ukuran paling besar
yaitu rata-rata panjang konidia 23,63 µm dan lebar 12,83 µm, sedangkan konidia
matang isolat asal kakao memiliki ukuran paling kecil, yaitu rata-rata panjang
konidia 15,40 µm dan lebar 10,67 µm. Perbedaan ukuran konidia matang dan
muda B. theobromae menunjukkan bahwa ada keragaman ukuran konidia antar
isolat yang berasal dari tanaman inang yang berbeda.
Rasio panjang/lebar konidia muda B. theobromae asal jeruk, kakao, karet,
dan pisang berbeda nyata (Tabel 4). Rasio panjang/lebar konidia matang dari
keempat isolat >1 sehingga konidia berbentuk jorong (Tabel 5). Bentuk konidia
akan semakin bulat jika rasio panjang/lebar mendekati 1. Konidia muda isolat asal
karet memiliki rasio panjang/lebar tertinggi yaitu 1,89 sedangkan konidia isolat
konidia muda lebih rendah dibanding konidia matang kecuali pada isolat asal
kakao, sehingga bentuk konidia matang lebih jorong dibanding konidia muda.
Karakter Molekuler Cendawan B. theobromae
Analisis molekuler terhadap DNA cendawan B. theobromae dilakukan
dengan teknik RAPD-PCR menggunakan primer OPD 06 (Gambar 7, Tabel 6)
dan OPN 07 (Gambar 8, Tabel 7). Gambar 7 menunjukkan pola RAPD-PCR
menggunakan primer OPD 06 dan Gambar 8 menggunakan primer OPN 07 dan
marker GeneRulerTM DNA Ladder. Gambar tersebut menunjukkan bahwa primer
OPD 06 dan OPN 07 dapat mengamplifikasi DNA cendawan B. theobromae asal
berbagai tanaman inang di beberapa lokasi pada genom cendawan tersebut dengan
ukuran amplikon yang berbeda-beda.
Gambar 7 Profil DNA lima isolat cendawan B. theobromae yang diamplifikasi dengan RAPD-PCR menggunakan primer OPD 06
Tabel 6 Ukuran fragmen DNA cendawan B. theobromae asal berbagai tanaman inang dengan RAPD menggunakan primer OPD 06
Keterangan: bp= base pair (pasangan basa)
Pita DNA ke- Ukuran (bp) pita DNA isolat B. theobromae asal
Jeruk Kakao Karet Manggis Pisang
1 1000 850 <500 <500 1000
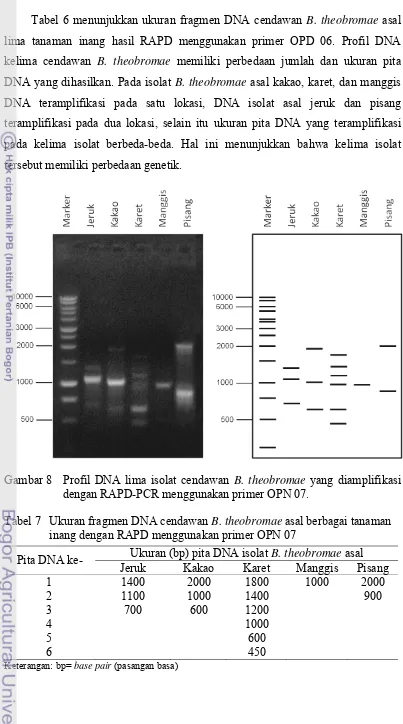
Tabel 6 menunjukkan ukuran fragmen DNA cendawan B. theobromae asal
lima tanaman inang hasil RAPD menggunakan primer OPD 06. Profil DNA
kelima cendawan B. theobromae memiliki perbedaan jumlah dan ukuran pita
DNA yang dihasilkan. Pada isolat B. theobromae asal kakao, karet, dan manggis
DNA teramplifikasi pada satu lokasi, DNA isolat asal jeruk dan pisang
teramplifikasi pada dua lokasi, selain itu ukuran pita DNA yang teramplifikasi
pada kelima isolat berbeda-beda. Hal ini menunjukkan bahwa kelima isolat
tersebut memiliki perbedaan genetik.
Gambar 8 Profil DNA lima isolat cendawan B. theobromae yang diamplifikasi dengan RAPD-PCR menggunakan primer OPN 07.
Tabel 7 Ukuran fragmen DNA cendawan B. theobromae asal berbagai tanaman inang dengan RAPD menggunakan primer OPN 07
Keterangan: bp= base pair (pasangan basa)
Pita DNA ke- Ukuran (bp) pita DNA isolat B. theobromae asal
Jeruk Kakao Karet Manggis Pisang
1 1400 2000 1800 1000 2000
2 1100 1000 1400 900
3 700 600 1200
4 1000
5 600
Tabel 7 menunjukkan ukuran fragmen DNA isolat B. theobromae asal lima
tanaman inang hasil RAPD menggunakan primer OPN 07. Profil DNA kelima
isolat B. theobromae menunjukkan perbedaan jumlah dan ukuran pita DNA yang
lebih beragam dibandingkan dengan pola RAPD dengan primer OPD 06. Pada
isolat B. theobromae asal manggis DNA teramplifikasi pada satu lokasi, DNA
isolat asal jeruk dan kakao teramplifikasi pada tiga lokasi, sedangkan DNA isolat
asal karet teramplifikasi pada enam lokasi. Selain itu ukuran pita DNA yang
teramplifikasi pada kelima isolat berbeda-beda (Gambar 8), hal ini menunjukkan
bahwa keempat isolat tersebut memiliki perbedaan genetik yang cukup nyata.
RAPD menggunakan primer tunggal pendek dengan urutan nukleotida acak,
dilakukan dengan suhu annealing rendah dan menghasilkan beberapa produk PCR
yang menghasilkan pola pita setelah dilakukan pemisahan oleh elektroforesis
(Edel 1998).
Menurut Edel (1998), analisis DNA menggunakan RAPD umumnya
dilakukan dengan primer non-spesifik sehingga kondisi reaksi dan thermocycle
RAPD lebih sensitif dibandingkan tes PCR konvensional. Dengan demikian
konsentrasi dari semua campuran bahan dalam reaksi harus akurat. Selain itu
kualitas dari template DNA dan Taq polymerase merupakan faktor yang juga
dapat mempengaruhi hasil RAPD.
Gejala Penyakit oleh Cendawan R. solani
Penyakit yang disebabkan oleh R. solani pada tiga tanaman inang
menunjukan gejala yang beragam (Gambar 9). Gejala yang disebabkan oleh
R. solani pada tanaman jagung (Gambar 9A) yaitu terdapat bercak tidak teratur
berwarna putih kotor atau cokelat muda dan pada bagian pinggir bercak berwarna
cokelat tua. Bercak terus meluas dari mulai bagian pelepah hingga ke seluruh
jaringan tanaman. Pada bagian tanaman yang terserang cukup parah, seluruh
bagian tanaman menjadi berwarna cokelat dan kering, kemudian tanaman mati.
Gambar 9 Gejala penyakit yang disebabkan oleh cendawan R. solani pada tiga tanaman inang. Jagung (A); Padi (B); Sorghum (C).
Pelepah tanaman padi yang terserang cendawan R. solani (9B) terdapat
bercak tidak beraturan berwarna cokelat hingga hitam dengan pusat bercak
berwarna putih, abu-abu atau cokelat muda, biasanya cendawan tersebut
menyerang pada bagian bawah pelepah kemudian akan terus menyebar ke bagian
atas. Pelepah bagian atas yang terserang menjadi kering, sedangkan pelepah
bagian bawah menjadi lembek dan mudah hancur atau patah karena pada bagian
bawah pelepah memiliki kelembaban yang lebih tinggi.
Tanaman Sorghum (9C) yang terserang R. solani menunjukkan gejala yang
khas, yaitu terdapat bercak meluas yang bersudut pada bagian bawah bercak
dengan pusat bercak berwarna putih, putih kotor atau cokelat muda. Pada bagian
pinggir bercak berwarna cokelat tua. Bagian yang terserang parah akan menjadi
kering dan kemudian tanaman mati. Pada bagian tanaman yang mati terdapat
sklerotia berwarna cokelat.
Karakter Morfologi R. solani
Hasil pengamatan karakter morfologi terhadap cendawan R. solani yang
berasal dari lima inang yaitu: jagung, nanas, padi, sorghum, dan ubi jalar (Gambar
10), menunjukkan bahwa koloni kelima isolat R. solani memiliki warna yang
berbeda. Pada isolat asal jagung miselium berwarna kuning cerah, isolat asal
nanas berwarna cokelat, isolat asal padi berwarna cokelat kemerahan, isolat asal
sorghum berwarna cokelat muda, sedangkan isolat asal ubi jalar miselium
berwarna hitam pada bagian tengah koloni dan berwarna cokelat tua pada
pinggiran koloni. Pada isolat asal jagung, nanas dan sorghum perubahan warna
merata pada seluruh miselium seiring waktu, sedangkan pada isolat asal padi dan
ubi jalar perubahan warna dimulai dari tengah koloni dan terus bertambah gelap
hingga bagian pinggir koloni.
4 HST
18 HST
Gambar 10 Koloni isolat cendawan R. solani dari lima tanaman inang pada umur 4 dan 18 HST pada media PDA. jagung (A); nanas (B); padi (C); sorghum (D); ubi jalar (E).
Koloni mengalami perubahan warna dengan bertambahnya umur koloni.
Pada isolat asal jagung miselium berwarna putih hingga 2 HST kemudian berubah
menjadi berwarna kuning hingga 5 HST dan menjadi kuning cerah hingga 18
HST. Sedangkan pada isolat nanas, padi dan sorghum miselium berwarna putih
hingga 3 HST kemudian menjadi berwarna kuning muda hingga 4 HST dan terus
bertambah gelap hingga 15 HST. Isolat asal ubi menunjukkan perubahan warna
paling cepat diantara isolat lain yaitu berwarna putih hingga 1 HST kemudian
terus bertambah gelap hingga 5 HST.
Kecepatan pertumbuhan koloni R. solani pada lima tanaman inang berbeda
nyata (Tabel 8). Koloni isolat asal jagung memiliki kecepatan tumbuh paling
cepat yaitu rata-rata pertumbuhan 4,20 cm per 12 jam, sedangkan isolat asal ubi
jalar menunjukkan kecepatan pertumbuhan paling lambat yaitu rata-rata 1,60 cm
per 12 jam. Pertumbuhan maksimum koloni R. solani pada media PDA di dalam
cawan petri adalah 9 cm. Umumnya pertumbuhan koloni cendawan R. solani
mencapai maksimum pada 48-120 jam setelah tanam (JST).
Gambar 11 Grafik pertumbuhan koloni cendawan R. solani pada media PDA.
Tabel 8 Pertumbuhan diameter koloni cendawan R. solani
Tanaman Inang Kecepatan pertumbuhan koloni isolat asal (cm)/12 jam ± SD
Jagung 4,20 a ± 0.36
Nanas 2,37 b ± 0.58
Padi 1,87 bc ± 0.15
Sorghum 1,80 bc ± 0.17
Ubi Jalar 1,60 c ± 0.17
Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05)
SD = standar deviasi
Pada Gambar 11 ditunjukkan bahwa pertumbuhan miselium paling cepat
adalah isolat asal jagung, yaitu pada 48 JST dan yang paling lambat adalah isolat
asal ubi jalar yaitu pada 120 JST. Terdapat perbedaan kecepatan pertumbuhan
pada kelima isolat tersebut.
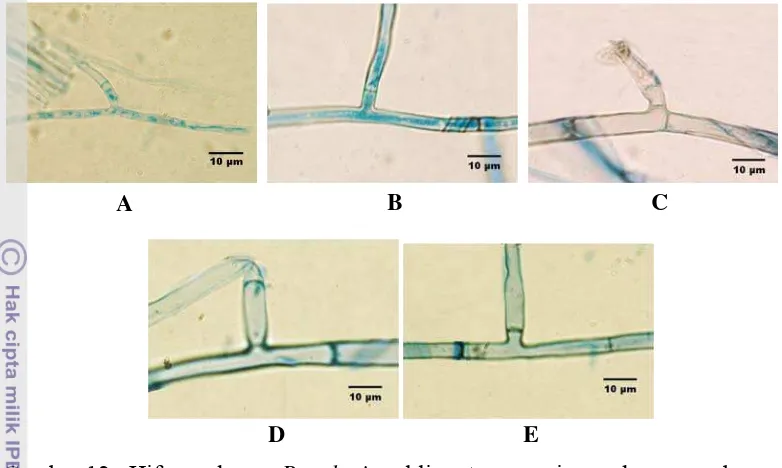
Gambar 12 merupakan hifa R. solani yang berasal dari lima tanaman
inang, dengan pewarnaan lactophenol blue. Hifa R. solani memiliki percabangan
yang tegak lurus, berwarna hialin dan memiliki sekat. Menurut Schumann &
D’Arcy (2006) R. solani dapat diidentifikasi dari karakter hifa yang khas, yaitu
sudut percabangan yang tegak lurus yang membedakan dengan cendawan lainnya.
0 1 2 3 4 5 6 7 8 9 10
12 24 36 48 60 72 84 96 108 120
Diam
eter Koloni
(cm
)
Umur Biakan (Jam)
[image:42.595.108.503.81.581.2]
Gambar 12 Hifa cendawan R. solani asal lima tanaman inang dengan perbesaran 10 X 100 dan pewarnaan lactophenol blue. Jagung (A); nanas (B); padi (C); sorghum (D); ubi jalar (E).
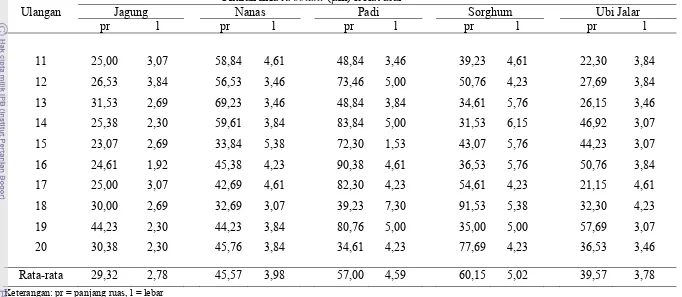
Tabel 9 Ukuran panjang ruas dan lebar hifa cendawan R. solani pada lima tanaman inang
Tanaman Inang Ukuran hifa (µm)
Panjang ruas ± SD Lebar ± SD Jagung 29,32 c ± 7,36 2,78 c ± 0,46
Nanas 45,57 b ± 13,21 3,98 b ± 0,52
Padi 56,99 a ± 18,54 4,59 a ± 1,13
Sorghum 60,15 a ± 23,16 5,01 a ± 0,83
Ubi Jalar 39,57 b ± 11,03 3,78 b ± 0,67
Keterangan: Huruf berbeda menunjukkan perbedaan nyata dengan uji selang ganda Duncan (α = 0,05)
SD = standar deviasi
Panjang ruas dan lebar hifa R. solani asal padi dengan asal sorghum tidak
berbeda nyata dan isolat asal nanas dengan asal ubi jalar tidak berbeda nyata,
sedangkan isolat asal jagung berbeda nyata terhadap keempat isolat lainnya.
R. solani asal sorghum memiliki panjang ruas dan lebar yang paling besar diantara
isolat lainnya yaitu panjang ruas 32-104 µm dan lebar 4-7 µm, sedangkan jagung
memiliki panjang ruas dan lebar yang paling kecil diantara isolat lainnya yaitu
panjang ruas 18-48 µm dan lebar 2-4 µm (Tabel 9).
B C
[image:42.595.112.503.84.318.2]
Hifa R. solani pada lima tanaman inang yaitu, jagung, nanas, padi, sorghum
dan ubi jalar memiliki rata-rata sudut percabangan yang berbeda-beda namun
tidak berbeda nyata. Sudut percabangan cendawan tersebut pada kelima tanaman
inang hampir tegak lurus mendekati 90º. Hifa isolat asal ubi jalar memiliki sudut
tumpul yang paling besar yaitu dengan rata-rata 108,95º, kemudian isolat asal
sorghum dengan sudut tumpul 106,1º, isolat asal padi 105,75º, isolat asal jagung
105,3º, sedangkan isolat asal nanas cenderung lebih tegak lurus dibandingkan
isolat lainnya karena memiliki sudut tumpul yang paling kecil yaitu 103º.
Gambar 13 Sklerotia cendawan R. solani. Sklerotia muda (A); sklerotia tua (B).
Sklerotia merupakan sekumpulan hifa yang mengalami pemadatan,
berwarna gelap dan mampu betahan dalam kondisi lingkungan yang tidak
menguntungkan (Agrios 2005). Sklerotia merupakan struktur bertahan pada
cendawan R. solani (Gambar 13), terbentuk ketika cendawan dalam kondisi
kekurangan nutrisi namun kelembaban cukup. Sklerotia R. solani memiliki
permukaan kasar dengan bentuk yang tidak beraturan serta memiliki struktur yang
keras. Pada hari pertama terbentuk sklerotia berwarna putih yang merupakan
sklerotia muda, kemudian hari kedua hingga hari keempat sklerotia akan berubah
menjadi warna cokelat.
Karakter Molekuler Cendawan R. solani
Analisis molekuler terhadap DNA R. solani dilakukan dengan teknik
RAPD-PCR menggunakan primer OPD 06 dan OPN 07. Gambar 14 menunjukkan
pola RAPD-PCR dengan primer OPD 06, sedangkan Gambar 15 merupakan pola
RAPD-PCR menggunakan primer OPN 07 dan marker GeneRulerTM DNA
B
Ladder. Dari kedua gambar tersebut dapat dilihat bahwa kedua primer dapat
mengamplifikasi DNA cendawan R. solani dari lima tanaman inang di berbagai
lokasi pada genom cendawan tersebut.
Gambar 14 Profil DNA empat isolat cendawan R. solani yang diamplifikasi dengan RAPD-PCR menggunakan primer OPD 06.
Tabel 10 Ukuran fragmen DNA cendawan R. solani asal berbagai tanaman inang dengan RAPD menggunakan primer OPD 06
Keterangan: bp= base pair (pasangan basa)
Tabel 10 menunjukkan ukuran fragmen DNA cendawan R. solani asal
berbagai tanaman inang hasil RAPD dengan primer OPD 06. Profil DNA keempat
cendawan R. solani menunjukkan perbedaan jumlah dan ukuran pita DNA yang
dihasilkan. Pada isolat R. solani asal jagung DNA teramplifikasi pada satu lokasi, Pita DNA ke- Ukuran (bp) pita DNA isolat R. solani asal
Jagung Nanas Padi Sorghum Ubi Jalar
1 750 1500 1400 1100 1400
2 1100 700 900 800
3 900 600 500
isolat asal sorghum teramplifikasi pada dua lokasi, isolat asal nanas dan ubi jalar
teramplifikasi pada tiga lokasi, sedangkan isolat asal padi teramplifikasi pada
empat lokasi. Ukuran pita DNA dan jumlah DNA yang teramplifikasi pada kelima
isolat berbeda-beda, hal ini menunjukkan bahwa kelima isolat tersebut
menunjukkan perbedaan genetik yang cukup nyata.
Gambar 15 Profil DNA empat isolat cendawan R. solani yang diamplifikasi dengan RAPD-PCR menggunakan primer OPN 07.
Tabel 11 Ukuran fragmen DNA cendawan R. solani asal berbagai tanaman inangdengan RAPD menggunakan primer OPN 07
Keterangan: bp= base pair (pasangan basa)
Pita DNA ke- Ukuran (bp) pita DNA isolat R. solani asal
Jagung Nanas Padi Sorghum Ubi Jalar
1 1100 500 400 400 600
2 750 600 500 900
3 700 650 1000
4 900 1000 1300
5 1300 1300 1400
6 1400 1400 1700
Tabel 11 menunjukkan ukuran fragmen DNA cendawan R. solani asal
berbagai tanaman inang hasil RAPD menggunakan primer OPN 07. Profil DNA
keempat cendawan R. solani menunjukkan perbedaan jumlah dan ukuran pita
DNA yang dihasilkan dan lebih beragam dibandingkan pola RAPD dengan primer
OPD 06. Pada isolat R. solani asal nanas DNA teramplifikasi pada dua lokasi,
DNA isolat asal padi dan sorghum teramplifikasi pada enam lokasi, sedangkan
DNA isolat asal ubi jalar teramplifikasi pada tujuh lokasi. Selain itu ukuran pita
DNA yang teramplifikasi pada keempat isolat juga berbeda-beda, hal ini
menunjukkan bahwa keempat isolat tersebut menunjukkan perbedaan genetik
KESIMPULAN DAN SARAN
Kesimpulan
Karakter morfologi dan molekuler isolat cendawan Botryodiplodia
theobromae yang berasal dari tanaman inang yang berbeda sangat beragam. Isolat
cendawan B. theobromae yang berasal dari tanaman jeruk, kakao, karet, manggis
dan pisang menunjukkan keragaman karakter dari segi warna dan kecepatan
tumbuh koloni, kemampuan pembentukan piknidia, serta ukuran dan bentuk
konidia muda dan konidia matang pada media PDA dan WA+jerami. Isolat
B. theobromae asal jeruk, karet, dan pisang mampu membentuk konidia