REKAYASA BIOPOLIMER DARI LIMBAH
PERTANIAN BERBASIS SELULOSA DAN
APLIKASINYA SEBAGAI MATERIAL SEPARATOR
HENNY PURWANINGSIH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI DISERTASI DAN
SUMBER INFORMASI
Dengan ini saya menyatakan bahwa disertasi Rekayasa Biopolimer dari Limbah Pertanian berbasis Selulosa dan Aplikasinya sebagai Material Separator adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir disertasi ini.
Bogor, Januari 2012
HENNY PURWANINGSIH. Biopolymer Engineering of Cellulose-Based Agricultural Waste Materials and Its Application for Separator. Under direction of TUN TEDJA IRAWADI, ZAINAL ALIM MAS’UD, and ANAS MIFTAH FAUZI.
Natural biopolymers such as polysaccharides e.g. cellulose, is known to be used as polymer backbone in order to produce a separator material. Agricultural wastes such as sago waste, sugarcane bagasse, and rice straw are potential raw materials because they contain cellulose in large quantities. In addition to cheap and untapped, potential biopolymers of the three materials are very abundant in Indonesia. Use of local materials will be very economical and sustainable, while also address the environmental problems caused by poor waste management. To improve the properties owned by a natural polysaccharide of these three raw materials it needs to be engineered by graft copolymerization and cross-linking. The objective of this study is to obtain a molecular separator material through biopolymer engineering-based agricultural waste cellulose by graft copolymerization and cross-linking technique. This study consists of several stages. The first stage is the analysis of chemical components of raw materials. The second stage is the isolation and characterization of cellulosic isolate. The third stage is the determination of biopolymer engineering through graft copolymerization and cross-linking technique. The fourth stage is to evaluate the performance of the product as a molecular separator material. The next stage is to analyze the financial and value-added products. The results showed that the separator material from sugarcane bagasse is potential to be developed. This material is able to separate the active components in the extract of java turmeric with good resolution.
HENNY PURWANINGSIH. Rekayasa Biopolimer dari Limbah Pertanian Berbasis Selulosa dan Aplikasinya Sebagai Material Separator. Dibimbing oleh TUN TEDJA IRAWADI, ZAINAL ALIM MAS’UD, dan ANAS MIFTAH FAUZI.
Tahap isolasi, pemisahan, dan pemurnian dalam rangka menghasilkan senyawa aktif murni merupakan langkah utama yang dibutuhkan dan terus dikembangkan sampai saat ini. Kromatografi merupakan salah satu teknik pemisahan yang banyak digunakan dalam teknologi pemisahan. Saat ini, teknik kromatografi yang dibutuhkan adalah yang memiliki tingkat selektivitas yang tinggi dan efisien dalam memisahkan campuran senyawa yang kompleks.
Biopolimer berupa polisakarida alami seperti selulosa diketahui dapat dijadikan polimer backbone untuk menghasilkan material separator. Limbah pertanian berupa ela sagu, bagas tebu, dan jerami padi merupakan bahan baku yang potensial karena mengandung selulosa dalam jumlah banyak. Selain murah dan belum termanfaatkan, potensi biopolimer dari ketiga bahan ini sangat berlimpah di Indonesia. Pemanfaatan material lokal ini akan sangat ekonomis dan berkesinambungan, selain itu juga mengatasi masalah lingkungan akibat pengelolaan limbah yang belum tepat. Untuk tujuan tertentu, polisakarida alami seperti selulosa tidak dapat langsung digunakan. Oleh karena itu, perlu dilakukan rekayasa dengan cara kopolimerisasi cangkok dan taut silang dengan tujuan memperbaiki sifat yang dimiliki oleh polisakarida alami ini sesuai peruntukkannya.
Penelitian ini bertujuan mendapatkan material separator molekul melalui rekayasa biopolimer limbah pertanian berbasis selulosa dengan teknik kopolimerisasi cangkok dan taut silang. Penelitian terdiri atas beberapa tahap. Tahap pertama adalah analisis koomponen kimia bahan baku. Tahap kedua adalah isolasi dan pencirian selulosa dari bahan baku. Tahap ketiga adalah penentuan kondisi rekayasa biopolimer melalui teknik kopolimerisasi cangkok dan taut silang. Tahap keempat adalah melakukan uji kinerja terhadap produk sebagai material separator molekul. Tahap berikutnya adalah melakukan analisis finansial dan nilai tambah produk pada prototipe material separator yang potensial.
Dari tahap pertama diperoleh karakteristik awal bahan baku untuk dijadikan acuan pada tahap isolasi. Kandungan selulosa alfa dari ketiga bahan baku di atas 20%. Ela sagu memiliki kandungan pati yang cukup tinggi (47,03%). Bagas tebu dan jerami padi memiliki kandungan lignin yang tinggi (22,28 dan 32,07%).
isolat yang dihasilkan adalah selulosa.
Dari tahap ketiga diperoleh kondisi rekayasa biopolimer melalui kopolimerisasi cangkok dan taut silang akrilamida (Am) yang dilakukan dalam suasana hampa udara menggunakan aliran gas N2 dengan amonium persulfat (APS) sebagai inisiator dan N,N’-metilena-bis-akrilamida (MBAm). Pencirian dilakukan dengan teknik SEM untuk melihat morfologi permukaan, teknik spektroskopi FTIR untuk melihat gugus fungsi, teknik difraksi sinar X untuk menganalisis kristalinitas, dan teknik DTA untuk menganalisis ketahanan produk terhadap suhu. Kajian dilakukan terhadap kemampuan produk hasil rekayasa dalam menjerap air (swelling factor), kekuatan mekanik, dan ketahanan terhadap pelarut. Spektrum FTIR dan mikrograf SEM menunjukkan bahwa kopolimerisasi cangkok dan taut silang telah terjadi pada permukaan rantai selulosa. Produk hasil rekayasa memiliki kestabilan termal yang lebih baik. Indeks kristalinitas meningkat dengan meningkatnya jumlah penaut silang, sedangkan swelling factornya menurun.
Material separator berbasis bagas tebu dievaluasi kinerjanya melalui teknik kromatografi kolom. Puncak dengan luas terbesar pada kromatogram diidentifikasi sebagai senyawa xantorizol dan bisdemetoksikurkumin. Resolusi pemisahan diperoleh sebesar 6,44, lebih tinggi dari standar Center for Drug Evaluation and Research U.S Food and Drug Administration (CDER-FDA), yaitu >2. Efisiensi kolom yang dihasilkan dalam penelitian ini memiliki pelat teoritis <2.000 dengan tailing factor sebesar 2,3. Standar pelat teoritis yang ditetapkan CDER-FDA adalah >2.000 dan tailing factor <2. Jadi, material separator berbasis bagas tebu memiliki resolusi pemisahan yang baik untuk memisahkan senyawa aktif xantorizol dan kurkuminoid, namun efisiensi kolom masih perlu ditingkatkan. Informasi lain yang dihasilkan adalah selain dapat memisahkan xantorizol dan kurkuminoid, material separator ini juga dapat digunakan untuk memisahkan senyawaan kurkuminoid (kurkumin, demetoksikurkumin, dan bisdemetoksikurkumin).
Material separator berbasis bagas tebu berpotensi dikembangkan untuk mendukung teknologi separasi di Indonesia. Kelayakan finansial dan analisis nilai tambah dilakukan untuk mengevaluasi potensi material separator berbasis bagas tebu secara ekonomi. Hasil menunjukkan bahwa secara finansial industri material separator berbasis bagas tebu ini menguntungkan karena memiliki nilai benefit cost ratio (rasio B/C) lebih dari satu, yaitu 1,22. Jumlah produksi per tahun adalah 30.000 kg material separator dengan penerimaan aktual sebesar Rp 30.000.000.000,00 jauh lebih besar daripada jumlah produksi saat titik impas (BEP), yaitu 2.682 kg dan penerimaan saat BEP (Rp 2.682.448.009,00). Nilai tambah yang diperoleh dari industri material separator berbasis bagas tebu adalah Rp 469.709,44 per kg bagas tebu. Kenaikan pada upah tenaga kerja, harga bahan baku dan bahan kimia, serta sumbangan input lainnya sampai dengan 10% dan harga penjualan yang tetap masih dapat menguntungkan perusahaan.
© Hak Cipta milik IPB, tahun 2012
Hak Cipta dilindungi Undang-Undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa
mencantumkan atau menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan
karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah
b. pengutipan tersebut tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
PERTANIAN BERBASIS SELULOSA DAN
APLIKASINYA SEBAGAI MATERIAL SEPARATOR
HENNY PURWANINGSIH
Disertasi
sebagai salah satu syarat untuk memperoleh gelar Doktor pada
Program Studi Teknologi Industri Pertanian
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Ujian Tertutup pada
Hari : Senin
Tanggal : 30 Januari 2012
Pukul : 09.00-12.00
Tempat : Ruang Sidang Dekanat Fateta Penguji : 1. Prof. Dr. Purwantiningsih, MS
2. Prof. Dr. Ir. Erliza Noor, M.Sc
Ujian Terbuka pada
Hari : Selasa
Tanggal : 31 Januari 2012
Pukul : 13.00-16.00
Tempat : Ruang Sidang Konferensi Faperta Penguji : 1. Prof (APU). Dr. Ir. Gustan Pari, MS
Disetujui
Komisi Pembimbing
Prof. Dr. Ir Tun Tedja Irawadi, MS Ketua
Dr. Zainal Alim Mas’ud, DEA Anggota
Prof. Dr. Ir. Anas Miftah Fauzi, M.Eng Anggota
Diketahui
Ketua Program Studi
Teknologi Industri Pertanian
Dekan Sekolah Pascasarjana IPB
Dr. Ir. Machfud, MS Dr. Ir. Dahrul Syah, MSc.Agr
Puji dan syukur penulis panjatkan kepada Allah SWT atas segala karunia-Nya sehingga karya ilmiah ini bisa diselesaikan. Judul yang dipilih dalam penelitian yang dilaksanakan sejak Januari 2010 sampai Oktober 2011 ini ialah Rekayasa Biopolimer dari Limbah Pertanian berbasis Selulosa dan Aplikasinya sebagai Material Separator.
Dengan selasainya disertasi ini, maka dengan hati yang tulus dan ikhlas perkenankan penulis mengucapkan terima kasih yang tak terhingga dan penghargaan yang setinggi-tingginya kepada yang terhormat Prof. Dr. Ir. Tun Tedja Irawadi, MS sebagai ketua komisi pembimbing, Dr. Zainal Alim Mas’ud, DEA, dan Prof. Dr. Ir. Anas Miftah Fauzi, M.Eng sebagai anggota komisi pembimbing yang telah banyak memberikan saran dalam penelitian ini. Ucapan terima kasih juga disampaikan kepada Kepala Laboratorium Kimia Terpadu IPB Dr. Zainal Alim Mas’ud DEA dan Kepala Divisi Penelitian Laboratorium Kimia Terpadu IPB Prof (Emeritus). Dr. Ir. M. Anwar Nur, M.Sc atas sarana dan fasilitas yang diberikan kepada penulis selama melakukan penelitian. Penghargaan dan ucapan terima kasih untuk pengelola Program Pascasarjana IPB, Dekan dan Sekretaris Sekolah Pascasarjana, Dekan dan Wakil Dekan FATETA, Ketua dan Sekretaris Program Studi TIP atas dorongan semangat, kesempatan, kemudahan dan fasilitas yang diberikan selama penulis melaksanakan studi.
Begitu pula kepada seluruh staf Laboratorium Kimia Terpadu IPB (khususnya Indah, Baim, Wida, Sarah, Mas Khotib, Riki) atas kerja samanya yang baik dan bantuan kepada penulis selama melakukan penelitian dan penulisan disertasi ini. Ucapan terima kasih juga disampaikan kepada Dekan FMIPA IPB dan Ketua Departemen Kimia FMIPA IPB, atas ijin dan kesempatan yang diberikan kepada penulis untuk melanjutkan pendidikan S3.
Tidak ketinggalan terima kasih yang tak terhingga kepada rekan-rekan staf pengajar Departemen Kimia FMIPA IPB dan teman-teman TIP angkatan 2005 (Bu Cut, Pak Novizar, Pak Bagus, Pak Luluk, Pak Yuli, Pak Fahmi, dan Bu Rizki) atas dukungannya, yang selalu mendoakan, memberikan motivasi, dan banyak membantu penulis dalam menjalani pendidikan dan menyelesaikan studi S3 ini.
Secara khusus, penulis menyampaikan terima kasih dan kasih sayang yang tak terhingga kepada keluarga tercinta, suami Ir. Nasruddin Suyuti, anak Rahma Fitriyanti Suyuti, Papih H. Djaidiono, Mamah Hj. Sri Maryati, dan adik-adikku (Tri Tjahyono, M.Si dan keluarga serta Dwi Prasetiyo, S.Kom dan keluarga), bulek dan paklek beserta keluarga yang penuh pengertian, kesabaran, pengorbanan, dan kesetiaan senantiasa mendoakan serta memberikan semangat dan dorongan kepada penulis selama mengikuti pendidikan S3 dan menyelesaikan disertasi ini.
Januari 2012
pertama dari tiga bersaudara dari pasangan H. Djaidiono dan Hj. Sri Maryati. Pada tahun 2003, penulis menikah dengan Ir. Nasruddin Suyuti dan dikaruniai seorang puteri bernama Rahma Fitriyanti Suyuti.
Pendidikan sarjana ditempuh di Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor (IPB) dan lulus pada tahun 1998. Pada tahun 1999, penulis melanjutkan studi pada Program Magister Kimia Universitas Indonesia dan lulus pada tahun 2002. Selanjutnya, penulis memperoleh kesempatan untuk melanjutkan program Doktor di Program Studi Teknologi Industri Pertanian, Fakultas Teknologi Pertanian IPB pada tahun 2005 dengan bantuan dana dari BPPS Departemen Pendidikan Nasional.
Penulis bekerja sebagai staf pengajar honorer di Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor sejak tahun 1999 dan diangkat sebagai pegawai negeri sipil di tempat yang sama pada tahun 2005. Sejak tahun 2002 sampai sekarang, penulis berkesempatan untuk bergabung di Laboratorium Kimia Terpadu IPB pada Divisi Layanan Jasa Analisis dan bertanggung jawab terhadap bagian mutu. Pada tahun 2005 sampai sekarang, penulis dipercaya menjadi Kepala Lembaga Sertifikasi Produk Laboratorium Kimia Terpadu IPB. Pada tahun 2009-2010, melalui kerja sama antara IPB dan Pemda Halmahera Barat, penulis berkesempatan menjadi dosen tamu di Sekolah Tinggi Pertanian dan Kewirausahaan (STPK) Banau, Halmahera Barat untuk mata kuliah Kimia Pertanian.
DAFTAR GAMBAR... xvi
DAFTAR LAMPIRAN... xviii
PENDAHULUAN Latar Belakang... 1
Perumusan Masalah... 5
Tujuan Penelitian... 6
Manfaat Penelitian... 6
Hipotesis... 7
Ruang Lingkup Penelitian... 7
Kebaruan... 8
Pencangkokan dan Taut Silang... 19
Kromatografi... 20
Material Separator... 23
Temu Lawak... 24
Analisis Finansial dan Nilai Tambah... 26
METODE PENELITIAN Tempat dan Waktu Penelitian... 29
Rancangan Penelitian... 29
ISOLASI DAN PENCIRIAN SELULOSA DARI ELA SAGU, BAGAS TEBU, DAN JERAMI PADI Abstrak... 33
Abstract……….. 33
Pendahuluan... 34
Bahan dan Metode... 35
Hasil dan Pembahasan... 38
Simpulan... 56
REKAYASA BIOPOLIMER DENGAN TEKNIK PENCANGKOKAN DAN TAUT SILANG Abstrak... 57
Abstract……….. 57
Pendahuluan... 58
Bahan dan Metode... 60
Hasil dan Pembahasan... 62
UJI KINERJA MATERIAL SEPARATOR
Abstrak... 83
Abstract……… 83
Pendahuluan... 84
Bahan dan Metode... 85
Hasil dan Pembahasan... 87
Simpulan... 90
ANALISIS NILAI TAMBAH DAN PENDAPATAN USAHA INDUSTRI MATERIAL SEPARATOR BERBASIS BAGAS TEBU Abstrak... 91
Abstract………. 91
Pendahuluan... 92
Metode……... 92
Hasil dan Pembahasan... 98
Simpulan... 102
SIMPULAN DAN SARAN... 103
DAFTAR PUSTAKA... 105
2 Derajat polimerisasi berbagai jenis selulosa... 11 3 Kondisi isolasi dan rendemen polisakarida... 42 4 Viskositas intrinsik, derajat polimerisasi, dan bobot molekul... 48 5 Absorbansi relatif isolat selulosa dan produk hasil rekayasa ela sagu... 71 6 Absorbansi relatif isolat selulosa dan produk hasil rekayasa bagas
tebu... 72 7 Absorbansi relatif isolat selulosa dan produk hasil rekayasa jerami
padi... 72 8 Jenis pelarut pada fraksinasi ekstrak temu lawak... 86
9 Format analisis nilai tambah pengolahan... 96 10 Biaya produksi dan pendapatan industri material separator berbasis
bagas tebu... 99 11 Harga pokok, harga jual, dan keuntungan industri material separator
berbasis bagas tebu... 100 12 Nilai B/C Ratio industri material separator berbasis bagas tebu... 101 13 Titik impas industri material separator berbasis bagas tebu... 101
2 Bahan lignoselulosa berdasarkan sumbernya... 10
3 Ikatan hidrogen intra dan antar rantai selulosa... 12
4 Model fibril struktur supramolekul selulosa... 12
5 Skema ekstraksi pati sagu... 13
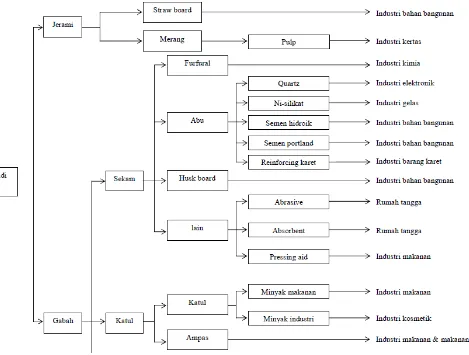
6 Pohon industri sagu... 14
7 Proses pembuatan gula pada pabrik gula ... 15
8 Pohon industri tebu... 16
9 Proses menghasilkan padi... 17
10 Pohon industri padi... 18
11 A Skema fisisorpsi (I), grafting to (II), grafting form (III); B Skema crosslinking antarmolekul (I) dan intramolekul (II)... 19
12 Profil kromatogram... 20
13 Profil kromatogram terkoreksi... 22
14 (a) Tanaman temu lawak dan (b) rimpang temu lawak... 24
15 (a)Struktur kimia kurkuminoid dan (b) Struktur kimia xantorizol….. 26
16 Bagan alir penelitian... 30
17 Metode isolasi selulosa secara umum (A) dan metode isolasi selulosa yang digunakan dalam penelitian ini (B)... 39 18 Komposisi kimia bahan baku... 41
19 Komposisi selulosa alfa... 43
20 Komposisi lignin... 43
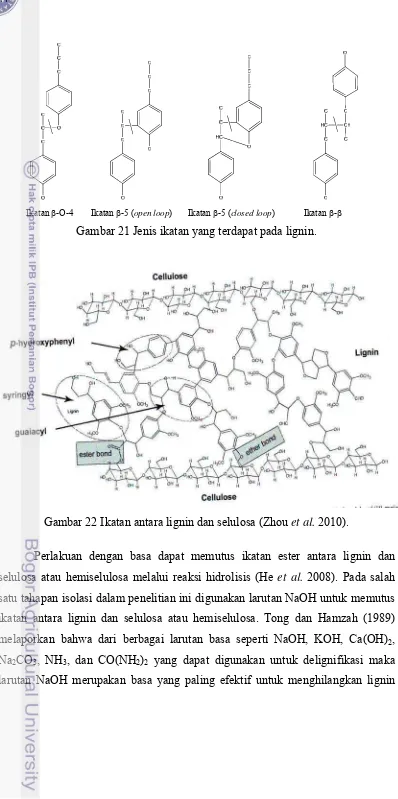
21 Jenis ikatan yang terdapat pada lignin... 44
22 Ikatan antara lignin dan selulosa... 44
23 Skema reaksi kompleks karbohidrat lignin dengan NaOH... 45
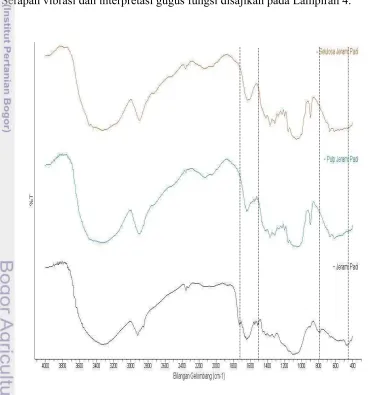
24 Spektra FTIR bahan baku awal, pulp, dan selulosa dari ela sagu... 49
25 Spektra FTIR bahan baku awal, pulp, dan selulosa dari bagas tebu… 50 26 Spektra FTIR bahan baku awal, pulp, dan selulosa dari jerami padi.. 51
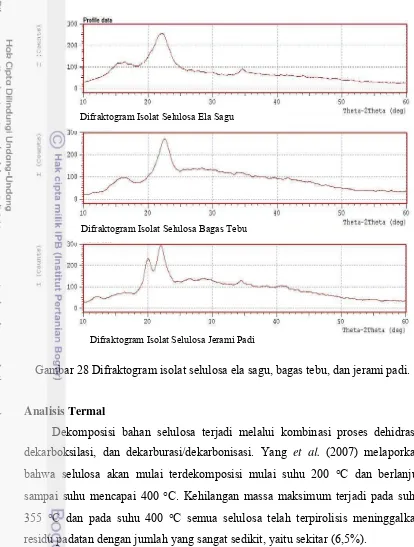
27 Mikrograf (a) bagas tebu, (b) jerami padi, dan (c) ela sagu... 52 28 Difraktogram isolat selulosa ela sagu, bagas tebu, dan jerami padi… 54
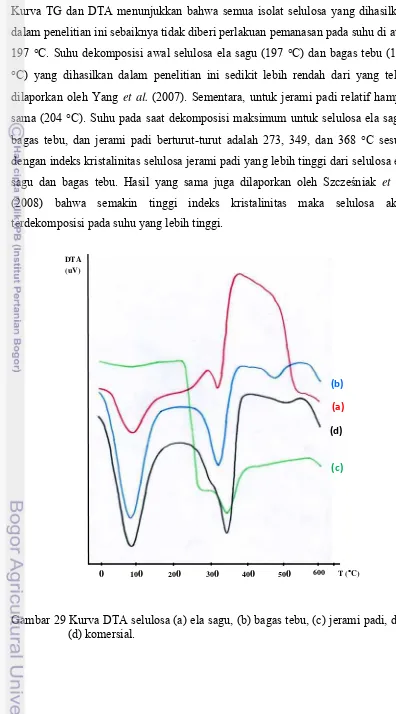
29 Kurva DTA selulosa (a) ela sagu, (b) bagas tebu, (c) jerami padi, dan (d) komersial...
55 30 Mekanisme kopolimerisasi cangkok akrilamida dan taut silang
MBAm... 65
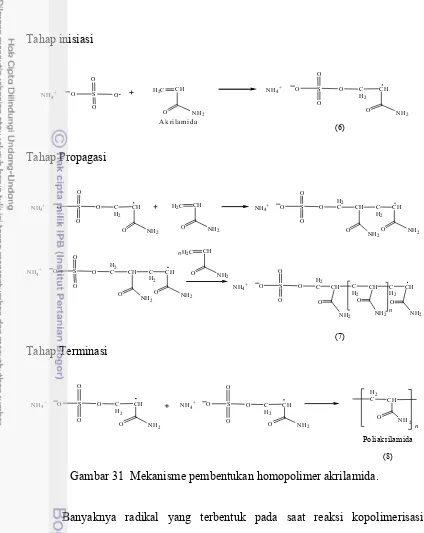
31 Mekanisme pembentukan homopolimer akrilamida ... 66
32 Pengaruh jumlah penaut silang terhadap (a) kadar nitrogen, (b) nisbah pencangkokan, dan (c) efisiensi pencangkokan... 68
33 Spektra FTIR selulosa ela sagu dan produk hasil rekayasa... 69
34 Spektra FTIR selulosa bagas tebu dan produk hasil rekayasa... 70
35 Spektra FTIR selulosa jerami padi dan produk hasil rekayasa…... 70
36 Mikrograf selulosa dan produk hasil rekayasa (a) ela sagu, (b) bagas tebu, dan (c) jerami padi... 73
37 Pengaruh jumlah penaut silang terhadap indeks kristalinitas... 74
38 Kurva DTA selulosa, homopolimer, dan produk rekayasa dari ela sagu... 76
39 Kurva DTA selulosa, homopolimer, dan produk rekayasa dari bagas tebu. ... 76
40 Kurva DTA selulosa, homopolimer, dan produk rekayasa dari jerami padi... 77
41 Daya serap air sebelum dan sesudah saponifikasi... 78
42 Hidrolisis parsial gugus amida pada rantai poliakrilamida... 79
43 Indeks refraksi selulosa dan produk rekayasa ela sagu... 80
44 Indeks refraksi selulosa dan produk rekayasa bagas tebu... 80
45 Indeks refraksi selulosa dan produk rekayasa jerami padi... 80
2 Serapan vibrasi FTIR ela sagu, pulp ela sagu, dan selulosa ela sagu…. 119 3 Serapan vibrasi FTIR bagas tebu, pulp bagas tebu, dan selulosa bagas
tebu... 120
4 Serapan vibrasi FTIR jerami padi, pulp jerami padi, dan selulosa jerami padi... 121
5 Serapan vibrasi FTIR dari selulosa ela sagu dan produk hasil rekayasa... 122
6 Serapan vibrasi FTIR dari selulosa bagas tebu dan produk hasil rekayasa... 123
7 Serapan vibrasi FTIR dari selulosa jerami padi dan produk hasil rekayasa... 124
8 Mikrograf selulosa dan produk hasil rekayasa... 125
9 Difraktogram selulosa ela sagu dan produk hasil rekayasa... 126
10 Difraktogram selulosa bagas tebu dan produk hasil rekayasa... 127
11 Difraktogram selulosa jerami padi dan produk hasil rekayasa... 128
12 Kurva DTA selulosa dan produk hasil rekayasa ela sagu... 129
13 Kurva DTA selulosa dan produk hasil rekayasa bagas tebu... 130
14 Kurva DTA selulosa dan produk hasil rekayasa jerami padi... 131
15 Hasil kurva termogravimetri... 132
16 Kromatogram standar zantorizol... 133
17 Kromatogram standar kurkumin... 134
18 Kromatogram ekstrak kasar temu lawak... 135
19 Kromatogram hasil fraksi ekstrak kasar temu lawak... 136
20 Perkiraan biaya investasi industri material separator berbasis bagas tebu... 150
21 Biaya tenaga kerja tidak langsung dan langsung... 152
22 Biaya bahan baku, bahan kimia, dan utilitas... 153
23 Perkiraan biaya perawatan... 154
24 Perkiraan biaya penyusutan... 154
25 Sumbangan input lain di luar bahan baku dan gaji pengelola... 155
26 Analisis nilai tambah pada nilai 100 %... 156
27 Analisis nilai tambah pada nilai 110 %... 157
Kajian bioprospeksi senyawa aktif dari bahan alam dan cara memperoleh senyawa aktif murni merupakan salah satu topik penelitian yang terus digali seiring dengan meningkatnya kebutuhan dan permintaan akan senyawa aktif murni dalam industri farmasi maupun kimia. Untuk menghasilkan senyawa aktif murni tersebut maka tahap isolasi, pemisahan, dan pemurnian menjadi langkah utama yang dibutuhkan dan terus dikembangkan sampai saat ini. Dari beberapa teknik pemisahan untuk menghasilkan senyawa aktif murni, kromatografi merupakan teknik yang paling banyak digunakan. Kromatografi merupakan teknik pemisahan yang cepat, mudah, dan tidak membutuhkan contoh yang banyak (Sastrohamidjojo 1991).
Pada prinsipnya, semua teknik kromatografi melibatkan dua fase, yaitu fase diam (stationary phase) dan fase gerak (mobile phase). Klasifikasi utama metode kromatografi dilakukan berdasarkan fase geraknya, subklasifikasi lebih lanjut didasarkan pada fase diam dan interaksi antara analit dan fase diam (Miller 1975). Fase diam dalam kromatografi dapat berupa zat padat atau zat cair, sedangkan fase gerak dapat berupa zat cair atau gas. Fase diam yang berbentuk zat padat pada teknik kromatografi untuk selanjutnya disebut material separator dalam penelitian ini.
Pemilihan dan penggunaan material separator dalam kromatografi bergantung pada sifat dan jenis senyawa aktif yang akan dipisahkan (Sastrohamidjojo 1991). Salah satu material separator yang dapat digunakan untuk pemisahan senyawa aktif adalah material separator yang berbasis senyawa polisakarida, seperti selulosa dan amilosa. Material separator jenis ini telah digunakan sebagai fase diam pada kolom HPLC (high performance liquid
chromatography) dan dapat diperoleh secara komersial. Beberapa material
diperoleh dengan cara mengimpor dan harganya relatif mahal. Sebagai ilustrasi untuk kolom HPLC Astec Cellulose DMP dengan panjang kolom 25 cm, diameter internal 2,1 mm, dan ukuran partikel sebesar 5 µm mempunyai harga 2.365 SGD
(dolar Singapura).
Di dalam material separator berbasis senyawa polisakarida, salah satu polimer backbone yang dapat digunakan adalah selulosa. Selulosa merupakan senyawa penyusun utama hampir sebagian besar jaringan tanaman. Jumlahnya yang cukup banyak menjadikan selulosa sebagai bahan baku potensial yang dapat digunakan di berbagai industri. Selulosa dapat diisolasi dari kayu dan bahan organik lainnya. Limbah pertanian seperti ampas sagu atau ela sagu, ampas tebu atau bagas tebu, jerami padi, ampas tapioka, dan lain-lain dapat dijadikan sumber alternatif untuk mendapatkan selulosa. Di dalam penelitian ini, 3 jenis limbah pertanian, yaitu ela sagu, bagas tebu, dan jerami padi digunakan sebagai bahan baku untuk menghasilkan polimer backbone pada material separator.
Di Indonesia, potensi ela sagu sangat besar. Sampai saat ini, luas area tanaman sagu belum dapat diketahui dengan pasti. Namun, beberapa pakar memperkirakan luas lahan sagu mencapai 2.201.000 ha, dengan luas lahan terbesar berada di Papua (Papilaya 2009). Satu hektar lahan sagu memiliki rerata masak tebang 20 pohon dengan tingkat produksi sekitar 4.400 kg tepung sagu. Sementara itu, nisbah antara tepung sagu dan ela sagu yang dihasilkan adalah 1:6 (Rumalatu 1981 yang diacu Matitaputty dan Alfons 2006). Dengan demikian, ela sagu yang dapat dihasilkan dapat mencapai kira-kira 58 juta ton.
Selain ela sagu, ampas tebu juga berpotensi sebagai sumber alternatif selulosa. Ampas tebu atau lazimnya disebut bagas (bagasse) adalah hasil samping dari proses ekstraksi (pemerahan) cairan tebu di pabrik gula. Pada tahun 2009, produksi tebu di Indonesia mencapai 2,7 juta ton per tahun dengan luas lahan ±
400 ribu ha (Direktorat Jenderal Perkebunan 2010). Areal perkebunan tebu di Indonesia tersebar di Medan, Lampung, Semarang, Solo, dan Makassar. Ampas tebu yang dapat dihasilkan setiap pabrik gula sekitar 35-40% dari berat tebu yang digiling (Husin 2007). Jumlah total tebu giling pada tahun 2009 sebesar 33,3 juta ton sehingga ampas tebu yang dihasilkan mencapai 9,9 juta ton. Sebanyak 60% dari ampas tebu yang dihasilkan tersebut dimanfaatkan oleh pabrik gula itu sendiri sebagai bahan bakar, sedangkan sisanya sekitar 3,96 juta ton ampas tebu per tahun belum dimanfaatkan secara maksimal. Jumlah ini akan terus bertambah seiring dengan penambahan lahan perkebunan tebu dan peningkatan produktivitas tanaman tebu yang telah dicanangkan oleh Pemerintah Indonesia dalam rangka menuju swasembada gula di tahun 2012.
Kajian pemanfaatan bagas tebu selain sebagai bahan bakar adalah sebagai bahan baku industri kertas, bahan baku industri kanvas rem, pakan ternak (Tarmidi 2004; Widodo 2006), membran (Rodrigues et al. 2000), campuran pembuatan asbes (Mubin & Fitriadi 2005), produksi furfural (Wijanarko et al. 2006), produksi bioetanol (Samsuri et al. 2007), metilselulosa (Viera et al. 2007), plastisizer (Hamid et al. 2009), dan lain-lain. Bagas tebu juga telah dimanfaatkan sebagai bahan baku pembuatan papan partikel serta bahan bakar. Sampai saat ini, belum diperoleh informasi mengenai pemanfaatan selulosa dari bagas tebu sebagai polimer backbone dalam material separator.
Beberapa kajian tentang pemanfaatan jerami padi telah dilaporkan, di antaranya sebagai bahan baku pembuat kertas (Sun et al. 2000), bahan untuk pupuk kompos (Zayed dan Abdel-Motaal 2005), bahan baku untuk pakan ternak (van Soest 2006), karbon aktif (Basta et al. 2009; Fierro et al. 2010), adsorben (Gong et al. 2008), bahan bakar gas hidrogen (Huang et al. 2010) ), papan partikel
(Li et al. 2011). Sampai saat ini, belum diperoleh informasi mengenai
pemanfaatan selulosa dari jerami padi sebagai polimer backbone dalam material separator.
Untuk memperbaiki/meningkatkan sifat fisik dan kimia biopolimer yang dihasilkan dari limbah pertanian berbasis selulosa seperti ela sagu, bagas tebu, dan jerami padi, maka perlu dilakukan kajian untuk merekayasa biopolimer tersebut melalui teknik pencangkokan (grafting) dan taut silang (crosslinking). Berbagai jenis polimer dapat dicangkokkan ke rantai selulosa melalui gugus hidroksil pada posisi C2, C3, dan C6 (Enomoto-Rogers et al. 2009). Dengan memilih monomer yang tepat, maka kekuatan mekanik dan stabilitas termal material berbasis selulosa yang direkayasa/dimodifikasi dengan teknik pencangkokan dan taut silang juga dapat ditingkatkan (Princi 2005). Selain itu, produk yang dihasilkan akan memiliki struktur makromolekular seperti gel atau hidrogel, resin polimer, membran atau material komposit yang dapat diaplikasikan untuk teknologi pemisahan (Crini 2005).
separator dievaluasi sebagai kolom pemisahan pada teknik kromatografi untuk memisahkan senyawa aktif xantorizol pada ekstrak kasar temu lawak.
Rekayasa biopolimer dari limbah pertanian berbasis selulosa untuk diaplikasikan sebagai material separator seperti yang dilakukan pada penelitian ini dapat menjadi solusi permasalahan dalam teknologi separasi dan juga permasalahan yang ditimbulkan akibat pemanfaatan limbah pertanian yang belum optimal. Selain itu, akan mendorong kemandirian nasional dalam memenuhi kebutuhan material separator dan penyediaan senyawa aktif xantorizol ekstrak kasar temu lawak untuk kebutuhan industri farmasi.
Perumusan Masalah
Berbagai limbah pertanian seperti ela sagu, bagas tebu, dan jerami padi diketahui mengandung selulosa (Awg-Adeni et al. 2010; Samsuri et al. 2007; Jiang et al. 2011). Selulosa yang diperoleh dari tanaman berbeda akan memiliki karakteristik yang berbeda pula, sehingga melalui tahapan isolasi dan pencirian selulosa akan diperoleh informasi karakteristik selulosa dari ela sagu, bagas tebu, dan jerami padi. Selanjutnya, selulosa dari ela sagu, bagas tebu, dan jerami padi akan dijadikan sebagai backbone pada tahap rekayasa untuk menghasilkan material separator.
Selulosa merupakan polimer hidrofilik dengan tiga gugus hidroksil reaktif di tiap unit hidroglukosa, tersusun atas ribuan gugus anhidroglukosa yang tersambung melalui ikatan 1,4-β-glikosida membentuk molekul berantai yang
panjang dan linier (Lehninger 1993). Gugus hidroksil pada selulosa ini dapat dimanfatkan pada saat memodifikasi selulosa, yaitu dengan cara memasukkan gugus fungsi tertentu pada selulosa melalui teknik pencangkokan. Modifikasi kimia dengan teknik pencangkokan ini bertujuan memperbaiki dan meningkatkan sifat hidrofilik atau hidrofobik, elastisitas, kemampuan pertukaran ion, ketahanan panas, dan ketahanan terhadap serangan mikroba. Modifikasi lebih lanjut terhadap selulosa melalui teknik taut silang membuat struktur material polimer yang terbentuk menjadi lebih kuat dan stabil (Saika dan Ali 1999; Princi 2005).
Pada penelitian ini, material separator yang dihasilkan memiliki multigugus fungsi (-OH, -COOH, -COONH2, dsb.) yang diharapkan dapat meningkatkan resolusi dan efisiensi pemisahan melalui sistem multipartisi. Adanya taut silang juga dapat membantu proses pemisahan melalui efek sterik, di samping memberikan kontribusi terhadap stabilitas material separator sehingga lebih tahan dan dapat diregenerasi untuk penggunaan ulang. Teknik kopolimerisasi pencangkokan dan taut silang terhadap selulosa dari limbah pertanian berbasis selulosa yang dipadu dengan proses hidrolisis parsial, memungkinkan diperoleh material separator dengan multigugus fungsi seperti tersebut di atas.
Secara spesifik permasalahan yang akan diteliti adalah sebagai berikut: 1. Kondisi proses isolasi selulosa dari ela sagu, bagas tebu, dan jerami padi,
serta karakteristik selulosa yang dihasilkan dari ketiga contoh tersebut di atas
2. Kondisi proses rekayasa biopolimer untuk menghasilkan material separator dengan menggunakan selulosa sebagai polimer backbone, akrilamida sebagai monomer untuk menghasilkan polimer cangkok, dan N,N’-metilena-bis-akrilamida sebagai pereaksi penaut silang.
3. Uji kinerja material separator dalam pemisahan senyawa aktif xantorizol pada ekstrak temu lawak.
Tujuan Penelitian
Penelitian ini bertujuan mendapatkan material separator molekul melalui rekayasa biopolimer dari limbah pertanian berbasis selulosa dengan teknik kopolimerisasi cangkok dan taut silang.
Manfaat Penelitian
Hipotesis
Hipotesis yang diajukan dalam penelitian ini adalah:
1. Selulosa yang diperoleh dari ketiga jenis limbah pertanian yang digunakan bersifat khas/unik. Hal ini akan terlihat melalui nilai derajat polimerisasi, bobot molekul, indeks kristalinitas, dan stabilitas termal.
2. Material separator dapat diperoleh melalui rekayasa biopolimer selulosa melalui teknik kopolimerisasi cangkok dan taut silang.
3. Material separator yang dihasilkan dapat memisahkan senyawa aktif xantorizol secara efektif dan efisien. Hal ini akan terlihat dari efisiensi dan resolusi pemisahan senyawa tersebut dengan teknik kromatografi.
Ruang Lingkup Penelitian
Ruang lingkup tahapan penelitian yang dikerjakan adalah sebagai berikut: 1. Analisis komponen kimia ela sagu, bagas tebu, dan jerami padi
2. Isolasi dan pencirian selulosa yang diperoleh dari ela sagu, bagas tebu, dan jerami padi.
3. Penentuan kondisi rekayasa biopolimer dengan teknik kopolimerisasi cangkok dan taut silang dari ela sagu, bagas tebu, dan jerami padi untuk menghasilkan material separator
4. Uji kinerja material separator untuk pemisahan senyawa aktif xantorizol dalam ekstrak kasar temu lawak dengan teknik kromatografi
Kebaruan
Kebaruan dari penelitian ini adalah:
1. Teknik isolasi selulosa, khususnya isolasi selulosa dari ela sagu
2. Rekayasa biopolimer selulosa dari ela sagu, bagas tebu, dan jerami padi dengan teknik pencangkokan dan taut silang menggunakan akrilamida dan N,N’-metilena-bis-akrilamida.
3. Teknik pemisahan senyawa aktif xantorizol dari ekstrak temu lawak dengan material separator berbasis limbah pertanian
Selulosa adalah homopolimer yang tersusun dari subunit D-glukosa yang ditautkan satu sama lain dengan ikatan β-(1→4)-glikosida. Unit penyusun (building block) selulosa adalah selobiosa karena unit keterulangan dalam molekul selulosa adalah 2 unit gula (D-glukosa). Selulosa adalah senyawa yang tidak larut di dalam air dan ditemukan pada dinding sel tumbuhan terutama pada tangkai, batang, dahan, dan semua bagian berkayu dari jaringan tumbuhan. Selulosa merupakan polisakarida struktural yang berfungsi untuk memberikan perlindungan, bentuk, dan penyangga terhadap sel, dan jaringan. (Lehninger 1993). Gambar 1 menyajikan struktur kimia dari selulosa.
Gambar 1 Struktur kimia selulosa.
Gambar 2 Bahan lignoselulosa berdasarkan sumbernya (Hu et al. 2008).
Tabel 1 Komposisi kimia beberapa bahan yang mengandung lignoselulosa
Sumber Komposisi (%) Pustaka Acuan Lignoselulosa Selulosa Hemiselulosa Lignin
Jerami padi 36,5 33,8 12,3 Sun et al. (2000) Bagas tebu 43,6 33,5 18,1 Sun et al. (2004a)
Abaka 63,72 5-10 21,83 Hon (1996) Tongkol jagung 45 35 15 Hon (1996)
Kapas 95 2 0,9 Hon (1996)
Sisal 73 11 13 le Digabel dan Avérous (2006) Jerami gandum 39,4 24,0 11,2 Kham et al. (2005) Serat rami 65,0 15,8 12,7 Jahan et al. (2011)
Jumlah unit glukosa di dalam molekul selulosa dapat dilihat melalui derajat polimerisasinya (DP). Derajat polimerisasi didefinisikan sebagai berikut:
glukosa unit
satu molekul bobot
selulosa molekul
Derajat polimerisasi dapat ditentukan secara viskometri. Derajat polimerisasi selulosa sangat bervariasi, nilai DP bergantung pada sumber dan perlakuan yang diberikan. Perlakuan kimia secara intensif seperti pembuatan pulp, pengelantangan, dan transfromasi akan sangat menurunkan harga DP. Proses delignifikasi dan ekstraksi juga dapat menurunkan DP selulosa. Selain itu, semakin tua umur pohon, maka derajat polimerisasi juga semakin menurun (Fengel dan Wegener 1995). Derajat polimerisasi juga menggambarkan perkiraan bobot molekul dari selulosa. Tabel 2 menyajikan derajat polimerisasi berbagai bahan yang mengandung selulosa.
Tabel 2 Derajat polimerisasi berbagai jenis selulosa
Bahan Kisaran DP
Native cotton Up to 12000
Scoured & bleached cotton 800-1800
Wood pulp 600-1200
Man-made cellulose filaments and fibers 250-500
Cellulose powders (prepared by partial hyrolysis and mechanical disintegration)
100-200
Sumber: Klemm et al. (1998)
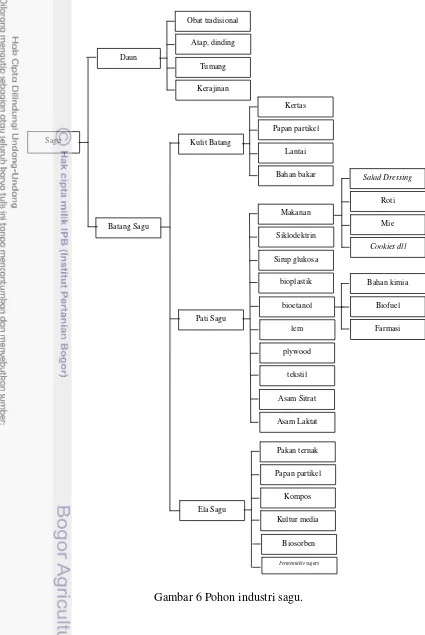
Selulosa memiliki struktur yang unik karena kecenderungannya membentuk ikatan hidrogen yang kuat. Ikatan hidrogen intramolekular terbentuk antara: (1) gugus hidroksil C3 pada unit glukosa dan atom O cincin piranosa yang terdapat pada unit glukosa terdekat, (2) gugus hidroksil pada C2 dan atom O pada C6 unit glukosa tetangganya. Ikatan hidrogen antarmolekul terbentuk antara gugus hidroksil C6 dan atom O pada C3 di sepanjang sumbu b (Gambar 3). Dengan adanya ikatan hidrogen serta gaya van der Waals yang terbentuk, maka struktur selulosa dapat tersusun secara teratur dan membentuk daerah kristalin. Di samping itu, juga terbentuk rangkaian struktur yang tidak tersusun secara teratur yang akan membentuk daerah nonkristalin atau amorf. Semakin tinggi packing density-nya maka selulosa akan berbentuk kristal, sedangkan semakin rendah
packing density maka selulosa akan berbentuk amorf. Derajat kristalinitas selulosa
kristalin akan bergabung dengan bagian nonkristalin. Mikrofibril-mikrofibril akan bergabung membentuk fibril, selanjutnya gabungan fibril akan membentuk serat (Gambar 4).
Gambar 3 Ikatan hidrogen intra dan antar rantai selulosa (Klemm et al. 1998).
Ela Sagu
Ela sagu (hampas) adalah limbah padat selain kulit batang yang dihasilkan pada saat ekstraksi pati sagu (Metroxylon sagu). Pada saat ekstraksi pati sagu akan dihasilkan 3 (tiga) limbah, yaitu kulit batang sagu (bark), limbah padat berserat (ela sagu~hampas), dan air limbah. Skema ekstraksi pati sagu disajikan pada Gambar 5.
Gambar 5 Skema ekstraksi pati sagu.
Jumlah ela sagu yang dihasilkan pada setiap proses ekstraksi pati sagu bergantung pada kualitas proses ekstraksi di tempat tersebut. Menurut Awg-Adeni et al. (2010), ela sagu mengandung sekitar 66% pati dan 14% serat kasar serta
25% lignin. Pada proses ekstraksi pati sagu, limbah padat berserat yang masih mengandung sedikit pati merupakan masalah utama, khususnya untuk pabrik berskala besar, karena jumlahnya yang sangat banyak. Penanganan limbah ela sagu ini juga sulit karena kelembabannya yang tinggi sehingga tidak mudah kering dan masih mengandung pati. Pada kondisi ini, ela sagu mudah menjadi media tumbuh mikroorganisme. Selain pati, ela sagu mengandung sejumlah selulosa dan lignin. Beberapa kajian tentang pemanfaatan ela sagu telah dilaporkan pada pohon industri sagu yang disajikan pada Gambar 6.
Sago Pith
Debarking
Pulping
Starch Extraction
Drying & Packing
Bark
Hampas
Fiber
Starch
Bagas Tebu
Ampas tebu atau lazimnya disebut bagas (bagasse) adalah hasil samping dari proses ekstraksi (pemerahan) cairan tebu di pabrik gula. Gambar 7 menyajikan proses pembuatan gula pada pabrik gula.
Gambar 7 Proses pembuatan gula pada pabrik gula.
Jerami Padi
Jerami padi adalah limbah pertanian yang dihasilkan dalam jumlah cukup banyak setiap tahunnya. Jerami padi dihasilkan sebagai proses penggabahan. (Gambar 9). Pohon industri dari tanaman padi disajikan pada Gambar 10.
Gambar 9 Proses menghasilkan padi.
Pencangkokan dan Taut Silang
Penggabungan monomer dan polimer dapat dilakukan dengan berbagai teknik, di antaranya adalah dengan fisisorpsi, pencangkokan (grafting), dan taut silang (crosslinking) (Bhattacharya et al. 2009). Istilah fisisorpsi digunakan jika melibatkan ikatan secara fisik. Proses fisisorpsi ini adalah proses yang dapat balik (reversibel). Pencangkokan melibatkan ikatan secara kovalen dan bersifat tidak dapat balik (irreversibel). Teknik pencangkokan terbagi menjadi grafting to dan grafting from. Pada grafting to, polimer backbone membawa gugus fungsional X
reaktif yang terdistribusi secara random dan bereaksi dengan polimer lain yang membawa gugus fungsi Y. Teknik grafting from terjadi jika polimer backbone membawa tapak aktif yang digunakan untuk menginisiasi polimerisasi monomer lain. Teknik grafting form akan menghasilkan polimer dengan derajat grafting yang tinggi. Proses grafting secara skematis disajikan pada Gambar 11a. Taut silang adalah menggabungkan polimer-polimer melalui suatu ikatan kimia. Pada sebagian kasus, taut silang bersifat tidak dapat balik. Ikatan yang terbentuk melalui taut silang dapat berbentuk intra- atau antarmolekul. Proses taut silang secara skematis disajikan pada Gambar 11b.
Kromatografi
Kromatografi berasal dari kata chroma yang berarti warna dan graphein yang artinya menulis. Kromatografi adalah salah satu teknik yang digunakan di laboratorium untuk pemisahan campuran. Pada prinsipnya semua kromatografi menggunakan dua cara, yaitu fase diam (stationary phase) dan fase gerak (mobile phase). Pemisahan bergantung pada gerakan relatif dari kedua fase ini.
Keuntungan penggunaan teknik kromatografi adalah cepat, murah, dapat memisahkan campuran yang kompleks, dan membutuhkan analit yang sedikit (Miller 1975; Ahuja 2002).
Pada beberapa jenis kromatografi, kolom merupakan tempat untuk memisahkan. Kolom selalu berbentuk tabung yang dapat diatur menjadi kumparan atau lurus. Jika suatu analit dimasukkan ke dalam alat kromatografi, maka akan ada waktu dimana analit ditahan oleh kolom. Waktu ini disebut waktu penahanan (tR). Pada kondisi ideal dengan pemisahan yang sempurna, puncak yang dihasilkan oleh suatu campuran analit adalah berbentuk garis tipis (Gambar 12a), namun demikian kondisi ini jarang terjadi. Puncak yang sering didapatkan adalah puncak dengan bentuk kurva-kurva Gauss dengan pelebaran puncak (Gambar 12b), atau pada keadaan tertentu dapat dihasilkan puncak berekor dengan pemanjangan di muka.
Gambar 12 Profil kromatogram. Injeksi
A B
D C
d
W1
W2
Resolusi Pemisahan
Resolusi pemisahan adalah pemisahan nyata antara 2 puncak yang saling berdekatan. Resolusi pemisahan (R) dinyatakan sebagai:
2
Jika R=1 maka pemisahan dikatakan 98%. Untuk pemisahan yang baik, maka R harus ≥ 1.5. Hal ini berarti pemisahan yang terjadi adalah ≥ 99.7%
Pemisahan dari puncak-puncak dalam kromatogrfi erat hubungannya dengan dua faktor, yaitu:
1. Efisiensi Kolom: Pelebaran puncak merupakan hasil dari bentuk kolom dan kondisi operasi
2. Efisiensi Pelarut: Hasil dari interaksi antara cuplikan dengan fase diamnya. Efisiensi pelarut menentukan relatif dari jalur-jalur solut dalam suatu kromatogram.
Efisiensi Kolom
Efisiensi kolom diukur sebagai jumlah pelat teoritis (N). HETP (The height equivalent to a theoretical plate) didefinisikan sebagai:
N L
HETP=
N adalah jumlah pelat teoritis dalam suatu kolom dan L adalah panjang kolom(cm). Efisiensi kolom tergantung pada:
1. Pelarut-fase diam
2. Analit/zat yang dilarutkan 3. Suhu
Efisiensi Pelarut
Kromatografi dapat memisahkan campuran kompleks yang memiliki titik didih sama. Pada kondisi ini, pemisahan tidak akan bisa dilakukan melalui teknik distilasi. Pelarut mempunyai interaksi yang spesifik dengan analit. Pemisahan akan tergantung pada harga koefisien partisi (K).
Efisiensi pelarut didefinisikan sebagai perbandingan dari koefisien partisi atau waktu retensi yang telah diatur. Profil kromatogram terkoreksi disajikan pada Gambar 13.
Keterangan:
X1, X2 adalah waktu retensi (volume) dari puncak 1,2 X1’, dan X2’ adalah waktu retensi terkoreksi
Gambar 13 Profil kromatogram terkoreksi.
Efisiensi pelarut (α) dinyatakan sebagai:
1
Selain itu dapat didefinisikan juga faktor pemisahan (SF) sebagai:
1 2 x x
SF =
Faktor kapasistas untuk suatu pemisahan didefinisikan sebagai:
Koefisien partisi (K) akan tergantung pada suhu. Harga K akan turun dengan meningkatnya suhu karena molekul-molekul akan tertahan lebih lama di dalam fase gas pada suhu yang tinggi dan efisiensi pelarut akan tetap pada kisaran suhu tertentu. Akan tetapi, pada suhu yang relatif tinggi, harga K akan menjadi sangat kecil sehingga pemisahan akan menjadi tidak sempurna. Hal ini disebabkan pemisahan hanya terjadi di fase cairnya saja.
Secara umum dapat diperkirakan jumlah pelat teoritis (N) yang dibutuhkan dalam suatu pemisahan atau dengan kata lain dapat diperkirakan panjang kolom yang dibutuhkan untuk menghasilkan pemisahan yang baik, melalui persamaan berikut ini:
Nyangdibutuhkan α
α
dengan R adalah resolusi pemisahan, α adalah efisiensi pelarut, dan k2’ adalah faktor kapasistas.
Material Sepator
Senyawa selulosa dan turunan selulosa telah digunakan dalam teknologi separasi sebagai material separator, khususnya dalam teknik kromatografi misalnya pada kromatografi kertas sampai kromatografi cair kinerja tinggi. Aplikasi senyawa turunan selulosa sebagai penukar ion pada kromatografi lapis tipis dilaporkan memberikan hasil yang cepat dan akurat dalam pemisahan ion-ion anorganik pada konsentrasi yang kecil. Beberapa kajian terkait dengan pemisahan ion logam ini telah dilaporkan di antaranya menggunakan karboksimetil selulosa (CMC) (Shimizu et al. 1976), menggunakan selulosa fosfat (Shimizu et al. 1980), menggunakan polietilenimina-selulosa (Shimizu et al. 1989).
Kajian beberapa material separator berbasis selulosa sebagai chiral stationary phases (CSP) telah dilaporkan di antaranya oleh Ficarra et al. (2000)
O,O-dialkil-2-benziloksikarbonilaminoarilmetil fosfonat (Yang et al. 2002). Lipka et al. (2005) melakukan pemisahan secara kiral pada derivat senyawa melatoninergat menggunakan kolom kiral berbasis selulosa. Su-lian et al. (2007) menggunakan etil selulosa (EC) dan paduan etil selulosa/selulosa asetat (EC/CA) sebagai column packing material pada HPLC (high performance liquid chromatography).
Temu Lawak
Temu lawak (Curcuma xanthorrhiza) merupakan salah satu jenis tanaman unggulan yang mememilik banyak manfaat, di antaranya sebagai bahan tambahan makanan, obat-obatan, dan suplemen energi (Hwang et al. 2004). Klasifikasi tanaman temu lawak adalah sebagai berikut: kingdom Plantae, divisi Spermatophyta, subdivisi Angiospermae, kelas Monocotyledonae, ordo Zingeberales, famili Zingiberaceae, genus Curcuma, dan spesies Curcuma xanthorrhiza. Temu lawak memiliki beberapa nama, misalnya koneng gede (Jawa
Barat), temu lawak (Jawa Tengah), temu lobak (Madura), dan tetemu lawak (Sumatera) (Supriadi 2001).
Temu lawak termasuk tanaman tahunan yang tumbuh merumpun. Setiap rumpun tanamannya terdiri atas beberapa anakan dengan 2-9 helai daun. Temu lawak memiliki rimpang dengan daging rimpang berwarna kuning, berbau tajam, dan terasa pahit. Tanaman dan rimpang temu lawak disajikan pada Gambar 14.
(a) (b)
Gambar 14 (a) Tanaman temu lawak dan (b) rimpang temu lawak.
Temu lawak dilaporkan memiliki berbagai aktivitas biologis seperti antitumor, antiinflamasi, antioksidan, hepatoprotektif, dan antibakteri (Ravindran et al. 2007). Sementara itu, Irawati (2008) melaporkan bahwa kapasitas antioksidan temu lawak menggunakan metode CUPRAC dengan pelarut THF sebesar 131,5937 µmol tr/g ekstrak. Aktivitas tersebut disebabkan adanya senyawa aktif dalam temu lawak, terutama kurkuminoid dan xantorizol (Hwang et al. 2004)
Temu lawak dapat dimanfaatkan untuk mengobati berbagai macam penyakit, yaitu gangguan hati, demam, sakit kuning, pegal-pegal, sembelit, perangsang air susu, dan obat peluruh haid. Selain itu, rimpang temu lawak juga berkhasiat untuk obat kejang, antijerawat, malaria, diare, kurang nafsu makan, kurang darah, cacar air, radang lambung, getah empedu, cacingan, kencing darah, dan radang ginjal (Sidik et al. 1995).
Kurkuminoid (Gambar 15a) merupakan komponen yang memberi warna kuning atau jingga pada rimpang temu lawak, berbentuk serbuk, berasa pahit, memiliki aroma yang khas, dan tidak bersifat toksik. Senyawa ini larut dalam aseton, alkohol, asam asetat glasial, dan alkali hidroksida kurkuminoid berkhasiat menetralkan racun, menurunkan kadar kolesterol dan trigliserida darah, antibakteri, analgesik, dan antiinflamasi (Ravindran et al. 2007).
Keterangan : 1. Kurkumin R1 = R2 = −OCH3
2. Demetoksikurkumin R1 = H, R2 = −OCH3
3. Bisdemetoksikurkumin R1 = R2 = −H
a. Struktur kimia kurkuminoid.
b. Struktur kimia xantorizol.
Gambar 15 Struktur kimia kurkuminoid (a) dan xantorizol (b)
Analisis Finansial dan Nilai Tambah
Dalam pendirian suatu pabrik terdapat investasi, yaitu kegiatan yang menuntut akan waktu yang singkat, dan tingkat keyakinan yang tinggi akan keberhasilan suatu pertukaran penggunaan untuk harapan berkembangnya penggunaan tersebut di masa mendatang (Holmes 1998). Menurut Sutojo (2002), kajian terhadap keadaan dan prospek suatu industri dilakukan atas aspek-aspek tertentu di antaranya aspek pasar dan pemasaran, aspek produksi, teknis dan teknologis, aspek manajemen dan sumber daya manusia serta aspek keuangan dan ekonomi.
dibiayai dengan pinjaman dari pihak ketiga, serta dari mana sumbernya dan berapa besarnya.
Beberapa hal yang perlu diperhatikan dalam analisis finansial, yaitu modal investasi, modal kerja, dan penyusutan. Menurut Kadariah et al. (1999), analisis finansial suatu proyek memandang perbandingan pengeluaran uang dan perolehan keuntungan dari proyek tersebut. Bila analisis tersebut menunjukkan keuntungan (benefit) yang bernilai positif, maka rencana proyek dapat dilanjutkan. Bila sebaliknya yaitu bernilai negatif, maka rencana investasi tersebut sebaiknya dibatalkan. Analisis finansial dapat dilakukan dengan menghitung biaya investasi dan biaya produksi, yang kemudian dinilai kelayakan investasinya melalui beberapa penilaian di antaranya Net Present Value (NPV), Internal Rate of Return (IRR), Net Benefit-Cost Ratio (net B/C), Break Even Point (BEP), Pay Back Period (PBP), dan analisis sensitivitas. Di dalam penelitian ini, penilaian terhadap
analisis finansial dilakukan terhadap (a) analisis biaya dan pendapatan yang meliputi biaya produksi, penerimaan, dan keuntungan; (b) rasio B/C; dan (c) nilai BEP
Tempat dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Kimia Terpadu, Laboratorium Kimia Fisik, dan Laboratorium Kimia Organik-Departemen Kimia, Institut Pertanian Bogor. Beberapa pencirian juga dilakukan di laborotorium pendukung lainnya, seperti di Puslitbang Hutan, Bogor dan di Faperta IPB. Waktu penelitian berlangsung dari bulan Januari 2010-Oktober 2011
Rancangan Penelitian
Penelitian rekayasa biopolimer ini dilakukan dalam beberapa tahapan, meliputi:
1. Preparasi dan pencirian bahan baku limbah pertanian berbasis selulosa 2. Isolasi dan pencirian selulosa
3. Rekayasa biopolimer dengan teknik kopolimerisasi cangkok dan taut silang untuk menghasilkan material separator
4. Uji kinerja material separator 5. Analisis nilai tambah
Gambar16 Bagan alir penelitian.
Preparasi dan Isolasi Air, NaOH,
HCl, H2O2
3 Prototipe Material Separator (ela, bagas, jerami)
Uji Kinerja & Seleksi
Homopolimer pereaksi sisa
Residu dan pereaksi sisa
Monomer, inisiator, crosslinker
1 Prototipe Material Separator Terbaik
Sampling
Bahan Baku Limbah Pertanian
berbasis Selulosa
Rekayasa Biopolimer Biopolimer
(Selulosa)
Preparasi dan Pencirian Bahan Baku Limbah Pertanian Berbasis Selulosa
Bahan baku yang akan digunakan dalam penelitian ini berupa limbah pertanian berbasis selulosa, yaitu: a) ampas tebu (bagas) yang diperoleh dari pabrik gula Modjopanggung di Tulungagung, Jawa Timur, b) ela sagu yang diperoleh dari industri pengolahan sagu di Cimahpar, Kab. Bogor, Jawa Barat, dan c) jerami padi dari daerah Kab. Purwakarta, Jawa Barat. Masing-masing bahan baku dicuci dan dihaluskan dengan ukuran kira-kira 100 mesh serta dicampur secara homogen. Bahan baku yang telah mengalami perlakuan tersebut terlebih dahulu dicirikan melalui analisis proksimat, seperti karbohidrat, protein, lemak, mineral, dan air dengan mengacu pada metode standar (AOAC 2005). Selain itu, komposisi selulosa, hemiselulosa, dan lignin juga akan ditentukan dengan mengacu pada metode standar TAPPI (1961) dan ASTM (1981). Rincian tahapan penelitian ini disajikan pada bagian Isolasi dan Pencirian Selulosa.
Isolasi dan Pencirian Selulosa
Tahap isolasi selulosa diawali dengan penghilangan protein dan lemak melalui teknik ekstraksi Soxhlet menggunakan campuran toluena-etanol 2:1 v/v. Tahap selanjutnya adalah delignifikasi dan demineralisasi (dengan perlakuan asam) dan dilanjutkan dengan fraksionasi untuk memperoleh isolat selulosa. Isolat yang diperoleh kemudian dikeringkan dan dibuat dalam bentuk bubuk (100 mesh). Isolat ini lebih lanjut akan digunakan sebagai bahan backbone untuk pembuatan material separator.
Rekayasa Biopolimer
Rekayasa biopolimer dilakukan dengan teknik kopolimerisasi cangkok dan taut silang secara radikal bebas yang mengacu pada metode Doane (2009)dalam atmosfir inert (menggunakan gas nitrogen). Monomer yang akan digunakan adalah jenis akrilamida (Am), sedangkan sebagai inisiator dan penaut silang berturut-turut adalah amonium persulfat (APS) dan N,N’-metilena-bis-akrilamida (MBAm). Kajian pengaruh penaut silang terhadap total substrat akan dilakukan. Keberhasilan rekayasa ini akan dipantau dengan paduan teknik fourier transform
infrared (FTIR) spectrometric dan gravimetrik. Melalui spektrum FTIR akan
diperoleh informasi menyangkut keberlangsungan proses grafting-crosslinking copolimerization secara kualitatif, sedangkan teknik gravimetrik (kuantitatif) akan
digunakan untuk mengevaluasi kopolimerisasi cangkok dan taut silang menggunakan parameter nisbah pencangkokan dan efisiensi pencangkokan. Rincian tahapan penelitian ini disajikan pada bagian Rekayasa Biopolimer dengan Teknik Pencangkokan dan Taut Silang.
Uji Kinerja Material Separator
Uji kinerja akan dilakukan terhadap satu prototipe material separator terbaik hasil prototipe potensial yang diperoleh pada tahap sebelumnya. Evaluasi kinerja meliputi resolusi dan efisiensi pemisahan mengacu pada Ahuja (2002). Uji kinerja material separator dilakukan dengan mengaplikasikan material separator untuk pemisahan senyawa aktif xantorizol ekstrak kasar temu lawak dengan teknik kromatografi.
Analisis Finansial dan Nilai Tambah
Abstrak
Selulosa diisolasi dari ela sagu, bagas tebu, dan jerami padi. Delignifikasi dilakukan dengan metode peroksida bersuasana basa (H2O2 5% pH 12 T=70 °C, t=3 jam) pada contoh yang telah diberi perlakukan basa pekat (NaOH). Rendemen polisakarida yang dihasilkan dari ela sagu, bagas tebu, dan jerami padi adalah 5, 41, 11%, yang mengandung α-selulosa sebesar 62,53-77,47% dan sisa lignin sebesar 0,81-1,62%. Isolat selulosa dikaji melalui teknik degradasi seperti analisis termal dan teknik non-degradasi seperti spektroskopi FTIR dan mikroskopi elektron pemayaran. Selain itu, juga ditentukan indeks kristalinitas dari masing-masing isolat selulosa. Spektrum FTIR, mikrograf, dan kurva analisis termal menunjukkan bahwa sebagian besar isolat yang dihasilkan adalah selulosa.
Kata kunci: selulosa, isolasi, hidrogen peroksida
Abstract
Cellulose were isolated from sago waste, sugarcane bagasse, and rice staw.
Delignification was carried out by alkaline peroxide method (H2O2 5% pH 12
T=70°C, t=3 jam) after extraction with concentrated alkali (NaOH). The
polysaccharide yields from sago waste, sugarcane baggase, and rice straw were
5, 41, 11%, which contained 62,53-77,47% α-cellulose and 0,81-1,62%
remaining lignin. The cellulose isolates were comparatively studied by both
degradation technique such as thermal analysis and non-degradation techniques
such as FTIR spectroscopy and scanning electron microscopy (SEM), and the
cristallinity index was also comparatively estimated. FTIR spectrum, SEM
micrograph, and thermal analysis curve confirmed that the isolates were
cellulose.
Pendahuluan
Selulosa adalah komponen utama yang terdapat pada jaringan tanaman, yaitu sekitar 30-50% bagian jaringan tanaman. Secara kimia, selulosa adalah polimer alam berantai lurus dari monomer anhidroglukosa yang terikat secara β -1,4-glikosida. Selulosa merupakan komponen utama pada tumbuhan tinggi, seperti kayu, kapas, tebu, serat rami, jerami (Sun et al. 2004a).
Limbah hasil pertanian seperti ela sagu, bagas tebu, dan jerami padi merupakan sumber selulosa yang potensial. Di Indonesia, ketiga limbah pertanian ini dapat ditemukan dalam jumlah yang cukup banyak. Limbah jerami padi mencapai 94,23 juta ton (Kim dan Dale 2004; BPS 2010), ela sagu sebesar 58,08 juta ton (Rumalatu 1981 yang diacu Matitaputty dan Alfons 2006; Papilaya 2009), dan bagas tebu 9,9 juta ton (Direktorat Jenderal Perkebunan 2010). Ketiga jenis limbah pertanian ini belum dimanfaatkan secara optimal. Oleh karena itu, pemanfaatan limbah pertanian berbasis selulosa untuk mendapatkan nilai tambahnya menarik untuk terus dikaji lebih lanjut.
Kebutuhan selulosa sebagai bahan baku potensial yang banyak digunakan di sejumlah industri merupakan daya tarik dalam pengembangan kajian metode isolasinya. Berbagai kajian yang berkaitan dengan teknik isolasi selulosa dari kayu atau bahan organik lainnya terus dikembangkan. Umumnya selulosa ditemukan tidak dalam bentuk murni melainkan berada bersama-sama dengan senyawa lain seperti hemiselulosa dan lignin, oleh karena itu fokus kajian dalam pengembangan metode isolasinya adalah memperoleh metode isolasi yang efektif dan efisien untuk menghilangkan senyawa-senyawa selain selulosa tersebut.
telah digunakan pada tahap isolasi selulosa dari jerami Barley (Sun et al. 2005), jerami gandum (Sun et al. 2004b), dan bagas tebu ( Sun et al. 2004a).
Tahap penelitian ini bertujuan mendapatkan (1) selulosa dari berbagai limbah pertanian, yaitu ela sagu, bagas tebu, dan jerami padi melalui tahap asidifikasi, pulping, dan delignifikasi menggunakan hidrogen peroksida (2) karakteristik isolat selulosa melalui analisis komponen kimia, analisis derajat polimerisasi dengan teknik viskometri, analisis gugus fungsi dengan teknik spektroskopi IR (infrared), analisis morfologi permukaan dengan teknik mikroskopi, analisis kristalinitas dengan teknik difraksi sinar X, dan analisis termal.
Bahan dan Metode Bahan dan Alat
Ela sagu diperoleh dari industri pengolahan sagu di daerah Cimahpar, Bogor. Bagas tebu diperoleh dari pabrik gula tebu Modjo Panggung, Tulungagung, Jawa Timur. Jerami padi diperoleh dari daerah Dramaga, Bogor. Pereaksi yang digunakan di antaranya HCl p.a (E-Merck), H2O2 p.a (E-Merck), pelet NaOH murni (E-Merck). Semua pereaksi langsung dipakai tanpa perlakuan awal terlebih dahulu. Peralatan yang dipakai adalah peralatan gelas, oven, dan peralatan instrumen yang digunakan pada tahap pencirian.
Metode Penelitian Tahap Isolasi
suhu 70 °C sambil diaduk pada kecepatan 1000 rpm selama 3 jam. Selanjutnya, campuran disaring dan dinetralkan dengan akuades. Tahapan ini diulang berturut-turut untuk 3 jam dan 2 jam. Residu hasil perlakuan pada tahap ini adalah holoselulosa ampas sagu (A4). Kemudian contoh A4 ditambahkan larutan NaOH 10%, selanjutnya campuran dimaserasi pada suhu 20 °C selama 10 jam. Campuran disaring dan dinetralkan dengan akuades. Residu yang diperoleh pada tahap ini adalah selulosa ampas sagu (A5).
Isolasi Selulosa Ampas Tebu. Ampas tebu yang telah kering digiling sampai berukuran 100 mesh (B1). Ampas tebu giling selanjutnya dianalisis komponen kimianya. Contoh B1 ditambahkan akuades dan diaduk dengan pengaduk magnet selama 5 menit. Campuran disaring dengan pencucian dilakukan tiga kali kemudian residu dikeringkan pada suhu 50 °C hingga bobotnya konstan. Residu hasil penyaringan tersebut telah bebas dari komponen polisakarida yang larut dalam air (B2). Contoh B2 ditambahkan NaOH 4% dan dipanaskan pada suhu 80 °C selama 4 jam. Campuran kemudian disaring dengan bantuan vakum. Kemudian, residu yang diperoleh dari penyaringan dicuci dengan akuades hingga pH filtratnya tidak berubah dan diperoleh contoh B3 yang selanjutnya dikeringkan pada suhu 50 °C hingga bobotnya konstan. Contoh B3 ditambahkan 500 mL larutan H2O2 5% pH 12 dan dipanaskan dalam penangas air bersuhu 70 °C yang dijaga konstan selama 3 jam kemudian campuran disaring dan endapannya dicuci dengan akuades sampai pH netral. Perlakuan dengan larutan peroksida diulang kembali 2 kali dengan penambahan waktu pemanasan berturut-turut 3 jam dan 2 jam. Setelah itu, campuran disaring dan endapan dicuci hingga pH netral dan dikeringkan dalam oven bersuhu 60 °C. Residu yang diperoleh adalah selulosa bagas tebu (B4).
jerami padi. Sejumlah contoh C2 ditambahkan larutan NaOH 20%, kemudian campuran dipanaskan pada suhu 80 °C selama 2 jam. Campuran disaring dan endapannya dicuci dengan akuades hingga pH filtratnya netral. Residu dikeringkan pada suhu 50 °C hingga bobotnya konstan (C3). Contoh C3 ditambahkan larutan H2O2 5% pH 12 dan dipanaskan dalam penangas air bersuhu 70 °C yang dijaga konstan selama 3 jam kemudian campuran disaring dan endapannya dicuci dengan akuades sampai pH netral. Perlakuan dengan larutan peroksida diulang kembali 2 kali dengan penambahan waktu pemanasan berturut-turut 3 jam dan 2 jam. Setelah itu, campuran disaring dan endapan dicuci hingga pH netral dan dikeringkan dalam oven bersuhu 60 °C. Residu yang diperoleh adalah selulosa jerami padi (C4).
Pencirian
Analisis Komponen Kimia. Analisis komponen kimia dilakukan terhadap bahan baku awal dengan analisis proksimat, seperti karbohidrat, protein, lemak, mineral, dan air dengan mengacu pada metode standar SNI (1992) dan AOAC (2005). Selain itu, komposisi selulosa, hemiselulosa, dan lignin juga ditentukan dengan mengacu pada metode standar TAPPI (1961) pada contoh bahan baku dan isolat selulosa.
Analisis Gugus Fungsi dengan Spektrometer FTIR. Spektra IR isolat selulosa direkam melalui spektrometer FTIR Perkin Elmer Spectrum One menggunakan pelet KBr dari bilangan gelombang 4000 cm-1 sampai 400 cm-1 dengan resolusi 8 cm-1 dan pemayaran 45 x per contoh.
Analisis Morfologi Permukaan dengan Mikroskop Elektron Pemayaran
(Scanning Electron Microscope, SEM). Produk hasil isolat ditempelkan di atas tempat contoh menggunakan perekat elektrokonduktif. Pengamatan morfologi dilakukan pada JEOL 6400 mikroskop elektron dengan tegangan 20 kV.
Analisis Kristalinitas dengan Difraktometer Sinar X. Difraksi sinar X
adalah indeks kristalinitas, I002 adalah intensitas maksimum pada kisi difraksi 002, dan Iam adalah intesitas puncak fasa amorf.
Analisis Termal dengan TG/DTA. Thermogravimetric (TG) dan differential
thermogravimetric analysis (DTA) dilakukan dengan DTG-60H FC-60A
TA-60WS. Suhu yang digunakan mulai 27 sampai 600 °C dengan laju pemanasan 10
°C menit-1.
Hasil dan Pembahasan
Selulosa adalah polisakarida yang jumlahnya paling melimpah di alam. Oleh karena ketersediaannya yang banyak dan bersifat dapat diperbarui serta keteraturan strukturnya, selulosa merupakan polimer alami yang murah dengan sifat fisik dan kimia yang khas. Selulosa dapat diperoleh melalui: (1) pemisahan poliosa utama dan sisa lignin dari holoselulosa, (2) isolasi langsung dari kayu, dan (3) penentuan kandungan selulosa dengan hidrolisis total kayu, holoselulosa atau selulosa alfa diikuti dengan penentuan gula yang dihasilkan (Fengel dan Wegener 1984; Achmadi 1990).
Gambar 17 menyajikan metode isolasi selulosa secara umum (A) dan metode isolasi selulosa yang digunakan dalam penelitian ini (B).
Gambar 17 Metode isolasi selulosa secara umum (A) dan metode isolasi selulosa yang digunakan dalam penelitian ini (B).
Komponen Kimia
Analisis proksimat dilakukan terhadap 3 bahan baku, yaitu ela sagu, bagas tebu, dan jerami padi. Analisis proksimat yang dilakukan meliputi penentuan kadar air, kadar abu, kadar protein, kadar lemak, dan kadar karbohidrat total. Selanjutnya, dilakukan juga analisis komponen kimia seperti kandungan α -selulosa, holo-selulosa, hemi-selulosa, dan lignin. Jumlah kandungan komponen kimia bahan baku awal selanjutnya dibandingkan dengan isolat selulosa yang diperoleh untuk mengevaluasi keberhasilan tahap isolasi. Hasil analisis proksimat dan komponen kimia adalah karakteristik untuk setiap bahan baku.
Ela Sagu. Dari ketiga bahan baku yang digunakan, ela sagu memiliki kadar air yang cukup tinggi, yaitu 10,17% (Lampiran 1). Menurut Silahooy (2006), kadar air ela sagu segar dapat mencapai 18%. Kadar air yang cukup tinggi ini menyebabkan penanganan bahan baku ela sagu menjadi lebih sulit dibandingkan dua bahan baku lainnya. Ela sagu segar tidak dapat langsung disimpan melainkan
A
Sumber Lignoselulosa
Holoselulosa + Lignin
Holoselulosa
Selulosa
Delipifikasi dengan pelarut
Delignifikasi dengan CH3COOH/NaClO2
Penghilangan hemiselulosa dengan NaOH pekat
B
Sumber Lignoselulosa
Holoselulosa + Lignin
Selulosa + Lignin
Selulosa
Delipifikasi dengan pelarut
Penghilangan hemiselulosa dengan NaOH pekat
harus segera dikeringkan sesaat setelah dilakukan pengambilan contoh karena ela sagu akan mudah menjadi media tumbuh jamur atau mikroorganisme. Berdasarkan komposisi komponen kimia, ela sagu memiliki komposisi komponen kimia yang paling kecil jika dibandingkan dari ketiga bahan baku yang digunakan (Gambar 18). Ela sagu memiliki kandungan selulosa alfa sebesar 22,45% dan lignin 11,52%. Ela sagu memiliki kandungan pati cukup besar, yaitu 47,03% (selisih kandungan karbohidrat total dan holoselulosa). Kandungan pati yang cukup besar ini menunjukkan bahwa proses ekstraksi pati sagu yang dilakukan di tempat pengambilan contoh masih belum efektif. Kandungan pati yang cukup besar ini menjadi pertimbangan khusus pada tahap awal isolasi selulosa dari ela sagu. Pemanfaatan air panas (ASTM D 1110-56) yang semula digunakan untuk menghilangkan polisakarida pati menjadi tidak efektif dan tidak efisien karena untuk mendapatkan preparat ela sagu yang bebas pati membutuhkan air panas dalam jumlah yang cukup besar dan waktu yang lama. Oleh karena itu, pada tahap awal isolasi pada ela sagu digunakan larutan asam encer untuk menghidrolisis pati tersebut. Selain dapat menghidrolisis pati, perlakuan dengan asam dapat juga digunakan untuk menghidrolisis hemiselulosa menjadi mono atau oligosakarida yang dapat larut sehingga lebih mudah untuk diekstraksi (Zhang et al. 2010).
Bagas Tebu. Berdasarkan kandungan komponen kimia bahan baku
(Gambar 18), bagas tebu memiliki kandungan selulosa alfa yang paling tinggi (43,06%), selanjutnya diikuti oleh jerami padi dan ela sagu. Kandungan selulosa alfa yang tinggi menjadikan bagas tebu sebagai sumber selulosa yang potensial. Namun demikian, kandungan lignin pada bagas tebu juga relatif tinggi. Hal ini menjadi pertimbangan khusus pada tahap penghilangan senyawa lignin untuk mendapatkan selulosa dari bagas tebu. Dalam penelitian ini, penghilangan senyawa lignin pada isolasi selulosa dari bagas tebu menggunakan larutan H2O2 5%. Konsentrasi H2O2 yang digunakan ini lebih tinggi dari yang telah digunakan oleh Sun et al. (2004a).
selulosa dari jerami padi. Perlakuan dengan asam encer pada tahap awal isolasi selulosa dari jerami padi bertujuan melarutkan mineral yang terkandung di dalamnya. Kandungan lignin yang mencapai 32,07% pada jerami padi menyebabkan tahap penghilangan lignin dilakukan secara berulang menggunakan larutan H2O2 5%. Konsentrasi H2O2 yang digunakan ini mengacu pada tahap delignifikasi bagas tebu dengan pertimbangan bahwa kandungan lignin jerami padi yang juga cukup tinggi.
Gambar 18 Komposisi kimia bahan baku.
Evaluasi Keberhasilan Tahap Isolasi
Dari berbagai metode isolasi yang telah dilaporkan selama ini, untuk mendapatkan selulosa dalam bentuk murni sangat sulit dilakukan. Oleh karena itu, selulosa yang diperoleh adalah selulosa dalam bahan kasar (crude) berupa selulosa alfa (α-selulosa), yaitu selulosa yang tidak larut dalam larutan NaOH pekat. Evaluasi keberhasilan tahap isolasi dalam penelitian ini dapat dilihat dari rendemen hasil isolat, peningkatan kandungan α-selulosa, dan penurunan kadar lignin.
Rendemen Polisakarida. Rerata rendemen untuk ketiga bahan baku sangat
bervariasi (Tabel 3). Jumlah rendemen polisakarida yang dihasilkan bergantung pada komposisi awal dari bahan baku dan perlakuan yang diberikan selama tahap isolasi. Rerata rendemen dalam penelitian ini dihitung berdasarkan bobot kering dari bahan baku awal sebelum diberi perlakuan. Dari hasil penelitian, rerata
0
Karbohidrat Selulosa alfa Hem iselulosa Lignin
rendemen polisakarida tertinggi dihasilkan oleh bagas tebu, yaitu mencapai 41%. Sun et al. (2004a) juga melaporkan rerata rendemen polisakarida yang diperoleh dari bagas tebu, yaitu sekitar 40%. Sementara itu, rerata rendemen polisakarida yang dihasilkan dari jerami padi pada penelitian ini (11%) lebih tinggi dari yang dilaporkan oleh Sun et al. (2000), yaitu 6,5%. Rerata rendemen polisakarida terendah dihasilkan oleh ela sagu (5%). Hal ini disebabkan tingginya kandungan pati pada bahan baku awal (47,03%), sehingga terjadi kehilangan bobot yang cukup besar pada tahap penghilangan pati, yaitu sekitar 80% dari bobot kering bahan baku awalnya. Sampai saat ini, belum ditemukan kajian terkait isolasi selulosa dari ela sagu sehingga rendemen polisakarida yang diperoleh dalam penelitian ini belum dapat dibandingkan dengan hasil penelitian dari peneliti lain.
Tabel 3 Kondisi isolasi dan rendemen polisakarida Bahan
Baku
Kondisi Isolasi Rendemen
(%)
lignin bahan baku awal (22,28%). Sementara itu, kandungan lignin pada jerami padi berhasil berkurang hampir 97% dari kandungan lignin awal, yaitu dari 32,07% menjadi 0,81%. Komposisi selulosa alfa dan lignin berturut-turut disajikan pada Gambar 19 dan 20.
0
Ela Sagu Bagas Tebu Jerami Padi
Bahan Baku Isolat Selulosa
Gambar 19 Komposisi selulosa alfa.
0
Ela Sagu Bagas tebu Jerami Padi
Bahan Baku Isolat Selulosa
Gambar 20 Komposisi lignin
Delignifikasi