DAYA
TAHAN
HIDUP
NYAMUK
Aedes
aegypti
(Linn)
S
ETELAH
TERPAPAR
TEMEFOS
PADA
FASE
LARVA
YULIDAR
SEKOLAH
PASCASARJANA
INSTITUT
PERTANIAN
BOGOR
PERNYATAAN
MENGENAI
TESIS
DAN
SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa tesis Daya tahan hidup nyamuk Aedes aegypti (Linn) setelah terpapar temefos pada fase larva adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
ABSTRACT
YULIDAR. The survival of Aedes aegypti (Linn) after exposure of temephos at
larval stage. Dwi Jayanti Gunandini and Singgih H. Sigit
The purpose of this research was to find out the effect of exposure to concentration of temephos upon the survival of Ae. aegypti. The temephos concentration used KL0 : 0,180 mg/liter, KL25 : 0,285 mg/liter, KL50 : 0,330
mg/liter, KL75 : 0,384 mg/liter; KL90: 0,433 mg/liter and control. The data were
analyzed using descriptif, probit analysis and analysis of variance, if there were significant differences followed by Tuckey's mean test. The results show that the larvae and eggs abnormality, larvae activity decreased, while the larvae and pupae longevity were increased, but the lifespan of the adult stage become shorter. The adult stage fecundity decreased as well as the number of egg batches, however hatchability, ecdicis and eclotion also decreased. The adult female emergences was less than male after treated by temephos.
RINGKASAN
Yulidar. Daya tahan hidup nyamuk Aedes aegypti (Linn) setelah terpapar
temefos pada fase larva. Dibimbing oleh Dwi Jayanti Gunandini dan Singgih
H. Sigit.
Penyakit demam berdarah dengue (DBD) merupakan masalah cukup besar yang menyangkut kesehatan masyarakat di negara beriklim tropis dan sub tropis. Aedes aegypti merupakan vektor utama penyakit tersebut, oleh karena itu pengendalian Ae. aegypti dengan sanitasi lingkungan yang bertujuan untuk mengurangi habitat larva merupakan kunci strategi program pengendalian vektor. Penggunaan larvasida untuk mengendalikan populasi nyamuk Ae. aegypti sebagai vektor penyakit DBD adalah cara yang paling umum digunakan oleh masyarakat. Larvasida yang digunakan di Indonesia sejak tahun 1976 adalah temefos. Pada tahun 1980, temefos ditetapkan sebagai larvasida dalam program pengendalian masal larva Ae. aegypti (Depkes, 2005). Mengingat masa penggunaan temefos telah lebih dari tiga dasa warsa, maka perlu dipelajari pengaruh temefos terhadap daya tahan hidup nyamuk Ae. aegypti bila terpapar dengan insektisida tersebut. Penelitian dilaksanakan di Laboratorium Entomologi Kesehatan Fakultas Kedokteran Hewan Institut Pertanian Bogor (PEK-FKH IPB), Bogor. Penelitian ini berlangsung sejak bulan November 2010 sampai dengan Juni 2011 dalam empat tahap : (1) tahap persiapan yaitu pemeliharaan dan perbanyakan Ae. aegypti, (2) tahap penelitian pendahuluan yaitu penetapan konsentrasi uji, (3) tahap penelitian utama yaitu pemaparan konsentrasi uji, pengamatan dan pengumpulan data, serta (4) analisis & penyajian data. Tahap persiapan merupakan tahap perbanyakan Ae. aegypti secara massal di insektarium. Pemeliharaan dan perbanyakan Ae. aegypti dilakukan selama satu bulan sampai dihasilkan koloni Ae. aegypti dewasa dan pradewasa dengan jumlah yang mencukupi untuk penelitian. Tahap penelitian pendahuluan dilakukan untuk menentukan konsentrasi temefos yang akan digunakan. Tahap penelitian utama merupakan tahap pemaparan konsentrasi temefos KL0, KL25, KL50, KL75, dan
KL90 dibandingkan dengan kontrol yang dipaparkan pada larva instar 3 (L3).
Konsentrasi temefos yang digunakan adalah 0 mg/liter (Kontrol ); 0,180 mg/liter (KL0); 0,285 mg/liter (KL25); 0,330 mg/liter (KL50); 0,384 mg/liter (KL75), dan
0,433 (KL90). Setelah dipaparkan dengan temefos larva dipindahkan ke media air,
abnormalitas bentuk telur dan larva, aktivitas gerak larva untuk menempuh jarak sejauh 30 cm semakin lambat. Fenomena trade-off energi yang dilakukan oleh nyamuk Ae. aegypti jangka hidup pradewasa (larva dan pupa) yang semakin lambat sedangkan jangka hidup dewasa (jantan dan betina) yang semakin pendek, ukuran tubuh yang lebih kecil dibandingkan dengan normal sehingga berat badan menyebabkan penurunan berat badan stadium pradewasa dan stadiumdewasa. Pemaparan temefos pada nyamuk Ae. aegypti tahap larva juga menyebabkan penurunan jumlah telur dan kelompok telur, penurunan persentase daya tetas telur, penurunan persentase ekdisis dan eklosi, serta ratio kelamin jantan yang lebih banyak dibandingkan dengan betina pada keturunannya.
Hak Cipta milik IPB, tahun 2012 Hak Cipta dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan kepentingan yang wajar IPB.
DAYA
TAHAN
NYAMUK
AEDES
AEGYPTI
(Linn)
SETELAH
TERPAPAR
TEMEFOS
PADA
FASE
LARVA
YULIDAR
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Parasitologi dan Entomologi Kesehatan
SEKOLAH
PASCASARJANA
INSTITUT
PERTANIAN
BOGOR
Judul Tesis
: Daya Tahan Hidup Nyamuk Aedes aegypti (Linn) Setelah Terpapar Temefos Pada Fase Larva
Nama : Yulidar
NIM : B252090061
Disetujui, Komisi Pembimbing
DR. Drh. Dwi Jayanti Gunandini, M.Si Prof. drh. Singgih H. Sigit, M.Sc., PhD
Ketua Anggota
Diketahui,
Ketua Program Studi/Mayor Dekan Sekolah Pascasarjana Parasitologi dan Entomologi
Kesehatan
drh. Upik Kesumawati Hadi, MS., Ph.D Dr. Ir. Dahrul Syah, M.ScAgr
PRAKATA
Rasa syukur yang tak terhingga penulis panjatkan Ke-hadirat ALLAH SWT karena tanpa ridha dan kehendak-NYA tidak mungkin penulis bisa mneyelesaikan pendidikan ini dan selawat beserta salam penulis panjatkan ke pangkuan Nabi Besar Muhammad SAW.
Ucapan terimakasih kepada Dr. Drh. Dwi Jayanti Gunandini, M.Si sebagai ketua pembimbing dan Prof. drh. Singgih H. Sigit, M.Sc., PhD sebagai anggota pembimbing dalam penelitian atas segala saran, pengarahan, bimbingan dan nasihat sejak dari penyusunan proposal, selama penelitian sampai selesainya tahap penulisan tesis ini.
Terimakasih juga penulis sampaikan kepada Keluarga Besar Bagian Parasitologi dan Entomologi Kesehatan (PEK)-FKH IPB yang telah membimbing saya untuk mempelajari entomologi kesehatan, teman-teman pascasarjana PEK angkatan 2009, Keluarga Besar LokaLitbang Biomedis Aceh atas saran dan motivasinya, Badan LitbangKes Jakarta yang telah membiayai pendidikan saya dan Keluarga Besar Ikatan Mahasiswa Pascasarjana Aceh-IKAMAPA yang selalu meramaikan tahap-tahap penyelesaian tesis ini.
Dan akhir kata, ucapan rindu dan terimakasihku untuk Ibuku, Ibu Zubaidah H. Hamid dan Bapak M. Yacob Puteh (alm)...(tiada kata)....serta Kakakku Yusniar Yacob, Yusadi Yacob dan adindaku Yulia Yacob yang selalu mengingatkan untuk segera menyelesaikan pendidikan pascasarjana ini.
RIWAYAT
Penulis dilahirkan tanggal 16 september 1978 di Bireuen-Aceh, anak ketiga dari empat bersaudara, Yusniar Yacob, Yusadi Yacob, Yulidar Yacob, dan Yulia Yacob dari Ibu Zubaidah Hamid dan Bapak M.Yacob Puteh (alm). Pendidikan dasar di SDN No 8 Bireuen tamat tahun 1991, SMPN No 1 Bireuen tamat tahun 1994, SMAN No 2 Bireuen tamat tahun 1997 dan kuliah di MIPA Biologi UNSYIAH Banda Aceh selesai tahun 2002. Program Parasitologi dan Entomologi Kesehatan (PEK) Pascasarjana IPB tahun 2009. Sejak tahun 2006 sampai dengan sekarang bekerja di Badan Penelitian dan Pengembangan Biomedis Kementrian Kesehatan-Aceh.
Wassalam
DAFTAR
ISI
Halaman
DAFTAR TABEL --- xiv
DAFTAR GAMBAR --- xv
DAFTAR LAMPIRAN --- xvi
1 PENDAHULUAN --- 1
1.1 Latar Belakang --- 1
1.2 Perumusan Masalah --- 2
1.3 Tujuan Penelitian --- 2
1.4 Manfaat Penelitian --- 2
2 TINJAUAN PUSTAKA --- 3
2.1 Kemampuan dan Plastisitas Fenotip Serangga --- 3
2.2 Temefos --- 4
2.3 Pengaruh Cekaman Insektisida Terhadap Daya Tahan Serangga --- 5
3 BAHAN DAN METODE KERJA --- 11
3.1 Lokasi dan Waktu Penelitian --- 11
3.2 Cara Kerja --- 11
3.3 Alur Penelitian --- 20
3.4 Analisa Data --- 21
4 HASIL DAN PEMBAHASAN --- 22
4.1 Abnormalitas Bentuk Larva dan Telur Ae. aegypti --- 22
4.2 Aktivitas Gerak Larva Nyamuk Ae. aegypti --- 26
4.3 Jangka Nyamuk Ae. aegypti --- 28
4.4 Berat Badan Nyamuk Ae. aegypti --- 32
4.5 Jumlah Telur dan Kelompok Telur Selama Nyamuk Betina Ae. aegypti --- 36
4.6 Daya Tetas Telur Nyamuk Ae. aegypti --- 40
4.7 Kemampuan Ekdisis dan Eklosi Nyamuk Ae. aegypti --- 42
4.8 Ratio Kelamin Jantan dan Betina Nyamuk Ae. aegypti --- 45
4.9 Pembahasan Umum --- 46
5 KESIMPULAN --- 53
DAFTAR PUSTAKA--- 54
DAFTAR TABEL
Tabel Halaman
1. Jumlah pakan nyamuk Ae. aegypti yang disesuaikan dengan
perkembangan instar --- 12 2. Konsentrasi temefos yang diuji --- 15 3. Rata-rata waktu tempuh larva Ae. aegypti sejauh 30 cm setelah
terpapar temefos --- 27 4. Rata-rata jangka pradewasa nyamuk Ae. aegypti setelah terpapar
temefos --- 29 5. Rata-rata jangka dewasa nyamuk Ae. aegypti setelah terpapar
temefos --- 30 6. Rata-rata berat basah dan berat kering pradewasa nyamuk Ae.
aegypti setelah terpapar temefos --- 32 7. Rata-rata berat basah dan berat kering nyamuk Ae. aegypti dewasa
setelah terpapar temefos --- 34 8. Rata-rata jumlah telur dan kelompok telur selama hidup nyamuk
Ae. aegypti betina setelah terpapar temefos --- 37 9. Rata-rata persentase daya tetas telur Ae. aegypti setelah terpapar
temefos --- 40 10. Rata-rata kemampuan ekdisis dan eklosi nyamuk Ae. aegypti
setelah terpapar temefos --- 42 11. Rata-rata persentase ratio kelamin nyamuk Ae. aegypti setelah
terpapar temefos --- 45 12. Jangka hidup larva Ae. aegypti setelah terpapar temefos --- 47 13. Berat badan nyamuk Ae. aegypti detelah terpapar temefos pada
fase L3 --- 49
14. Fekunditas nyamuk Ae. aegypti setelah terpapar temefos pada
DAFTAR GAMBAR
Gambar Halaman
1. Struktur kimia temefos --- 4
2. Kandang tempat pemeliharaan dan perbanyakan Ae. aegypti --- 12
3. Pemberian pakan darah --- 13
4. Ovitrap --- 13
5. Kemasan temefos --- 14
6. Regresi konsentrasi temefos yang diuji --- 15
7. Pipa paralon yang dibelah memanjang --- 17
8. Kandang perlakuan --- 17
9. Wadah tempat penetasan telur untuk pengamatan daya tetas telur dan ekdisis --- 19
10. Wadah tempat pemeliharaan pupa eklosi dan ratio kelamin --- 20
11. Bagan alur penelitian --- 20
12. Abnormalitas morfologi telur Ae. aegypti setelah terpapar temefos dibandngkan dengan kontrol --- 22
13. Abnormalitas morfologi larva Ae. aegypti setelah terpapar temefos dibandingkan dengan kontrol --- 24
14. Rata-rata waktu tempuh larva (L3) nyamuk Ae. aegypti sejauh 30 cm setelah terpapar temefos --- 27
15. Rata-rata jangka pradewasa nyamuk Ae. aegypti setelah terpapar temefos --- 29
16. Rata-rata jangka hidup nyamuk dewasa Ae. aegypti (jantan dan betina) setelah terpapar temefos--- 30
17. Rata-rata berat basah dan berat kering larva nyamuk Ae. aegypti setelah terpapar temefos --- 33
18. Rata-rata berat basah dan berat kering pupa nyamuk Ae. aegypti setelah terpapar temefos --- 33
19. Rata-rata berat basah dan berat kering nyamuk jantan Ae. aegypti setelah terpapar temefos --- 34
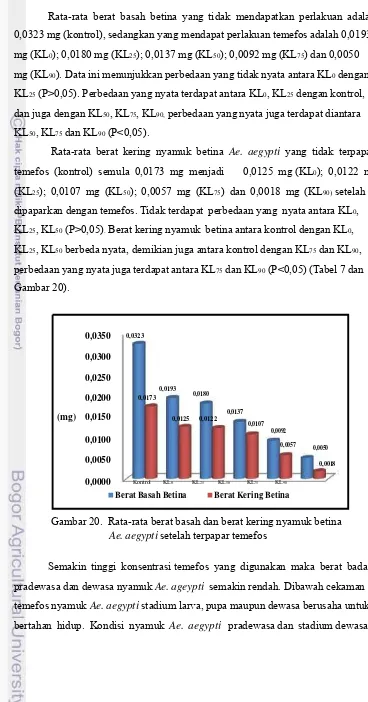
20. Rata-rata berat basah dan berat kering nyamuk betina Ae. aegypti setelah terpapar temefos --- 35
21. Rata-rata jumlah telur/ekor nyamuk betina Ae. aegypti setelah terpapar temefos --- 37
22. Rata-rata jumlah kelompok telur/ekor nyamuk betina Ae.aegypti setelah terpapar temefos --- 38
23. Rata-rata persentase daya tetas telur nyamuk Ae. aegypti setelah terpapar temefos --- 41
24. Rata-rata kemampuan ekdisis nyamuk Ae. aegypti setelah terpapar temefos--- 43
25. Rata-rata kemampuan eklosi nyamuk Ae. aegypti setelah terpapar temefos --- 44
DAFTAR
LAMPIRAN
Lampiran
Halaman
Lampiran 1. Penetapan Konsentrasi Uji --- 58
Lampiran 2. Aktivitas Gerak Larva Nyamuk Ae. aegypti --- 60
Lampiran 3. Jangka Nyamuk Ae. aegypti --- 61
Lampiran 4. Berat Badan Nyamuk Ae. aegypti --- 65
Lampiran 5. Jumlah Telur dan Kelompok Telur Ae. aegypti --- 67
Lampiran 6. Daya Tetas Telur Nyamuk Ae. aegypti --- 70
1
PENDAHULUAN
1.1
Latar
Belakang
Penyakit demam berdarah dengue (DBD) merupakan masalah cukup besar yang menyangkut kesehatan masyarakat di negara beriklim tropis dan sub tropis. Aedes aegypti merupakan vektor utama penyakit tersebut, oleh karena itu pengendalian Ae. aegypti dengan sanitasi lingkungan yang bertujuan untuk mengurangi habitat larva merupakan kunci strategi program pengendalian vektor. Penggunaan insektisida sebagai larvasida adalah cara yang paling umum digunakan oleh masyarakat untuk mengendalikan larva Ae. aegypti. Larvasida yang digunakan di Indonesia adalah temefos yang termasuk dalam golongan organofosfat.
Penggunaan temefos di Indonesia untuk mengendalikan larva Ae. aegypti sudah digunakan sejak tahun 1976, kemudian pada tahun 1980 temefos ditetapkan sebagai larvasida dalam program pengendalian masal larva Ae. aegypti (Depkes, 2005). Temefos merupakan insektisida organofosfat non sistemik yang dapat digunakan dengan cara ditabur di bak mandi, tempayan atau tempat-tempat penampungan air rumah tangga. Temefos tersedia dalam bentuk emulsi, serbuk (wettable powder) dan bentuk granul. Senyawa murni temefos berupa kristal putih padat dengan titik lebur 30-30,50C (EPA, 2009). Penetrasi temefos dengan
konsentrasi efektif ke dalam tubuh larva dapat diabsorpsi dalam waktu 1-24 jam setelah perlakuan, dengan efek residu masih efektif dalam wadah yang tidak pernah dibersihkan selama 15 minggu sampai 5 bulan (Matsumura, 1975; Chen & Lee, 2006; Tavara et al. 2005).
organik pada serangga diikuti oleh kegelisahan, hipereksitasi, tremor, konvulsi dan kemudian kelumpuhan otot (Matsumura, 1997).
Setiap organisme memiliki kemampuan untuk mempertahankan diri dan keturunannya walaupun hidup pada lingkungan yang tidak optimal dibawah cekaman insektisida (Schneider, 2011). Menurut Uvarov (1961) setiap organisme memiliki kemampuan untuk menyesuaikan diri melalui perubahan fisiologis dan kemampuan adaptasi dengan lingkungan yang sifatnya reversibel, keadaan demikian memberikan pengaruh yang besar terhadap dinamika populasi.
Penelitian ini dilakukan untuk mengetahui daya tahan hidup nyamuk Ae. aegypti dalam mempertahankan diri dan keturunannya setelah dipaparkan temefos pada fase larva instar 3 (L3).
1.
2.
Perumusan
Masalah
Temefos telah digunakan lebih dari 30 tahun (sejak tahun 1976) dalam pengendalian larva Ae. aegypti, untuk itu perlu dipelajari pengaruh cekaman insektisida temefos terhadap daya tahan hidup nyamuk Ae. aegypti.
1.
3.
Tujuan
Penelitian
Penelitian ini bertujuan untuk mengetahui daya tahan hidup nyamuk Ae. aegypti dibawah cekaman temefos yang dipaparkan pada fase larva instar 3 (L3).
.
1.
4.
Manfaat
Penelitian
2
TINJAUAN PUSTAKA
2.1
Kemampuan
Hidup
dan
Plastisitas
Fenotip
Serangga
Serangga dengan daur hidup yang kompleks memiliki kemampuan adaptasi yang lebih tinggi terhadap lingkungannya dibandingkan dengan serangga yang dalam siklus hidupnya tidak kompleks. Ae. aegypti adalah serangga dengan daur hidup yang kompleks sehingga memiliki adaptasi yang tinggi dalam mempertahankan hidupnya. Nyamuk ini dapat hidup dan bertelur dalam habitat yang kecil, minim sumber nutrisi, suhu yang kurang optimum dan cekaman dari luar (Hoffmann & Hercus, 2000; Badvaev, 2005).
Kelenturan organisme untuk menyesuaikan diri terhadap lingkungan menunjukkan adanya kelenturan sifat yang dimiliki sebagai hasil interaksi dengan lingkungan, kelenturan ini dikenal dengan istilah plastisitas fenotip. Suatu hubungan antara dua sifat yang dimiliki satu individu karena sesuatu hal dapat menyebabkan sifat yang satu mengalami peningkatan sedangkan sifat yang lain mengalami penurunan, hal ini karena jumlah energi yang digunakan sangat terbatas, peristiwa ini dikenal dengan istilah “trade-off” (Begon et al. 1996). Peristiwa “trade-off” terjadi akibat peningkatan cekaman karena perubahan lingkungan misalnya ketersediaan nutrisi, adanya predator, kompetisi dan paparan insektisida (Agnew et al. 2000; Bedhomme et al. 2003; Schneider et al. 2011).
Fenomena trade off yang ditampakkan oleh nyamuk Ae. aegypti untuk mempertahankan hidupnya dibawah cekaman insektisida antara lain adalah dengan mengalami perubahan ukuran tubuh dan sayap, jumlah betina menjadi lebih sedikit dalam populasi serta proses pupasi menjadi lebih lambat akibat kekurangan energi (Yan et al. 1998; Koella & Offenberg, 1999).
Gunandini (2002) menyatakan bahwa Ae. aegypti yang diseleksi pada stadium larva dengan malation sampai generasi ke-20 memperlihatkan perubahan pada daur hidupnya sebagai suatu usaha untuk beradaptasi dibawah cekaman insektisida. Perubahan daur hidup yang terjadi yaitu stadium pradewasa semakin lambat sebaliknya stadium dewasa semakin singkat, sedangkan ratio kelamin jantan menjadi lebih besar dibanding kelamin betina. Kemampuan nyamuk Ae. aegypti untuk beradaptasi terhadap malation ditunjukkan dengan jumlah kelompok telur, jumlah telur dan daya tetas telur yang tidak berubah.
2.2
Temefos
Temefos merupakan larvasida golongan organofosfat yang sedikit beracun (toksisitas kelas III) sehingga dapat digunakan secara umum (EPA, 2009). Penggunaannya pada tempat penampungan air minum telah dinyatakan aman oleh WHO, dapat digunakan di bak mandi serta tempat penampungan air rumah tangga (DepKes RI, 2005) selain itu temefos juga dapat digunakan untuk membasmi kutu pada anjing, kucing dan manusia (EPA, 2009).
Gambar 1. Struktur kimia temefos
Temefos tersedia dalam bentuk emulsi, serbuk (Wettable powder) dan bentuk granul. Senyawa murni temefos berupa kristal putih padat dengan titik lebur 30-30,50C. Produk komersial temefos berupa cairan kental berwarna coklat,
tidak larut dalam air pada suhu 200C dan heksana, tetapi larut dalam aseton,
2.2.1 Cara kerja temefos
Temefos bekerja dengan cara menghambat enzim kolinesterase, sehingga menimbulkan gangguan pada aktivitas syaraf akibat tertimbunnya asetilkolin pada ujung syaraf. Keracunan fosfat organik pada serangga diikuti oleh gelisah, hipereksitasi, tremor dan konvulsi, kemudian kelumpuhan otot (paralise). Penetrasi temefos ke dalam tubuh larva Ae. aegypti berlangsung cepat karena dapat mengabsorpsi lebih dari 99% temefos dalam waktu 24 jam. Setelah diabsorpsi, temefos diubah menjadi produk-produk metabolik, sebagian dari produk metabolik tersebut diekskresikan melalui air (Matsumura, 1997).
Menurut Thavara et al. (2005), saat ini konsentrasi efektif temefos yang dianjurkan di Thailand 1 gr/200 liter air untuk wadah yang gelap dan 2-5 gr/200 liter air untuk wadah yang terang, hal ini berkaitan dengan efek temefos yang rendah bila terdegradasi dengan sinar matahari. Di Indonesia sendiri konsentrasi temefos yang dianjurkan untuk membunuh larva Ae. aegypti dalam air minum adalah 10 gr/100 liter air dalam wadah yang terlindungi oleh sinar matahari (DepKes RI, 2005).
Temefos relatif aman dan tidak menimbulkan gangguan kesehatan pada manusia, meskipun demikian konsentrasi tinggi temefos dapat menimbulkan overstimulasi sistem syaraf. Pada pajanan yang sangat tinggi temefos dapat menyebabkan paralise nafas dan kematian (Matsumura, 1978). Reyes-Villanueva et al. (1990 & 1992) menyatakan bahwa konsentrasi temefos sebesar 0,009 mg/liter; 0,013 mg/liter; 0,015 mg/liter; 0,016 mg/liter; 0,020 mg/liter dan 0,025 mg/liter dapat mengakibatkan penurunan kesuburan (fecundity) dan memperlambat jangka hidup (longevity) Ae. aegypti. Taviv (2005) menyatakan bahwa temefos masih sangat efektif untuk pengendalian larva Ae. aegypti dengan KL50 : 0,28 mg/100 liter dan KL90: 0,79 mg/100 liter.
2.3
Pengaruh
Cekaman
Insektisida
Terhadap
Daya
Tahan
Hidup
Serangga
kehidupan secara normal dialihkan penggunaannya untuk beradaptasi di bawah cekaman insektisida (Sibly & Calow, 1988 dalam Gunandini, 2002).
Setiap organisme memiliki kemampuan untuk tetap hidup dan mempertahankan kesuksesan keturunannya walaupun hidup pada lingkungan yang tidak optimal di bawah cekaman insektisida (Schneider et al. 2011). Kehidupan bukanlah hal yang kaku sehingga suatu kelenturan (plastisitas) dapat terjadi akibat interaksi individu dengan lingkungannya. Termasuk di dalam kerangka plastisitas fenotip adalah kelenturan dalam skala waktu (Begon et al. 1996).
Fenomena yang ditunjukkan oleh nyamuk Ae. aegypti dalam mempertahankan diri dan keturunan akibat cekaman insektisida organofosfat telah dilaporkan oleh Reyes-Villanueva et al. (1990 & 1992) dan Gunandini (2002). Cekaman insektisida pada nyamuk ini mengakibatkan antara lain penurunan kesuburan (fecundity) dan menyebabkan jangka hidup (longevity) stadium pradewasa semakin panjang serta stadium dewasa semakin pendek.
2.3.1 Jangka Hidup Nyamuk Ae. aegypti
Pengaruh insektisida terhadap jangka hidup pradewasa nyamuk Ae. aegypti yang dipaparkan dengan temefos pada stadium larva instar 3 (L3)
mengakibatkan rata-rata jangka hidup larva menjadi lebih panjang, dari semula 32,1 hari (kontrol) menjadi 36,6 hari (0,016 ppm); 37,0 hari (0,020 ppm) dan 34,3 hari (0,025 ppm) (Reyes-Villanueva et al. (1992). Penelitian Gunandini (2002) juga membuktikan bahwa masa pertumbuhan larva Ae. aegypti menjadi lebih lambat setelah diseleksi malation. Rata-rata jangka hidup larva 5,46 hari (F0)
menjadi 5,63 hari (F5); 6,06 hari (F10); 6,58 hari (F15) dan 6,64 hari (F20).
Fenomena yang sama juga dilaporkan oleh Sudjatmiko (2002), pemaparan insektisida BPMC (golongan karbamat) pada larva Anopheles aconitus menunjukkan jangka hidup larva menjadi lebih panjang dari 3,147 hari (KL0)
menjadi 4,113 hari (KL30).
yang semula 25,9 hari (0 ppm) menjadi 28,7 hari (0,016 ppm); 32,4 hari (0,020 ppm) dan 30,93 hari (0,025 ppm. Larva Ae. aegypti yang telah diseleksi dengan malation juga menunjukkan jangka hidup pupa yang lebih lambat dari normal. Jangka hidup pupa yang semula 2,10 hari (F0) menjadi 2,26 hari (F5); 2,33 hari
(F10); 2,34 hari (F15) dan 2,39 (F20) (Gunandini, 2002).
Malation mempengaruhi jangka hidup nyamuk Ae. aegypti jantan. Di bawah cekaman insektisida ini nyamuk Ae. aegypti jantan akan memperpendek jangka hidupnya. Gunandini (2002) melaporkan bahwa jangka hidup nyamuk jantan dari awalnya 18,88 hari (F0) menjadi 17,53 hari (F5); 13,93 hari (F10);
13,67 hari (F15) dan 9,83 hari (F20). Hal yang sama juga dilaporkan oleh Antonio
et al. (2009), insektisida spinosad 0,06 mg/l yang dicampur dengan dengan sukrosa 10% diberikan secara ad-libitum selama 1x24 jam mengakibatkan perubahan jangka hidup jantan yang lebih singkat yaitu semula 40,2 hari menjadi 38,1 hari.
Pengaruh insektisida terhadap jangka hidup nyamuk Ae. aegypti betina juga dilaporkan oleh Gunandini (2002). Seleksi malation menyebabkan jangka hidup nyamuk Ae. aegypti betina semakin lambat, jangka hidup Ae. aegypti betina berubah dari 34,53 hari (F0) menjadi 30,42 hari (F5); 21,85 hari (F10); 19,20 hari
(F15) dan 14,35 hari (F20).
2.3.2 Berat Badan Nyamuk Ae. aegypti
organisme sebagai kompensasi dari mempertahankan hidup dan keturunannnya (Schneider et al. 2011).
Peningkatan berat badan pada serangga ternyata bisa juga terjadi akibat penggunaan insektisida. Sujatmiko (2002) melaporkan bahwa penggunaan insektisida BPMC konsentrasi 0,071 ppm (KL10); 0,0963 ppm (KL20) dan 0,113
ppm (KL30) pada larva instar 2 (L2) mengakibatkan peningkatan berat badan
nyamuk Anopheles aconitus. Berat basahnya semula 0,443 mg (0 ppm) menjadi 0,497 mg (KL10); 0,557 mg (KL20) dan 0,490 mg (KL30), sedangkan berat kering
semula 0,417 mg (kontrol) menjadi 0,460 mg (KL10); 0,503 mg (KL20) dan 0,477
mg (KL30). Pada nyamuk betina, berat basah semula 0,117 mg (kontrol) menjadi
0,130 mg (KL10); 0,143 mg (KL20) dan 0,140 mg (KL30), sedangkan berat kering
betina dari 0,130 mg (0 ppm) menjadi 0,153 mg (KL10); 0,163 mg (KL20); 0,147
mg (KL30).
2.3.3 Jumlah Telur dan Kelompok Telur Nyamuk Ae. aegypti
Setiap organisme berusaha untuk tetap hidup dan mempertahankan diri dengan meneruskan keturunannya, walaupun hidup pada lingkungan yang tidak optimal di bawah cekaman insektisida (Schneider et al. 2011).
Nyamuk Ae. aegypti betina yang dipaparkan malation menjadi lebih singkat hidupnya sehingga jumlah telur dan kelompok telur yang dihasilkan selama hidup betina menjadi lebih sedikit. Peningkatan jumlah telur terjadi pada tahap awal, kemudian pada tahap selanjutnya jumlah telur cenderung menurun. Nyamuk Ae. aegypti yang diseleksi oleh insektisida malation menghasilkan telur rata-rata 117,65 butir (F0) menjadi 139,05 butir (F5); 133,02 butir (F10); 89,88
butir (F15) dan 78,33 butir (F20). Rata-rata jumlah kelompok telur 6,83 batch (F0);
6,49 batch (F5); 4,85 batch (F10); 3,57 batch (F15) dan 2,04 batch (F20)
(Gunandini, 2002).
(2007) menggunakan insektisida nabati spinosad pada Ae. aegypti gravid. Rata- rata jumlah telur yang dihasilkan adalah 274,4 butir (kontrol) menjadi 245,6 butir (5 ppm) dan 241,8 butir (20 ppm). Kumar et al. (2009) menyatakan bahwa Ae. aegypti menunjukkan penurunan jumlah telur, semula 99 butir (kontrol) menjadi 91 butir (F20) dan 64 butir (F40).
2.3.4 Penurunan Daya Tetas Telur Nyamuk Ae. aegypti
Efek pemberian insektisida deltamethrin terhadap nyamuk Ae. aegypti yang dipaparkan pada stadium larva dengan kosentrasi 0,004585 ppm (F20) dan
0,082965 ppm (F40) mengakibatkan penurunan daya tetas telur, rata-rata
persentase daya tetas telur semula adalah 82,5% (F0) menjadi 67,8% (F20) dan
57,2% (F40). Penurunan daya tetas telur pada nyamuk Ae. aegypti juga terjadi
akibat pemaparan insektisida nabati spinosad, rata-rata daya tetas telur semula 86,90% (kontrol) menjadi 58,20% (5 ppm) dan 62,40% (20 ppm) (Perez et al. 2007). Antonio et al. (2009) juga melaporkan bahwa konsentrasi 0,06 ppm spinosad menyebabkan perubahan daya tetas telur nyamuk Ae. aegypti dari 84,90% (kontrol) menjadi 72,60%.
Pemaparan insektisida BPMC (golongan karbamat) pada nyamuk Anopheles aconitus pada tahap larva mengakibatkan perubahan daya tetas telur, semula 59,69% (kontrol) menjadi 63,58% (KL10); 56,87% (KL20) dan 58,37%
(KL30). Hal ini menunjukkan bahwa sampai konsentrasi tertentu cekaman
insektisida dapat meningkatkan daya tetas telur sebelum selanjutnya kembali menurun (Sujadmiko, 2000).
2.3.5 Kemampuan Ekdisis dan Eklosi Nyamuk Ae. aegypti
Kemampuan ekdisis dan eklosi cenderung menurun akibat pemaparan insektisida. Gunandini (2002) melaporkan bahwa nyamuk Ae. aegypti yang diseleksi malation menurunkan kemampuan ekdisis yang awalnya 91% (F0)
menjadi 82% (F5), 89% (F10), 89% (F15) dan 84% (F20). Adanan et al. (2005)
Efek malation juga menurunkan kemampuan ekdisis Ischiodon scutellaris Fabr (Diptera : Syrphidae) semula 73,95% (kontrol) menjadi 55,38% (25 µg/ml); 66,86% (100 µg/ml); 47,77% (150 µg/ml)., 54,98% (200 µg/ml) dan 33,46% (250 µg/ml) (Hoe et al. 1983). Perez et al. (2007) menyatakan bahwa penggunaan temefos (0,1 gr) pada Ae. aegypti yang sedang gravid menyebabkan penurunan kemampuan eklosi dari 41,20% (kontrol) menjadi 38,70%. Gunandini (2002) juga menyatakan bahwa larva Ae. aegypti yang diseleksi dengan malation menghasilkan penurunan kemampuan eklosi, semula 93% (F0) menjadi 82%
(F5), 81% (F10), 86% (F15) dan 91% (F20).
Adanan et al. (2005) menyatakan D-allethrin (36 mg/mat) dan Prallethrin (15 mg/mat) mampu menurunkan kemampuan eklosi nyamuk Ae. aegypti dari 99,91% (kontrol) menjadi 99,05% (Prallethrin) dan 97,29% (D-allethrin). Braga et al. (2005) melaporkan bahwa pemakaian insektisida IGR metophren mempengaruhi kemampuan eklosi nyamuk Ae. aegypti. Kemampuan eklosi menurun dari 96,20% (kontrol) menjadi 79,80% (5µ mg/l) dan 78,10 (10 mg/l).
2.3.6 Ratio Kelamin Jantan dan Betina Nyamuk Ae. aegypti
Perubahan pupa menjadi dewasa secara normal pada awalnya didominasi oleh jenis kelamin jantan (Christophers, 1960). Gunandini (2002) melaporkan bahwa nyamuk Ae. aegypti yang diseleksi dengan malation meningkatkan jenis nyamuk berkelamin jantan, persentase ratio kelamin jantan dan betina semula 46 : 54 (F0) menjadi 49 : 51% (F5); 49 : 51 (F10), 50 : 50 (F15) dan 54 : 46 (F20).
3
BAHAN DAN METODE KERJA
3.1
Lokasi
Penelitian
dan
Waktu
Penelitian
Penelitian dilaksanakan di Laboratorium Entomologi Bagian Parasitologi dan Entomologi Kesehatan, Departemen Ilmu Penyakit Hewan dan Kesehatan Masyarakat Veteriner (IPHK), Fakultas Kedokteran Hewan Institut Pertanian Bogor (FKH-IPB) sejak November 2010 sampai dengan Juni 2011.
Penelitian ini dibagi menjadi empat tahap, yaitu : (1) tahap persiapan dimulai dari pemeliharaan dan perbanyakan nyamuk Ae. aegypti, (2) tahap penelitian pendahuluan untuk menentukan konsentrasi temefos yang akan diuji, (3) tahap penelitian utama yaitu perlakuan pemaparan temefos pada tahap larva L3
dilanjutkan dengan pengamatan dan pengumpulan data serta (4) analisis & penyajian data.
3.2
Cara
Kerja
3.2.1 Tahap Persiapan
Tahap persiapan merupakan tahap perbanyakan Ae. aegypti secara massal di insektarium. Pemeliharaan dan perbanyakan Ae. aegypti dilakukan selama satu bulan sampai dihasilkan koloni Ae. aegypti dewasa dan pradewasa dengan jumlah yang mencukupi untuk penelitian. Pemeliharan Ae. aegypti dilakukan pada suhu kamar 27-310C dengan kelembaban relatif 85-90%.
Media Air
Media untuk pemeliharaan larva yang digunakan adalah air tanah yang diendapkan. Air endapan ini merupakan air yang selalu digunakan untuk pemeliharaan dan perbanyakan Ae. aegypti di insektarium, sehingga bias akibat dari kandungan zat yang ada di dalam air dapat diabaikan.
Untuk pemeliharaan larva, media air diganti setiap 2 hari sekali. Setelah larva menjadi pupa segera pupa dimasukkan ke dalam gelas plastik bervolume 200 ml yang diisi air ¾ bagian. Gelas yang telah berisi pupa tersebut dimasukkan ke dalam kandang nyamuk yang berukuran 40x40x40 cm3. Rusuk kandang terbuat
Gambar 2. Kandang tempat pemeliharaan dan perbanyakan
Ae. aegypti
Pakan Nyamuk
Pakan larva adalah pelet makanan ikan yang sebelumnya dihaluskan, jumlah pemberian pakan disesuaikan dengan perkembangan setiap instar larva sebagaimana tertera pada Tabel 1.
Tabel 1. Jumlah pakan larva nyamuk Ae. aegypti yang disesuaikan dengan perkembangang instar (Christophers, 1960 & Gerberg et al. 1994).
Sebagai pakan nyamuk Ae. aegypti dewasa adalah air gula dengan konsentrasi 10% yang secara periodik diganti setiap dua hari sekali. Pemberian pakan darah khusus untuk nyamuk betina dilakukan setiap empat hari sekali sesuai dengan siklus gonotropik. Pakan darah yang diberikan berasal dari darah manusia yaitu darah peneliti. Waktu pemberian pakan darah dilakukan sehari dua kali yaitu pada pukul 11.00 s/d 13.00 dan pukul 15.00 s/d 17.00 selama 2-3 jam sampai nyamuk Ae. aegypti betina kenyang darah (Gambar 3).
Umur larva Jumlah pakan/larva
1 hari 2 hari 3 hari 4 hari 5 hari 6 hari 7 hari
8 hari sampai larva menjadi pupa
Gambar 3. Pemberian pakan darah
Tempat peletakan telur (ovitrap) berupa gelas plastik bervolume 200 ml yang diisi air ¾ bagian dengan kertas saring diletakkan mengelilingi permukaan air tersebut (Gambar 4). Nyamuk Ae. aegypti betina akan meletakkan telur di sepanjang bagian kertas saring. Kertas saring diambil bersama-sama dengan telur yang telah melekat diatasnya, kemudian kertas tersebut dimasukkan ke dalam nampan penetasan. Pekerjaan ini terus menerus diulangi sesuai dengan siklus gonotrofik nyamuk setiap empat hari sekali.
Gambar 4. Ovitrap
3.2.2 Tahap Penelitian Pendahuluan
Temefos yang digunakan dalam penelitian ini adalah Abate® dengan bahan
larutan induk mempunyai konsentrasi 10 gr dalam 100 liter air (sesuai konsentrasi yang tertera pada label kemasan). Larutan induk ini selanjutnya diencerkan untuk konsentrasi uji selanjutnya.
Gambar 5. Kemasan temefos
Penetapan Konsentrasi Uji
Penetapan konsentrasi temefos KL0, KL25, KL50, KL75 dan KL90
diperoleh dari data kematian larva L3 merujuk pada hasil penelitian pendahuluan.
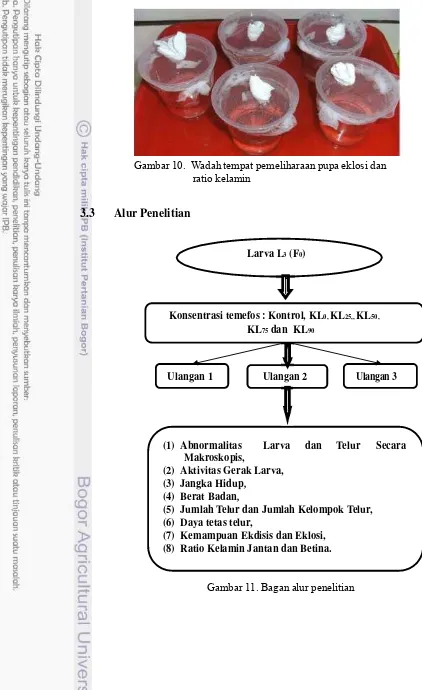
Temefos dalam bentuk granul digerus sampai halus kemudian ditimbang 0,1 gr (100 mg) dan dilarutkan dalam 1 liter air (100 ppm). Larutan ini dijadikan sebagai larutan induk yang akan diencerkan sesuai dengan konsentrasi uji yang digunakan (Tabel 2, Gambar 6 dan Lampiran 1). Perhitungan larutan induk berdasarkan konsentrasi anjuran :
10 gr/100 liter = 0,1 gr/liter = 100 mg/liter
= 100 ppm (1 mg/liter = 1 ppm)
Dari hasil analisis probit kematian larva L3 diperoleh konsentrasi temefos
0,180 ppm (KL0); 0,285 ppm (KL25); 0,330 ppm (KL50); 0,384 ppm (KL75); dan
(ppm)
konsentrasi uji perlakuan dalam penelitian. Untuk membuat 1.500 ml larutan dengan konsentrasi yang sesuai dengan konsnetrasi temefos yang diinginkan digunakan rumus :
N1 x V1 = N2 x V2
Keterangan :
N1 : konsentrasi awal (100 ppm),
V1 : volume awal (volume dicari, berapa volume yang akan diambil dari konsentrasi awal), N2 : konsentrasi uji (ppm),
V2 : volume media yang dibutuhkan (sesuai kebutuhan untuk media perlakuan)
Tabel 2. Konsentrasi temefos yang diuji 0,5 0,45 Y = 1,22 (x) + 0,65 0,4 0,35 0,3 0,25 0.180 0.285
mg/liter 0.330
mg/liter 0.384 mg/liter 0.433 mg/liter 0,2 0,15 0,1 0,05 0 mg/liter 0 SD= 1.08+ 0,22
Gambar 6. Regresi konsentrasi temefos yang diuji
3.2.3 Tahap Penelitian Utama 3.2.3.1 Pemaparan Konsentrasi Uji
Dari setiap konsentrasi larutan uji diambil 500 ml larutan kemudian dimasukkan ke dalam larutan uji tersebut sebanyak 100 ekor larva instar 3 (L3)
Ae. aegypti, untuk setiap konsentrasi dilakukan tiga kali ulangan. Lamanya pemaparan dengan temefos berlangsung selama 1x24 jam. Konsentrasi temefos
Konsentrasi larutan uji
Volume pengenceran yang diambil dari larutan induk
Total Volume
Kontrol KL0 (0,180 ppm)
KL25 (0,285 ppm)
KL50 (0,330 ppm)
KL75 (0,384 ppm)
KL90 (0,433 ppm)
0 2,70 ml 4,25 ml 4,95 ml 5,76 ml 6,50 ml
[image:30.612.104.491.205.695.2]yang digunakan adalah KL0 (0,180 ppm), KL25 (0,285 ppm), KL50 (0,330 ppm),
KL75 (0,384 ppm), KL90 (0,433 ppm) dan kontrol.
3.2.3.1 Pengamatan daya tahan hidup
Larva yang telah terpapar temefos dengan konsentrasi uji kemudian dipindahkan ke media tanpa temefos (500 ml air tanpa temefos). Dari setiap konsentrasi perlakuan diambil 25 ekor larva untuk diamati lama stadium pradewasa sampai dewasa, selanjutnya diamati sesuai dengan parameter penelitian.
(1) Abnormalitas bentuk larva dan telur
Abnormalitas larva yaitu perubahan morfologi larva yang terjadi akibat pemaparan dengan temefos selama 1x24 jam. Semua larva yang mati dikumpulkan dan dipisahkan dari yang masih hidup, kemudian dikelompokkan menurut konsentrasi perlakuan. Analisis dilakukan secara deskriptif dibandingkan dengan larva normal. Abnormalitas telur yaitu perubahan morfologi telur yang dihasilkan oleh nyamuk betina dewasa yang telah terpapar temefos pada tahap larva instar 3 (L3). Telur yang dihasilkan kemudian dikelompokkan menurut
konsentrasi perlakuan. Analisis dilakukan secara deskriptif dibandingkan dengan telur normal. Pengamatan dan pengambilan gambar dilakukan di bawah mikroskop. Foto diambil dengan kamera Sony Series ecp 12,8 megapixel.
(2) Aktivitas gerak larva
Gambar 7. Pipa paralon yang dibelah memanjang
(3) Jangka hidup nyamuk Ae. aegypti
Jangka hidup Ae. aegypti pradewasa dibedakan antara larva dengan pupa. Jangka hidup larva merupakan perubahan dari L3 sampai menjadi pupa,
sedangkan jangka hidup pupa dimulai dari pupa sampai dewasa.
Gambar 8. Kandang perlakuan.
Pengamatan terhadap jangka hidup larva dan pupa dilakukan setiap jam sampai terjadi perubahan stadium. Penggantian media air dilakukan setiap dua hari sekali agar tidak terjadi kekurangan oksigen akibat penimbunan sisa makanan dan kulit sisa moulting. Jangka hidup Ae. aegypti dewasa dibedakan antara jantan dan betina. Pupa yang akan menyilih dimasukkan kedalam kandang pengamatan berukuran 20x20x20 cm3 (Gambar 8). Pengamatan dilakukan setiap dua hari
sekali.
(4) Berat badan Ae. aegypti
[image:32.612.58.504.65.663.2] [image:32.612.159.522.80.165.2]berat basah larva dilakukan terhadap 20 larva instar 3 (L3) setelah larva
dipaparkan dengan temefos 1x24 jam.
Penimbangan dilakukan dengan menggunakan timbangan elektronik OHAUS GA200. Larva dan pupa yang akan ditimbang di letakkan di atas plastik sebagai alas ukuran 10x6 cm2 yang di atasnya ditempel kertas saring ukuran 3x3
cm2 untuk menyerap air, berat alas 0,6 mg yang nantinya tidak dihitung (sebagai
pengurang). Setelah penimbangan berat basah, larva dikeringkan dalam oven pada suhu 880C selama 3 jam untuk penimbangan berat kering (Sujatmiko, 2000).
Penimbangan berat badan Ae. aegypti dewasa dibedakan antara jantan dan betina. Nyamuk Ae. aegypti dewasa yang akan ditimbang berumur maksimal 24 jam, belum diberi pakan darah maupun cairan sukrosa. Untuk mendapatkan berat basah, sebelum ditimbang Ae. aegypti dewasa dianestesi dengan menggunakan eter selama 40 detik. Berat kering diperoleh dengan menimbang nyamuk yang sama setelah penimbangan berat basah. Pengeringan dilakukan dengan oven pada suhu 880C selama 3 jam (Sujatmiko, 2000).
(5) Jumlah telur dan kelompok telur
Pada penelitian ini ternyata tidaklah sama jumlah nyamuk yang bertahan hidup, karena semakin tinggi konsentrasi temefos yang dipaparkan maka semakin sedikit pula nyamuk yang hidup. Untuk mengamati jumlah telur dan kelompok telur yang dihasilkan selama hidup nyamuk, diambil perbandingan antara betina dengan jantan sebesar 2 : 1. Untuk memenuhi kriteria perbandingan betina dengan jantan 2 : 1 maka diambil 20 betina : 10 jantan (Kontrol, KL0, KL25 dan KL50),
sedangkan untuk KL75 digunakan 14 betina : 7 jantan, terakhir untuk KL90
digunakan 4 betina : 2 jantan. Nyamuk jantan dan betina ini kemudian dimasukkan ke dalam kandang berukuran 20x20x20 cm3. Di dalam kandang
disediakan larutan glukosa 10% yang diganti setiap dua hari sekali
yang diperoleh selama hidup nyamuk sedangkan setiap sekali panen dihitung sebagai satu kelompok telur.
(6) Daya tetas telur
Telur yang akan ditetaskan dimasukkan ke dalam nampan berukuran 20x14x4 cm3 yang berisi air 500 ml (Gambar 9). Daya tetas telur dihitung
berdasarkan persentase telur yang menetas diantara total telur yang dihasilkan nyamuk. Telur dianggap tidak menetas apabila melewati 15 hari.
Gambar 9. Wadah tempat penetasan telur untuk pengamatan daya tetas telur dan ekdisis
(7) Kemampuan ekdisis dan eklosi
Kemampuan ekdisis dihitung berdasarkan persentase larva yang berhasil menjadi pupa diantara jumlah total larva, sedangkan kemampuan eklosi dihitung berdasarkan pupa yang berhasil menjadi dewasa dari total pupa.
(8) Ratio kelamin jantan dan betina
Gambar 10. Wadah tempat pemeliharaan pupa eklosi dan
ratio kelamin
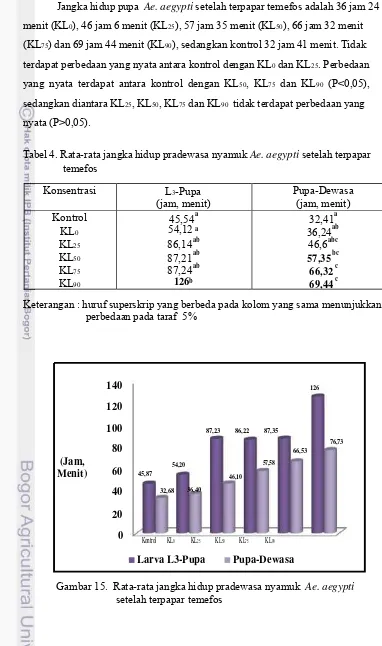
3.3
Alur
Penelitian
Larva L3 (F0)
Konsentrasi temefos : Kontrol, KL0, KL25,, KL50,
KL75 dan KL90
Ulangan 1
Ulangan 2
Ulangan 3
(1) Abnormalitas Larva dan Telur Secara Makroskopis,
(2) Aktivitas Gerak Larva,
(3) Jangka Hidup,
(4) Berat Badan,
(5) Jumlah Telur dan Jumlah Kelompok Telur, (6) Daya tetas telur,
(7) Kemampuan Ekdisis dan Eklosi, (8) Ratio Kelamin Jantan dan Betina.
[image:35.612.53.475.71.761.2]
3.4
Analisis
Data
4
HASIL DAN PEMBAHASAN
4.1
Abnormalitas
Bentuk
Telur
dan
Larva
Ae.
aegypti
4.1.1 Abnormalitas bentuk telur Ae. aegypti
Pada kondisi normal telur Ae. aegypti berukuran kecil (50µ), sepintas lalu tampak bulat panjang dan berbentuk lonjong (oval). Pada dinding luar (exochorion) telur nyamuk ini tampak adanya garis-garis dan terdapat bahan lengket (glikoprotein) yang mengeras bila kering (Christophers, 1960).
Kontrol KL25 Normal, bentuk oval
telur rapuh, mudah pecah
KL0 KL50 piph KL75 KL90
Telur terpotong
[image:37.612.125.506.203.672.2]
Temefos merupakan racun kontak yang dapat masuk ke dalam tubuh larva melalui spirakel, segmen tubuh pada abdomen, dan mulut. Akumulasi temefos terbesar di dalam otot. Pemaparan temefos pada larva instar 3 (L3) terakumulasi
paling besar dalam otot dan beredar keseluruh tubuh melalui hemolim. Penetrasi insektisida dipengaruhi oleh daya larutnya dalam lemak, semakin larut suatu insektisida dalam lemak maka semakin mudah insektisida tersebut masuk kedalam tubuh serangga (Matsumura, 1978). Temefos terpenetrasi ke dalam ovum pada proses embriogenesis yang menyebabkan terhambatnya pertumbuhan dan terganggunya sintesis protein ke kuning telur. Terakumulasinya temefos didalam folikel ovum menyebabkan pertumbuhan telur atau kesuburan telur menurun dan kerapuhan pada dinding telur (Inwang, 1968 dalam Kumar et al. (2009). Pemaparan temefos konsentrasi KL0, KL25 dan KL50 menyebabkan
kerapuhan dinding telur sehingga telur mudah pecah, bentuk telur pipih (KL50),
salah satu ujung yang tidak sempurna (KL75) dan telur yang membelah secara
melintang (KL90) (Gambar 12).
4.1.2 Abnormalitas bentuk larva Ae. aegypti
Secara normal larva nyamuk Ae. aegypti memiliki comb scale pada ruas abdomen kedelapan sebanyak 8-21 yang berjajar 1-3 baris. Bentuk individu dari comb scale seperti duri dengan lekukan yang jelas yang merupakan ciri dari larva Ae. aegypti. Larva normal juga dan memiliki corong udara atau sifon. Pada sifon terdapat pekten serta sepasang rambut yang berjumbai. Selain itu, larva juga memiliki rambut-rambut berbentuk kipas (palmate hairs) di sepanjang sisi tubuh (Christophers, 1960; Dekpes, 2008).
Kontrol
Larva normal
Kepala, torak dan sifon, ruas abdomen
rambut seta rontok
KL0
belakang yang menghitam KL25
Abdomen yang mengkerut dan KL50
Abdomen yang memanjang memendek
KL75 KL90
Gambar 13. Abnormalitas morfologi larva Ae. aegypti setelah terpapar temefos dibandingkan dengan kontrol
[image:39.612.103.513.70.632.2]
asetilkolinterase sehingga enzim ini tidak dapat menghidrolisis asetilkolin. Hal ini yang menyebabkan paralisis atau kelumpuhan dan kematian larva.
Pemaparan temefos KL0 menyebabkan kerontokan seta. Pemaparan
temefos KL25 menyebabkan tubuh larva yang semakin memanjang. Proses
pemanjangan dan pemendekan tubuh larva Ae. aegypti setelah terpapar temefos diduga akibat perbedaan kandungan air dalam tubuh larva dengan lingkungan. Pengaturan keseimbangan air merupakan kesetimbangan kimia larutan (Murray et al. 1995). Penentuan kandungan air tubuh larva dihitung menggunakan rumus di bawah ini (Sudjatmiko, 2000) :
Kadar air = x 100%
Kandungan air rata-rata dalam tubuh larva setelah terpapar temefos pada konsentrasi normal (kontrol), KL0 dan KL25 adalah adalah 35% (Kontrol) dalam
keadaan larva hidup, 37% (KL0), 36% (KL25), 61% (KL50), 55% (KL75) dan 72%
(KL90) dalam keadaan larva sudah mati. Semakin tinggi kandungan temefos pada
media air menyebabkan kadar air pada tubuh larva semakin tinggi akibatnya terjadi perbedaan tekanan osmotik. Tekanan osmotik merupakan tekanan koligatif larutan yang dapat menghentikan perpindahan molekul-molekul pelarut ke dalam larutan melalui membran sel semi-permeabel.
Pemaparan temefos dengan konsentrasi KL50 memperlihatkan perubahan
warna pada sifon dan ruas abdomen belakang menjadi kehitaman. sifon dan ruas abdomen belakang menghitam kemungkinan disebabkan oleh proses oksidasi biologis yang terhambat di dalam tubuh larva Ae. aegypti. Kelangsungan hidup larva dipengaruhi oleh pH atau tingkat keasaman.
Perbedaan sifat kimia air berpengaruh terhadap pertumbuhan dan perkembangan larva. Larva Ae. aegypti dapat hidup pada lingkungan dengan pH antara 5,8-8,6 (Chan et al. 1971), penelitian Hidayat et al. 1997 menemukan bahwa larva nyamuk Ae. aegypti dapat hidup pada pH 5-9. pH lambung atau usus larva adalah 5,5-5,8 (Christophers, 1960). Keasamaan atau pH ekstraseluler lingkungan yang normal makhluk hidup adalah 7,35-7,45 (Murray, 1995). Hasil pengukuran pH larutan normal adalah 7,5 (kontrol) dan larutan temefos KL0,
KL25, KL50, KL75 dan KL90 secara berurutan adalah 6,8; 7,1; 7,4; 8,3 dan 9,5.
Perbedaan pH tubuh larva dengan pH lingkungan berpengaruh terhadap transportasi oksigen dalam tubuh larva. Akumulasi temefos menghambat masuknya oksigen sehingga proses oksidasi biologis (pembakaran) di dalam otot ikut terhambat (Tarumingkeng, 1992). Terhambatnya transportasi oksigen menyebabkan terganggunya pembentukan enzim sitokromoksidase, enzim sitokromoksidase merupakan enzim respirasi dalam proses oksidasi biologi atau metabolisme (Murray et al. 1995). Perubahan warna ini diduga akibat akumulasi temefos yang masuk melalui sifon sehingga aliran oksigen terhambat.
Pemaparan temefos KL75 dan KL90 menyebabkan tubuh larva Ae. aegypti
memendek diduga akibat kandungan air dari tubuh larva keluar melalui ruas-ruas abdomen ke dalam lingkungan. Perpindahan air dari tubuh larva ke lingkungan adalah akibat kandungan temefos yang tinggi (0,433 ppm atau KL90) di dalam
larutan, hal ini menyebabkan tekanan osmotik lingkungan lebih tinggi. Akibat air keluar dari tubuh larva maka tubuh larva mengkerut dan memendek.
4.2
Aktivitas
Gerak
Larva
Nyamuk
Ae. aegyptidan 24 menit 35 detik (KL90) sedangkan waktu tempuh larva Ae. aegypti yang
tidak terpapar dengan temefos (kontrol) adalah 2 menit 57 detik.
Tabel 3. Rata-rata waktu tempuh larva nyamuk Ae. aegypti sejauh 30 cm setelah terpapar temefos
Keterangan : huruf superskrip yang berbeda pada kolom yang sama menunjukkan perbedaan pada taraf 5%.
24,35
25,00
20,00
14,36
(menit, 15,00
detik)
10,00
5,00
0,00
9,20
2,57 2,395 3,49
Kontrol KL0 KL25 KL50 KL75 KL90
Waktu Tempuh
Gambar 14. Rata-rata waktu tempuh larva (L3) Ae. aegypti sejauh 30 cm
setelah terpapar temefos
Waktu tempuh yang dibutuhkan oleh larva Ae. aegypti yang terpapar temefos KL0 dan KL25 bila dibandingkan dengan kontrol tidak terdapat
perbedaan yang nyata (P>0,05). Perbedaan yang nyata terlihat pada waktu tempuh yang diperlukan oleh larva Ae. aegypti KL50, KL75, KL90 dengan kontrol,
sedangkan antara KL50, KL75, dan KL90 masing-masing berbeda nyata (P<0,05).
Larva Ae. aegypti menyukai habitat yang tenang tanpa aliran air (genangan air dalam wadah) dan terlindungi dari cahaya secara langsung karena sifat larva menjauhi cahaya atau dengan kata lain bersifat fototropisme negatif.
Konsentrasi Waktu tempuh (menit, detik) Kontrol
KL0
KL25
KL50
KL75
KL90
a
2,57
a
2,39
a
3,49 b
9,2 c 14,36
d
[image:42.612.130.487.159.770.2]Larva lincah dan aktif bergerak dengan memperlihatkan gerakan-gerakan naik ke permukaan air dan turun ke dasar wadah secara berulang atau zig-zag. Gerakan yang dilakukan oleh larva adalah untuk mempertahankan kelangsungan hidupnya, dengan tujuan untuk memperoleh makan dan oksigen. Larva mengambil makanan di dasar wadah, oleh karena itu larva Ae. aegypti disebut pemakan makanan di dasar atau bottom feeder. Pada saat larva mengambil oksigen dari udara, larva bergerak menempatkan corong udara (sifon) pada permukaan air seolah-olah badan larva berada pada posisi membentuk sudut dengan permukaan air (Christophers, 1960).
Pada penelitian ini adanya cahaya lampu TL 5 watt yang dipasang pada salah satu ujung pipa memaksa larva Ae. aegypti untuk bergerak menjauhi arah cahaya lampu. Gerakan menjauhi cahaya lampu membuktikan bahwa larva Ae. aegypti berusaha untuk memepertahankan diri meskipun dalam kondisi lemah akibat cekaman temefos. Semakin tinggi konsentrasi temefos yang dipaparkan semakin lambat aktivitas larva, hal ini terlihat dari semakin lamanya waktu yang diperlukan oleh larva untuk bergerak sejauh 30 cm. Waktu yang semula diperlukan 2 menit 57 detik menjadi 24 menit 35 detik setelah terpapar temefos dengan konsentrasi tertinggi yaitu 0,433 ppm (KL90). Keracunan temefos
menyebabkan gangguan transmisi impuls pada ujung syaraf akibatnya terjadi gangguan pada aktivitas larva sehingga larva menjadi kejang-kejang dan aktivitas geraknya semakin lambat.
4.3
Jangka
Hidup
Nyamuk
Ae.
aegypti
4.3.1
Jangka hidup larva dan pupa nyamuk Ae. aegyptiJangka hidup larva (L3 sampai menjadi pupa) adalah 54 jam 12 menit
(KL0), 86 jam 14 menit (KL25), 87 jam 21 menit (KL50), 87 jam 24 menit (KL75),
dan 126 jam (KL90), sedangkan yang tidak terpapar temefos (kontrol) adalah 45
jam 54 menit. Jangka hidup larva (L3 sampai menjadi pupa) tidak berbeda nyata
antara KL0, KL25, KL50, KL75 (P>0,05). Perbedaan yang nyata terdapat antara
Jangka hidup pupa Ae. aegypti setelah terpapar temefos adalah 36 jam 24 menit (KL0), 46 jam 6 menit (KL25), 57 jam 35 menit (KL50), 66 jam 32 menit
(KL75) dan 69 jam 44 menit (KL90), sedangkan kontrol 32 jam 41 menit. Tidak
terdapat perbedaan yang nyata antara kontrol dengan KL0 dan KL25. Perbedaan
yang nyata terdapat antara kontrol dengan KL50, KL75 dan KL90 (P<0,05),
sedangkan diantara KL25, KL50, KL75 dan KL90 tidak terdapat perbedaan yang
nyata (P>0,05).
Tabel 4. Rata-rata jangka hidup pradewasa nyamuk Ae. aegypti setelah terpapar temefos
Keterangan : huruf superskrip yang berbeda pada kolom yang sama menunjukkan perbedaan pada taraf 5%
140 120 100 87,23 86,22 87,35 126
80 66,53 76,73
(Jam,
Menit)
60 45,87 54,20
46,10 57,58 40 20 0
32,68 36,40
Kontrol KL0 KL25 KL50 KL75 KL90
Larva L3-Pupa Pupa-Dewasa
Gambar 15. Rata-rata jangka hidup pradewasa nyamuk Ae. aegypti setelah terpapar temefos
Konsentrasi L3-Pupa
(jam, menit)
Pupa-Dewasa (jam, menit) Kontrol
KL0
KL25
KL50
KL75
KL90
a 45,54 54,12 a
ab 86,14 ab 87,21 ab 87,24
126b
a 32,41ab 36,24
abc 46,6
bc
57,35 c 66,32
c
[image:44.612.110.492.87.733.2]
4.3.2
Jangka hidup nyamuk jantan dan betina Ae. aegyptiJangka hidup nyamuk Ae. aegypti jantan setelah terpapar temefos adalah 39 hari (KL0); 24,2 hari (KL25); 23,8 hari (KL50); 23,14 hari (KL75); 22 hari
(KL90), sedangkan secara normal nyamuk jantan dapat hidup rata-rata 42,6 hari
(kontrol). Perbedaan yang tidak nyata terdapat pada KL0, KL25, KL50 dengan
kontrol (P>0,05). Perbedaan yang tidak nyata juga terdapat pada KL0, KL25,
KL50, KL75 dan KL90 (P>0,05), tetapi terdapat perbedaan yang nyata bila
dibandingkan antara kontrol dengan KL75 dan KL90(P<0,05).
Tabel 5. Rata-rata jangka hidup nyamuk dewasa Ae. aegypti setelah terpapar temefos
Keterangan : huruf superskrip yang berbeda pada kolom yang sama menunjukkan perbedaan pada taraf 5%.
60,00 54,20
50,00 42,60 46,70
40,00 39,00 37,90 36,90 32,71
(hari) 30,00 20,00
10,00 0,00
27,00 24,20 23,80 23,14 22,00
Kontrol KL0 KL25 KL50 KL75 KL90
Jantan Betina
Gambar 16. Rata-rata jangka hidup nyamuk dewasa Ae. aegypti (jantan dan betina) setelah terpapar temefos
Konsentrasi Dewasa (hari)
Jantan Betina
Kontrol KL0
KL25
KL50
KL75
KL90
a 42,6 39ab ab 24,2 ab 23,8 b 23,14 2