TERHADAP INFEKSI
CHILLI VEINAL MOTTLE VIRUS
ZAHRATUL MILLAH
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI TESIS
DAN SUMBER INFORMASI
Dengan ini saya menyatakan bahwa tesis yang berjudul Pewarisan Karakter Ketahanan Tanaman Cabai terhadap Infeksi Chilli Veinal Mottle Virus adalah benar hasil karya saya sendiri dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun yang tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir tesis ini.
Bogor, Desember 2007
Zahratul Millah
NIM A351030111
Key words : chillipepper, inheritance, resistance, chilli veinal mottle virus.
ZAHRATUL MILLAH. Inheritance Study of Resistance to Chilli Veinal Mottle Virus on chillipepper.Supervised by SRIANI SUJIPRIHATI and SRI HENDRASTUTI HIDAYAT
One of the major problem in chillipepper production was virus infection, with Chilli Veinal Mottle Virus (ChiVMV) as one of the most important viruses in Asia. Strategy to manage virus infection is not easy. The use of resistant varieties was considered as the best strategy to control viral disease. Important steps in plant breeding for development of resistance varieties involved obtaining of resistance source and understanding genetic control of the trait.
The research was conducted in three stages: 1) Resistance evaluation of chillipepper to ChiVMV infection (2) development of genetic material for the inheritance study and (3) inheritance study and estimation the genetic control of chillipepper resistance to ChiVMV infection.
Evaluation for resistance was undergone to find resistant and susceptible parents for further inheritance study. This evaluation involve 14 genotypes from the collection of Genetic and Plant Breeding laboratory, Department of Agronomy and Horticultura. ChiVMV isolat Cikabayan was used for the source of inoculum. From this evaluation three genotypes were identified as resistant parents i.e. PBC495, VC211a-3-1-1-1 and CCA321, and only one genotype was identified as susceptible parent.
Basic population for genetic materials in inheritance study was developed. This population consisted of: P1 (resistant parent), P2 (susceptible parent), F1 (filial of cross between resistant and susceptible parent), F1R (filial of reciprocal cross), BC1P1 (filial of backcross with resistant parent), BC1P2 (filial of backcross with susceptible parent) and F2 (second filial of the cross) populations.
Following the 1st and 2nd experiments above, inheritance study for chillipepper resistance to ChiVMV infection was conducted. On this study, 6 generations population from the cross between PBC495 and ICPN12#4 was used. Disease incidence (DI) and score of absorbance value at λ 405 nm were used as variables for resistance response.
Kata kunci : cabai, pewarisan, ketahanan, chilli veinal mottle virus.
ABSTRAK
ZAHRATUL MILLAH. Pewarisan Karakter Ketahanan Tanaman Cabai terhadap Infeksi Chilli Veinal Mottle Virus. Dibimbing oleh SRIANI SUJIPRIHATI dan SRI HENDRASTUTI HIDAYAT
Chilli Veinal Mottle Virus (ChiVMV) merupakan salah satu kendala utama dalam produksi cabai. Pengendalian secara konvensional terhadap ChiVMV seringkali tidak efisien. Metode pengendalian yang paling praktis dan dapat diharapkan keberhasilannya adalah dengan menggunakan kultivar tahan. Tahapan yang penting dalam program pemuliaan tanaman untuk menghasilkan varietas yang tahan terhadap penyakit adalah mendapatkan sumber ketahanan dan mengetahui kendali genetik dari karakter ketahanan tersebut.
Penelitian terdiri atas 3 tahapan, yaitu: (1) Evaluasi respons ketahanan tanaman terhadap infeksi ChiVMV (2) pembentukan materi kegenetikaan, (3) studi pola pewarisan dan pendugaan komponen genetik ketahanan cabai terhadap infeksi ChiVMV.
Penelitian tahap pertama bertujuan mendapatkan tetua tahan dan tetua rentan untuk studi pola pewarisan. Pada percobaan ini telah dievaluasi 14 genotipe cabai, koleksi bagian Genetika dan Pemuliaan Tanaman IPB, dengan ChiVMV isolat Cikabayan. Berdasarkan respon dari dua kali evaluasi pada genotipe terpilih didapatkan tetua tahan yaitu genotipe PBC495, VC211a-1-1-1 dan CCA321 serta tetua rentan yaitu ICPN12#4 .
Kegiatan penelitian tahap kedua bertujuan untuk pembentukan populasi dasar sebagai bahan untuk studi pola pewarisan, yaitu populasi P1 (tetua tahan), P2 (tetua rentan), F1 (hasil persilangan antara tetua tahan dan tetua rentan), F1R (hasil persilangan resiprok), BC1P1 (silang balik dengan tetua tahan), BC1P2 (silang balik dengan tetua rentan) dan F2 (keturunan kedua hasil persilangan).
Tahapan ketiga penelitian bertujuan untuk mempelajari pola pewarisan karakter ketahanan cabai terhadap infeksi ChiVMV. Pada tahapan ini digunakan populasi enam generasi hasil persilangan PBC495 dengan ICPN12#4, dengan peubah ketahanan indeks gejala dan nilai absorban.
© Hak Cipta Milik Institut Pertanian Bogor, tahun 2007 Hak cipta dilindungi Undang-undang
1. Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa menyebutkan sumber
a. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik atau tinjauan suatu masalah
b. Pengutipan tidak merugikan kepentingan yang wajar IPB
2. Dilarang mengumumkan dan memperbanyak sebagian atau seluruh karya
PEWARISAN KARAKTER KETAHANAN TANAMAN CABAI
TERHADAP INFEKSI
CHILLI VEINAL MOTTLE VIRUS
ZAHRATUL MILLAH
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Departemen Agronomi dan Hortikultura
SEKOLAH PASCASARJANA
INSTITUT PERTANIAN BOGOR
Puji syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan karuniaNya, sehingga penulis dapat menyelesaikan penulisan tesis yang berjudul
Pewarisan Karakter Ketahanan Cabai terhadap Infeksi Chilli Veinal Mottle Virus.
Ucapan terima kasih dan penghargaan penulis sampaikan kepada Dr. Ir. Sriani Sujiprihati, MS selaku ketua komisi pembimbing, dan Dr. Ir. Sri Hendrastuti Hidayat, MSc selaku anggota komisi pembimbing yang telah dengan sabar memberikan arahan, kritik, saran dan dukungan moril hingga penulis dapat menyelesaikan penyusunan tesis ini.
Penulis juga menyampaikan ucapan terima kasih kepada Rektor, Dekan dan Ketua Jurusan Agronomi Fakultas Pertanian Universitas Sultan Ageng Tirtayasa yang telah memberikan izin untuk melanjutkan program master, Departemen Pendidikan Nasional yang telah memberikan dukungan dana melalui BPPS Dikti, Dr. Ir. Sri Hendrastuti Hidayat selaku ketua Tim Program Kerjasama Faperta IPB- AVRDC atas dukungan dana penelitiannya serta selaku Kepala Laboratorium Virologi Dept. Proteksi Tanaman IPB atas fasilitas penelitian yang diberikan, Kepala Bagian Genetika dan Pemuliaan Tanaman Dept. AGH IPB atas bantuan bahan genetik dan fasilitas di Labdik. Pemuliaan Tanaman, dan kepada Pemprov Banten atas bantuan dana melalui program bantuan biaya penelitian Dispenda Prov. Banten.
Ucapan terima kasih penulis sampaikan pula kepada asisten laboratorium, asisten kebun, rekan-rekan penulis dan adik-adik mahasiswa baik di Laboratorium Virologi Tumbuhan maupun di Labdik. Pemuliaan Tanaman yang telah berbagi ilmu, materi penelitian, pengalaman dan bantuan selama penulis melaksanakan penelitian dan menyusun tesis ini.
Kepada kedua orang tua, kakanda dan adik-adik tercinta, serta kepada ayah dan ibu mertua beserta segenap keluarga besar atas segala doa, dorongan semangat dan kasih sayangnya penulis haturkan ucapan terimakasih.
Untuk anak-anak tersayang, Arifa Khairunnisa dan Batrisyia Khairunnisa, bunda mohon maaf atas waktu dan perhatian bunda untuk kalian yang banyak tersita demi menyelesaikan studi bunda. Kepada suami tersayang, Ir. Khairul M. Lubis MM., adek ucapkan terima kasih yang tak terhingga atas segala doa, kasih sayang, dukungan baik moril maupun materiil serta segenap pengorbanan yang diberikan selama ini.
Terakhir penulis sampaikan ucapan terima kasih kepada teman-teman di komplek IPB II, atas jalinan persaudaraan yang diberikan, semoga jalinan ini tak akan lekang oleh jarak dan waktu, serta kepada pihak-pihak lain yang tidak dapat penulis sebutkan satu per satu, yang telah memberikan doa, bantuan, dorongan, kritik dan sarannya selama penulis kuliah dan menyelesaikan penelitian.
Akhir kata penulis berharap semoga tulisan ini dapat bermanfaaat dan memberikan tambahan informasi, khususnya dalam usaha pemuliaan tanaman cabai.
Bogor, Desember 2007
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 19 Desember 1977 sebagai anak kedua dari lima bersaudara dari ayah H. Zahruddin Zen BA dan ibu Hj. Ifah Hanifah BA. Penulis menikah dengan Ir. Khairul M Lubis, MM. pada tanggal 18 Januari 2004 dan telah dikaruniai dua orang putri, Arifa Khairunnisa dan Batrisyia Khairunnisa.
Pendidikan dasar dan menengah diselesaikan penulis di Jakarta pada tahun 1996. Kemudian pada tahun yang sama penulis diterima di program studi Pemuliaan Tanaman Jurusan Budidaya Pertanian Fakultas Pertanian Universitas Padjadjaran melalui jalur SPMB dan lulus pada tahun 2002. Pada tahun 2003 penulis diterima di Program Studi Agronomi Sekolah Pascasarjana IPB.
Halaman
DAFTAR TABEL ………. xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ………... xiii
PENDAHULUAN ………... 1
Latar Belakang ……….. 1
Tujuan Penelitian ...…...………... 4
Hipotesis ………...……… 4
Manfaat Penelitian ………. 4
TINJAUAN PUSTAKA ……….…. 6
Syarat Tumbuh Tanaman Cabai ………... 6
Biologi Tanaman Cabai ………... 7
Hama dan Penyakit Tanaman Cabai ……….... 8
Virus Sebagai Patogen Tanaman ………... 9
Chilli Veinal Mottle Potyvirus (ChiVMV) ….………... 10
Pemuliaan untuk Ketahanan Tanaman terhadap Virus ……..… 11
BAHAN DAN METODE PENELITIAN .………... 21
Tempat dan Waktu Penelitian ……...……… 21
Bahan dan Alat ..………. 21
Metode Penelitian ……..………... 21
Pelaksanaan Percobaan ……..………... 26
Analisis Data ………. 31
HASIL DAN PEMBAHASAN ……….. 39
Respon Ketahanan Beberapa Genotipe Cabai koleksi terhadap infeksi ChiVMV ………... 39
Pembentukan Materi Kegenetikaan ... 42
Pola Pewarisan Karakter Ketahanan terhadap ChiVMV ……... 42
SIMPULAN DAN SARAN ……….... 51
Simpulan ... 51
Saran ... 51
DAFTAR PUSTAKA ………... 53
DAFTAR TABEL
Halaman
1. Interaksi antara gen tanaman inang dan gen virus ……… 13
2. Penentuan indeks gejala pada tanaman cabai yang terinfeksi
ChiVMV ……….. 29
3.. Penentuan peringkat ketahanan tanaman cabai terhadap ChiVMV.. 29
4. Penentuan skor titer virus berdasarkan nisbah nilai absorban dari sampel tanaman cabai yang diinokulasi oleh ChiVMV ... 30
5. Klasifikasi derajat dominansi berdasarkan nilai potensi rasio (hp) .. 32
6. Koefisien komponen genetik dalam Joint Scaling Test ... 36
7. Hasil evaluasi respon ketahanan cabai terhadap infeksi ChiVMV tahap I ... 39
8. Hasil evaluasi respon ketahanan cabai terhadap infeksi ChiVMV tahap II ... 41
9. Koefisien korelasi antara peubah kejadian penyakit, intensitas gejala dan titer virus ... 41
10. Nilai rata-rata, galat baku, hasil uji beda nilai tengah (Uji T) dan hasil uji kehomogenan ragam (Uji F) dari peubah indeks gejala dan peubah titer virus populasi F1 dan F1 resiprok ...
42
11. Nilai rata-rata dan galat baku peubah indeks gejala dan titer virus dari populasi P1, P2 dan F1, serta nilai potensi rasio dari kedua peubah ... 43
12. Hasil uji kesesuaian sebaran frekuensi ketahanan terhadap ChiVMV berdasarkan indeks gejala pada populasi F2 dan BC1P2 dengan hipotesis histogram berpuncak dua terhadap beberapa model nisbah Mendel ...
46
13. Hasil uji kesesuaian sebaran frekuensi ketahanan terhadap ChiVMV berdasarkan skor titer virus pada populasi F2 dengan hipotesis histogram berpuncak dua terhadap beberapa model nisbah Mendel ... 48
14. Uji skala individu dan skala gabungan kesesuaian model aditif dominan untuk peubah titer virus ... 49
Halaman
1. Bagan Alir Penelitian Pewarisan Karakter Ketahanan Tanaman
Cabai terhadap Infeksi Chilli Veinal Mottle Virus ... 22
2. Teknik Persilangan Buatan pada Cabai .……… 24
3. Teknik inokulasi virus secara mekanik ………. 27
4. Tipe Gejala Infeksi ChiVMV ……….. 28
5. Skema posisi relatif nilai rata-rata F1 terhadap nilai rata-rata tetua tahan (P1) dan tetua rentan (P2) serta nilai tengah kedua tetua (MP) ………... 43
6. Histogram sebaran frekuensi tanaman berdasarkan indeks gejala pada populasi P1, P2, F1, BC1P1, BC1P2 dan F2 ……….. 45
7. Sebaran frekuensi tanaman berdasarkan titer virus pada populasi P1, P2, F1, BC1P1, BC1P2 dan F2 ………. 47
8. Sebaran frekuensi tanaman berdasarkan titer virus pada populasi F2 ………..….. 47
DAFTAR LAMPIRAN
Halaman
1. Daftar galur cabai merah yang digunakan ………... 58
2. Penampilan buah dari delapan genotipe cabai yang dievaluasi pada tahap II ... 59 3. Genotipe cabai yang tahan terhadap ChiVMV berdasarkan hasil
evaluasi respon ketahanan: A. PBC495; B. VC211a-3-1-1-1; C.
CCA321 ………. 60
4. Genotipe ICPN12#4 yang rentan terhadap ChiVMV berdasarkan
hasil evaluasi respon ketahanan ... 60
5. Buah dari masing-masing generasi keturunan persilangan genotype PBC495 dengan ICPN12#4 ... 61 6. Uji normalitas sebaran frekuensi populasi F2 untuk peubah titer
virus ………... 61
Latar Belakang
Cabai (Capsicum annuum L.) adalah salah satu tanaman ekonomis penting
di dunia dan telah dibudidayakan secara meluas (Rubatzky dan Yamaguchi 1997).
Kegunaannya yang beragam menjadikan cabai sebagai salah satu komoditas
andalan yang bernilai ekonomis tinggi. Selain dimanfaatkan sebagai bumbu
masak pada skala rumah tangga, cabai juga digunakan sebagai bahan campuran
dalam berbagai industri pengolahan makanan dan minuman, serta untuk
pembuatan obat-obatan dan kosmetik (Duriat 1996a; Suwandi et al. 2002).
Kandungan vitamin A dan C pada buah cabai yang cukup tinggi merupakan
nilai tambah dari komoditas ini (Kalloo 1988; Rubatzky dan Yamaguchi 1997;
Kusandriani 1996). Rata-rata setiap 100 g buah cabai mengandung 58 kilo kalori,
2.8 g protein, 2.3 g lemak dan 6.6 g karbohidrat, 3 mg kalsium, 18 mg fosfor, 1.3
mg zat besi, 10 000 IU vitamin A dan 16 mg vitamin C (Thai Horticulture 2006).
Sejalan dengan kebutuhan manusia dan teknologi yang semakin
berkembang, permintaan akan ketersediaan cabai semakin meningkat. Sayangnya
peningkatan ini belum diikuti oleh produktivitas nasional cabai yang masih
tergolong rendah. Produktivitas nasional cabai pada tahun 2004 hanya sebesar
6.49 ton/ha dan bahkan mengalami penurunan menjadi 6.39 ton/ha pada tahun
2005 (Deptan 2006). Nilai ini masih sangat kecil dibandingkan dengan potensi
produksi nasional yang dapat mencapai 18 ton/ha (Kusandriani 1996).
Salah satu kendala utama dalam produksi cabai adalah penyakit yang
disebabkan oleh virus. Diketahui terdapat sekitar 45 jenis virus yang dapat
menyerang tanaman cabai (Duriat 1996b). Salah satu virus yang cukup penting
secara ekonomi, yang mengganggu budidaya tanaman cabai adalah chilli veinal
mottle virus (ChiVMV).
ChiVMV merupakan satu dari lima virus yang paling sering menyerang
cabai di Asia (Yoon 1987, diacu dalam Duriat et al. 1995b). Laporan tahunan
AVRDC (2003) menyatakan bahwa ChiVMV adalah virus paling penting yang
menyerang cabai di Asia subtropis dan tropis, dimana virus ini terdapat di 10 dari
2
Di Indonesia, keberadaan ChiVMV telah dilaporkan oleh Duriat et al. pada
tahun 1989 (Sulyo et al. 1995). Berdasarkan hasil survei lapangan yang dilakukan
Taufik et al. (2005) pada 11 lokasi survei yang menyebar di Jawa dan Sulawesi
Selatan dibuktikan bahwa penyebaran ChiVMV di Indonesia cukup luas. Virus ini
selalu ditemukan pada setiap pertanaman cabai yang diamati.
Infeksi ChiVMV pada fase pertumbuhan awal mengurangi ukuran daun
yang diikuti dengan distorsi, serta produksi buahnya lebih sedikit dan lebih kecil
(Shah dan Khalid 2001). Selain itu, akibat infeksi virus ini telah dilaporkan dapat
menyebabkan kehilangan hasil hingga 100% (AVRDC 2003). Ong et al. (1980),
diacu dalam Ang (1995) melaporkan bahwa ChiVMV tidak hanya mengurangi
keseluruhan hasil, tetapi juga kualitas dari buah cabai.
ChiVMV dapat menimbulkan gejala yang bervariasi pada daun tanaman
cabai yang terinfeksi. Gejala pada daun cabai dapat berupa bercak berwarna hijau
tua yang tidak beraturan (belang) dan penebalan tulang daun, permukaan daun
tidak rata, daun menjadi lebih kecil dan kadang diikuti dengan malformasi daun
serta tanaman menjadi kerdil (Siriwong et al. 1995). Keparahan penyakit pada
tanaman tergantung pada kultivar dan waktu infeksi (Chiemsombat dan
Kittipakorn 1996; CABI 2000).
Penyakit yang disebabkan oleh virus pada umumnya sulit dikendalikan.
Hal ini disebabkan oleh beberapa faktor, diantaranya : (1) tanaman yang terinfeksi
tidak dapat disembuhkan dan dapat menjadi sumber inokulum untuk tanaman
disekitarnya; (2) kebanyakan penularan virus di alam terjadi melalui kutu daun
dan bersifat non persisten (Palukaitis et al. 1992); (3) virus umumnya memiliki
kisaran inang yang luas (Matthews 1991) sehingga target pengendalian menjadi
lebih sulit karena penyebaran virus ke seluruh areal pertanaman dapat berlangsung
dalam waktu singkat; dan (4) virus umumnya memiliki keragaman genetik yang
tinggi yang ditunjukkan oleh banyaknya strain virus tersebut yang dapat
menimbulkan gejala atau keparahan penyakit yang berbeda-beda (Palukaitis et al.
1992).
Pengendalian secara konvensional terhadap ChiVMV seringkali tidak
efisien, karena penyebarannya yang sangat cepat secara non-persisten melalui
keberhasilannya adalah dengan menggunakan kultivar tahan (Green dan Kim
1994). Strategi pengendalian penyakit menggunakan kultivar tahan cukup
menjanjikan karena murah, aman dan tidak mencemari lingkungan, tidak
memerlukan keterampilan khusus bagi petani dan dapat mengendalikan virus
kapanpun (Fraser 1992; Duriat 1996b).
Diantara tujuan pemuliaan tanaman cabai di Indonesia adalah perbaikan
daya ketahanan cabai terhadap penyakit. Evaluasi ketahanan beberapa kultivar
cabai terhadap ChiVMV telah beberapa kali dilakukan, namun informasi tentang
pewarisan karakter ketahanan terhadap ChiVMV pada cabai masih sangat sedikit.
Chew dan Ong (1990), diacu dalam Shah dan Khalid (2001) melaporkan
bahwa sepasang gen resesif memberikan ketahanan kepada genotipe-genotipe
terhadap infeksi ChiVMV. Menurut Chew (1993), diacu dalam Green dan Kim
(1994) ketahanan terhadap ChiVMV dikendalikan oleh sepasang gen resesif
(kemungkinan sejumlah gen resisten independen terlibat). Sementara Caranta dan
Palloix (1995) melaporkan bahwa ketahanan terhadap ChiVMV berdasarkan
pengujian terhadap keturunan F1 double haploid hasil persilangan cabai perennial
India dengan “Yolo wonder” dikendalikan oleh dua gen independen, dengan efek
dominan yang jelas.
Informasi tentang pewarisan suatu karakter yang meliputi ada tidaknya efek
maternal, jumlah gen pengendali, aksi gen dan heritabilitas adalah sangat penting
dalam menentukan strategi pemuliaan tanaman selanjutnya agar perbaikan
karakter tersebut menjadi lebih efektif. Dengan mengetahui pola pewarisan suatu
karakter pada tanaman akan memungkinkan bagi kita untuk mengendalikan
pewarisan tanaman dan membentuk tipe baru (Hermiati 2000).
Pada tanaman cabai, ketahanan terhadap ChiVMV dilaporkan telah
ditemukan pada galur tertentu spesies C. annuum, C. frustecens dan C. chinensis
(Green dan Kim 1994). Berdasarkan berbagai penelitian diketahui bahwa tingkat
ketahanan terhadap ChiVMV antar genotipe cabai tidak sama. Hal ini
menunjukkan adanya variabilitas genetik ketahanan terhadap ChiVMV pada
4
Melalui pesilangan antara genotipe cabai yang berbeda karakter
ketahanannya diharapkan mampu memperlihatkan model pewarisannya
berdasarkan sebaran fenotipe pada keturunan F2-nya.
Tujuan Penelitian
Penelitian ini bertujuan untuk
1. Mengevaluasi respon ketahanan beberapa genotipe cabai terhadap infeksi
ChiVMV
2. Mengetahui ada tidaknya efek maternal dalam pewarisan karakter ketahanan
terhadap ChiVMV
3. Menduga jumlah dan aksi gen yang mengendalikan karakter ketahanan
terhadap ChiVMV
4. Menduga nilai heritabilitas dari karakter ketahanan terhadap ChiVMV
Hipotesis
1. Terdapat respon ketahanan yang berbeda dari genotipe cabai terhadap infeksi
ChiVMV
2. Tidak terdapat efek maternal pada pewarisan karakter ketahanan terhadap
ChiVMV
3. Pewarisan karakter ketahanan terhadap ChiVMV pada tanaman cabai
dikendalikan oleh sedikit gen dengan aksi gen sederhana (simple genic)
4. Nilai duga heritabilitas karakter ketahanan terhadap ChiVMV ini adalah
tinggi.
Manfaat Penelitian
Penelitian yang dilakukan diharapkan dapat memberikan informasi
mengenai:
1. Derajat ketahanan beberapa genotipe cabai koleksi yang diuji terhadap infeksi
ChiVMV.
2. Peubah yang efektif untuk seleksi ketahanan tanaman cabai terhadap infeksi
ChiVMV
3. Kendali genetik pewarisan karakter ketahanan tanaman cabai terhadap infeksi
Informasi tersebut diharapkan dapat menjadi bahan masukan dalam menentukan
strategi pemuliaan yang efektif dan efisien untuk menghasilkan kultivar cabai
TINJAUAN PUSTAKA
Syarat Tumbuh Tanaman CabaiTanaman cabai dapat ditanam mulai dari ketinggian permukaan laut hingga
13.000 m. Tanaman ini memerlukan cuaca yang panas untuk pertumbuhannya.
Suhu siang yang ideal untuk pertumbuhan tanaman cabai rata-rata adalah 20oC
hingga 25oC. Pertumbuhan tanaman meningkat ketika suhu malam tidak melebihi
20oC. Bunga tidak terbuahi pada suhu udara di bawah 16°C atau di atas 32°C
karena produksi tepung sari yang tidak baik. Pembungaan dan pembuahan akan
optimum pada suhu antara 20oC dan 25oC (Rubatzky dan Yamaguchi 1997).
Cabai tidak menghendaki curah hujan yang tinggi atau iklim yang basah,
karena pada keadaan tersebut tanaman akan mudah terserang penyakit, terutama
yang disebabkan oleh cendawan. Curah hujan yang baik untuk pertumbuhan
tanaman cabai adalah sekitar 600-1250 mm per tahun (Sumarni 1996).
Tanaman cabai dapat tumbuh pada berbagai jenis tanah, asal drainase dan
aerasi tanah cukup baik. Bila diharapkan panen yang lebih cepat, cabai sebaiknya
ditanam pada tanah lempung berpasir. Bila diharapkan panen lebih lambat cabai
lebih cocok ditanam pada tanah yang lebih berat atau tanah liat. Tanah juga harus
mengandung cukup bahan organik, unsur hara, dan air, serta bebas dari gulma,
nematoda dan bakteri layu. Tingkat kemasaman (pH) tanah: 5.5-6,8 merupakan
keadaan yang baik untuk tanaman cabai (Knott dan Deanon 1970; Knott 1962,
diacu dalam Sumarni 1996). Keadaan pH tanah sangat penting karena erat
kaitannya dengan ketersediaan unsur hara dalam tanah. Apabila ditanam pada
tanah yang mempunyai pH lebih dari 7, tanaman cabai akan menunjukkan gejala
klorosis, yakni tanaman kerdil dan daun menguning yang disebabkan oleh
kekurangan unsur hara besi (Fe). Sebaliknya, pada tanah yang ber-pH kurang dari
5, tanaman cabai juga akan tumbuh kerdil, karena kekurangan unsur hara kalsium
(Ca) dan magnesium (Mg) atau keracunan alumunium (Al) dan mangan (Mn)
(Knott 1962, diacu dalam Sumarni 1996).
Tanah yang paling ideal untuk tanaman cabai adalah yang mengandung
bahan organik sekurang-kurangnya 1.5% dan mempunyai pH 6.0-6.5. Suhu tanah
juga merupakan faktor penting karena sangat erat hubungannya dengan
peningkatan suhu tanah dari 13.3oC menjadi 14.4°C dapat meningkatkan produksi
buah cabai (Knott dan Deanon 1970, diacu dalam Sumarni, 1996).
Biologi Tanaman Cabai
Cabai termasuk tanaman dikotil berbentuk semak, batangnya berkayu, tipe
percabangannya tegak atau menyebar dengan karakter yang berbeda-beda
tergantung spesiesnya. Struktur perakarannya diawali dari akar tunggang yang
sangat kuat, yang bercabang-cabang ke samping dengan akar rambut. Pola
pertumbuhannya vegetatif berupa percabangan-percabangan dikotomi dari batang
utama dan tunas-tunas lateralnya. Daun cabai merupakan daun tunggal dengan
helai daun berbentuk bulat telur lebar atau lanset. Daun berwarna hijau atau hijau
tua, tumbuh pada tunas-tunas samping berurutan, pada batang utama dan tunggal
tersusun secara spiral (Rubatzky dan Yamaguchi 1997).
Bunga tanaman cabai umumnya bersifat tunggal dan tumbuh pada ujung
ruas, serta merupakan bunga sempurna (hermaprodit). Mahkota bunga berwarna
putih atau ungu tergantung kultivarnya, helaian mahkota bunga berjumlah lima
atau enam helai. Diameter mahkota bunga antara 8 – 15 mm, tergantung pada
spesiesnya. Pada dasar bunga terdapat daun buah berjumlah lima helai,
kadang-kadang bergerigi. Setiap bunga memiliki satu putik (stigma), dengan kepala putik
berbentuk bulat. Terdapat lima sampai delapan helai benang sari dengan kepala
sari berbentuk lonjong, berwarna biru keunguan (Greenleaf 1986; Kusandriani
1996).
Pada saat bunga mekar, kotak sari masak dan dalam waktu relatif singkat
tepung sari keluar mencapai kepala putik dengan perantaraan serangga atau angin.
Tepung sari berbentuk lonjong, terdiri dari tiga segmen, berwarna kuning
mengkilat. Dalam satu kotak sari berkembang sekitar 11.000 sampai 18.000 butir
tepung sari. Tepung sari umumnya mempunyai ukuran hampir sama antar kultivar
(Kusandriani 1996).
Ukuran buah cabai beragam dari pendek sampai panjang, sedangkan
ujungnya runcing atau tumpul. Bentuk buah umumnya memanjang. Kedudukan
buah adalah buah tunggal pada masing-masing ruas (ketiak daun) atau
kadang-kadang fasciculate. Permukaan kulit dan warna buah bervariasi dari halus sampai
kadang-8
kadang ungu pada waktu muda dan menjadi merah waktu matang (Greenleaf
1986; Kusandriani 1996).
Buah cabai berongga dengan jumlah rongga bergantung pada kultivarnya. Di
dalam rongga buah terdapat plasenta tempat melekatnya biji. Ukuran rongga buah
berbeda-beda tergantung ukuran buah. Daging buah renyah, tetapi kadang-kadang
lunak tergantung pada kultivarnya. Buah mengandung banyak biji yang terletak di
dalam buah, melekat pada plasenta. Umumnya biji cabai berwarna putih
kekuningan berbentuk ginjal dan keras, kecuali biji C. pubescens yang berwarna
hitam (Kusandriani 1996).
Cabai termasuk tanaman yang menyerbuk sendiri, meskipun demikian
penyerbukan silang dapat terjadi di lapangan, terutama oleh serangga dan angin.
Di antara kultivar-kultivar cabai terdapat perbedaan dalam hal letak kepala putik
terhadap kotak sari yang disebut heterostyly. Persilangan sering terjadi pada bunga
yang memiliki tangkai putik (stylus) yang panjang dan kepala putik (stigma) yang
lebih tinggi daripada kotak sari. Penyerbukan sendiri terjadi pada bunga yang
memiliki tangkai putik yang pendek, sehingga letak kepala putik lebih rendah
daripada kotak sari (Greenleaf 1986; Kusandriani 1996).
Protogyny, yaitu fase dimana putik mencapai masa siap dibuahi (receptive)
sebelum tepung sari (pollen) masak, terjadi pada beberapa spesies cabai. Hal ini
penting dalam mencegah terjadinya penyerbukan silang untuk menjaga kemurnian
varietas cabai (Kusandriani 1996).
Kemampuan bersilang antar spesies (species crossability) bervariasi,
walaupun semua populasi alami adalah diploid dengan jumlah kromosom 2n = 2x
= 24. Namun demikian, pada persilangan antar spesies tertentu terdapat halangan
(barrier) (Greenleaf 1986; Kusandriani 1996).
Hama dan Penyakit Tanaman Cabai
Hama dan penyakit adalah kendala biologis yang sering dihadapi dalam
usahatani cabai. Hama yang paling sering merugikan meliputi trip (Thrips
parvispinus Karny), tungau (Polyphagotarsonemus latus Banks.) dan kutu daun
(Myzus parsicae Sulz. dan Aphis gossypii) (Rubatzky dan Yamaguchi 1997).
Penyakit yang sangat merugikan dan merupakan kendala biologis terpenting
gloeosporioides. Patogen ini mulai menyerang saat buah menjelang matang dan
seringkali menjadi penyakit pascapanen (Black et al. 1991).
Selain cendawan, patogen lain yang seringkali sangat merugikan usahatani
cabai adalah virus (Black et al. 1991). Diketahui terdapat sekitar 45 jenis virus
yang dapat menyerang tanaman cabai (Duriat 1996b). Berbeda dengan antraknosa
yang serangan awalnya terjadi pada buah, virus terutama menyerang bagian
vegetatif tanaman. Oleh karena itu serangan virus pada perkembangan awal
tanaman dapat menyebabkan kerugian hingga 100% (Green dan Kim 1991).
Virus sebagai Patogen Tanaman
Virus adalah satu unit molekul asam nukleat yang biasanya terbungkus
dalam protein atau lipoprotein pembungkus, berukuran sangat kecil, dapat
berreplikasi hanya di dalam sel inang yang sesuai, dan berkemampuan
menyebabkan penyakit (Matthews 1991). Dari 2000 virus yang telah diketahui,
seperempatnya dapat menyerang dan menyebabkan penyakit pada tumbuhan.
Virus menyebabkan penyakit tidak dengan cara mengkonsumsi sel atau
membunuhnya dengan toksin, tetapi dengan menggunakan substansi sel inang,
mengisi ruangan dalam sel dan mengganggu proses dan komponen seluler, yang
selanjutnya mengacaukan metabolisme sel dan menyebabkan kondisi dan
substansi sel abnormal yang mengganggu fungsi dan kehidupan sel atau
organisme (Agrios 1997).
Virus masuk ke dalam jaringan tumbuhan antara lain melalui luka yang
dibuat secara mekanik atau oleh vektor atau masuk ke dalam ovule bersama
tepung sari yang terinfeksi. Infektivitas virus sangat ditentukan oleh bagian asam
nukleatnya, yang pada sebagian besar virus tumbuhan berupa RNA. Beberapa
jenis virus tumbuhan membutuhkan enzim RNA transkriptase untuk
memperbanyak diri dan menginfeksi. Kemampuan RNA virus memproduksi baik
RNAnya sendiri maupun protein tertentu, menunjukkan bahwa RNA membawa
faktor genetik tertentu (Matthews 1991; Bos 1994).
lnfeksi tanaman oleh virus terjadi jika virus mampu memperbanyak diri di
dalam sel awal yang terinfeksi dan mampu pindah dari sel yang satu ke sel yang
lain sehingga menyebar secara sistemik di dalam jaringan tanaman (Mathews
10
merupakan penghubung antar sel. Perpindahan melalui plasmodesmata tersebut
terjadi antara lain dengan bantuan movement proteins (MPs) yang berfungsi
meningkatkan ukuran plasmodesmata dan mengikat RNA virus untuk melewati
plasmodesmata. Adanya MPs tersebut menyebabkan virus dapat melewati
plasmodesmata walaupun diameter virus lebih besar daripada diameter
plasmodesmata. Sebagian besar virus dapat dengan cepat terangkut dalam jarak
jauh melalui floem. Apabila virus telah masuk ke dalam floem, maka selanjutnya
virus tersebut dengan cepat menuju titik tumbuh atau menuju daerah pemanfaatan
bahan makanan seperti umbi dan rhizome (Agrios 1997; Mathews 1991).
Chilli Veinal Mottle Virus (ChiVMV)
Chilli veinal mottle virus (ChiVMV) adalah virus paling penting yang
menyerang cabai di Asia subtropis dan tropis, dimana virus ini terdapat di 10 dari
11 negara yang disurvei (AVRDC 2002). Hasil survei lapangan yang dilakukan
Taufik et al. (2005a) pada 11 lokasi yang menyebar di Jawa dan Sulawesi Selatan
membuktikan bahwa penyebaran ChiVMV di Indonesia cukup luas. Virus ini
selalu ditemukan pada setiap pertanaman cabai yang diamati.
ChiVMV tergolong ke dalam genus Potyvirus, famili Potyviridae. Potyvirus
merupakan kelompok terbesar diantara virus-virus yang menyerang tanaman
(Agrios 1997). Partikel virus berbentuk filamen, tidak beramplop dan lentur.
Panjang partikel 750 sampai 765 nm dan diameter 12 sampai 13 nm (Siriwong et
al. 1995, diacu dalam CABI 2000). Genom ChiVMV merupakan utas tunggal
RNA dan genom diekspresikan sebagai poliprotein, dengan berat molekul sekitar
9.7 kb (Hull 2002). ChiVMV membentuk badan inklusi yang berbentuk cakra
(pinwheel) (Hull 2002; Samad 1986, diacu dalam Lee et al. 1994).
ChiVMV dapat ditularkan secara mekanik, melalui penyambungan dan
serangga vektor. Serangga yang menjadi vektor bagi ChiVMV adalah A.
craccivora, A. gossypii, A. spiraecola, M. persicae, Toxoptera citricidus,
Hysteroneura setariae, dan Rhopalosiphum maydis. ChiVMV bersifat non
persisten dan tidak dapat ditularkan melalui benih (Ong et al. 1978, diacu dalam
Ang 1995; Ong et al. 1979, diacu dalam Murayama et al. 1998).
ChiVMV memiliki kisaran inang yang cukup luas, meliputi gulma dan
tabaccum, N. glutinosa, N. megalosiphon, N. benthamiana, N. sylvestris, Physalis
floridana, P. minima, Datura stramonium, D. metel, L. esculentum, Nicandra
physalodes, Petunia hybrida, dan S. melongena (CABI 2000). Infeksi ChiVMV
pada fase pertumbuhan awal mengurangi ukuran daun yang diikuti dengan
distorsi, serta produksi buahnya lebih sedikit dan lebih kecil (Shah dan Khalid,
2001). Selain itu, akibat infeksi virus ini telah dilaporkan dapat menyebabkan
kehilangan hasil lebih dari 50 % di Malaysia (Ong et al.1979, 1980, diacu dalam
Shah dan Khalid 2001). AVRDC (2003) bahkan melaporkan bahwa kehilangan
hasil akibat infeksi ChiVMV bisa mencapai 100%. Ong et al. (1980), diacu
dalam Ang (1995) melaporkan bahwa ChiVMV tidak hanya mengurangi
keseluruhan hasil, tetapi juga kualitas dari buah cabai.
ChiVMV dapat menimbulkan gejala yang bervariasi pada daun tanaman
cabai yang terinfeksi. Gejala pada daun cabai dapat berupa bercak berwarna hijau
tua yang tidak beraturan (belang) dan penebalan tulang daun, permukaan daun
tidak rata, daun menjadi lebih kecil dan kadang diikuti dengan malformasi daun
serta tanaman menjadi kerdil (Siriwong et al 1995, diacu dalam Taufik et al.
2005b). Keparahan penyakit pada tanaman tergantung pada kultivar dan waktu
infeksi (Chiemsombat dan Kittipakorn 1996; CABI 2000).
Pemuliaan untuk Ketahanan Tanaman terhadap Virus
Secara umum ada tiga metode yang biasa digunakan untuk mengendalikan
virus. Pertama, menghilangkan sumber inokulum di lapangan diantaranya dengan
cara melakukan eradikasi tanaman yang telah terinfeksi virus, dan membersihkan
gulma yang menjadi inang virus. Kedua, mencegah atau menghambat penyebaran
virus dari satu pertanaman ke pertanaman lain. Karena virus sebagian besar
ditularkan oleh serangga, maka pencegahan penyebaran virus dapat dilakukan
dengan mengendalikan serangga vektor, baik secara kimiawi maupun biologis.
Ketiga adalah dengan menggunakan kultivar tahan (Harrison 1987).
Diantara berbagai metode pengendalian virus tersebut, penggunaan kultivar
tahan adalah yang paling baik. Di samping memberikan kepastian pengendalian
virus yang lebih baik, metode ini merupakan yang paling murah, aman, tidak
mencemari lingkungan, tidak memerlukan ketrampilan khusus bagi petani dan
12
1992). Namun demikian, oleh karena virus umumnya memiliki kisaran inang yang
sangat luas, penggunaan kultivar tahan harus dibarengi dengan metode
pengendalian lain, seperti pembersihan gulma inang virus dan pengendalian
serangga vektor (Palukaitis et al.).
Tanaman yang tahan terhadap virus adalah tanaman yang mampu
menghambat replikasi dan penyebaran virus di dalam tanaman atau perkembangan
gejala (Russell 1981). Tahan adalah karakter tanaman yang berkebalikan dari
rentan, dan dapat dikelompokkan menjadi sangat tahan, tahan, dan rentan.
Ketahanan ini dapat diwujudkan sebagai kemampuan tanaman untuk membatasi
perkembangan virus dalam sel tertentu sehingga virus tidak menyebar ke sel-sel
yang lain (Greenleaf 1986; Matthews 1991). Matthews (1991) juga menyatakan
bahwa mekanisme ketahanan dalam tanaman dapat berupa penghambatan dalam
penyebaran virus dari: 1) sel yang terinfeksi ke sel sekitarnya (penyebaran antar
sel), 2) sel parenkima ke jaringan pengangkut (penyebaran antar jaringan), dan 3)
jaringan pengangkut ke sel parenkima daun baru (penyebaran antar organ
tanaman).
Ketahanan tanaman terhadap virus dapat dikelompokkan menjadi tiga tipe,
yaitu ketahanan non-inang (non-host resistance), ketahanan kultivar, dan
ketahanan terinduksi (Fraser 1987). Ketahanan non-inang adalah bila seluruh
individu dari suatu spesies tidak dapat terinfeksi oleh suatu jenis virus tertentu.
Spesies tersebut memang bukan inang bagi virus yang dimaksud. Ketahanan
kultivar adalah kultivar tertentu tahan terhadap virus yang dapat menginfeksi
kultivar lain dalam spesies tersebut. Sedangkan ketahanan terinduksi adalah
ketahanan yang muncul pada suatu spesies rentan akibat terinduksi oleh suatu
kondisi tertentu, seperti ketahanan yang timbul akibat proteksi silang strain atau
jenis virus lain. Di antara ketiga tipe ketahanan tersebut, hanya ketahanan kultivar
saja yang dapat bermanfaat bagi program pemuliaan.
Konsep ketahanan terhadap penyakit diungkapkan oleh Flor pada tahun
1942 melalui hipotesis gene for gene (Plank Van der 1986). Dalam konsep ini
dikemukakan bahwa setiap gen yang mengendalikan sifat tahan pada tanaman
inang memiliki pasangan gen komplementer yang mengendalikan sifat virulensi
mengendalikan sifat tahan pada tanaman inang berpasangan dengan gen avirulen
patogen. Bila patogen memiliki gen virulen pada pasangan tersebut, maka inang
akan menunjukkan reaksi rentan (Plank Van der 1986; Fehr 1987) . Interaksi
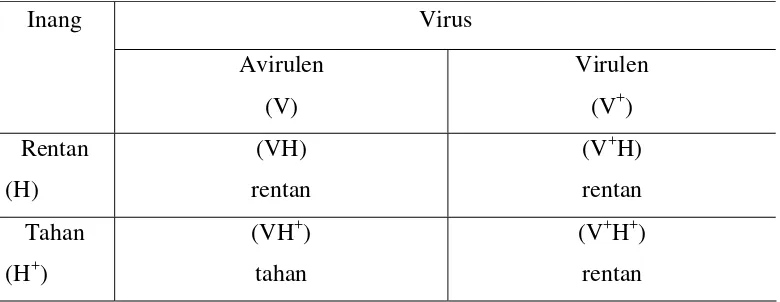
inang dan virus dapat digambarkan dalam model interaksi seperti pada Tabel 1.
Tabel 1. Interaksi antara gen tanaman inang dan gen virus
Virus
sumber: van der Plank, 1968
Respon tahan hanya terjadi jika inang tahan berinteraksi dengan virus
avirulen. Respon rentan terjadi jika inang rentan berinteraksi dengan virus
avirulen atau virulen, atau inang tahan berinteraksi dengan virus virulen.
Fraser (1992) menyatakan bahwa alel resisten dominan sempurna umumnya
berkaitan dengan mekanisme lokalisasi virus yang melibatkan lesio lokal. Alel
dominan atau resesif tidak sempurna memungkinkan virus menyebar ke seluruh
tanaman, tetapi menghambat multiplikasi virus atau perkembangan gejala.
Sedangkan alel resesif penuh mungkin berkaitan dengan kekebalan.
Tahapan yang penting dalam program pemuliaan tanaman untuk
menghasilkan varietas yang tahan terhadap penyakit adalah mendapatkan sumber
ketahanan dan menentukan pola pewarisan sifat ketahanan tanaman inang serta
sifat genetik dan interaksi antara inang dengan patogen (Hayes dan Johnson 1971;
Allard 1960; Russel 1981). Tahapan tersebut dapat dilaksanakan dengan baik jika
pengkajian dilakukan pada lingkungan epidemik bagi patogen, baik dalam
laboratorium, rumah kaca maupun di lapang. Masalah yang sering dihadapi
adalah: 1) penentuan dan penilaian ketahanan, 2) identifikasi genetik dari sifat
ketahanan yang melibatkan interaksi gen yang tidak sealel, kaitan gen, serta
14
Penentuan dan penilaian ketahanan diperlukan untuk membedakan antara
tanaman yang tahan dan rentan secara tepat. Untuk keperluan tersebut maka
dalam setiap pengujian dan seleksi ketahanan tanaman perlu diusahakan
terciptanya kondisi lingkungan epidemik yang mampu memberikan kondisi
epifitotik patogen (Russell 1981).
Metode yang umum dilakukan untuk membuat kondisi seluruh tanaman
yang teruji terinfeksi virus adalah melakukan inokulasi buatan. Hal yang perlu
diperhatikan untuk mendapatkan keberhasilan inokulasi buatan adalah: 1)
inokulum harus tetap bermutu tinggi, 2) penerapan inokulasi sedapat mungkin
diusahakan seragam untuk setiap tanaman, 3) kondisi lingkungan pada saat
inokulasi dan dalam jangka waktu inkubasi harus sesuai bagi pertumbuhan parasit
yang bersangkutan, dan 4) tanaman inang yang akan diuji harus bebas dari
penyakit lain dan harus dalam keadaan fisiologik yang cocok untuk terjadinya
infeksi atau serangan patogen (Green 1991).
Tanaman tahan dan tanaman rentan dapat dibedakan dengan mudah jika
ketahanan dikendalikan oleh satu atau dua gen mayor. Pada keadaan tersebut
ragam ketahanan akan menunjukkan sebaran terputus atau diskontinyu. Seringkali
pada ketahanan yang dikendalikan oleh banyak gen, tidak ada perbedaan yang
jelas antara individu tanaman tahan dan tanaman rentan dalam populasi yang
bersegregasi dan ragam ketahanan tersebut akan menunjukkan sebaran yang
kontinyu dengan perubahan perbedaan ketahanan yang kecil. Oleh karena itu
Russell (1981) menyatakan sangat penting sekali untuk melakukan pengukuran
atau pendugaan terhadap besarnya intensitas serangan dengan sistem pemberian
nilai skor atas gejala yang muncul (indeks penyakit).
Varietas tanaman yang tahan virus dapat dirakit melalui seleksi plasma
nutfah dan persilangan antar tetua terpilih. Sifat tahan ini dapat berasal dari
varietas yang berbeda, varietas komersial, spesies liar sekerabat, spesies lain
dalam satu genus, atau genus lain (Kallo 1988; Niks et al. 1993). Dalam upaya
tersebut diperlukan adanya beberapa persyaratan yang harus dipenuhi antara lain:
(1) diantara tanaman yang dibudidayakan, terdapat genotipe yang tahan terhadap
dengan sifat agronomis yang tidak diinginkan, dan (3) pemindahan gen dari
tanaman tahan ke tanaman penerima harus dapat dilakukan melalui hibridisasi.
Evaluasi genotipe dan kultivar cabai untuk ketahanan terhadap ChiVMV
telah banyak dilakukan, dan dilaporkan adanya genotipe-genotipe atau kultivar
yang memiliki potensi untuk digunakan sebagai sumber gen ketahanan terhadap
ChiVMV (Green dan Kim 1994; Duriat et al. 1995a,1995b; Ang 1995; Dolores
1995; Chiemsombat dan Kittipakorn 1995, Sulyo et al. 1995).
Transfer gen ketahanan terhadap virus dari genotipe donor ke genotipe
penerima umumnya dilakukan melalui seri persilangan silang balik. Persilangan
antar varietas dalam satu spesies adalah yang paling mudah karena memiliki
tingkat keberhasilan yang tinggi. Apabila sifat yang diharapkan berada pada
spesies lain maka perlu dilakukan persilangan antar spesies. Salah satu hal yang
sering menjadi kendala adalah adanya inkompatibilitas antar spesies yang cukup
tinggi (Greenleaf 1986).
Agar program pemuliaan yang dilakukan menjadi efektif, pola pewarisan
karakter dimaksud terlebih dahulu harus diketahui. Informasi tentang ada tidaknya
efek maternal, aksi dan jumlah gen pengendali, serta nilai duga heritabilitas adalah
sangat penting. Karakter yang pewarisannya dikendalikan oleh efek maternal
menandakan bahwa gen pengendali karakter tersebut berada di luar inti (Mather
dan Jink 1982). Ada tidaknya efek maternal dapat diuji dengan membandingkan
data pengamatan pada F1 dan F1-resiprok (F1R).
Apabila terdapat pewarisan sitoplasmik atau pengaruh tetua betina maka
keturunan persilangan resiproknya masing-masing akan berbeda, dan
keturunannya hanya memperlihatkan ciri dari tetua betina (Gardner et al. 1991),
sehingga untuk mempelajari pola pewarisannya antara keturunan F1 dan F1R-nya
tidak dapat digabung, karena segregasi populasi F2-nya akan berbeda dan
menyimpang dari hukum Mendel. Sebaliknya, apabila tidak terdapat pewarisan
secara sitoplasmik atau pengaruh tetua betina, persilangan resiproknya akan
memberikan hasil yang sama, sehingga antara keturunan F1 dan F1R-nya dapat
digabungkan.
Petr dan Frey (1966) menggunakan pendugaan terhadap nilai potensi rasio
16
resesif. Potensi rasio adalah nisbah selisih nilai tengah kedua tetua (mid parent)
dari rata-rata populasi F1 terhadap nilai tengah kedua tetua (mid parent) dari
rata-rata tetua tertinggi. Mather dan Jink (1982) mengemukakan bahwa aksi gen
dominan atau resesif dapat juga diketahui melalui besaran nilai pendugaan
parameter genetik dominan [h].
Aksi gen dominan atau resesif sangat menentukan dalam pelaksanaan
metode silang balik (back cross). Pada karakter yang dikendalikan oleh gen
resesif, diperlukan uji progeni pada setiap tahapan seleksi karena individu yang
mengandung gen ketahanan tidak dapat dipisahkan langsung pada populasi silang
balik yang dihasilkan Pada karakter yang dikendalikan oleh gen dominan, maka
individu tahan dapat langsung diseleksi dari populasi silang balik tanpa harus
melalui uji progeni (Halloran et al. 1979; Fehr 1947).
Penampilan karakter suatu tanaman dapat digolongkan menjadi dua
kelompok, yaitu karakter kualitatif dan karakter kuantitatif (Poehlman 1987).
Karakter-karakter kualitatif umumnya dikendalikan oleh sedikit gen (monogenic
ataupun oligogenic) yang dicirikan dengan sebaran fenotipe pada generasi F2-nya
diskontinyu, pengaruhnya secara individu mudah dikenali (gen mayor), cara
pewarisannya sederhana, tidak atau sedikit dipengaruhi lingkungan, sehingga
memiliki nilai duga heritabilitas yang tinggi, dan penyidikan pengaruh gen dapat
dilakukan dengan genetika Mendel (Allard 1961; Fehr 1987, Poehlman 1987).
Karakter-karakter kuantitatif umumnya dikendalikan oleh banyak gen (poligenic)
yang dicirikan dengan variasi fenotipik pada generasi F2-nya menyebar normal
(kontinyu) dengan pembagian kelas fenotip yang perbedaannya tidak jelas dan
sulit diidentifikasi karena pengaruh masing-masing gen secara individu terhadap
ekspresi suatu sifat adalah kecil (gen minor) dan bersifat kumulatif, ekspresinya
sangat dipengaruhi oleh lingkungan, sehingga memiliki nilai duga heritabilitas
yang rendah (Allard 1961; Fehr 1987; Poehlman 1987).
Pendugaan awal apakah suatu karakter dikendalikan oleh gen mayor, gen
minor atau keduanya sekaligus dilakukan melalui pengamatan sebaran frekuensi
pada populasi F2. Sebaran frekuensi F2 diskret menandakan bahwa karakter
dimaksud dikendalikan oleh gen mayor. Sebaran terusan satu puncak dan normal
sebaran terusan dengan dua puncak atau lebih, maka karakter tersebut
dikendalikan oleh beberapa gen mayor dan gen minor sekaligus (Fehr 1987)
Analisis genetik untuk karakter yang dikendalikan oleh gen mayor biasanya
dilakukan dengan analisis genetika Mendel, yaitu membandingkan nisbah
frekuensi fenotipik hasil pengamatan pada populasi F2 terhadap nisbah Mendel,
atau nisbah fenotipik tertentu dengan uji Chi-Kuadrat (Fehr 1987; Crowder 1993).
Untuk keperluan ini fenotipe pada populasi F2 dikelompokkan ke dalam
kelas-kelas tertentu sesuai dengan jumlah kelas-kelas dalam nisbah pembanding. Pendekatan
ini menghasilkan dugaan jumlah dan aksi gen yang bersegregasi untuk karakter
yang dipelajari.
Tidak semua turunan yang bersegregasi dapat dipisahkan ke dalam
kategori-kategori tertentu yang nyata dengan rasio yang sederhana. Variasi rasio Mendel
dijelaskan dengan dasar interaksi gen, yaitu: pengaruh satu alel dengan alel
lainnya pada lokus yang sama (intra alelik) dan pengaruh satu gen pada satu lokus
terhadap gen pada lokus yang lainnya (inter alelik).
Persilangan yang melibatkan satu pasangan alel (interaksi alel-alel pada
lokus yang sama), berdasarkan hukum Mendel, dapat memberikan konsekuensi
rasio fenotipik keturunan F2 hasil hibridisasi sebagai berikut (Strickberger 1972):
(1) 3:1 (satu gen bersifat dominan sempurna atau satu gen dengan aksi gen alel
ganda), (2) 1:2:1 (satu gen bersifat dominan sebagian), dan (3) 1:2 (satu gen
dengan aksi gen lethal).
Persilangan yang melibatkan dua pasang alel yang memberikan pengaruh
pada penampilan karakter yang sama (interalelik), berdasarkan hukum segregasi
dan kombinasi secara bebas dari Mendel, akan memberikan konsekuensi rasio
fenotipik keturunan F2 hasil hibridisasi sebagai berikut (Strickberger 1972):
(1) 9:3:3:1 (dua pasang gen bersifat dominan sempurna; fenotipe baru
dihasilkan dari interaksi di antara homozigos dominan maupun resesif)
(2) 9:3:4 (dua pasang gen bersifat dominan sempurna, tetapi satu pasang gen
bila berada dalam keadaan homozigot resesif akan memberikan pengaruh
kepada pasangan yang lain).
(3) 9:7 (dua pasang gen bersifat dominan sempurna, tetapi keduanya bila berada
18
(4) 12:3:1 (dua pasang gen bersifat dominan sempurna, tetapi satu pasang gen
bila berada dalam keadaan homozigot dominan akan memberikan pengaruh
kepada pasangan yang lain).
(5) 15:1 (dua pasang gen bersifat dominan sempurna, tetapi keduanya bila
berada dalam keadaan homozigot resesif akan saling memberikan
pengaruh).
(6) 13:3 (dua pasang gen bersifat dominan sempurna, tetapi satu pasang gen bila
berada dalam keadaan dominan akan memberikan pengaruh kepada
pasangan gen ke-dua, dan pasangan gen ke-dua bila berada dalam keadaan
homozigot resesif akan memberikan pengaruh kepada pasangan gen
pertama).
(7) 9:6:1 (dua pasang gen bersifat dominan sempurna; interaksi di antara
pasangan dominan akan memunculkan fenotipe baru).
(8) 7:6:3 (dua pasang gen, dengan satu pasang gen bersifat dominan sempurna
dan pasangan gen yang lain bersifat dominan sebagian; pasangan gen yang
pertama jika berada dalam keadaan homozigos resesif akan memberikan
pengaruh kepada pasangan gen ke-dua).
(9) 6:3:3:4 (dua pasang gen, dengan satu pasang gen bersifat dominan
sempurna dan pasangan gen yang lain bersifat dominan sebagian;
masing-masing bila berada dalam keadaan homozigot resesif saling memberikan
pengaruh, dan bila kedua pasangan gen hadir bersama dalam keadaan
homozigos resesif, pasangan gen ke-dua akan memberikan pengaruh pada
pasangan gen pertama).
(10) 7:4:3:2 (dua pasang gen, dengan satu pasang gen bersifat dominan
sempurna dan pasangan gen yang lain bersifat dominan sebagian; fenotipe
heterozigot gen dominan sebagian sama dengan homozigot resesif pada
pasangan gen dominan sempurna, dan menimbulkan suatu pengaruh aditif
bila keduanya muncul bersama).
(11) 1:2:2:1:4:1:2:2:1 (dua pasang gen bersifat dominan sebagian dan
menimbulkan pengaruh aditif untuk setiap bagian gen dominan).
Nilai duga heritabilitas adalah parameter yang sangat penting dalam
didefinisikan sebagai proporsi total variabilitas yang disebabkan oleh faktor
genetik terhadap variabilitas fenotipik suatu karakter (Allard 1960; Fehr 1987;
Crowder 1993). Heritabilitas tipe ini dikenal sebagai heritabilitas arti luas (broad
sense heritability) (h2bs), dan dihitung sebagai nisbah ragam genetik terhadap
ragam fenotipe.
Kontribusi genetik suatu individu merupakan nilai kumulatif dari komponen
genetik aditif, komponen genetik dominan dan komponen interaksi (epistasis).
Komponen genetik aditif merupakan komponen yang dapat tetap diwariskan,
karena itu karakter-karakter yang memiliki proporsi komponen aditif yang besar
sangat diharapkan dalam bidang pemuliaan. Falconer (1989) merumuskan
heritabilitas sebagai proporsi ragam genetik aditif terhadap ragam fenotip, yang
menggambarkan seberapa besar suatu karakter diwariskan ke keturunannya.
Heritabilitas tipe ini dikenal sebagai heritabilitas arti sempit (narrow sense
heritability) (h2ns), dan dihitung sebagai nisbah ragam genetik aditif terhadap
ragam fenotip (Falconer 1989).
Heritabilitas bukan merupakan besaran yang konstan. Besarnya nilai duga
heritabilitas sangat bergantung pada metode pendugaan yang digunakan. Beberapa
metode yang biasa digunakan meliputi: metode pendugaan komponen ragam,
metode regresi tetua dan keturunan, dan metode pendugaan ragam lingkungan
secara tidak langsung (Fehr 1987). Metode lain, yang biasa digunakan untuk
menduga heritabilitas arti sempit, adalah dengan menggunakan populasi silang
balik (Warner 1952). Klasifikasi tinggi rendahnya heritabilitas suatu karakter
ditentukan oleh tinggi rendahnya nilai duga yang diperoleh. Menurut Stansfield
(1983), heritabilitas dianggap rendah bila h2 < 0.2, sedang bila 0.2 ≤ h2 ≤ 5 0.5,
dan tinggi bila h2> 0.5.
Apapun metode yang digunakan, ada beberapa asumsi yang harus dipenuhi
untuk mendapatkan nilai duga heritabilitas yang akurat. Asumsi tersebut meliputi:
1) tidak ada interaksi non-alelik, 2) tidak ada interaksi genetik x lingkungan, 3)
tidak ada interaksi antar gen, dan 4) ragam lingkungan pada populasi F2 dan silang
balik adalah sama (Warner 1952). Tidak terpenuhinya asumsi-asumsi
20
Uji Skala (Scaling Test) dan Uji Skala Gabungan (Joint Scaling Test) adalah
metode yang dapat digunakan untuk menguji ada tidaknya interaksi non-alelik
(epistasis) ataupun interaksi genetik x lingkungan melalui pengujian kesesuaian
model aditif - dominan (Singh dan Chaudary 1979; Mather dan Jink 1982).
Hubungan nilai tengah antar generasi yang mengikuti model aditif-dominan
merupakan indikasi tidak ada interaksi non-alelik ataupun interaksi genetik x
lingkungan.
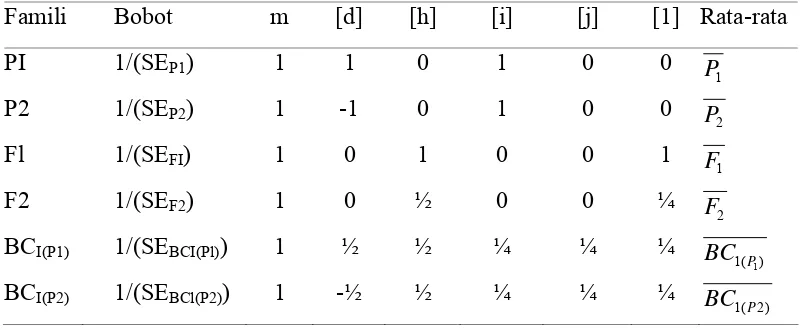
Uji skala gabungan juga dapat digunakan untuk melacak model genetik yang
sesuai, sekaligus menduga nilai parameter nilai tengah generasi (m), parameter
genetik aditif [d], dominan [h], interaksi genetik aditif x aditif [i], interaksi genetik
aditif x dominan [j], dan interaksi dominan x dominan [1]. Berdasarkan nilai duga
parameter genetik tersebut dapat diketahui komponen genetik yang
Tempat dan Waktu Penelitian
Percobaan dilaksanakan di rumah kaca Kebun UF IPB, Tajur dan di rumah
kaca kedap serangga Departemen Proteksi Tanaman Faperta IPB, Cikabayan, dari
bulan Juli 2005 sampai dengan bulan Oktober 2006. Analisis laboratorium
dilakukan di laboratorium Virologi Faperta IPB.
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah 13 genotipe cabai koleksi
AVRDC serta 2 kultivar lokal Tit Super dan Jatilaba koleksi Bagian Genetika dan
Pemuliaan Tanaman. Sebagai bahan penguji digunakan inokulum ChiVMV isolat
Cikabayan, koleksi laboratorium Virologi Tumbuhan Departemen Proteksi
Tanaman Faperta IPB.
Metode Penelitian
Untuk menguji hipotesis yang telah disajikan pada bab sebelumnya maka
metode dan pelaksanaan penelitian dibagi menjadi tiga tahapan seperti yang dapat
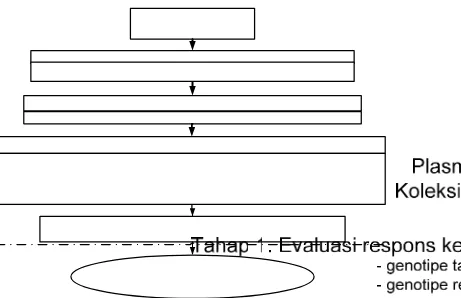
dilihat pada bagan alir penelitian (Gambar 1) yaitu:
1. Evaluasi respon ketahanan tanaman terhadap infeksi ChiVMV
Kegiatan ini dimaksudkan untuk meguji hipotesis 1, yaitu bahwa terdapat
respon ketahanan terhadap infeksi ChiVMV yang bervariasi pada genotipe cabai
yang diuji. Selain itu, kegiatan ini juga dimaksudkan untuk memilih tetua yang
paling tahan dan yang paling rentan sebagai bahan pembuatan populasi dalam
studi pewarisan ketahanan terhadap inveksi ChiVMV.
Percobaan dilakukan dalam 2 tahap. Evaluasi tahap I, yang merupakan
evaluasi pendahuluan, dilakukan terhadap 13 genotipe cabai. Pengamatan
dilakukan terhadap kejadian penyakit (KP) berdasarkan ELISA. Paling sedikit
digunakan 30 tanaman untuk setiap genotipe yang diinokulasi. Evaluasi ketahanan
tahap II dilakukan terhadap genotipe terpilih hasil evaluasi tahap I, yang mewakili
genotipe dengan karakter tahan dan sangat rentan. Evaluasi tahap II ini dilakukan
dengan rancangan acak lengkap (RAL) 2 faktor (genotipe dan perlakuan
22
pada genotipe-genotipe terpilih. Pengamatan dilakukan terhadap kejadian
penyakit, intensitas gejala, dan titer virus.
Gambar 1. Bagan Alir Penelitian Pewarisan Karakter Ketahanan Tanaman Cabai terhadap Infeksi chilli veinnal motle virus
Kejadian penyakit (KP) adalah proporsi tanaman yang menunjukkan reaksi
ELISA positif dalam suatu populasi tanaman tertentu pada 14 HSI. Intensitas
gejala diukur berdasarkan tingkat keparahan gejala yang muncul (indeks gejala)
secara visual. Titer virus diduga melalui nilai absorban ELISA yang dapat
menggambarkan tinggi rendahnya konsentrasi virus pada tanaman setelah
tanaman terinfeksi. Peubah tersebut merupakan tolok ukur ketahanan tanaman
terhadap infeksi virus (Green 1991). Genotipe yang paling tahan adalah yang
menunjukkan respon KP paling rendah, intensitas serangan paling rendah, dan
tingkat konsentrasi virus paling rendah.
Perbedaan respon antar genotipe cabai terhadap infeksi ChiVMV dilihat
berdasarkan peringkat ketahanan mengikuti peringkat yang dikemukakan oleh
koefisien variasi fenotipik menggunakan rumus Singh dan Chaudhary (1979);
Steel dan Torrie (1981).
%
Dengan KK, s dan X berturut-turut adalah koefisien keragaman, standar deviasi,
dan nilai rata-rata pengamatan. Untuk menentukan tinggi rendahnya keragaman
respon berdasarkan koefisien keragaman mengikuti pengelompokan yang
dikemukakan oleh Mattjik dan Sumertajaya (2000), yaitu rendah (KK < 20%),
sedang (20% ≤ KK ≤ 25%), dan tinggi (KK > 25%).
Koefisien korelasi antar peubah yang diamati dihitung berdasarkan rumus
Singh dan Chaudhary (1979); Steel dan Torrie (1981) sebagai berikut:
y
Menurut Young (1982) dikutip Djarwanto dan Subagyo (1993) derajat
keeratan hubungan antar peubah yang dianalisis dapat dilihat dari nilai koefisien
korelasinya (r). Nilai 0.7 < r < 1.0 menunjukkan keterkaitan yang erat, 0.4 < r ≤
0.7 sedang, dan r ≤ 0.2 adalah tidak berkaitan.
2. Pembuatan materi kegenetikaan untuk studi pola pewarisan
Persilangan dilakukan secara buatan (Gambar 2) antara tetua yang memiliki
karakter tahan terhadap infeksi ChiVMV dengan tetua rentan. Persilangan
dilakukan antara pukul 9.00 – 11.00 pagi (saat hari cerah). Bunga tetua betina
dipilih yang masih kuncup, tetapi telah mencapai ukuran penuh. Pada fase ini
diperkirakan putik sudah matang tetapi kotak sari belum pecah. Emaskulasi
dilakukan dengan cara membuka mahkota bunga dan membuang seluruh benang
24
Gambar 2. Teknik persilangan buatan pada cabai. A. Bunga betina yang siap diserbuki; B. Kastrasi; C. Emaskulasi; D. Hasil kastrasi dan emaskulasi; E. Bunga jantan siap diambil serbuksarinya; F. Pengambilan serbuksari; G. Hasil pengumpulan serbuksari; H. Pernyerbukan dengan pinset; I. Penyerbukan menggunakan tabung; J. Pemasangan label; K. Isolasi menggunakan isolatif; L. Setelah diisolasi dan dilabel (Sumber: Yunianti 2007)
Setiap kali akan digunakan untuk emaskulasi, pinset terlebih dahulu
dicelupkan ke dalam alkohol 70% dan dikeringkan. Hal ini dilakukan untuk
menghindari kontaminasi terhadap bunga yang diemaskulasi oleh serbuk sari dari
bunga yang diemaskulasi sebelumnya (Greenleaf, 1986).
Bunga yang telah diemaskulasi selanjutnya diserbuki dengan serbuk sari
bunga tetua jantan yang diambil dari bunga mekar yang masih segar. Penyerbukan
dilakukan segera setelah emaskulasi guna menghindari persilangan yang tidak
satu minggu. Bunga tersebut diberi label kecil pada tangkainya, bertuliskan
kombinasi persilangan dan tanggal persilangan.
Buah dipanen pada saat telah berwarna merah penuh, yang merupakan tanda
buah telah matang. Ekstraksi biji dilakukan dengan membelah buah secara
membujur, biji-bijinya dikeluarkan dan dijemur sampai kering. Biji dari buah
hasil persilangan (F1, F1R, BC1(P1), dan BC1(P2)) dan hasil silang dalam tanaman F1
diekstraksi secara terpisah untuk masing-masing buah.
3. Studi Pola Pewarisan Ketahanan terhadap ChiVMV
Bahan percobaan yang digunakan adalah satu set populasi hasil persilangan
tetua tahan dan tetua rentan ChiVMV yang diseleksi pada tahap sebelumnya. Satu
set populasi tersebut terdiri atas tetua tahan (P1), tetua rentan (P2), hasil
persilangan antara tetua tahan dan tetua rentan (F1), hasil persilangan resiproknya
(F1R), silang balik dengan tetua tahan (BC1(P1)), silang balik dengan tetua rentan
(BC1(P2)) dan keturunan kedua hasil persilangan (F2).
Populasi tanaman dalam famili F2 berasal dari satu tanaman F1. Sejumlah
buah F1 diambil secara acak, kemudian benihnya dicampur. Jumlah buah yang
diambil disesuaikan dengan jumlah tanaman minimum yang diperlukan dalam
famili F2.
Jumlah tanaman minimum dalam F2 ditentukan berdasarkan perhitungan
populasi minimum yang diperlukan untuk memperoleh paling sedikit satu
genotipe yang diinginkan. Rumus yang digunakan untuk menentukan besarnya
populasi minimum adalah sebagai berikut (Burnham, 1961):
…….(Rumus 3)
dengan n, F dan q berturut-turut adalah jumlah tanaman minimum yang
dibutuhkan, taraf kesalahan (α) yaitu 0.05, dan peluang kegagalan mendapatkan
genotipe yang diinginkan.
Dengan asumsi bahwa ketahanan terhadap ChiVMV dikendalikan paling
banyak oleh tiga gen, maka jumlah tanaman minimum pada populasi F2 adalah
26
Peubah yang diamati adalah indeks penyakit dan nilai absorban ELISA
untuk menduga titer virus.
Pelaksanaan Percobaan
1. Pembibitan
Sebelum disemai, benih terlebih dahulu direndam dalam air panas (50oC)
selama satu jam untuk menghilangkan hama dan patogen yang menempel pada
kulit biji dan mempercepat perkecambahan. Benih disemai di baki yang berisi
campuran tanah dan pupuk kandang matang (1:1), yang telah disterilisasi, dengan
kedalaman lubang 0.5 – 1 cm. Baki kemudian ditutup dengan kain lembab hingga
benih berkecambah.
Bibit berumur 3 minggu setelah semai dipindahkan ke polibag berdiameter
40 cm yang berisi 8 kg media steril (campuran tanah dan pupuk kandang dengan
perbandingan 1:1 berdasarkan volume). Pemeliharaan dilakukan di rumah kaca
kedap serangga. Selama pembibitan, kelembaban harus tetap dijaga. Penyiraman
dilakukan secukupnya, tidak terlampau basah, sebab dapat mengakibatkan
damping off. Pemupukan dilakukan pada saat tanaman berumur dua minggu,
melalui penyemprotan pupuk daun Gandasil D (1.5 g/l) bersamaan dengan
pencegahan hama dan penyakit, dengan frekuensi seminggu sekali. Pencegahan
hama dan penyakit dilakukan dengan insektisida Curacron, Supracide, Furadan
3G dan Kelthane, bakterisida Dithane M-45 dan fungisida Antracol dengan dosis
sesuai anjuran.
2. Inokulasi
Inokulasi dilakukan secara mekanik (Gambar 3). Inokulum disiapkan
dengan cara menggerus daun tanaman yang terinfeksi ChiVMV dalam mortar
steril bersama dengan larutan penyangga fosfat 0.01 M, pH 7, dengan
perbandingan 1 g daun terinfeksi virus per 5 ml larutan penyangga fosfat (1:5
b/v). Inokulasi dilakukan dengan cara mengoleskan sap tersebut ke permukaan
daun tanaman yang akan diuji dengan bola kapas secara hati-hati, segera setelah
penggerusan. Inokulasi dilakukan pada dua helai daun termuda yang telah
membuka penuh (4 – 5 minggu setelah semai). Sebelum diinokulasi permukaan
pelukaan, agar infeksi virus dapat terjadi pada saat pengolesan. Pengolesan sap
dimulai dari bagian pangkal daun ke bagian ujung secara searah, tanpa
mengulangi pada daerah yang sama. Segera setelah pengolesan sap dilakukan
pembilasan sisa-sisa sap yang masih melekat pada permukaan daun tanaman uji
menggunakan air mengalir. Inokulasi diulang satu minggu setelah inokulasi
pertama, untuk memastikan seluruh tanaman dapat terinfeksi.
Gambar 3. Teknik inokulasi virus secara mekanis. A. Tanaman cabai yang siap diinokulasi (± umur 4 mss); B. Persiapan inokulum; C. Penaburan bahan abrasive pada permukaan daun yang akan diinokulasi; D dan E. Pengolesan sap inokulum dengan bola kapas; F. Pembilasan sisa-sisa sap setelah inokulasi.
Dalam penelitian ini digunakan isolat ChiVMV asal Cikabayan.
Berdasarkan hasil penelitian Taufik (2005) diketahui bahwa isolat ChiVMV asal
Cikabayan memiliki virulensi yang lebih baik karena dapat menginfeksi hampir
semua galur inang diferensial yang digunakannya. Berdasarkan reaksinya pada
inang diferensial, diketahui bahwa isolat ChiVMV asal Cikabayan adalah strain
yang berbeda dengan isolat-isolat lainnya. Perbanyakan isolat virus dilakukan
dengan cara menularkan virus dari tanaman terinfeksi ke tanaman paprika (C.
28
3. Pengamatan
Tipe Gejala. Tipe gejala ditunjukkan oleh tekstur warna dan penampilan
pada daun termuda yang telah membuka penuh. Tipe gejala infeksi ChiVMV
secara umum adalah belang berwarna hijau tua dan pemucatan pada tulang daun,
mosaik serta kelainan bentuk pada daun. Belang merupakan bercak-bercak tanpa
batas yang jelas. Mosaik adalah bercak-bercak kekuningan yang dibatasi dengan
tulang daun. Tipe gejala ini diklasifikasikan berdasarkan tingkat keparahan atau
kualitasnya untuk kemudian diindeks.
Intensitas Gejala. Intensitas gejala diukur berdasarkan indeks gejala yang
diamati pada 5 minggu setelah inokulasi (awal fase generatif). Indeks gejala untuk
infeksi ChiVMV pada tanaman cabai ditentukan berdasarkan tipe gejala (Gambar
4) seperti pada Tabel 2. Penghitungan intensitas gejala dilakukan dengan
menggunakan rumus 4, dan pengelompokan tanaman berdasarkan tingkat
ketahanannya terhadap ChiVMV dilakukan sesuai dengan kriteria Dolores (1996)
seperti tertera pada Tabel 3.
Gambar 4. Tipe gejala infeksi ChiVMV: 0. Tidak ada gejala; 1. Belang ringan; 2. Belang dan permukaan daun tidak rata; 3. Belang berat dan atau malformasi daun serta pengkerdilan tanaman (Sumber: koleksi pribadi dan kutipan dari CABI 2000)
Intensitas gejala (I) dihitung dengan rumus:
(
)
% 100
× ×
×
=
∑
V N
v n
dengan n adalah jumlah tanaman pada tiap indeks gejala, v = indeks gejala pada
tiap tanaman yang diamati, N = jumlah total tanaman yang diamati, dan V =
indeks gejala tertinggi, yaitu 3.
Tabel 2. Penentuan indeks gejala pada tanaman cabai yang terinfeksi ChiVMV Indeks Gejala Gejala
0
belang dan permukaan daun tidak rata
belang berat dan atau malformasi daun serta pengkerdilan
tanaman
Tabel 3. Penentuan peringkat ketahanan tanaman cabai terhadap ChiVMV
Intensitas Serangan
(%)
Hasil ELISA Peringkat Ketahanan *
0
Titer Virus. Uji serologi dilakukan dengan DAS-ELISA (Double antibody
sandwich- Enzyme-link imunosorbance assay) untuk menduga titer virus pada
tanaman (Green 1991). Pengujian dilakukan terhadap daun termuda yang telah
berkembang penuh, satu minggu setelah inokulasi terakhir. Deteksi dilakukan
dengan DAS-ELISA sesuai petunjuk dari DSMZ-Plant Virus Collection
(Braunschweig, Germany). Tahapan uji tersebut adalah Coating, sumuran plat
mikrotiter diisi dengan 200μl antiserum ChiVMV yang telah disuspensikan ke
dalam bufer coating. Plat mikrotiter diinkubasikan pada suhu 37oC selama 2 – 4
jam. Setelah proses inkubasi selesai, plat mikrotiter dicuci dengan PBST dengan