DISTRIBUSI LOGAM BERAT PADA KERANG HIJAU
(
Perna viridis
) DARI PERAIRAN KAMAL MUARA,
TANGERANG - JAKARTA
ASIH RAHAYU
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR BOGOR
DISTRIBUSI LOGAM BERAT PADA KERANG HIJAU
(
Perna viridis
) DARI PERAIRAN KAMAL MUARA,
TANGERANG - JAKARTA
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Perikanan pada
Departemen Teknologi Hasil Perairan
DEPARTEMEN TEKNOLOGI HASIL PERAIRAN
FAKULTAS PERIKANAN DAN ILMU KELAUTAN
INSTITUT PERTANIAN BOGOR
BOGOR
2014
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA*
Dengan ini saya menyatakan bahwa skripsi berjudul Distribusi Logam Berat pada Kerang Hijau (Perna viridis) dari Perairan Kamal Muara, Tangerang-Jakarta adalah benar karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, 6 Mei 2014
Asih Rahayu
ABSTRAK
ASIH RAHAYU. Distribusi Logam Berat Kerang Hijau (Perna viridis) dari Perairan Kamal Muara, Tangerang-Jakarta. Dibimbing oleh RUDDY SUWANDI dan PIPIH SUPTIJAH.
Kerang merupakan hewan filter feeder yang menyaring makanan menggunakan insang sehingga memungkinkan terjadinya akumulasi bahan logam dalam tubuh. Sifat utama logam berat adalah sulit didegradasi, sehingga keberadaannya secara alami sulit terurai. Penelitian dilaksanakan di Laboratorium Karakteristik Bahan Baku Hasil Perairan, Departemen Teknologi Hasil Perairan untuk preparasi dan untuk analisis logam di Laboratorium MIPA Bersama, Fakultas Peternakan, Institut Pertanian Bogor dari bulan November 2013 hingga Januari 2014. Tujuan dari penelitian ini untuk menentukan penyebaran kandungan logam berat kerang hijau pada berbagai ukuran dengan bagian tubuh yaitu daging, insang, dan jeroan dengan menggunakan metode Atomic absorption spectrophotometer.
Hasil penelitian menunjukkan logam tertinggi pada kerang hijau (Perna viridis) yaitu Cu. Distribusi logam berdasarkan ukuran kerang (besar, sedang, dan kecil) pada daging, insang, dan jeroan yaitu ukuran besar (1,667 ± 0,104 ppm; 1,329 ± 0,05 ppm; dan 1,542 ± 0,064 ppm), sedang (1,517 ± 0,05 ppm; 1,427 ± 0,073 ppm; dan 2,512 ± 0,05 ppm), dan kecil (1,521 ± 0,210 ppm; 1,101 ± 0,028 ppm; dan 1,655 ± 0,127 ppm).
Kata kunci: daging, insang, jeroan, kerang hijau (Perna viridis) ABSTRACT
Shells are filter feeder animals which use gills to shift feed. This process accumulated metallic substance in the body. The nature of major heavy metal is difficult be degraded, so easy to be accumulated in aquatic environment and natural substance. The research was carried out at Laboratory of Raw Material Characteristic of Aquatic Product, Departement of Aquatic Product Technology, Faculty of Fisheries and Marine Science for preparation; metal analyses at Laboratory MIPA Bersama, Faculty of Animal Science, Bogor Agriculture University from November 2013 to January 2014. Objectives of this study is to determine the distribution of heavy metal on variety of size and body part of green mussle that are meet, gills, and viscera using Atomic absorption spectrophotometer.
Result showed the highest metal in sample is Cu. Based on the size shells metal distribution on meat, gills, and the viscera were large (1.667 ± 0.104 ppm; 1.329 ± 0.05 ppm; and 1.542 ± 0.064 ppm), medium (1.517 ± 0.05 ppm; 1.427 ± 0.073 ppm; and 2.512 ± 0.05 ppm), and small (1.521 ± 0.210 ppm; 1.101 ± 0.028 ppm; and 1.655 ± 0.127 ppm).
© Hak Cipta Milik IPB, Tahun 2014 Hak Cipta Dilindungi Undang-Undang
Dilarang mengutip sebagian atau seluruh karya tulis ini tanpa mencantumkan atau menyebutkan sumbernya. Pengutipan hanya untuk kepentingan pendidikan, penelitian, penulisan karya ilmiah, penyusunan laporan, penulisan kritik, atau tinjauan suatu masalah; dan pengutipan tersebut tidak merugikan IPB
Judul Skripsi : Distribusi Logam Berat pada Kerang Hijau (Perna viridis) dari Perairan Kamal Muara, Tangerang-Jakarta
Nama : Asih Rahayu
NIM : C34100069
Program Studi : Teknologi Hasil Perairan
Disetujui oleh
Dr Ir Ruddy Suwandi, MS, MPhil Pembimbing I
Dra Pipih Suptijah, MBA Pembimbing II
Diketahui oleh
Prof Dr Ir Joko Santoso, MSi Ketua Departemen
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada kehadirat Allah subhanahu wa ta’ala, atas segala rahmat, karunia, serta hidayah-Nya sehingga skripsi ini dapat diselesaikan. Skripsi yang berjudul Distribusi Logam Berat pada Kerang Hijau (Perna viridis) dari Perairan Kamal Muara, Tangerang-Jakarta merupakan salah satu syarat memperoleh gelar sarjana perikanan di Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor. Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu dalam penulisan skripsi ini, terutama kepada:
1 Dr Ir Ruddy Suwandi, MS, MPhil selaku dosen pembimbing I, atas segala bimbingan dan pengarahan yang diberikan kepada penulis.
2 Dr Dra Pipih Suptijah, MBA selaku dosen pembimbing II, atas segala bimbingan dan pengarahan yang diberikan kepada penulis.
3 Dr Ir Sri Purwaningsih MSi selaku dosen penguji.
4 Staff Dosen dan Administrasi Departemen Teknologi Hasil Perairan, Institut Pertanian Bogor
5 Kedua orangtua tersayang yang telah memberikan cinta, kasih sayang, dan doanya kepada penulis. Kakak Adi Susanto dan Adik Arya Wiranata yang telah memberikan semangat dan dukungan kepada penulis.
6 Maya Sofia, Suwindyastuti, Yani Doremi, Khalida Hanum, Mulita Indiani, Sakti Mahardika selaku tim dalam satu pembimbing atas kebersamaan dan semangat yang telah diberikan.
7 Widya Lestari, Frianka Anindea, Novitha Sari, dan teman-teman THP 47 atas kebersamaan dan semangat yang diberikan.
8 Bapak Ade Kamal Muara, kakak kelas THP 45, dan 46 yang telah membantu penulis atas informasi yang mendukung penyelesaian skripsi ini. 9 Semua pihak yang telah membantu penulis yang tidak dapat disebutkan
satu persatu.
Penulis menyadari bahwa skripsi ini memiliki banyak kekurangan. Penulis mengharapkan saran dan kritik yang bersifat membangun untuk perbaikan. Semoga skripsi ini bermanfaat bagi semua pihak yang memerlukannya.
Bogor, 6 Mei 2014
DAFTAR ISI
DAFTAR TABEL... V
DAFTAR GAMBAR ... V
DAFTAR LAMPIRAN ... V
PENDAHULUAN ... 1
Latar Belakang ... 1
Perumusan Masalah ... 2
Tujuan Penelitian ... 2
Manfaat Penelitian ... 2
Ruang Lingkup Penelitian ... 3
METODE PENELITIAN ... 3
Waktu dan Tempat ... 3
Bahan ... 3
Alat ... 3
Lokasi Pengambilan Kerang Hijau (Perna viridis) ... 3
Prosedur Penelitian ... 3
Prauji Logam Berat (AOAC 2002) ... 4
Analisis Logam Berat dengan Atomic absorption spechtrophotometer (AAS) .. 5
HASIL DAN PEMBAHASAN ... 6
Morfometrik Kerang Hijau (Perna viridis) ... 6
Kandungan Logam Berat Hg ... 7
Kandungan Logam Berat Cd ... 8
Kandungan Logam Berat Pb ... 9
Kandungan Logam Berat Cu ... 11
KESIMPULAN DAN SARAN ... 12
Kesimpulan ... 12
Saran ... 13
DAFTAR PUSTAKA ... 13
LAMPIRAN ... 15
DAFTAR TABEL
1 Morfometrik dan bobot utuh kerang hijau berdasarkan ukuran ... 6
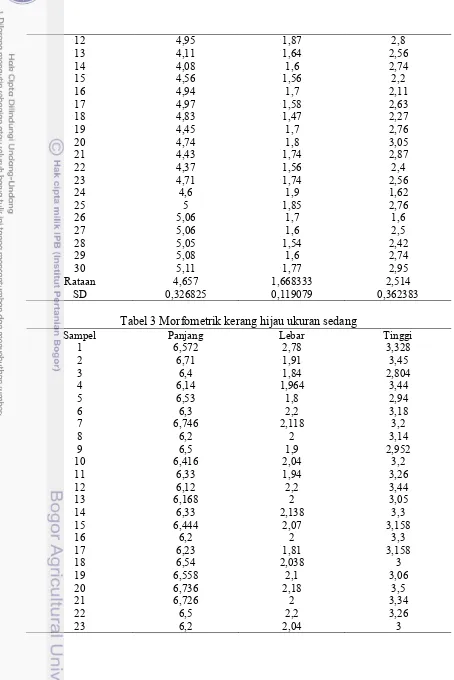
2 Morfometrik kerang hijau ukuran kecil ... 17
3 Morfometrik kerang hijau ukuran sedang ... 18
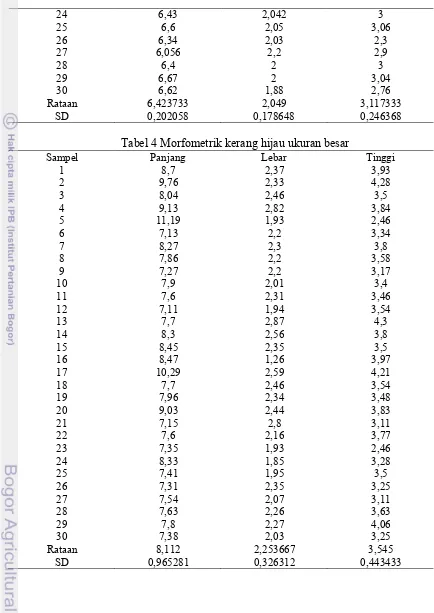
4 Morfometrik kerang hijau ukuran besar ... 19
5 Kandungan logam berat Hg ... 20
6 Kandungan logam berat Cd ... 20
7 Kandungan logam berat Pb ... 20
8 Kandungan logam berat Cu ... 20
DAFTAR GAMBAR
1 Diagram alir penelitian ... 42 Kerang hijau (Perna viridis) ... 6
3 Diagram kandungan logam berat Hg ... 7
4 Diagram kandungan logam berat Cd ... 8
5 Diagram kandungan logam berat Pb ... 10
6 Diagram kandungan logam berat Cu ... 11
DAFTAR LAMPIRAN
1 Alat spektrofotometer AAS ... 162 Bagian organ dalam kerang ... 16
3 Morfometrik sampel... 16
4 Data statistik ... 16
5 Data morfometrik kerang hijau (Perna viridis) ... 17
PENDAHULUAN
Latar Belakang
Laut merupakan tempat bermuaranya aliran sungai yang memiliki potensi sebagai tempat berkumpunya zat-zat pencemar. Zat tersebut umumnya berasal dari kegiatan industri dan aktivitas manusia. Peningkatan jumlah industri dan aktivitas manusia akan selalu diikuti oleh pertambahan jumlah limbah. Limbah yang dihasilkan sangat bervariasi tergantung dari jenis dan ukuran industri, pengawasan pada proses industri, derajat penggunaan air, dan derajat pengolahan air limbah yang ada. Banyaknya pabrik ataupun industri, seringkali membuang limbah ke sungai tanpa adanya pengolahan terlebih dahulu. Limbah yang terbuang mengandung bahan kimia beracun dan berbahaya terbawa oleh aliran sungai, yang pada akhirnya bermuara ke laut sehingga akan mencemari lingkungan.
Salah satu perairan laut yang kualitas perairannya sudah melewati batas ambang baku mutu kualitas perairan menurut kriteria Men KLH (1988) adalah Teluk Jakarta. Hal ini diduga adanya masukan limbah ke dalam perairan yang dibawa oleh 13 sungai yang bermuara ke dalamnya. Masuknya limbah ke perairan dapat menimbulkan pencemaran terhadap perairan sehingga mengkontaminasi perairan sungai maupun laut dan akan berakumulasi dalam rantai makanan. Logam berat dapat masuk dan terakumulasi dalam tubuh biota akuatik misalnya udang, cumi-cumi, dan kekerangan. Golongan moluska terutama jenis kekerangan merupakan komoditas hasil perairan yang memiliki nilai ekonomis penting yang dapat dilihat dari volume produksi. Volume produksi perikanan tangkap khususnya kerang di Indonesia pada periode tahun 2004-2012 mengalami fluktuasi, yaitu sebesar 4 ton, 5 ton, 1.515 ton, 420 ton, 14 ton, 30 ton, 447 ton, dan 2.867 ton, 2.970 ton dengan kenaikan rata-rata tahun 2010-2012 sebesar 272,49 % (KKP 2013).
Kehidupan kerang khususnya kerang hijau dapat dijumpai di daerah pasang surut yang memiliki subsrat berlumpur dan berpasir. Subsrat mengandung berbagai macam bahan organik maupun anorganik yang diperlukan untuk metabolisme. Bahan diabsorpsi dari perairan yang terkontaminasi memungkinkan adanya logam berat yang masuk dan terakumulasi dalam tubuh. Logam berat tersebut di antaranya merkuri (Hg), cadmium (Cd), tembaga (Cu), dan timbal (Pb). Bahan pencemar logam berat umumnya berasal dari daratan. Pencemaran logam yang masuk ke lingkungan laut umumnya terjadi akibat adanya buangan limbah industri yang masuk melalui tiga cara yaitu pembuangan industri yang tidak dikontrol, lumpur minyak yang mengandung logam berat dengan kandungan tinggi, serta adanya pembakaran minyak hidrokarbon dan batubara di daratan (Payung et al. 2013). Logam terakumulasi melalui proses rantai makanan sehingga terjadi biotransformasi dan biomagnifikasi pada tubuh organisme termasuk manusia. Semakin tinggi kadar logam berat di suatu perairan, semakin tinggi pula logam berat yang terakumulasi dalam tubuh biota.
2
terkontaminasi oleh cemaran. Kemampuan dalam mengakumulasi logam berat, yang memungkinkan kerang hijau digunakan untuk memperoleh gambaran tingkat pencemaran pada lingkungan (Apriadi 2005). Hal ini disebabkan kerang dapat mengakumulasi logam lebih besar daripada hewan air lainnya karena habitat hidupnya menetap, lambat untuk menghindari diri dari pengaruh polutan, mempunyai toleransi yang tinggi terhadap logam tertentu, dan mempunyai toleransi yang besar terhadap tekanan ekologis yang tinggi.
Perumusan Masalah
Kegiatan industri meliputi rumah tangga, pertanian, dan pertambangan seringkali menghasilkan buangan limbah yang tidak digunakan kembali ke lingkungan. Akibatnya, lingkungan menjadi tercemar. Pencemaran lingkungan diikuti dengan peningkatan industri dan aktivitas manusia. Bahan pencemar dari hasil aktivitas manusia berupa bahan berbentuk padat, cair, dan gas. Bahan tersebut berujung mengalir ke muara perairan pada suatu lingkungan, yang memberikan dampak tersendiri terhadap biota dan mengganggu kesetimbangan biologis. Logam berat termasuk salah satu bahan pencemar yang dihasilkan dari kegiatan industri. Limbah ini dikategorikan ke dalam bahan beracun berbahaya (B3) kerena efek samping yang ditimbulkannya apabila masuk ke dalam tubuh organisme termasuk manusia. Hal ini dapat dilakukan pengujian logam berat terhadap biota untuk membuktikan biota tersebut aman atau tidak untuk dikonsumsi. Metode uji dengan alat Atomic absorption spectrophotometer (AAS) sering digunakan dalam uji logam untuk medeteksi kandungan logam pada biota khususnya kerang.
Tujuan Penelitian
Penelitian ini bertujuan untuk menentukan penyebaran kandungan logam berat pada berbagai ukuran dengan bagian tubuh kerang hijau (Perna viridis) yaitu bagian daging, insang, dan jeroan.
Manfaat Penelitian
Ruang Lingkup Penelitian
Ruang lingkup penelitian ini adalah pengambilan contoh sampel yang berasal dari perairan Kamal Muara, pengukuran morfometrik, pengujian logam berat, serta penulisan laporan.
METODE PENELITIAN
Waktu dan Tempat
Penelitian dilaksanakan pada bulan November 2013 hingga Januari 2014. Pengambilan contoh dilakukan di Kamal Muara, Tangerang-Jakarta. Preparasi bahan baku dan perhitungan morfometrik dilakukan di Laboratorium Karakteristik Bahan Baku Hasil Perairan, Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan. Analisis logam berat dilakukan di Laboratorium Bersama MIPA Kimia, Fakultas Peternakan, Institut Pertanian Bogor.
Bahan
Bahan baku yang digunakan adalah kerang hijau (Perna viridis). Bahan untuk analisis logam berat yaitu asam nitrat p.a 65 %, asam perkhlorat p.a 70-72 %, dan air bebas ion.
Alat
Alat yang digunakan untuk preparasi bahan baku adalah timbangan analitik, jangka sorong, dan pisau dapur. Alat yang digunakan untuk analisis logam yaitu
Atomic absorption spectrophotometer (AAS) tipe Shimadzu 7000 (Lampiran 1), botol plastik, cawan porselen, gelas ukur, labu erlenmeyer, desikator, dan hot plate.
Lokasi Pengambilan Kerang Hijau (Perna viridis)
Pengambilan kerang hijau dari Kamal Muara dilakukan nelayan di wilayah pantai pada koordinat 06o05’00”LS - 06o04’30”LS dan 93o25’00”BT - 93o30’00”BT. Penentuan koordinat berdasarkan acuan peta yang diperoleh dari Badan Koordinasi Survei dan Pemetaan Nasional (BAKOSURTANAL) dengan skala 1 : 25.000. Perahu yang digunakan dalam pengambilan sampel memiliki volume 12 m x 2 m x 2 m dengan anak buah kapal (ABK) berjumlah 2 orang.
Prosedur Penelitian
4
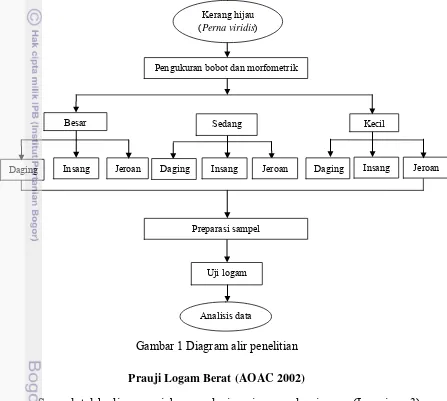
kondisi sampel masih segar. Langkah awal penelitian yaitu kerang hijau dilakukan pengukuran bobot utuh dan morfometrik meliputi panjang, lebar, dan tinggi berdasarkan ukuran. Sampel kemudian dilakukan preparasi dengan memisahkan bagian daging, insang, dan jeroan (Lampiran 2). Sampel yang telah dipreparasi, diuji logam berat dengan alat Atomic absorption spectrophotometer (AAS). Diagram penelitian disajikan pada Gambar 1.
Gambar 1 Diagram alir penelitian Prauji Logam Berat (AOAC 2002)
Sampel telah dipreparasi berupa daging, insang, dan jeroan (Lampiran 3). Bagian-bagian tersebut sebelum dianalisis dengan alat Atomic absorption spectrophotometer (AAS), dilakukan preparasi terlebih dahulu. Langkah awal yang dilakukan yaitu destruksi sebanyak 1 gram contoh ditimbang ke dalam erlenmeyer, ditambahkan 5 ml asam nitrat p.a, dan 1 ml asam perkhlorat p.a, didiamkan satu malam. Esoknya sampel dipanaskan pada suhu 100 ˚C selama 1 jam 30 menit, suhu ditingkatkan menjadi 130 ˚C selama 1 jam, kemudian suhu ditingkatkan lagi menjadi 150 ˚C selama 2 jam 30 menit (sampai uap kuning habis, bila masih ada uap kuning, waktu pemanasan ditambah). Setelah uap kuning habis, suhu ditingkatkan menjadi
Daging Insang Jeroan Daging Insang Jeroan Daging Insang Jeroan
Besar Sedang Kecil
Uji logam
Analisis data Preparasi sampel
Pengukuran bobot dan morfometrik Kerang hijau
5
170 ˚C selama 1 jam, kemudian suhu ditingkatkan lagi menjadi 200 ˚C selama 1 jam
(terbentuk uap putih). Destruksi selesai dengan terbentuknya endapan putih. Ekstrak didinginkan kemudian diencerkan dengan air bebas ion menjadi 10 ml, lalu dikocok.
Analisis Logam Berat dengan Atomic absorption spechtrophotometer (AAS) Spektrofotometer serapan atom merupakan alat untuk menganalisis unsur-unsur logam dan mineral dalam jumlah renik (trace). Teknik ini didasarkan pada absorpsi, emisi, dan fluoresensi dari radiasi elektromagnetik oleh partikel-parikel atom. Sampel dalam hal ini perlu diatomisasi untuk mendapatkan spektrum ultraviolet dan sinar tampak lalu diubah menjadi partikel atom berbentuk gas. Spektrum absorpsi, emisi, dan fluoresensi dari atom suatu unsur yang terdiri dari sejumlah garis dengan panjang atom tertentu (Anderson 1999).
Analisis Data Metode Deskriptif
Kandungan logam berat dilakukan dengan mengukur logam yang terdapat pada daging, insang, dan jeroan serta dibandingkan dengan kandungan maksimum logam berat dalam tubuh moluska menurut baku mutu BSN (2009) mengenai batas maksimum cemaran logam dalam produk pangan dan FAO (1972) mengenai food composition table for use in East Asia.
Statistik Rancangan Acak Faktorial
Data hasil penelitian dianalisis dengan menggunakan model satatistik rancangan acak faktorial (RAF) yang meliputi kelompok (ukuran), perlakuan (pemisahan bagian tubuh), dan ulangan (Lampiran 4). Model statsitik disajikan sebagai berikut.
Keterangan:
Yijk = Nilai pengamatan pada percobaan ke-k yang memperoleh kombinasi
HASIL DAN PEMBAHASAN
Morfometrik Kerang Hijau (Perna viridis)
Kerang hijau (Perna viridis) merupakan salah satu biota yang mampu bertahan hidup dan berkembangbiak pada tekanan ekologis yang tinggi, bersifat filter feeder, dandominan hidup pada ekosistem litoral (wilayah pasang surut) dan sublitoral yang dangkal.
Hendirk dan Cappenberg (2008) menyatakan bahwa kerang hijau hidup pada perairan estuari, teluk, dan daerah mangrove dengan kondisi lingkungan yang dasar perairannya pasir berlumpur, serta salinitas yang tidak terlalu tinggi. Umumnya hidup menempel dan bergerombol pada subsrat yang keras yaitu batu karang, kayu, bambu dengan bantuan bysus. Kerang hijau tergolong dalam hewan sessile yang hidup bergantung pada ketersediaan zooplankton, fitoplankton, dan material yang kaya akan bahan organik. Sampel yang digunakan disajikan pada Gambar 2.
Sumber: Dokumentasi pribadi 2013 Gambar 2 Kerang hijau (Perna viridis)
Kerang hijau dibagi atas tiga kelompok ukuran yaitu ukuran kecil (4-5 cm) dengan umur panen 3-4 bulan, sedang (6-7 cm) dengan umur panen 5-6 bulan, dan besar (> 7 cm) dengan umur panen > 6 bulan. Penetapan ini berdasarkan hasil wawancara langsung dengan nelayan pembudidaya kerang hijau di perairan Kamal Muara, Tangerang-Jakarta. Pengukuran morfometrik sampel kerang hijau meliputi panjang, lebar, dan tinggi cangkang berdasarkan ukuran dari 30 sampel yang digunakan disajikan pada Tabel 1.
Tabel 1 Morfometrik dan bobot utuh kerang hijau berdasarkan ukuran
Ukuran Parameter Bobot utuh
(gram) Panjang (cm) Lebar (cm) Tinggi (cm)
Besar 8,112 ± 0,965 3,545 ± 0,443 2,254 ± 0,326 14,247 ± 4,676
Sedang 6,424 ± 0,202 3,117 ± 0,246 2,049 ± 0,179 8,367 ± 1,245
Kecil 4,657 ± 0,327 2,514 ± 0,362 1,668 ± 0,119 4,574 ± 1,049
Keterangan: data diperoleh dari 30 kerang hijau pada masing-masing ukuran
7
laju perubahan waktu. Hal ini terkait dengan besarnya penyerapan bahan dari lingkungan yang mengandung logam. Igwemmar et al. (2013) menyatakan bahwa besarnya penyerapan logam berat bergantung pada kondisi ekologi, fisika, kimia, dan biologi perairan setempat.
Kondisi ekologi berhubungan dengan habitat kerang hijau. Kerang hijau yang diperoleh dari Muara Kamal dengan perairan dalam kondisi tercemar memiliki kandungan bahan organik yang tinggi serta kaya unsur hara. Bahan organik dihasilkan dari masukan limbah industri, kegiatan domestik, dan pertanian berupa padat, cairan, ataupun gas.
Kandungan Logam Berat Hg
Hasil uji logam berat Hg kerang hijau (Perna viridis) pada berbagai ukuran tubuh (besar, sedang, dan kecil) disajikan pada Gambar 3.
Gambar 3 Diagram kandungan logam berat Hg ( )Besar ( ) Sedang ( ) Kecil
Gambar 3 menunjukkan hasil uji distribusi logam berat Hg pada kerang hijau rataan tertinggi terakumulasi pada bagian insang kerang besar yaitu 10,34 ± 0,48 ppb, sedang 62,42 ± 0,86 ppb, dan kecil 18,38 ± 0,05 ppb. Insang merupakan organ yang berperan menyaring partikel bahan yang masuk ke dalam tubuh. Pengaturan atau ekskresi bahan umumnya terjadi melalui insang, usus, jeroan, dan urin. Penelitian Ambedkar (2013) mengenai bioakumulasi dan distribusi logam berat pada jaringan tubuh bivalvia Parreysia corrugate terhadap kandungan logam berat Hg dengan perlakuan perbedaan waktu paparan 10 hari dan 20 hari didapatkan hasil tertinggi terletak pada bagian insang sebesar 25,61 ± 3,81 ppm dan 54,51 ± 4,73 ppm. Kandungan akumulasi logam berat bergantung pada jenis jaringan kerang dan sifat kimia logam.
8
berbagai bagian tubuh (p > 0,05). Hasil uji BNT pada selang kepercayaan 95 % bahwa kerang ukuran kecil memberikan pengaruh nyata terhadap distribusi logam berat Hg dengan hasil yang diperoleh sebesar 0,6902 ppb. Suyanto et al. (2010) menyatakan bahwa logam berat yang masuk ke dalam jaringan tubuh melalui beberapa jalan yaitu saluran pernapasan (insang), pencernaan (makanan), dan penetrasi kulit yang diabsorpsi oleh darah dan didistribusikan ke seluruh jaringan tubuh. Insang pada kerang merupakan perluasan permukaan tubuh yang membentuk lembaran tipis berfungsi untuk meningkatkan area permukaan pertukaran gas.
Merkuri dalam perairan diserap oleh biota akuatik dalam bentuk metilmerkuri, yang oleh bakteri metanogenik yaitu Metanobacterium osmenlaski diubah melalui proses metilasi untuk melindungi dirinya di dasar perairan baik secara aerobik maupun anaerobik. Merkuri dalam kondisi anaerobik bereaksi dengan sulfida membentuk senyawa kompleks yang tidak larut dalam air sehingga tidak berpengaruh buruk pada lingkungan. Apabila merkuri terserap oleh organisme bentik akan bersifat larut dan berbahaya pada kesehatan manusia jika termakan (Mukhtasor 2007). Medeiros et al. (2012) menyatakan bahwa biota akuatik yang tercemar logam berat apabila dikonsumsi oleh manusia maka akan menimbulkan permasalahan pada kesehatan. Efek logam berat terhadap kesehatan manusia tergantung pada bagian mana dari logam tersebut terikat dalam tubuh serta besarnya dosis paparan. Kerang hijau hasil penelitian memiliki kandungan logam berat Hg yang rendah sehingga biota aman untuk dikonsumsi. Batas maksimum kandungan logam berat Hg yang masih cukup aman dikonsumsi menurut FAO (1972) sebesar 0,0005 ppb, sedangkan batas maksimum cemaran logam berat dalam pangan menurut BSN (2009) sebesar 1 ppm.
Kandungan Logam Berat Cd
Hasil uji logam berat Cd kerang hijau (Perna viridis) pada berbagai ukuran tubuh (besar, sedang, dan kecil) disajikan pada Gambar 4.
9
Gambar 4 menunjukkan hasil uji distribusi logam berat Cd pada kerang hijau rataan tertinggi terakumulasi pada bagian insang kerang besar yaitu sebesar 0,04 ± 0,004 ppm, sedang 0,03 ± 0,0006 ppm, dan kecil 0,02 ± 0,0005 ppm. Semakin besar ukuran maka akumulasi bahan dalam tubuh semakin tinggi. Hal ini bergantung pada fungsi masing-masing organ. Perairan yang keruh dapat dapat menutupi insang atau elemen penyaring pada biota yang makan dengan cara menyaring. Penelitian Lata et al. (2013) mengenai variasi kandungan logam berat pada tiram Crassostrea madrasensis, kerang Pelymesoda, dan ikan Laurata liza dari pantai India menunjukkan logam Cd pada insang ikan 0,029 ppm, tiram 0,049 ppm, dan kerang 0,113 ppm. Logam Cd pada insang kerang lebih tinggi, diikuti dengan tiram dan ikan. Hal ini dikarenakan bagian insang berperan dalam menyaring makanan.
Kandungan logam berat Cd kerang hijau melalui uji statistik rancangan acak faktorial menunjukkan bahwa adanya pengaruh ukuran terhadap distribusi logam pada berbagai bagian tubuh (p > 0,05). Hasil uji lanjut BNT pada selang kepercayaan 95 % ukuran kerang tidak memberikan pengaruh nyata terhadap distribusi logam berat Cd pada berbagai bagian tubuh yaitu daging, insang, dan jeroan.
Bustamante et al. (2002) menyatakan bahwa Cd dikaitkan dengan lisosom dan protein sitosol yang memainkan peran dalam penyimpanan dan detoksifikasi logam. Mekanisme detoksifikasi melibatkan penyimpanan logam pada tempat yang tidak aktif dalam tubuh makhluk hidup untuk sementara atau permanen. Penyimpanan sementara dengan terikatnya logam pada protein, polisakarida, asam amino dalam jaringan lunak misalnya hati dan ginjal.
Distibusi logam berat pada berbagai bagian tubuh berbeda-beda dikarenakan faktor lingkungan ikut mempengaruhi kandungan logam pada kerang hijau, dalam hal ini tergantung pada kandungan kandungan logam pada kolom air, sedimen, salinitas, suhu, pH air, dan kekeruhan (Darmono 2001). Kerang hijau hasil penelitian memiliki kandungan logam berat Cd yang rendah sehingga biota aman untuk dikonsumsi. Batas maksimum kandungan logam yang ditetapkan berdasarkan FAO (1972) adalah 1 ppm, sama halnya yang ditetapkan oleh BSN (2009) mengenai batas maksimum cemaran logam berat dalam pangan.
Kandungan Logam Berat Pb
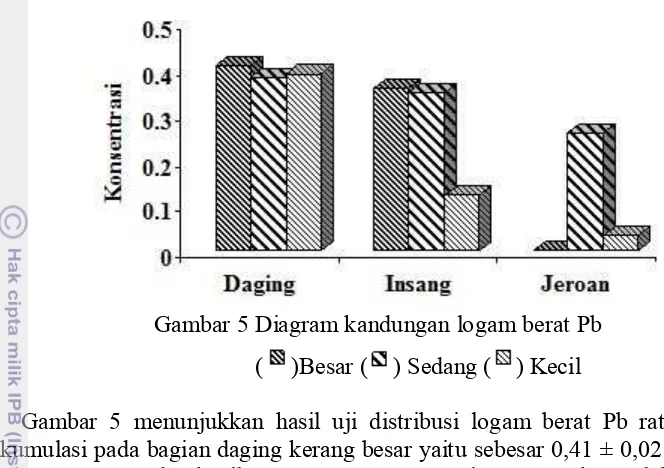
10
Gambar 5 Diagram kandungan logam berat Pb ( )Besar ( ) Sedang ( ) Kecil
Gambar 5 menunjukkan hasil uji distribusi logam berat Pb rataan tertinggi terakumulasi pada bagian daging kerang besar yaitu sebesar 0,41 ± 0,02 ppm, sedang 0,38 ± 0,005 ppm, dan kecil 0,39 ± 0,01 ppm. Daging merupakan salah satu bagian tubuh yang mengakumulasi pemasukan bahan dalam jaringan tubuh selama proses penyerapan. Bahan yang terserap mengandung cemaran logam. Logam diserap oleh darah, berikatan dengan protein darah yang berfungsi sebagai pengikat atau perangkap logam yang dikenal dengan metallotionin, dan didistribusikan ke seluruh jaringan tubuh.
Distribusi logam berat pada berbagai bagian tubuh, terutama terhadap kandungan logam berat Pb yang dibuktikan melalui uji statistik rancangan acak faktorial menunjukkan adanya pengaruh ukuran (P > 0,05). Hasil uji BNT pada selang kepercayaan 95 % bahwa kerang ukuran besar dan sedang memberikan pengaruh nyata terhadap distribusi logam berat Pb pada berbagai bagian tubuh yaitu sebesar 0,0472 ppm dan 0,0735 ppm.
Penelitian Masak dan Rachmansyah (2006) pada ikan bandeng, akumulasi logam Pb tertinggi pada organ ginjal dan diikuti dengan organ hati, usus, daging, dan insang. Logam Pb yang masuk dalam lingkungan perairan akan diserap dan terkandungan dalam jaringan biota akuatik melalui beberapa jalur misalnya daging, kulit, dan insang. Berbeda halnya dengan penelitian Su et al. (2009) mengenai status logam berat pada air, ikan, dan makroinvertebrata menunjukkan tingginya tingkat akumulasi Pb terutama terdistribusi dalam insang dan jaringan otot kepiting. Hal ini dikarenakan pengaruh perbedaan ukuran, spesies, dan kondisi salinitas yang berbeda.
11
toksisitas logam, umur muda lebih peka terhadap toksisitas logam dibandingkan umur dewasa (Apriadi 2005).
Kerang hijau hasil penelitian memiliki kandungan logam berat Pb yang rendah sehingga biota aman untuk dikonsumsi. Batas maksimum cemaran logam berat Pb kerang dalam pangan menurut BSN (2009) sebesar 1,5 ppm. Organisme air dimana kadar maksimum Pb yang aman dalam air sebesar 50 ppb (EPA 1973).
Kandungan Logam Berat Cu
Hasil uji logam berat Cu kerang hijau (Perna viridis) pada berbagai ukuran tubuh (besar, sedang, dan kecil) disajikan pada Gambar 6.
Gambar 6 Diagram kandungan logam berat Cu ( )Besar ( ) Sedang ( ) Kecil
Gambar 6 menunjukkan hasil uji distribusi logam berat Cu rataan tertinggi terakumulasi pada bagian jeroan kerang besar yaitu sebesar 1,54 ± 0,06 ppm, sedang 2,51 ± 0,05 ppm, dan kecil 1,65 ± 1,27 ppm. Hal ini dikarenakan jeroan sebagai tempat terakumulasinya sisa hasil penyerapan dalam tubuh. Uwem et al. (2012) dalam penelitiannya mengenai distribusi logam secara spasial terhadap tiga jenis ikan yaitu Tilapia zili, Oreochromis niloticus, dan Schibel mystus organ hati mengandung logam Cu tertinggi diikuti dengan insang dan tulang. Toksisitas logam Cu pada ikan berasal dari penyerapan logam dalam perairan melalui insang dan disimpan dalam hati. Absorpsi terjadi melalui permukaan pernapasan, jalur gastrointestinal (pencernaan) kemudian didistibusikan ke seluruh jaringan tubuh dan mengendap pada tempat akhir yaitu jeroan. Jeroan sebagai tempat terakumulasinya sisa penyerapan bahan dalam tubuh.
Logam Cu merupakan logam esensial yang diperlukan dalam tubuh khususnya untuk fungsi enzimatik. Kandungan logam Cu pada kerang hijau tinggi dikarenakan perairan dalam kondisi tercemar. Berbeda halnya apabila perairan dalam kondisi tidak tercemar maka kandungan logam Cu dalam perairan rendah. Pengambilan logam esensial melebihi tingkat akan mengganggu mekanisme homeostatis yang berperan mengendalikan tingkat kandungan di dalam tubuh. Mekanisme homeostatis terhambat dan mulai terjadi proses bioakumulasi pada jaringan tubuh biota karena laju pengambilan melebihi laju pengurangan (Connel dan Miller 1995).
Kerang hijau diketahui tidak dapat mengeksresikan logam dengan baik sehingga terakumulasi secara terus menerus dalam jaringan sesuai dengan kenaikan logam pada kolom air. Jenis hewan lunak tersebut memiliki mobilitas yang lamban atau tidak bergerak serta tidak dapat mengeluarkan logam (Payung et al. 2013). Kerang hijau hasil penelitian memiliki kandungan logam Cu yang tinggi sehingga biota tidak aman dikonsumsi. Batas aman maksimum kandungan logam Cu berdasarkan FAO (1972) yaitu 1 ppm.
Teluk Jakarta adalah salah satu kawasan yang mengalami tekanan kontaminasi cukup berat dibandingkan pesisir lain di Indonesia. Pertumbuhan jumlah penduduk dan industri memberikan dampak besar pada lingkungan, tidak hanya di darat tetapi juga di perairan teluk. Akibatnya, produksi limbah (bahan pencemar) semakin meningkat dengan cepat, terutama limbah B3. Limbah tersebut dihasilkan oleh industri antara lain adalah logam berat, sianida, pestisida, cat dan zat warna, minyak, zat pelarut, serta zat kimia berbahaya lainnya (Lasut 2002).
KESIMPULAN DAN SARAN
Kesimpulan
Distribusi logam berat Hg, Cd, Pb, dan Cu kerang hijau (Perna viridis) pada berbagai ukuran berdasarkan uji statistik dengan rancangan acak faktorial menunjukkan bahwa ukuran mempengaruhi distribusi logam berat pada berbagai bagian tubuh yaitu daging, insang, dan jeroan. Kandungan logam berat Hg dari hasil uji BNT memberikan pengaruh nyata terhadap distribusi logam berat pada kerang kecil pada berbagai bagian tubuh yaitu sebesar 0,6902 ppb. Kandungan logam berat Cd dari hasil uji BNT tidak memberikan pengaruh nyata terhadap distribusi logam berat pada berbagai ukuran.
Saran
Penelitian lebih lanjut perlu dilakukan untuk menentukan dan mengetahui sejauh mana ditribusi penyebaran logam berat pada biota akuatik yang berbeda misalnya jenis ikan, krustasea, maupun moluska terhadap bagian organ lainnya, mengetahui pengaruh perbedaan kedalaman perairan terhadap kandungan logam pada berbagai bagian tubuh berbeda, serta dilakukannya penurunan logam pada jaringan tubuh.
DAFTAR PUSTAKA
[AOAC] Association of Official Analytical Chemists. 2002. Official Methods of Analysis of The Association of Official Analytical of Chemist. Arlington Virginia USA: The Association of Official Analytical Chemist, Inc.
[BSN] Badan Standarisasi Nasional. 2009. Batas Maksimum Cemaran Logam Berat pada Pangan. Jakarta: Badan Standarisasi Nasional.
[KKP] Kementerian Kelautan dan Perikanan. Statistik Perikanan Tangkap Indonesia 2012. 2013. Jakarta: Direktorat Jendral Perikanan Tangkap.
[FAO] Food and Agriculture Organization. 1972. Food Composition Table for Use in East Asia. Food and Nutrition Division, Food and Agriculture Organisazion of The United Nation. Rome.
Anderson A Kim. 1999. Analytical Techniques for Inorganic Contamination. Amerika: AOAC International.
Apriadi D. 2005. Kandungan logam berat Hg, Pb, dan Cr pada air, sedimen, dan kerang hijau (Perna viridis L.) di perairan Kamal Muara, Teluk Jakarta. [Skripsi]. Bogor: Departemen Manajemen Sumberdaya Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Ambedkar B. 2013. Bioaccumulation and Distribution of Heavy Metals in Different Soft Body Tissues of The Freshwater Bivalve, Parreysia corrugata. Research Paper. India: Departemen of Zoology, Marathwada University.
Bustamante P, Cosson RP, Gallien I, Caurant F, Miramand P. 2002. Cadmium detoxification processes in the digestive gland of cephalopods in relation to accumulated cadmium concentration. Journal Environmental 53: 227-241. Chakraborty S, Ray M, Ray S. 2010. Toxicity of sodium arsenite in the gill of an
economically important mollusk of India. Journal Fish and Shellfish Immunology 29: 136-148.
Connel W dan Miller GJ. 1995. Kimia dan Ekotoksikologi Pencemaran. Jakarta: UI Press.
Darmono. 2001. Lingkungan Hidup dan Pencemaran: Hubungan dengan Toksikologi Senyawa Logam. Jakarta: UI Press.
EPA. 1973. Water Quality Criteria. Washington: Ecology Research Series.
14
Igwemmar NC, Kolawole SA, Odunoku SO. 2013. Heavy metal concentration in fish species sold in gwagwalada market, Abuja. International Journal of Science and Research 2 (11): 2319-7064.
Lata G, Chari H, Sarma VV, Ingole BS. 2013. Variation in heavy metals concentration in the edible oyster Crassostrea madrasensis, clam Polymesoda erosa, and grey mullet Liza aurata from coastline of India. Journal of Science
2 (4): 59-63.
Lasut MT. 2002. ‘Metallothionein’: suatu parameter kunci yang penting dalam
penetapan baku mutu air laut (BMAL) Indonesia. Jurnal EKOTON 2(1): 61-68. MENKLH. 1988. Keputusan Menteri Kependudukan dan Lingkungan Hidup Nomor:
02/MENKLH/1988, tentang pedoman penetapan baku mutu lingkungan. Jakarta : Sekretariat MENKLH.
Mukhtasor. 2007. Pencemaran Pesisir dan Laut. Jakarta: PT Pradya.
Medeiros RJ, Dos Santos LMG, Freire AS, Santelli RE, Braga AMCB, Krauss TM, Jacob SD. 2012. Determination of inorganic trace elements in edible fish from Rio de Janeiro State, Brazil. Journal Food Control 23(2): 535-541.
Payung LP, Ruslan, Birawida AB. 2013. Studi kandungan dan distribusi spasial logam berat timbale (Pb) pada sedimen dan kerang (Anadara Sp.) di wilayah pesisir kota Makassar. [Laporan Penelitian]. Makassar: Fakultas Kesehatan Masyarakat.
Masak PRP dan Rachmansyah. 2006. Distribusi residu logam berat timbal (Pb) dalam organ ikan bandeng (Chanos chanos) pada salinitas air berbeda. Jurnal Perikanan 8(1): 44-49.
Setyobudiandi I. 2000. Sumberdaya hayati moluska mytilidae. [Skripsi]. Bogor: Laboratorium Manajemen Sumberdaya Perikanan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor.
Su GS, Martillano KJ, Alcantara TP, Ragragio E, Jesus JD, Hallare A, Ramos G. 2009. Assesing heavy metals in the waters, fish, and macroinvertebrates in manila bay, Philippines. Journal of Applied Science in Environmental Sanitation 4 (3): 187-195.
Suyanto A, Kusmiyati S, Retnaningsih Ch. 2010. Jurnal Pangan dan Gizi 1(2). Uwem GU, Emile AF, Udo IJ, Bassey AA. 2013. Bioaccumulation of heavy metal in
Lampiran 1 Alat spektrofotometer AAS
Lampiran 2 Bagian organ dalam kerang
Lampiran 3 Morfometrik sampel
Panjang Tinggi Lebar
Lampiran 4 Data statistik
Anova: Two-Factor With Replication
SUMMARY Besar Sedang Kecil Total
Daging
Count 3 3 3 9
Sum 15,366 8,281 27,279 50,926
Average 5,122 2,760333 9,093 5,658444 Variance 0,145993 0,182529 0,348327 7,850335
Insang
Count 3 3 3 9
Sum 31,028 187,252 55,151 273,431
17
Lampiran 5Data morfometrik kerang hijau (Perna viridis)
Tabel 2 Morfometrik kerang hijau ukuran kecil
Sampel Panjang Lebar Tinggi
1 4,64 1,7 2,42 Variance 0,103321 1,026881 0,007663 0,948957
Total
Count 9 9 9
Sum 77,885 221,394 110,72
Average 8,653889 24,59933 12,30222 Variance 7,140597 811,4161 20,9144
ANOVA Interaction 3525,798 4 881,4495 2840,255
6,19E-25 2,927744
Within 5,586149 18 0,310342
18
Tabel 3 Morfometrik kerang hijau ukuran sedang
Sampel Panjang Lebar Tinggi
19
Rataan 6,423733 2,049 3,117333
SD 0,202058 0,178648 0,246368
Tabel 4 Morfometrik kerang hijau ukuran besar
Sampel Panjang Lebar Tinggi
20
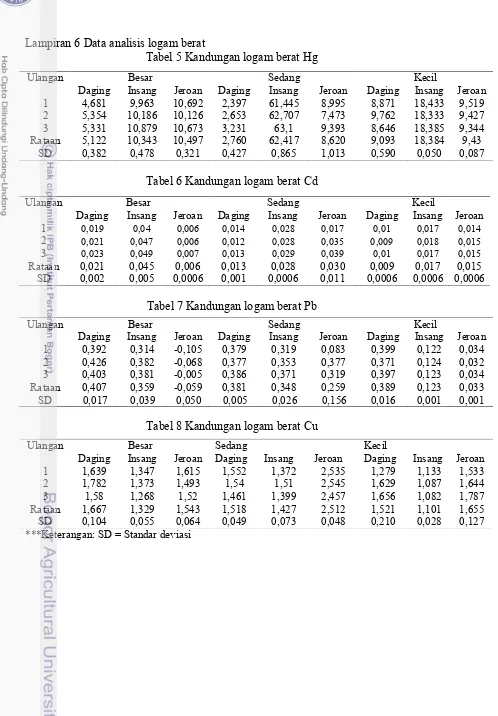
Lampiran 6 Data analisis logam berat
Tabel 5 Kandungan logam berat Hg
Tabel 6 Kandungan logam berat Cd
Tabel 7 Kandungan logam berat Pb
Tabel 8 Kandungan logam berat Cu
***Keterangan: SD = Standar deviasi
Ulangan Besar Sedang Kecil
Daging Insang Jeroan Daging Insang Jeroan Daging Insang Jeroan
1 4,681 9,963 10,692 2,397 61,445 8,995 8,871 18,433 9,519
Daging Insang Jeroan Daging Insang Jeroan Daging Insang Jeroan
1 0,019 0,04 0,006 0,014 0,028 0,017 0,01 0,017 0,014
Daging Insang Jeroan Daging Insang Jeroan Daging Insang Jeroan
1 0,392 0,314 -0,105 0,379 0,319 0,083 0,399 0,122 0,034
Daging Insang Jeroan Daging Insang Jeroan Daging Insang Jeroan
1 1,639 1,347 1,615 1,552 1,372 2,535 1,279 1,133 1,533
2 1,782 1,373 1,493 1,54 1,51 2,545 1,629 1,087 1,644
3 1,58 1,268 1,52 1,461 1,399 2,457 1,656 1,082 1,787
Rataan 1,667 1,329 1,543 1,518 1,427 2,512 1,521 1,101 1,655
21
RIWAYAT HIDUP
Penulis lahir di Serang tanggal 19 Juni 1992 dari pasangan Bapak Wastino dan Ibu Ila Yusrotun yang merupakan anak kedua dari tiga bersaudara. Pendidikan formal ditempuh penulis mulai dari TK Pondok Indah Cilegon pada tahun 1997-1998. Penulis melanjutkan pendidikan di SD Negeri II Cilegon pada tahun 1998-2004. Tahun 2007 penulis lulus dari SMP Negeri 1 Cilegon kemudian melanjutkan studinya di SMA Negeri 3 Cilegon hingga tahun 2010. Penulis diterima sebagai mahasiswa Departemen Teknologi Hasil Perairan, Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor melalui jalur USMI (Undangan Seleksi Masuk IPB).