Dibuat Untuk Mendapatkan Gclar Sarjana Pada Jurusan Teknik Kimia
Fakultas Teknik
Universitas Muhammadiyah Palembang
Disusun oleh:
Rikco Saputra
12.2010.021
P R O G R A M STUDI K I M I A
F A K U L T A S T E K N I K
UNIVERSITAS MUHAMMADIYAH PALEMBANG
PEMURNIAN B I O E T A N O L DENGAN PROSES
ADSORPSI-DISTILASI MENGGUNAKAN ADSORBENT BENTONITE
Nama : Rikco Saputn (12.2010.021) Dosea PerabiinbiDg : 1. Ir. Agussidi Najib, M,Si
2. AUkah, ST. MT
Palembang. Agustus201S
Icngetahui,
Pembimbing PembijtfNas 11
Ir. Agug?i4i ISflijib. M>§i) (Atikah .ST.MT)"
Mengetahui. Ketua Prodi Teknik Kimia
(Dr. Eko Arivanto. ST. M.Chcm.Eng)
Judul Penelitian :
PEMURNIAN B I O E T A N O L DENGAN PROSES ADSORPSI-OISTILASI MENGGUNAKAN A D S O R B E N T B E N T O N I T E
O L E H :
R I K C O SAPUTRA (12 2010 021)
DisetHjni dan Disahkan sekaligus telah Dbidangkan pada : Hari : Sabtu
Tanggal : IS Agustus 2015
Tempat : Di Ruang Aula Fakultas Teknik
Universitas Muhammadiyah Palembang
Disetujui O l e h :
1. ir* Agussidi Najib, M.St
2. A t i k a h , S T . M T
3. Ir. M. Arief Karim. M.Sc 4. I r . Ummi Katsum, M T
Segala puji dan syukur kami panjatkan kepada Allah SWT, karena berkat
rahmat dan hidayah-Nya laporan penelitian ini dapat kami selesaikan tepat pada
waktunya. Laporan ini berjudul '^Pemurnian Bioetanol Dengan Proses Adsorpsi-Distilasi Menggunakan Adsorbent Bentonite". Laporan ini disusun berdasarkan hasi! penelitian yang telah dilaksanakan di Laboratorium Penelitian
Kimia Organik Jurusan Teknik kimia Fakultas Teknik Universitas
Muhammadiyah Palembang pada bulan April sampai Mei 2015.
Penyusun menyadari sepenuhnya bahwa hasil dari tugas akhir ini tidak
terlepas dari ke kurangan, untuk itu kritik dan saran yang sifatnya membangun,
pcnulis sangat harapkan guna kesempumaan tugas akhir ini. Ucapan terima kasih
penulis haturkan terutama kepada dosen pembimbing akhir, Bapak Ir. Agussidi
Najib,M.Si selaku pembimbing I dan Ibu Atikah, ST. MT selaku pembimbing I I ,
yang telah banyak meluangkan waktu dan membantu membukakan cakrawala
berpikir penyusun melalui arahan, motivasi dan bimbingannya.
Pada kesempatan ini juga penyusun menyampaikan ucapan terima kasih
kepada:
1. Bapak Dr. Kgs. A. Roni, MT selaku Dekan Fakultas Teknik Universitas
Muhammadiyah Palembang.
2. Bapak Dr. Eko Ariyanto, ST. M.ChemEng selaku ketua prodi Teknik
4. Bapak Ir. Agussidi Najib,M.Si selaku pembimbing I .
5. Ibu Atikah, ST.MT selaku pembimbing II.
6. Misparadita Putri selaku assistant Laboratorium Jurusan Teknik Kimia
Fakultas Teknik Universitas Muhammadiyah Palembang.
7. Bapak Abdullah, ST selaku staff jurusan Teknik Kimia Fakultas Teknik
Universitas Muhammadiyah Palembang.
8. Para Dosen dan staff administrasi Jurusan Teknik Kimia Fakultas Teknik
Universitas Muhammadiyah Palembang.
9. Rekan-rekan Mahasiswa di Fakultas Teknik Jurusan Teknik Kimia
Universitas Muhammadiyah Palembang angkatan 2008-2014 yang telah
membantu dan memberi dukungan yaitu Kak Sandy, Agung Firmansyah,
Okta Mahardika, Dimas Tommy Adinata, Afif, Ahmad Puad, M . Rizky
Sunardi, Arif Madi, Eko Pumama, Akhyar Agung, Elly Noviana, Agus
Fermana, Ema Luvita Sari, Arif Wahyu, Arman Aulia, Agie Kurniawan,
Krismanto, Sonia Wulandari, Rini Marindah, Shelina, Danang, Tri Widya
Sari, Lianto, Tri Anggraini, Irawan, Maryama, Tiara Putri, Nurdin Saputra,
Tela Pumama Sari, Ines Ngesti, Yeyen Jayanti, Nanda, Jaka Sanjaya, Asri
Novita Sari, Tiara Indah Agustina, M . Roy, Lia, Rahayu, Sahidah, Herty,
Tiara Ganti, Ragil, Rahmat, Haseni, Hendra, Husna, Rani, Alexander
Baharsa, Elpin, Fajar Ramadhan, Angraini Larasati, Diah, Erlin Erhani,
Ochi, Melani, Deni Maulana, Fachmdin, Reza Pratama, Mubin, Intan
Randy, Gilang, Riki, dan Ikbal.
10. Terkhusus untuk kedua Orang tercinta Bapak Muhammad Juddin dan Ibu
Dewi Rina Martini, Scluruh Saudara dan Keluarga Riki dan Karin,
Rekan-rekan diluar kampus, Agus, Dwi Dianaulina, Apriliana Umi Lestari, Alfa
Rizky Cahya Septiadi, Mayong Prayogo, Arya Kuncara, Harly, Fatona,
Etchy, Monalisa Agustin, Devi Arlinda, Restu, Redy, Lutfi, Angga
Kusuma, Ridho, Selamet, Najib, Friyadi, Melly, Defri, Trendi, Venty
Lestari, Riki, Rangga, Tari, Michelle Arsyad, Ummi Muslimah, Agus
Yudi Arman, Angga Saputra, Yayan Rizky Putri, Agensia Ayu Melinda,
Muhammad Eko Wahyu Utama, Dini Fuadillah Sofyan, Isyana Dewi
Maya Lestari, dan semua pihak yang tidak dapat penyusun sebutkan satu
persatu yang telah banyak berkonstribusi baik langsung maupun tidak
langsung.
11, Semua pihak yang telah membantu saya.
Terima kasih atas semua bantuannya, semoga tugas penelitian ini dapat
bermanfaat untuk kita semua, Amin
Palembang, Juli 2015
HALAMAN
HALAMAN ,HIDUL i HALAMAN PENGESAHAN ii
K A T A PENGANTAR Hi
DAFTAR ISI vi DAFTAR T A B E L viii DAFTAR GAMBAR x DAFTAR LAMPIRAN xi BAB I PENDAHULIIAN 1
1.1 Lalar Belakang 1 1.2 Perumusan Masalah 3 1.3 Tujuan Penelitian 3 1.4 Manfaat Penelitian 4
BAB n TINJAIIAN P I S T A K A 5
2.1 Bioetanol 5 2.2 Etanol 7 2.3 Proses Produksi Bioetanol 10
2.4 GC-MS (Gas Chromatography-Mass Spectrometry) 12
2.5 Proses Adsorpsi 13 2.6 Bentonite 16 2.7 Aktivasi Adsorben 21
2.8 Penelitian Dan Proses Terkait Yang Pemah Dilakukan 24
BAB m M E T O D O L O G I P E N E L I T I A N 26
3.1 Waktu Dan Tempat 26 3.2 Alat Dan Bahan 26
3.2.1 Aiat-Alat Yang Digunakan 26 3.2.2 Bahan-Bahan Yang Digunakan 26
3.3 Rancangan Percobaan 27 3.3.1 Gambar Rangkaian Alat 27
3.4.3 Proses Adsorpsi Distilasi Dengan Bentonite Teraktivasi . 30
BAB IV H A S I L DAN PEMBAHASAAN 31
4.1 Hasil Penelitian 31 4.4.1 Pengaruh Variabel Pada Proses Adsorpsi-Distilasi 31
4.2 Pengaruh Penurunan Kadar Air 39 4.2 Perbandingan Yang Mendekati Pada Penelitian Sebeiumnya ... 48
BAB V K E S I M P U L A N DAN SARAN 50
5.1 Kesimpulan 50 5.2 Saran 50
D A F T A R PUSTAKA 51
LAMPIRAN 54
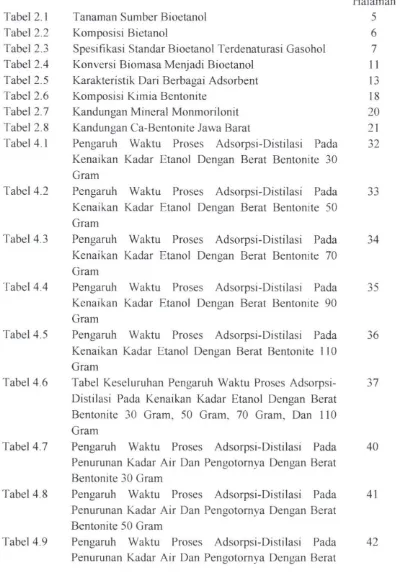
Tanaman Sumber Bioetanol Komposisi Bietanol
Spesifikasi Standar Bioetanol Terdenaturasi Gasohol Konversi Biomasa Menjadi Bioetanol
Karakteristik Dari Berbagai Adsorbent Komposisi Kimia Bentonite
Kandungan Mineral Monmorilonit Kandungan Ca-Bentonite Jawa Barat
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 30 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 50 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Beral Bentonite 70 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 90 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 110 Gram
Tabel Keseluruhan Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 30 Gram, 50 Gram, 70 Gram, Dan 110 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 30 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 50 Gram
Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat
Bentonite 90 Gram
Tabel 4,11 Pengamh Waktu Proses Adsorpsi-Distilasi Pada 44 Penurunan Kadar Air Dan Pengotomya Dengan Berat
Bentonite 110 Gram
Tabel 4.12 Tabel Keseluruhan Pengamh Waktu Proses Adsorpsi- 46 Distilasi Pada Penurunan Kadar Air Dan Pengotomya
Dengan Berat Bentonite 30 Gram, 50 Gram, 70 Gram, 90 Gram, Dan 110 Gram
Halaman
Gambar 2.1 Struktur Molekul Etanol 6
Gambar 2.2 Bentonite 17 Gambar 2.3 Struktur Bentonite 19
Gambar 3.1 Rangkaian Alat Adsorpsi-Distilasi 27 Gambar 4.1 Gratlk Hubungan Kadar Etanol (%) Dengan Waktu 32
(menit) Distilasi Bentonite 30 Gram
Gambar 4.2 Grafik Hubungan Kadar Etanol (%) Dengan Waktu 33 (menit) Distilasi Bentonite 50 Gram
Gambar 4.3 Grafik Hubungan Kadar Etanol (%) Dengan Waktu 34 (menit) Distilasi Bentonite 70 Gram
Gambar 4.4 Grafik Hubungan Kadar Etanol (%) Dengan Waktu 35 (menit) Distilasi Bentonite 90 Gram
Gambar 4.5 Grafik Hubungan Kadar Etanol (%) Dengan Waktu 36 (menit) Distilasi Bentonite 110 Gram
Gambar 4.6 Grafik Kesel uruhan Kadar Etanol (%) Dengan 3 8 Waktu (menit) Distilasi Berat Bentonite 30 Gram,
50 Gram, 70 Gram, 90 Gram, Dan 110 Gram
Gambar 4.7 Grafik Hubungan Kadar Air (%) Dan Pengotomya 40 Dengan Waktu (menit) Distilasi Bentonite 30 Gram
Gambar 4.8 Grafik Hubungan Kadar Air (%) Dan Pengotomya 41 Dengan Waktu (menit) Distilasi Bentonite 50 Gram
Gambar 4.9 Grafik Hubungan Kadar Air (%) Dan Pengotomya 42 Dengan Waktu (menit) Distilasi Bentonite 70 Gram
Gambar 4.10 Grafik Hubungan Kadar Air (%) Dan Pengotomya 43 Dengan Waktu (menit) Distilasi Bentonite 90 Gram
Gambar 4.11 Grafik Hubungan Kadar Air (%) Dan Pengotomya 44 Dengan Waktu (menit) Distilasi Bentonite 110
Gram
Gambar 4.12 Grafik Keseluruhan Hubungan Kadar A i r (%)Dan 47 Pengotomya Dengan Waktu (menit) Distilasi Berat
Bentonite 30 Gram, 50 Gram, 70 Gram, 90 Gram, Dan 110 Gram
Halaman
Lampiran A Data Dan Perhitungan 54 Lampiran B Foto Penelitian 62
Bioetanol merupakan senyawa alkohol yang diperoleh dengan proses fermentasi
biomassa dengan hantuan mikroorganisme Saccharomyces cerevisiae. Adsorpsi
(penyerapan) merupakan suatu proses pemisahan dimana komponen dari suatu
fuse fluida berpindah ke permukaan zat padat yang menyerap (adsorbent).
Penelitian ini bertujuan untuk mengkaji proses pemurnian bioetanol
menggunakan proses adsorpsi-distilasi dengan pengaruh variasi variabelnya.
Pada proses distilasi menghasilkan kadar etanol yang tidak terlalu tinggi
sehingga perlu dikaji suatu proses yang dapat meningkatkan kemumian bioetanol
dengan yaitu dengan proses adsorpsi-distilasi. Pemurnian bioetanol dengan
proses adsorpsi-distilasi menggunakan adsorbent bentonite sebagai media
adsorbentnya dilakukan dengan 2 variabel yaitu: berdasarkan berat bentonite
dan waktu proses adsorpsi-distilasi. Dari hasil penelitian didapatkan bahwa
proses yang paling efektif untuk pemurnian etanol adalah dengan berat bentonite
50 gram, suhu proses 80°C, waktu proses II0 menit. Kadar etanol yang
dihasilkan sebesar 93,292%. Penggunaan metode adsorpsi-distilasi dalam
pemurnian bioetanol merupakan hal yang ciikup efisien, metode dan peralatan
yang digunakan hanya menggunakan satu rangkaian alat yang sama sedangkan
dari sisi bahan baku penggunaan bentonite sebagai media adsorbentnya cukup
terjangkau di karenakan di Jindonesia ketersediaan bentonite cukup melimpah
dengan harga yang bahan baku yang relatif lebih murah dibandingkan
menggunakan adsorbent lain yang harganya lebih mahal dan ketersediaanya
harus diimport dari negara luar. Pada penelitian ini kadar etanol yang dihasilkan
belum mencapai target yang diinginkan sesuai dengan Standar Fuel Grade
Ftanol (FGF,) sebesar 99,6 %>, karena Etanol tertinggi yang dihasilkan hanya
93,292%. Hal ini dikarenakan faklor suhu yang kurang terjaga dan disebabkan
adanya bentonite yang terikut pada hasil distilat saat dilakukan proses
adsorpsi-distilasi sehingga menggotori hasil akhir sampei.
1.1 Latar Belakang
Seiring meningkatnya perkembangan di berbagai bidang ilmu dan meningkatnya populasi masyarakat dunia dalam beberapa dekade lerakhir. Mengakibatkan semakin meningkat dan besar pula kebutuhan akan ketersediaannya sumber daya alam (energi dan mineral) yang ada. Hal ini tidak terlepas dikarenakan energi merupakan faktor pendukung terpenting sebagai sumber kehidupan, termasuk didalamnya energi yang berasal dari bahan tambang salah satunya yaitu minyak bumi. Akan tetapi dibalik meningkatnya kebutuhan akan konsumsi energi yang ada, mengakibatkan semakin berkurang pula ketersediaannya yang ada didalam bumi. Karena minyak bumi merupakan salah satu energi yang keberadaanya tidak dapat diperbarui {imrenewahle energy).
Melihat hal ini, sudah saatnya untuk mencari solusi dan menemukan altematif energi lain yang keberadaanya dapat diperbaharui sehingga ketergantungan akan minyak bumi dapat diatasi. Pada dasamya sudah banyak dikemukakan ide-ide dengan berbagai wacana untuk menganti minyak bumi dengan bahan bakar energi altematif Iain diantaranya dengan pembuatan bahan bakar dari biodiesel (bahan pencampur solar), bioetanol (bahan pencampur BBM bensin/premium), dan biogas yang merupakan energi altematif penganti gas elpiji. Dengan diberlakukannya energi altematif ini diharapkan kebutuhan akan energi minyak bumi dapat diatasi dan biaya pengeluaran konsumsi masyarakat akan harga bahan bakar semakin tinggi dapat dikurangi dengan ketersediannya yang mencukupi.
Salah satu energi altematif yang menjanjikan pada saat ini yaitu bioetanol. Bioetanol adalah senyawa etanol yang sumber utamanya berasal dari bahan alam
(Organik) dengan mengunakan proses fermentasi sebagai salah satu rangkaian metodenya hingga menghasilkan bioetanol. Bioetanol (Etanol atau etil alkohol)
C3H5OH mempakan cairan bening tak berwama, yang temrai secara biologis
{biodegradable) memiliki toksisitas rendah dan tidak menimbulkan polusi yang besar apabila terkontaksi di udara. Akan tetapi untuk menghasilkan bioetanol saja
tidak cukup, diperlukan perlakuan khusus untuk menghasilkan bioetanol yang tinggi hingga mencapai syarat Bioetanol FGE [Fuel Grade Etanol) dengan kadar 99,55-100% v/v sehingga bioetanol dapat aman dipergunakan. Karena keberadaan air dalam bahan bakar walaupun dengan kadar sedikit sangat berpengaruh terhadap performa mesin.
Metode konvensional yang umum digunakan dalam purifikasi bioetanol adalah dengan destilasi. Proses destilasi dapat menghasilkan bioetanol hingga kadar 95,6 % volume. Kadar bioetanol meningkat dengan semakin seringnya didistilasi. Tetapi penggunaan metode distilasi juga memiliki kelemahan, yaitu tidak dapat memurnikan bioetanol secara sempuma dan juga penggunaan energi pada purifikasi bioetanol dengan metode destilasi ini sangat besar dan akan terjadi kehilangan etanol berlebih {etanol lose) dalam proses ini.
Oleh karena itu, diperlukan adanya suatu metode baru dengan nilai ekonomis yang tinggi dan lebih baik dalam purifikasi bioetanol, salah satunya adalah purifikasi bioetanol dengan menggunakan suatu adsorbent. Adsorbent dapat memisahkan campuran bioetanol dan air dengan cara menyerap air tersebut, sehingga kadar bioetanol yang dihasilkan dari proses adsorpsi yang dilanjutkan dengan proses distilasi akan lebih tinggi dibandingkan purifikasi dengan menggunakan distilasi biasa. Dan penggunaan adsorbent dalam proses pemurnian
{purifikasi) bioetanol ini adalah dengan menggunakan adsorbent Bentonite
sebagai media penyerapnya. Bentonite mempunyai sifat mengadsorpsi karena ukuran partike! koloidnya sangat kecil dan memiliki kapasitas pennukaan ion yang tinggi (Teplitskiy, 2005).
Pada penelitian ini akan dilakukan purifikasi bioetanol menggunakan adsorbent Bentonite dengan metode Adsorpsi-Distilasi. Penggunaan metode
1.2 Perumusan Masalah
Berdasarkan uraian latar belakang yang dikemukakan diatas, maka perumusan masalah yang dibahas dalam penelitian ini dapat dirumuskan sebagai berikut;
1. Bagaimana proses pemurnian pada bioetanol dengan metode Adsorpsi-Distilasi menggunakan adsorbent bentonite hingga diperoleh kadar bioetanol. 2. Apakah metode Adsorpsi-Distilasi merupakan hal yang baik dalam purifikasi
bioetanol dibandingkan dengan menggunakan metode lain.
3. Apakah penggunaan bentonite sebagai media adsorbent merupakan hal yang efektif dalam segi niiai ekonomis dalam purifikasi bioetanol.
4. Berapakah kadar bioetanol yang dihasilkan dan proses purifikasi dengan menggunakan metode Adsorpsi-Distilasi dengan menggunakan adsorbent bentonite.
5. Apakah metode purifikasi bioetanol dengan cara Adsorpsi-Distilasi
merupakan metode yang etisien bita digunakan untuk mendapatkan kemumian bioetanol maksimum.
1.3 Tujuan Penelitian
Berdasarkan permasalahan tersebut, maka tujuan dari penelitian ini adalah sebagai berikut:
1. Untuk mengetahui proses Adsorpsi-Distilasi dengan mengunakan adsorbent bentonite pada purifikasi bioetanol hingga diperoleh kadar bioetanol yang tinggi.
2. Untuk mengetahui apakah pemurnian bioetanol dengan proses Adsorpsi-Distilasi merupakan metode yang efisien,
1.4 Manfaat Penelitian
Adapun manfaat yang diharapkan dari penelitian ini adalah :
1. Dapat memberi konstribusi untuk perkembangan teknologi dibidang purifikasi bioetanol untuk digunakan sebagai metode altematif baru dalam produksi bioetanol di Indonesia.
2. Hasil penelitian ini diharapkan dapat memberikan informasi dan menjadi acuan untuk penelitian selanjulnya dalam pengembangan metode dan bahan baku purifikasi pembuatan bioetanol.
3. Mengkaji lebih lanjut pemanfaatan bentonite sebagai media penyerapan
{adsorbent) dalam peningkatan kemumian bioetanol.
2.1 Bioetanol
Bioetanol merupakan salah satu jenis biofuel (bahan bakar cair dari pengolahan tumbuhan) di samping Biodiesel. Bioetanol adalah etanol yang dihasilkan dari fermentasi glukosa (gula) yang dilanjutkan dengan proses distilasi. Proses distilasi dapat menghasilkan etanol dengan kadar 95% volume, untuk digunakan sebagai bahan bakar (biofuel) perlu lebih dimumikan lagi hingga mencapai 99% yang lazim disebut fuel grade ethanol (FGE). Proses pemurnian dengan prinsip dehidrasi umumnya dilakukan dengan metode Molecular Sieve, untuk memisahkan air dari senyawa etanol. Bahan baku bioetanol yang dapat digunakan antara lain Cassava'ubi kayu, sorgum, tebu, sagu dan lain-lain,
Bioetanol berasal dari dua kata yaitu "bio" dan "etanol" yang berarti sejenis alkohol yang merupakan bahan kimia yang terbuat dari bahan baku tanaman yang mengandung pati, misalnya cassava, ubi jalar, jagung dan sagu. Etanol merupakan senyawa alkohol yang mempunyai dua atom karbon (C2H5OH).
Rumus kimia umumnya adalah CnH^n+lOH. Karena merupakan senyawa alkohol, etanol memiliki beberapa sifat yaitu larutan yang tidak berwama (jernih), berfase cair pada temperatur kamar, mudah menguap, serta mudah terbakar. Etanoi dapat diperoleh melalui proses fermentasi biomassa. Oleh karena berbahan dasar biomassa, maka selanjutnya lebih dikenal dengan bioetanol.
Bioetanol adalah sebuah bahan altematif yang diolah dari tumbuhan, dimana memiliki keunggulan mampu menurunkan emisi CO: hingga 18%. Ada 3 tanaman sumber bioetanol :
Table 2.1 Tanaman Sumber Bioetanol No Jenis Kandungan Jenis Tanaman
1. Pati Cassava, kelapa sawit, tengkawang, kelapa,
kapuk, jarak pagar, rambutan, sirsak.
2. Bergula Tebu, nira aren, nira tebu,dan nira sorgum manis.
3. Serat solulosa batang sorgum, batang pisang, jerami, kayu dan bagas.
Tidak ada perbedaan antara etanol biasa dengan bioetanol yang membedakan hanyalah bahan baku pembuatan dan proses pembuatan. Etanol adalah sejenis cairan yang mudah menguap, mudah terbakar, tidak berwama dan merupakan alkoho! yang sering digunakan dalam kehidupan sehari hari. Senyawa ini merupakan obat psikoaktif dan dapat ditemukan pada minuman yang beralkohol. Etano! tennasuk kedalam alkohol rantai tunggal dengan rumus kimia
C3H5OH dan mmus empiris C3H6O ia merupakan isomer konstitusional dan
dimetil eter. (Hartono 2013)
H
H
I
C
H H
/
C - 0
H H
Gambar 2.1. Struktur Molekul Etanol
Bioetanol adalah etanol yang dibuat dari hiomass yang mengandung komponen pati atau selulosa, seperti cassava dan tetes tebu. Dalam dunia industri, etanol umumnya dipergunakan sebagai bahan baku industri turunan alkohol, campuran untuk minuman keras (seperti sake atau gin), serta bahan baku farmasi dan kosmetika. Unsur-unsur kimia yang terkandung dalam bioetanol yang digunakan dapat diperlihatkan pada tabel 2.2.
Tabel 2.2. Komposisi Bioetanol
Senyawa Kimia Persentase (%)
Etil Alkohol 7 0 %
Benzalkonium Chloride 0,05 %
Aqua 29,95 %
Berdasarkan kadar alkoholnya, etanol terbagi menjadi tiga grade sebagai berikut:
1. Grade industri dengan kadar alkohol 90-94%.
2. Netral dengan kadar alkohol 96-99,5%, umumnya digunakan untuk minuman keras atau bahan baku obat dalam industri iaimasi.
3. Grade bahan bakar dengan kadar alkohol diatas 99,5%. (Prihardana, R.,dkk. 2008).
Tabel 2.3 Spesifikasi Standar Bioetanol Terdenaturasi Gasohol No. Sifat Unit, Min/Maks Spesifikasi
1. Kadar etanol % V, min 99,5(sebelumdenaturasi)
94,0 (setelah denaturasi)
2. Kadar metanol Mg/L, maks 300
3. Kadar air % V, maks 1
4. Kadar denaturan % V, min
% V, maks
2 5
5. Kadar tembaga (cu) Mg/kg, maks 0,1
6. Keasamaan sebagai
CH3COOH
Mg/L, maks 30
7. Tampakan Jernih dan terang, tidak
ada endapan dan kotoran
8. Kadar ion klorida (CI) Mg/L, maks 40
9. Kandungan belerang (S) Mg/L, maks 50
10. Kadar getah (gum) Mg/lOOml, maks 5,0
11. pH Mg/L, maks 6,5-9,0
(Sumber :SN1 7390: 2008)
2.2 Etanol
Etanoi atau bioetanol adalah alkohol yang paling banyak digunakan daiam kehidupan sehari-hari. Karena sifatnya tidak beracun, etanol banyak dipakai sebagai pelarut dalam dunia farmasi dan industri makanan dan minuman. Etanol tidak berwama dan tidak berasa tetapi memiliki bau yang khas dan memabukkan jika diminum. Etanol sering ditulis dengan EtOH, dengan rumus molekul adalah
C2H5OH atau C2H6O dan mempunyai titik didih 78,3 °C (www,wikipedia.com). Etanol adalah senyawa organik yang tcrdiri dari karbon, hidrogen dan oksigen, sehingga dapat dilihat sebagai derivat senyawa hidrokarbon yang mempunyai gugus hidroksil dengan rumus C2H5OH. Etanol merupakan zat cair, tidak berwama, berbau spesifik, mudah terbakar dan menguap, dapat bercampur dengan air dengan segala perbandingan.
a. Sifat-sifat fisis etanol
1) Rumus molekul : C2H5OH
2) Berat molekul : 46,07 gram / mol
3) Titik didih pada 1 atm : 78,4°C 4) Titikbeku : -112X
5) Bentuk dan wama : cair tidak berwama
(Perry, 1984) b. Sifat-sifat kimia etanol
1) Berbobot molekul rendah sehingga larut dalam air 2) Diperoleh dari fermentasi gula
Struktur pembentukan etanol :
C6H12O6 "^"^ > CH3CH2OH
glukosa etanol
3) Pembakaran etanol menghasilkan CO2 dan H2O
Struktur pembakaran etanol:
CH3CH2OH + 3O2 > 2CO2 + 3H2O - energi
(Fessenden & Fessenden, 1997)
diperoleh dari hasil samping dari proses industri gula yaitu sugarcane. Urutan reaksi pembuatan etanol adalah reaksi hidroiisa dengan memecahkan bagian selulosa menjadi larutan gula yang kemudian difermentasikan menjadi etanol dengan bantuan enzim zymase sebagai katalis.
Ci2H220n
+ H20 >G
.H12O6
+ QNi^Of, Sukrosa Air Fruktosa Glukosa/ymase
QHi20(,
> 2
C2H5OH + 2CO2
Sukrosa Air Fruktosa Glukosa
Dalam perdagangan dikenal tingkat-tingkat kualitas etanol sebagai berikut (Tjpkroadikoesoemo, 1996):
1. Etanol Teknis (96,5 person)
Etanol ini digunakan untuk kepentingan indutri. Digunakan sebagai bahan pelarut organik, bahan bakar, dan sebagai bahan baku atau bahan antara untuk memproduksi senyawa organik lainnya.
2. Spritus(88 Persen)
Nama lain diberikan kepada etanol/alkohol 176 proof yang telah didenaturasikan dan diberi wama. Etanol ini biasanya digunakan sebagai bahan bakar untuk alat pemanas ruangan dan alat penerangan.
3. Etanol Absolut atau Etanol Kering
Digunakan sebagai bahan pembuatan obat-obatan dan juga sebagai bahan pelarut atau bahan antara di dalam pembuatan senyawa-senyawa organik lain dalam skala laboratorium. Etanol ini dapat dicampur dengan premium/bensin sebagai bahan bakar kendaraan bermotor. Kecenderungan pemakaian etanol ini sebagai bahan pencampur bensin cenderung meningkat karena harga minyak dunia cukup tinggi.
Secara garis besar penggunaan etanol adalah sebagai pelarut untuk zat organik maupun anorganik, bahan dasar industri asam cuka, esier, spirtus, asetaldehid, antiseptik dan sebagai bahan baku pembuatan efer dan etil ester,
Etanol juga untuk campuran minuman dan dapat digunakan sebagai bahan bakar
Proses pembuatan etanol dalam industri lerdiri dari dua cara, yaitu :
1. Cara non fermentasi
Suatu proses pembuatan alkohol yang sama sekali tidak menggunakan enzim atau jasad renik.
2. Cara fennentasi
Fermentasi merupakan proses metabolisme dimana terjadi perubahan kimia dalam substrat/bahan oranik karena enzim yang dihasilkan jasad renik. (wahono, 2006).
2.3 Proses Produksi Bioetanol
Secara umum, proses pengolahan bahan berpati (Starch) seperti Cassava, jagung dan sagu untuk menghasilkan bioetanol dilakukan dengan proses urutan. Pertama adalah proses hidrolisis, yakni proses konversi pati menjadi glukosa. Pati merupakan homopolimer glukosa dengan ikatan a-glikosidik. Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas, fraksi terlarut disebut amilosa dan fraksi tidak terlarut disebut amilopeUin. Amilosa mempunyai struktur lurus dengan ikatan a-(l,4)-D-glikosidik sedangkan amilopektin mempunyai struktur bercabang dengan ikatan a-( l,6)-D-glikosidik sebanyak 4-5% dari berat total.
Tahap kedua adalah proses fermentasi untuk mengkonversi glukosa (gula) menjadi etanoi dan CO2. Fermentasi etanol adalah perubahan 1 mol gula menjadi 2 mol etanol dan 2 mol CO2. Pada proses fermentasi etanol, khamir terutama akan memetabolisme glukosa dan fruktosa membentuk asam piruvat melalui tahapan reaksi pada jalur Embden-Meyerhof-Pamas, sedangkan asam piruvat yang dihasilkan akan didekarboksilasi menjadi asetaldehida yang kemudian mengalami dehidrogenasi menjadi etanol (Amerine et al., 1987).
Khamir yang sering digunakan dalam fermentasi alkohol adalah
Saccharomyces cerevisiae, karena jenis ini dapat berproduksi tinggi, toleran terhadap alkohol yang cukup tinggi (12-18% v/v), tahan terhadap kadar gula yang tinggi dan tetap aktif melakukan fermentasi pada suhu 4-32°C.
Setelah proses fennentasi selesai, dilakukan destilasi untuk memisahkan etanol. Distilasi merupakan pemisahan komponen berdasarkan titik didihnya. Titik didih etanol mumi adalah 78°C sedangkan air adalah 100°C (Kondisi standar), Dengan memanaskan larutan pada suhu rentang 78 - 100°C akan mengakibatkan sebagian besar etanol menguap, dan melalui unit kondensasi akan bisa dihasilkan etanol dengan konsentrasi 95 % volume.
Terdapat dua tipe proses destilasi yang banyak diapiikasikan, yaitu
continuous-feed distillation column system dan pot-type distillation system. Selain tipe tersebut, dikenal juga tipe destilasi vakum yang menggunakan tekanan rendah dan suhu yang lebih rendah untuk menghasilkan konsentrasi alkohol yang lebih tinggi.
Tabel 2.4 Konversi Biomasa Menjadi Bioetanol Biomassa Jumlah
Biomasa (kg) Kandungan Gula (kg) Jumlah hasil bioetanol (Liter)
Biomassa : Bioetanol
Ubi kayu 1.000 250-300 166,6 6,5 : 1
Ubi jalar 1.000 150-200 125 8 : 1
Jagung 1.000 600-700 400 2,5: 1
Sagu 1.000 120-160 90 12 : I
Tetes 1.000 500 250 4 : 1
Biotanol adaiah etanol (alkohol) yang diperoleh dan fermentasi bahan-bahan yang mengandung gula. Bioetanol dapat diperoleh dari hasil fermentasi bahan yang mengandung gula oleh ragi (yeasf) Sacchar amy cess cereviceae. Ragi
Saccharomycess cereviceae bersifat fakul tatif anaerobik. Pada kondisi aerobik sebagai akseptor elektron terakhir pada jalur reaksi bioenergetik adalah oksigen. Pemanfaatan pada keadaan ini menghasilkan penambahan biomassa sel dengan persamaan reaksi sebagai berikut:
Cf,Hi206 CO2 + H2O + biomassa sel
Pada kondisi anaerobik, Saccharomycess cereviceae menggunakan senyawa organik sebagai akseptor elektron terakhir pada jalur reaksi bioenergetik. Dalam ha! ini yang digunakan adaiah monosakarida dari substrat dengan hasil akhir perombakan berupa etanol, aldehid, asam organik, dan fusse! oil. Reaksi yang berlangsung dalam keadaan anaerobik tersebut adalah sebagai berikut:
C6H12O6 2C2H5OH + 2CO2 + produk samping
Bahan-bahan yang dapat difermentasi adalah bahan-bahan yang mengandung glukosa dan bahan-bahan yang dapat dihidrolisa menjadi glukosa seperti gula (sukrosa), bahan berpati dan bahan berselulosa.
Pembuatan bioetanol secara garis besar melalui tiga proses, yaitu : 1. Persiapan bahan baku
2. Fermentasi
3. Pemurnian (destilasi)
2.4 GC-MS (Gas Chromatography-Mass Spectrometry)
puncak absorbsi. Sampei yang telah melalui instrumen GC diteruskan menuju instrumen MS untuk diionisasi dengan menggunakan serangan elektron sehingga terbentuk molekul atau fragmen molekul yang bermuatan dan kemudian diukur rasio massa per muatan (mass-to-charge (m/z)) yang dimilikinya, melalui fragmen yang terbentuk tersebut dapat di identifikasi senyawa penyusun sampei yang diuji. Hasil analisis GC-MS adalah berupa data kuantitatif (GC) dan kualitatif (MS) (Charles, N.,dkk., 1996).
2.5 Proses Adsorpsi
Adsorpsi adalah proses pengikatan molekul dalam suatu fluida baik cair maupun gas ke permukaan pori benda padat. Proses adsorpsi biasanya dilakukan dengan mengkontakan larutan atau gas dengan padatan, sehingga sebagian komponen larutan atau gas diserap pada pennukaan pori padatan, akibatnya akan mengubah komposisi larutan tersebut. Bahan yang dipakai untuk melakukan proses adsorpsi dinamakan adsorben, sedangkan bahan yang disebut adsorbat. Adsorben yang baik harus memiliki kapasitas dan selektifitas adsorpsi terhadap molekul adsorbat (Kumar, K V, Et al., 2004). Tabel 2.5 memberikan perbandingan beberapa adsorben berdasarkan karakteristik, aplikasi dan kelemahannya.
Tabel 2.5 Karakteristik Dari Berbagai Adsorbent
Tipe Karakteristik Manfaat Kelemahan
Arang Aktif Hidrofobik, favors
organics over water
Menghilangkan polutan organik
Sulit diregenerasi
Zeolit Hidrofilik, polar, regular channel
Pemisahan gas, dehidrasi
Kapasitas total rendah
Silica Gel Kapasitas besar, hidrofilik Pengeringan aliran gas
Penyerapan kurang efektif Alumina
Aktif
Kapasitas besar, hidrofilik Pengeringan aliran gas
Pada dasarnya adsorpsi dapat dibedakan menjadi dua bagian, yaitu adsorpsi fisis dan adsorpsi kimia (Amri, A. Et al., 2004). Kedua jenis adsorpsi ini dapat dijelaskan sebagai berikut:
E Adsorpsi Fisis
Adsorpsi ini sering disebut dengan adsorpsi Van Der Walls yang disebabkan oleh gaya intermolekuler yang lemah. Adsorpsi ini bersifat reversible penuh sehingga dapat terjadi desorpsi. Adsorpsi terjadi tidak pada site yang spesifik dan molekul yang teradsorpsi menyelimuti seluruh permukaan. Panas adsorpsi yang terjadi cukup rendah yaitu dibawah 20 kcal/mol
2. Adsorpsi Kimia
Noll, et al., (1992) menjelaskan bahwa pada asorpsi ini terlibat ikatan kimia antar molekul adsorbat dan pennukaan adsorben. Proses ini terjadi secara irreversible. Adsorpsi terjadi pada sites spesifik dan panas adsorpsi yang dihasilkan yaitu 20 sampai 100 kcal/mol (sukresni, 2002)
3. Pertukaran Ion
Pertukaran ion merupakan bentuk khusus dari adsorpsi kimia. Pertukaran ion adalah suatu fenomena atau suatu proses yang melibatkan pertukaran dapat balik dari ion-ion di dalam larutan dengan ion terikat di dalam bahan bakar penukar ion. Pada proses tersebut tidak ada perubahan permanen di dalam struktur padatan. Mekanisme pertukaran ion ini didasarkan pada sifat sorptif dari tempat yang bermuatan negatif dalam absorben terhadap ion positif yang terjadi karena gaya coloumb.
Kebanyakan adsorben adalah bahan yang mempumyai porositas yang tinggi untuk menempatkan adsorbat pada dinding pori. Pemilihan adsorben berdasarkan pada kapasitas, selektifitas, kecepatan penyerapan, tidak mengandung pencemar berbahaya, murah harganya dan mudah regenerasinya. Dalam proses penyerapan, permukaan adsorben yang sifatnya polar akan mengikat molekul yang sifatnya polar dan permukaan adsorben non-polar akan mengikat molekul yang sifatnya non-polar (Sunamo, 2000).
Beberapa faktor yang mempengaruhi adsorpsi pada permukaan zat padat antara lain :
Syarat-syarat yang harus dipenuhi dalam pemilihan adsorben adalah memiliki permukaan kontak yang luas, mempunyai pori-pori aktif dan murni serta tidak bereaksi dengan adsorbat.
b. Jenis Adsorbat
Syarat-syarat yang diperlukan agar adsorbat terjerap dengan baik adalah : Ukuran Adsorbat
Molekul yang terjerap haruslah mempunyai ukuran partikel yang lebih kecil dari ukuran diameter pori adsorben.
1. Jenis kepolaran adsorbat
Umumnya adsorbat bersifat ionik dengan polaritas tinggi, jika diametemya sebanding maka molekul-moiekul polar terjerap lebih kuat dari pada molekul non-polar.
2. Jenis ikatan
Senyawa tidak jenuh lebih baik dijerap bila dibandingkan dengan senyawa jenuh.
3. Temperatur
Pada adsorpsi fisis kenaikan temperatur menyebabkan adsorpsi menurun. Ha! ini disebabkan mobilitas dari atom-atom suatu zat yang diadsorpsi bertambah dengan naiknya temperatur. Oleh karena itu, zat yang dijerap cenderung meninggalkan zat penjerap, Sedangkan pada adsorpsi kimia, adsorpsi bertambah dengan naiknya temperatur. Kenaikan temperatur juga dapat menyebabkan pori-pori adsorben lebih terbuka karena unsur-unsur pengotor pada permukaan akan teroksidasi.
4. pH
Adsorpsi antara fasa padat-cair sangat dipengaruhi oleh pH larutan. Adsorpsi yang dilakukan pada pH tinggi cenderung memberikan hasil yang kurang sempurna, karena pada kondisi basa terbentuk senyawa oksida dari unsur pengotor lebih besar sehingga akan menutupi permukaan adsorben.
5. Waktu Kontak
2.6 BeDtonite
Bentonite adalah istilah untuk lempung {clay) yang mengandung monmorilonit di daiam dunia perdagangan dan termasuk kelompok Jioktahedral
(Puslitbang Tekmira, 2005). Bentonite termasuk mineral lempung clay golongan smektit diokiahedral yang mengandung sekitar 80% monmorilonit dan sisanya antara lain kaolit, illit, feldspar, gypsum, abu vulkanik, kalsium karbonat, pasir kuarsa dan mineral lainya (Gunister ei al., 2004),
Istilah bentonit pertama kali dikenaikan oleh W. C. Knight pada tahun 1989. Penamaan ini diberikan karena bentonit ditemukan di daerah Fort Benton, Wyoming Amerika Serikat, sedangkan istilah monmorilonit berasal dari Prancis yang ditemukan di Montmorillone Veinne. Bentonite adalah adsorben alluminio phyllosilicate yang terdapat pada clay yang mengandung 80 persen montmoritlonite dengan formula (Na,Ca)o,33 (Al,Mg)2SiOi{)(OH)2(H20)n (Sneanabrezovska, et a!., 2004).
Bentonite terbentuk dari proses mekanik dan kimiawi dari batuan yang dipengaruhi cuaca (pada lingkungan alkali), batuan tersebut umumnya berasal dari batuan ledakan gunung berapi, bisa juga berasal dari batuan andesit, riolit, basal, dan lain-lain, kebanyakan adalah batuan tersier. Keberadaan bentonit sangat melimpah di Indonesia, antara lain tersebar di pulau Jawa. pulau Sumatra, sebagian pulau Kalimantan Timur dan pulau Sulawesi (Puslitbang Tekmira, 2005).
Karakteristik Bentonite berdasarkan yaitu : Nama Umiah : Bentonite
Kompisi Kimia ; (Mg, Ca)O.Al203.5Si02.nH:0
Nama Dagang : Soap clay, taylorite, bleaching clay, fuller's earth.
Wama Massa Jenis Bentuk Fisik
konfolensit, safonit, atau smegmatit dan stolpenit. : Padatan (Solid), butiran halus
: Kuning Muda, Putih, Abu-abu, coklat : 2,2 - 2,7 g/L
Indeks Bias : 1,547- 1,557
Titik Lebur : 1330- 1430 °C
Kadar keasaman (pH) ; Na-bentonite = 8,5 - 9,8 Mg, Ca-bentonite = 4 - 7
Struktur penyusun : H^ Na"", Ca^\ Al"", Mg^^, SiO:, O2',
Bahan mineral ini bersifat lunak dengan tingkat kekerasan satu pada skala Mohs, berat jenisnya berkisar antara 1,7 sampai 2,7, mudah pecah, terasa berlemak bila dipegang, mempunyai sifat mengembang bila kena air (Sukandarrumidi, 1999). Bentonite Juga sering disebut sebagai soapclay, taylorite, bleaching clay, fuller's earth, konfolensit, safonit, atau smegmatit dan stolpenit.
Bentonite mempunyai sifat mengadsorbsi karena ukuran partikel koloidnya sangat kecil dan memiliki kapasitas permukaan ion yang tinggi (Teplitskiy, 2005). Pengembangan bentonite disebabkan oleh adanya penggantian isomorphous pada lapisan oktohedral (Mg oleh Al) dalam menghadapi kelebihan muatan di ujung kisi-kisinya.
Secara umum bentonite dapat dibedakan tergantung kepada sifat fisika dan kimianya (kapasitas pertukaran basa, waktu pengendapan, kekuatan mengembang, nilai pH , dan lainnya) serta komposisi bahannya. Terdapat 2 jenis bentonite :
1. Swelling (Sodium Bentonite): bentonite yang bisa mengembang
Bentonit jenis ini disebut juga bentonit tipe Wyoming (Nabentonit
-Swelling bentonite) atau drilling bentonit mengandung ion Na+ relative lebih
t- +
banyak jika dibandingkan dengan ion Ca^ dan in Mg^ . Na bentonit memiliki
8,5-9,8 (bersifat basa), tidak dapat diaktifkan, posisi pertukaran diduduki oleh ion-ion sodium (Na+) Mineral ini sering dipergunakan untuk Lumpur pemboran, penyumbat kebocoran bendungan, bahan pencampur pembuatan cat, bahan baku farmasi, dan perekat pasir cetak pada industri pengecoran logam. Berdasarkan kandungan bentonit yang digunakan peneliti, termasuk bentonit jenis Natrium. 2. Non-Swelling (Calcium bentonite): bentonite yang tidak bisa mengembang
Bentonit jenis ini disebut Mg, Ca-bentonit (Ca-hentonit-nonswelling bentonite). Jenis ini mengandung kalsium (K^O) dan magnesium (MgO) lebih
banyak dibandingkan natriumnya dan mempunyai sifat sedikit menyerap air sehingga apabiia didipersikan dalam air akan cepat mengendap (tidak membentuk suspensi), tetapi secara alami atau setelah diaktifkan mempunyai sifat menghisap yang baik. Perbandingan kalVdungan Na dan Ca rendah, suspensi keloidal memiliki pH 4-7 (bersifat asam). Posisi pertukaran ion lebih banyak diduduki oleh ion-ion kalsium dan magnesium. Dalam keadaan kering bersifat rapid slaking.
berwama abu-abu, biru, kuning, merah dan coklat. Penggunaan mineral ini dipergunakan untuk bahan pemucat wama untuk minyak. Bentonite termasuk mineral yang memiliki gugus aluminosilikat. Unsur-unsur kimia yang terkandung dalam Na-bentonite dan Ca-Bentonite diperlihatkan pada tabel 2.6.
Tabel 2.6. Komposisi Kimia Bentonite
Senyawa Na-Bentonite (%) Ca-Bentonite (%)
S1O2 61,3-61,4 62,12
AI2O3
19,8 17,33Fe203 3,9 5,30
CaO 0,6 3,68
MgO 1,3 3,30
Na20 2,2 0,50
K2O 0,4 0,55
H2O 7,2 7,22
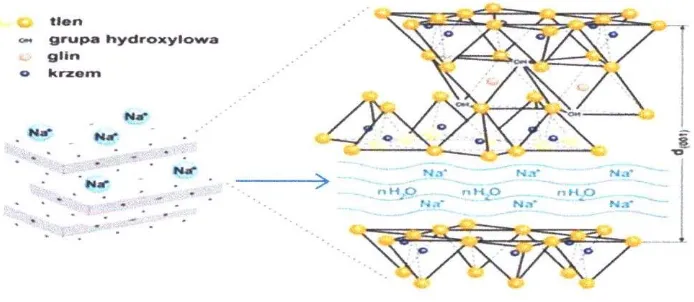
Partikel bentonite bermuatan negatif yang diimbangi dengan kation yang dapat dipertukarkan dan terikat lemah (Na, Ca, Mg, atau K). Adanya kation yang dapat dipertukarkan ini memungkinkan bentonite memisahkan logam berat dari air, dan juga memisahkan senyawa organik kationik melalui mekanisme pertukaran ion.
Adanya gaya elektostatis yang mengikat kristal pada jarak 4,5 A*^ dari permukaan cukup kuat untuk mempertahankan unit-unitnya, an akan tetap terjaga unit itu untuk tidak saling merapat. Pada pencampuran dengan air, adanya pengembangan membuat jarak antara setiap unit makin melebar dan lapisannya menjadi bentuk serpihan, serta mempunyai permukaan luas jika dalam zat pengsuspensi (Sneanabrezovska, et a l , 2004).
Gambar 2.3. Struktur Bentonite
Tabel 2.7. Kandungan Mineral Monmorilonit Senyawa Kimia rersentase (To)
SlUz O 1 — 06 /o
A l / U i Z 1 - Z4 70
1 — Z 70
Xa\J Z — J /O
MgO 3 - 4 %
K 2 0 < 0,05 %
Na20 0 - 1 %
H 2 0 1 0 - 1 1 %
(Sumber : PD. Agribisnis dan Pertambangan, 2007)
Faklor terpenting dan utama daiam pengunaan adsorbent adalah adanya ketersediaan bahan baku yang cukup melimpah di wilayah lokal. Hal ini penting bertujuan untuk meminimalisir atau mengurangi besarnya biaya pengeluaran akan biaya operasional. Pada penelitian ini digunakan absorbent Ca-Bentonite sebagai media penyerapan, pemilihan penggunaan Ca-bentonite sebagai bahan penyerapan pada proses pemurnian bioetanol didasarkan pada pertimbangan ketersediaan bentonite yang melimpah di Indonesia termasuk dari jenis Na-Bentonite dan Ca-bentonite yang ada didalamnya.
Tabel 2.8. Kandungan Ca-Bentonite Jawa Barat
65 07 % 15,86 % 3 73 %
XaKJ
7
OA0/
IVIuO
lyigo
1
QO %K2O
1,32%Na20
1,34%H2O
0,71 %TiO: 0,29 %
Cu 0,00 %
Cadangan mineral bentonite banyak diketemukan di Indonesia, diperkirakan cadangan mineral bentonite mencapai 8 juta ton (khusus di Jawa Barat). Beberapa daerah di Indonesia telah diteliti cadangan mineral bentonitenya seperti : Seurela (Sumatera Utara), Desa Petai, Nia, Lembu (Riau), Kabupaten Tanjungenim (Sumatera Selatan), Kabupaten Bengkulu Utara (Bengkulu), Jasinga kabupaten Bogor, Kabupaten Kawalu Tasikmalaya, Kabupaten Subang (Jawa Barat), Sumber Lawang Sragen, Kabupaten Boyolali, Kabupaten Grobogan (Jawa Tengah), Patuk, Sepat, Kabupaten Gunung Kidul (D.I. Yogyakarta), Sokokidul Trenggalek, Jatipokoh Ponorogo, Donorejo Pacitan, Sumber Lawang Ngawi, Pandangan Lamongan, kampung Jabon, Sumber Agung Malang (Jawa Timur). (Sukandarrumidi, 1998)
2.7 Aktivasi Adsorben
(Rosita,et al., 2004). Selain itu bentonite juga bisa diaktifkan dengan menggunakan uap air dengan suhu yang tinggi (Setyanto, 2008).
Proses aktivasi bentonite dapat dilakukan dalam 2 cara yaitu secara fisika dan Kimia :
a. Aktivasi Fisika
Aktivasi fisika biasanya dilakukan dengan pemanasan yang bertujuan untuk menguapkan air yang terperangkap tinggi dalam pori-pori kristal bentonite, sehingga luas permukaan pori-pori bertambah. Bentonite yang dipanaskan pada temperatur tinggi menyebabkan molekul air yang ada dalam bentonite mengalami dehidrasi. Sifat dehidrasi bentonite ini berpengaruh terhadap sifat adsorbsinya.
Pemanasan dilakukan dalam oven biasa pada suhu 300-400°C (untuk skala laboratorium), atau mengumpulkan tungku putar dengan pemanasan secara penghamparan selama 3 jam atau tanpa penghamparan selama 5-6 jam (skala besar). Pemanasan modemit pada suhu 300-1000°C menyebabkan destruksi struktur kristal, kandungan modemit berkurang hampir 25 % pada suhu 700°C. b. Aktivasi Kimiawi
Pada aktivasi kimia, dealuminasi adalah yang paling penting dan dominan. Dealuminasi dapat digunakan untuk mengontrol aktivasi keasaman dan untuk mengontrol ukuran pori-pori bentonite. Hal ini sangat penting terutama berhubungan dengan fungsi bentonite sebagai adsorben.
Aktivasi secara kimia dilakukan dengan lamtan asam atau basa, dengan tujuan untuk membersihkan permukaan pori, membuang senyawa pengotor, dan mengatur kembali letak atom yang dapat dipertukarkan. Aktivasi bentonite dengan asam menyebabkan temetralisasinya muatan negatif pada permukaan bentonite. Asam-asam yang dapat digunakan untuk aktivasi adalah HCl,
HNO3,
H2SO4,
danH3PO4.
Diantara asam-asam tersebut yang paling efektif untuk dealuminasi adalah HCl. Aktivasi bentonite dilakukan untuk menaikan kapasitas adsorpsi dan mendapatkan sifat bentonite yang diinginkan. Dalam keadaan awal, bentonite memiliki kemampuan adsorpsi yang rendah tetapi melalui aktivasi (penambahan asam dan pemanasan) daya adsorpsinya akan meningkat.dapat diganti seperti struktur bagian dasar dengan cara penambahan asam. Asam tersebut akan menyebabkan penggantian ion-ion K"*", dan Ca^ dengan dalam ruang interlamelar, serta akan meiepaskan ion-ion Al^"*, Fe^^ dan Mg^^ dan kisi strukturnya sehingga menjadikan bentonite lebih aktif.
Aktivasi bentonite dipengaruhi oleh konsentrasi asam yang digunakan. Selain itu, perlu diperhatikan sifat dasar, distribusi ukuran pori, keasaman dan nilai SiO:, atau
AI2O3
dalam bentonite. Faktor-faktor tersebut bergantung juga kepada komposisi mineral serta metoda aktivasinya. Aktivasi yang dilakukan dengan asam menimbulkan 3 tahap proses ;1. Mula-mula asam melarutkan komponen Fe203, ALO^, CaO dan MgO yang mengisi pori-pori adsorben. Hal ini menyebabkan terbukanya pori-pori yang tertutup sehingga menambah luas permukaan adsorben.
2. Selanjutnya ion-ion Ca^" dengan Mg^^ yang berada permukaan adsorben diganti oleh ion-ion dan asam.
3. Sebagian ion H^ yang telah menggantikan ion Ca^" dan Mg^' akan ditukar oleh ion Al^" yang telah larut dalam larutan asam dengan reaksi:
Ca^' 2H"^ + Ca"'
Bentonite f + 4 H Bentonite
^ M g " ' ' ^ 2 H " + M g " '
^ 2 H " ' ^ Ar-' + Ca"' Bentonite \^ + 4 Al"^ Bentonite C^
2.8 Penelitian Dan Proses Terkait Yang Pemah Dilakukan
Penelitian mengenai pemurnian bioetanol dengan mengunakan absorbent dan metode-metode lain sudah banyak dilaksanakan serta dipublikasikan dengan maksud menambah referensi dari berbagai macam bahan baku yang bersumber dari alam. Adapun penelitian-penelitian tersebut adalah :
1) Pemurnian bioetanol menggunakan proses adsorpsi dan distilasi adsorpsi dengan adsorbent zeolit yang dilakukan oleh (Dewi Novitasari, Djati Kusumaningrum, Tutuk D. Kusworo, 2014).
Penelitian ini bertujuan untuk mengkaji proses pemurnian bioetanol menggunakan proses adsorpsi dan distilasi adsorpsi dengan pengaruh variasi variabelnya. Pada proses distilasi menghasilkan kadar etanol yang tidak terlalu tinggi sehingga perlu dikaji suatu proses yang dapat meningkatkan kemumian bioetanol dengan proses ditilasi adsorpsi. Proses pemurnian bioetanol menggunakan zeolit sebagai adsorbentnya dengan 4 variabel berubah pada proses adsorpsi, yaitu: jenis zeolit, waktu pengadukan, waktu pendiaman, dan berat zeolit.Sedangkan pada proses ditilasi adsorpsi menggunakan 4 variabel berubah, yaitu: jenis zeolit, suhu, berat zeolit, dan waktu. Dari hasil penelitian didapatkan bahwa proses yang paling efektif untuk pemurnian etanol adalah proses distilasi adsorpsi dengan adsorbent zeolit 4A dengan berat 100 gram, suhu proses 78°C,waktu proses 50 menit. Kadar etanol yang dihasilkan sebesar 98,42%.
2) Pembuatan adsorben dari zeolit alam malang untuk pemurnian bioetanol menjadi Fuel Grade Ethanol {FGE) yang dilakukan oleh (Diesta Noer Pratama Widjaja, Aprilianus Yohan, Yemima Miracle Sutjahjo, 2013).
Bioetanol dengan indeks bias tertinggi diuji dengan GC dan zeolit alam termodifikasi dikarakterisasi dengan EDX. Dari hasil penelitian diperoleh daya adsorpsi air tertinggi zeolit alam sebesar 0,45 gram air/gram adsorben dengan kondisi proses aktivasi zeolit yaitu menggunakan larutan H2S04 2% dan suhu kalsinasi 600°C. Konsentrasi bioetanol setelah adsorpsi sebesar 99,7%.
3) Metode flow system dalam purifikasi bioetanol dengan menggunakan dual adsorben (KS-SG) yang dilakukan oleh (Putri Anisa, 2014).
3.1 Waktu Dan Tempat
Penelitian mengenai pemurnian bioetanol dengan proses adsorpsi-distilasi menggunakan adsorbent bentonite dilakukan di laboratorium Kimia Organik Prodi Teknik Kimia Fakultas Teknik Universitas Muhammadiyah Palembang. Dari tanggal 11 April - 11 Mei 2015,
3.2 Alat Dan Bahan
3.2.1. Alat-Alat Vang Digunakan
- Thermometer - Pipet Volume - Gelas Ukur -Pipet Tetes - Gelas Beaker - Pipet ukur - Statif klem - Screening - Neraca Analitik - Pengaduk - Almunium Foil - Selang
- Erienmeyer - Cawan Porselen - Hot Plate - Kertas Saring - Corong Kaca - Pemanas
- Rangkaian Alat Adsorpsi Distilasi - Labu Leber Dua
- Piknometer - Furnace - Penyumbat - PH Meter
3.2.2. Bahan- Bahan Vang Digunakan
-Asam klorida ( H C l ) - Aquadest
- Bentonite (Non-Swelling/Ca-Bentonite) - Bioetanol (70%)
3
Gambar 3.1 Rangkaian Alat Adsorpsi-Distilasi
Keterangan Gambar
1. Temiometer 2. Penyumbat 3. Labu Leber Dua 4. Pemanas
3.4 Prosedur Percobaan Pengamatan
D I A G R A M A L I R PROSES B I O E T A N O L DAN A K T I V A S I B E N T O N I T E
Aquadest + HCL
(300 ml - / N)
Aquadest
3/ Adsorbent, Bentonite Aktivasi
(30 gram, 50 gram, 70, gram, 90 gram,
dan 110 gram)
Bentonite
Penggilingan
w Pengayakan
(100 mesh)
V Aktivasi
Pembiiasan Air
Pengeringan
(Suhul50 °C, waktu I Jam)
Bentonite Aktif
Bioetanol
V
Adsorpsi-Distilasi
(Suhu 80%, Waktu 30 menit, 50 menit, 70 menit,
90 menit, dan 110 menit)
Gas Chron latography
3.4.1. Proses Pembuatan Bentonite
1. Ca-Bentonite yang masih kasar dihaluskan dengan cara pengayakan menggunakan screening hingga diperoleh ukuran partikel sebesar 100 mesh.
2. Besaran penggunaan Ca-Bentonite kemudian ditimbang dan disesuaikan dengan variabel yang telah ditentukan (30 gram, 50 gram, 70 gram, 90 gram, dan 110 gram) kemudian di lakukan penambahan aquadest dengan perbandingan konsentrasi sebanyak (1:1) b/v atau gr/ml untuk dilakukan pembiiasan agar menghilangkan baban-baban pengotor yang terdapat pada bentonite. Selanjutnya bentonite disaring untuk memisahkan air dan padatan.
3. Bentonite kemudian dikeringkan dalam oven pada suhu 150 °C dengan waktu 1 jam.
3.4.2 Proses Aktivasi Bentonite
Proses aktivasi dilakukan dengan tujuan membuka dan menambah pori-pori pada bentonite. Bertambabnya jumlah pori-pori pada bentonite akan meningkatkan luas permukaan bentonite yang mengakibatkan kapasitas penyerapannya menjadi bertambah besar.
Tahapan pembuatan bentonite aktivasi:
1. Pembuatan bentonite aktivasi sesuai variable berat bentonite (30 gram, 50 gram, 70 gram, 90 gram, 110 gram) yang sebeiumnya berbentuk butiran-butiran balus, masing-masing bentonite direndam ke dalam 300 mL aquadest denngan HCL 1 N selama kurang lebih 3 jam. Penggunaan konsentrasi HCL 1 N pada bentonite merupakan kondisi optimum proses aktivasi bentonite. Apabila kosentrasi yang digunakan berlebih maka dikbawatirkan bentonite akan mengalami pelepesan (Dealuminasi)
unsur pengikatnya dalam jumlah berlebih sehingga gugus alkil akan berkurang dan struktur bentonite menjadi rusak.
2. Selanjutnya dilakukan pengadukan agar sampei bentonite tercampur secara bomogen. 3. Campuran tersebut kemudian disaring dan dibilas dari bahan pengotomya dengan
aquadest kembali. Kemudian dikeringkan dalam oven pada suhu sekitar 150 % selama 1 jam.
3.4.3 Proses Adsorpsi Distilasi Bioetanol Dengan Bentonite Teraktivasi
Proses Adsorpsi Distilasi dilakukan dengan beberapa tahapan yaitu :
1. Proses adsorpsi-distilasi dilakukan secara simultan dengan memasukkan etanol dengan kadar 70% sebanyak 200 ml bersama bentonite yang telah teraktivasi sebeiumnya ke dalam labu leher dua kemudian dilakukan pengadukan selama 5 menit agar keduanya tercampur secara merata. Selanjutnya dilakukan pendiaman sementara selama 30 menit.
2. Etanol dan bentonite yang telah berada di dalam labu leher dua tadi selanjutnya dilakukan proses distilasi, Kemudian dipanaskan sampai terbentuk uap hingga menghasilkan cairan etanol mumi.
3. Pemanasan dihentikan jika telah diperoleh distilat hasil adsorpsi-distilasi tadi yang dilakukan secara simultan. Waktu lamanya adsorpsi-distilasi disesuaikan dengan variabel waktu (30 menit, 50 menit, 70 menit, 90 menit, dan 110 menit) dengan temperature suhu konstan 80°C.
4. Distilat ini kemudian di analisis kandungan persentase kemurnian bioetanolnya dengan menggunakan Gas Chromatography (GC).
Menganalisa besaran kadar air, dan kadar abu pada adsorbent bentonite, a. Analisa kadar air
Sampei yang diperoleh ditimbang kemudian dimasukkan dalam oven pada suhu 100-105 °C sehingga massanya konstan (A.O.A.C., 1970).
b. Analisis kadar abu
Pengujian diawali dengan menimbang 2-10 gram sampei dalam cawan porselen yang telah diketahui bobotnya. Proses dilanjutkan dengan membakar sampei sampai tidak berasap dan mengabukannya dalam tanur pada suhu 600°C selama 5 jam. Selanjutnya bahan ditimbang hingga diperoleh bobot yang konstan. (A.O.A.C., 1995):
Kadar Air (%) = Kehilangan Berat X 100% Berat Sampei
Bobotabu Kadar Abu (%) =
Penelitian ini dilakukan dengan maksud dan bertujuan untuk meningkatkan kemumian kadar bioetanol. Bioetanol yang digunakan sebagai umpan yaitu Bioetanol dengan kadar 70%. Untuk mendapatkan kemumian bioetanol yang optimal maka pada penelitian ini menggunakan tahapan proses Adsorpsi-Distilasi. Mekanisme yang dilakukan adalah pertama untuk mengetahui variabel yang berpengaruh pada proses adsorpsi yaitu berdasarkan variable berat adsorbent bentonite dan lamanya waktu proses Adsorpsi-Distilasi.
4.1. Hasil Penelitian
4.1.1 Pengaruh Variabel Pada Proses Adsorpsi-Distilasi
Proses adsorpsi-distilasi adalah suatu proses penyerapan dan pemisahan dilakukan secara bersamaan dimana komponen dari suatu fase fluida berpindah ke pennukaan zat padat yang menyerap (adsorbent) hal ini bertujuan untuk mengeffisiensi lamanya waktu operasi dan penggunaan bahan yang digunakan. Pada proses adsorpsi-distilasi dilakukan variasi variabel untuk mengetahui variabel yang paling mempengamhi proses. Umpan bioetanol yang digunakan adalah etanol dengan kadar 70%. Sedangkan variasi variabel yang digimakan adalah berat bentonite dan lamanya waktu adsorpsi-distilasi.
Di bawah ini mempakan hasil data penelitian yang telah dilakukan sebeiumnya, kemudian hasil yang diperoleh disajikan pada Tabel 4.1. sampai dengan Tabel 4.6., dan untuk memudahkan hasil pembahasan. Ditampilkan pada Gambar 4.1 sampai Gambar 4.6.
Dari masing - masing tabel disajikan pengaruh variasi berat bentonite 30 gram, 50 gram, 70 gram, 90 gram, dan 110 gram yang kemudian dikombi nasi kan dengan variasi waktu lamanya distilasi 30 menit, 50 menit, 70 menit, dan 110 menit.
Tabel 4.1. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 30 Gram
Waktu (Menit)
Persentase Kenaikan Kadar Etanol (%) Waktu
(Menit) Suhu (°C) Etanol Awal Etanol Akhir
30 80 70 88,67
50 80 70 85,69
70 80 70 88,84
90 80 70 87,36
110 80 70 91,38
Tabel 4.2. Pengarub Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 50 Gram
Waktu (Menit)
Persentase Kenaikan Kadar Etanol (%) Waktu
(Menit) Suhu i°C) Etanoi Awal Etanoi Akhir
30 80 70 89,03
50 80 70 88,51
70 80 70 90,64
90 80 70 87,35
110 80 70 93,29
Tabel 4.3. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 70 Gram
Waktu (Menit)
Persentase Kenaikan Kadar Etanol (%) Waktu
(Menit) Suhu G O Etanol Awal Etanol Akhir
30 80 70 89,61
50 80 70 86,79
70 80 70 90,88
90 80 70 90,62
n o 80 70 87,17
100
Gambar 4.3 Grafik Hubungan Kadar Etanol (%) Dengan Waktu (menit) Distilasi
Tabel 4.4, Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 90 Gram
Waktu (Menit)
Persentase Kenaikan Kadar Etanol (%) Waktu
(Menit) Suhu C^C) Etanoi Awal Etanol Akhir
30
80
70
91,18
50
80
70
90,65
70
80
70
89,76
90
80
70
86,61
n o
80
70
89,26
100
30 60
Waktu (Menit)
90 120
G a m b a r 4.4 G r a f i k Hubungan K a d a r Etanol (%) Dengan W a k t u (menit) Distilasi
Tabel 4.5. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 110 Gram
Waktu (Menit)
Persentase Kenaikan Kadar Etanol (%) Waktu
(Menit) Suhu (°C) Etanol Awal Etanol Akhir
30 80 70 88,36
50 80 70 84,59
70 80 70 82,52
90 80 70 90,23
n o 80 70 92,66
Tabel 4.6. Tabel Keseluruhan Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Kenaikan Kadar Etanol Dengan Berat Bentonite 30 Gram, 50 Gram,
70 Gram, 90 Gram, Dan 110 Gram
No. Identitas Sampei Waktu Hasil (%)
1. Bentonite 30 gram 30 menit 88,67
2. Bentonite 30 gram 50 menit 85,69
3. Bentonite 30 gram 70 menit 88,84
4. Bentonite 30 gram 90 menit 87,36
5. Bentonite 30 gram 110 menit 91,38
6. Bentonite 50 gram 30 menit 89,03
7. Bentonite 50 gram 50 menit 88,51
8. Bentonite 50 gram 70 menit 90,64
9. Bentonite 50 gram 90 menit 87,35
10. Bentonite 50 gram 110 menit 93,29
11. Bentonite 70 gram 30 menit 89,61
12. Bentonite 70 gram 50 menit 86,79
13. Bentonite 70 gram 70 menit 90,88
14. Bentonite 70 gram 90 menit 90,62
15. Bentonite 70 gram 110 menit 87,17
16. Bentonite 90 gram 30 menit 91,18
17. Bentonite 90 gram 50 menit 90,65
18. Bentonite 90 gram 70 menit 89,76
19. Bentonite 90 gram 90 menit 86,61
20. Bentonite 90 gram 110 menit 89,26
21. Bentonite 110 gram 30 menit 88,36
22. Bentonite 110 gram 50 menit 84,54
23. Bentonite 110 gram 70 menit 82,52
24. Bentonite 110 gram 90 menit 90,23
100
95
-0 2-0 4-0 6-0 8-0 1-0-0 12-0 Waktu (menit)
••^"Benloiiile 30 gram ^^^Bentonitc 50 gram ——-• Bentonite 70 gram » Denlonile 90 gram " ' • ' Iknlonile 110 gram
G a m b a r 4.6 Grafik Keseluruhan Hubungan K a d a r Etanol (%) Dengan W a k t u (menit) Distilasi
Pengaruh waklu proses adsorpsi-distilasi terhadap kenaikan kadar etanol akan ditampilkan pada Tabel 4.6 dan Gambar 4.6 diatas, data ini diambil pada suhu tetap 80°C. Variasi waktu yang digunakan adalah dengan waktu adsorpsi-distilasi 30 menit, 50 menit, 70 menit, 90 menit, dan 110 menil. Dan Tabel 4.6 tersebut diatas didapatkan variasi waktu yang paling optimal adalah pada waktu
110 menit proses. Sedangkan dari variasi beral diperoleh kadar etanol yang paling optimal yaitu sebesar 93,29 % dengan berat bentonite yang digunakan sebesar 50 gram.
adsorbent maka jumlah etanol yang terserap juga semakin banyak (Sherviena dkk.,2010).
Adanya konsentrasi larutan etanol mula inula yang tetap, maka air yang terjerap akan semakin banyak. Flow rate etanol dipengaruhi oleh volume etanol yang dihasilkan dari proses adsorpsi-distilasi itu sendiri. Volume etanol yang diperoleh, dipengaruhi oleh porositas bentonite, luas penampang bentonite yang semakin besar dan daya scrap benonite terhadap molekul air dalam larutan etanol. Pengaruh penggunaaan bentonite yang digunakan terhadap lama waktu proses adsorpsi-distilasi terhadap peningkatan kadar etanol dapat dilihat pada Gambar 4.6.
Setiap adsorbent mempunyai daya scrap terhadap etanol yang berbeda-beda tergantung dari jenis adsorbent yang digunakan. Dan juga setiap penambahan berat adsorbent yang digunakan akan memberikan kemampuan menyerap etanol yang berbeda pula terhadap kenaikan kadar etanol. Hal ini sesuai dengan tujuan penelitian yang dilakukan yaitu untuk dapat mengetahui pemurnian bioetanol menggunakan proses adsorpsi-distilasi dengan menggunakan adsorbent bentonite sehingga mendapatkan hasil penyerapan etanol yang optimal dengan hasil kadarisasi etanol yang dapat mencapai etanol dengan standar Fuel Grade Etanol (FGE).
4.2. Pengaruh Penurunan Kadar air Dan Pengotomya
Proses adsorpsi adalah suatu proses pemisahan dimana komponen dari suatu tase fluida berpindah ke pennukaan zat padat yang menyerap (adsorbent).
Sedangkan variasi variabel yang digunakan adalah berat bentonite, dan waktu adsorpsi-distilasi. Di bawah ini merupakan hasil dari penurunan jumlah kadar air yang akan disajikan pada Tabel 4.7. sampai dengan Tabel 4.12. Dari masing - masing tabel disajikan pengaruh dari variasi berat bentonite 30 gram, 50 gram, 70 gram, 90 gram, dan 110 gram yang dikombinasikan dengan variasi waktu bentonite sehingga didapatkan besaran jumlah penurunan kadar air dan pengotomya dari masing-masing sampei.
Tabel 4.7. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 30 Gram
Waktu (menit)
Konsentrasi Kadar Air (%) Waktu
(menit) Kadar Air Awal Kadar Air Akhir Penurunan Kadar Air
30 30 11,32 18,67
50 30 14,30 15,69
70 30 11,15 18,84
90 30 12,63 17,36
110 30 8,61 21,38
Waktu (menit)
Pada Tabel 4.7 dan Gambar 4.7 diatas dapat dilihat hasil penelitian terbaik yang diambil berdasarkan pengaruh waktu proses Adsorpsi-Distilasi pada penurunan kadar air untuk berat bentonite 30 gram. Dimana dilakukan proses adsorpsi-distilasi secara simultan pada kondisi suhu SOX.
Kemudian didapatkan hasi! kondisi yang optimal untuk bentonite 30 gram adalah pada waktu operasi selama 1 10 menit dengan kadar air awal yang semula 30 % didapatkan hasil kadar air akhir menjadi 8,61 %, terjadi penurunan kadar air dengan range sebesar 21,38 %.
Tabel 4.8. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 50 Gram
Waktu (menit)
Konsentrasi Kadar Air (%) Waktu
(menit) Kadar Air Awal Kadar Air Akhir Penurunan Kadar Air
30 30 10,96 19,03
50 30 11,48 18,51
70 30 9,35 20,64
90 30 12,64 17,35
n o 30 6,70 23,29
35
0 20 40 60 80 100 120 Waktu (menit)
Pada Tabel 4.8 dan Gambar 4.8 diatas dapat dilihat hasil penelitian terbaik yang diambil berdasarkan pengaruh waktu proses Adsorpsi-Distilasi pada penurunan kadar air untuk berat bentonite 50 gram. Dimana dilakukan proses adsorpsi-distilasi secara simultan pada kondisi suhu SO'^C.
Kemudian didapatkan hasil kondisi yang optimal untuk bentonite 50 gram adalah pada waktu operasi selama 110 menit dengan kadar air awal yang semula 30 % didapatkan hasil kadar air akhir menjadi 6,70 %, terjadi penurunan kadar air dengan range sebesar 23,29 %.
Tabel 4.9. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 70 Gram
Waktu (menit)
Konsentrasi Kadar Air (%) Waktu
(menit) Kadar Air Awal Kadar Air Akhir Penurunan Kadar Air
30 30 10,38 19,61
50 30 13,20 16,79
70 30 9,11 20,88
90 30 9,37 20,62
n o 30 12,82 17,17
35
ir air
Waktu (menit)
Pada Tabel 4.9 dan Gambar 4.9 diatas dapat dilihat hasil penelitian terbaik yang diambil berdasarkan pengaruh waktu proses Adsorpsi-Distilasi pada penurunan kadar air untuk berat bentonite 70 gram. Dimana dilakukan proses adsorpsi-distilasi secara simultan pada kondisi suhu 80°C.
Kemudian didapatkan hasil kondisi yang optimal untuk bentonite 70 gram adalah pada waktu operasi selama 70 menit dengan kadar air awal yang semula 30 % didapatkan hasil kadar air akhir menjadi 9,11 %, terjadi penurunan kadar air dengan range sebesar 20,88 %.
Tabel 4.10. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 90 Gram
Waktu (menit)
Consentrasi Kadar Air (%) Waktu
(menit) Kadar Air Awal Kadar Air Akhir Penurunan Kadar Air
30 30 8,81 21,18
50 30 9,34 20,65
70 30 10,23 19,76
90 30 13,38 16,61
110 30 10,73 19,26
air
Waktu (menit)
Pada Tabel 4.10 dan Gambar 4.10 diatas dapat dilihat hasil penelitian terbaik yang diambil berdasarkan pengaruh waktu proses Adsorpsi-Distilasi pada penurunan kadar air untuk berat bentonite 90 gram. Dimana dilakukan proses adsorpsi-distilasi secara simultan pada kondisi suhu 80°C.
Kemudian didapatkan hasil kondisi yang optimal untuk bentonite 90 gram adalah pada waktu operasi selama 30 menit dengan kadar air awal yang semula 30 % didapatkan hasil kadar air akhir menjadi 8,81 %, terjadi penurunan kadar air dengan range sebesar 21,18%.
Tabel 4.11. Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 110 Gram
Waktu (menit)
Konsentrasi Kadar Air (%) Waktu
(menit) Kadar Air Awa! Kadar Air Akhir Penurunan Kadar Air
30 30 11,63 18,36
50 30 15,45 14,54
70 30 17,47 12,52
90 30 9,76 20,23
n o 30 7,33 22,66
35
0 20 40 60 80 100 120 Waktu (menit)
Pada Tabel 4,11 dan Gambar 4.11 diatas dapat dilihat hasil penelitian terbaik yang diambil berdasarkan pengaruh waklu proses Adsorpsi-Distilasi pada penurunan kadar air untuk berat bentonite 110 gram. Dimana dilakukan proses adsorpsi-distilasi secara simultan pada kondisi suhu 80°C.
Tabel 4.12. Tabel Keseluruhan Pengaruh Waktu Proses Adsorpsi-Distilasi Pada Penurunan Kadar Air Dan Pengotomya Dengan Berat Bentonite 30
Gram, 50 Gram, 70 Gram, 90 Gram, Dan 110 Gram
No. Berat Bentonite Waktu Awal (%) iiasil (%) Penurunan Kadar Air (%)
1. Bentonite 30 gram 30 menit 30 11,32 18,67
2. Bentonite 30 gram 50 menit 30 14,30 15,69
-1
j>. Bentonite 30 gram 70 menit 30 11,15 18,84
4. Bentonite 30 gram 90 menit 30 12,63 17,36
5. Bentonite 30 gram 110 menit 30 8,61 21,38
6. Bentonite 50 gram 30 menit 30 10,96 19,03
7. Bentonite 50 gram 50 menit 30 11,48 18,51
8. Bentonite 50 gram 70 menit 30 9,35 20,64
9. Bentonite 50 gram 90 menit 30 12,64 17,35
10. Bentonite 50 gram n o menu 30 6,70 23,29
11. Bentonite 70 gram 30 menit 30 10,38 19,61
12. Bentonite 70 gram 50 menit 30 13,20 16,79
13, Bentonite 70 gram 70 menit 30 9,11 20,88
14. Bentonite 70 gram 90 menit 30 9,37 20,62
15. Bentonite 70 gram 110 menit 30 12,82 17,17
16. Bentonite 90 gram 30 menit 30 8,81 21,18
17. Bentonite 90 gram 50 menit 30 9,34 20,65
18. Bentonite 90 gram 70 menit 30 10,23 19,76
19. Bentonite 90 gram 90 menit 30 13,38 16,61
20. Bentonite 90 gram 110 meni! 30 10,73 19,26
21. Bentonite 110 gram 30 menit 30 11,63 18,36
22. Bentonite 110 gram 50 menit 30 15,45 14,54
23. Bentonite 110 gram 70 menit 30 17,47 12,52
24. Bentonite 110 gram 90 menit 30 9,76 20,23
Waktu (menit)
•—Bentonite 30 gram —•—Bentonite 50 gram Bentonite 70 gram
Bentonite 90 gram ——'Bentonite 110 gram
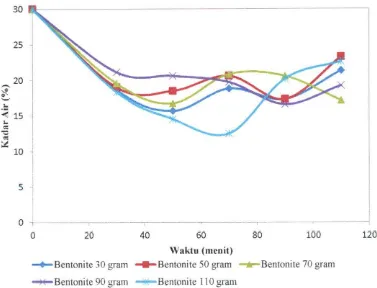
Gambar 4.12 Grafik Keseluruhan Hubungan Kadar Air (%) Dan Pengotomya Dengan Waktu (menit) Distilasi
Pengaruh waktu proses adsorpsi-distilasi terhadap penurunan kadar air akan ditampilkan pada tabel 4.12 dan Gambar 4.12 diatas, data ini diambil pada suhu tetap 80°C. Variasi waktu yang digunakan adalah dengan waktu adsorpsi-distilasi 30 menit, 50 menit, 70 menit, 90 menit, dan 110 menit. Dari Tabel 4.12 tersebut diatas didapatkan variasi waklu yang paling optimal adalah pada waktu
110 menit proses. Sedangkan dari variasi berat diperoleh hasil kadar air yang paling baik dengan nilai 6,70 % dengan hasil penurunan kadar air sebesar 23,29 % dengan berat bentonite yang digunakan sebanyak 50 gram.
pori-pori bentonite, hai ini juga sekaiigus menandakan adanya pertukaran ion yang telah terjadi pada luas permukaan bentonite sehingga proses transfer massa etanol ke dalam adsorbent juga semakin bertambah banyak. Semakin kecil ukuran partikel bentonite yang digunakan maka akan semakin besar pula daya scrap bentonite terhadap molekul air dalam larutan etanol tergantung dari jenis absorbent dan proses aktivasi adsorbent yang digunakan.
4.3. Perbandingan Yang Mendekati Pada Penelitian Sebeiumnya
Penelitian mengenai pemurnian bioetanol dengan mengunakan absorbent dan metode-metode lain sudah banyak dilaksanakan serta dipublikasikan dengan maksud menambah referensi dari berbagai macam bahan baku yang bersumber dari alam. Adapun penelitian-penelitian tersebut adalah :
1) Pemurnian bioetanol menggunakan proses adsorpsi dan distilasi adsorpsi dengan adsorbent zeolit yang dilakukan oleh (Dewi Novitasari, Djati Kusumaningrum, Tutuk D. Kusworo, 2014).
Pada penelitian ini proses pemurnian bioetanol menggunakan proses adsorpsi dan distilasi adsorpsi dengan pengaruh varia