INTISARI
Tujuan penelitian ini untuk mengetahui efek toksik penggunaan biji
Persea americana Mill. pada pemberian subakut terhadap perubahan struktural histopatologis hati tikus galur Sprague Dawley dan mengetahui reversibilitas sifat efek toksik yang ditimbulkannya.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Lima puluh ekor tikus galur Sprague Dawley
(25 jantan dan 25 betina), umur 2-3 bulan, dibagi dalam 5 kelompok secara acak. Kelompok I-IV dipejankan infusa biji alpukat selama 28 hari secara peroral pada dosis 202,25 ; 360 ; 640,8 ; 1140,6 mg/kgBB, Kelompok V kontrol negative 14.285 mg/kgBB. Pada hari ke-29 sebanyak tiga tikus dari tiap dosis dikorbankan lalu dilakukan pembedahan untuk melihat histopatologis hati. Sisa hewan uji dipelihara tanpa diberi perlakuan selama 14 hari untuk melihat reversibilitas efek toksik yang ditimbulkan. Pada hari ke-15, tikus yang tersisa dikorbankan dan diambil organ hati untuk dilakukan pemeriksaan histopatologis. Perubahan struktural histopatologis hati yang diamati meliputi kejadian degenerasi dan nekrosis dari sel hati di sekitar vena porta dan vena sentralis. Pengamatan dilakukan di bawah mikroskop cahaya (Olympus PP 10®) di Laboratorium Patologi Fakultas Kedokteran Hewan UGM, Yogyakarta.
ABSTRACT
The aim of this study is to determine the subacute toxic effects of the use of Persea americana Mill. seed infusion on structural changes of liver histopathologic in Sprague Dawley rats and to know reversibility of toxic effects caused.
This study is a pure experimental design with randomized design pattern. A total of 50 Sprague Dawley rats (25 males and 25 females), aged 2-3 months, were randomly divided into 5 groups. Group I-IV were administered avocado seed infusion during 28 days, orally at a dose of 202.25; 360; 640.8; 1140.6 mg/kg, Group V negative control 14.285 mg/kg. On day 29, three rats from each dose was sacrificed and then performed surgery to examine the liver histopathology. The rest of the test animals were reared without treated for 14 days to see the reversibility of toxic effects caused. On the 15th day, the remaining rats were sacrificed and the liver was taken for histopathological examination. Structural changes in liver histopathologic which is observed were the incidence of degeneration and necrosis of liver cells around the portal vein and central vein. Observations were carried out under a light microscope (Olympus PP 10®) at the Faculty of Veterinary Pathology UGM Laboratory, Yogyakarta.
Liver histopathologic analysis results showed that there are no subacute toxic effects of the use of Persea americana Mill. seed infusion on structural changes of liver histopathologic in Sprague Dawley rats. Reversibility of toxic effects of the use of Persea americana Mill. seed infusion can not be determined because there are no structural changes in liver histopathologic due to the usage of
Persea americana Mill. seeds infusion in Sprague Dawley rats.
UJI TOKSISITAS SUBAKUT INFUSA BIJI Persea americana Mill. TERHADAP GAMBARAN HISTOPATOLOGIS HATI
TIKUS SPRAGUE DAWLEY
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Trifonia Ingrid Octavia NIM : 118114138
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
UJI TOKSISITAS SUBAKUT INFUSA BIJI Persea americana Mill. TERHADAP GAMBARAN HISTOPATOLOGIS HATI
TIKUS SPRAGUE DAWLEY
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Trifonia Ingrid Octavia NIM : 118114138
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Filipi 1:6: “Akan hal ini aku yakin sepenuhnya, yaitu Ia, yang memulai
pekerjaan yang baik di antara kamu, akan meneruskannya sampai pada
akhirnya pada hari Kristus Yesus.”
Apapun yang telah Tuhan mulai dalam kehidupanku, Ia akan menyelesaikan karyaNya hingga pada akhirnya, Ia tidak akan meninggalkan karya yang telah Ia
mulai. Kita bisa meninggalkan Allah, namun Allah tidak akan pernah meninggalkan kita, meskipun kita sering meninggalkan dan mengecewakan Allah.
Kupersembahkan karya ini bagi ....
Tuhan Yesus yang selalu menerangi jalanku dikala ku tersesat dan tak kenal arah
serta melimpahkan berkat kasih karunia kepadaku.
Keluarga tercinta yang selalu mendukung dan melimpahiku dengan kasih yang menguatkan aku.
vii PRAKATA
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas
segala berkat dan rahmat-Nya, sehingga penulis dapat menyelesaikan skripsi
dengan judul “Uji Toksisitas Subakut Infusa Biji Persea americana Mill. terhadap
Gambaran Histopatologis Hati Tikus Sprague Dawley” ini dengan baik. Skripsi
ini disusun untuk memenuhi persyaratan memperoleh gelar Sarjana Strata Satu
Program Studi Fakultas Farmasi Universitas Sanata Dharma.
Penulis menyadari bahwa dalam pelaksanaan dan penyusunan skripsi ini
tidak terlepas dari bantuan dan campur tangan berbagai pihak. Oleh karena itu
penulis hendak mengucapkan terima kasih kepada :
1. Dekan Fakultas Farmasi Universitas Sanata Dharma
2. Ibu drh. Sitarina Widyarini MP., PhD selaku Pembimbing I skripsi ini, atas
segala kesabaran dalam membimbing, memberi masukan dan memotivasi
penulis selama pelaksanaan dan penulisan skripsi.
3. Ibu Phebe Hendra, M.Si., Ph.D., Apt., selaku Pembimbing II skripsi ini atas
segala kesabaran untuk selalu membimbing dan memberikan masukan kepada
penulis selama penelitian dan penyusunan skripsi ini.
4. Bapak Ipang Djunarko, M.Sc., Apt. selaku Dosen Penguji skripsi atas
bantuan dan masukkan kepada penulis selama penyusunan skripsi ini.
5. Bapak Prof. Dr. C.J. Soegihardjo, Apt. selaku Dosen Penguji skripsi atas
viii
6. Ibu Agustina Setiawati, M.Sc., Apt., selaku Kepala Laboratorium Fakultas
Farmasi yang telah memberikan ijin dalam penggunaan semua fasilitas
laboratorium selama penelitian ini.
7. Bapak Heru Purwanto selaku Laboran Farmakologi dan Toksikologi, Bapak
Supardjiman selaku Laboran Imono, Bapak Kayatno selaku Laboran Biokimia,
Bapak Wagiran selaku Laboran Farmakognosi-Fitokimia, Bapak Kunto selaku
Laboran Kimia Analisis, Bapak Ottok selaku pengelola gudang kefarmasian atas
segala bantuan selama pelaksanaan penelitian skripsi ini.
8. Bapak Sugiyono yang telah banyak membantu dalam pemeriksaan dan
menentukan diagnosis histopatologis organ, serta Bapak Lilik selaku laboran
Laboratorium Patologi Fakultas Kedokteran Hewan UGM yang membantu
dalam pembuatan preparat histopatologis.
9. Segenap dosen dan karyawan atas ilmu yang diberikan.
10. Kedua orang tua penulis, Yusuf Evol Chairul dan Merani Leo yang
memberikan doa, kasih sayang, semangat dan telah mendanai sebagian besar
penelitian untuk menyelesaikan skripsi ini.
11. Keponakan tersayang Golvinus Noah Suciptan yang selalu menjadi semangat
dikala sedih, kakak perempuan Theresia Imelda Octavia dan sepupu
tersayang Sunny Cheryline yang selalu mendukung dalam penyelesaian
penelitian dan penyusunan skripsi ini.
12. Sahabat dan rekan sekerja “Tim Biji Alpukat” Marselina Cresentia Tisera,
Agustina Iswara Maharani, Rosita Olimpia Bagiastrasari, Christina Desi,
ix
perjuangan, dan kebersamaan selama penelitian dan pengerjaan skripsi ini
sampai akhir.
13. Sahabat terkasih, Verni Emelia, Esterina Dwi Astuti, Fransisca Andriani,
Theresia Eviani, Gretta Paulina, Lusia Drikti, Stefani Agustina, Juventia Tjoa,
dan Daisy Orlana atas bantuan, dukungan, perhatian dan motivasi dalam suka
maupun duka selama ini.
14. Teman-teman Farmasi angkatan 2011, khususnya FSM C dan FKK B 2011
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta yang selalu
memberikan dukungan, motivasi dan masukan terhadap penelitian maupun
penyusunan skripsi ini.
15. Semua pihak yang tidak dapat penulis sebutkan satu per satu sehingga penulis
dapat menyelesaikan tugas akhir ini dengan baik.
Penulis menyadari bahwa tugas akhir ini belum sempurna dan masih
banyak kekurangan. Oleh karena itu, penulis mengharapkan kritik, saran dan
masukan demi kemajuan di masa yang akan datang. Penulis berharap semoga
tugas akhir ini dapat memberikan manfaat sekecil apapun bagi perkembangan
ilmu pengetahuan khususnya di bidang ilmu kefarmasian, serta semua pihak, baik
mahasiswa, maupun masyarakat.
Yogyakarta, 22 April 2015
x DAFTAR ISI
HALAMAN JUDUL …... i
HALAMAN PERSETUJUAN PEMBIMBING …... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN …... iv
PERNYATAAN KEASLIAN KARYA …... v
PERNYATAAN PERSETUJUAN PUBLIKASI …... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN... xvi
INTISARI ... xvii
ABSTRACT ... xviii
BAB 1. PENGANTAR ... 1
A. Latar Belakang ... 1
1. Rumusan masalah ... 3
2. Keaslian penelitian ... 4
3. Manfaat penelitian ... 6
a. Manfaat teoritis ... 6
xi
B. Tujuan Penelitian ... 6
1. Tujuan umum ... 6
2. Tujuan khusus ... 6
BAB II. PENELAAHAN PUSTAKA ... 7
A. Persea americana Mill. ... 7
1. Deskripsi tanaman ... 7
2. Taksonomi biji alpukat ... 8
3. Kandungan kimia dan kegunaannya ... 8
B. Toksikologi ... 9
C. Toksisitas Subakut ... 10
D. Hati ... 12
1. Anatomi hati ... 12
2. Fisiologi hati ... 15
E. Hepatotoksisitas ... 16
F. Infusa ... 18
G. Keterangan empiris ... 18
BAB III. METODE PENELITIAN ... 19
A. Jenis dan Rancangan Penelitian ... 19
B. Variabel dan Definisi Operasional ... 19
1. Variabel utama ... 19
2. Variabel pengacau ... 19
3. Definisi operasional ... 20
xii
D. Alat atau Instrumen Penelitian ... 22
1. Alat pembuatan simplisia ... 22
2. Alat penetapan kadar air ... 22
3. Alat pembuatan infusa biji Persea americana Mill. ... 22
4. Alat uji perlakuan dan pemeriksaan histopatologis ... 23
E. Tata Cara Penelitian ... 23
1. Determinasi serbuk biji Persea americana Mill. ... 23
2. Pengumpulan bahan ... 23
3. Pembuatan serbuk ... 23
4. Penetapan kadar air serbuk biji Persea americana Mill…... 23
5. Pembuatan infusa biji Persea americana Mill. ... 24
6. Penetapan dosis infusa biji Persea americana Mill. ... 24
7. Penetapan dosis kontrol negatif (aquadest )... 25
8. Penyiapan hewan uji ... 26
9. Pengelompokkan dan perlakuan hewan uji ... 26
10.Prosedur pelaksanaan penelitian ... 26
11.Prosedur pemusnahan hewan uji ... 27
12.Pengamatan ... 27
a. Penimbangan berat badan hewan uji ... 27
b. Pengukuran asupan pakan dan minum hewan uji... 27
13.Pembuatan preparat dan pemeriksaan histologis ... 28
F. Tata Cara Analisis Hasil ... 29
xiii
2. Uji reversibilitas ... 29
3. Pengamatan berat badan hewan uji ... 29
4. Pengukuran asupan pakan dan minum hewan uji ... 29
G. Alur Penelitian ... 30
BAB IV. HASIL DAN PEMBAHASAN ... 31
A. Determinasi Tanaman ... 31
B. Penetapan Kadar Air Serbuk Biji Persea americana Mill. ... 31
C. Gambaran Histopatologis Hati Tikus Sprague Dawley yang Diberi Infusa Biji Persea americana Mill. ... 32
D. Perubahan Berat Badan ... 41
E. Asupan Pakan Tikus Jantan dan Betina ... 44
F. Asupan Minum Tikus Jantan dan Betina ... 46
BAB V. KESIMPULAN DAN SARAN ... 49
A. Kesimpulan ... 49
B. Saran ... 49
DAFTAR PUSTAKA ... 50
LAMPIRAN ... 53
xiv
DAFTAR TABEL
Tabel I. Hasil pemeriksaan histopatologis hati pada tikus jantan hari
ke-28 ... 33
Tabel II. Hasil pemeriksaan histopatologis hati pada tikus betina hari
ke-28 ... 33
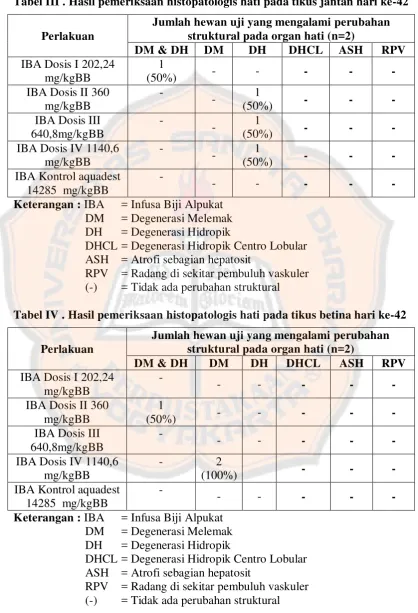
Tabel III. Hasil pemeriksaan histopatologis hati pada tikus jantan hari
ke-42 ... 39
Tabel IV. Hasil pemeriksaan histopatologis hati pada tikus betina hari
ke-42 ... 39
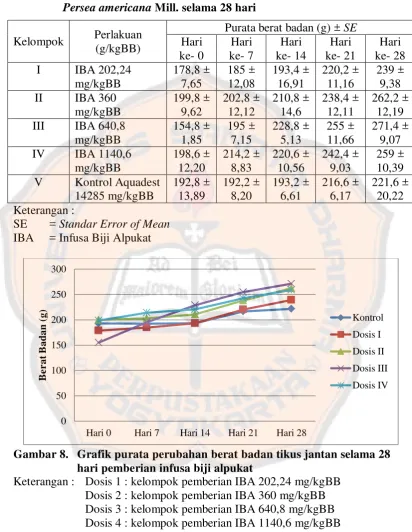
Tabel V. Purata berat badan ± SE tikus jantan akibat pemberian infusa biji
Persea americana Mill. selama 28 hari ... 42 Tabel VI. Purata berat badan ± SE tikus betina akibat pemberian infusa biji
xv
DAFTAR GAMBAR
Gambar 1. Buah Persea americana Mill. ... 7
Gambar 2. Hati dalam sistem pencernaan ... 12
Gambar 3. Hati tampak depan ... 13
Gambar 4. Struktur dasar lobulus hati ... 13
Gambar 5. Histopatologi hati ... 14
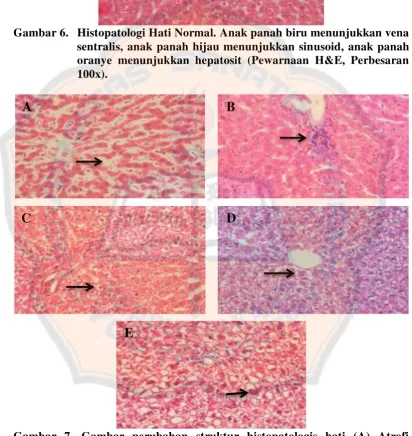
Gambar 6. Histopatologi hati normal ... 38
Gambar 7. Gambar perubahan struktur histopatologis hati ... 38
Gambar 8. Grafik perubahan berat badan tikus jantan selama 28 hari pemberian infusa biji alpukat ... 42
Gambar 9. Grafik perubahan berat badan tikus betina selama 28 hari pemberian infusa biji alpukat ... 43
Gambar 10. Grafik asupan pakan tikus jantan selama 28 hari pemberian infusa biji Persea americana Mill. ... 45
Gambar 11. Grafik asupan pakan tikus betina selama 28 hari pemberian infusa biji Persea americana Mill. ... 45
Gambar 12. Grafik asupan minum tikus jantan selama 28 hari pemberian infusa biji Persea americana Mill. ... 47
xvi
DAFTAR LAMPIRAN
Lampiran 1. Foto biji Persea americana Mill. ... 54
Lampiran 2. Foto serbuk biji Persea americana Mill. ... 54
Lampiran 3. Foto infusa biji Persea americana Mill. ... 54
Lampiran 4. Foto instrumen pembuatan infusa biji Persea americana Mill. ... 55
Lampiran 5. Hasil replikasi perhitungan kadar air serbuk biji Persea americana Mill. ... 55
Lampiran 6. Surat pengesahan determinasi biji Persea americana Mill. ... 56
Lampiran 7. Surat pengesahan Medical and Health Research Ethics Commitee (MHREC) ... 57
Lampiran 8. Surat Amandment ApprovalMedical and Health Research Ethics Commitee (MHREC) ... 58
Lampiran 9. Hasil histopatologi ... 59
Lampiran 10. Analisis statistik berat badan tikus jantan ... 61
xvii INTISARI
Tujuan penelitian ini untuk mengetahui efek toksik penggunaan biji
Persea americana Mill. pada pemberian subakut terhadap perubahan struktural histopatologis hati tikus galur Sprague Dawley dan mengetahui reversibilitas sifat efek toksik yang ditimbulkannya.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Lima puluh ekor tikus galur Sprague Dawley
(25 jantan dan 25 betina), umur 2-3 bulan, dibagi dalam 5 kelompok secara acak. Kelompok I-IV dipejankan infusa biji alpukat selama 28 hari secara peroral pada dosis 202,25 ; 360 ; 640,8 ; 1140,6 mg/kgBB, Kelompok V kontrol negative 14.285 mg/kgBB. Pada hari ke-29 sebanyak tiga tikus dari tiap dosis dikorbankan lalu dilakukan pembedahan untuk melihat histopatologis hati. Sisa hewan uji dipelihara tanpa diberi perlakuan selama 14 hari untuk melihat reversibilitas efek toksik yang ditimbulkan. Pada hari ke-15, tikus yang tersisa dikorbankan dan diambil organ hati untuk dilakukan pemeriksaan histopatologis. Perubahan struktural histopatologis hati yang diamati meliputi kejadian degenerasi dan nekrosis dari sel hati di sekitar vena porta dan vena sentralis. Pengamatan dilakukan di bawah mikroskop cahaya (Olympus PP 10®) di Laboratorium Patologi Fakultas Kedokteran Hewan UGM, Yogyakarta.
xviii ABSTRACT
The aim of this study is to determine the subacute toxic effects of the use of Persea americana Mill. seed infusion on structural changes of liver histopathologic in Sprague Dawley rats and to know reversibility of toxic effects caused.
This study is a pure experimental design with randomized design pattern. A total of 50 Sprague Dawley rats (25 males and 25 females), aged 2-3 months, were randomly divided into 5 groups. Group I-IV were administered avocado seed infusion during 28 days, orally at a dose of 202.25; 360; 640.8; 1140.6 mg/kg, Group V negative control 14.285 mg/kg. On day 29, three rats from each dose was sacrificed and then performed surgery to examine the liver histopathology. The rest of the test animals were reared without treated for 14 days to see the reversibility of toxic effects caused. On the 15th day, the remaining rats were sacrificed and the liver was taken for histopathological examination. Structural changes in liver histopathologic which is observed were the incidence of degeneration and necrosis of liver cells around the portal vein and central vein. Observations were carried out under a light microscope (Olympus PP 10®) at the Faculty of Veterinary Pathology UGM Laboratory, Yogyakarta.
Liver histopathologic analysis results showed that there are no subacute toxic effects of the use of Persea americana Mill. seed infusion on structural changes of liver histopathologic in Sprague Dawley rats. Reversibility of toxic effects of the use of Persea americana Mill. seed infusion can not be determined because there are no structural changes in liver histopathologic due to the usage of
Persea americana Mill. seeds infusion in Sprague Dawley rats.
1 BAB I PENGANTAR
A.Latar Belakang Penelitian
Di Indonesia ini, penggunaan obat tradisional sebagai terapi utama atau
alternatif telah menjadi trend saat ini. Munculnya trend penggunaan obat tradisional ini disebabkan karena obat tradisional memiliki harga yang murah,
mudah didapat dan adanya sugesti bahwa obat tradisional tidak memiliki efek
samping dan aman digunakan (Ozolua, Anaka, Okpo, Idogun, 2009).
Biji alpukat (Persea americana Mill.) merupakan salah satu obat tradisional yang telah diketahui sebelumnya melalui uji praklinik efek
farmakologinya memiliki fungsi sebagai antihipertensi dan penyakit
kardiovaskuler (Imafidon dan Amaechina, 2010), agen nefroprotektif (Yoseph,
2013), agen hepatoprotektif (Permatasari, 2013), dapat menurunkan kadar gula
darah (Alhassan, Sule, Atiku, Wudil, Abubakar, dan Mohammed, 2012), memiliki
aktivitas antimikroba (Idris, Ndukwe, dan Gimba, 2009), dan memiliki aktivitas
antiinflamasi dan meningkatkan sistem imun (Arukwe, Amadi, Duru, Agomuo,
Adindu, Odika, et al., 2012).
Secara farmakokinetika, setiap senyawa xenobiotika yang masuk ke
dalam tubuh akan mengalami proses absorbsi, distribusi, metabolisme, dan
eliminasi. Hati merupakan kelenjar terbesar dalam tubuh manusia dan memiliki
kapasitas yang tinggi untuk mengikat zat kimia (Baradero, Dayrit, dan Siswadi,
2008). Hati juga merupakan filter utama untuk mengeliminasi senyawa
terjadinya penumpukkan senyawa xenobiotika pada hati sehingga dapat
menimbulkan efek hepatotoksik. Salah satu wujud efek ketoksikan pada hati
adalah perubahan struktural, yakni seperti degenerasi melemak, nekrosis, dan
lain-lain (Gad, 2002), di mana telah diketahui meskipun hati berperan penting dalam
tubuh, organ hati rentan terhadap kerusakan dan penyakit diakibatkan sistem
sirkulasi darahnya yang tidak biasa (Wibowo dan Paryana, 2009).
Bahaya pemaparan suatu zat pada manusia dapat diketahui dengan
mempelajari efek kumulatif, dosis yang dapat menimbulkan efek toksik pada
manusia, dan lain-lain. Informasi tersebut dapat diperoleh dari uji toksisitas,
meliputi uji toksisitas akut, toksisitas subakut, dan lain-lain, tergantung dari tujuan
penggunaan suatu zat dan kemungkinan terjadinya risiko akibat pemaparan pada
manusia (Badan Pengawas Obat dan Makanan Republik Indonesia, 2014). Uji
toksisitas subakut merupakan salah satu contoh uji ketoksikan tak khas yang
dirancang untuk mengevaluasi keseluruhan spektrum efek toksik suatu senyawa
pada aneka ragam hewan uji (Donatus, 2005). Uji ini dapat memberikan
gambaran tentang toksisitas calon obat herbal terstandar pada penggunaan
berulang untuk jangka waktu yang relatif lama dan kecenderungan akumulasi dan
reversibilitas efek toksik calon obat herbal terstandar (Menteri Kesehatan
Republik Indonesia, 1992).
Penelitian ini merupakan penelitian paralel di mana pengamatan yang
dilakukan antara lain toksisitas akut, kadar BUN dan kreatinin, kadar SGPT dan
SGOT, kadar glukosa darah, histopatologis ginjal, histopatologis hati,
penelitian ini peneliti berpusat pada perubahan struktural histopatologis hati.
Penelitian ini penting dilakukan untuk memperoleh informasi efek toksik pada
penggunaan obat tradisional infusa biji Persea americana Mill. secara subakut terhadap perubahan struktural histopatologis hati tikus galur Sprague Dawley, serta untuk mengetahui efek kumulatif dan efek reversibilitas sifat efek toksik
yang ditimbulkan infusa biji Persea americana Mill. terhadap perubahan struktural hati.
Sedian infusa dipilih peneliti karena merupakan salah satu bentuk
sederhana dalam pembuatan obat tradisional yang sering digunakan oleh
masyarakat dan mudah dilakukan (Badan Pengawas obat dan Makanan Republik
Indonesia, 2010).
1. Perumusan masalah
Berdasarkan latar belakang di atas, dirumuskan permasalahan sebagai
berikut :
a. Apakah pemberian infusa biji Persea americana Mill. secara subakut memiliki efek toksik pada tikus Sprague Dawley yang dilihat dari wujud perubahan struktural histopatologis hati tikus?
2. Keaslian penelitian
Penelitian yang pernah dilakukan pada biji alpukat, yaitu:
a. “Chemical Composition of Persea americana Leaf, Fruit and Seed” yang
menyatakan bahwa biji Persea americana Mill. mengandung tanin, saponin, flavonoid, alkaloid, steroid, sianogenik glikosida dan fenol yang
memiliki aktivitas antiinflamasi, antioksidan serta meningkatkan sistem
imun (Arukwe, et al., 2012).
b. “Pengaruh Waktu Pemberian Infusa Biji Alpukat Persea Americana Mill Secara Akut sebagai Hepatoprotektif terhadap Aktifitas ALT-AST Serum
pada Tikus Terinduksi Karbon Tetraklorida” menyatakan bahwa
pemberian infusa biji Persea americana Mill. pada dosis 360,71 mg/kgBB dan dalam jangka waktu 4 jam setelah tikus terinduksi karbon tetraklorida
mampu memberikan efek hepatoprotektif (Permatasari, 2013).
c. “Efek Nefroproktetif Pemberian Jangka Panjang Infusa Biji Persea Americana Mill. terhadap Kadar Kreatinin dan Gambaran Histologi Ginjal
Tikus Terinduksi Karbon Tetraklorida” menyatakan bahwa variasi dosis
biji alpukat (Persea americana Mill.) 360,71 mg/kgBB; 642,06 mg/kgBB; 1142,86 mg/kgBB mampu memberikan efek nefroprotektif (Yoseph,
2013).
d. “Effects of Aqueous Seed Extract of Persea americana Mill. (Avocado) on
Blood Pressure and Lipid Profile in Hypertensive Rats” menyatakan
e. “Analisis Senyawa Metabolit Sekunder dan Uji Toksisitas Ekstrak Etanol
Biji alpukat (Persea americana Mill.)” menyatakan bahwa biji alpukat
(Persea americana Mill.) mengandung alkaloid, triterpenoid, tannin, flavonoid dan saponin serta Nilai LC50 biji alpukat biasa segar dan kering
yaitu masing-masing sebesar 42,270 mg/L, 36,078 mg/L, 36,924 mg/L dan
34,302 mg/L (Marlinda, Sangi, dan Wuntu, 2012).
f. “Acute and Sub-acute Americana Mill (Lauraceae) in Rats” penelitian ini
bertujuan untuk mengetahui keamanan serta ketoksisitasan ekstrak air
serbuk biji alpukat yang direndam selama 24 jam serta dibuat konsentrat
dengan rotari evaporator dan dikeringkan di oven pada suhu 300C selama 3 hari. Penelitian ini menyatakan bahwa LD50 tidak ditemukan pada uji
toksisitas akut sedangkan pada uji toksisitas subakut ditemukan kenaikan
jumlah minum pada tikus dan kenaikan total protein pada hematologi
darah (Ozulua, dkk., 2009) Perbedaan penelitian yang dilakukan Ozulua,
dkk. (2009) dengan penelitian yang akan dilakukan adalah cara pembuatan
infusa biji alpukat dan pengamatan yang dilakukan.
Dengan demikian, dapat dipastikan bahwa penelitian uji toksisitas
subakut infusa biji alpukat terhadap gambaran histopatologis hati tikus jantan
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat memberikan sumbangan
terhadap perkembangan ilmu pengetahuan khususnya pengetahuan
kefarmasian dalam memberikan kajian efek toksik subakut mengenai
penggunaan infusa biji alpukat (Persea americana Mill.).
b. Manfaat praktis. Penelitian ini diharapkan dapat memberikan informasi
tentang dosis yang menyebabkan toksisitas infusa biji alpukat (Persea americana Mill.) pada penggunaan subakut terhadap wujud perubahan struktural histopatologis dan reversibilitas sifat efek toksik hati.
B.Tujuan Penelitian 1. Tujuan umum
Penelitian ini bertujuan untuk mengetahui potensi ketoksikan dari
pengunaan infusa biji alpukat (Persea americana Mill.) secara subakut.
2. Tujuan khusus
a. Penelitian ini bertujuan untuk mengungkapkan ada tidaknya efek toksik
pada pemberian infusa biji Persea americana Mill. secara subakut yang diberikan pada tikus Sprague Dawley terhadap wujud perubahan struktural histopatologis hati tikus.
b. Penelitian ini bertujuan untuk mengevaluasi reversibilitas dari sifat efek
7 BAB II
PENELAAHAN PUSTAKA
A. Persea americana Mill. 1. Deskripsi tanaman
Gambar 1. Buah Persea americana Mill. (Plantamor, 2012)
Pohon Persea americana Mill. berukuran sedang hingga besar dengan tinggi ±10 m, batang berkayu, bulat, bercabang, berwarna coklat. Daun
tunggal, bulat telur, bertangkai, letak tersebar, ujung dan pangkal runcing,
berbulu, panjang 10-20 cm dan lebar 3-10 cm. Warna daun kemerahan ketika
masih muda dan ketika menua berwarna hijau tua dan teksturnya halus.
Bunganya majemuk, bentuk malai, berkelamin dua, tumbuh di ujung ranting,
benang sari duabelas, ruang kepala sari empat, berwarna putih kekuningan
dengan diameter 1-1,5 cm. Biji bulat, diameter 2,5-5cm, keping biji putih
kemerahan. Akar tunggang, bulat berwarna coklat (Napitupulu dan Wisaksono,
2008). Buahnya memiliki biji tunggal yang besar, berbentuk bulat hingga
lonjong (Gambar 1.) dan beratnya hingga 2,3 kg. Buah matang berwarna hijau,
hitam, ungu atau kemerahan tergantung dari varietasnya (World Agroforestry
2. Taksonomi biji alpukat
Kingdom : Plantae (Tumbuhan)
Subkingdom : Tracheobionta (Tumbuhan berpembuluh)
Super Divisi : Spermatophyta (Menghasilkan biji)
Divisi : Magnoliophyta (Tumbuhan berbunga)
Kelas : Magnoliopsida (berkeping dua / dikotil)
Sub Kelas : Magnoliidae
Ordo : Laurales
Famili : Lauraceae
Genus : Persea
Spesies : Persea americana Mill.
(Plantamor, 2012)
3. Kandungan kimia dan kegunaannya
Berdasarkan penelitian yang dilakukan Malangngi, Meiske, dan Jessy,
(2012), biji Persea americana Mill. memiliki kandungan kimia berupa tannin. Selain itu, biji Persea americana Mill. juga memiliki kandungan saponin, flavonoid, alkaloid, steroid, glikosida sianogen dan fenol (Arukwe, dkk., 2012).
Infusa biji alpukat dapat digunakan sebagai agen nefroprotektif pada
tikus terinduksi karbon tertraklorida (Yoseph, 2013). Infusa biji alpukat dapat
digunakan sebagai agen hepatoprotektif pada tikus terinduksi karbon
tertraklorida (Permatasari, 2013). Ekstrak etanol biji alpukat memiliki aktivitas
antioksidan yang mampu menangkap radikal bebas DPPH (Malangngi dkk.,
penyakit kardiovaskular (Imafidon dan Amaechina, 2011). Ekstrak air biji
alpukat juga memiliki efek hipoglikemik pada tikus diabetes yang terinduksi
aloksan (Alhassan, et al., 2012) dan memiliki aktivitas antimikroba (Idris dkk., 2009). Biji alpukat memiliki aktivitas antiinflamasi dan meningkatkan sistem
imun (Arukwe, et al., 2012).
B. Toksikologi
Toksikologi dapat didefinisikan sebagai cabang ilmu yang mempelajari
antaraksi berbahaya zat kimia atau senyawa asing terhadap sistem biologi
makhluk hidup (Donatus, 2005).
Kondisi efek toksik adalah keadaan atau faktor yang mempengaruhi
keefektifan absorpsi, distribusi, dan eliminasi zat beracun di dalam tubuh sehingga
menentukan keberadaan (kadar dan lama tinggal) senyawa atau metabolitnya di
tempat aksi dan keefektifan antaraksinya (mekanisme aksi). Keadaan ini
bergantung pada kondisi pemejanan dan kondisi makhluk hidup (Donatus, 2005).
Uji toksisitas adalah suatu uji untuk mendeteksi efek toksik suatu zat
pada sistem biologi dan untuk memperoleh data dosis-respon yang khas dari
sediaan uji. Data yang diperoleh dapat digunakan untuk memberi informasi
mengenai derajat bahaya sediaan uji tersebut bila terjadi pemaparan pada manusia,
sehingga dapat ditentukan dosis penggunaannya demi keamanan penggunaan pada
manusia (Badan Pengawas Obat dan Makanan Republik Indonesia, 2014).
Pada dasarnya, uji toksikologi dapat dibagi menjadi dua golongan, yakni
toksikologi yang dirancang untuk mengevaluasi keseluruhan atau spektrum efek
toksik suatu senyawa pada aneka ragam jenis hewan uji. Contoh uji ketoksikan
tak khas adalah uji ketoksikan akut, subkronis dan kronis. Uji ketoksikan khas
adalah uji toksikologi yang dirancang untuk mengevaluasi secara rinci efek yang
khas suatu senyawa pada aneka ragam jenis hewan uji. Contoh uji ketoksikan khas
adalah uji potensiasi, kekarsinogenikan, kemutagenikan, reproduksi, kulit, mata,
dan perilaku (Donatus, 2005).
C. Toksisitas Subakut
Toksisitas subakut merupakan salah satu jenis uji toksikologi. Uji
toksisitas subakut adalah uji ketoksikan suatu senyawa yang diberikan dengan
dosis berulang pada hewan uji tertentu, selama kurang dari 3 bulan (Gad, 2002).
Tujuan uji toksisitas subakut adalah untuk memperoleh informasi adanya efek
toksik zat yang tidak terdeteksi pada uji toksisitas akut; informasi kemungkinan
adanya efek toksik setelah pemaparan sediaan uji secara berulang dalam jangka
waktu tertentu; informasi dosis yang tidak menimbulkan efek toksik (No Observed Adverse Effect Level / NOAEL); dan mempelajari adanya efek kumulatif dan efek reversibilitas zat tersebut (Kepala Badan Pengawas Obar dan
Makanan Republik Indonesia, 2014).
Uji ini dapat memberikan gambaran tentang toksisitas calon obat herbal
terstandar pada penggunaan berulang untuk jangka waktu yang relatif lama.
terstandar juga dapat dinyatakan dari hasil uji toksisitas subakut (Menteri
Kesehatan Republik Indonesia, 1992).
Uji toksisitas subakut tidak difokuskan pada titik akhir tertentu,
melainkan untuk mengeksplorasi secara luas keseluruhan efek biologis yang
ditimbulkan pada tempat aksi yang diberikan pada rentang dosis tertentu. Uji
toksisitas subakut dapat menentukan toksisitas secara kualitatif (organ target dan
efek yang ditimbulkan) dan kuantitatif (perubahan struktural atau efek yang
ditimbulkan terhadap jaringan dan plasma darah) dari pemberian dosis berulang
pada hewan uji (Gad, 2002).
Sarana utama dalam mendeteksi respon toksisitas apabila tidak terdapat
kematian seperti organisme atau jaringan adalah:
1. Perubahan biokimia melibatkan efek pada enzim seperti inhibitor atau
perubahan jalur metabolik tertentu. Munculnya enzim atau substansi tertentu
dalam cairan tubuh menunjukkan kebocoran dari jaringan dan merupakan
indikasi perubahan patologis.
2. Perubahan status normal yakni perubahan berat badan, asupan makanan dan
minuman, output urin, dan berat organ merupakan indicator umum dan spesifik untuk toksisitas (Timbrell, 2008).
Reversibilitas (keterbalikan) toksisitas terjadi apabila efek yang tidak
diinginkan (efek toksik) dapat dikembalikan apabila perlakuan dihentikan.
Reversibilitas toksisitas bergantung pada sejumlah faktor, antara lain tingkat
pemaparan (waktu dan jumlah racun) dan kemampuan jaringan yang terkena
D. Hati
1. Anatomi hati
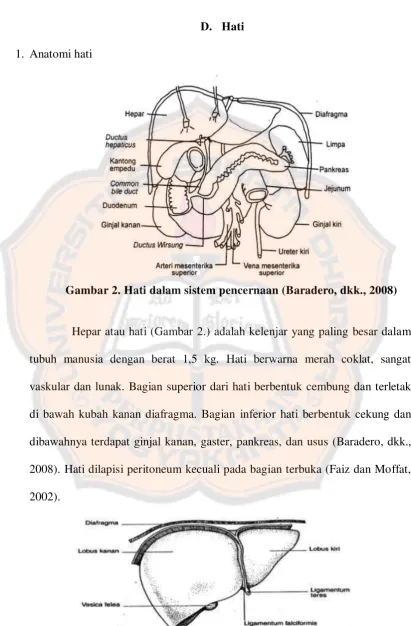
Gambar 2. Hati dalam sistem pencernaan (Baradero, dkk., 2008)
Hepar atau hati (Gambar 2.) adalah kelenjar yang paling besar dalam
tubuh manusia dengan berat 1,5 kg. Hati berwarna merah coklat, sangat
vaskular dan lunak. Bagian superior dari hati berbentuk cembung dan terletak
di bawah kubah kanan diafragma. Bagian inferior hati berbentuk cekung dan
dibawahnya terdapat ginjal kanan, gaster, pankreas, dan usus (Baradero, dkk.,
2008). Hati dilapisi peritoneum kecuali pada bagian terbuka (Faiz dan Moffat,
2002).
Hati (Gambar 3.) terdiri dari banyak unit fungsional yaitu lobulus.
Setiap lobulus terdiri dari sel-sel hati yang berbentuk segi enam atau
heksagonal. Hati dibagi menjadi dua lobus, yaitu lobus kiri dan kanan.
Ligamen falsiform membagi lobus kanan menjadi segmen anterior dan posterior serta membagi lobus kiri menjadi segmen medial dan lateral. Dari
hati, ligamen falsiform melintasi diafragma sampai ke dinding abdomen
anterior (Baradero, dkk., 2008).
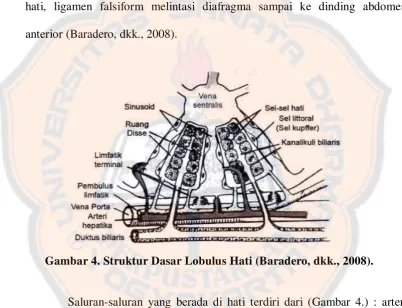
Gambar 4. Struktur Dasar Lobulus Hati (Baradero, dkk., 2008).
Saluran-saluran yang berada di hati terdiri dari (Gambar 4.) : arteri
hepatika yang berfungsi untuk menyuplai darah ke hati; vena porta hepatika
yang berfungsi untuk membawa darah dari vena ke seluruh traktus
gastrointestinal ke hati, darah yang dibawa ini mengandung zat-zat makanan
yang telah diserap oleh vili usus halus; vena sentralis berfungsi untuk
membawa darah vena dari hati ke vena inferior; saluran-saluran bilier juga
menyatu dan menyalurkan empedu yang dihasilkan oleh sel-sel hati (Baradero,
dkk., 2008).
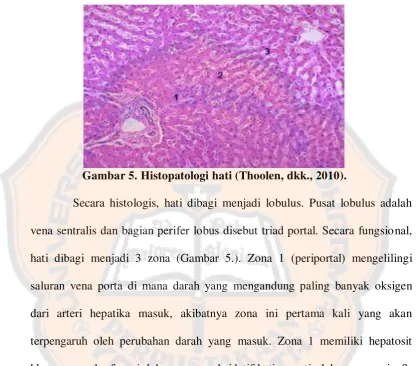
Gambar 5. Histopatologi hati (Thoolen, dkk., 2010).
Secara histologis, hati dibagi menjadi lobulus. Pusat lobulus adalah
vena sentralis dan bagian perifer lobus disebut triad portal. Secara fungsional,
hati dibagi menjadi 3 zona (Gambar 5.). Zona 1 (periportal) mengelilingi
saluran vena porta di mana darah yang mengandung paling banyak oksigen
dari arteri hepatika masuk, akibatnya zona ini pertama kali yang akan
terpengaruh oleh perubahan darah yang masuk. Zona 1 memiliki hepatosit
khusus yang berfungsi dalam proses oksidatif hati seperti glukoneogenesis, β
-oksidasi asam lemak, dan sintesis kolesterol. Zona 2 (transitional; midzonal)
merupakan zona sel yang memberikan respon kedua terhadap darah yang
masuk. Zona 3 (centro lobular) terletak disekitar vena sentralis, di mana zona
ini menerima darah yang sedikit mengandung oksigen, sehingga zona ini
paling rentan terhadap cidera iskemik. Hepatosit pada zona 3 berfungsi dalam
proses glikolisis, lipogenesis, dan detoksifikasi xenobiotika oleh sitokrom
Hati mempunyai struktur seragam yang terdiri dari kelompok sel-sel
yang dipersatukan oleh sinusoid (Gambar 4.). Sinusoid adalah saluran
pembuluh darah yang dilapisi oleh hepatosit. Di mana darah yang mengalir
melalui sinusoid akan diproses dan diolah oleh hepatosit serta sel Kupffer yang
bertugas untuk membersihkan darah dari patogen asing seperti bakteri sebelum
akhirnya bermuara keluar melalui vena sentralis (Barron, 2009). Sel-sel hepar
mendapat suplai darah dari vena porta hepatika yang kaya akan makanan, tidak
mengandung oksigen dan terkadang toksik, serta dari arteri hepatika yang
mengandung oksigen menuju vena sentralis, karena mempunyai sistem
peredaran darah yang tidak biasa ini, maka sel-sel hepar mendapat darah relatif
kurang oksigen. Keadaan ini menjelaskan mengapa hati lebih rentan terhadap
kerusakan dan penyakit (Wibowo dan Paryana, 2009).
2. Fisiologi hati
Fungsi hati bersangkutan dengan metabolisme tubuh, khususnya
mengenai pengaruhnya atas makanan dan darah. Hati merupakan pabrik kimia
terbesar dalam tubuh, dalam hal menjadi “perantara metabolisme”, artinya hati
mengubah zat makanan yang diabsorpsi dari usus dan disimpan, guna
dikeleluarkan sesuai pemakaiannya di dalam jaringan tubuh. Hati juga
berfungsi menghancurkan atau mengubah zat toksik menjadi senyawa yang
kurang berbahaya bagi tubuh (Pearce, 2009).
Beberapa fungsi penting lain hati yakni memproduksi empedu, yang
digunakan oleh usus kecil untuk mengahancurkan dan menyerap lemak,
dan melepaskan bilirubin, menghasilkan berbagai protein darah, seperti
protrombin dan fibrinogen, yang membantu dalam pembekuan darah (Gylys
dan Wedding, 2009).
E. Hepatotoksisitas
Hati merupakan organ yang luar biasa dalam mempertahankan fungsinya,
sehingga masih dapat mempertahankan fungsi normalnya meskipun hanya dengan
10-12% unit fungsional yang normal (Soeksmanto, 2008). Enzim-enzim yang
biasanya digunakan dalam mendiagnosis kerusakan hati adalah SGPT dan SGOT.
Keberadaan aktivitas SGPT dalam plasma menunjukkan bahwa adanya kerusakan
pada hati, sedangkan enzim GOT tersebar dalam sel-sel tubuh di mana terbanyak
dimiliki oleh otot jantungm kemudian hepar, otot tubuh, ginjal, dan pankreas. Bila
terjadi kerusakan pada membran sel hati maka kenaikan SGPT lebih menonjol.
Bila terjadi kerusakan organel sel hati maka kenaikan SGOT akan lebih menonjol.
Pada cidera sederhana yang meluas, kadar SGPT dan SGOT umumnya tidak
memperlihatkan peningkatan, sehingga produksi enzim GOT dan GPT tidak
bertambah (Carl, Edward, David, 2006).
Jenis-jenis kerusakan hati yang digunakan sebagai parameter perubahan
struktural histopatologis hati :
1. Nekrosis hati: kematian hepatosit, dapat bersifat fokal (sentral, pertengahan,
perifer) atau difus. Nekrosis hati merupakan suatu manifestasi toksik yang
berbahaya tetapi tidak kritis, karena hati memiliki kemampuan regenerasi
2. Sirosis hati: penyakit kronis pada hati dengan inflamasi dan fibrosis serta
hilangnya sebagian besar fungsi hati. Menurut Lu (2006), sirosis ditandai oleh
adanya septa kolagen, kumpulan hepatosit dan jaringan parut yang tersebat di
sebagian besar hati.
3. Degenerasi hidropik adalah degenerasi sel dalam bentuk hidropik adalah
adanya akumulasi cairan pada sitoplasma sel yang terlihat seperti vakuola.
Secara mikroskopis terlihat bahwa sel mengandung ruang-ruang jernih yang
mengelilingi hati Cheville (2006). Degenerasi hisropik merupakan perubahan
struktural akut yang bersifat reversibel yang dihasilkan sebagai respon
terhadap cidera yang tidak mematikan. Degenerasi hidropik merupakan
akumulasi air pada intrasitoplasma yang disebabkan karena ketidakmampuan
sel untuk mempertahankan homeostasis ion dan cairan sehingga
menyebabkan gangguan integritas sel membran. Jika terjadi pada organ hati
biasanya disebabkan oleh hepatitis atau hipoksia (Danciu, Mihailovici, Dima,
Cucu, 2014).
4. Steatosis (perlemakan/degenerasi lemak): adanya penimbunan trigliserida di
hepatosit yang bersifat reversible (Corwin, 2009). Degenerasi melemak
adalah munculnya droplet lemak dalam sitoplasma sel tanpa perubahan
nukleus. Degenerasi melemak muncul akibat ketidakmampuan hati untuk
F. Infundasi
Infusa adalah sediaan cair yang dibuat dengan cara mengekstraksi
simplisia nabati dengan air pada suhu 900C selama 15 menit. Pembuatan infusa merupakan cara yang paling sederhana untuk membuat sediaan herbal dan dapat
diminum panas atau dingin. Cara pembuatan infusa adalah dengan mencampur
simplisia dengan derajat halus yang sesuai dalam panci dengan air secukupnya,
panaskan ditangas air selama 15 menit terhitung mulai suhu mencapai 900C sambil sekali-sekali diaduk. Penyarian dilakukan menggunakan kain flanel dengan
penambahan air panas secukupnya melalui ampas hingga diperoleh volume infusa
yang diinginkan (Badan Pengawas obat dan Makanan Republik Indonesia, 2010).
G. Keterangan Empiris
Penelitian ini merupakan penelitian eksploratif untuk mendapatkan bukti
adanya tidaknya efek toksik subakut dari infusa biji alpukat terhadap perubahan
19 BAB III
METODE PENELITIAN
A. Jenis Dan Rancangan Penelitian
Penelitian toksisitas subakut infusa biji Persea americana Mill.terhadap gambaran hispatologis hati tikus Sprague Dawley ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Penelitian
menggunakan hewan uji ini telah mendapatkan ethical clearance dari Komisi Etik Fakultas Kedokteran Universitas Gajah Mada (Lampiran 7 dan 8).
B. Variabel Dan Definisi Operasional 1. Variabel utama
a. Variabel bebas. Variabel bebas dalam penelitian ini adalah variasi dosis
pemberian infusa biji Persea americana Mill.
b. Variabel tergantung. Variabel tergantung penelitian ini adalah wujud
perubahan struktural histopatologis hati tikus galur Sprague Dawley.
2. Variabel pengacau
a. Variabel pengacau terkendali. Variabel pengacau terkendali dalam
penelitian ini adalah, kondisi hewan uji, yaitu tikus galur Sprague Dawley,
jenis kelamin jantan dan betina, berat badan 150-250 g, dan umur 2-3 bulan
diperoleh dari Laboratorium Hayati Imono, Fakultas Farmasi, Universitas
Sanata Dharma, Yogyakarta. Selain itu variabel pengacau juga dari bahan
mempunyai waktu panen, waktu tumbuh dan panen yang sama. Frekuensi
pemberian infusa biji Persea americana Mill. secara per oral satu kali sehari selama dua puluh delapan hari berturut-turut dengan waktu pemberian yang
sama di mana bahan uji berupa biji Persea americana Mill. diperoleh dari Depot Es Teller 77, Galeria Mall, Yogyakarta yang diambil pada bulan Juni
2014.
b. Variabel Pengacau tak terkendali. Variabel pengacau tak terkendali dalam
penelitian ini adalah keadaan patologis tikus jantan dan betina galur
Sprague Dawley yang digunakan.
3. Definisi operasional
a. Biji Persea americana Mill. Biji Persea americana Mill. yang digunakan adalah biji alpukat segar dan tidak busuk.
b. Infusa biji Persea americana Mill. Infusa didapatkan dengan cara menginfudasi 8 g serbuk kering biji Persea americana Mill. ke dalam 100,0 ml air pada suhu 900C selama 15 menit sehingga diperoleh konsentrasi infusa biji P. americana Mill. 8% b/v.
c. Dosis infusa biji P. americana Mill. Dosis yang diberikan kepada hewan uji yakni : Dosis I = 202,24 mg/kgBB, Dosis II = 360 mg/kgBB, Dosis III
=640,8 mg/kgBB dan Dosis IV = 1140,6 mg/kgBB.
d. Parameter efek toksisitas subakut. Parameter efek toksisitas subakut pada
organ hati ditunjukkan dengan adanya perbedaan gambaran histopatologis
e. Perubahan struktural histopatologis hati. Perubahan histopatologis hati
merupakan gambaran perubahan struktural histopatologis kelompok
perlakuan yang dibandingkan terhadap kelompok kontrol negatif.
f. Sifat efek toksik. Sifat efek toksik yang mungkin muncul adalah reversible
atau irreversible pada organ hati.
g. Uji toksisitas subakut. Uji toksisitas subakut adalah uji ketoksikan infusa
biji Persea americana Mill. secara per oral satu kali sehari selama dua puluh delapan hari berturut-turut pada waktu yang sama.
C. Bahan Penelitian
Bahan penelitian yang digunakan dalam penelitian ini adalah sebagai
berikut :
a. Biji Persea americana Mill. yang diperoleh dari Depot Es Teller 77, Galeria Mall, Yogyakarta, pada bulan Juni 2014.
b. Hewan uji yang digunakan, yaitu tikus galur Sprague Dawley, umur 2-3 bulan, berat badan 150-250 g yang diperoleh dari Laboratorium Imono, Fakultas
Farmasi, Universitas Sanata Dharma, Yogyakarta.
c. Aquadest yang digunakan sebagai pelarut infusa dan larutan kontrol negatif
hewan uji, diperoleh dari Laboratorium Farmakognosi-Fitokimia, Fakultas
Farmasi, Universitas Sanata Dharma, Yogyakarta.
d. Moisture Balanced, alat penetapan kadar air serbuk biji Persea americana
Mill. yang berasal dari Laboratorium Kimia Analisis, Fakultas Farmasi,
e. Pellet AD-2, asupan pakan hewan uji dan air reverse osmose, asupan minum hewan uji yang diperoleh dari Laboratorium Imono, Fakultas Farmasi,
Universitas Sanata Dharma, Yogyakarta.
f. Bahan pemeriksaan histologis adalah formalin 10% yang dibuat dengan
mengencerkan formalin 30% dengan aquadest sesuai volume yang telah
dihitung menggunakan rumus pengenceran. Formalin 30% diperoleh dari
Laboratorium Kimia Analisis, Fakultas Farmasi, Sanata Dharma, Yogyakarta.
D. Alat Atau Instrumen Penelitian
1. Alat pembuatan simplisia : timbangan digital, oven, blender, ayakan no.40, wadah untuk menyimpan serbuk biji alpukat.
2. Alat penetapan kadar air : Moisture balanced dan sendok.
3. Alat pembuatan infusa biji Persea americana Mill. : panci enamel, termometer,
stopwatch, bekker glass, gelas ukur, cawan porselen, batang pengaduk, corong, labu alas bulat, penangas air, timbangan analitik, kain flannel.
4. Alat uji perlakuan dan pemeriksaan histopatologis : kandang metabolik
(metabolic cage) tikus, jarum suntik per oral, spuit injeksi, timbangan, seperangkat alat bedah, pipa kapiler (haematokrit), eppendorf alat-alat gelas
E.Tata Cara Penelitian 1. Determinasi serbuk biji Persea americana Mill
Determinasi serbuk biji Persea americana Mill. dilakukan di Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta.
2. Pengumpulan bahan
Bahan uji yang digunakan adalah biji Persea americana Mill. yang diperoleh dari Penjual dari Depot Es Teller 77, Galeria Mall, Yogyakarta pada
bulan Juni 2014.
3. Pembuatan serbuk
Biji Persea americana Mill. dibersihkan dari kulit luarnya lalu dicuci dengan air mengalir kemudian dipotong tipis, lalu dikeringanginkan hingga biji
tidak tampak basah kemudian dilakukan pengeringan menggunakan oven pada
suhu 50˚C selama 72 jam. Potongan biji yang sudah kering kemudian diserbuk
dan diayak dengan ayakan no. 40 agar kandungan fitokimia yang terkandung
lebih mudah terekstrak karena luas permukaan serbuk yang berkontak dengan
pelarut semakin besar (Lampiran 3.).
4. Penetapan kadar air serbuk biji Persea americana Mill.
5. Pembuatan infusa biji Persea americana Mill.
Serbuk biji Persea americana Mill.yang kering ditimbang sebanyak 8 g. Kemudian serbuk kering tersebut dibasahi aquadest dengan 2
kali bobot serbuk. Lalu dimasukkan ke dalam 100,0 ml pelarut aquadest,
sehingga total aquadest yang digunakan adalah 116,0 ml. Campuran tersebut
diinfudasi pada suhu 900C selama 15 menit, waktu 15 menit dihitung ketika suhu campuran mencapai 900C. Setelah 15 menit, campuran tersebut diambil dan diperas menggunakan kain flannel lalu dimasukkan ke dalam labu ukur.
Apabila infusa yang didapatkan belum tepat 100,0 ml maka ditambahkan
dengan air panas melalui flannel tersebut kembali (Lampiran 4.).
6. Penetapan dosis infusa biji Persea Americana Mill.
Peringkat dosis infusa biji alpukat didasarkan pada pengobatan yang
biasa digunakan oleh masyarakat yaitu ± 2 sendok makan (4 g) serbuk yang
direbus dengan 250 ml air. Maka dosis perlakuan yang digunakan adalah
4g/70kgBB manusia. Berdasarkan data di atas maka konversi dosis manusia 70
kg ke tikus 200 g = 0,018
Dosis untuk tikus 200 g = 0,018 x 4 g – 0,72 g/200 g BB = 360 mg/kgBB
Berdasarkan hasil orientasi infusa penelitian yang dilakukan oleh
Yoseph (2013), konsentrasi maksimal infusa biji alpukat yang dapat dibuat
adalah 8g/100ml dengan asumsi berat badan hewan uji maksimal adalah 350 g
Maka dilakukan perhitungan untuk menetukan dosis tinggi perlakuan
dengan rumus : D x BB = C X V
D x 350 g = 8 g/100ml x 5 ml
D = 1142,8 mg/kgBB
Kemudian dihitung faktor kelipatan dari dosis rendah dan dosis tinggi
untuk menentukan peringkat dosis infusa biji Persea americana Mill. dilakukan perhitungan sebagai berikut:
√
= √
(Faktor Kelipatan)
Berdasarkan faktor kelipatan yang maka diperoleh 4 peringkat dosis yaitu:
Dosis I : 360 mg/kgBB : 1,78 = 202,24 mg/kgBB
Dosis II : 360 mg/kgBB
Dosis III : 360 mg/kgBB x 1,78 = 640,8 mg/kgBB
Dosis IV : 640,8 mg/kgBB x 1,78 = 1140,6 mg/kgBB
7. Penetapan dosis kontrol negatif (aquadest)
Berdasarkan perhitungan di atas diasumsikan berat badan hewan uji
maksimal adalah 350 g dan volume maksimal pemberian infusa secara p.o = 5 ml.
Menurut Jendral Pengawasan Obat dan Makanan (1995) konsentrasi aquadest
sebesar 0,998 g/ml yang dibulatkan menjadi 1g/ml maka didapatkan dosis kontrol
negatif (aquadest), yakni :
D x BB = C x V
D x 350 g = 1 g/ ml x 5 ml
D =
D =
D = 14285 mg/kgBB
Maka dosis aquadest adalah 14285 mg/kgBB
8. Penyiapan hewan uji
Hewan uji tikus yang digunakan berjumlah 50 ekor (25 ekor jantan
dan 25 ekor betina) dari galur Sprague Dawley dengan umur 2-3 bulan dan berat badan 150-250 g. Hewan uji ditempatkan dalam metabolic cage secara acak. Sebelum perlakuan hewan uji diadaptasikan dengan lingkungan selama 3
hari. Penelitian dengan hewan coba telah mendapat ethical clearance dari Komisi Etik Fakultas Kedokteran Universitas Gajah Mada (Lampiran 7 dan 8.).
9. Pengelompokkan dan perlakuan hewan uji
Penelitian ini menggunakan 50 ekor tikus yakni 25 ekor tikus jantan
dan 25 ekor tikus betina yang masing-masing dibagi secara acak ke dalam lima
kelompok di mana setiap kelompok akan berisi 5 ekor tikus. Kelompok I
sampai IV diberi perlakuan infusa biji alpukat dengan peringkat dosis
berturut-turut 202,24 ; 360 ; 640,8 ; 1140,6 mg/kgBB. Kelompok V adalah tikus yang
diberikan aquadest sebagai kontrol negatif. Pemberian infusa biji Persea americana Mill. dilakukan satu kali sehari selama dua puluh delapan hari berturut-turut secara peroral.
10. Prosedur pelaksanaan penelitian
Uji toksisitas subakut dilakukan dengan cara pemberian infusa biji
sebanyak 3 ekor hewan uji dari tiap kelompok dilakukan pembedahan baik
jantan maupun betina. Sementara hewan uji yang tersisa yakni sebanyak 2 ekor
dipelihara tanpa diberi perlakuan infusa biji Persea americana Mill., selama 14 hari untuk melihat sifat efek toksik reversible atau irreversible, lalu pada hari ke-15 hewan uji dilakukan pembedahan.
11. Prosedur pemusnahan hewan uji
Sebelum pembedahan, hewan uji dikorbankan dengan cara anastetika
overdosis yakni memasukkan tikus kedalam wadah tertutup berisi eter yang
akan diinhalasi oleh tikus. Setelah dibedah, organ yang diinginkan diambil
menggunakan pinset dan gunting bedah, kemudian organ dicuci dengan larutan
NaCl 0,9% dan dimasukkan kedalam pot formalin 10% untuk diawetkan.
Hewan uji yang telah diambil organnya kemudian dikubur.
12. Pengamatan
a. Penimbangan berat badan hewan uji
Data penimbangan berat badan hewan uji dihitung purata
perubahan berat badan tiap kelompok hewan uji pada hari ke-0, 7, 14, 21
dan 28. Data perubahan berat badan hewan uji antar minggu dan
kelompok perlakuan dianalisis secara statistik dengan menggunakan
General Linier Model (Multivariate).
b. Pengukuran asupan pakan dan minum hewan uji
Hewan uji asupan 30 g setiap harinya dan asupan minum 100 ml
setiap harinya. Pengukuran dilakukan dengan cara menimbang sisa pakan
pertama dan kedua dihitung sebagai asupan pakan yang dikonsumsi pada
hari pertama, metode yang sama juga dilakukan pada pengukuran asupan
minum setiap harinya selama 28 hari perlakuan.
13. Pembuatan preparat dan pemeriksaan histopatologis
Organ yang telah disimpan dalam larutan formalin 10% dilakukan
trimming yakni pemotongan tipis jaringan setebal ±4mm dengan orientasi
sesuai dengan organ yang akan dipotong. Potongan jaringan kemudian
dimasukkan dalam embeding cassete lalu dilanjutkan dengan proses dehidrasi menggunakan tissue processor untuk mengeluarkan kandungan air dalam jaringan organ. Proses dehidrasi ini menggunakan cairan dehidran, seperti
etanol atau isopropil alkohol. Cairan dehidran kemudian dibersihkan dari
jaringan menggunakan reagen pembersih, yaitu xilol selama 1 jam, yang
kemudian diganti dengan parafin dengan metode penetrasi ke dalam jaringan
selama 2 jam. Setelah melalui proses dehidrasi, jaringan yang berada dalam
embeding cassete dipindahkan ke base mold yang berisi parafin cair. Jaringan kemudian dipotong menggunakan mikrotom, lalu dilakukan pewarnaan
menggunakan hematoksilin-eosin. Setelah jaringan pada preparat diwarnai,
kaca preparat ditutup dengan cover glass (Carson, 1990). Preparat yang sudah dibuat, dilakukan pembacaan dan pengamatan untuk mendiagnosis gambaran
histopatologis organ hati. Prosedur ini dilakukan oleh pihak Laboratorium
Patologi Klinik Fakultas Kedokteran Hewan, Universitas Gadjah Mada,
F. Tata Cara Analisis Hasil 1. Pemeriksaan histopatologis organ
Data pemeriksaan histopatologis organ dianalisis secara kualitatif
dengan menggunakan mikroskop cahaya (Olympus dp 10) berdasarkan
perubahan struktural yang terjadi dibandingkan dengan kelompok kontrol
negatif. Data ini digunakan untuk melihat hubungan antara dosis dan spektrum
efek toksik.
2. Uji reversibilitas
Data uji reversibilitas dianalisis secara kualitatif berdasarkan
perubahan struktural yang terjadi pada kelompok tikus yang diberhentikan dari
pemberian infusa biji alpukat dibandingkan dengan kelompok kontrol negatif.
3. Pengamatan berat badan hewan uji
Data penimbangan berat badan hewan uji dihitung purata perubahan
berat badan tiap kelompok hewan uji pada hari ke-0, 7, 14, 21 dan 28. Data
perubahan berat badan hewan uji antar minggu dan kelompok perlakuan
dianalisis secara statistik dengan analisis General Linier Model (Multivariate). 4. Pengukuran asupan pakan dan minum hewan uji
Data asupan pakan dan minum dianalisis dengan cara menghitung
purata makanan dan minuman yang dihabiskan tiap kelompok hewan uji setiap
G. Alur Penelitian
50 ekor tikus yakni 25 jantan dan 25 betina masing-masing dibagi kedalam 5 kelompok
Kel.
Selama 28 hari injeksi infusa biji alpukat secara peroral pada hewan uji dilakukan pada jam yang sama dengan hari pertama
Kemudian 2 hewan uji sisanya dipelihara tanpa perlakuan selama 14 hari untuk uji reversibilitas, pada hari ke-15
diakukan pembedahan dan pengamatan histopatologis Kel.
Hewan uji ditempatkan dalam metabolic cage secara acak dan diadaptasikan selama 3 hari sebelum memulai perlakuan
Hari I hewan uji diberikan
infusa biji Persea americana Mill. secara peroral
Hewan uji dikembalikan dalam metabolic cage dan diberi asupan pakan
31 BAB IV
HASIL DAN PEMBAHASAN
Penelitian toksisitas subakut ini bertujuan untuk membuktikan ada
tidaknya potensi efek toksik dari infusa biji Persea americana Mill. terhadap histopatologis hati tikus Sprague Dawley serta mengungkapkan sifat efek toksik senyawa bersifat reversibel atau tidak.
A. Determinasi Tanaman
Tujuan dari determinasi serbuk biji Persea americana Mill. ini adalah untuk membuktikan bahwa serbuk biji yang digunakan dalam penelitian benar
berasal dari tanaman Persea americana Mill. Determinasi dilakukan dengan cara mencocokan ciri-ciri morfologi dari biji Persea americana Mill. dengan biji
Persea americana Mill. yang telah diketahui pasti merupakan biji tanaman Persea americana Mill.. Determinasi ini dilakukan oleh Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta. Hasil determinasi membuktikan bahwa biji yang
digunakan benar berasal dari tanaman Persea americana Mill. (Lampiran 6.)
B. Penetapan Kadar Air Serbuk Biji Persea americana Mill.
Sebelum digunakan untuk penelitian, serbuk biji Persea americana Mill. terlebih dahulu dilakukan penetapan kadar air yang bertujuan untuk mengetahui
kandungan air dalam serbuk biji tersebut memenuhi persyaratan kadar air serbuk
dan Makanan RI (1995), syarat kadar air yang baik adalah kurang dari 10%,
dikarenakan simplisia yang memiliki kadar air lebih dari 10% memungkinkan
tumbuhnya mikroorganisme yang nantinya akan menjadi kontaminan yang dapat
mengganggu hasil penelitian.
Penetapan kadar air ini dilakukan dengan menggunakan alat Moisture Balanced. Prinsip penetapan kadar air pada alat Moisture Balanced ini adalah penetapan jumlah sampel berdasarkan pengukuran berat zat konstan (Sujadi,
2010). Sebanyak 5g serbuk biji Persea americana Mill. dipanaskan di dalam alat pada suhu 105˚C selama 15 menit. Hasil rata-rata kadar air yang diperoleh yaitu
5,63% (Lampiran 5.) sehingga diketahui bahwa serbuk biji Persea americana
Mill. yang digunakan telah memenuhi syarat kadar air simplisia yang baik yaitu
kurang dari 10%.
C. Gambaran Histopatologis Hati Tikus Sprague Dawley yang Diberi Infusa Biji Persea americana Mill.
Tujuan dari penelitian ini adalah untuk mengungkapkan ada tidaknya
efek toksik pada pemberian infusa biji Persea americana Mill. secara subakut (selama 28 hari) yang diberikan pada tikus Sprague Dawley terhadap gambaran histopatologis hati tikus, oleh karena itu pada hari ke-28 dibuat preparat dari 3
ekor tikus jantan dan betina dari masing-masing kelompok perlakuan dan kontrol
aquadest. Selain itu, untuk mengetahui sifat efek toksik bersifat reversible atau
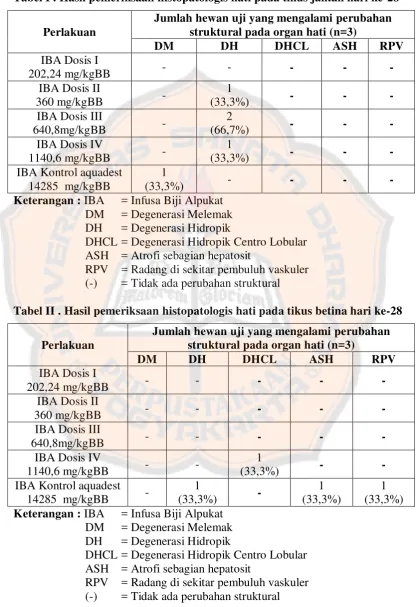
Tabel I . Hasil pemeriksaan histopatologis hati pada tikus jantan hari ke-28
Perlakuan
Jumlah hewan uji yang mengalami perubahan struktural pada organ hati (n=3)
DM DH DHCL ASH RPV
Keterangan : IBA = Infusa Biji Alpukat DM = Degenerasi Melemak DH = Degenerasi Hidropik
DHCL = Degenerasi Hidropik Centro Lobular ASH = Atrofi sebagian hepatosit
RPV = Radang di sekitar pembuluh vaskuler (-) = Tidak ada perubahan struktural
Tabel II . Hasil pemeriksaan histopatologis hati pada tikus betina hari ke-28
Perlakuan
Jumlah hewan uji yang mengalami perubahan struktural pada organ hati (n=3)
DM DH DHCL ASH RPV
Keterangan : IBA = Infusa Biji Alpukat DM = Degenerasi Melemak DH = Degenerasi Hidropik
DHCL = Degenerasi Hidropik Centro Lobular ASH = Atrofi sebagian hepatosit
Gambar 6. Histopatologi Hati Normal. Anak panah biru menunjukkan vena sentralis, anak panah hijau menunjukkan sinusoid, anak panah oranye menunjukkan hepatosit (Pewarnaan H&E, Perbesaran 100x).
Gambar 7. Gambar perubahan struktur histopatologis hati (A) Atrofi sebagian hepatosit pada tikus betina kelompok kontrol aquadest, (B) Radang di sekitar pembuluh vaskuler pada tikus betina kelompok kontrol aquadest, (C) Degenerasi Hidropik pada tikus jantan kelompok dosis 640,8 mg/kgBB, (D) Degenerasi Hidropik Centro Lobular tikus betina kelompok dosis 1140,6 mg/kgBB, (E) Degenerasi Melemak pada tikus jantan kelompok kontrol aquadest, (Pewarnaan H&E, Perbesaran 400 x).
A
B
C
D
Berdasarkan Tabel I dan II. di atas dapat dilihat bahwa tidak terjadi
perubahan struktural histopatologis hati (Gambar 6.) pada tikus jantan dosis
202,24 mg/kgBB, tikus betina dosis I 202,24 mg/kgBB, dosis II 360 mg/kgBB,
dan dosis III 640,8 mg/kgBB, namun sebagian tikus baik jantan dan betina baik
pada kelompok pemberian infusa biji Persea americana Mill. maupun kelompok kontrol aquadest menunjukkan beberapa perubahan struktural pada histopatologis
hati, di mana berdasarkan urutan keparahannya, yaitu, pertama adalah atrofi
sebagian hepatosit, kedua adalah radang di sekitar pembuluh vaskular, ketiga
adalah degenerasi hidropik, degenerasi hidropik centro lobular, dan degenerasi
melemak yang memiliki tingkat keparahan perubahan struktural yang sama.
Atrofi sebagian hepatosit ditandai dengan penyusutan sel-sel hepatosit
dan pelebaran sinusoid yang disebabkan oleh mengecilnya sel atau berkurangnya
jumlah sel. Kondisi ini terjadi dikarenakan lingkungan sel atau asupan sel yang
tidak memadai sehingga sel tersebut perlu mengecil sampai ke tingkat di mana sel
dapat melangsungkan kehidupannya. Perubahan struktural ini hanya merupakan
homeostatis adaptif yang bersifat reversibel jika penyebabnya dapat dieliminasi
atau diperbaiki (Donatus,2005). Penyebab dari atrofi dapat disebabkan oleh
banyak faktor, antara lain karena berkurangnya aktivitas, fisiologis/proses
metabolik normal dalam tubuh misal saat infant berubah menjadi dewasa akan
membuat menghilangnya timus, pasokan darah yang kurang/anemia, nutrisi yang
tidak adekuat, luka pada sistem saraf, hilangnya stimulasi endokrin, kondisi
patologis hewan uji dan penuaan (Kumar, Cotran, Robbins, 2007). Atrofi sebagian
hari (Tabel II.), sehingga dapat diketahui bahwa atrofi sebagian hepatosit yang
terjadi tidak diakibatkan dari pemberian infusa biji Persea americana Mill.. Radang di sekitar pembuluh vaskuler ditandai dengan munculnya
neutrofil dan limfosit di sekitar pembuluh darah vena porta. Inflamasi merupakan
respon luka ekstra sel yang muncul sebagai mekanisme pertahanan diri dan respon
terhadap xenobiotika agar sel yang cidera dapat diperbaiki (Donatus, 2005).
Radang di sekitar pembuluh vaskular (Gambar 7.) ini terjadi pada tikus betina
kontrol aquadest perlakuan 28 hari (Tabel II.), sehingga dapat diketahui bahwa
radang di sekitar pembuluh vaskuler yang terjadi tidak diakibatkan dari pemberian
infusa biji Persea americana Mill..
Hati merupakan organ yang mampu memperbaiki dan melindungi dirinya
sendiri, tergantung pada keparahan cidera yang terjadi padanya dan kemampuan
beregenerasi hati itu sendiri (Gupta, 2007). Degenerasi hidropik merupakan
manifestasi pertama yang muncul pada hampir semua jenis cidera sel. Degenerasi
hidropik merupakan perubahan struktural akut yang bersifat reversibel (Kumar,
Abbas, Aster, 2015). Degenerasi hidropik ditandai dengan pelebaran vakuola
berbatas tidak jelas pada sel epitel kuboid di sitoplasma (Gambar 7.). Degenerasi
ini terjadi akibat adanya gangguan oksidasi pada sel hati (kerusakan mitokondria,
penghentian produksi ATP, kegagalan pompa natrium), sehingga meningkatkan
tekanan osmotik dan menyebabkan sel tidak dapat mengeliminasi air dan air
tertimbun di dalam sel, sehingga terjadi pembengkakan (Donatus, 2005).
Degenerasi hidropik dapat disebabkan oleh beberapa faktor, antara lain trauma