KINETIKA REAKSI PEMBUATAN KALSIUM KARBONAT
DARI LIMBAH MARMER DENGAN
NA TRIUM KARBONAT
Retno Dewati
Jurusan Teknik Kimia Fakultas Teknologi Industri UPN "Veteran" Jawa Timur JI. Raya Rungkut Madya - Gunung Anyar - Surabaya
Email: dewati.r@gmail.com
a「Nセエイ。ォ@
Penelitian ini dilakllkan dengan tlljllan mempelajari killetika reaksi pembuatan kalsium
karhonat (CoCo) dengan proses soda dengan jalan menentllkan tingkat reaksi kimia (orde reaksi)
sel'la menentllkan lajll reaksi kimia dan mempelajari pengart/h peuhah-pellhah proses, $111m dOli waktu proses. AlaI ulnma pada pelle/ilion ini adalah labu /eher liga yang dilenglulpi magnetic slirrer. Lart/lan StlSU ka/wr direaksikan dengan lart/lan soda ash dalam labu leher liga, kemtldian diaduk del/gan kecepalall konstall. Adaplln petlha}mya adalah suml reaks; 60"C, 7ffe, 80"C, I OffC, dan waklll reaksi 50, 60, 70,80, 90 (menU). Diperoleh CaC03 lerbesar yaitu pada suhu60°C dan waklll 90 menil, dengan kOl1slanla kecepatan reaksi 0,458 menir', harga ellergi pengaklijannya sehesar 193, -199 cal/mol dan konversi lerlillggi dicapai sebesar 36,9%. Reaksi 101'111011 Co (OH)2 dan lam Ian Na;zCO,? berlangsllng pada orde satll.
Kata kline; : Kinelika reaksi, proses soda, susu kapllr
Abstract
The aim of Ihis research was to stlldy the reaction kinetics of calcium carbonate (CaCY)))
preparation by soda process by means determinc the chemical reaction order (reaction order) and determilling the chemical reactioll rate and study the effect of process variables, temperatllre process time. The major eqllipmellf in this research was a three-neck pask equ.pped with magnetic stirrer. Lime sO/lltioll was reacted with soda ash solution in the three-neck flask then they were stirred hy constant rale. While the variables lYere the reaction temperature of 60°C, 70°C, 80°C, 100°C,and the reactioll time of 50, 60, 70, 8e, 90 (ill minutes). It was obtained Ihe largesl CaCO; namely at 60°C and in the lime period of 90 mim/les, with reaction rale constanl of 0.458 minule-', its aclivation energy value was qf 193.499 callmol and the highest conversion was achieved as large as 36.9%.
Reactioll
(i
Ca(OH) 2 and Na2CO; done look place ill order one.Keywords: Reaction kinetics, soda process, lime stone
PENDAHULUAN
Indonesia dikenal dengan kekayaan alamnya yang berlimpah ruah, baik itu dapat diperbarui· ataupun yang tidak dapat diperbarui,tetavi yang perlu disayangkan adalah pemanfaatan kekayaan aJam yang teratur, terarah dan dengan memperhatikan masalah lingkungan.
Diantara kekayaan alam itu adalah batuan marmer yanJ banyak dijumpai di beberapa tempat di Indonesia, seperti di daerah Tulungagung, Trenggalek, Ujung pan
-dang, Bandung dan kota-kota lainnya. Batuan marmer setelah mengalami proses-proses tertentu hasilnya dapat digunakan sebagai ubin lantai untuk keperluan arsitektur dan untuk hiasan rumah tangga serta kerajinan. Limbah darj batuan marmeT dapat dimanfaatkan menjadi hahan kimia, salah satunya adaJah kalsium karbonat.
dan sejalan dengan perkembangan kebudayaan umat. Sejalan pula dengan perkembangan teknologi modem di jaman sekarang lUI, pemakaian CaC03' telah
mengalami kemajuan - kemajuan yang sangat pesat, terutama di bidang-bidung industri. (Othmer, 1965).
Departemen Perindustria:l membuat kalsium karbonat dari batu bintang pada tabun 1981,dan Carlos E. pada tabun 1997 membuat kalsium karbonat dari pasta kalsium hydroxide Ca (OHh.
Pada penelitian ini akan dibuat kalsium karbonat dari Iimbah marmer dengan mereaksikannya dengan soda abu melalui proses soda.
Dari hasil penelitian diharapkan diperoleh data-data kinetika reaksi pembuatan kalsium karbonat dalam tangki berpengaduk dapat menunjang industri kimia serta dapat menunjang industri kimia serta
dapat menunjang pengembangan ilmu
pengetahuan.
Secara sederhana proses pembentukan batu marmer terjadi karena proses dari alam. Batu marmer yang terbentuk berupa bongkahan batu yang sangat besar dan biasanya terdapat pada daerah pegunungan batu kapur.
Pada awalnya ーイッウ・セ@ pengolahan batu marmer hanya melalui proses pemotongan, namun saat ini proses pengolahan batu marmer tidak hanya melalui proses pemotongan, tetapi sudah mulai berkembang sampai proses pemolesan atau penghalusan dan finishing.
Saat ini banyak ditemukan kemajuan-kemajuan dalam teknik pengolahan marmer, baik itu kemajuan dalam pemaduan corak marmer, penggunaan wama marmer dalam membuat hasH kerajinan dari marmer. Selajn di Indonesia di negara-negara Eropa kerajinan marmer juga diminati sehingga memungkinkan untuk menyimpan bahan baku dari Eropa seperti Turki, Italia, dan negara Asia seperti Cina. Selain itu batu marmer import, batu-batu marmer lokal berasal dari Tulungagung. Trenggalek, Ujung Pandang, Bandung dan lain-lain.
Diimportnya batu marmer dari negeri tersebut dikarenakan batu marmer dari luar negeri memiliki struktur corak yang berbeda dan kekuatan yang berbeda pula. Selain alasan tersebut batu marmer yang diimport dari luar negeri lebih bagus sehingga clapat dihasilkan kerajinan batu marmer yang lebih bagus dan inovatif.
Jurnal
Teknik KimiaVo1.2,No.2 April 2008
Batu marmer setelah mengalami proses-proses tertentu hasilnya dapat digunakan sebagai ubin lantai untuk keperluan arsitektur dan untuk hiasan rumah tangga dan kerajinan. Salah satll jenis batuan metamorfosa adalah batwm marmer. Proses metamorfosa ini diakibatkan tckanan dan panas yang berada jauh di bawah permukaan bumi. Proses ini yang membuat batu kapur sangat padat dan keras schingga menjadi batu marmer atau batu pualam.
Batu marmer sangat banyak
dimanfaatkan untuk dokorasi bangunan, baik sebagai interior maupun eksterior, sehingga
bangunan tersebut mempunyai nHai
keindahan yang tinggi. Pemanfaatan batu marmer tersebut diantaranya Lntuk:
a. Tegel mozaik marmer b. Tegel torazzo marmer c. Seni ukir dan pahat
Pada penelitian ini memanfaatkan limbah marmer yang bentuknya berupa lempengan-lempengan atau berupa butiran-butiran keci\. Limbah mamler ini banyak ditemukan di depar.. rumah penduduk di daerah pertambangan marmer Besole, Tulungagung yang setiap harinya bisa menghasilkan sampai 0,5 m3 limbah marmer untuk pengrajin yang berskala besar.
Batuan Manner
Kata marmer berasal dari Bahasa Yunani "marmoros" yang berarti batu yang asli atau yang lebih popular disebut batu pualam. Definisi batu marmer adalah sejenis batu alam yang tersusun dari satu atau lebih macam hablur mineral kalsit, dol mit dan supertin. Semua ini bersatu memadat dan mampu untuk digosok halus sehingga mengkilap atau bisa dipoles.
Batu marmer terdapat di beberapa belahan bumi, yang terbentuk melalui proses kristalisasi. Proses ini berlangsung alami puluhan juta tahun (30-60 juta tahun) yang lalu. Komposisi bahan marmer secara umum dalam % berat adalah:
Si02
Fez03
+
AI203 CaC03MgO
1-1,5% 1%
= 95 - 97%
1%
Penambangan batu marmer di Jawa Timur berlokasi di Besole, Tulungagung. Batu marmer ditambang melalui beberapa proses, yaitu:
Tahap awal disebut "stripping". yaitu proses penghilang deposit marmer yang masih mentah untuk mendapatkan batuan
marmer berkualitas baik yang berupa blok-blok marmer.
Tahap kedua, batuan marmer diolah yang meliputi penggergajian blok-blok marmer diu bah menjacii lempengan-lempengan 、ゥァセイゥョ、。@ dan dipoles hingga mengkilap.
Batuan marmer disebut juga dengan kalsium karbonat (CaC03). Kalsium karbonat
ini merupakan padatan putib kristalin Gernih seperti kristal) semua jenis kalsium karbonat hampir tidak dapat lamt dalam air mumi tetapi teljadi penguraian, dengan adanya
karbon dioksida untuk pembentukan
hydrogen karbonate (bikarbo'1at).
CaC03 + H20 + CO2 セc。RK@ + 2HC03'
... (1)
Kalsium Karbonat
Kalsium karbonat adalah salah satu bahan yang tertua yang dikenal manusia. Pemakaian dari kalsium karbonat oleh manusia sudah lama dan sejalan dengan perkembangan kebudayaan umat manusia.
Seeara umum masyarakat mengenal CaC03 hanya sebagai kalsium karbonat berat.
Tetapi sebenamya CaCO) berat dan CaCO) ringan. Berdasarkan sifat kimianya kedua jenis CaCO) ini hampir sama, perbedaan dasar terdapat pada kerapatan ruah (bulk
density), karbonat berat mempunyai
kerapatan ruah I - 1,2 sedangkan karbonat ringan hanya 0,15 - 0,6. hal ini disebabkan karbonat berat tetjadi seeara alamiah dan dikenal di alam sebagai batu kapur atau lime
stone sementara karbonat ringan tetjadi
melalui proses kimia (Artiticial).
Kalsium karbonat umumnya
digunakan untuk mendukung p"brik kimia lainnya. Penggunaannya antara lain sebagai berikut (Othmer, 1965).
I. Sebagai bahan pembantu pada industri pulp, kertas dan industri fartilasi. 2. Unt.uk refrigeration brine, cheap
drying agent, dust proofing pengendali es dan food additive.
3. Digunakan pada industri fungisida. 4. Digunakall pad a industri tambang
sebagai freeze proofing batu bara dan gas.
5. Digunakan untuk campuran beton untuk meningkatkan kekuatan awal dan ultimate strength.
Kebutuhan kalsium karbonat sejak tahun 1983 terus meningkat seiring dengan perkembangan industri, pemakaiannya antara lain: industri cal, pipa lJlastik, PVC
compound, ban, sepatu karet, kosilletik, k"lit imitasi, pasta gigi dan industri lain. Berdasarkan data yang ada kebutuhan kalsium karbonat mencapai 62,967 ton terdiri dari import dan komoditi dalam negeri.
Sifat-sifat kalsium karbonat (Arthur & Ross, 1950)
a. Sifat-sifat fisika CaC03 (Calcite) Mempakan bubuk putih atau kristal-kristal transparant.
Tidak berbau dan tidak berasa Bentuk padatan
Tidak leleh 1339°C Specific gravity 2,711 b. Sifat-sifat kimia CaCOl (Calcite)
Rumus kimia CaCO) Berat molekul ] 00,09 Kelarutan dalam air
0,0014 grl100 gr H20 pada 25°C
0,002 grll00 gr H20 pada 100°C
Sifat-sifat bahan Kalsium Hidroksida (Cn(0H)2 merupakan baso'\ yang agak kuat dengan seriikit lamt dalam air. Bita ditambah CO2 akan membentuk CaCO) yang tak dapat larut. Kalsium hidroksida dapat dibuat dengan menambahkan air pada padatan kalsium oksida menu rut reaksi :
CaO + H20 セ@ Ca(OH)2 ... (2)
Dengan mengeluarkan panas.
Macam-Macam Proses Pembuatan CaCOJ
Pembuatan kalsium karbonat secara kimiawi, dapat dilakukan melalui berbagai bahan dan cara, antara lain:
1. Proses soda adalah proses pembentukan kalsium karbonat dengan mereaksikan soda abu dan susu kapur (Kobe, 1948).
NB2C0:l + Ca(OHh セ@ CaC0:l + 2 NaOH. ... " ... (3) 2. Mereaksikan susu kapur dengan gas
C02 (Agra dkk, 1971). Reaksi yang tetjadi:
Ca (OHh + CO2 -> CaC03 + 2H20
... " (4)
3. Kalsium klorida, Ammonium
hidroksida dan gas CO2 (Kirk dan
Othmer, 1980). Reaksi yang tetjadi:
CaCh + 2NH40H + CO2 -> CaC03 +
2NRt + H20 "" ... " ... ". (5)
Proses Soda
karena pad a suhu tersebut kapur akan berdisosiasi, menurut persamaan reaksi:
CaC03 + Panas セ@ CaO + C02 ... (6) (BPPI, 1981)
Kapur Tohor (CaO) yang terbentuk diproses lebih lanjut sesuai dengan tujuan.
Bila kapur tohor tersebut ditambah air, akan tcrhidrasi menjadi kalsium hidroksida, menurut persamaan reaksi:
CaO + H20 -+ Ca(OH)2 ... (7)
(Shreve, 1956)
Proses soda adalah pembentukan kalsium karbonat dengan mereaksikan susu kapur dengan soda abu.
Reaksi yang terjadi :
Ca (OH)2 + Na2C03 -+ CaC03 + 2NaOH ... (8) Pada penelitian terdahulu (Sudjarno) kalsium karbonat dapat dibuat dari hasil samping industri pupuk ZA Penelitian limbah pup uk ZA ini dilaksanakan analisa uji hasil pembakaran dari percobaan yang dilakukan, maksud ana lisa ini adalah untuK mengetahui komposisi yang tericandung dalam hasil percobaan tersebut, yang kemudian dari hasil uji analisa ini dicari jenis limbah ZA yang menghasilkan kadar CaO terbesar, sehingga dapat digunakan untuk bahan pembuatan karbonat (CaCO). Kalsium kat bonat dapat juga dibuat dari Iimbah industri marmer dengan variabel yang berbeda pula, antara lain variabel tetap (volume susu kapur dan putaran pengadukan) dan variabel yang dijalankan (waktu, suhu dan perbandingan mol), sehingga nanti diharapkan adanya peningkatan dalam pemanfaatan limbah industri marmer menjadi k&lsium karbonat Hc。cッセI@ apabiJa digunakan variabel-variabel tersebut. Selain itu limbah marmer dapat juga dimanfaatkan untuk
pembuatan marmer sintetis. (Agus
Wahyudiono, 2002).
Kinetika reaksi merupakan ilmu yang mempelajari kecepatan atau laju reaksi kimia juga faktor-faktor yang mempengaruhinya.
Pada penelitian kinetika reaksi pembulltan CaC03 dari marmer bertujuan untuk menentukan tingkat reaksi (orde reaksi), konstanta /aju reaksi.
Sedangkan laju reaksi adalah suatu laju perubahan konsentrasi pereaksi terhadap waktu (-dc/dt). Reaksi pada proses soda adalah:
Jurnal Teknik Kimia Vo1.2,No.2 April 2008
aA + bB -+ cC + dD... (9)
Persamaan laju reaksi di atas dapat ditulis:.
-rA=k.CA.CB ... (10)
Reaksi
oi
atas adalah orde A terhadap B, jadi orde total =: (a+
b), dimlina k sebagai konstanta kecepatan reaksi. Apabi/a mekanisme reaksi tidak diketahll;, harlls mencoba dengan data-data percobaan paJa persamaan kecepatan reaksi lIntuk orde-orde sebagai berikut:a. Reaksi orde satu Persamaan reaksi:
dC A
-rA= - - =k. CA ... (11) dt
dCA
- - - =k. dt ... (12)
C
AC
A dCA t
- f
-
=
k.J
dl ... (13)C CA 0
"AO
- (In CA + In CAO) = k.t ... (14)
CA
- I n -
=
kt ... (IS)C
AODengan CA = CAO (1 - X.0, maka
CA(l-XA)
- In = kt ... (16)
C
AODidapat persamaan:
-In (1 - XA ) = k t ... ... ... (17)
Plot antara -In(I-XA) vs t merupakan garis lurus, maka reaksi adalah reaksi orde satu dengan harga k sebagai slope-nya.
b. Reaksi Orde Dua Persamaan reaksi:
-dCA
-rA
= - - =
k. CA2 ... (I 8) dtdC
A 2 '. 2- - - 2
=
k. c,\ - k. CAO0 -
XA) .(19)C
APersamaan yang didapat
1 XA
C aセM x
(1 _
X
A)
= k . t.. ... (21)X
Plot antara A versus t merupakan l-XA
garis lurus, m.lka reaksinva adalah reaksi orde dua dengan slope
=
k .
CAo.Faktor-Faktor yang Berpengaruh pada Proses Soda
Faktor-taktor yang berpengaruh pada kecepatan reaksi pembentukan kalsium karbonat dengan proses soda antara lain: I. Waktu
Pada reaksi: A + B --+ C + D, dengan
waktu reaksi ya'lg semakin lama, maka jumlah mol A semakin berkurang shg kecepatan reaksi berkurangnya A semakin keci!. Sebaliknya jumlah C yang terbentuk bertambah dan kecepatan
'reaksi pembentukan C semakin
bertambah. 2. Suhu
Apabila suhu dinaikan maka kecepatan reaksi makin bertambah cepat pula, yang mana hal ini sesuai dengan rumus Arrhenius.
k = ko . e .E.:RT... (22)
-E
In k
=
R . T + In ko ... (23)Dimana ォッョウセ。ョエ。@ kecepatan ieaksi (k) sebanding dengan suhu shg apabila k bertambah besar maka kerepatan reaksi juga bertambah besar.
3. Konsentrasi larutan
Terdapat sualu hubungan yg sederhana antara kecepatan reaksi & konsentrasi. Semakin tinggi konsentrasi larutan semakin cepat laju reaksinya begitu juga sebaliknya.
METODE PENELITIAN
nahan Yang Digunakan Marmer
Na2C03 (Natrium Karbonat) Aquadest
[image:5.526.84.440.58.692.2]Rangkaian Alat
Gambar 1. Susunan peralatan
Keterangan gambar:
1. Labu leher tiga 4. Thermometer
2. Pengaduk 5. Kondensor
3. Water Batch 6. Statip
Varinbel yang ditetapkan I. Volume Ca(OH)2, kadar
=250 mI, 25% 2. Pengadukan
= 250 rpm
Varia bel yang diialankan l. Suhu pemanasan (oc)
60 ; 70 ; 80 ; 90 ; 100
2. Waktu proses (menit) 50 . 60 . 70 . 80 . 90
3. Perbanding;n
ュセエ@
antara Ca(OH)2 dan Na2C031 : 1 ; 1 ; 1,5 ; 1 : 2 ; 1 : 2,5 ; 1 : 3
Prosedur Penelitian
1. Marmer dihancurkan sampai halus kemudian dikalsinasi dengan suhu ±
1000"C selama 1 jam dalam furnance. 2. Setelah itu tambahkan air dan diamkan
selama 24 jam untuk pembuatan susu kapur.
3. Kemudian susu kapur diambil sebanyak 250 ml dan tambahkan soda abu sesuai variabe!.
4. Peralatan disiapkan dan masukkan dalam labu leher tiga.
5. Panaskan dan pengaduk dinyalakan. Pemanasan dan pengadukan sesuai dengan variabel yang dijalankan. 6. Setelah itu diamkan dan pisahkan,
HASIL DAN PEMBAHASAN
HasH Penelitian
Untuk Mendapatkan CaC03 dari limbah marmer dilakukan percobaan dengan memvariasikan peubah yang ditunjukkan dalam tabel di bawah ini:
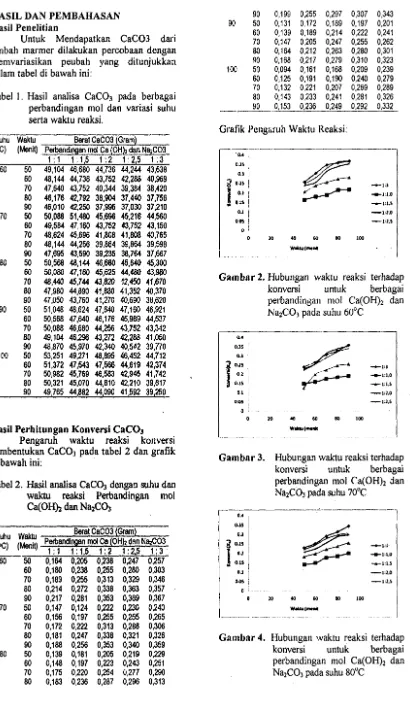
Tabel I. Hasil analisa CaC03 pada berbagai perbandingan mol dan variasi suhu serta waktu reaksi.
Suhu Waktu Serat CaC03 (Gram) ('C) (Manit) MM[pZ[M・M[Mイ「。ョMMZW、ゥョァ。M]ョZZGZGュッiセcセ。@ 7.:(O?-:::H:;'::n セ、。lMョ@ 77NB2C"""=O=-=-3
60 50 60 70 80 90 70 50 60 70 80 90 80 50 60 70 80 90 90 50 60 70 80 90 100 50 60 70 80 90
1 : 1 1: 1 ,5 1 : 2 1 : 2,5 1 : 3 49,104 46,680 44,736 44,244 43,638 48,144 44,736 43,752 42,288 40,969 47,640 43,752 40,344 39,384 38,420 48,176 42,792 38,904 37,440 37,756 46,010 42,250 37,996 37,030 37,210 50,088 51,480 45,696 45,216 44,560 49,584 47,160 43,752 43,752 43,150 48,624 45,696 41,808 41,808 40,765 48,144 44,256 39,864 39,864 39,598 47,695 43,590 39,235 38,764 37,667 50,568 48,144 46,680 45,640 45,300 50,080 47,160 45,625 44,480 43,980 48,440 45,744 43,820 12,450 41,670 47,980 44,890 41,880 41,352 40,370 47,050 43,760 41,270 40,690 36,620 51,048 48,624 47,640 47,160 46,921 50,568 47,640 46,176 45,969 44,537 50,088 46,680 44,256 43,752 43,342 49,104 46,296 43,272 42,288 41,050 48,870 45,970 42,340 40,542 39,no
53,251 49,271 48,895 46,452 44,712 51,372 47,543 47,566 44,619 42,374 50,982 45,769 46,583 42,945 41,742 50,321 45,070 44,610 42,210 39,617 49,765 44,882 44,090 41,592 39,250
Basil Perhitungan Konversi CaCOJ
Pengaruh waktu reaksi konversi pembentukan CaCOJ pada tabel 2 dan grafik
di bawah ini: .
Tabel 2. Hasil analisa c。cセ@ dengan suhu dan waktu reaksi Perbandingan mol Ca(OHh dan n。Rcセ@
Suhu Waktu M[ZMセMZZM]b・ZNNZ[イ。ZN][エLM]cWM。c[ZN[oZZNN[ZSセHgWNMイ。ZZZNュ[ZN\IMZMZMセM[ZM
(oC) (Manit) Peroandingan mol Ca (OHn dAn NIl2C03
Nセ@ __ セQセZQセQセZセQLセUMKQセZRセWQZセRセLUセQᄆZSセ@
60 50 0,164 0,205 0,238 0,247 0,257 60 0,180 0,238 0,255 0,280 0,303 70 0,189 0,255 0,313 0,329 0,346 80 0,214 0,272 0,338 0,363 0,357 90 0,217 0,281 0,353 0,369 0,367 70 50 0,147 0,124 0,222 0,230 0,240 60 0,156 0,197 0,255 0,255 0,265 70 0,172 0,222 0,313 0,288 0,306 80 0,181 0,247 0,338 0,321 0,326 90 0,188 0,256 0,353 0,340 0,359 60 50 0,139 0,181 0,205 0,219 0,229 60 0,148 0,197 0,223 0,243 0,251 70 0,175 0,220 0,254 0,277 0,290 80 0,183 0,236 0,287 0,296 0,313
Jurnal
Teknik KimiaVo1.2,No.2 April 2008
90 0,199 0,255 0.297 0,307 0,343 90 50 0.131 0,172 0,189 0,197 0,201 60 0,139 0,189 0,214 0,222 0,241 70 0,147 0,205 0,247 0,255 0,262 80 0,164 0,212 0,263 0,280 0,301 90 0,168 0,217 0,279 0,310 0,323 100 50 0,094 0,161 0,168 0,209 0,239 60 0,125 0,191 0,190 0,240 0,279 70 0,132 0,221 0,207 0,269 0,289 80 0,143 0,233 0,241 0,281 0,326 90 0,153 0,236 0,249 0,292 0,332
Grafik Pengaruh Waktu Reaksi:
'OA \
0.15 I
0.1 !
tr
O.1S1
0.1!
O.IS0.1
o.os
10 40 60 80 100
W_I ...
[image:6.536.263.470.35.781.2]... 1:3 _1:1,0 -r-l:1.S -1:1,0 -1:l,S
Gambar 2. Hubungan waktu reaksi terhadap
konversi untuk berbagai
perbandingan mol Ca(OH)2 dan Na2C03 pada suhu 60°C
0.4 0.3$ :
0.1
i
O.1S .1
ッセ[Z@
i0.1 : O.OS : o l_
Gambar3.
0.4 us
0.1
il us
1
0.1!
us 0.1O.os
...1:3
セャZャLo@
• ... 1:1,5 -1:1,0 -1:1,5
Hubungan waktu reaksi terhadap konversi untuk berbagai perbandingan mol Ca(OH1 dan Na2C03 pada suhu 70°C
-'-1:1.5 -1:1.0
-I:I,S
Gambar 4. Hubungan waktu reaksi terhadap
konversi untuk berbagai
perbandingan mol Ca(OHh dan Na2C03 pada suhu 80°C
[image:6.536.61.471.60.771.2] [image:6.536.274.470.64.329.2]US 0.1 O.IS
2
0.1) O.IS
0.1 O.OS
o
o 10
-+-1:3 __ U.D
セQZQNウ@
-1'2.0
[image:7.529.40.226.68.410.2] [image:7.529.251.462.70.724.2]- I , U
Gambar 5. Hubungan waktu reaksi terhadap
konversi untuk berbagai
per')andingan mol Ca(OH)2 dan Na2C03 pada suhu 90°C
O.IS 0.1
us . iJ 0.2 '
J
O.IS ;0.1
i
o.os i o '
o
セャZj@
_1,1.0 __ 1:1,5 -1:1.0 -1,2.S
Gambar 6. Hubungan waktu reaksi terhadap
konversi untuk berbagai
perband:ngan mol Ca(OHh dan Na2CO, pada suhu 100°C
Dari gambnr 2 - 6 di atas dapat disimpulkan bahwa semakin tinggi waktu reaksi pada berbagai perbandingan mol maka semakin tinggi pula konversi yang didapatkan. Hal ini disrbabkan karena kontak antara reaktan semakin sempurna sehingga produk yang dil.asilkan semakin besar. Dari semua grafik di atas kondisi terbaik dicapai pada waktu reaksi 90menit dan perbandingan mol 1
: 3 kecuali pada suhu 60°C kondisi terbaik dicapai pada perbandingan moll: 2,5.
0.1 0.2S
It 0.2 ,
J
O.IS '0.1 , O.OS
o •
20 00 60 10 100 110
-loCI
___ 1:) _1:1.0 __ I:U -1:2.0 -1:loS
Gambar 7. Hubungan suhu reaksi terhadap'
konvcrsi untuk berbagai
perbandingan mol Ca(OHhdan Na2C03 pada waktu reaksi 50 menit.
us
0.3
o.n
i
OJ ) O.IS 0.1 .o.os o '
20 00 60 10 100 120
_loCI
-+-1:) ... 1:1.0 -r-l:1.S -1,2.0
--I,l,S
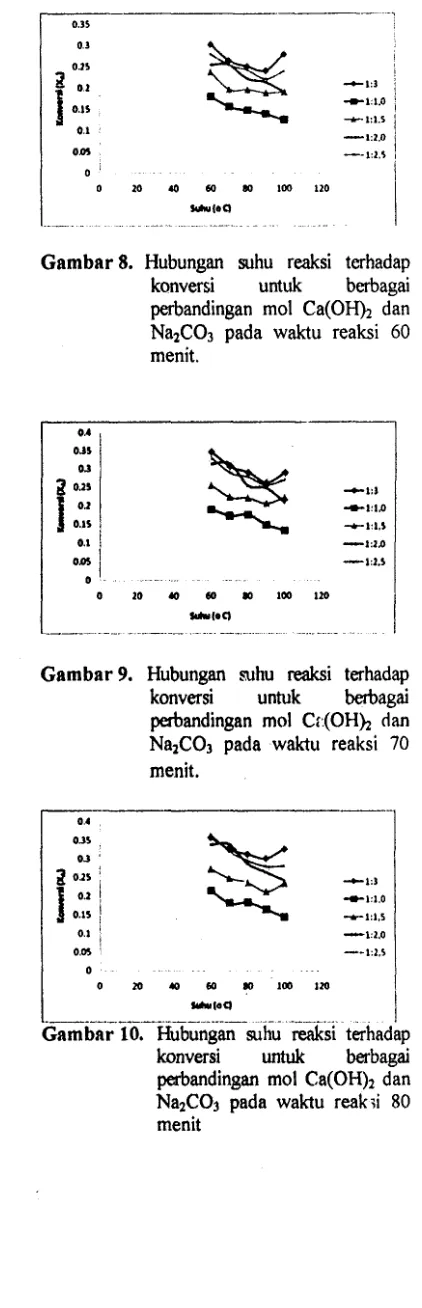
Gambar 8. Hubungan suhu reaksi terhadap
konversi untuk berbagai
perbandingan mol Ca(OHh dan Na2C03 pada waktu reaksi 60 menit.
0.4 1 us
U
i
O.ISJ
oセiセ@
0.1
I
o.os I
o
I
o 20 " (0 10 100 120
... 1:1
_1,1.0 -+-I,U -1,2.D -1,2.S
Gambar 9. Hubungan ruhu reaksi terhadap
konversi untuk berbagai
perbandingan mol Ct(OHh dan Na1C03 pad a waktu reaksi 70
menit.
u
us . U '
i
OlS :J
oセiセ@
0.1 O.OS
20 " (0 10 100 120 -4-1:)
_u.o
... 1:1.5 -1:2.0
--u.s
______________
セセセ⦅セ@
_________ . __ . '. . . I
. . . eo:
0.4
1 OJ!
セ@
0.3
i
0.25 -1:3J
OJセ@
_1:1.00.15 ... iZiNセ@
0.1 -1:2.0
0.05 -1:2,5
o . . ... .. .. ...
-o 20 40 60 80 100 120
WluloC)
Gambar 11. Hubungan suhu reaksi terhadap konversi untuk berbagai perbandingan. mol Ca(OHh dan NazCO) pada waktu reaksi 90 menit.
Dari gambar 7 -I I di atas dapat dj,impulkan bahwa semakin tinggi suhu reaksi pada berbagai perbandingan mol maka konversi yang diperoleh. semakin rendah. Hal ini disebabkan reaksi mengarah pada orde
sam.
Konstanta Laju Reaksi dan Orde Reaksi Penentuan orde dan laju reaksi mengarah pada orde satu dapat dilihat pada persamaan:
- Ln (1 - XA) = k . t
Dimana:
XA
=
Konversit Waktu reaksi, Menit
k Tetapan Jaju reaksi, menif1
Apabila diplotkan antara -Ln (1 - XA) terhadap t waktu merupakan garis lurus, maka persamaan garis Jurus tersebut adalah orde satu dimana k merupakan harga slope.
Tabel3. Hasil analisa CaC03 dengan suhu dan waktu reaksi Perbandingan mol Ca(OH)z dan Na2C03
Waktu
(Manit) XII ·Ln (1 -XII) Suhu (OC)
60 50 0.247 0.284
60 0.280 0.329
70 0.329 0.399
80 0.363 0.451
90 0.369 0.460
70 50 0.230 0.261
60 0.255 0.294
70 0.288 0.339
80 0,321 0,387
90 0.340 0,416
80 50 0.219 0.247
60 0,243 0,278
Jurnal
Teknik KimiaVo1.2,No.2 April 2008
70 0.277 0.324
80 0,296 0.351
90 0,307 0.367
90 50 0,197 0,219
60 0.222 0.251
70 0,255 0,2&4
80 0.280 0.329
90 0,310 0,371
100 50 0.209 0.234
60 0.240 0.274
70 0.269 0.313
80 0,281 0.329' ,
90 0.292 0.345
0.6 "I
セ@
.900(I
.'-00( ,600( 0.5
·700(
0.1 800(
[image:8.536.278.459.60.318.2]20 80 100
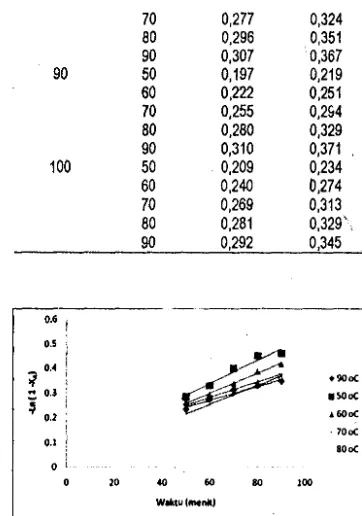
Gambar 12. Hubungan antara waktu dan -Ln (l - XA) pada berbagai suhu Wltuk
perbandingan moll :2,5
Pada suhu 60°C sampai suhu 100°C dengan waktu reaksi yang semakin lama akari memperbesar hasil konversi. Hubungan antara waktu dan - In (1 - XA) menunjukkan garis Iinier, maka reaksi pembentukan CaC03 mengarah pada reaksi orde satu. Dimana harga k pada suhu 60°C sebesar 0,0055, pada suhu 70°C
sebesar
0,0048 pada suhu 80°C sebesar 0,0044, pada suhu 90°C sebesar 0,0042, pada suhu 100°C sebesar 0,0042, dengan waktLJ yang semakin lama akan mengkonstankan hasil konversi karen a reaktan sudah mulai jenuh.Pembuatan CaC03 dari limbah
marmer dan NaC03 merupakan reaksi orde
satu. ApabiJa k yang diperoleh dibuat hubungan antara -Lnl: dengan liT maka diperold, hubungan garis lurus.
K Ko. e·FJRT
E
LnK --+1.n Ko
RT
Dimana persamaan di atas apabila
dihubungkan antara Ln K dengan Iff c:kan diperoleh E/R sebagai slope dan Ln Ko sebagai interceptnya.