ANALISA PROKSIMAT BAHAN PAKAN TERNAK 1.1 Landasan Teori
Segala sesuatu yang dapat dijadikan pakan dinamakan bahan pakan. Tetapi tidak semua yang dapat dimakan bermanfaat bagi tubuh. Komponen bahan pakan yang dapat dicerna, diserap serta bermanfaat bagi tubuh disebut zat pakan. Ada 6 macam zat pakan yaitu air, karbohidrat, protein, lemak, vitamin dan mineral.
Zat Pakan terdiri atas berbagai macam, kecuali air. Misalnya, mineral tidak kurang 15 – 21 macam, vitamin terdiri dari 13 – 15 macam. Hal ini menyebabkan analisa bahan pakan menjadi banyak sekali, jika semuanya dianalisa akan makan banyak waktu, tenaga dan biaya. Mengingat sangat kompleksnya analisa bahan pakan, manusia mencoba membuat penyederhanaan yaitu mengelompokkan zat-zat pakan berdasar sifat fisik dan kimianya. Analisa lain yang tidak terwakili oleh pengelompokkan itu dilakukan secara khusus. Usaha ini telah dirintis oleh para sarjana Jerman sejak awal abad 19, antara lain oleh Thaer pada tahun 1809. Kemudian pada tahun 1860 oleh Henneberg dan Stohman dari Weende (nama salah satu Laboratorium di Jerman Timur) metode Thaer disempurnakan.
Metode ini sampai sekarang dikenal dengan nama analisa Proksimat Weende.
Proksimat berarti gambaran secara kasar yang artinya garis besar (bentuk kasar) dalam menggambarkan komposisi zat pakan suatu bahan pakan. Metode tersebut sangat popular hingga kini.
Pengelompokkan zat pakan suatu bahan pakan menurut analisa proksimat digambarkan dalam ilustrasi sebagai berikut :
Bahan --- Air pakan
--- Bahan --- Abu/ mineral Kering
--- Bahan --- Protein Organik
--- BOTN --- Lemak
--- Karbohidrat --- Serat Kasar
Ilustrasi tersebut nampak bahwa bahan pakan terbagi ke dalam 10 zat pakan, 5 diantaranya, yaitu bagian atas bagan pembagian tersebut, diperoleh dengan jalan analisa dan 5 lainnya dihitung sebagai selisih.
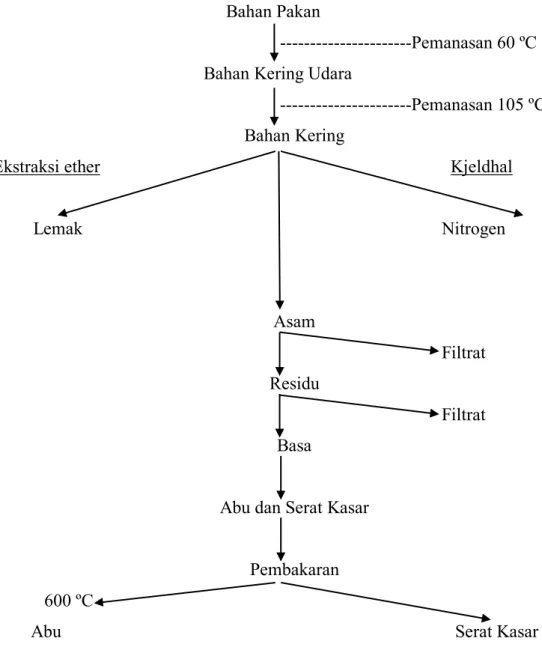
Analisa proksimat didasarkan atas komposisi kimia dari bahan pakan, dengan skema sebagai berikut :
Bahan Pakan
---Pemanasan 60 ºC
Bahan Kering Udara
---Pemanasan 105 ºC
Bahan Kering
Ekstraksi ether Kjeldhal
Lemak Nitrogen Asam Filtrat Residu Filtrat Basa
Abu dan Serat Kasar Pembakaran 600 ºC
Abu Serat Kasar
Melalui pemanasan bahan pakan pada suhu 105º C, seluruh air yang dikandung bahan pakan itu akan menguap, yang tertinggal adalah bahan kering. Bila pemanasan dilanjutkan pada suhu 600º C maka seluruh bahan organik akan menguap dan yang tertinggal adalah Abu (mineral). Selisih antara Bahan Kering dan Abu adalah Bahan Organik.
Protein bahan pakan ditentukan dengan metode Kjeldhal. Metode ini menganut asumsi bahwa semua Nitrogen bahan pakan berasal dari protein dan semua protein mengandung Nitrogen sebesar 16 %, maka protein bahan pakan ditentukan dengan menganalisa kandungan Nitrogennya. Hasil yang diperoleh dikalikan denngan 100/ 16 atau 6,25. Prinsip metode Kjeldahl adalah sebagai berikut : Nitrogen bahan pakan diubah menjadi ammonium sulfat dengan jalan memasaknya di dalam asam sulfat pekat. Kemudian setelah didinginkan diencerkan dengan aquadest, lalu dibuat basa dengan menambahkan NaOH. Maka ammonia akan dibebaskan. Amonia ditangkap oleh larutan asam borat,kemudian dititrasi dengan asam sulfat yang telah ditentukan normalitasnya.
Bahan kering setelah dikurangi dengan N dinamakan Bahan Organik Tanpa Nitrogen (BOTN). BOTN ada yang larut dalam pelarut organik ada yang tidak. Fraksi yang larut dinamakan lemak sedangkan yang tidak larut dinamakan karbohidrat.
Analisa proksimat kadar lemak ditentukan dengan jalan mengekstraksikan bahan pakan ke dalam pelarut organik (misal petroleum ether atau hexan).
Karbohidrat terbagi menjadi 2 fraksi yaitu Serat Kasar dan Bahan Ekstrak Tanpa Nitrogen (BETN). Serat kasar adalah karbohidrat yang tidak larut setelah dimasak berturut-turut dalam larutan H2SO4 1,25 % mendidih selama 30 menit dan dalam larutan NaOH 1,35 %
mendidih selama 30 menit.
CARA MENYIAPKAN SAMPEL UNTUK DI ANALISA
1. Semua contoh (sampel) yang akan dianalisa di Laboratorium harus ditimbang dengan segera, baik masih segar maupun sudah kering.
2. Bila contoh terdiri dari hijauan segar, maka hijauan tersebut harus dikeringkan lebih dahulu dengan cara menjemur di panas matahari atau dimasukkan ke dalam alat pengering pada suhu 40 – 60 ºC selama 24 – 28 jam dan sesudah dingin ditimbang kembali.
3. Buah-buahan dan biji-bijian yang mempunyai kulit, lebih dahulu harus dikupas dan bagian-bagian yang tidak dapat dipisahkan dari bagian-bagian yang dapat dimakan ditimbang berturut-berturut dan baru dikeringkan dan kemudian ditimbang lagi.
4. Semua bahan yang akan dianalisa harus dihaluskan terlebih dahulu dengan gilingan dan disaring dengan saringan yang bergaris tengah satu millimeter.
5. Semua contoh/ sampel bahan yang akan dianalisa harus diberi kode dan arti dari kode tersebut harus dicatat di dalam buku khusus.
PENGAMBILAN SAMPEL
Sampel merupakan bagian dari suatu bahan yang diambil secara acak dari bahan tersebut untuk selanjutnya dievaluasi. Dalam pengambilan sampel suatu bahan harus dilakukan secra benar agar diperoleh sampel yang benar-benar representatif, yang mampu menggambarkan keadaan bahan yang diambil sampelnya secara tepat. Untuk tujuan tersebut maka pengambilan sampel perlu diperhatikan hal-hal sebagai berikut:
1. Homogenitas sampel
Salah satu faktor yang menentukan tingkat represetatif sampel yang diambil adalah homogenitas bahan yang akan diambil sampelnya. Efek ukuran dan berat partikel sangat berpengaruh terhadap homogenitas bahan, dimana bagian yang berukuran dan berat yang lebih besar kemungkinan akan berpisah dengan bagian lebih kecil atau ringan (segresi). Sehingga pada bahan yang ditumpuk atau dimuat diatas truk, bagian bahan yang mempunyai ukuran dan berat partikel yang lebih besar terletak pada bagian bawah atau bagian dasar dari tumpukan tersebut. Oleh karena itu sebelum bahan diambil sampelnya harus dicampur secara merata sehingga bahan benar-benar homogen, atau sampel diambil secara acak dari beberapa bagian baik bagian dasar, tengah maupun bagian atas sehingga diperoleh sampel yang benar-benar representatif. Demikian juga pada hijauan disuatu lahan, kualitas hijauan pada tiap-tiap bagian lahan, kemungkinan mempunyai kualitas yang berbeda karena adanya kemungkinan perbedaan kesuburan tanah pada lahan tersebut. Oleh karena itu agar diperoleh sampel yang representatif, pengambilan sampel harus dilakukan pada beberapa bagian lahan secara acak, sehingga data yang diperoleh memberikan informasi yang benar terhadap kualitas bahan tersebut.
a. Aselectif yaitu cara pengambilan sampel yang dilakukan secara acak dari keseluruhan bahan tanpa memperhatikan atau memisahkan bagian-bagian dari bahan tersebut. Misalnya dalam pengambilan sampsatria14el pada rumput gajah, sampel kita ambil dari seluruh bagian rumput gajah tersebut baik bagian daun maupun bagian batang, kemudian dipotong-potong dan dicampur secara merata agar diperoleh bahan yang benar-benar homogeny, sehingga sampel yang diambil benar-benar representatif. b. Selectif yaitu cara pengambilan sampel yang dilakukan secara acak dari
bagian-bagian tertentu dari suatu bahan. Misalnya dalam pengambilan sampel bagian-bagian batang dan bagian daun rumput gajah, maka sebelum diambil sampelnya bagian-bagian tersebut harus dipisah terlebih dahulu, baru masing-masing bagian diambil sampelnya dengan tetap memperhatikan homogenitas bahan tersebut.
3. Jumlah sampel
Jumlah sampel yang diambil akan sangat berpengaruh terhadap tingkat representatif sampel yang diambil. Jumlah sampel yang diambil tergantung pada kebutuhan untuk evaluasi dan jumlah bahan yang diambil sampelnya. Sebagai pedoman jumlah sampel yang diambil adalah 10% dari jumlah bahan. Pada bahan yang berjumlah banyak misalnya lebih dari 100 kg, sampel diambil 10% dari jumlah tersebut secara acak, kemudian sampel diambil lagi 10% dari sampel yang diambil tersebut.
4. Penanganan sampel
Sampel yang telah diambil harus segera diamankan agar tidak rusak atau berubah sehingga mempunyai sifat yang berbeda dengan bahan dari mana sampel tersebut diambil. Misalnya terjadinya penguapan air, pembusukan atau tumbuhnya jamur, ketengikan dan lain-lain. Sampel yang diproleh dari bahan dengan kadar air rendah (kurang dari 15%), kemungkinan terjadinya kerusakan sampel sangat kecil sekali. Sehingga sampel dapat lansung dimasukkan kedalam kantong plastik dan dibawa ke labolatorium untuk dianalisa.
Sedang sampel yang diperoleh dari bahan segar misalnya hijauan atau silase, maka kemungkinan terjadinya penguapan air besar sekali. Sehingga untuk mengontrol
penguapan air selama penganan sampel, maka sampel yang telah diambil harus segera ditimbang, dimasukkan kedalam kantong plastik yang kedap udara, dibawa ke
labolatorium dan segera dianalisa kadar bahan keringnya, sehingga kemungkinan terjadinya penguapan air kecil sekali dan bahan tidak mudah rusak. Hal ini mungkin dilakukan jika lokasi pengambilan sampel dengan labolatorium. Tetapi jika lokasi pengambilan sampel jauh dari labolatorium maka sampel yang telah diambil segera ditimbang, dikeringkan atau dijemur sampai beratnya konstan ditempat yang aman (diusahakan tidak terdapat bagian sampel yang hilang), kemudian dibawa ke labolatorium untuk dianalisa.
5. Prosesing sampel
Untuk tujuan evaluasi terutama evaluasi secara mikroskopik, kimia dan biologi semua sampel harus digiling lebih dulu sehingga diperoleh sampel yang halus.
Analisa bahan pakan secara kimiawi dapat dilakukan dengan beberapa cara. Analisa proksimat merupakan salah satu cara yang sering dilaksanakan, melalui analisa proksimat dapat diketahui kualitas suatu bahan pakan.
EVALUASI KUALITAS PAKAN
Penentuan kualitas suatu bahan pakan ternak sulit jika dilakukan dengan indra, serta dalam membandingkan dua atau lebih bahan pakan tanpa analisa baik secara fisik, khemis, maupun biologis. Dua macam hay atau bijian seperti jagung atau kedelai mungkin terlihat mirip satu dengan lainnya, namun yang satu mungkin mengadung bahan kering 12% dan lainnya 18%. Sehingga analisa keduanya harus dilakukan. Analisa kimia saja tidak akan cukup, percobaan dengan menggunakan ternakpun harus dilakukan karena bahan pakan yang bernutrisi tinggi tapi mempunyai daya cerna yang rendah adalah hanya pengisi perut saja.
Pendekatan yang sistematik untuk mengukur kualitas suatu bahan pakan sudah dilakukan sejak tahun 1800, cara ini terus berkembang dan memungkinkan pengukuran bermacam-macam bahan pakan yang lebih detail. Pada abad 20 isolasi dan identifikasi dari faktor-faktor pemacu pertumbuhan dan nutrisi seperti vitamin sudah dapat dilaksanakan. Pengetahuan dasar biokimia sejajar dengan ilmu nutrisi dapat diadopsikan untuk menganilisis dan mengevaluasi bahan pakan. Cara-cara baru dan canggih banyak digunakan di dalam industri pakan ternak untuk mendeteksi komponen bahan pakan dalam ukuran 10-6
Keuntungan adalah kriteria utama dari kesuksesan di dalam pengoperasian peternakan, dan biaya pakan adalah faktor penting dalam penentuan kesuksesan. Nilai komposisi bahan pakan dalam beberapa buku menyajikan rataan dari sekumpulan data yang diperoleh dari beberapa hasil analisa yang dapat digunakan sebagai pedoman dalam menentukan komposisi kimia suatu bahan pakan. Tetapi karena kmposisi kimia suatu bahan pakan dipengaruhi oleh beberapa faktor, seperti umur tanaman, kondisi tanah, iklim dan lain-lain, maka dalam penyusunan pakan bahan-bahan penyusunnya harus dianalisa agar diperoleh pakan yang seimbang.
Analisa bahan pakan hanya akan dicapai secara baik jika pengambilan sampel dilakukan secara benar dan representatif.
1. PENETAPAN KADAR BAHAN KERING UDARA (HIJAUAN SEGAR) Alat-alat : - Sabit - Gunting rumput - Timbangan - Kantong plastik - Kotak kertas - Oven Cara kerja :
- Memotong rumput yang tumbuh di dalam petak-petak, sedangkan rumput yang tumbuh pada bagian pinggir petak sebagai Border Effect. Rumput dipotong dengan ketinggian 15-20 cm dari tanah. Kemudian rumput di masukkan ke dalam kantong plastic untuk menghindari adanya penguapan.
- Kemudian rumput dipotong kecil-kecil sekitar 2-5 cm, dimasukkan ke dalam kotak kertas dan di timbang sebagai berat A
- Masukkan kotak kertas + sampel ke dalam oven dengan suhu 60-70°C selama 24 jam. - Setelah itu dikeluarkan dan diangin-anginkan di dalam ruangan selama 2-3 jam,
kemudian ditimbang. Sebagai berat B. Perhitungan :
Kadar BK Udara (%) = 𝐵𝐵
𝐴𝐴
× 100 %
Keterangan :
A : Berat kotak kertas
B : Berat kotak kertas + Sampel
2. PENETAPAN KADAR BAHAN KERING
Prinsip :
Dengan pemanasan 105°C, air yang terkandung dalam suatu bahan pakan akan menguap seluruhnya. Bahan yang tertinggal setelah penguapan air disebut bahan kering.
Alat-alat :
- Cawan porselin atau aldisk - Oven 105° C
- Eksikator - Penjepit
- Timbangan analitik Cara Kerja :
- Cawan porselin dimasukkan dalam oven 105°C selama 1 jam.
- Cawan diambil dan dimasukkan eksikator (gunakan tang penjepit) selama 1 jam. Dalam praktikum pekerjaan ini biasanya sudah dilakukan oleh laboran.
- Timbang cawan tersebut dengan teliti, misalnya beratnya A gram.
- Masukkan sampel ± 2 gram dalam cawan dan ditimbang kembali. Misalnya beratnya B gram. Kemudian masukkan cawan yang berisi sampel tersebut kedalam oven 105°C sampai berat konstan yaitu sekitar 4 jam.
- Cawan diambil, dimasukkan dalam eksikator selama 1 jam, kemudian ditimbang beratnya dengan teliti, misalnya C gram. Pada waktu mengambil cawan, gunakan tang penjepit. Perhitungan : Kadar BK (%) = 𝐶𝐶−𝐴𝐴 𝐵𝐵−𝐴𝐴
× 100 %
Keterangan : A= berat cawanB= berat cawan + sampel
3. PENETAPAN KADAR BAHAN ANORGANIK (ABU)
Prinsip :
Dengan pemanasan menggunakkan tanur dengan suhu 550-600° C semua bahan organik akan terbakar. Bahan anorganik yang tidak tebakar disebut abu.
Alat- alat:
- Alumunium disk atau cawan porselin - Tanur 550-600° C
- Eksikator - Penjepit
- Timbangan analitis Cara kerja :
- Ambil cawan porselin dan masukkan ke dalam Oven (105 0 C) selama 1 jam.
- Dengan menggunakan tang penjepit cawan porselin dimasukkan dalam eksikator diamkan selama 1 jam. Dalam praktikum pekerjaan ini biasanya sudah dilakukan oleh laboran.
- Timbang cawan porselin tersebut, misal beratnya A gram. Ambil sampel ± 2 gram masukkan dalam cawan porselin dan ditimbang kembali, misal beratnya B gram. - Masukkan cawan porselin yang berisi sampel ke dalam tanur 600°C sampai warnanya
berubah menjadi putih atau telah berubah menjadi abu. Tidak boleh terdapat warna hitam (± 4 jam).
- Cawan porselin diambil dimasukkan ke dalam eksikator diamkan selama 1 jam kemudian ditimbang dengan teliti (beratnya C gram).
Perhitungan : Kadar Abu (%) = 𝐶𝐶−𝐴𝐴 𝐵𝐵−𝐴𝐴
× 100 %
Keterangan : A= berat cawanB= berat cawan + sampel
4. PENETAPAN KADAR PROTEIN KASAR
Prinsip :
Asam sulfat pekat dengan katalisator dapat memecah ikatan N organik dalam bahan pakan menjadi ammonium sulfat, kecuali ikatan N = N; NO; NO2. Ammonium sulftat dalam
suasana basa akan melepaskan NH3 yang kemudian didestilasi. Hasil destilasi ditampung
dalam beaker glass yang berisi H2SO4 0,1 N yang telah diberi indicator campuran. Setelah
selesai destilasi, larutan penampung di titrasi dengan NaOH 0,1 N sampai warna berubah. Cara yang umum digunakan adalah cara Kjeldahl :
a. Proses destruksi (oksidasi)
Pengubahan N-protein menjadi ammonium sulfat.
Sampel dipanaskan dengan asam sulfat pekat (H2SO4) dan katalisator dapat memecah
semua ikatan N dalam bahan pakan menjadi (NH4)2SO4 kecuali ikatan N = N, NO dan
NO2. Amoniak dalam asam sulfat terdapat dalam bentuk ammonium sulfat. CO2 dan H2O
terus menguap. SO2 yang terbentuk adalah hasil reduksi dari sebagian N asam sulfat, SO2
pun menguap.
N-organik + H2SO4 CO2 + H2O + (NH4)2SO4 + SO2
Dalam reaksi ini digunakan katalisator selenium /Hg/Cu. Destruksi dihentikan setelah larutan berwarna hijau jernih. b. Proses destilasi (penyulingan)
Setelah larutan menjadi jernih dan berwarna hijau labu destruksi didinginkan kemudian dengan pengenceran 60 ml aquades larutan dimasukkan dalam labu Erlenmeyer 300 ml. Pengenceran dilakukan untuk mengurangi kehebatan reaksi jika larutan ditambah alkali larutan dijadikan basa dengan menambahkan NaOH 40 %, labu dipasang pada alat penyuling.
Hasil sulingan (uap NH3 dan air) ditangkap oleh larutan H2SO4 yang terdapat dalam labu
Erlenmeyer dan membentuk senyawa (NH4)2SO4. Senyawa ini dalam suasana basa akan
Sulfat. Penyulingan dihentikan jika semua N sudah tertangkap oleh asam sulfat dalam labu Erlenmeyer (2/3 bagian cairan dalam labu penyuling telah menguap).
2NH3 + 2H2SO4 (NH4)2SO4 + H2SO4
c. Proses Titrasi
Kelebihan H2SO4 yang digunakan untuk menangkap N dititrasi dengan Natrium
Hidroksida. Titrasi dihentikan jika larutan berubah dari ungu ke biru kehijauan. Alat-alat :
- Timbangan analitis
- Labu didih kjeldhal (50 ml) - Gelas ukur 5 ml atau dispenser - Erlenmeyer (300 ml)
- Beaker glas (300 ml) - Alat untuk destilasi
- Pipet volume 25 ml atau dispenser - Buret 50 ml
Bahan kimia :
- H2SO4 pekat (95 – 97 %)
- Katalisator (Tablet Kjehldahl) - Aquadest
- NaOH 40 % - H2SO4 0,1 N
- Indikator (2 gram methyl red + methyl blue per liter etanol 96 %) - NaOH 0,1 N
Cara Kerja :
1. DESTRUKSI
- Timbang kertas minyak, misal berat A gram. Ambil sampel kira-kira 0,3 gram untuk bahan yang mengandung protein rendah atau 0,2 gram untuk bahan yang mengandung
protein tinggi, tuangkan dalam kertas minyak dan timbang kembali, misal beratnya B gram. Masukkan sampel (tidak dengan kertas minyak) ke dalam labu kjeldahl.
- Tambahkan 1,2 gram katalisator. Kemudian tambahkan 5 ml H2SO4 pekat (di dalam
lemari asam) dengan menggunakan dispenser.
- Didestruksi sampai warna menjadi hijau bening. Biarkan menjadi dingin.
- Tambahkan 60 ml aquadest (dibagi 4 kali), kocok dan masukkan larutan ke dalam Erlenmeyer 300 ml.
2. DESTILASI
- Ambil beaker glas 300 ml, isi dengan H2SO4 0,1 n sebanyak 25 ml dengan
menggunakan dispenser. Tambahkan 3 tetes indikator mix, warna menjadi ungu. Kemudian letakkan beaker glas dibawah ujung alat destilasi (ujung alat destilasi harus masuk kedalam cairan penampung, agar tidak ada NH3 yang hilang).
- Untuk destilasi, tambahkan 20 ml NaOH 40 % dalam Erlenmeyer hasil destruksi, kemudian dengan cepat (agar tidak ada NH3 yang hilang) pasang dalam alat destilasi.
- Selama destilasi warna tetap ungu. Destilasi selesai kalau larutan di dalam erlenmeyer 300 ml mulai mendidih tidak lancar lagi.
3. TITRASI
- Beaker glas yang berisi hasil sulingan dititrasi dengan NaOH 0,1 n sampai warna berubah menjadi hijau jernih. Misal jumlah NaOH untuk titrasi C ml.
- Buat blanko, caranya sama tetapi tidak memakai sampel (Misal untuk titrasi perlu D ml NaOH 0,1n).
Perhitungan :
Kadar PK = (D−C)x n NaOH x 0,014 x 6,25
B−A
× 100 %
Keterangan :
A = berat kertas minyak B = berat kertas minyak plus sampel
C = jumlah NaOH untuk titrasi sampel D = jumlah NaOH untuk titrasi Blanko
5. PENETAPAN KADAR LEMAK KASAR
Prinsip :
Eter dipanaskan terus menerus kemudian didinginkan secara kondensasi akan mengekstrak semua bahan-bahan yang larut dalam eter. Bahan ekstraksi dikumpulkan dalam suatu tabung. Jika proses sudah selesai (4 jam). Eter dikumpulkan ditempat lain dan sisa lemak kasar dikeringkan dalam oven, setelah dingin ditimbang.
Lemak adalah sekelompok zat-zat yang tidak larut dalam air tetapi larut dalm eter, kloroform, dan benzene. Yang termasuk dalam golongan lipida adalah lemak, fosfatida, seterol, dll. Lemak merupakan bagian yang terpentin dari golongan zat-zat tersebut.
Lemak mengandung C, H, dan O. dalam perbandingannya lemak lebih banyak mengandung C dan H daripada O, misalnya C57H110O6. Lemak memberikan 2,25 kali energy
lebih banyak disbanding dengan karbohidrat jika mengalami metabolism karena lemak mengandung unsur H lebih banyak daripada unsur O.
Alat-alat :
- Alat ekstraksi Goldfish
- Beaker glas khusus untuk lemak kasar - Selongsong S
- Gelas ukur
- Oven vacuum 80 ºC - Timbangan analitis - Eksikator
- Tabung Penangkap n-Hexan Bahan Kimia :
Cara Kerja :
- Masukan beaker glass ke dalam oven dengan suhu 105 ºC selama 1 jam.
- Ambil beaker glas dan masukkan dalam eksikator selama 1 jam. Pekerjaan ini biasanya sudah dilakukan oleh laboran.
- Timbang sampel sebanyak 1,5 gram diletakkan diatas kertas saring, misal beratnya A gram. Bungkus sampel dengan menggunakan kertas saring tersebut, kemudian masukkan sampel ke dalam selongsong S.
- Ambil beaker glas khusus untuk analisa lemak dari eksikator dan ditimbang, misal beratnya B gram. Isi beaker glas dengan 50 ml n-hexan dengan menggunakan gelas ukur. - Kemudian beaker glas dan alat porselin (atau selongsong S) dipasang ke alat ekstraksi
Goldfish, dan di ekstraksi selama 2 jam. Suhu alat diatur pada skala 5
- Ambil selongsong S dengan sampel dengan labu khusus untuk mengumpulkan hexan lagi, sampai hexan dalam beaker glas tinggal sedikit saja.
- Beaker glas yang telah berisi lemak dimasukkan ke dalam oven vacum 80 ºC. - Lalu dihisap udara dari oven, beaker glas di oven selama 1,5 jam.
- Beaker glas dimasukkan ke dalam eksikator selama 1 jam, dan ditimbang dengan teliti, misal beratnya C gram.
Perhitungan :
Kadar Lemak (%) = C−B
A
× 100 %
Keterangan :
A : Berat Sampel B : Berat Beaker Glass
6. PENETAPAN KADAR SERAT KASAR
Prinsip :
Serat kasar adalah suatu indikator dari daya cerna dan bulkiness dari suatu bahan. Serat kasar merupakan senyawa yang tidak larut jika direbus berturut-turut dalam larutan H2SO4 0,3
N selama 30 menit dan NaOH 1,5 N selama 25 menit. Tujuan penambahan H2SO4 untuk
menguraikan senyawa N dalam pakan, penambahan NaOH untuk menguraikan/ penyabunan senyawa lemak dalam pakan sehingga mudah larut. Sisa bahan pakan yang tidak tercerna setelah proses perebusan kemudian ditimbang dan diabukan. Perbedaan berat residu pertama dan berat residu setelah diabukan menunjukkan jumlah serta yang terdapat dalam suatu bahan pakan.
Fraksi serat kasar terdiri dari selulosa, hemiselulosa dan lignin. Pada ternak ruminansia dan herbivora non ruminansia selulosa dapat dicerna melalui degradasi mikroba. Mendekati 95 % dari serat kasar adalah selulosa. Sistem ini dikembangkan oleh Van Soest untuk mengevaluasi fraksi-fraksi dari suatu bahan pakan yang dapat dicerna.
Alat-alat :
- Timbangan analitis
- Beaker glas khusus untuk serat kasar - Alat untuk mendidihkan
- Cawan filtrasi (crusible) serta alat filtrasinya - Eksikator - Oven 105 ºC - Tanur 550 – 600 ºC Bahan Kimia : - H2SO4 0,3 N - NaOH 1,5 N - HCl 0,3 N - EDTA
Cara Kerja :
- Timbang sampel ±1 gram taruh diatas kertas minyak, misal beratnya A gram. Tuangkan sampel (kertas minyak tidak diikutkan) dalam beaker glas khusus untuk analisa serat kasar dan tambahkan H2SO4 0,3 N sebanyak 50 ml dengan menggunakan gelas ukur, didihkan
selam 30 menit. (Dihitung saat air sudah mulai mendidih)
- Selanjutnya dengan cepat ditambahkan 25 ml NaOH 1,5 N dan didihkan lagi selama 25 menit tepat. (Dihitung saat air sudah mulai mendidih)
- Dengan cepat pula ditambah 0,5 gram EDTA kemudian didihkan lagi selama 5 menit tepat. - Matikan tombol pemanas. Ambil beaker glas.
- Saring dengan cawan filtrasi / cawan crucible.
- Bilas beaker glas dengan aquadest panas sesedikit mungkin sampai semua larutan masuk ke cawan filtrasi.
- Lalu tambahkan 50 ml HCl 0,3 n diamkan 1 menit lalu dihisap dengan pompa vacum. - Ditambah dengan 50ml aquadest panas
- Kemudian ditambahkan lagi 40 ml aceton, diamkan 1 menit lalu dihisap sampai kering. - Selanjutnya dioven pada suhu 105 ºC selama 1,5 jam, kemudian masukkan ke dalam
eksikator selama 1 jam dan ditimbang dengan teliti (beratnya B gram).
- Setelah itu masukkan ke dalam tanur 550 – 600 ºC selama 2 jam, keluarkan dengan tang penjepit dan masukkan kembali ke dalam eksikator, diamkan selama 1 jam dan timbanglah dengan teliti (beratnya C gram).
Perhitungan :
Kadar Serat Kasar (%) = B−C
A
× 100 %
Keterangan :
A : berat sampel
B : berat setelah di oven 105 ºC C : berat setelah di tanur 550 – 600 ºC