commit to user
ANALISIS MISKONSEPSI KIMIA PADA PEMBELAJARAN TERMOKIMIA SISWA KELAS XI SMAN 2 SUKOHARJO
SKRIPSI
oleh
WAHYU PUJI LESTARI K3304010
FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS SEBELAS MARET
commit to user
i
ANALISIS MISKONSEPSI KIMIA PADA PEMBELAJARAN TERMOKIMIA SISWA KELAS XI SMAN 2 SUKOHARJO
SKRIPSI
oleh
WAHYU PUJI LESTARI K3304010
FAKULTAS KEGURUAN DAN ILMU PENDIDIKAN UNIVERSITAS SEBELAS MARET
commit to user
vi ABSTRAK
WAHYU PUJI LESTARI. Analisis Miskonsepsi Kimia pada Pembelajaran Termokimia Siswa Kelas XI SMAN 2 Sukoharjo. Skripsi. Surakarta : Fakultas Keguruan dan Ilmu Pendidikan, Universitas Sebelas Maret Surakarta, Januari 2012.
Tujuan penelitian ini adalah untuk mengetahui : (1) adakah miskonsepsi
kimia dalam pembelajaran termokimia siswa SMAN 2 Sukoharjo, (2) bentuk
miskonsepsi kimia yang terjadi pada siswa SMAN 2 Sukoharjo, dan (3) hal-hal
yang menyebabkan terjadinya miskonsepsi kimia pada pembelajaran termokimia
siswa SMAN 2 Sukoharjo.
Penelitian ini menggunakan metode deskriptif kualitatif. Populasi yang
diambil dalam penelitian ini adalah siswa kelas XI SMAN 2 Sukoharjo tahun
pelajaran 2008/2009 dengan jumlah seluruhnya 7 kelas. Sampel diambil dengan
teknik non random sampling. Pengumpulan data dilakukan dengan menggunakan
tes diagnostik miskonsepsi berbentuk tes objektif beralasan, observasi, angket,
dan wawancara.
Berdasarkan hasil penelitian dapat disimpulkan : (1) terjadi miskonsepsi
dalam pembelajaran konsep-konsep kimia pada pokok bahasan termokimia pada
siswa SMAN 2 Sukoharjo, (2) miskonsepsi yang terjadi adalah miskonsepsi
dalam bentuk konsep teoritik, korelasional, dan klasifikasional, dan (3) penyebab
terjadinya miskonsepsi adalah motivasi belajar yang kurang dan prakonsepsi yang
kurang benar dari siswa, kurangnya interaksi antara guru dengan siswa, buku
pegangan yang kurang lengkap dan sukar dipahami, dan metode pembelajaran
yang tidak mengarah pada pembentukan konsep.
commit to user
x
KATA PENGANTAR
Puji syukur penulis panjatkan ke hadirat Allah SWT atas segala rahmat dan
hidayah-Nya sehingga penulisan skripsi ini dapat diselesaikan. Sholawat dan
salam penulis curahkan kepada junjungan nabi Muhammad SAW.
Penulisan skripsi ini tidak dapat terselesaikan dengan baik tanpa adanya
bantuan dari berbagai pihak. Oleh karena itu penulis menyampaikan ucapan
terima kasih yang setulusnya atas bantuan yang telah diberikan kepada :
1. Prof. Dr. M. Furqon Hidayatullah, M.Pd selaku Dekan Fakultas Keguruan
dan Ilmu Pendidikan, Universitas Sebelas Maret Surakarta yang telah
memberikan izin atas penyusunan skripsi ini.
2. Sukarmin, M.Si, Ph.D selaku Ketua Jurusan Pendidikan Matematika dan Ilmu
Pendidikan Alam, yang telah menyetujui atas permohonan penyusunan
skripsi ini.
3. Dra. Bakti Mulyani, M.Si selaku Ketua Program Kimia yang telah
memberikan izin atas penyusunan skripsi ini.
4. Elfi Susanti VH, S.Si, M.Si selaku Pembimbing Akademik dan Dosen
Pembimbing I yang dengan tulus dan sabar telah memberikan bimbingan dan
pengarahannya sehingga skripsi ini dapat selesai.
5. Dra. Tri Redjeki, M.S selaku Dosen Pembimbing II yang dengan sabar telah
memberikan pengarahan dan bimbingannya sehingga skripsi ini dapat selesai.
6. Drs. Joko Sugiharto selaku Kepala Sekolah SMAN 2 Sukoharjo yang telah
memberikan izin penelitian di SMAN 2 Sukoharjo.
7. Sri Martini R., S.Pd selaku guru Kimia yang mengajar di kelas XI IPA yang
telah bersedia mengijinkan pelaksanaan penelitian di kelas tersebut.
8. Semua pihak yang belum dapat penulis sebutkan satu per satu yang telah
memberikan bantuan dalam penyusunan skripsi ini.
Penulis menyadari bahwa dalam penulisan skripsi ini masih memiliki
commit to user
xi
diharapkan untuk meningkatkan kualitas karya sejenis di masa yang akan datang.
Semoga skripsi ini dapat bermanfaat bagi perkembangan ilmu pengetahuan.
Surakarta, Januari 2012
commit to user
xii DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PENGAJUAN... ii
HALAMAN PERSETUJUAN ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN PERNYATAAN ... v
ABSTRAK ... vi
ABSTRACT... vii
HALAMAN MOTTO ... viii
HALAMAN PERSEMBAHAN ... ix
KATA PENGANTAR... x
DAFTAR ISI... xii
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
A.Latar Belakang Masalah... 1
B. Identifikasi Masalah ... 4
C.Pembatasan Masalah ... 4
D.Perumusan Masalah... 5
E. Tujuan Penelitian ... 5
F. Manfaat Penelitian... 5
BAB II KERANGKA TEORITIS DAN PENGAJUAN HIPOTESIS ... 7
A.Kajian Teori ... 7
1. Belajar Konsep ... 7
2. Prakonsepsi, Konsep, Konsepsi, dan Miskonsepsi ... 9
3. Pokok Bahasan Termokimia ... 15
B. Kerangka Berpikir ... 26
commit to user
xiii
BAB III METODOLOGI PENELITIAN... 28
A. Tempat dan Waktu Penelitian ... 28
B. Metode Penelitian ... 28
C. Sumber Data... 28
D. Teknik Pengumpulan Data ... 29
E. Populasi dan Sampel ... 30
F. Instrument Penelitian... 30
G. Teknik Analisis Data ... 34
H. Prosedur Penelitian ... 36
BAB IV HASIL PENELITIAN DAN PEMBAHASAN ... 37
A. Hasil Penelitian ... 37
B. Pembahasan... 45
BAB V KESIMPULAN, IMPLIKASI, DAN SARAN ... 53
A. Kesimpulan ... 53
B. Implikasi ... 53
C. Saran ... 54
DAFTAR PUSTAKA ... 55
commit to user
1 BAB I PENDAHULUAN
A. Latar Belakang Masalah
Pendidikan merupakan salah satu faktor yang penting dalam kehidupan
manusia. Pendidikan yang berkualitas akan menghasilkan manusia-manusia yang
memiliki kemampuan berpikir kritis, kreatif, bersikap terbuka, dan memiliki
keterampilan. Dalam pelaksanaannya, kegiatan pendidikan banyak menghadapi
hambatan baik yang bersifat internal maupun eksternal. Di Indonesia, kualitas
pendidikan masih tergolong rendah. Oleh karena itu, pemerintah telah berupaya
untuk memperbaiki kualitas pendidikan Indonesia, antara lain dengan
mengeluarkan kebijaksanaan yang mengatur, membina, dan mengembangkan
pendidikan nasional yang disesuaikan dengan kebutuhan dan tuntutan
perkembangan pembangunan pendidikan nasional.
Salah satu faktor yang mempengaruhi kualitas pendidikan adalah proses
belajar mengajar dalam kelas. Pada proses belajar mengajar, terjadi interaksi
khusus antara guru dan siswa karena siswa menghadapi tugas belajar dan guru
mendampingi siswa dalam belajar. Tiap siswa memiliki kepribadian yang khas
yang dibentuk oleh dirinya melalui lingkungan keluarga dan masyarakatnya.
Guru memiliki tugas yang berat karena harus memperhatikan segala jenis siswa
dengan berbagai sifatnya. Keadaan yang ideal bila guru sebagai pendidik
mengetahui dan mengenal tiap jenis siswa sehingga dapat membantunya untuk
membangkitkan perhatian dan motivasi serta meningkatkan kemampuan belajar.
Salah satu aspek dalam proses belajar adalah belajar konsep. Belajar adalah
suatu aktivitas mental/psikis yang berlangsung dalam interaksi aktif dengan
lingkungan yang menghasilkan perubahan-perubahan dalam pengetahuan,
pemahaman, keterampilan, dan nilai sikap (Winkel, 2005:36). Menurut Ausubel
dalam Ratna Wilis Dahar (1989:81) konsep-konsep diperoleh dengan dua cara
yaitu formasi konsep dan asimilasi konsep. Oleh sebab itu, belajar merupakan
commit to user
hanya meniru atau merefleksikan apa yang diajarkan atau apa yang ia baca
melainkan menciptakan pengertian.
Pembentukan konsep merupakan proses induktif (Ratna Wilis Dahar,
1989:81). Jika anak dihadapkan dengan stimulus-stimulus dari lingkungannya, ia
akan mengabstraksi sifat-sifat atau atribut-atribut tertentu yang sama dari berbagai
stimulus-stimulus tersebut. Fakta menunjukkan bahwa otak siswa sudah terisi
pengetahuan yang berhubungan dengan pelajaran yang didapat dari pengalaman.
Dengan demikian siswa telah membentuk suatu intuisi dan “teori siswa” yang
belum tentu benar. Intuisi ini membentuk suatu prakonsepsi dari yang sederhana
sampai kompleks, cukup logis, dan konsisten serta sulit diubah. Prakonsepsi yang
dibawa siswa dapat sesuai dengan konsep ilmiah tetapi terkadang berbeda dengan
konsep ilmiah. Biasanya prakonsepsi ini kurang lengkap atau kurang sempurna
sehingga perlu dikembangkan dan dibenahi dalam pelajaran formal di sekolah.
Tidak jarang bahwa konsep awal ini meskipun berbeda dengan konsep ilmiah
dapat bertahan lama dan sulit diperbaiki atau diubah selama pendidikan formal.
Hal ini disebabkan konsep yang salah ini mampu menjelaskan persoalan yang
terjadi di lingkungan mereka. Konsep awal yang tidak sesuai dengan konsep
ilmiah inilah yang biasanya disebut miskonsepsi atau salah konsep.
Miskonsepsi terjadi jika pemahaman siswa terhadap suatu konsep berbeda
dengan apa yang dimaksud oleh masyarakat ilmiah atau konsepsi ilmuwan.
Selain prakonsepsi yang salah dan metode pengajaran yang kurang tepat seperti
yang telah disebutkan, miskonsepsi juga dapat terjadi karena pemakaian buku teks
yang kurang tepat, pengetahuan guru yang kurang memadai, dan keterbatasan kata
atau bahasa yang digunakan oleh guru.
Mata pelajaran kimia merupakan bagian dari IPA yang mempelajari tentang
sifat, struktur materi, komposisi materi, perubahan materi, serta energi yang
menyertai perubahan materi secara umum yang diperoleh melalui hasil-hasil
eksperimen dan penalaran (Depdiknas, 2003:2). Taber dalam Ghassan Sirhan
(2007:2) menyebutkan bahwa kurikulum kimia biasanya menyertakan banyak
konsep-konsep abstrak, yang berpusat pada pembelajaran lebih lanjut pada baik
commit to user
dipelajari saling mempunyai keterkaitan dan hubungan yang tidak dapat berdiri
sendiri antara konsep yang satu dengan konsep yang lain. Di dalam materi
termokimia terdapat banyak konsep ilmu yang terkait dengan konsep-konsep pada
materi yang sebelumnya. Konsep ilmu tersebut membutuhkan pemahaman yang
tinggi sehingga besar kemungkinan terjadinya miskonsepsi dalam bentuk konsep
klasifikasional, korelasional, atau teoritik.
Berdasarkan data yang diperoleh dari daftar nilai pengetahuan dan
pemahaman konsep SMAN 2 Sukoharjo kelas XI IA.2 tahun ajaran 2006/2007
dan 2007/2008, hasil belajar pada bidang studi kimia SMAN 2 Sukoharjo rata-rata
masih rendah. Pada tahun pelajaran 2006/2007 rata-rata nilai semester untuk mata
pelajaran kimia 64,00 sedangkan pada tahun pelajaran 2007/2008 menjadi 65,03.
Berdasarkan penelitian pendahuluan yang dilakukan oleh Rosilasari (2001:43),
rendahnya hasil belajar siswa secara umum dapat terjadi oleh beberapa hal antara
lain, (1) pemahaman siswa terhadap suatu masalah belum tuntas, akibatnya
konsep-konsep yang dimaksud belum dipahami, (2) terjadinya miskonsepsi
terhadap konsep-konsep esensial yang mengganggu pemahaman siswa terhadap
konsep tertentu, (3) rendahnya kualitas pembelajaran di kelas akibat dari
rendahnya mutu guru baik dari segi penguasaan materi maupun dari segi
metodologinya.
Proses belajar mengajar yang banyak dijumpai di SMAN 2 Sukoharjo
adalah dengan menggunakan metode ceramah. Melalui metode ceramah, siswa
akan banyak memiliki pengetahuan tetapi tidak terlatih untuk menemukan
pengetahuan baru, untuk menemukan konsep, dan mengembangkan ilmu
pengetahuan (Conny Semiawan dkk, 2008:24). Guru menyampaikan informasi
berupa fakta-fakta pada siswa yang merupakan proses transfer konsep dari guru ke
siswa melalui ceramah. Terkadang siswa salah menafsirkan maksud penjelasan
dari guru. Sering juga pada siswa terjadi ketidakpastian pada tahap pengumpulan
dan pemrosesan banyak data, mempertimbangkan cara pemecahan lain yang
mungkin, dan akhirnya menentukan pilihan. Jika hal ini terus terjadi, akan terjadi
commit to user
Dengan memperhatikan hal tersebut, perlu adanya penelitian untuk
menganalisis apakah telah terjadi miskonsepsi pada siswa SMAN 2 Sukoharjo dan
untuk mengetahui penyebab miskonsepsi jika benar telah terjadi miskonsepsi.
B. Identifikasi Masalah
Dari latar belakang masalah yang telah diuraikan, terdapat beberapa masalah
yang berkaitan dengan proses belajar mengajar dan hasilnya. Permasalahan yang
berkaitan dengan konsep termokimia pada penelitian ini adalah:
1. Apakah telah terjadi miskonsepsi kimia pada pembelajaran termokimia siswa
SMAN 2 Sukoharjo.
2. Bentuk miskonsepsi kimia apa yang terjadi pada siswa SMAN 2 Sukoharjo.
3. Apa yang menjadi penyebab terjadinya miskonsepsi kimia pada pembelajaran
termokimia siswa SMAN 2 Sukoharjo.
C. Pembatasan Masalah
Penelitian harus mempunyai arah yang jelas dan pasti, sehingga perlu
diberikan batasan masalah. Berdasarkan latar belakang masalah dan identifikasi
masalah, maka pengkajian dan pembatasan masalah dititikberatkan pada :
1. Sampel penelitian
Siswa yang digunakan sebagai sampel adalah siswa kelas XI SMAN 2
Sukoharjo Tahun Ajaran 2008/2009.
2. Materi pelajaran
Materi pokok termokimia mempunyai konsep yang banyak sehingga hanya
diambil konsep-konsep yang dimungkinkan pada siswa terjadi miskonsepsi
yaitu konsep-konsep:
a. reaksi eksoterm dan endoterm
b. perubahan entalpi
c. energi ikatan
d. perubahan entalpi penguraian
e. hukum Hess
commit to user
3. Dasar penggolongan miskonsepsi
Dasar penggolongan miskonsepsi yang digunakan adalah pembagian
miskonsepsi menurut bentuk konsepnya. Bentuk konsep yang dimaksud
adalah klasifikasional, korelasional, dan teoritik.
4. Penyebab terjadinya miskonsepsi
Penyebab terjadinya miskonsepsi di sini dibatasi pada kondisi siswa, interaksi
antara guru dan siswa, penggunaan buku pegangan, serta pemberian metode
pembelajaran.
D. Perumusan Masalah
Dari masalah yang timbul, dapat dirumuskan sebagai berikut:
1. Apakah terjadi miskonsepsi kimia pada pembelajaran termokimia siswa
SMAN 2 Sukoharjo?
2. Bagaimanakah bentuk miskonsepsi kimia yang dialami oleh siswa SMAN 2
Sukoharjo?
3. Apakah penyebab terjadinya miskonsepsi kimia pada pembelajaran
termokimia siswa SMAN 2 Sukoharjo?
E. Tujuan Penelitian Penelitian ini bertujuan untuk mengetahui :
1. Terjadi atau tidaknya miskonsepsi kimia dalam pembelajaran termokimia
siswa SMAN 2 Sukoharjo.
2. Bentuk miskonsepsi kimia yang terjadi pada siswa SMAN 2 Sukoharjo.
3. Hal-hal yang menyebabkan terjadinya miskonsepsi kimia pada pembelajaran
termokimia siswa SMAN 2 Sukoharjo.
F. Manfaat Penelitian Hasil penelitian ini diharapkan bermanfaat:
1. Memberikan sumbangan pemikiran bagi guru kimia di SMAN 2 Sukoharjo
commit to user
terjadi miskonsepsi kimia pada pembelajaran termokimia siswa yang dapat
menghambat kelancaran proses belajar.
2. Sebagai bahan acuan dalam penelitian lebih lanjut, sehingga dapat
memberikan sumbangan bagi upaya peningkatan mutu pendidikan khususnya
pendidikan kimia.
3. Sebagai wacana untuk menentukan strategi pembelajaran yang tepat agar
dalam proses pembelajaran tidak terjadi miskonsepsi atau meminimalkan
commit to user
7 BAB II
KERANGKA TEORITIS DAN PENGAJUAN HIPOTESIS
A. Kajian Teori 1. Belajar Konsep
Seringkali siswa dalam kegiatan belajar hanya menghafal suatu konsep
tanpa memperhatikan hubungan dengan konsep sebelumnya. Hal ini
menyebabkan konsep baru tidak masuk dalam jaringan konsep yang berada dalam
kepala siswa tetapi berdiri sendiri tanpa hubungan dengan konsep yang lain.
Akibatnya konsep tersebut tidak memiliki arti sebab arti konsep berasal dari
hubungan dengan konsep lain (Berg, 1991:9).
Ratna Wilis Dahar (1989:79) menyatakan bahwa belajar konsep merupakan
hasil utama pendidikan. Konsep-konsep merupakan batu-batu pembangun
(building blocks) berpikir. Konsep-konsep merupakan dasar bagi proses-proses
mental yang lebih tinggi untuk merumuskan prinsip-prinsip dan
generalisasi-generalisasi. Untuk memecahkan masalah, seorang siswa harus mengetahui
aturan-aturan yang relevan dan aturan-aturan ini didasarkan pada konsep-konsep
yang diperolehnya.
Ausubel dalam Ratna Wilis Dahar (1989:81) berpendapat bahwa
konsep-konsep diperoleh dengan dua cara yaitu formasi konsep-konsep (concept formation) dan
asimilasi konsep (concept assimilation). Formasi konsep terutama merupakan
bentuk perolehan konsep-konsep sebelum anak-anak masuk sekolah atau bisa
disebut prakonsepsi (prior knowledge). Menurut Gagne dalam Ratna Wilis Dahar
(1989:81), formasi konsep dapat disamakan dengan belajar konsep-konsep
konkret. Asimilasi konsep merupakan cara utama untuk memperoleh
konsep-konsep selama dan sesudah sekolah.
Teori belajar yang mendasari belajar konsep adalah teori kognitifitas dimana
proses belajar lebih penting daripada hasil belajar itu sendiri.
Pendekatan-pendekatan kognitif tentang belajar memusatkan pada proses perolehan
konsep-konsep dan pada bagaimana konsep-konsep-konsep-konsep itu disajikan dalam struktur kognitif
commit to user
Menurut Gagne dalam Ratna Wilis Dahar (1989:85), belajar konsep
merupakan satu bagian dari suatu hierarki dari delapan bentuk belajar. Dalam
hierarki ini, setiap tingkat belajar tergantung pada tingkat-tingkat sebelumnya.
Hierarki belajar tersebut adalah :
a. belajar tanda
b. belajar stimulus
c. chaining/menghubungkan
d. asosiasi verbal
e. belajar diskriminasi
f. belajar konsep konkrit
g. konsep :
1) terdefinisi
2) aturan
h. pemecahan masalah
Klausmeier dalam Ratna Wilis Dahar (1989:88) menghipotesiskan bahwa
ada empat tingkat pencapaian konsep. Tingkat-tingkat ini muncul dalam urutan
yang invarian. Orang sampai pada pencapaian tingkat tertinggi dengan kecepatan
yang berbeda-beda dan ada konsep-konsep yang tidak pernah tercapai pada
tingkat yang paling tinggi. Empat tingkat pencapaian tersebut adalah tingkat
konkret, tingkat identitas, tingkat klasifikatori, dan tingkat formal.
Piaget dalam Ratna Wilis Dahar (1989:150-151) menyatakan bahwa
perkembangan intelektual didasarkan pada dua fungsi yaitu organisasi dan
adaptasi. Organisasi memberikan pada manusia kemampuan untuk
mensistematikkan atau mengorganisasi proses-proses fisik atau proses-proses
psikologis menjadi sistem-sistem yang teratur dan berhubungan atau
struktur-struktur. Adaptasi memberikan kemampuan pada manusia untuk menyesuaikan
diri dengan lingkungan mereka. Cara adaptasi ini berbeda untuk tiap manusia.
Adaptasi terhadap lingkungan dilakukan melalui dua proses yaitu asimilasi dan
akomodasi. Dalam proses asimilasi, seseorang menggunakan struktur atau
kemampuan yang sudah ada untuk menanggapi masalah yang dihadapi dalam
commit to user
struktur mental yang ada dalam mengadakan respons terhadap tantangan
lingkungannya. Pernyataan tersebut mengandung arti bahwa untuk menyesuaikan
stimulus yang belum diketahui sebelumnya, otak akan membentuk konsep baru
atau memodifikasi struktur konsep yang telah ada sehingga akan dapat
mengasimilasi dalam otak dan digeneralisasikan.
Menurut Euwe Van den Berg (1991:11), mengajar konsep pada siswa
diharapkan siswa dapat:
a. Mendefinisikan konsep.
b. Menjelaskan perbedaan konsep satu dengan yang lainnya.
c. Menjelaskan hubungan konsep satu dengan lainnya.
d. Menjelaskan arti konsep dalam kehidupan sehari – hari dan menerapkan
dalam memecahkan masalah dalam kehidupan sehari – hari.
Dapat disimpulkan bahwa belajar konsep adalah suatu proses aktif siswa
untuk mengartikan suatu konsep dan menghubungkannya dengan konsep-konsep
awal yang telah mereka miliki sehingga terbentuk suatu konsepsi pengetahuan
yang benar.
2. Prakonsepsi, Konsep, Konsepsi, dan Miskonsepsi a. Prakonsepsi
Banyak dari konsep-konsep yang sudah kita peroleh, berkembang
semasa kita kecil. Akan tetapi, konsep-konsep itu telah mengalami
modifikasi atau perubahan yang disebabkan oleh pengalaman-pengalaman
kita sehingga secara aktif otak pada seorang anak akan berkembang melalui
proses asimilasi dan akomodasi. Dengan isi otak semula dan
perkembangannya sejak lahir, dalam otak manusia terbentuk “prakonsepsi”
(preconception) atau sejenis “teori anak” mengenai suatu peristiwa fisika
(Euwe Van den Berg, 1991:5). Konsep-konsep ini terutama diperoleh
melalui pembentukan konsep.
Pembentukan konsep merupakan proses induktif (Ratna Wilis Dahar,
1989:81). Jika anak dihadapkan pada stimulus dari lingkungan, ia
commit to user
berbagai stimulus-stimulus. Pengertian prakonsepsi adalah konsepsi yang
dimiliki siswa sebelum pelajaran walaupun mereka sudah mendapat pelajaran
formal.
Prakonsepsi atau konsepsi awal merupakan hal yang sangat penting
untuk diperhatikan karena prakonsepsi atau konsepsi awal mempengaruhi
penerimaan konsep-konsep selanjutnya. Ketika siswa memasuki kelas atau
laboratorium untuk mempelajari ilmu pengetahuan, mereka tidak memiliki
pemikiran yang sepenuhnya kosong. Mereka memilki sebentuk
“perpustakaan” pengetahuan meskipun kurang sempurna, kurang lengkap,
atau terkadang cacat untuk diperhalus dan atau digabungkan (Rhoda D.
Beskeni dkk, 2011:607). Suatu pemahaman bagaimana cara siswa belajar
dapat membantu para guru untuk merencanakan strategi mengajar yang
efektif (Ghassan Sirhan, 2007:2).
b. Konsep
Setiap objek di lingkungan kita memiliki bentuk, ukuran, dan ciri-ciri
berlainan yang menghasilkan suatu konsep tertentu. Misalkan konsep yang
sederhana yaitu “meja” merupakan benda yang berbentuk persegi panjang,
bundar, segitiga. Kata meja merupakan abstraksi yang mempunyai kesamaan
pada semua meja. Kesamaan itulah yang ditunjukkan dengan simbol oleh
manusia sehingga membentuk suatu konsep.
Menurut Rosser dalam Ratna Willis Dahar (1989:80), konsep adalah
suatu abstraksi yang mewakili satu kelas objek-objek, kejadian- kejadian,
kegiatan-kegiatan, atau hubungan-hubungan yang mempunyai atribut-atribut
yang sama. Karena orang mengalami stimulus-stimulus yang berbeda-beda,
orang membentuk konsep sesuai dengan pengelompokan stimulus-stimulus
dengan cara tertentu. Karena konsep-konsep itu adalah abstraksi-abstraksi
yang didasarkan pengalaman dan karena tidak ada dua orang yang
mempunyai pengalaman yang persis sama, konsep-konsep yang dibentuk
orang mungkin juga berbeda. Walaupun konsep-konsep kita berbeda,
konsep-konsep itu cukup serupa bagi kita untuk dapat berkomunikasi dengan
commit to user
telah kita setujui bersama. Nama-nama atau kata-kata ini adalah
simbol-simbol arbitrer digunakan untuk menyatakan konsep-konsep, yang
merupakan abstraksi internal itu. Nama-nama itu sendiri bukanlah
konsepnya.
Ratna Willis Dahar (1989:79) menyatakan bahwa konsep merupakan
penyajian-penyajian internal dari sekelompok stimulus-stimulus.
Konsep-konsep itu tidak dapat diamati, Konsep-konsep-Konsep-konsep harus disimpulkan dari
perilaku. Walaupun kita dapat memberikan suatu definisi verbal dari suatu
konsep, suatu definisi tidak mengungkapkan semua hubungan-hubungan
antara konsep itu dengan konsep-konsep yang lain.
Brunner ,seperti yang dikutip oleh Degeng (1989), memandang bahwa
suatu konsep memiliki lima unsur dan seseorang dikatakan memahami suatu
konsep apabila ia mengetahui semua unsur dari konsep itu. Kelima unsur
konsep tersebut adalah :
1). Nama
Nama adalah istilah yang diberikan pada suatu kategori.
2). Contoh-contoh
Contoh-contoh mengacu kepada suatu konsep, yang meliputi contoh
positif (meliputi contoh konsep) dan contoh negatif (contoh bukan
konsep).
3). Karakteristik
Karakteristik atau atribut mengacu pada kekhususan-kekhususan atau
ciri-ciri umum yang menyebabkan kita memasukkan contoh-contoh
dalam kategori yang sama. Dalam hal ini harus dibedakan karakteristik
pokok dengan karakteristik yang tidak pokok dari suatu konsep.
4). Rentangan karakteristik
Rentangan karakteristik mengacu kepada karakteristik-karakteristik
yang dapat diterima oleh suatu konsep sehingga dapat dipakai untuk
commit to user
5). Kaidah
Kaidah mengacu pada suatu definisi atau pernyataan yang
menspesifikasikan karakteristik-karakteristik pokok suatu konsep.
Kaidah yang jelas menyatakan hakekat dari suatu konsep dengan
menunjukkan semua karakteristik pokok.
Menurut Moh. Amien (1987:15), konsep adalah suatu ide atau gagasan
yang digeneralisasikan dari pengalaman tertentu yang relevan. Dengan
demikian untuk membentuk suatu konsep diperlukan pengalaman dan
generalisasi serta abstraksi dan ciri-ciri suatu objek untuk mempermudah
komunikasi manusia.
Setiap konsep dapat dibedakan menurut bentuknya. Menurut Moh.
Amien, konsep dapat dibedakan berdasar bentuknya menjadi tiga yaitu :
1) Konsep klasifikasional
Bentuk konsep ini didasarkan atas klasifikasi fakta-fakta ke dalam
bagan-bagan yang terorganisir. Dengan kata lain fakta tertentu
diorganisir untuk menerangkan suatu objek atau suatu gejala.
Contoh : Insekta adalah hewan berkaki enam dan tubuhnya terdiri dari
kepala, dada dan perut.
2) Konsep korelasional
Konsep ini dibentuk dari kejadian-kejadian khusus yang saling
berhubungan atau observasi-observasi yang terdiri dari dugaan. Konsep
ini terdiri dari suatu dimensi yang menyatakan adanya hubungan antara
dua variabel yang dirumuskan dengan jika … maka ….
Contoh : Apabila udara di dalam sebuah botol tertutup dipanasi, maka
tekanan udara di dalamnya akan naik.
3) Konsep teoritik
Bentuk konsep ini mempermudah penjelasan terhadap fakta atau
kejadian-kejadian dalam sistem yang terorganisir. Konsep ini
menyangkut proses pengembangan mulai dari yang diketahui sampai
commit to user
Contoh : Zat terbentuk dari partikel-partikel yang disebut atom, sebuah
atom materi terdiri dari elektron, proton, neutron dan partikel-partikel
lain.
Dari penjelasan-penjelasan yang telah dikemukakan maka dapat
disimpulkan bahwa konsep adalah gambaran mental seseorang terhadap suatu
obyek atau proses dalam bentuk jaringan pemikiran (ide) yang berguna untuk
menjelaskan segala sesuatu atau hal-hal lain yang berkaitan dengan obyek
atau proses tersebut.
c. Konsepsi
Dalam memahami konsep-konsep kimia, tidak semua siswa mempunyai
pemahaman dan penafsiran yang sama. Tafsiran perorangan dari suatu konsep
ilmu disebut dengan konsepsi (Euwe Van den Berg, 1991:10). Sedang
konsepsi menurut kamus bahasa Indonesia berarti pengertian, pendapat atau
paham. Konsepsi siswa pada konsep termokimia adalah penafsiran siswa
tentang konsep-konsep yang ada dalam termokimia. Misalnya konsep
tentang reaksi eksoterm dan endoterm, perubahan entalpi, energi ikatan,
perubahan entalpi penguraian, hukum Hess, dan perubahan entalpi
pembakaran.
d. Miskonsepsi
Miskonsepsi adalah suatu konsep yang tidak sesuai dengan pengertian
ilmiah atau pengertian yang diterima pakar dalam bidang itu (Paul Suparno,
2008:4). Miskonsepsi adalah konsepsi siswa yang berbeda atau bertentangan
dengan konsepsi para ahli dan biasanya miskonsepsi menyangkut kesalahan
siswa dalam pemahaman hubungan antar konsep (Van den Berg, 1991: 10).
Dari pendapat tentang miskonsepsi tersebut, dapat diambil kesimpulan
bahwa miskonsepsi adalah perbedaan pemahaman yang dimaksud masyarakat
ilmiah atau para ilmuwan, yang sangat dipengaruhi oleh prakonsepsi yang ada
pada diri siswa sebelum mendapatkan materi pelajarran. Dapat dikatakan
pula bahwa miskonsepsi terjadi dalam menghubungkan konsep dengan
konsep-konsep yang lain, antara konsep baru dengan konsep yang sudah ada
commit to user
Pada suatu proses belajar mengajar, sering ditemui suatu masalah yang
dapat menghambat tercapainya indikator yang telah ditentukan. Salah satu
penghambat tersebut yaitu terjadinya miskonsepsi pada siswa. Menurut Paul
Suparno (2008:29), secara garis besar penyebab miskonsepsi dapat diringkas
dalam lima kelompok yaitu siswa, guru, buku teks, konteks, dan metode
mengajar.
Penyebab yang berasal dari siswa dapat terdiri dari berbagai hal, seperti
prakonsepsi, kemampuan, tahap perkembangan, minat, cara berpikir, dan
teman lain. Penyebab kesalahan dari guru dapat berupa ketidakmampuan
guru, kurangnya penguasaan bahan, cara mengajar yang tidak tepat, atau
sikap guru dalam berelasi dengan siswa yang kurang baik. Penyebab
miskonsepsi dari buku teks biasanya terdapat pada penjelasan atau uraian
yang salah dalam buku tersebut. Konteks, seperti budaya, agama, dan bahasa
sehari-hari juga mempengaruhi miskonsepsi siswa. Sedangkan metode
mengajar yang hanya menekankan satu segi sering memunculkan salah
pengertian pada siswa.
Abraham dan kawan-kawan (1992), membagi derajat pemahaman
konsep menjadi tiga kelompok yaitu derajat memahami konsep, miskonsepsi,
dan tidak memahami konsep. Pengelompokan ini berdasar pada
pengelompokan derajat pemahaman yang telah dilakukan oleh Marek (1986)
dan dikutip oleh Abraham (1992) seperti terlihat dalam Tabel 1.
Miskonsepsi dapat diidentifikasi dengan tes diagnostik. Dari tes
diagnostik, kemampuan siswa dalam mengerjakan soal dapat diketahui dan
disimpulkan dari jawaban-jawaban soal tersebut. Tes objektif beralasan
adalah salah satu cara tes diagnostik yang digunakan untuk mengidentifikasi
miskonsepsi. Dengan tes objektif beralasan maka suatu item dapat dikontrol
dengan item yang lain, di mana keduanya mempersoalkan hal yang sama.
Siswa dianggap menguasai apabila bisa mengerjakan kedua item itu dengan
commit to user
Tabel 1. Kategori Derajat Pemahaman Siswa menurut Marek
No. Derajat
b. Menjawab tak berhubungan
dengan pertanyaan
c. Jawaban tidak jelas
Tidak
memahami
3. Miskonsepsi a. Menjawab namun penjelasan
tidak benar atau tidak logis
Sumber : Abraham, Grzybowski, Renner, Marek, 1992:112
3. Pokok Bahasan Termokimia
Termokimia merupakan bagian dari ilmu kimia yang mempelajari
perubahan kalor suatu zat yang menyertai suatu reaksi. Secara operasional,
termokimia berkaitan dengan pengukuran dan penafsiran perubahan kalor yang
menyertai reaksi kimia, perubahan keadaan, dan pembentukan larutan.
Termokimia merupakan pengetahuan dasar yang perlu dipelajari bukan saja untuk
commit to user
reaksi-reaksi kimia, tetapi juga perlu sebagai pengetahuan dasar untuk pengkajian
teori ikatan kimia dan struktur (Keenan, 1984 : 473).
a. Hukum kekekalan energi dalam sistem dan lingkungan
Setiap materi memiliki energi. Energi biasanya dinyatakan sebagai
kapasitas atau kemampuan untuk melakukan kerja, yang dimiliki oleh suatu
zat dan dapat menyebabkan terjadinya suatu proses. Salah satu bagian kimia
yang berkaitan dengan energi adalah termodinamika. Hukum termodinamika
pertama pada dasarnya adalah hukum kekekalan energi yang menyatakan
bahwa pada perubahan fisika dan kimia, energi tidak dapat diciptakan atau
dimusnahkan tetapi dapat diubah dari suatu bentuk ke bentuk yang lain.
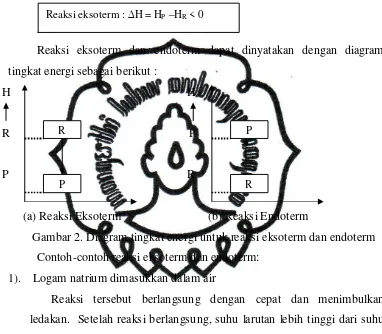
Pada pembahasan termodinamika dan termokimia dikenal istilah sistem
dan lingkungan. Sistem adalah zat atau proses yang sedang dipelajari
perubahan energinya sedangkan segala sesuatu di luar sistem dengan apa
sistem mengadakan pertukaran energi disebut lingkungan. Misalnya, kita
mereaksikan zat A dan zat B di dalam sebuah tabung reaksi. Lingkungannya
adalah tabung reaksi serta udara yang berada di luar tabung reaksi, sedangkan
sistemnya adalah zat A dan zat B.
(a) lingkungan (b)
Gambar 1. Proses reaksi : (a). eksoterm dan (b) endoterm
Energi yang dikandung oleh suatu zat atau materi dapat digolongkan
ke dalam energi kinetik atau energi potensial. Energi kinetik adalah energi
yang dimiliki suatu benda apabila benda itu bergerak seperti molekul-molekul
commit to user
potensial. Energi total yang dimiliki suatu benda adalah jumlah energi kinetik
dan energi potensial.
Jika kita tinjau suatu zat yang dalam keadaan diam (tidak bergerak),
maka zat tersebut hanya memiliki energi potensial, yaitu energi yang
tersimpan dalam zat yang disebut energi dalam (internal energy) dan
disimbolkan dangan U. Dapat dikatakan bahwa energi dalam (U) adalah
energi total dari suatu zat dalam keadaan diam pada keadaan tertentu. Energi
dalam suatu zat atau sistem dapat berubah jika zat atau sistem itu menyerap
atau membebaskan kalor. Jika suatu zat atau sistem menyerap kalor maka
energi dalamnya akan bertambah. Pertambahan energi dalam ini
menyebabkan kenaikan suhu. Sebaliknya, jika suatu zat atau sistem
membebaskan kalor maka energi dalamnya akan menurun. Penurunan energi
dalam menebabkan penurunan suhu. Energi dalam suatu zat juga dapat
berubah jika zat itu melakukan atau menerima kerja. Jika zat melakukan
kerja, maka energi dalamnya akan berkurang walaupun zat itu tidak melepas
kalor. Sebaliknya jika zat atau sistem menerima kerja maka energi dalam
sistem bertambah. Harga mutlak dari energi dalam tidak dapat ditentukan
tetapi perubahan energi dalam (∆U) dapat ditentukan dengan menggunakan
hukum pertama termodinamika yaitu : ∆U = q – w
Keterangan:
∆U : perubahan energi dalam sistem
q : kalor yang dilepaskan atau diserap sistem, bernilai positif jika
sistem menyerap kalor dan bernilai negatif jika sistem
melepaskan kalor
w : kerja yang dilakukan atau diterima sistem, bernilai positif jika
sistem melakukan kerja dan bernilai negatif jika sistem
menerima kerja
commit to user
b. Entalpi (H) dan perubahan entalpi (DH)
Entalpi (H) sistem adalah jumlah energi sistem dalam segala bentuk
yaitu energi dalam (U) dan kerja (w). Hal ini dapat dituliskan H = U + w.
Harga entalpi suatu zat atau sistem tidak dapat diukur atau dihitung, yang
dapat ditentukan adalah perubahan entalpinya. Perubahan entalpi atau kalor
yang terjadi selama proses penerimaan atau pelepasan kalor dinyatakan
dengan DH. Besarnya perubahan entalpi adalah sama dengan selisih jumlah
entalpi hasil reaksi dan jumlah entalpi pereaksi.
Untuk reaksi : R à P
dengan HR = entalpi pereaksi (R)
HP = entalpi produk (P)
Apabila reaksi berlangsung pada tekanan tetap dan jenis kerja yang
menyertainya hanya kerja ekspansi, maka perubahan entalpi reaksi sama
dengan jumlah kalor yang diserap atau dibebaskan :
DH = U + w = (qp – w) + w = qp
qp = kalor reaksi pada tekanan tetap.
Karena reaksi-reaksi kimia umumnya berlangsung pada tekanan tetap
maka kalor reaksi selalu dituliskan sebagai perubahan entalpi. Jadi, jika suatu
sistem membebaskan kalor sebesar q kJ pada tekanan tetap maka entalpi
sistem berkurang sebesar q kJ. Sebaliknya jika sistem menyerap kalor sebesar
q kJ pada tekanan tetap maka entalpi sistem bertambah sebesar q kJ.
(Parning dkk, 2006:48)
c. Reaksi eksoterm dan endoterm
Reaksi kimia dapat melepaskan atau menyerap kalor. Reaksi kimia
dengan sistem melepaskan kalor ke lingkungan disebut reaksi eksoterm
sedangkan reaksi kimia dengan sistem menyerap kalor disebut reaksi
endoterm. Pada reaksi endoterm entalpi sistem bertambah, artinya entalpi
produk (HP) lebih besar daripada entalpi pereaksi (HR). Oleh karena itu,
perubahan entalpinya bertanda positif.
commit to user
Sebaliknya pada reaksi eksoterm, entalpi sistem berkurang, artinya
entalpi produk (HP) lebih kecil daripada entalpi pereaksi (HR). Oleh karena
itu, perubahan entalpinya bertanda negatif.
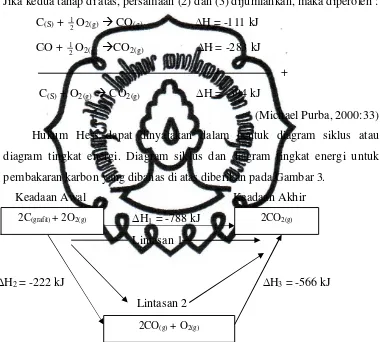
Reaksi eksoterm dan endoterm dapat dinyatakan dengan diagram
tingkat energi sebagai berikut :
H H
R P
P R
(a) Reaksi Eksoterm (b) Reaksi Endoterm
Gambar 2. Diagram tingkat energi untuk reaksi eksoterm dan endoterm
Contoh-contoh reaksi eksoterm dan endoterm:
1). Logam natrium dimasukkan dalam air
Reaksi tersebut berlangsung dengan cepat dan menimbulkan
ledakan. Setelah reaksi berlangsung, suhu larutan lebih tinggi dari suhu
lingkungan sehingga otomatis kalor mengalir dari sistem ke lingkungan.
Jadi reaksi ini adalah reaksi eksoterm.
2). Pembuatan etanol dari hasil peragian glukosa
Reaksi tersebut berlangsung lambat dengan hasil sampingan berupa
gas CO2. Setelah reaksi berlangsung, suhu sistem lebih tinggi dari suhu
lingkungan sehingga kalor akan mengalir dari sistem ke lingkungan.
Reaksi ini adalah reaksi eksoterm.
Reaksi endoterm : DH = HP – HR > 0
R
P
P
R
commit to user
3). Urea dilarutkan dalam air
Reaksi ini berlangsung cepat. Setelah urea melarut, suhu sistem
lebih rendah dari suhu lingkungan sehingga kalor mengalir dari
lingkungan ke sistem. Reaksi ini adalah reaksi endoterm
4). Reaksi antara gas N2 dengan gas O2
Reaksi ini berlangsung pada suhu tinggi. Setelah reaksi berlangsung,
suhu sistem mengalami penurunan sehingga kalor mengalir dari
lingkungan ke sistem. Reaksi ini adalah reaksi endoterm.
(Parning dkk, 2006:50)
d. Jenis-jenis perubahan entalpi standar (∆H°) 1). Perubahan entalpi reaksi
Perubahan entalpi dari suatu reaksi kimia disebut perubahan entalpi
reaksi. Perubahan entalpi reaksi yang diukur pada keadaan standar (298
K, 1 atm) disebut perubahan entalpi reaksi standar, yang dinyatakan
dengan lambang DHoreaksi atau DH298. Kondisi standar bagi berbagai
DHreaksi adalah 298 K dan 1 atm. Satuan DH adalah kJ dan satuan DH
molar reaksi adalah kJ/mol.
2). Perubahan entalpi pembentukan
Perubahan entalpi pada pembentukan 1 mol suatu zat langsung dari
unsur-unsurnya dalam bentuk standar yang diukur pada 298 K dan 1 atm
disebut perubahan entalpi pembentukan standar (∆H°f). Dari pengertian
tersebut, entalpi pembentukan standar dari CO2(g) sebesar –393 kJ/mol
berarti pada pembentukan 1 mol CO2 dari unsur C dan O2 dilepaskan
kalor sebesar 393 kJ. Persamaan termokimianya adalah :
C(s) + O2(g) → CO2(g) ; ∆H°f = –393 kJ/mol
3). Perubahan entalpi penguraian
Reaksi penguraian adalah kebalikan dari reaksi pembentukan.
Entalpi suatu reaksi sama dengan entalpi reaksi kebalikannya, tetapi
tandanya menjadi berlawanan. Jadi, perubahan entalpi penguraian standar
(∆H°d) adalah perubahan entalpi dari suatu reaksi penguraian 1 mol zat
commit to user
ΔHfº H2O(l) = -286 kJ/mol maka entalpi penguraian H2O(l) menjadi gas
hidrogen dan gas oksigen adalah +286 kJ/mol, persamaan termokimianya
adalah sebagai berikut :
H2O(l) → H2(g) + ½O2(g) ; ∆H°d = +286 kJ/mol
4). Perubahan entalpi pembakaran
Reaksi suatu zat dengan oksigen disebut reaksi pembakaran. Zat-zat
yang mudah terbakar adalah unsur karbon, hidrogen, belerang atau
senyawa-senyawa dari unsur-unsur tersebut. Perubahan entalpi pada
pembakaran sempurna 1 mol suatu zat yang diukur pada 298 K dan 1 atm
disebut perubahan entalpi pembakaran standar (∆H°c). Misalkan ∆H°c
dari metana adalah –802 kJ/mol, maka persamaan termokimianya adalah
sebagai berikut :
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) ; ∆H°c = –802 kJ/mol
(Parning dkk, 2006:56-60)
e. Kalorimeter
Pengukuran jumlah kalor yang dilepaskan pada suatu reaksi kimia
disebut kalorimetri. Sedangkan alat yang digunakan untuk mengukur
perubahan entalpi suatu reaksi disebut kalorimeter. Banyaknya kalor yang
dibebaskan ataupun diserap diperoleh dengan menaruh suatu kuantitas yang
ditimbang dari pereaksi-pereaksi dalam wadah, membiarkan reaksi
berlangsung, dan kemudian mencatat perubahan temperatur dalam air di
sekitarnya. Dari bobot bahan-bahan yang terlibat (air, hasil reaksi, dan
kalorimeter), perubahan temperaturnya, dan kapasitas panas, maka banyaknya
perubahan kalor selama reaksi dapat dihitung (Keenan, 1984:475).
Jumlah kalor yang diperlukan untuk menaikkan suhu 1 gram zat
sebesar 1oC atau 1 K disebut kalor jenis. Kalor jenis dinyatakan dalam joule
per gram per derajat Celcius (J g-1 oC-1) atau joule per gram Kelvin (J g-1 k-1).
Secara umum berlaku rumus :
dengan :
q = jumlah kalor (dalam joule)
commit to user
m = massa zat (dalam gram)
c = kalor jenis
Dt = perubahan suhu (takhir – tawal)
Jumlah kalor yang diperlukan oleh suatu zat atau suatu sistem untuk
menaikkan suhu 1oC atau 1 K disebut kapasitas kalor (C). Kapasitas kalor
dinyatakan dalam joule per derajat celcius (J oC-1) atau dalam joule per
Kelvin (JK-1). Apabila kapasitas kalor diketahui, maka rumus menjadi sebagai
berikut :
Dengan :
q = jumlah kalor
C = kapasitas kalor
Dt = perubahan suhu (takhir – tawal)
(Michael Purba, 2000:28-29)
f. Hukum Hess atau hukum penjumlahan kalor
Berdasarkan hasil percobaan German H. Hess ,orang Swiss-Rusia,
tentang kalor reaksi menyatakan bahwa apabila suatu reaksi dapat dinyatakan
sebagai penjumlahan aljabar dari dua atau lebih reaksi, maka kalor reaksi juga
merupakan penjumlahan aljabar dari kalor yang menyertai reaksi-reaksi itu.
Hukum Hess pada dasarnya merupakan bagian dari hukum
termodinamika pertama atau hukum kekekalan energi yang berkaitan dengan
reaksi kimia. Hukum ini menyatakan bahwa kalor reaksi yang dilepaskan atau
diserap oleh suatu reaksi tidak bergantung dari kondisi zat-zat yang bereaksi
dan zat-zat hasil reaksi. Salah satu contoh adalah pembakaran karbon (grafit).
Jika karbon dibakar dengan oksigen berlebihan terbentuklah karbondioksida
menurut persamaan :
C(S) + O2(g)à CO2(g) DH = -394 kJ.………(1)
Reaksi diatas dapat dilangsungkan menurut dua tahap. Mula-mula
karbon dibakar dengan oksigen yang terbatas sehingga membentuk karbon
commit to user
monoksida. Selanjutnya, karbon monoksida itu dibakar lagi untuk
membentuk karbon dioksida.
Persamaan termokimia untuk kedua reaksi yang terakhir ini adalah :
C(S) + 21O2(g)à CO(g) DH = -111 kJ...(2)
CO + 21O
2(g) àCO2(g) DH = -283 kJ………....……(3)
Jika kedua tahap di atas, persamaan (2) dan (3) dijumlahkan, maka diperoleh :
C(S) + 21O2(g)à CO(g) DH = -111 kJ
CO + 21O
2(g) àCO2(g) DH = -283 kJ
+
C(S) + O2(g)à CO2(g) DH = -394 kJ
(Michael Purba, 2000:33)
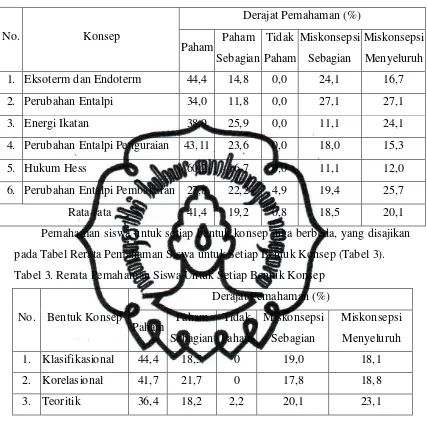
Hukum Hess dapat dinyatakan dalam bentuk diagram siklus atau
diagram tingkat energi. Diagram siklus dan diagram tingkat energi untuk
pembakaran karbon yang dibahas di atas diberikan pada Gambar 3.
Keadaan Awal Keadaan Akhir
DH1 = -788 kJ
Lintasan 1
DH2 = -222 kJ DH3 = -566 kJ
Lintasan 2
Gambar 3. Diagram siklus reaksi pembakaran grafit
Diagram siklus pembakaran grafit diatas menurut 2 lintasan. Lintasan 1
langsung membentuk CO2, lintasan 2 mula-mula membentuk CO, kemudian
CO2. Jadi DH1 = DH2 + DH3.
2C(grafit) + 2O2(g) 2CO2(g)
commit to user
Dengan hukum Hess, kalor reaksi dapat ditentukan secara tidak
langsung, artinya tidak melalui eksperimen. Penentuan kalor reaksi dapat
dilakukan melalui dua cara :
1). Berdasarkan kalor reaksi dari beberapa reaksi yang berhubungan.
Dalam hal ini reaksi-reaksi yang diketahui kalor reaksinya disusun
sedemikian rupa sehingga penjumlahannya sama dengan reaksi yang
diselidiki.
Jika diketahui :
(1) S(s) + O2(g)à SO2(g) DH = -296,8 kJ
(2) 2SO2(g) + O2(g)à 2SO3(g) DH = -197,8 kJ
Untuk menentukan perubahan entalpi dari reaksi :
S(s) +
pembentukan zat-zat pereaksi dan produknya. Dalam hal ini, zat-zat
pereaksi dianggap terlebih dahulu terurai menjadi unsur-unsurnya,
kemudian unsur-unsur itu bereaksi membentuk zat-zat produk. Secara
commit to user
g. Energi ikatan dan entalpi reaksi 1). Energi ikatan.
Reaksi kimia ada yang membebaskan kalor ada pula yang
menyerap kalor. Hal itu berhubungan dengan energi ikatan kimia dalam
zat pereaksi dan energi dalam produknya.
Atom-atom dalam molekul dipersatukan oleh suatu gaya yang
disebut ikatan kovalen. Untuk memutuskan ikatan antar atom itu
diperlukan energi. Makin kuat ikatan antar atom maka makin besar
energi yang diperlukan untuk memutuskannya.
Energi ikatan pada suatu molekul dwiatom didefinisikan sebagai
energi yang diperlukan untuk memutuskan ikatan kovalen antara dua
atom dalam 1 mol molekul berwujud gas. Energi ikatan dinyatakan
dalam satuan kilojoule per mol (kJ Mol-1) dengan lambang D.
Untuk molekul yang terdiri atas tiga atau lebih atom digunakan
pengertian energi ikatan rata-rata. Molekul yang mempunyai 2 atau lebih
ikatan, jumlah energi dari semua ikatan dalam molekul seperti itu sama
dengan entalpi standar reaksi endoterm yang digunakan untuk
memutuskan semua ikatan dalam molekulnya sehingga molekul itu
commit to user
diperlukan untuk menguraikan 1 mol molekul menjadi atom-atom
penyusunnya.
Energi ikatan antara dua atom bertambah besar, jika jumlah
pasangan elektron milik bersama bertambah banyak. Artinya ikatan
rangkap tiga lebih kuat daripada ikatan rangkap dua dan ikatan rangkap
dua lebih kuat daripada ikatan tunggal.
(Michael Purba, 2000:39)
2). Penentuan DH reaksi berdasarkan energi ikatan.
Reaksi kimia dapat dibayangkan berlangsung dalam dua tahap,
yaitu pemutusan ikatan pada pereaksi yang diikuti dengan pembentukan
ikatan pada produk. Oleh karena itu, perubahan entalpi reaksi sama
dengan jumlah energi ikatan pereaksi yang putus dikurangi dengan
jumlah energi ikatan produk yang terbentuk.
Entalpi reaksi yang dihitung berdasarkan harga entalpi pembentukan
standar.
Misalnya, entalpi reaksi pada pembakaran metana membentuk gas
karbon dioksida dan uap air, menurut persamaan reaksi berikut ini :
CH4(g) + 2O2(g)à CO2(g) + 2H2O(g)
Berdasarkan energi ikatan:
DHo = Senergi ikatan pereaksi yang putus - Senergi ikatan produk
yang terbentuk
DH = [4. DC-H + 2. DO=O] - [2. DC=O + 4. DH-O]
DH = [4(416 kJ) + 2(495 kJ)] + [2(799 kJ) + 4(463 kJ)]
DH = -796 kJ
Jadi, berdasarkan entalpi pembentukan standar adalah -803,1 kJ
mol-1. Sedangkan energi ikatan reaksi ini adalah -796 kJ mol-1.
(Michael Purba, 2000:40)
commit to user
B. Kerangka Berfikir
Dalam memahami konsep baru yang diberikan oleh guru, tidak semua siswa
mempunyai pemahaman dan penafsiran yang sama. Ada siswa yang benar-benar
memahami konsep yang diberikan guru sesuai dengan konsep para ahli, tetapi ada
juga siswa yang mengalami miskonsepsi, bahkan ada juga siswa yang sama sekali
tidak memahami konsep-konsep yang diberikan oleh guru.
Dalam materi termokimia, konsep yang terdapat di dalamnya berhubungan
dengan konsep-konsep materi sebelumnya yang diberikan oleh guru misalnya
konsep mol dan stoikiometri. Terjadinya pencampuran antara konsep-konsep yang
baru diberikan oleh guru dengan prakonsepsi yang dimiliki siswa serta adanya
hambatan-hambatan siswa seperti intelegensi, keterbatasan siswa dalam
memanfaatkan inderanya akan memungkinkan terjadinya miskonsepsi. Konsep
dalam termokimia dapat dikelompokkan dalam tiga konsep yaitu klasifikasional,
korelasional, dan teoritik. Adanya miskonsepsi pada konsep-konsep tersebut
sangat dimungkinkan sehingga penelitian miskonsepsi perlu dilakukan.
C. Pengajuan Hipotesis
Berdasarkan kajian teori dan kerangka berfikir di atas maka dapat
dirumuskan hipotesis sebagai berikut :
1. Terdapat miskonsepsi kimia pada pembelajaran termokimia siswa kelas XI
SMAN 2 Sukoharjo tahun pelajaran 2008 / 2009.
2. Miskonsepsi kimia pada pembelajaran termokimia terjadi dalam bentuk
konsep klasifikasional, korelasional dan teoritik.
3. Penyebab miskonsepsi yaitu kondisi siswa, interaksi antara guru dan siswa,
commit to user
28 BAB III
METODOLOGI PENELITIAN
A. Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di SMAN 2 Sukoharjo yang beralamat di Jalan
Raya Solo – Kartasura, Mendungan, Pabelan, Kartasura, Telp. (0271) 711615.
Penelitian dilakukan terhadap kelas XI tahun pelajaran 2008/2009 pada semester
ganjil atau semester 1 (Desember 2008).
B. Metode Penelitian
Sejalan dengan masalah dan tujuan yang ada maka penelitian ini
dilaksanakan dengan metode deskriptif kualitatif. Tujuan dari metode ini adalah
membuat gambaran atau mendeskripsikan secara faktual fakta-fakta yang
diperoleh dari subjek penelitian.
C. Sumber Data
Menurut Lofland dan Lofland dalam Moleong (2010 : 157), sumber data
utama dalam penelitian kualitatif adalah kata-kata dan tindakan dan selebihnya
adalah data tambahan seperti dokumen dan lain-lain. Kata-kata sebagai sumber
data dalam penelitian ini digali dari empat sumber sebagai berikut.
1. Peristiwa, yaitu proses belajar mengajar kimia khususnya yang terkait dengan
masalah termokimia di kelas yang menjadi tempat penelitian.
2. Hasil Tes Diagnostik, merupakan jawaban atas tes yang dirancang peneliti
untuk mengetahui pemahaman konsep termokimia dari siswa SMAN 2
Sukoharjo.
3. Informan, yaitu sejumlah siswa yang terindikasi mengalami miskonsepsi
dalam konsep termokimia, berdasarkan telaah hasil tes diagnostik.
4. Dokumen, yaitu informasi tertulis yang dapat digunakan sebagai data
tambahan terjadinya miskonsepsi pada siswa SMAN 2 Sukoharjo. Dokumen
yang dipilih adalah buku pelajaran dan LKS yang digunakan di SMA tersebut
commit to user
D. Teknik Pengumpulan Data
Sesuai dengan sumber data di atas maka dalam penelitian ini teknik
pengumpulan data yang digunakan adalah sebagai berikut :
1. Tes Diagnostik, dalam penelitian ini tes diagnostik yang digunakan adalah tes
tertulis dengan tipe multiple choice dengan alasan. Tes diagnostik dirancang
untuk mengetahui pemahaman siswa pada konsep termokimia. Tes ini
berfungsi untuk mengidentifikasi siswa yang terindikasi miskonsepsi pada
konsep termokimia, menemukan informan yang menjadi sasaran penelitian,
dan mengidentifikasi konsep-konsep mana yang menimbulkan miskonsepsi
pada siswa SMAN 2 Sukoharjo. Tes dilaksanakan setelah pokok bahasan
termokimia telah selesai diajarkan oleh guru selama kegiatan belajar
mengajar.
2. Observasi, dilakukan terhadap berlangsungnya kegiatan belajar mengajar
kimia pada pokok bahasan termokimia di kelas yang menjadi tempat
penelitian. Dalam hal ini, peneliti hadir di ruang kelas dan mengambil posisi
di belakang untuk mengetahui jalannya kegiatan belajar mengajar sambil
melakukan pencatatan yang diperlukan. Peneliti tidak berinteraksi dengan
guru atau siswa selama kegiatan belajar mengajar berlangsung.
3. Wawancara, dilakukan peneliti dengan siswa yang melalui tes diagnostik
dapat diketahui mengalami miskonsepsi pada konsep termokimia. Peranan
wawancara ini untuk dapat mengungkap latar belakang terjadinya
miskonsepsi yang terjadi. Wawancara berlangsung secara simultan dan
berkembang sesuai kebutuhan guna menemukan pola-pola umum
miskonsepsi dan penyebab terjadinya miskonsepsi.
4. Angket, diberikan peneliti untuk semua siswa yang mengalami miskonsepsi.
Peranan angket ini untuk memperkuat hasil wawancara. Angket digunakan
untuk mengungkap miskonsepsi pada siswa secara umum.
5. Analisis Dokumen, dilakukan terhadap buku pelajaran kimia dan lembar kerja
siswa (LKS) yang memuat konsep termokimia. Tujuannya adalah sebagai
informasi tambahan untuk menyimpulkan terjadinya masalah miskonsepsi
commit to user
E. Populasi dan Sampel 1. Populasi Penelitian
Populasi yang diambil dalam penelitian ini adalah siswa kelas XI SMAN 2
Sukoharjo tahun pelajaran 2008/2009 dengan jumlah seluruhnya 7 kelas.
2. Sampel Penelitian
Teknik sampling atau cuplikan yang digunakan adalah teknik non random
sampling diambil 1 kelas yaitu kelas XI IPA 2.
3. Teknik Pengambilan Sampel
Teknik pengambilan sampel dilakukan secara non random sampling.
Dalam penelitian ini diambil satu kelas sebagai sampel.
F. Instrumen Penelitian
Instrumen yang digunakan dalam penelitian ini yaitu tes diagnostik
miskonsepsi. Tes diagnostik miskonsepsi merupakan alat penelitian yang
dirancang khusus untuk mengidentifikasi miskonsepsi (Treagust, 1988:159-169).
Tes diagnostik miskonsepsi dalam penelitian ini dikembangkan oleh peneliti
dari soal-soal termokimia yang dibuat oleh guru kimia sekolah yang bersangkutan.
Tes ini terdiri atas konsep-konsep termokimia. Setiap butir soal disusun
berdasarkan proposi-proposi penting yang berkaitan dengan konsep-konsep pada
pembelajaran termokimia melalui observasi pendahuluan di lapangan.
Hasil observasi yang bersumber dari guru SMA, buku acuan, LKS, dan
soal-soal yang memuat konsep-konsep termokimia, diseleksi dan dianalisis. Temuan
letak-letak konsep yang dimungkinkan siswa mengalami miskonsepsi digunakan
sebagai acuan dalam menyusun tes diagnostik. Instrumen selanjutnya dicobakan
kepada siswa kelas XI IPA 1 SMAN 2 Sukoharjo tahun pelajaran 2008/2009.
Kemudian dilakukan uji validitas dan reliabilitas sebagai berikut :
1. Uji Validitas
Validitas adalah kualitas yang menunjukan hubungan antara suatu
pengukuran dengan tujuan kriteria belajar. Pada penelitian ini syarat validitas
yang digunakan adalah validitas isi dan validitas butir soal. Suatu tes dikatakan
commit to user
seharusnya diukur menurut tujuan kurikulum dan mencerminkan kemampuan
yang sebenarnya dari orang yang diukur (Masidjo, 2006 : 243). Validitas butir
soal dari suatu tes adalah ketepatan mengukur yang dimiliki oleh sebutir soal.
Teknik yang digunakan untuk menentukan validitas butir soal adalah
menggunakan teknik korelasi Biserial dengan rumus sebagai berikut :
Keterangan :
rpbis : koefisien korelasi biserial
Mp : rerata skor dari subyek yang menjawab betul bagi item yang dicari
validitasnya
Mt : rerata skor total
St : standar deviasi dari skor total
p : proporsi siswa yang menjawab benar
q : proporsi siswa yang menjawab salah
Kriteria pengujian
Kriteria item dinyatakan valid jika rxy > rtabel
Kriteria item dinyatakan tidak valid jika rxy ≤ rtabel
(Suharsimi Arikunto, 2007:337)
Kriteria validitas suatu tes (rxy) adalah sebagai berikut :
0,91 ─ 1,00 : Sangat Tinggi (ST)
0,71 ─ 0,90 : Tinggi (T)
0,41 ─ 0,70 : Cukup (C)
0,21 ─ 0,40 : Rendah (R)
Negatif ─ 0,20 : Sangat Rendah (SR)
(Masidjo, 2006:243)
2. Uji Reliabilitas
Reliabilitas soal menunjukan tingkat keterandalan soal. Suatu alat
pengukur dikatakan reliabel jika alat tersebut menghasilkan hasil pengukuran
yang benar-benar dapat dipercaya. Untuk menghitung reliabilitas tes
commit to user
n St2 - ∑pq
rtt =
n -1 St2
keterangan :
rtt = koefisien reliabilitas
n = jumlah item
S = deviasi standar
P = indeks kesukaran
q = 1 – P
(Masidjo, 2006:233)
Klasifikasi reliabilitas tes adalah sebagai berikut :
0,91 – 1,00 = sangat tinggi
0,71 – 0,90 = tinggi
0,41 – 0,70 = cukup
0,21 – 0,40 = rendah
Negatif – 0,20 = sangat rendah
(Masidjo, 2006:209)
3. Taraf Pembeda Soal Suatu Item
Taraf pembeda suatu item adalah taraf sampai di mana jumlah jawaban
benar dari siswa-siswa yang tergolong kelompok atas (pandai) berbeda dari
siswa-siswa yang tergolong kelompok bawah (kurang pandai) untuk suatu item
(Masidjo, 1995:196). Perbedaan jawaban benar dari siswa tergolong kelompok
atas dan bawah disebut Indeks Diskriminasi (ID).
Keterangan :
ID : indeks diskriminasi
KA : jumlah jawaban benar yang diperoleh
dari siswa tergolong kelompok atas
KB : jumlah jawaban benar yang diperoleh
commit to user
bawah
NKA atau NKB : jumlah siswa yang tergolong
kelompok atas atau bawah
NKA atau NKB x Skor maksimal : perbedaan jawaban benar dari
siswa-siswa yang tergolong kelompok atas
dan bawah yang seharusnya
diperoleh
(Masidjo, 2006:198)
Kualifikasi daya pembeda adalah sebagai berikut :
0,80 ─ 1,00 : Sangat Membedakan (SM)
0,60 ─ 0,79 : Lebih Membedakan (LM)
0,40 ─ 0,59 : Cukup Membedakan (CM)
0,20 ─ 0,39 : Kurang Membedakan (KM)
Negatif ─ 0,19 : Sangat Kurang Membedakan (SKM)
(Masidjo, 2006:201)
4. Taraf Kesukaran Suatu Item
Taraf kesukaran suatu item dapat diketahui dari banyaknya siswa yang
menjawab benar. Taraf kesukaran suatu item dinyatakan dalam bilangan
indeks yang disebut Indeks Kesukaran (IK), yaitu bilangan yang merupakan
hasil perbandingan antara jawaban benar yang diperoleh dengan jawaban yang
seharusnya diperoleh dari suatu item
Keterangan :
IK : indeks kesukaran
B : jumlah jawaban yang benar yang diperoleh siswa dari
suatu item
N : kelompok siswa
skor maksimal : besarnya skor yang dituntut oleh suatu jawaban benar
commit to user
N x skor maksimal : jumlah jawaban yang benar yang harus diperoleh dari
suatu item
(Masidjo, 2006:189)
Klasifikasi indeks kesukaran adalah sebagai berikut :
0,80 ─ 1,00 : Mudah Sekali (MS)
0,60 ─ 0,79 : Mudah (Md)
0,40 ─ 0,59 : Sedang/Cukup (Sd-C)
0,20 ─ 0,39 : Sukar (Sk)
Negatif ─ 0,19 : Sukar Sekali (SS)
(Masidjo, 2006:192)
G. Teknik Analisis Data
Langkah – langkah analisis data dalam penelitian ini adalah sebagai berikut:
1. Disusun tes diagnostik miskonsepsi.
2. Tes diagnostik miskonsepsi selanjutnya dikenakan pada subyek penelitian.
3. Jawaban siswa diperiksa dan dikategorikan dalam derajat memahami konsep,
miskonsepsi dan tidak memahami konsep.
Adapun pengkategorian siswa berdasar pada:
a. Jawaban siswa termasuk kategori memahami apabila jawaban benar dan
alasan yang diberikan juga benar.
b. Jawaban siswa termasuk kategori miskonsepsi sebagian apabila jawaban
siswa benar tetapi alasan salah, jawaban salah tetapi tidak memberikan
alas an, atau jawaban salah tetapi alasan benar.
c. Jawaban siswa termasuk kategori miskonsepsi menyeluruh bila jawaban
salah dan alasan yang diberikan juga salah.
d. Jawaban siswa termasuk kategori tidak memahami apabila siswa tidak
memberikan jawaban maupun alasan.
e. Jawaban siswa termasuk kategori memahami sebagian tanpa miskonsepsi
commit to user
4. Dihitung prosentase siswa yang memahami konsep untuk setiap butir soal.
% memahami = x 100 %
Dengan cara yang sama dihitung prosentase siswa yang mengalami
miskonsepsi dan siswa yang tidak memahami konsep. Setelah itu menghitung
rerata prosentase masing-masing konsep dan memasukan dalam tabel.
5. Dihitung rerata prosentase siswa yang memahami, miskonsepsi, dan yang
tidak memahami untuk masing-masing bentuk konsep dan dimasukan dalam
tabel.
6. Setelah dilakukan analisis data terhadap hasil tes diagnostik kemudian
dilakukan wawacara terhadap siswa-siswa yang mengalami miskonsespsi
untuk mengetahui sebab-sebab terjadinya mikonsepsi, dan apabila
commit to user
H. Prosedur Penelitian
Untuk memperjelas penelitian berikut digambarkan posedur penelitian yang
dilakukan :
Gambar 4. Gambaran Penelitian Miskonsepsi Siswa Observasi pendahuluan
Penyusunan tes miskonsepsi
Uji coba di SMAN 2 Sukoharjo
Instrumen penelitian yang valid
Tes miskonsepsi pada sampel
miskonsepsi tidak memahami
memahami
wawancara analisis
hipotesis hasil
analisis
kesimpulan hasil wawancara
commit to user
37 BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Hasil Penelitian 1. Data Hasil Observasi
Berdasarkan data hasil observasi selama kegiatan belajar mengajar pada
Lampiran 2, diperoleh data sebagai berikut:
1. Materi yang disampaikan dalam kegiatan belajar mengajar telah sesuai
dengan silabus.
2. Penyampaian materi oleh guru kurang sistematis. Beberapa kali guru tidak
menyampaikan sub pokok bahasan apa yang diberikan pada pertemuan
tersebut sehingga siswa mengalami kebingungan apakah materi masih berada
pada konsep yang sama atau telah berganti konsep.
3. Ada keterpaduan materi yang disampaikan pada kegiatan belajar mengajar
dengan kehidupan sehari-hari. Guru sebisa mungkin memberikan penjelasan
disertai contoh dalam kehidupan sehari-hari.
4. Metode mengajar yang digunakan oleh guru sebagian besar adalah metode
ceramah yang disertai tanya jawab.
5. Guru hanya menggunakan alat bantu ajar berupa papan tulis.
6. Pada saat kegiatan belajar mengajar, guru terlebih dahulu menjelaskan materi
pelajaran, menuliskan beberapa informasi di papan tulis kemudian
memberikan contoh soal beserta penyelesaiannya. Guru melakukan umpan
balik untuk mengetahui apakah materi yang telah disampaikan dapat
dimengerti dengan baik oleh siswa dengan cara mengajukan pertanyaan
ataupun soal untuk dikerjakan siswa di kelas. Lebih sering guru tidak
menunjuk siswa tertentu untuk menjawab pertanyaan, pertanyaan diajukan
untuk seluruh kelas. Jika ada jawaban yang kurang sempurna maka
dikerjakan dengan bimbingan guru. Guru juga memberikan kesempatan
kepada siswa yang masih belum paham untuk mengajukan pertanyaan untuk
commit to user
7. Sebagian besar siswa memperhatikan penjelasan dari guru selama kegiatan
belajar mengajar. Beberapa ada yang kurang memperhatikan tetapi tidak
mengganggu jalannya kegiatan belajar mengajar. Keadaan kelas tetap tenang.
8. Keaktifan siswa dalam bertanya kepada guru berkaitan dengan hal-hal yang
belum dimengerti kurang. Hanya beberapa siswa yang aktif mengajukan
pertanyaan terhadap hal-hal yang belum jelas yang berkaitan dengan materi
yang diajarkan selama kegiatan belajar mengajar.
9. Untuk keaktifan siswa dalam menjawab pertanyaan guru juga kurang. siswa
masih mengerjakan soal secara kurang sempurna.
10. Ketika pelajaran berakhir guru terkadang menarik kesimpulan terhadap
materi yang diajarkan pada pertemuan. Hal ini dikarenakan tidak adanya
waktu yang tersisa dalam proses belajar mengajar saat itu. Kegiatan
menyimpulkan pelajaran adalah penting karena untuk mempertegas dan
memperjelas materi yang telah dipelajari.
11. Guru jarang memberikan tugas ataupun pekerjaan rumah.
12. Pekerjaan rumah yang diberikan oleh guru, sebagian dikerjakan oleh siswa,
dan kebanyakan dari mereka tidak mengerjakan secara mandiri. Ada beberapa
siswa yang hanya mencontek saja jawaban temannya tanpa bertanya jika ada
hal yang belum dimengerti oleh siswa.
2. Data Hasil Tes Diagnostik
Berdasarkan data hasil tes diagnostik pada Lampiran 14, diperoleh bahwa derajat
pemahaman siswa untuk tiap konsep pada pokok bahasan termokimia sangat
beragam yang ditunjukkan oleh Tabel Rerata Pemahaman Siswa untuk Setiap
Konsep (Tabel 2). Dari tabel tersebut dapat dilihat bahwa miskonsepsi paling
banyak terjadi pada konsep perubahan entalpi. Kemudian pada konsep perubahan
entalpi pembakaran, konsep eksoterm dan endoterm, konsep energi ikatan, konsep
perubahan entalpi penguraian. Miskonsepsi paling sedikit terjadi pada konsep