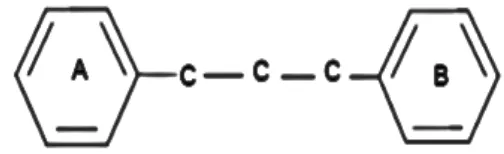BAB I
PENDAHULUAN
1.1LatarBelakang
Akibat peningkatan status sosial dan ekonomi, pelayanan kesehatan masyarakat, faktor lingkungan dan gaya yang tidak sehat, seperti makan berlebihan, berlemak, kurang akivitas fisik dan stress berperan besar sebagai pemicu diabetes. Tetapi diabetes juga bisa muncul akibat faktor keturunan. Tanaman pogun tanoh dimanadaunnya telah digunakan secara empiris dalam pengobatan diabetes oleh masyarakat Dairi (Harfina, 2012).
Keanekaragaman tumbuhan di Indonesia merupakan salah satu kekayaan alam yang perlu dilestarikan mengingat peranan dan khasiat tumbuhan dapat memberikan manfaat bagi kesehatan masyarakat. Tumbuh-tumbuhan merupakan salah satu sumber senyawa bahan alam hayati yang memegang peranan penting dalam pemanfaatan zat kimia berkhasiat. Pogun tanoh telah digunakan sebagai obat tradisional di Cina selatan sebagai pengobatan demam, infeksi herpes, kanker, dan antiinflamasi yang digunakan lebih dari 200 tahun yang lalu (Zou, et al., 2005).
Pugun tanoh merupakan tanaman berbatang basah dan berbaring (Redaksi Agromedia, 2008). Pugun tanoh tumbuh merambat. Tumbuhan pugun tanoh memiliki tinggi 40 sampai 60 cm. Batangnya bercabang-cabang, ramping, jarang dan berbulu halus.
Skrining fitokimia yang telah dilakukan menunjukkan bahwa pada ekstrak etil asetat herba pugun tanohmengandung curangin dan zat pahit (Redaksi Agromedia, 2008), flavonoid (Huang, et al., 1999), saponin (Fang, et al., 2009),tanin, glikosida (Jie, et al., 2005; Zou, et al., 2005; Zou, et al., 2004; Huang, et al., 1998) serta steroid/terpenoid (Wang, et al., 2006).
Flavonoida merupakan salah satu golongan fenol alam yang terbesar. Menurut perkiraan, kira-kira 2% dari seluruh karbon yang difotosintesis oleh tumbuhan diubah menjadi flavonoida atau senyawa yang berkaitan erat dengannya (Markham, 1988). Flavonoida adalah senyawa yang mengandung C
15terdiri atas dua inti fenolat yang dihubungkan dengan tiga satuan karbon (Sastrohamidjojo, 1985). Flavonoida yang terdapat di dalam tumbuhan dapat digunakan sebagai pelindung tubuh manusia dari radikal bebas dan dapat mengurangi resiko penyakit kanker dan peradangan (Nessa, 2003).
1.2Perumusan Masalah
Berdasarkan latar belakang di atas, maka perumusan masalah pada
penelitian ini adalah:
a. Apakah hasil karakteristik simplisia dan ekstrak etil asetat herba pugun tanoh?
b. Apa golongan senyawa kimia yang terdapat pada simplisia herba pugun tanoh? c. Apakah senyawa flavonoida yang diperoleh dari hasil isolasi dapat
diidentifikasi secara spektrofotometri UV-Visible menggunakan pereaksi geser
dan secara spektrofotometri IR?
1.3Hipotesis
Berdasarkan perumusan masalah di atas maka hipotesis pada penelitian ini
adalah:
a. Karakteristik simplisia herba pugun tanoh yang diteliti memenuhi persyaratan umum karakterisasi simplisia dan ekstrak.
b. Golongan senyawa kimia dari simplisia herba pugun tanoh dapat ditentukan dengan menggunakan prosedur skrining fitokimia pada Materia Medika Indonesia dan Farnsworth.
c. Senyawa flavonoida yang diperoleh dari hasil isolasi dapat diidentifikasi secara spektrofotometri UV-Visible menggunakan pereaksi geser dan secara FT-IR.
Adapun tujuan dari penelitian ini adalah untuk:
a. Untuk mengetahui karakteristik simplisia herba pugun tanoh yang diteliti. b. Untuk mengetahui golongan senyawa kimia yang terdapat dalam simplisia
herba pugun tanoh.
c. Untuk mengidentifikasi senyawa flavonoida yang diperoleh dari hasil isolasi secara spektrofotometri UV-Visible menggunakan pereaksi geser dan secara spektrofotometri FT-IR.
1.5Manfaat Penelitian
Manfaat penelitian ini adalah untuk memberikan informasi ilmiah tentang kandungan metabolit sekunder dan jenisflavonoida alam yang terkandung di dalamherba pugun tanohserta pengembangan flavonida dalam bidang farmasi.
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
2.1.1 Sistematika Tumbuhan
Menurut buku Curanga Amara,(2011) Sistematika tumbuhan pugun tanoh adalah sebagai berikut:
Kingdom : Plantae
Divisi : Spermatophyta Subdivisi : Angiospermae Kelas : Dicotyledoneae Ordo : Scrophulariales Famili : Scrophulariaceae Genus : Curanga
Spesies : Curanga fel-terrae (Lour.)Merr.(Anonim,2011)
2.1.2 Nama Daerah
Nama daerah dari tumbuhan ini adalah empedu taneh (Karo), pugun tanoh, pugun tana, pagon tanoh (Dairi), tamah raheut (Sunda), kukurang (Maluku) dan papaita (Ternate) (Fithra, 2013).
2.1.3 Morfologi Tumbuhan
merambat. Tumbuhan pugun tanoh memiliki tinggi 40 sampai 60 cm. Batangnya bercabang-cabang, ramping, jarang dan berbulu halus.
Tangkai daun tumbuh berhadapan, permukaan tidak berbulu, rata dan tipis. Tandan bunga bewarna merah (Agung dan Tinton, 2008), jumlah bunga 2-16, mahkota bunga bentuk tabung dan berbibir rangkap. Daunnya berbulu halus, berbentuk bundar telur dengan panjang 3-6 cm dan lebar 2-3 cm, ujung daun agak melancip dan tepi daun beringgit.
2.1.4 Kandungan Kimia Tumbuhan
Pugun tanoh mengandung curangin dan zat pahit (Agung dan Tinton, 2008), flavonoid (Huang, et al., 1999), saponin (Fang, et al., 2009), tanin, glikosida (Jie, et al., 2005; Zou, et al., 2005; Zou, et al., 2004; Huang, et al., 1998) serta steroid/terpenoid (Wang, et al., 2006).
2.1.5 Khasiat Tumbuhan
2.2 Senyawa Flavonoida
Senyawa-senyawa flavonoida adalah senyawa-senyawa polifenol yang mempunyai 15 atom karbon, terdiri dari dua cincin benzena yang dihubungkan menjadi satu oleh rantai linier yang terdiri dari tiga atom karbon. Senyawa-senyawa flavonoida adalah Senyawa-senyawa 1,3 diaril propana, Senyawa-senyawa isoflavonoida adalah senyawa 1,2 diaril propana, sedangkan senyawa-senyawa neoflavonoida adalah 1,1 diaril propana.
Istilah flavonoida diberikan pada suatu golongan besar senyawa yang berasal dari kelompok senyawa yang paling umum, yaitu senyawa flavon, suatu jembatan oksigen terdapat diantara cincin A dalam kedudukan orto, dan atom karbon benzil yang terletak disebelah cincin B. Senyawa heterosoklik ini, pada tingkat oksidasi yangberbeda terdapat dalam kebanyakan tumbuhan. Flavon adalah bentuk yang mempunyai cincin C dengan tingkat oksidasi paling rendah dan dianggap sebagai struktur induk dalam nomenklatur kelompok senyawa-senyawa ini (Markham, 1988).
2.2.1 Struktur Dasar Senyawa Flavonoida
Senyawa flavonoida mengandung C15 terdiri atas dua inti fenolat yang dihubungkan dengan tiga satuan karbon. Kerangka dasar dari struktur flavonoida adalah sistim C6-C3-C6. Struktur dasar flavonoida dapat digambarkan sebagai berikut:
Gambar 2.1 Kerangka dasar senyawa flavonoida
2.2.2 Klasifikasi Senyawa Flavonoida
Flavonoida mengandung sistem aromatik yang terkonjugasi sehingga menunjukkan pita serapan kuat pada daerah spektrum sinar ultraviolet dan spektrum sinar tampak, umumnya dalam tumbuhan terikat pada gula yang disebut dengan glikosida (Harborne, 1984). Tumbuhan yang mengandung flavonoida terdapat dalam berbagai struktur. Keragaman ini disebabkan oleh perbedaan tahap modifikasi lanjutan dari struktur dasar flavonoida tersebut, antara lain:
b. Flavonoida C-glikosida, gula terikat pada atom karbon flavonoida dan dalam hal ini gula tersebut terikat langsung pada inti benzena dengan suatu ikatankarbon-karbon yang tahan asam. Glikosida yang demikian disebut C-glikosida. Jenis gula yang terlibat ternyata jauh lebih sedikit ketimbang jenis gula pada O-glukosa, biasanya dari jenis glukosa yang paling umum, dan juga galaktosa, ramnosa, xilosa, dan arabinosa (Markham, 1988).
c. Flavonoida sulfat, senyawa ini mengandung satu ion sulfat, atau lebih, yang terikat pada hidroksil fenol atau gula. Senyawa ini sebenarnya bisulfat karena terdapat sebagai garam, yaitu flavon-O-SO3K. Banyak yang berupa glikosida bisulfat, bagian bisulfat terikat pada hidroksil fenol yang mana saja yang masih bebas atau pada gula (Markham, 1988).
d. Biflavonoida, yaitu flavonoida dimer. Flavonoida yang biasanya terlibat adalah flavon dan flavanon yang secara biosintesis mempunyai pola oksigenasi yang sederhana 5,7,4’ dan ikatan antar flavonoida berupa ikatan-ikatan karbon atau kadang-kadang eter. Monomer flavonoida yang digabungkan menjadi biflavonoida dapat berjenis sama atau berbeda, dan letak ikatannya berbeda-beda. Biflavonoida jarang ditemukan sebagai glikosida, dan penyebarannya terbatas, terdapat terutama pada gimnospermae (Markham, 1988).
Menurut Robinson (1995), flavonoida dapat dikelompokkan berdasarkan keragaman pada rantai C3 yaitu:
1. Flavonol
Flavonol paling sering terdapat sebagai glikosida, biasanya 3-glikosida, dan aglikon flavonol yang umum yaitu kamferol, kuersetin, dan mirisetin yang berkhasiat sebagaiantioksidan dan antiimflamasi. Flavonol lain yang terdapat di alam bebas kebanyakan merupakan variasi struktur sederhana dari flavonol. Larutan flavonol dalam suasana basa dioksidasi oleh udara tetapi tidak begitu cepat sehingga penggunaan basa pada pengerjaannya masih dapat dilakukan. 2. Flavon
Flavon berbeda dengan flavonol dimana pada flavon tidak terdapat gugusan 3-hidroksi. Hal ini mempunyai serapan UV-nya, gerakan kromatografi, serta reaksiwarnanya. Flavon yang paling umum dijumpai adalah apigenin danluteolin. Luteolin merupakan zat warna yang pertama kali dipakai di Eropa. Jenis yang paling umum adalah 7-glukosida dan terdapat juga flavon yang terikat pada gula melalui ikatan karbon-karbon. Contohnya luteolin 8-C-glikosida. Flavon dianggap sebagai induk dalam nomenklatur kelompok senyawa flavonoida. 3. Isoflavon
Isoflavon merupakan isomer flavon, tetapi jumlahnya sangat sedikit dan sebagai fitoaleksin yaitu senyawa pelindung yang terbentuk dalam tumbuhan
sebagai pertahanan terhadap serangan penyakit. Isoflavon sukar dicirikan karena
reaksinya tidak khas dengan pereaksi warna manapun tetapi kebanyakan tampak sebagai bercak lembayung yang pudar dengan amonia berubah menjadi coklat.
Flavanon terdistribusi luas di alam. Flavanon terdapat di dalam kayu, daun dan bunga. Flavanon glikosida merupakan konstituen utama dari tanaman genus prenus dan buah jeruk; dua glikosida yang paling lazim adalah neringenin dan hesperitin, terdapat dalam buah anggur dan jeruk.
5. Flavanonol
Senyawa ini berkhasiat sebagai antioksidan dan hanya terdapat sedikit sekali jika dibandingkan dengan flavonoida lain. Sebagian besar senyawa ini diabaikan karena konsentrasinya rendah dan tidak berwarna.
6. Katekin
Katekin terdapat pada seluruh dunia tumbuhan, terutama pada tumbuhan berkayu. Senyawa ini mudah diperoleh dalam jumlah besar dari ekstrak kental Uncaria gambir dan daun teh kering yang mengandung kira-kira 30% senyawa ini. 7. Leukoantosianidin
Leukoantosianidin merupakan senyawa tan warna, terutama terdapat pada tumbuhan berkayu. Senyawa ini jarang terdapat sebagai glikosida, contohnya melaksidin, apiferol.
8. Antosianin
Antosianin merupakan pewarna yang paling penting dan paling tersebar luas dalam tumbuhan. Pigmen yang berwarna kuat dan larut dalam air ini adalah penyebab hampir semua warna merah jambu, merah marak, ungu, dan biru dalam daun, bunga, dan buah pada tumbuhan tinggi. Secara kimia semua antosianin merupakan turunan suatu struktur aromatik tunggal yaitu sianidin, dan semuanya terbentuk dari pigmen sianidin ini dengan penambahan atau pengurangan gugus hidroksil atau dengan metilasi atau glikosilasi.
Khalkon adalah pigmen fenol kuning yang berwarna coklat kuat dengan sinar UV bila dikromatografi kertas. Aglikon khalkon dapat dibedakan dari glikosidanya, karena hanya pigmen dalam bentuk glikosida yang dapat bergerak pada kromatografi kertas dalam pengembang air (Harborne, 1984).
10. Auron
Auron berupa pigmen kuning emas yang terdapat dalam bunga tertentu dan briofita. Dalam larutan basa senyawa ini berwarna merah ros dan tampak pada kromatografi kertas berupa bercak kuning, dengan sinar ultraviolet warna kuning kuat berubah menjadi merah jingga bila diberi uap amonia (Robinson, 1995).
2.3 Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut dalam pelarut yang sesuai sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Ekstraksidengan menggunakan pelarut dapat dilakukan dengan beberapa cara yaitu :
A.Cara Dingin 1. Maserasi
Maserasi adalah proses ekstraksi simplisia dengan menggunakan pelarut dengan beberapa kali pengadukan pada temperatur ruangan (Ditjen POM RI, 2000). 2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses ini terdiri dari tahapan pengembangan bahan, tahap maserasi antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) (Ditjen POM RI, 2000).
1. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya,
selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan
adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu
pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna
(Ditjen POM RI, 2000).
2. Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang umumnya dilakukan
dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut
relatif konstan dengan adanya pendingin balik (Ditjen POM RI, 2000).
3. Digesti
Digesti adalah maserasi dengan pengadukan kontinu pada temperatur yang
lebih tinggi dari temperatur ruangan, yaitu secara umum dilakukan pada
temperatur 40-50 (Ditjen POM RI, 2000).
4. Infus
Infus adalah sediaan cair yang dibuat dengan menyari simplisia nabati
dengan air pada suhu 90selama 15 menit (Ditjen POM RI, 1979).
5. Dekok
Dekok adalah sediaan cair yang dibuat dengan menyari simplisia nabati
dengan air pada waktu yang lebih lama ± 30 menit dangan temperatur sampai titik
didih air (Ditjen POM RI, 2000).
Kromatografi adalah suatu metode pemisahan berdasarkan perbedaan perpindahan dari komponen-komponen senyawa diantara dua fase yaitu fase diam (dapat berupa zat cair atau zat padat) dan fase gerak (dapat berupa gas atau zat cair)(Ditjen POM RI,1995). Fase diam berupa zat padat maka cara tersebut dikenal sebagai kromatografi serapan, jika zat cair dikenal sebagai kromatografi partisi (Sastrohamidjojo, 1985).
2.4.1 Kromatografi lapis tipis
Kromatografi lapis tipis ialah metode pemisahan fisikokimia.Lapisan pemisah terdiri atas bahan berbutir-butir (fase diam), ditempatkan pada penyangga berupa plat gelas, logam atau lapisan yang cocok. Campuran yang akan dipisah berupa larutan yang di totolkan baik berupa bercak ataupun pita. Setelah plat atau lapisan dimasukkan ke dalam bejana tertutup rapat yang berisi larutan pengembang yang cocok (fase gerak), pemisahan terjadi selama perambatan kapiler (pengembangan)kemudian senyawa yang tidak berwarna harus ditampakkan (Stahl, 1985).
Nilai utama Kromatografi Lapis Tipis pada penelitian senyawa flavonoida ialah sebagai cara analisis cepat yang memerlukan bahan sangat sedikit. Menurut Markham, Kromatografi Lapis Tipis terutama berguna untuk tujuan berikut: 1. mencari pelarut untuk kromatografi kolom
2. analisis fraksi yang diperoleh dari kromatografi kolom 3.identifikasi flavonoida secara ko-kromatografi.
4. isolasi flavonoida murni skala kecil
5. penyerap dan pengembang yang digunakan umumnya sama denganpenyerap dan pengembang pada kromatografi kolom dan kromatografi kertas (Markham, 1988).
2.4.1.1 Fase diam (lapisan penyerap)
Fase diam pada kromatografi lapis tipis berupa lapisan tipis yang terdiri atas bahan padat yang dilapiskan pada permukaan penyangga datar yang biasanya terbuat dari kaca, dapat pula terbuat dari plat polimer atau logam. Lapisan melekat pada permukaan dengan bantuan bahan pengikat, biasanya kalsium sulfat atau amilum (pati).Penyerap yang umum dipakai untuk kromatografi lapis tipis
adalah silika gel, alumina, kieselgur, dan selulosa (Gritter, et al., 1985).
Dua sifat yang penting dari fasediam adalah ukuran partikel dan homogenitasnya, karena adhesi terhadap penyokong sangat tergantung pada kedua sifat tersebut.Ukuran partikel yang biasa digunakan adalah 1-25 mikron. Partikel yang butirannya sangat kasar tidak akan memberikan hasil yang memuaskan dan salah satu cara untuk memperbaiki hasil pemisahan adalah dengan menggunakan fase diam yang butirannya lebih halus. Butiran yang halus memberikan aliran pelarut yang lebih lambat dan resolusi yang lebih baik (Sastrohamidjojo, 1985).
Fase gerak ialah medium angkut yang terdiri atas satu atau beberapa pelarut.Jika diperlukan sistem pelarut multi komponen, harus berupa suatu
campuran sesederhana mungkin yang terdiri atas maksimum tiga komponen
(Stahl, 1985).
Pemisahan senyawa organik selalu menggunakan pelarut campur.Tujuan
menggunakan pelarut campur adalah untuk memperoleh pemisahan senyawa yang
baik. Kombinasi pelarut adalah berdasarkan atas polaritas masing-masing pelarut,
sehingga dengan demikian akan diperoleh sistem pengembang yang cocok. Pelarut pengembang yang digunakan dalam kromatografi lapis tipis antara lain:
n-heksana, karbontetraklorida, benzena, kloroform, eter, etilasetat, piridian, aseton,
etanol, metanol dan air (Gritter, et al., 1985).
2.4.1.3 Harga Rf (Retardation factor)
Proses mengidentifikasi noda-noda dalam kromatografi sangat lazim
menggunakan harga Rf (Retordation Factor) yang didefinisikan sebagai:
awal
Harga Rf beragam mulai dari 0 sampai 1. Faktor-faktor yangmempengaruhi harga
Rf (Sastrohamidjojo, 1985):
a. struktur kimia dari senyawa yang sedang dipisahkan
b. sifat Penjerap
c. tebal dan kerataan dari lapisan Penjerap
d. pelarut dan derajat kemurniannya
f. teknik percobaan
g. jumlah cuplikan yang digunakan
h. suhu
i. kesetimbangan
2.4.2 Kromatografi kolom
Kromatografi kolom adalah kromatografi yang menggunakan kolom
sebagai alat untuk memisahkan komponen dalam campuran. Alat tersebut berupa
pipa gelas yang dilengkapi suatu kran di bagian bawah kolom untuk
mengendalikan aliran zat cair. Ukuran kolom tergantung dari banyaknya zat
yang akan dipindahkan. Pemisahan tergantung kepada kesetimbangan yang
terbentuk pada bidang antar muka di antara butiran-butiran adsorben dan fase
bergerak serta kelarutan relatif komponen pada fase bergeraknya (Gritter, et al.,
1985).
Kromatografi cair yang dilakukan dalam kolom besar merupakan metode
kromatografi terbaik untuk pemisahan dalam jumlah besar (lebih dari 1 g).
Penggunaan kromatografi kolom, campuran yang akan dipisahkan diletakkan
berupa pita pada bagian atas kolom penyerap yang berada dalam tabung kaca,
tabung logam, dan tabung plastik. Pelarut atau fasa gerak dibiarkan mengalir
melalui kolom karena aliran yang disebabkan oleh gaya berat atau didorong
dengan tekanan. Pita senyawa yang larut bergerak melalui kolom dengan laju
yang berbeda, memisah, dan dikumpulkan berupa fraksi ketika keluar dari atas
Menggunakan cara ini, skala isolasi flavonoida dapat ditingkatkan hampir
ke skala industri. Secara umum cara ini meliputi penempatan campuran
flavonoida (berupa larutan) diatas kolom yang berisi serbuk penyerap (seperti
selulose, silika, atau poliamida), dilanjutkan dengan elusi beruntun setiap
komponen menggunakan pelarut yang cocok. Kolom hanya berupa tabung kaca
yang dilengkapi dengan keran pada salah satu ujung. Menempatkan larutan
cuplikan pada kolom sedemikian rupa sehingga terbentuk pita yang siap dielusi
lebih lanjut (Markham, 1988).
Pengisian kolom harus dikerjakan seragam, setelah adsorben dimasukkan
dapat diseragamkan kerapatannya dalam kolom dengan menggunakan vibrator.
Selain itu dapat juga dikerjakan dengan memasukkan adsorben dalam bentuk
larutan dan partikelnya dibiarkan mengendap. Pengisian kolom yang tidak
seragam dapat menghasilkan rongga-rongga ditengah-tengah kolom. Dibagian
bawah dan atas dari isian kolom diberi wool untuk menyangga isian. Saat kolom
telah diisi bahan isian permukaan cairan tidak boleh dibiarkan turun dibawah
permukaan bahan isian bagian atas, karena akan memberikan peluang masuknya
gelembung-gelembung udara masuk kedalam kolom (Hosttetman, 1995).
2.5 Spektrofotometri
Spektrofotometri adalah metode pengukuran dimana sumber energinya
berupa sinar atau cahaya dan sistem detektornya menggunakan sel fotolistrik
2.5.1 Spektrofotometri ultraviolet
Serapan molekul di dalam daerah ultra violet yang terlihat dari spektrum bergantung pada struktur ultra elektronik dari molekul yang disinari. Penyerapan sejumlah energi, menghasilkan percepatan dari elektron dalam orbital tingkat dasar ke orbital yang berenergi lebih tinggi di dalam keadaan tereskitasi (Silverstein, dkk., 1986).
Spektrum Flavonoida biasanya ditentukan dalam larutan dengan pelarut Metanol (MeOH) atau Etanol (EtOH). Spektrum khas terdiri atas dua maksima pada rentang 240-285 nm (pita II) dan 300-550 nm (pita I). Kedudukan yang tepat dan kekuatan nisbi maksima tersebut memberikan informasi yang berharga mengenai sifat flavonoida dan pola oksigenasinya. Ciri khas spektrum tersebut ialah kekuatan nisbi yang rendah pada pita I dalam dihidroflavon, dihidroflavonol, dan isoflavon serta kedudukan pita I pada spektrum khalkon, auron dan antosianin yang terdapat pada panjang gelombang yang tinggi (Markham, 1988).
2.5.1.1 Pereaksi geser (Shift reagen)
Kedudukan gugus hidroksi fenol bebas pada inti flavonoida dapat ditentukan dengan menambahkan pereaksi geser ke dalam larutan cuplikan dan mengamati puncak serapan yang terjadi (Markham,1988). Langkah pertama yang dilakukan dalam menafsirkan spektrum yaitu menentukan jenis flavonoida dengan memperhatikan:
1. bentuk umum spektrum dalam metanol 2. panjang gelombang pita serapan 3. data kromatografi kertas
2.5.2 Spektrofotometri inframerah
Spektrum inframerah suatu molekul adalah hasil transisi antara tingkat
energi getaran yang berlainan. Pancaran inframerah yang kerapatannya kurang
dari 100 cm-1 (panjang gelombang lebih daripada 100 µm) diserap oleh sebuah
molekul organik dan diubah menjadi putaran energi molekul. Penyerapan ini
tercantum, namun spektrum getaran terlihat bukan sebagai garis-garis melainkan
berupa pita-pita. Hal ini disebabkan perubahan energi getaran tunggal selalu
disertai sejumlah perubahan energi putara (Silverstein, dkk ., 1986).
Vibrasi molekul dapat dibagi dalam dua golongan , yaitu vibrasi regang