BAB 2
TINJAUAN PUSTAKA
2.1. Bahan Tambahan Pangan 2.1.1 Definisi
Bahan tambahan pangan adalah senyawa yang sengaja ditambahkan
kedalam makanan dengan jumlah dan ukuran tertentu dan terlibat dalam proses
pengolahan, pengemasan dan atau penyimpanan. Bahan ini berfungsi untuk
memperbaiki warna, bentuk, cita rasa, tekstur dan memperpanjang masa simpan
dan bukan merupakan bahan (ingredient) utama. Menurut Codex, bahan tambahan
pangan adalah bahan yang tidak lazim dikonsumsi sebagai makanan, yang
dicampurkan secara sengaja pada proses pengolahan makanan. Bahan ini ada yang
memiliki nilai gizi dan ada yang tidak (Saparinto, 2006).
Adapun menurut Peraturan Menteri Kesehatan No. 033 tahun 2012
Tentang Bahan Tambahan Pangan memiliki fungsi sebagai berikut :
1. Anti buih (Antifoaming Agent)
2. Anti kempal (Anticaking Agent)
3. Antioksidan (Antioxidant)
4. Bahan Pengkarbonasi (Carbonating Agent)
5. Garam Pengemulsi (Emulsifying Salt)
6. Gas Untuk Kemasan (Packaging Gas)
7. Humektan (Humectan)
8. Pelapis (Glazing Agent)
9. Pemanis (Sweetner)
10.Pembawa (Carrier)
11.Pembentuk Gel (Gelling Agent)
12.Pembuih (Foaming Agent)
13.Pengatur Keasaman (Acidity Regulator)
14.Pengawet (Preservative)
17.Pengental (Thickener)
18.Pengeras (Firming Agent)
19.Penguat Rasa (Flavour Enhancer)
20.Peningkat Volume (Bulking Agent)
21.Penstabil (Stabilizer)
22.Peretensi Warna (Colour Retention Agent)
23.Perisa (Flavouring)
24.Perlakuan Tepung (Flour Treatment Agent)
25.Pewarna (Colour)
26.Propelan (Propellant)
27.Sekuestran (Sequestrant)
Dan jenis bahan tambahan pangan dari masing-masing fungsi diatas yang
diizinkan sudah tercantum dalam Peraturan Menteri Kesehatan No 033 Tahun
2012 (Peraturan Menteri Kesehatan No 033 Tahun 2012).
Pengertian bahan tambahan pangan sebagai campuran makanan kerap kali
rancu dengan bahan tambahan kimia. Untuk menghindari itu kita harus
memahami tentang bahan tambahan pangan sebagai campuran makanan secara
terperinci (Saparinto, 2006). Pada umumnya bahan tambahan pangan dapat
digolongkan menjadi dua golongan besar, yaitu sebagai berikut :
1. Bahan tambahan pangan yang tidak sengaja ditambahkan yaitu bahan yang
tidak mempunyai fungsi dalam makanan tersebut, terdapat secara tidak
sengaja, baik dalam jumlah sedikit atau cukup banyak akibat perlakuan
selama proses produksi, pengolahan dan pengemasan. Bahan ini dapat pula
merupakan residu atau suatu kontaminan dari bahan yang sengaja
ditambahkan untuk tujuan produksi bahan mentah atau penanganannya yang
masih terus terbawa dalam makanan yang akan dikonsumsi. Contoh bahan
tambahan pangan dalam golongan ini adalah residu pestisida (termasuk
insektisida, herbisida, fungisida dan rodentisida) antibiotik dan hidrokarbon
2. Bahan tambahan pangan yang ditambahkan dengan sengaja kedalam makanan
dengan mengetahui komposisi bahan tersebut dan maksud penambahan ini
dapat mempertahankan kesegaran, cita rasa dan membantu pengolahan,
sebagai contoh pengawet, pewarna dan pengeras.
Penggunaan bahan tambahan pangan dapat dibenarkan apabila :
1. Dimaksudkan untuk mencapai masing-masing tujuan penggunaan dalam
pengolahan.
2. Tidak digunakan untuk menyembunyikan penggunaan bahan yang salah
atau tidak memenuhi persyaratan.
3. Tidak digunakan untuk menyembunyikan cara kerja yang bertentangan
dengan cara produksi yang baik untuk makanan dan
4. Tidak digunakan untuk menyembunyikan kerusakan makanan
(Cahyadi, 2006)
Jadi bahan yang dimaksud dengan bahan tambahan pangan adalah :
1. Tidak dikonsumsi sebagai makanan dan bukan merupakan ingredient makanan.
2. Mempunyai atau tidak mempunyai nilai gizi.
3. Sengaja ditambahkan kedalam makanan untuk mendukung proses
pembuatan, pengolahan, penyimpanan, perlakuan, pengepakan,
pengemasan dan atau pengangkutan makanan. Misalnya untuk
menghasilkan suatu komponen yang mempengaruhi sifat makanan
tersebut baik secara langsung atau tidak langsung.
4. Tidak mencakup cemaran atau bahan yang ditambahkan dengan tujuan
untuk mempertahankan atau meningkatkan nilai gizi. Misalnya vitamin C
dianggap sebagai bahan tambahan pangan jika tidak ditujukan untuk
memperbaiki nilai gizi tetapi sebagai antioksidan.
Sebenarnya tujuan penambahan bahan tambahan pangan sendiri secara umum
untuk meningkatkan nilai gizi makanan, memperbaiki nilai estetika dan sensor
2.1.2 Bahan Tambahan Yang Dilarang
Dahulu bahan tambahan pangan masih terbatas berupa bahan alami,
dengan berkembanganya teknologi produk instan sangat digemari oleh
masyarakat karena mudah didapat, cepat dan murah. Namun sekarang muncul
ekstrak bahan tambahan pangan dari bahan alami maupun sintetis bahan kimia .
Bahan tambahan pangan alami dan sintetis seringkali sulit dibedakan karena
memiliki aroma, rasa, warna dan sifat yang hampir sama. Diperlukan suatu
kejelian bagi konsumen untuk membedakan apakah makanan yang hendak
dibelinya mengandung bahan tambahan pangan alami atau sintetis. Penggunaan
bahan tambahan pangan sekarang ini sangat beragam dari pengawet sampai
pewarna, sayangnya penggunaan bahan tambahan pangan sering kali berakibat
buruk terhadap kesehatan. Karena alasan ekonomi sehingga penggunaan bahan
yang sebenarnya bukan untuk pangan menjadi salah. Sebagai contoh penggunaan
pewarna tekstil untuk bahan makanan karena harganya lebih murah dari pada
pewarna makanan (Saparinto, 2006).
Bahan tambahan pangan yang tidak boleh digunakan diantaranya adalah
yang mempunyai sifat-sifat sebagai berikut, dapat merupakan penipuan bagi
konsumen, menyembunyikan kesalahan dalam tehnik pengolahan, dapat
menurunkan nilai gizi makanan. Bahan tambahan yang dilarang merupakan suatu
bahan yang dapat bersifat toksisitas dan menimbulkan bahaya bagi kesehatan
yang mengkonsumsinya dan menggunakannya dalam bahan tambahan pangan.
Beberapa bahan tambahan pangan yang dilarang digunakan dalam makanan
menurut Peraturan Menteri Kesehatan No. 033 Tahun 2012, sebagai berikut :
1. Asam borat dan senyawanya (Boric acid)
2. Asam Salisilat dan garamnya (Salicylic acid and its salt) 3. Dietilpirokarbonat (Diethylpyrocarbonate, DEPC) 4. Dulsin (Dulcin)
5. Formalin (Formaldehyde)
6. Kalium bromat (Potassium bromated)
7. Kalium klorat (Potassium chlorate) 8. Kloramfenikol (Chloramphenicol)
10.Nitrofurazon (Nitrofurazone)
11.Dulkamara (Dulkamara)
12.Kokain (Cocaine)
13.Nitrobenzen (Nitrobenzene)
14.Sinamil antranilat (Cinnamyl anthranilate)
15.Dihidrosafrol (Dihydrosafrole)
16.Biji tonka (Tonka bean)
17.Minyak kalamus (Calamus oil)
18.Minyak tansi (Tansy oil)
19.Minyak sasafras (Sasafras oil)
2.2 Pengawet Dalam Kehidupan Sehari-hari
Memperpanjang masa simpan bahan pangan dapat dilakukan dengan
berbagai macam cara. Teknologi pengawetan makanan yang populer dikenal
antara lain pengawetan menggunakan suhu tinggi seperti pasteurisasi dan
sterilisasi. Kita juga mengenal pengawetan menggunakan suhu rendah, misalnya
penyimpanan suhu dingin dengan menggunakan lemari pendingin atau lemari es
dan penyimpanan beku menggunakan frezer. Pengawetan makanan juga dapat
dilakukan dengan cara pengeringan, yaitu dengan menjemur dibawah sinar
matahari ataupun menggunakan alat pengering. Cara pengawetan makanan
dengan mengandalkan teknologi pengolahan relatif aman dan dapat dilakukan
dalam rumah tangga. Sesuai dengan perkembangan teknologi pengolahan pangan
dan untuk peningkatan permintaan konsumen ada satu lagi cara pengawetan
makanan yang menggunakan bahan tambahan yaitu bahan pengawet (food preservatives).
Bahan pengawet makanan merupakan salah satu bahan tambahan makanan
(food additives) yang sebenarnya bukan sesuatu yang baru, yang sudah dikenal sejak lama, sejak manusia telah mengenal mengasinkan daging. Pengasinan
bertujuan untuk menambah daya keawetan daging. Dizaman modern, bahan
tambahan makanan digunakan dalam skala yang semakin luas. Luasnya cakupan
fungsi bahan tambahan makanan, menjadikan sulit bagi manusia dizaman modern
Misalnya tanpa bahan pengawet makanan tidak akan tahan lama jika makanan
tidak tahan lama, kita akan repot karena harus sering ke toko atau pasar. Kini
bahan pengawet pangan banyak diperbincangkan karena dianggap tidak baik
untuk kesehatan. Apalagi jika dikonsumsi dalam jumlah yang cukup banyak.
Pernyataan ini tidak semuanya tepat sebab ada bahan pengawet yang aman
digunakan untuk berbagai pengolahan pangan. Bahan pengawet atau proses
pengawetan terkadang sangat diperlukan untuk menjaga bahan pangan tidak rusak
dalam jangka waktu tertentu (Muaris, 2007).
Pengawet makanan adalah zat yang digunakan untuk menjaga makanan
agar tetap segar dan stabil serta memperpanjang umur simpan makanan. Itu
artinya jika makanan seharusnya sudah tidak layak konsumsi dalam jangka waktu
tiga hari jika diberikan tambahan pengawet dia akan menjadi tahan lama mungkin
mencapai umur satu minggu atau bahkan lebih. Pengawet makanan ini bisa
digunakan dalam makanan mentah ataupun makanan yang sudah siap santap.
Pengawet makanan terdiri dari pengawet alami dan buatan. Untuk pengawet alami
sendiri ada garam dan gula. Pengawet alami ini sering digunakan dalam
mengawetkan buah-buahan kaleng, daging serta berbagai jenis makanan kaleng
atau sayuran.
Pemakaian bahan pengawet dari satu sisi menguntungkan karena dengan
adanya bahan pengawet, bahan pangan dapat dibebaskan dari kehidupan mikroba,
baik yang bersifat patogen yang dapat menyebabkan keracunan atau gangguan
kesehatan lainnya maupun mikrobial yang non patogen yang dapat menyebabkan
kerusakan bahan pangan, mislanya pembusukan. Namun dari sisi lain, pemakaian
bahan pengawet pada dasarnya adalah senyawa kimia yang merupakan bahan
asing yang masuk kedalam tubuh bersama bahan pangan yang dikonsumsi apabila
kita menggunakan bahan pengawet kimia (Cahyadi, 2006).
2.3 Formalin
Menurut Peraturan Menteri Kesehatan No. 033 Tahun 2012, formalin
merupakan bahan kimia yang penggunaannya dilarang untuk produk makanan.
Formalin merupakan nama dagang larutan formaldehid. Formalin sebenarnya
berguna untuk mengawetkan spesimen biologi dan mayat dan dibidang industri
digunakan pada tekstil, pupuk dan bahan kimia. Senyawa ini termasuk golongan
aldehid yang paling sederhana karena hanya mempunyai satu atom karbon
(Widyaningsih, 2006).
Formalin merupakan cairan jernih yang tidak berwarna atau hampir tidak
berwarna dengan bau yang sangat menusuk, uapnya merangsang selaput lendir
hidung, tenggorokan dan seperti rasa terbakar. Berat tiap mililiter ialah 1,08 gram.
Dapat bercampur dalam air dan alkohol, tetapi tidak bercampur dengan eter
ataupun kloroform. Sifatnya yang mudah larut dalam air dikarenakan adanya
elektron sunyi pada oksigen sehingga dapat mengadakan ikatan hidrogen dengan
molekul air (Fessenden, 1986). Struktur formaldehid dapat dilihat pada gambar
2.1 dibawah ini :
Gambar 2.1 Struktur Bangun Formaldehid
Formaldehid berbentuk serbuk atau padatan disebut paraformaldehid.
Formalin dan paraformaldehid dapat melepaskan gas formaldehid. Formaldehid
memiliki rumus molekul CH2O dan memiliki nama lain yang diantaranya ialah
formol, metilen aldehid, paraform, morbisida, oksometan, polioksometilen glikol,
metanal, formorform, superlisoform, formiat aldehid, formalit, tetraoksi metilen,
metil oksida, karsan, trioksane, oksimetilen dan metilen glikol. Formaldehid
mempunyai massa molar 30,03 g/ml dengan titik didih 96OC (Susanti, 2010).
Penggunaan formalin yang sebenarnya bukan untuk makanan melainkan
sebagai antiseptik, germisida dan pengawet non makanan. Formalin sudah sangat
umum digunakan dalam kehidupan sehari-hari. Apabila digunakan secara benar,
formalin akan banyak kita rasakan manfaatnya, misalnya sebagai antibakteri atau
pembunuh kuman dalam berbagai jenis keperluan industri yakni pembersih lantai,
kapal, gudang dan pakaian, pembasmi lalat maupun berbagai serangga lainnya.
Formalin juga sering digunakan sebagai bahan pembuatan produk parfum,
pengawet produk kosmetika, pengeras kuku dan bahan untuk insulasi busa.
dibidang industri kayu formalin digunakan sebagai bahan perekat untuk produk
kayu lapis (Plywood). Dalam konsentrasi yang sangat kecil (<1%) digunakan sebagai bahan pengawet untuk berbagai barang konsumen seperti pembersih
rumah tangga, cairan pencuci piring, pelembut, perawat sepatu, shampo mobil,
lilin dan karpet. Didunia kedokteran formalin digunakan sebagai pengawet mayat.
Formalin juga dipakai untuk reaksi kimia yang bisa membentuk ikatan polimer
yang dapat menimbulkan warna produk menjadi lebih cerah. Oleh karena itu,
formalin juga banyak dipakai dalam produk rumah tangga seperti piring, gelas dan
mangkuk yang berasal dari plastik ataupun melamin. Bila piring atau gelas
tersebut digunakan untuk makanan atau minuman yang panas makan bahan
formalin yang terdapat didalamnya akan larut (Yuliarti, 2007).
Menurut Peraturan Menteri Kesehatan No. 033 Tahun 2012 formalin
merupakan bahan kimia yang penggunaannya dilarang untuk produk makanan.
Tetapi penggunaannya dalam bahan makanan semakin banyak didapatkan.
Beberapa hal yang menyebabkan pemakaian formalin untuk bahan tambahan
makanan (pengawet) meningkat antara lain :
1. Karena harganya yang jauh lebih murah dibanding pengawet lainnya,
seperti natrium benzoat atau natrium sorbet
2. Jumlah yang digunakan tidak perlu sebesar pengawet lainnya
3. Mudah digunakan untuk proses pengawetan karena bentuknya larutan
4. Waktu proses pengawetan juga lebih singkat
5. Mudah didapatkan ditoko bahan kimia dalam jumlah besar
6. Dan rendahnya pengetahuan masyarakat produsen tentang bahaya
formalin.
Maraknya penggunaan formalin pada bahan makanan sudah muncul ke
permukaan sejak beberapa tahun lalu. Balai Besar Pengawasan Obat dan Makanan
telah melakukan uji laboratorium pada 761 sampel makanan. Hasilnya beberapa
jenis bahan makanan olahan yaitu mi basah, bakso, tahu dan ikan asin positif
mengandung formalin (Widyaningsih, 2006).
Formalin merupakan bahan beracun dan berbahaya bagi kesehatan
manusia. Jika kandungannya tinggi didalam tubuh, akan bereaksi secara kimia
kematian sel yang mengakibatkan keracunan pada tubuh. Efek dari makanan
berformalin baru terasa beberapa tahun kemudian, kandungan formalin akan
meracuni tubuh, menyebakan iritasi lambung, alergi, bersifat karsinogenik dan
juga bersifat mutagen (menyebakan perubahan fungsi sel/jaringan), serta orang
yang mengkonsumsinya akan muntah, diare bercampur darah, kencing bercampur
darah. Formalin bila menguap diudara berupa gas yang tidak berwarna, dengan
bau yang menyesakkan sehingga merangsang hidung, tenggorokkan dan mata
(Cahyadi, 2006).
2.4 Tahu
Tahu merupakan salah satu jenis makanan yang dibuat dari kedelai dengan
jalan memekatkan protein kedelai dan mencetaknya melalui proses pengendapan
protein pada titik isoelektrisnya, dengan atau tanpa penambahan unsur-unsur lain
yang diizinkan. Tahu diproduksi dengan memanfaatkan sifat protein, yaitu ‘akan
menggumpal bila bereaksi dengan asam’. Penggumpalan protein oleh asam cuka
berlangsung secara cepat dan serentak diseluruh bagian cairan sari kedelai,
sehingga sebagian besar air yang semula tercampur dalam sari kedelai akan
terperangkap didalamnya. Pengeluaran air yang terperangkap tersebut dapat
dilakukan dengan memberikan tekanan. Semakin besar tekanan yang diberikan,
semakin banyak air dapat dikeluarkan dari gumpalan protein. Gumpalan protein
itulah yang kemudian disebut sebagai tahu (Suprapti, 2009).
Dalam perdagangan dikenal 2 jenis tahu, yaitu tahu biasa dan tahu Cina.
Kedua jenis tahu ini berbeda dalam bentuk dan cara pembuatannya. Pada
pembuatan tahu Cina, kedelai direbus terlebih dahulu sebelum direndam dan
biasanya mempunyai ukuran lebih besar. Tahu dikenal masyarakat sebagai
makanan sehari-hari yang umumnya sangat digemari serta mempunyai daya cerna
yang tinggi. Keuntungan lain pada pembuatan tahu adalah berkurangnya senyawa
antitripsin (tripsin inhibito) yang terbuang bersama whey dan rusak selama
pemanasan. Disamping itu adanya proses pemanasan juga dapat menghilangkan
Tahu adalah makanan yang empuk, lezat dan bergizi. Kelembutan tahu
membuat banyak orang dewasa maupun anak-anak menyukainya. Tahu dibuat
melalui penyaringan kedelai yang telah digiling dan ditambah air. Kelembutan
tekstur tahu membuat makanan ini mudah dikunyah ibarat daging tanpa tulang.
Kandungan protein tahu sangat berkualitas karena bahan dasar tahu adalah
kedelai. Daya cerna tahu dalam tubuh dapat mencapai 85-98% dan total protein
yang dapat dimanfaatkan tubuh adalah sebesar 65%. Sebagai makanan yang
merakyat ternyata tahu mengandung protein sejumlah 7,85. Protein tahu tidak
terlalu tinggi karena kadar air dalam tahu sangat tinggi, yaitu mencapai 84,8%.
Pada umumnya makanan-makanan yang berkadar air tinggi mengandung protein
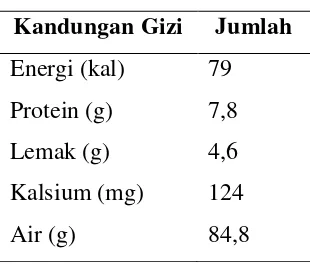
yang agak rendah. Kandungan gizi tahu ditunjukkan pada tabel 2.1 berikut ini :
Tabel. 2.1 Kandungan Gizi Tahu Per 100 g
Kandungan Gizi Jumlah Energi (kal) 79
Protein (g) 7,8
Lemak (g) 4,6
Kalsium (mg) 124
Air (g) 84,8
(Khomsan, 2008).
Pada dasarnya proses pembuatan tahu tediri dari dua bagian, yaitu
pembuatan susu kedelai dan penggumpalan proteinnya. Sebagai zat penggumpal,
secara tradisional biasanya digunakan biang yaitu cairan yang keluar pada waktu
pengepresan dan sudah diasamkan semalam, sebagai pengganti dapat digunakan
air jeruk, cuka, larutan asam laktat, larutan CaCl2 atau CaSO4 (Purwaningsih,
2010).
Sebagai makanan yang memiliki kandungan air tinggi, tahu cepat
mengalami penyimpangan bau maupun rasa. Cita rasa tahu dan kecepatannya
mengalami penyimpangan bau sangat tergantung pada kualitas kedelai, sumber air
pembuatannya, sanitasi alat-alat pembuatan tahu, dan pekerjaannya. Apabila
semua unsur tersebut diperhatikan kualitas tahu dapat dipertahankan selama 1-2
hari dengan cara disimpan dikulkas. Pada umumnya tahu direndam air bersih
pembusuk dari udara. Akan tetapi, jika air perendamannya tidak higenis, justru
lebih mempercepat kerusakan tahu. Cara lain agar lebih awet yaitu dengan
merebus tahu selama 30 menit, kemudian direndam dalam air yang telah dimasak,
keawetan tahu rebusan itu dapat bertahan hingga empat hari. Saat ini telah
diketahui bahwa ada produk-produk tahu yang menggunakan pengawet berbahaya
(formalin). Kadar formalin yang dicampurkan mungkin tidak terlalu banyak
sehingga konsumen tidak dapat membedakan tahu berformalin dan tahu tanpa
formalin. Namun, perlu diingat formalin adalah bahan yang dilarang, betapapun
kecilnya kandungan formalin dalam tahu hal itu harus tetap dianggap sebagai
unsur yang membahayakan kesehatan. Penelitian yang dilakukan Tresniani pada
tahun 2003 lulusan Departemen Gizi IPB mengungkapkan bahwa 11 industri tahu
kuning dan 9 industri tahu putih di Tangerang, semuanya terindikasi
menggunakan formalin sebagai pengawet. Tahu kuning mengandung 3,79 ppm,
27,48 ppm, sedangkan tahu putih 5,15 ppm dan 42,44 ppm (Khomsan, 2008).
2.5 Kitosan
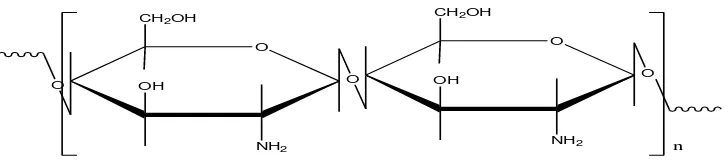
Kitosan adalah poli-(2-amino-2-deoksi-β-(1 4)-D-glukopiranosa) dengan
rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi kitin. Kitosan
juga dijumpai secara alamiah di beberapa organisme. Struktur polimer kitosan
dapat dilihat pada gambar 2.2 dibawah ini :
O
Gambar 2.2 Struktur Polimer Kitosan (Sugita, 2009)
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun
enzimatik. Proses kimiawi menggunakan basa, misalnya NaOH, dan dapat
menghasilkan kitosan dengan derajat deasetilasi yang tinggi, yaitu mencapai
85-93 % (Tsigos et al., 2000). Namun proses kimiawi menghasilkan kitosan dengan bobot molekul yang beragam dan deasetilasinya juga sangat acak sehingga sifat
Kitosan merupakan padatan amorf yang berwarna putih kekuningan
dengan rotasi spesifik [∝]D11 -3 hingga -10 ̊ (pada konsentrasi asam asetat 2%).
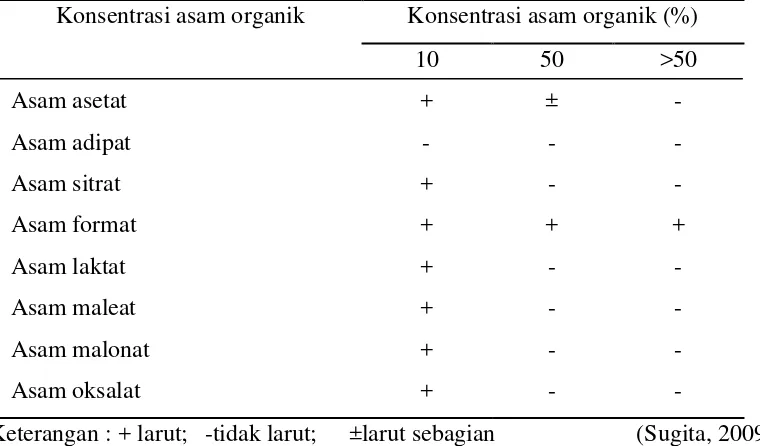
Kitosan larut pada kebanyakan larutan asam organik (Tabel 2.5.) pada pH sekitar
4,0, tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut
air, alkohol, dan aseton. Dalam asam mineral pekat seperti HCl dan HNO3,
kitosan larut pada konsentrasi 0,15-1,1%, tetapi tidak larut pada konsentrasi 10%.
Kitosan tidak larut dalam H2SO4 pada berbagai konsentrasi, sedangkan
didalam H3PO4 tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1%
sedikit larut. Perlu untuk kita ketahui, bahwa kelarutan kitosan dipengaruhi oleh
bobot molekul, derajat deasetilasi dan rotasi spesifiknya yang beragam bergantung
pada sumber dan metode isolasi serta transformasinya. Kelarutan kitosan pada
berbagai pelarut asam organik dapat dilihat pada tabel 2.2 berikut ini :
Tabel 2.2 Kelarutan kitosan pada berbagai pelarut asam organik
Konsentrasi asam organik Konsentrasi asam organik (%)
10 50 >50
Asam asetat + ± -
Asam adipat - - -
Asam sitrat + - -
Asam format + + +
Asam laktat + - -
Asam maleat + - -
Asam malonat + - -
Asam oksalat + - -
Keterangan : + larut; -tidak larut; ±larut sebagian (Sugita, 2009)
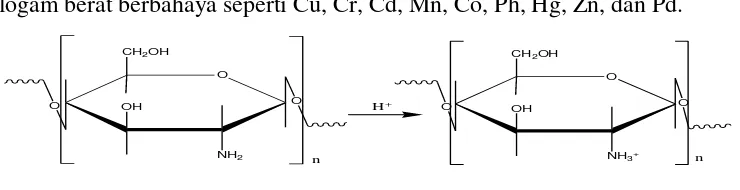
Kitosan dalam bentuk terprotonasi menunjukkan kerapatan muatan yang
tinggi dan bersifat sebagai polielektrolit kationik, seperti yang dapat dilihat pada
Gambar 2.3 dan sangat efektif berinteraksi dengan biomolekul bermuatan negatif
Sedangkan dalam bentuk netralnya, kitosan mampu mengkompleks ion
logam berat berbahaya seperti Cu, Cr, Cd, Mn, Co, Ph, Hg, Zn, dan Pd.
O
Gambar 2.3 Kitosan sebagai polielektrolit kationik (Sugita, 2009)
Kitosan dapat dimodifikasi, kitosan sebagai adsorben dapat berada dalam
berbagai bentuk, antara lain bentuk butir, serpih, hidrogel, dan membran (film).
Kitosan sebagai adsorben sering dimanfaatkan untuk proses adsorpsi ion logam
berat. Besarnya afinitas kitosan dalam mengikat ion logam sangat bergantung
pada karakteristik makrostruktur kitosan yang dipengaruhi oleh sumber dan
kondisi pada luas permukaannya. Semakin kecil ukuran kitosan akan semakin
besar dan proses adsorpsi pun dapat berlangsung dengan baik. Modifikasi kimia
kitosan menjadi gel kitosan dapat meningkat kapasitas jerapnya, keunggulan ini
disebabkan oleh bentuk butiran gel mempunyai volume pori yang lebih besar
dibandingkan dengan bentuk serpihan. Kitosan dengan bobot molekul tinggi akan
menghasilkan larutan dengan viskositas yang tinggi pula (Rao, 1993).
Secara umum adsorpsi adalah suatu proses pemisahan
komponen-komponen tertentu dalam fasa cair atau gas melewati suatu permukaan padat
yang disebut adsorben, sedangkan komponen yang diserap disebut adsorbat.
Ketika permukaan padatan dipaparkan pada molekul adsorbat, adsorbat akan
membentur permukaan padatan, sehingga sebagian akan menempel dipermukaan
padatan dan terjerap, sedangkan yang lain akan terpantul kembali. Pada awalnya,
laju adsorpsi cukup besar karena seluruh permukaan masih kosong. Namun,
setelah waktu kontak semakin lama, permukaan yang terisi oleh molekul gas
semakin banyak dan luas daerah kosong menyusut, sehingga laju adsorpsinya ikut
menurun. Bersamaan dengan itu, laju desorpsi, yaitu laju pelepasan kembali
molekul adsorbat, justru meningkat hingga tercapai suatu kesetimbangan dinamis
2.6 Asam Jawa
Asam jawa (Tamarindus Indica) merupakan sebuah kultivar daerah tropis dan termasuk tumbuhan berbuah polong. Batang pohonnya yang cukup keras
dapat tumbuh menjadi besar dan daunnya rindang. Daun asam jawa bertangkai
panjang , sekitar 17 cm dan bersirip genap. Bunganya berwarna kuning
kemerah-merahan dan buah polongnya berwarna coklat dengan rasa khas asam. Didalam
buah polong selain terdapat kulit yang membungkus daging buah, juga terdapat
biji yang berjumlah 2-5 yang pipih dengan warna coklat agak kehitaman. Buah
polong asam jawa mengandung senyawa kimia antara lain asam appel, asam
sitrat, asam anggur, asam tertrat, asam suksinat, pektin dan gula invert.
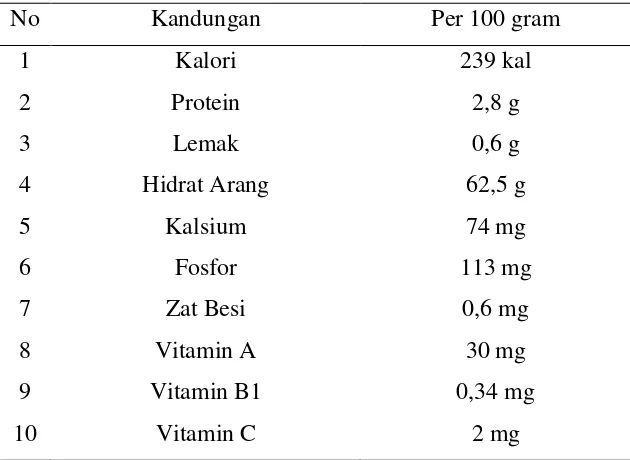
Kandungan asam jawa ditunjukkan pada tabel 2.3 berikut ini :
Tabel 2.3 Kandungan Asam Jawa
No Kandungan Per 100 gram
1 Kalori 239 kal
2 Protein 2,8 g
3 Lemak 0,6 g
4 Hidrat Arang 62,5 g
5 Kalsium 74 mg
6 Fosfor 113 mg
7 Zat Besi 0,6 mg
8 Vitamin A 30 mg
9 Vitamin B1 0,34 mg
10 Vitamin C 2 mg
Kulit bijinya mengandung phlobatannin dan bijinya mengandung albuminoid serta
pati (Thomas, 2012).
Sardeswara (2001) menyebutkan bahwa tanaman asam jawa sangat
berguna untuk kesehatan manusia. Daun asam jawa yang dikeringkan dan
didinginkan dapat digunakan untuk mengobati kelenjar empedu. Daun segar yang
direbus juga dapat mencegah infeksi radang. Kulit asam jawa yang astringent
Beberapa penelitian menyebutkan bahwa kulit asam jawa juga dapat
digunakan untuk mengobati penyakit asma. Hisa (2001) menyebutkan kandungan
aktif pada asam jawa seperti asam asetat, asam sirat, asam askorbat, sinamil
aldehida, geranikal, bekarotin, asam laktat dan metionin dapat digunakan untuk
melancarkan proses pencernaan dan buang air besar. Selain itu, asam jawa juga
dapat digunakan untuk mengobati disentri, demam, lepra, radang mata, infeksi
oral, penyakit pernafasan dan luka-luka. Asam juga berpengaruh terhadap bakteri
patogen yang sangat membahayakan tubuh manusia, seperti Escherichia Coli, Salmonella Typhimurium, dan Staphylococcus Aureus. Hasil penelitian (Samudera, 1992) menunjukkan bahwa efek bakterisial atau bakteristik asam jawa
disebabkan oleh rendahnya nilai pH yang ditimbulkannya, bukan akibat senyawa
antimikroba. Asam jawa juga mengandung komponen antioksidan, penelitian
(Huerta, 2000) menunjukkan bahwa asam jawa sangat berpotensi untuk
dikembangkan menjadi minuman fungsional karena mengandung komponen
antioksidan yang sangat berarti. De lumen (1986) menyebutkan bahwa diantara
jenis leguminosa yang lain, asam jawa mengandung komponen kimia yang paling
tinggi (Astawan, 2009).
2.7 Instrument
Spektrofotometri sesuai dengan namanya adalah alat yang terdiri dari
spektrofotometer dan fotometer. Spektrofotometer menghasilkan sinar dari
spektrum dengan panjang gelombang tertentu dan fotometer adalah alat pengukur
intensitas cahaya yang ditransmisikan atau diadsorbsi. Jadi spektrofotometer
digunakan untuk mengukur energi secara relatif jika energi tersebut
ditransmisikan, direfleksikan atau diemisikan sebagai fungsi dari panjang
gelombang.
Kelebihan spektrofotometer dibanding fotometer adalah panjang
gelombang dari sinar putih dapat lebih terseleksi dan ini diperoleh dengan alat
pengurai seperti prisma, grating atau celah optis. Suatu spektrofotometer tersusun
dari sumber spektrum tampak yang kontinyu, monokromator, sel pengabsorbsi,
untuk larutan sampel atau blanko dan suatu alat untuk mengukur perbedaan
Pada umumnya terdapat dua tipe instrument Spektrofotometer UV-Visible
yaitu Single-Beam dan Double-Beam.
a. Single-Beam Instrument
Single-Beam Instrument dapat digunakan untuk kuantitatif dengan
mengukur absorbansi pada panjang gelombang tunggal. Single-Beam
instrument mempunyai beberapa keuntungan yaitu sederhana, harganya
murah dan mengurangi biaya yang ada merupakan keuntungan yang nyata.
Beberapa instrument untuk pengukuran sinar ultra violet dan sinar tampak.
Panjang gelombang paling rendah adalah 190 sampai 210 nm dan paling
tinggi adalah 800 sampai 1000 nm (Skoog, 1996).
b. Double-Beam dibuat untuk digunakan pada panjang gelombang 190
sampai 750 nm. Double-Beam instrument dimana mempunyai dua sinar
yang dibentuk oleh potongan cermin yang berbentuk V yang disebut
pemecah sinar. Sinar pertama melewati larutan blanko dan sinar kedua
secara serentak melewati sampel, mencocokkan fotodetektor yang keluar
menjelaskan perbandingan yang ditetapkan secara elektronik dan
ditunjukkan oleh alat pembaca (Skoog, 1996).
Hukum Lambert-Beer menyatakan bahwa, bila cahaya monokromatik melewati
medium tembus cahaya, laju berkurangnya intensitas oleh bertambahnya
ketebalan, berbanding lurus dengan intensitas cahaya. Hal ini berarti bahwa
intensitas cahaya yang dipancarkan berkurang secara eksponensial dengan
bertambahnya ketebalan medium yang menyerap. Dengan menyatakan bahwa
lapisan manapun dari medium itu yang tebalnya sama akan menyerap cahaya
Hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan
zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan.
A = - Log T = - Log It/Io = ε.b.C
Dimana :
A = Absorbansi dari sampel yang akan diukur
T = Transmitansi
Io = Intensitas sinar masuk
It = Intensitas sinar yang diteruskan
ε = Koefisien ekstingsi
b = Tebal kuvet yang digunakan
C = Konsentrasi dari sampel
Dalam hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh
larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan.
Dalam hukum Lambert-Beer tersebut ada beberapa pembatasaan yaitu :
1. Sinar yang digunakan dianggap monokromatis.
2. Penyerapan terjadi dalam sutu volume yang mempunyai penampang luas
yang sama.
3. Senyawa yang diserap dalam larutan tersebut tidak tergantung terhadap
yang lain dalam larutan tersebut.
4. Tidak terjadi peristiwa fluoresensi atau forforesensi.
5. Indeks bias tidak tergantung pada konsentrasi larutan.
Alat-alat instumentasi Spektrofotometer UV-Visible terdiri dari
1. Sistem Optik
Pada umumnya konfigurasi dasar setiap spektrofotometer UV-Visible
berupa susunan peralatan optik yang terkonstruksi pada gambar 2.4
sebagai berikut :
Gambar 2.4 Bagan Alat Spektrofotometer UV-Visible
Keterangan :
SR = Sumber radiasi
M = Monokromator
SK = Sampel kompartemen
D = Detektor
A = Amplifier atau penguat
VD = Visual Display atau meter
Setiap bagian peralatan optik dari Spektrofotometer UV-Visible
memegang fungsi dan peranan tersendiri yang saling terkait fungsi
peranannya. Setiap fungsi dan peranan tiap bagian dituntut ketelitian
dan ketepatan yang optimal, sehingga akan diperoleh hasil pengukuran
yang tinggi tingkat ketelitian dan ketetapannya.
2. Sumber Radisi
Beberapa macam sumber radiasi yang dipakai pada Spektrofotometer
UV-Visible adalah lampu deuterium, lampu tungsten dan lampu
merkuri. Sumber radiasi deuterium dapat dipakai pada daerah panjang
gelombang 190 sampai 380 nm (daerah ultraviolet dekat), karena pada
rentangan panjang gelombang tersebut sumber radiasi deuterium
memberikan dua garis spektra yang dapat dipakai untuk mengecek
ketepatan panjang gelombang pada Spektrofotometer UV-Visible.
3. Monokromator
Monokromator berfungsi untuk mendapatkan radiasi monokromatis
dari sumber radiasi polikromatis. Monokromator pada
spektrofotometer UV-Visible biasanya terdiri dari susunan : celah
4. Sel atau Kuvet
Kuvet atau sel merupakan wadah sampel yang akan dianalisis. Ditinjau
dari pemakaiannya kuvet ada dua macam yang permanen terbuat dari
bahan gelas leburan silika atau kuvet disposable untuk satu kali
pemakaian yang terbuat dari teflon atau plastik. Ditinjau dari bahan
yang dipakai membuat kuvet, ada dua macam yaitu: kuvet dari leburan
silika (kuarsa) dan kuvet dari gelas. Kuvet dari leburan silika dapat
dipakai unutk analisis kualitatif dan kuantitatif pada daerah
pengukuran (380-1100 nm) karena bahan dari gelas mengadsorbsi
radiasi UV. Dianjurkan setiap kali memakai kuvet selalu dibersihkan
dengan alkohol absolut atau direndam didalamnya. Membersihkan
permukaan kuvet yang basah harus dipakai kertas lensa yang bagus
jangan sekali-kali memegang permukaan kuvet yang transparan.
5. Detektor
Detektor merupakan salah satu bagian dari Spektrofotometer
UV-Visible yang penting, oleh sebab itu kualitas detektor akan menentukan
kualitas Spektrofotometer UV-Visible. Fungsi detektor adalah
mengubah sinyal radiasi yang diterima menjadi sinyal elektronik.
Beberapa pustaka memberikan persyaratan tentang kualitas dan fungsi
detektor didalam Spektrofotometer UV-Visible antara lain :
1. Detektor harus mempunyai kemampuan untuk memberikan respon
terhadap radiasi yang diterima, tetapi harus memberikan derau
(noise) yang sangat minimum.
2. Detektor harus mempunyai kemampuan untuk memberikan respon
terhadap radiasi pada daerah panjang gelombang yang lebar
(UV-Visible).
3. Detektor harus memberikan respon terhadap radiasi dalam waktu
yang serempak.
4. Detektor harus memberikan jaminan terhadap respon kuantitatif
dan sinyal elektronik yang dikeluarkan harus berbanding lurus
5. Sinyal elektronik yang diteruskan oleh detektor harus dapat
diampifikasikan oleh amplifier ke rekorder (Mulja, 1995).
2.8 Analisa Formalin Dalam Makanan 2.8.1 Analisa Kualitatif Formalin
Terdapat banyak metode untuk mengetahui apakah suatu bahan makanan
mengandung formalin atau tidak mulai dari pengamatan secara fisik makanan
seperti warna pada makanan lebih terang, tekstur kaku dan yang dapat teramati
lebih detail adalah pada keawetan makanan tersebut. Namun pada konsentrasi
rendah pengamatan secara fisik akan sukar dilakukan sehingga perlu dilakukan
analisis kualitatif formalin dalam bahan makanan agar diketahui ada atau tidaknya
formalin. Analisis kualitatif cenderung mudah dilakukan yaitu dengan
menambahkan pereaksi tertentu kedalam bahan makanan yang diduga
mengandung formalin sehingga akan dihasilkan perubahan warna yang khas. Uji
seperti ini disebut juga spot test. Analisis kualitatif formalin dapat dilakukan dengan pereaksi KMnO4, K2Cr2O7, FeCl3, asam kromatofat, Schiff’s, Fehling,
Schryver dan Nash (Fauzy, 2016).
Persamaan reaksi yang terjadi antara formalin dengan
pereaksi-pereaksinya yaitu:
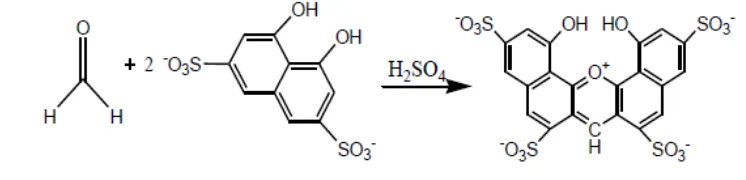
a. Peraksi Asam kromatofat (C10H6Na2O8S2.2H2O)
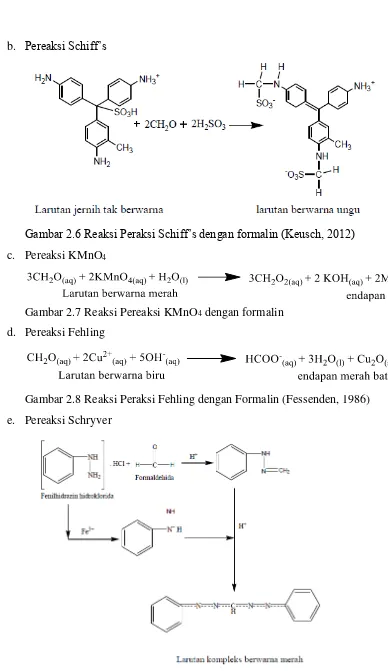
b. Pereaksi Schiff’s
Gambar 2.6 Reaksi Peraksi Schiff’s dengan formalin (Keusch, 2012)
c. Pereaksi KMnO4
Gambar 2.7 Reaksi Pereaksi KMnO4 dengan formalin
d. Pereaksi Fehling
Gambar 2.8 Reaksi Peraksi Fehling dengan Formalin (Fessenden, 1986)
e. Pereaksi Schryver
Gambar 2.9 Reaksi Pereaksi Schryver dengan Formalin (Suryadi, Herman,
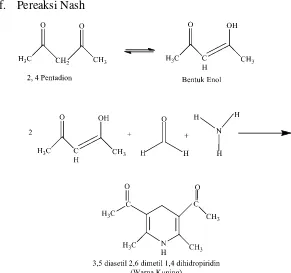
f. Pereaksi Nash
Gambar 2.10 Reaksi Peraksi Nash dengan Formalin (Herlich, 1990)
2.8.2 Analisa Kuantitatif Formalin
Analisis kuantitatif digunakan untuk menentukan kadar suatu senyawa dalam
sampel atau menetapkan banyaknya suatu zat tertentu yang ada dalam sampel.
Analisis kuantitatif formalin dapat dilakukan dengan menggunakan beberapa
metode yaitu dengan metode titrasi volumetri, atau titrasi asam-basa dengan
menambahkan hidrogen peroksida dan NaOH 1 N dan pemanasan hingga
pembuihan berhenti, dan dititrasi dengan HCl 1 N menggunakan indikator
fenolftalein (Ditjen POM, 1979). Selain itu metode spektrofotometri,
kromatografi gas dan kromatografi cair kinerja tinggi.
Metode kromatografi gas dan kromatografi cair kinerja tinggi memiliki
sensitivitas dan selektivitas yang sangat baik. Namun metode kromatografi gas
dan kromatografi cair kinerja tinggi memerlukan instrumentasi yang relatif mahal
dan rumit selain itu dibutuhkan proses derivatisasi menggunakan zat penderivat
yang mahal. Pada metode spektrofotometri dibutuhkan pereaksi dimana pereaksi
yang sering digunakan yaitu pereaksi asam kromatofat, pereaksi Nash dan
sensitivitas dan selektivitas yang cukup baik dan sudah di validasi. Formalin
dengan penambahan pereaksi Nash dan pemanasan 30 menit menghasilkan warna
kuning yang mantap, yang kemudian diukur pada panjang gelombang 412 nm
(Herlich, 1990).
Formalin ditemukan didalam sejumlah makanan ikan asin teri meda, ebi,
ikan asin kristal, ikan gembung asi, udang dan cumi-cumi segar. Preparasi sampel
yang dilakukan adalah dengan merendam masing-masing sampel dalam air panas
dan air dingin (Pane, 2009) dan dapat juga dilakukan dengan mendestilasi sampel
dengan asam posfat (Tarigan, 2008). Penetapan kadar secara kuantitatif dilakukan
dengan mengukur serapan larutan zat dalam suatu pelarut pada panjang
gelombang tertentu. Pengukuran serapan biasanya dilakukan pada panjang
gelombang serapan maksimum. Oleh karena serapan dapat berbeda jika
digunakan alat yang berbeda, maka sebaiknya pengukuran dilakukan pada
panjang gelombang serapan maksimum yang diperoleh dengan alat yang
digunakan syaratnya panjang gelombang yang diperoleh dengan alat tidak
berbeda lebih dari ± 0,5 nm pada daerah pengukuran 240-280 nm, tidak lebih dari
± 1 nm pada daerah pengukuran 280-320 nm serta tidak lebih dari ± 3 nm pada
daerah pengukuran diatas 320 nm dari panjang gelombang yang ditentukan. Jika
perbedaannya melebihi batas tersebut maka alat harus dikalibrasi. Pada
pengukuran serapan suatu larutan hampir semua digunakan blanko untuk
spektrofotometer agar panjang gelombang pengukuran mempunyai serapan nol.
Kegunaan blanko adalah mengoreksi serapan yang disebabkan oleh pelarut,
pereaksi, sel ataupun pengaturan alat. Blanko dapat berupa pelarut yang sama
seperti yang digunakan untuk melarutkan zat atau blanko pereaksi menyiapkan