BAB III
METODOLOGI PENELITIAN
3.1 LOKASI PENELITIAN
Penelitian ini akan dilaksanakan di Laboratorium Ekologi, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera Utara, Medan. Penelitian ini dilakukan selama lebih kurang 3 bulan.
3.2 BAHAN DAN PERALATAN
3.2.1 Bahan pada penelitian ini yang digunakan adalah: 1. Bahan Utama:
Sampah Organik + Kotoran Sapi Air
2. Bahan Pembantu
Penambahan trace metal Ni = 0,245 mg/L, Co = 0,245 mg/L dan campuran Ni dan Co masing-masing sebesar 0,25 mg/L.
3. Bahan Analisa
Kalium dikromat (K2Cr2O7)
Ferri sulfat heptahidrat (FeSO4.7H2O) Perak sulfat (Ag2SO4)
Merkuri sulfat (HgSO4) Asam sulfat pekat (H2SO4) Natrium Hidroksida (NaOH) Natrium Sulfat (Na2SO4) Natrium Karbonat (Na2CO3) 1,10-phenanthroline monohydrate Aquadest ( H2O)
Indikator Ferroin
3.2.2 Peralatan
Pada penelitian ini, peralatan yang digunakan antara lain: 1. Peralatan Utama, Digester anaerobik dari stoples platik 5L 2. Peralatan Analisa
Oven Desikator Alumunium Foil Kertas Saring pH meter Neraca analitik Selang plasik Suntikan
Alat-alat gelas seperti: beaker glass, erlenmeyer, gelas ukur, corong gelas, dan lain-lain.
3.2.3 Rangkaian peralatan
Gambar berikut menunjukkan rangkaian peralatan yang digunakan dalam pembuatan biogas.
Gambar 3.1 Rangkaian Peralatan Pembuatan Biogas Pengambil Contoh
Sampah organik + kotoran sapi + air
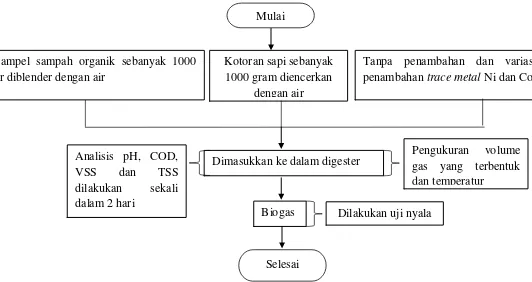
3.3 PROSEDUR PENELITIAN 3.3.1 Pembuatan biogas
Sampel sampah organik di campur (diblender) sebanyak 1000 gr dengan air kemudian ditambahkan kotoran sapi sebanyak 1000 gram yang telah diencerkan dengan air. Total air yang digunakan 2.000 ml. Ditambahkan trace metal Ni sebanyak 0,245 mg/L. Co sebanyak 0,245 mg/L dan campuran Ni dan Co masing-masing sebesar 0,25 mg/L masing-masing-masing-masing digester.Bahan isian dimasukkan ke dalam digester sebanyak 80 % dari volume digester (5L) yaitu sebanyak 4L. Tangki digester dihubungkan ke alat pengukur volume biogas, dimana volume gas diukur setiap hari. Pada tahap ini percobaan dilakukan pada digester anaerobik sistem batch. Dengan pH dijaga konstan antara 6,5-7,5 dan pada temperatur lingkungan (25 – 30 o
C). Selanjutnya difermentasikan selama 30 hari. Diamati paramater percobaan yaitu pH, temperatur, volume biogas yang dihasilkan dan parameter analisa, COD, TSS, VSS sekali dalam 2 hari.Dilakukan uji nyala terhadap biogas.
3.3.2 Flowchart pembuatan biogas
Adapun untuk memperoleh biogas dari sampah organic dan kotoran sapi dapat dilihat pada gambar 3.2, sebagai berikut :
Gambar 3.2 Flowchart Pembuatan Biogas Sampel sampah organik sebanyak 1000
gr diblender dengan air
Dimasukkan ke dalam digester Kotoran sapi sebanyak 1000 gram diencerkan
dengan air
Analisis pH, COD, VSS dan TSS dilakukan sekali dalam 2 hari
Tanpa penambahan dan variasi penambahan trace metal Ni dan Co
Pengukuran volume gas yang terbentuk dan temperatur
Biogas Mulai
Dilakukan uji nyala
3.4 PROSEDUR ANALISA 3.4.1 Analisa konsentrasi COD
Untuk melakukan penentuan harga COD dengan refluks terbuka, perlu dibuat beberapa larutan, antara lain :
1. Larutan baku kalium dikromat (K2Cr2O7) 0,25 N. 2. Larutan asam sulfat (H2SO4) – perak sulfat (Ag2SO4). 3. Larutan indicator ferroin.
4. Larutan FAS (Fe(NH4)2(SO4)2.6H2O) (FAS) 0,1N. 5. Larutan baku potassium hydrogen phthalate (KHP). 6. Asam sulfamat.
7. Serbuk merkuri sulfat (HgSO4).
Adapun peralatan yang diperlukan untuk melakukan penentuan harga COD dengan refluks terbuka antara lain :
1. Peralatan refluks, yang terdiri dari labu Erlenmeyer, pendingin Liebig 30 6. Timbangan analitik.
Adapun prosedur analisa COD adalah:
1. Dimasukkan 10 ml contoh uji ke dalam erlenmeyer 250 ml.
2. Ditambahkan 0,2 g serbuk raksa (II) sulfat (HgSO4) dan beberapa batu didih.
3. Ditambahkan 5 ml larutan kalium dikromat, (K2Cr2O7) 0,25 N.
4. Ditambahkan 15 ml pereaksi asam sulfat (H2SO4) – perak sulfat (Ag2SO4) perlahan-lahan sambil didinginkan dalam air pendingin.
5. Dihubungkan dengan pendingin Liebig dan dididihkan di atas hot plate selama 2 jam.
7. Didinginkan sampai temperatur kamar, ditambahkan indikator ferroin 2 sampai dengan 3 tetes, dititrasi dengan larutan ferro ammonium sulfat atau FAS 0,1 N sampai warna merah kecoklatan, dicatat kebutuhan larutan FAS.
8. Langkah 1 sampai dengan 7 dilakukan terhadap air suling sebagai blanko. Kebutuhan larutan FAS dicatat. Analisis blanko ini sekaligus melakukan pembakuan larutan FAS dan dilakukan setiap penentuan COD.
9.
Kandungan COD dapat dihitung berdasarkan rumus sebagai berikut: CODsampel ml
N)8000 )(
B A (
3.4.1.1 Flowchart penentuan harga COD
Mulai
Pipet 10 ml contoh uji, masukkan ke dalam erlenmeyer 250 ml
Tambahkan 0,2 g serbuk HgSO4dan beberapa batu didih
Tambahkan 5 ml larutan kalium dikromat 0,25 N
Tambahkan 15 ml pereaksi asam sulfat – perak sulfat perlahan-lahan sambil
didinginkan dalam air pendingin
Hubungkan dengan pendingin Liebig dan didihkan di atas hot plate selama 2 jam
Didinginkan dan cuci bagian dalam dari pendingin dengan air suling hingga volume contoh uji menjadi lebih kurang 70 ml
Didinginkan sampai temperatur kamar, tambhakan indicator ferroin 2 sampai dengan 3 tetes, titrasi dengan larutan FAS 0,1 N
samapi warna merah kecoklata, catat kebutuhan larutan FAS
Gambar 3.3 Flowchart penentuan harga COD 3.4.2 Analisanilai TSS
1. Berat kertas saring kering yang digunakan ditimbang. 2. Kertas saring dibasahi dengan sedikit air suling.
3. Sampel diaduk untuk memperoleh sampel yang lebih homogen. 4. Sampel dipipetkan ke penyaringan sebesar 5 ml
5. Kertas saring dicuci atau disaring dengan 3 x 10 ml aquadest.
6. Kertas saring dipindahkan secara hati-hati dari peralatan penyaring ke wadah timbang dengan aluminium sebagai penyangga.
7. Dikeringkan di dalam oven setidaknya selama 1 jam pada suhu 105ºC, didinginkan dalam desikator untuk menyeimbangkan suhu dan massanya.
8. Tahapan pengeringan, pendinginan dalam desikator, dan penimbangan diulangi sampai diperoleh berat konstan atau sampai perubahan berat lebih
kecil dari 4% terhadap penimbangan sebelumnya atau 0,5 mg.
9. Kandungan TSS dapat dihitung berdasarkan rumus sebagai berikut:
mL
Dilakukan langkah 1-7 terhadap air suling sebagai blanko. Catat kebutuhan larutan FAS. Analisis blanko ini sekaligus melakukan
pembakuan larutan FAS dan dilakukan setiap penentuan COD A
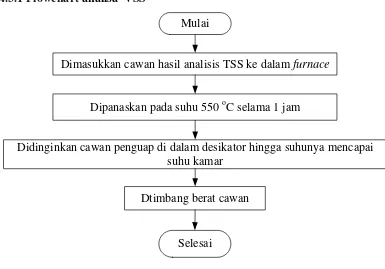
3.4.2.1 Flowchart analisa TSS
Tidak
Ya
Gambar 3.4 Flowchart analisa TSS Mulai
Kertas saring kering yang digunakan ditimbang
Sampel dipipetkan sebanyak 5 ml ke penyaringan Sampel diaduk hingga homogen
Kertas saring dicuci atau saringan dengan 3 x 10 mL aquadest
Kertas saring dipindahkan secara hati-hati ke wadah timbang aluminium
Sampel dimasukkan ke dalam oven pada suhu 105oC selama 1 jam
Cawan penguap didinginkan selama 15 menit di dalam desikator
Ditimbang berat cawan
Selesai Apakah berat
3.4.3 Analisa nilai VSS
Adapun prosedur analisis VSS adalah:
1.
Setelah terbakar sempurna atau bebas asap, selanjutnya sampel diabukandi dalam furnace pada suhu 550oC selama 1 jam.
2.
Setelah 1 jam, furnace dimatikan dan sampel diambil setelah suhufurnace sekitar 100oC dan disimpan di dalam desikator selama 15 menit
lalu ditimbang.
3.
Kandungan VSS dapat dihitung berdasarkan rumus sebagai berikut:mL sampel, volume
1000 B) -(A volatil/L
rsuspensi padatan te
mg
3.4.3.1Flowchart analisa VSS
Mulai
Dimasukkan cawan hasil analisis TSS ke dalam furnace
Selesai
Dipanaskan pada suhu 550 oC selama 1 jam
Didinginkan cawan penguap di dalam desikator hingga suhunya mencapai suhu kamar
Dtimbang berat cawan
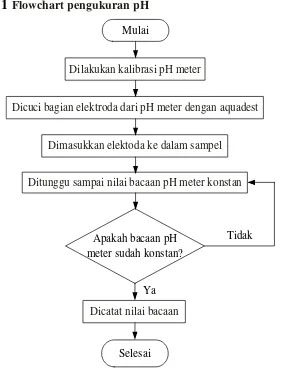
3.5 PROSEDUR PENGAMATAN 3.5.1 Pengukuran pH
Adapun prosedur analisa pH adalah:
1.
Kalibrasi pH meter dilakukan ke dalam pH 4, pH 7, dan pH 10.2.
Bagian elektroda dari pH meter dicuci dengan aquadest.3.
Elektroda dimasukkan ke dalam sampel yang akan diukur pH-nya.4.
Nilai bacaan pH meter ditunggu sampai konstan lalu dicatat nilaibacaannya
3.5.1.1
Flowchart pengukuran pH MulaiSelesai
Dilakukan kalibrasi pH meter
Dicuci bagian elektroda dari pH meter dengan aquadest
Dimasukkan elektoda ke dalam sampel
Ditunggu sampai nilai bacaan pH meter konstan
Apakah bacaan pH meter sudah konstan?
Dicatat nilai bacaan
Tidak
Ya
3.5.2 Pengukuran volume biogas
BAB IV
HASIL DAN PEMBAHASAN
4.1 KARAKTERISTIK LIMBAH ORGANIK DAN KOTORAN SAPI
Penelitian ini menggunakan bahan baku sampah sayuran yaitu kubis dan sawi putih yang diperoleh dari pasar tradisional dan kotoran sapi dari peternakan sapi. Komponen dan komposisi yang terdapat pada sampah sayuran (Tabel 4.1) dan kotoran sapi (Tabel 4.2) dapat dilihat pada tabel di bawah ini.
Tabel 4.1 Komponen dan komposisi sampah sayuran [13]
No. Komponen Komposisi
1. Air (%) 30 – 60
2. Lemak (mg/g sampah sayuran) 0,02 gr 3. Protein (mg/g sampah sayuran) 1,4 gr 4. Karbohidrat (mg/g sampah sayuran) 5,3 gr
5. Rasio C/N 18,44
Tabel 4.2 Komponen dan komposisi kotoran sapi [6]
No. Komponen Komposisi (%)
1. Air 20 - 70
2. Lemak 2,65
3. Protein 6,71
4. Karbohidrat 36,64
5. Rasio C/N 16,6 - 25
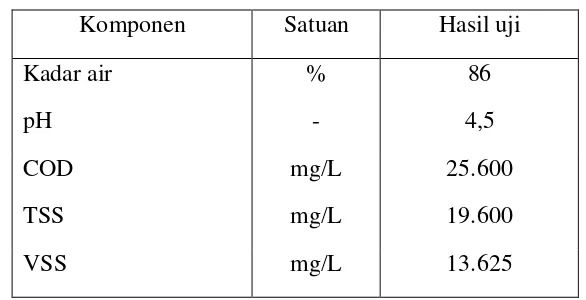
potensi substrat dalam proses digestasi anaerobik. Adapun komponen yang diukur dapat dilihat pada tabel 4.3.
Tabel 4.3 Komponen campuran sampah sayuran dan kotoran sapi Komponen Satuan Hasil uji
Tabel 4.3 menunjukkan campuran sampah sayuran dan kotoran sapi memiliki kandungan bahan organik yang tinggi. Hal ini dapat dilihat dari nilai COD dan TSS yang tinggi. Nilai COD dan TSS tersebut menunjukkan limbah ini bersifat mudah dibiodegradasi.
4.2 PROFIL TEMPERATUR FERMENTASI AKIBAT PENAMBAHAN
TRACE METAL
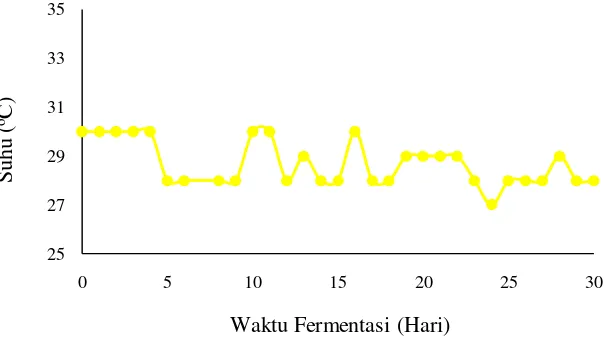
Temperatur merupakan faktor yang sangat mempengaruhi aktivitas mikroorganisme pada fermentasi anaerobik. Pada penelitian ini kondisi temperatur dijaga konstan pada kisaran 25-30 oC dan dilakukan penambahan trace metal dengan tujuan menyediakan kebutuhan mikronutrien bagi mikroorganisme yang tidak tersedia secara alami. Profil temperatur fermentasi terhadap penambahan trace metal dapat dilihat pada gambar 4.1a (tanpa trace metal), 4.1b (penambahan nikel), 4.1c (penambahan cobalt) dan 4.1d (penambahan Ni+Co).
Gambar 4.1b Grafik profil temperatur penambahan nikel
Gambar 4.1c Grafik Profil Temperatur Penambahan Cobalt
Gambar 4.1 (a,b,c,d) menunjukkan profil temperatur terhadap penambahan trace metal Nikel dan Cobalt pada fermentasi anaerobik selama 30 hari memiliki trend yang hampir sama bila dibandingkan dengan temperatur yang diperoleh pada fermentasi anaerobik tanpa penambahan trace metal. Pada umumnya digester anaerob skala kecil bekerja pada suhu antara 25 - 37oC karena pada suhu ini mikroorganisme tidak terlalu sensitif terhadap perubahan lingkungan, sehingga bakteri metanogenesis dapat bekerja untuk mencerna bahan organik dan memproduksi gas metana, karbon dioksida serta hidrogen sulfida [19].
4.3 PROFIL pH FERMENTASI AKIBAT PENAMBAHAN TRACE METAL
Derajat keasaman (pH) merupakan faktor yang sangat berpengaruh terhadap aktivitas mikroorganisme. Kondisi pH yang lebih kecil atau lebih besar akan menjadi toksik bagi bakteri anaerobik. Pada penelitian ini pH harus dijaga konstan pada kisaran 6,5 - 7,5 karena pH pada kondisi ideal pertumbuhan mikroorganisme antara 6,6 - 7,6. Profil pH fermentasi terhadap penambahan trace metal dapat dilihat pada gambar 4.2a (tanpa penambahan trace metal), 4.2b (penambahan nikel), 4.2c (penambahan cobalt) dan 4.2d (penambahan ni+co).
Gambar 4.2a Grafik profil pH fermentasi tanpa trace metal 5
5,5 6 6,5 7
0 5 10 15 20 25 30
pH
Gambar 4.2b Grafik profil pH fermentasi penambahan nikel
Gambar 4.2c Grafik profil pH fermentasi penambahan cobalt
Gambar 4.2d Grafik profil pH fermentasi penambahan Ni+Co 5
5,5 6 6,5 7
0 5 10 15 20 25 30
pH
Waktu Fermentasi (Hari)
5 5,5 6 6,5 7
0 5 10 15 20 25 30
pH
Waktu Fermentasi (Hari)
5 5,5 6 6,5 7
0 5 10 15 20 25 30
pH
Gambar 4.2 (a,b,c,d) menunjukkan trend profil pH dengan penambahan trace metal yang hampir sama bila dibandingkan dengan tanpa penambahan trace metal. pH sebelum fermentasi untuk semua variasi dikondisikan pada pH 6,5. Setelah fermentasi digester anaerob dioperasikan diperoleh pada hari ke-2 terjadi penurunan pH dari kondisi awal untuk semua perlakuan. Hal ini terjadi disebabkan karena terbentuknya asam-asam pada tahap asidogenesis dan asetogenesis. Kondisi pH yang menurun dari pH sebelum fermentasi tidak mendukung terhadap syarat pH dalam aktivitas bakteri metanogenik dalam fermentasi anaerobik secara batch karena dapat menurunkan aktivitas bakteri metanogenik. Hal ini menyebabkan perlunya dilakukan penambahan NaHCO3(buffer) yang dapat meningkatkan nilai pH yang dibutuhkan oleh mikroba dan mempertahankan kondisi pH [20].Pada grafik dapat dilihat perolehan pH setelah penambahan NaHCO3mengalami peningkatan setelah hari ke-2. pH yang diperoleh sampai dengan 30 hari fermentasi berada pada kondisi pH ideal mikroba bertumbuh.
4.4 PENGARUH PENAMBAHAN TRACE METAL TERHADAP
PRODUKSI BIOGAS
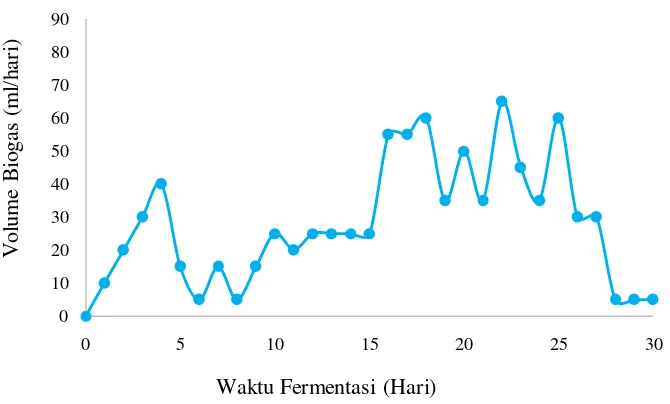
4.4.1 Pengaruh penambahan trace metal terhadap produksi biogas harian
Gambar 4.3a Grafik tanpa trace metal terhadap produksi biogas harian
Gambar 4.3c Grafik pengaruh penambahan cobalt terhadap produksi biogas harian
Gambar 4.3d Grafik pengaruh penambahan Ni+Co terhadap produksi biogas harian
Gambar 4.3 (a,b,c,d) menunjukkan pengaruh penambahan trace metal terhadap volume biogas yang diamati setiap hari selama 30 hari. Grafik4.3a (sebagai kontrol) memiliki kecenderungan yang sama dengan grafik dengan penambahan trace metal. Produksi biogas yang dihasilkan perharinya mengalami fluktuasi. Fluktuasi produksi biogas yang dihasilkan sangat dipengaruhi oleh aktivitas mikroorganisme anaerob. Kenaikan yang terjadi mengindikasikan bahwa mikroorganisme dalam fermentor
telah beradaptasi dengan baik sedangkan penurunan yang terjadi memungkinkan mikroorganisme sedang beradaptasi terhadap kondisi didalam fermentor. Pertumbuhan mikroorganisme selama fermentasi akan tetap terjadi apabila terdapatnya elemen khusus (trace metal) yang dibutuhkan oleh mikroorganisme untuk menguraikan beban organik [22]. Menurut Aresta et al , 2002 bahwa setiap logam baik Fe, Ni maupun Co akan menghasilkan efek yang berbeda pada komposisi biogas sesuai dengan peran enzim masing-masing logam dalam konsentrasi yang diizinkan [23].Pada penelitian ini, apabila ditinjau dari produksi biogas harian dapat disimpulkan bahwa penambahan trace metal tidak berpengaruh secara signifikan.
4.4.2 Pengaruh penambahan trace metal terhadap produksi biogas kumulatif
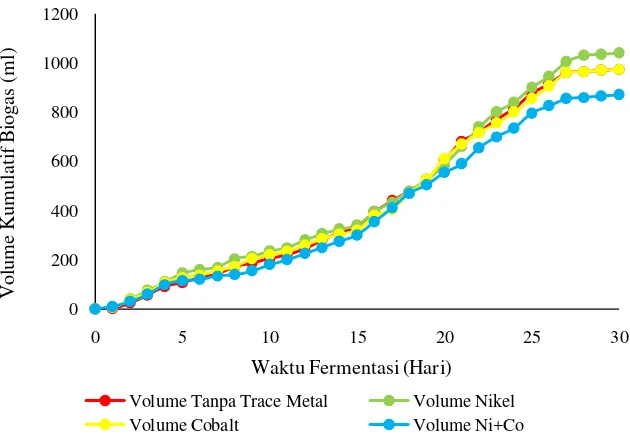
Pengaruh penambahan trace metal terhadap produksi biogas kumulatif yang terbentuk pada digester kontrol dan uji dapat dilihat pada gambar 4.4.
Gambar 4.4 Grafik pengaruh penambahan trace metal terhadap produksi biogas kumulatif
Gambar 4.4 menunjukkan volume kumulatif biogas yang dihasilkan dengan penambahan trace metal nikel lebih besar jumlahnya dibandingkan dengan volume biogas kumulatif yang dihasilkan pada tanpa penambahan trace metal. Grafik di atas menunjukkan pertumbuhan mikroba secara signifikan di hari ke-15 dimana mikroorganisme yang telah mengalami adaptasi mulai memperbanyak diri untuk merombak bahan-bahan organik dalam fermentor. Total volume biogas untuk tanpa
0
Volume Tanpa Trace Metal Volume Nikel
Volume Cobalt Volume Ni+Co
penambahan trace metal (sebagai kontrol) sebesar 975 ml, penambahan nikel sebesar 1.040 ml, penambahan cobalt sebesar 975 ml dan penambahan ni+co sebesar 870 ml. Penambahan logam nikel menghasilkan lebih besar jumlah biogas secara kumulatif dikarenakan logam nikel berfungsi sebagai enzim untuk metabolisme CO, urea dan metanogenesis [16]. Hal ini menunjukkan bahwa pada penelitian ini ketersediaan trace metal nikel sangat dibutuhkan dalam fermentasi biogas. Berdasarkan perbedaan volume biogas kumulatif ini, dapat disimpulkan bahwa penambahan trace metal berpengaruh terhadap produksi biogas.
4.5 PENGARUH PENAMBAHAN TRACE METAL TERHADAP REDUKSI
COD, % REDUKSI COD
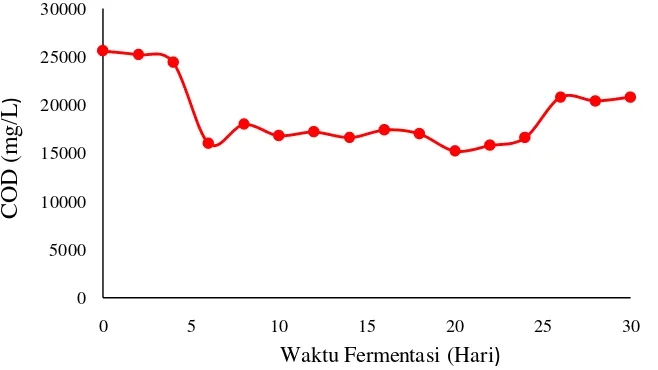
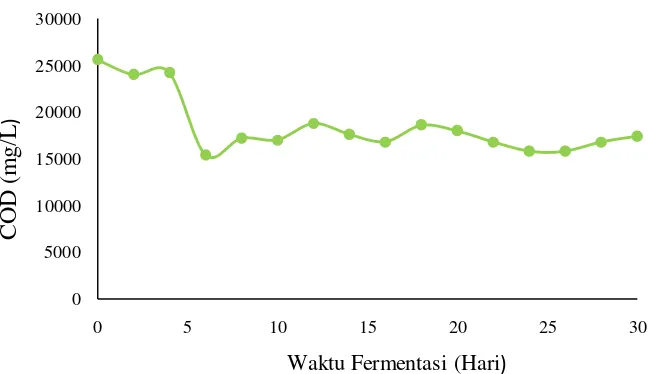
Chemical Oxygen Demand (COD) merupakan jumlah oksigen yang dibutuhkan oleh oksidator untuk mengoksidasi seluruh material baik organik maupun anorganik yang terdapat dalam air. Chemical Oxygen Demand dapat dijadikan sebagai salah satu parameter penentuan kinerja mikroba di dalam fermentor [24]. Pada penelitian ini dilakukan penambahan trace metal dengan konsentrasi yang telah ditentukan. Pengaruh penambahan trace metal terhadap reduksi COD untuk masing-masing perlakuan dapat dilihat pada gambar 4.5a (tanpa penambahan), 4.5b (penambahan nikel), 4.5c (penambahan cobalt) dan 4.5d (penambahan ni+co).
Gambar 4.5b Grafik pengaruh penambahan nikel terhadap reduksi COD
Gambar 4.5c Grafik pengaruh penambahan cobalt terhadap reduksi COD
Gambar 4.5 (a,b,c,d) memperlihatkan grafik yang memiliki trend yang hampir sama antara pengaruh penambahan trace metal dan tanpa penambahan trace metal terhadap reduksi COD. Nilai COD yang diperoleh mengalami fluktuasi. Penurunan nilai COD dapat disebabkan telah terjadinya proses hidrolisis, sedangkan peningkatan COD dapat terjadi karena adanya bahan organik yang baru mulai terdegradasi [25]. Setiap perlakuan menunjukkan fluktuasi yang berbeda. Hal ini dapat dikarenakan perbedaan penggunaan masing-masing trace metal oleh mikroorganisme dalam mendegrasi bahan-bahan organik. Besarnya % reduksi COD yang dialami masing-masing perlakuan dapat dilihat pada gambar 4.6.
Gambar 4.6a Grafik tanpa trace metal terhadap % reduksi COD
Gambar 4.6c Grafik pengaruh penambahan cobalt terhadap % reduksi COD
Gambar 4.6d Grafik pengaruh penambahan Ni+Co terhadap % reduksi COD Gambar 4.6 menunjukkan pengaruh penambahan trace metal terhadap % reduksi COD. Persen reduksi COD terbesar untuk tanpa trace metal terjadi pada hari ke 20 sebesar 40,63% ; penambahan nikel terjadi pada hari ke 6 sebesar 39,84% ; penambahan cobalt terjadi pada hari ke 14 sebesar 46,48% dan penambahan Ni+Co terjadi pada hari ke 12 sebesar 32,81%. Perbedaan besarnya persentase reduksi COD pada masing-masing perlakuan dipengaruhi oleh kinerja mikroorganisme. Kehidupan mikroorganisme yang diawali dengan tahap adaptasi belum dapat mendegradasi
senyawa organik dengan optimum. Pada tahap hidrolisis senyawa yang tidak larut seperti selulosa, protein dan lemak dipecah menjadi monomer (fragmen yang larut dalam air) [26] yang kemudian didegradasi lebih lanjut menjadi asam lemak volatil (VFA) [27]. Aktivitas mikroorganisme pada proses asidogenesis dan asetogenesis dalam memproduksi asam akan menciptakan kondisi yang penting bagi mikroorganisme penghasil metan. Adanya mikronutrien sesuai dengan konsentrasi yang dibutuhkan akan melangsungkan fermentasi secara optimum [4]. Namun, trace metal yang tersedia seperti nikel dan cobalt hanya bertujuan untuk meningkatkan produksi biogas, tidak berpengaruh pada perubahan metana pada reaktor biogas [28]. Pada penelitian ini dalam grafik dapat dilihat bahwa % reduksi COD tertinggi ditunjukkan oleh % reduksi COD dengan penambahan cobalt yang dicapai pada hari ke- 14.
4.6 PENGARUH PENAMBAHAN TRACE METAL TERHADAP REDUKSI
TSS, % REDUKSI TSS
TSS merupakan parameter yang menunjukkan banyaknya zat yang tersuspensi dalam volume tertentu di dalam air. TSS akan mengalami penurunan akibat aktivitas mikroorganisme.Menurunnya kadar TSS terjadi karena bahan organik mengalami degradasi pada saat proses hidrolisis. Selama proses hidrolisis, padatan tersuspensi berkurang karena telah berubah menjadi terlarut [29]. Pada gambar 4.7 akan ditunjukkan pengaruh penambahan trace metal terhadap reduksi TSS.
Gambar 4.7a Grafik tanpa trace metal terhadap reduksi TSS 0
Waktu Fermentasi (Hari)
Gambar 4.7b Grafik pengaruh penambahan nikel terhadap reduksi TSS
Gambar 4.7c Grafik pengaruh penambahan cobalt terhadap reduksi TSS 0
Waktu Fermentasi (Hari)
0
Waktu Fermentasi (Hari)
Gambar 4.7d Grafik pengaruh penambahan Ni+Co terhadap reduksi TSS Gambar 4.7 (a,b,c,d) memperlihatkan bahwa pengaruh penambahan trace metal memiliki kecenderungan yang sama dengan tanpa penambahan trace metal terhadap reduksi TSS. Perolehan total suspended solid pada grafik di atas mengalami fluktuasi untuk masing – masing perlakuan jika dibandingkan dengan tanpa penambahan trace metal. Penurunan nilai total suspended solid yang terjadi dikarenakan bahan-bahan organik mengalami degradasi pada saat proses hidrolisis. Pada proses hidrolisis, molekul kompleks yang ada dipecah menjadi molekul yang sederhana dan larut dalam air. Selama proses hidrolisis, padatan tersuspensi berkurang karena telah berubah menjadi terlarut yang selanjutnya digunakan pada tahap asidogenesis [25]. Adanya beberapa titik yang mengalami peningkatan total suspended solid terjadi karena kemungkinan bahan-bahan organik di dalam fermentor baru mulai terdegradasi. Setiap perlakuan menunjukkan fluktuasi yang berbeda, Hal ini dapat dikarenakan perbedaan penggunaan masing-masing trace metal oleh mikroorganisme dalam mendegrasi bahan-bahan organik. Besarnya % reduksi TSS yang dialami masing-masing perlakuan dapat dilihat pada gambar 4.8
0
Waktu Fermentasi (Hari)
Gambar 4.8a Grafik tanpa trace metal terhadap % reduksi TSS
Gambar 4.8b Grafik pengaruh penambahan nikel terhadap % reduksi TSS 0%
Waktu Fermentasi (Hari)
%
Waktu Fermentasi (Hari)
Gambar 4.8c Grafik pengaruh penambahan cobalt terhadap % reduksi TSS
Gambar 4.8d Grafik pengaruh penambahan Ni+Co terhadap % reduksi TSS Gambar 4.8 (a,b,c,d) menunjukkan pengaruh penambahan trace metal terhadap % reduksiTSS. Nilai % reduksi total suspended solid terbesar untuk semua perlakuan terjadi pada hari ke-30 yaitu untuk tanpa trace metal sebesar 88,78% ; trace metal nikel sebesar 88,67% ; trace metal cobalt sebesar 88,78% dan trace metal Ni+Co sebesar 85%. Rata-rata % reduksi total suspended solid terhadap pengaruh penambahan trace metal ditunjukkan pada gambar 4.9.
0%
Waktu Fermentasi (Hari)
%
Waktu Fermentasi (Hari)
Gambar 4.9 Rata-rata % reduksi TSS
Rata-rata % reduksi TSS tertinggi yang ditunjukkanpada gambar 4.8 diperoleh dengan penambahan trace metal nikel sebesar 46,20%. Menurut Sutarma, 2000 bahwa trace metal nikel berfungsi sebagai enzim untuk metabolisme mikroba dalam proses metanogenesis. Pada penelitian ini, penambahan trace metal sangat berpengaruh secara signifikan.
4.7 PENGARUH PENAMBAHAN TRACE METAL TERHADAP REDUKSI
VSS
VSS merupakan salah satu cara pengukuran mikroorganisme secara tidak langsung [30]. Konsentrasi volatile suspended solid dapat menjadi indikator pertumbuhan mikroorganisme aktif dalam reaktor.Pengaruh penambahan trace metal terhadap profil pertumbuhan mikroorganisme dapat dilihat pada Gambar 4.10
0%
Tanpa Trace Metal Nikel Cobalt Ni+Co
Gambar 4.10a Grafik tanpa trace metal terhadap reduksi VSS
Gambar 4.10b Grafik pengaruh penambahan nikel terhadap reduksi VSS 0
Waktu Fermentasi (Hari)
R
Waktu Fermentasi (Hari) Waktu Fermentasi (Hari)
Gambar 4.10c Grafik pengaruh penambahan cobalt terhadap reduksi VSS
Gambar 4.10d Grafik pengaruh penambahan Ni+Co terhadap reduksi VSS Gambar 4.10 (a,b,c,d) memperlihatkan pengaruh penambahan trace metal memiliki kecenderungan yang sama dengan tanpa penambahan trace metal terhadap volatile suspended solid. Nilai volatile suspended solid yang diperoleh mengalami fluktuasi untuk masing-msing perlakuan. Fluktuasi ini terjadi dikarenakan perbedaan penggunaan masing-masing logam oleh bakteri dalam mendegradasi bahan-bahan organik [25] dan dapat juga karena tidak adanya pengadukan yang dilakukan selama fermentasi berlangsung sehingga terjadinya penumpukan. Pada proses digesti
0
Waktu Fermentasi (Hari)
R
Waktu Fermentasi (Hari)
anaerob pengadukan berperan penting dalam mengembangbiakkan mikroorganisme dikarenakan dengan pengadukan substrat dalam fermentor akan homogen dan merata sehingga proses perombakan akan lebih efektif dan menghindari padatan-padatan mengendap yang dapat mengurangi keefektifan proses digesti [31]. Pada perlakuan tanpa penambahan trace metal diperoleh konsentrasi VSS sebesar 1.280 – 16.780 mg/L ; penambahan trace metal nikel 4.580 – 13.880 mg/L; penambahantrace metal cobalt sebesar 2.280 – 16.540 mg/L dan pada penambahan kombinasi Ni+Cosebesar 2.500 –16.480 mg/L.Profil pertumbuhan mikroba terbaik untuk setiap perlakuan dapat dilihat pada gambar 4.11.
Gambar 4.11 Pengaruh penambahan trace metal terhadap pertumbuhan mikroba terbaik masing-masing perlakuan
Gambar 4.11 memperlihatkan bahwa pertumbuhan mikroba terbaik untuk perlakuan tanpa trace metal diperoleh pada hari ke-2 sebesar 16.780 mg/L; penambahan trace metal nikel diperoleh pada hari ke-18 sebesar 13.880 mg/L ; penambahan trace metal cobalt pada hari ke-2 sebesar 16.540 mg/L dan penambahan kombinasi Ni+Co diperoleh pada hari ke-18 sebesar 16.480 mg/L. Pada penelitian ini, penambahan trace metal berpengaruh terhadap pertumbuhan mikroorganisme.
.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Adapun kesimpulan yang dapat diperoleh dari penelitian pembuatan biogas dari sampah organik dan kotoran sapi dengan menambahkan trace metal adalah:
1. % Reduksi COD tertinggi diperoleh dengan penambahan trace metal cobalt yang diperoleh pada hari ke-14 sebesar 46.48%.
2. % Reduksi TSS tertinggi dieroleh pada hari ke-30 dengan penambahan trace metal cobalt sebesar 88,78%.
3. Konsentrasi VSS tertinggi diperoleh dengan penambahan trace metal cobalt pada hari ke-2 sebesar 16.540 mg/L.
4. Volume biogas terbesar diperoleh dengan penambahan trace metal cobalt sebesar 85 mL.
5.2 Saran
Adapun saran yang dapat diberikan untuk peneliti berikutnya adalah:
1. Dilakukan analisa awal terhadap bahan baku yang digunakan dalam penelitian terhadap semua parameter yang dibutuhkan.
2. Digunakan pengaduk pada reaktor untuk mengekfektifkan kerja mikroorganisme.
3. Dilakukan dua tahap pembuatan biogas secara batch untuk memaksimalkan proses pembuatan biogas.