34
Submitted : 23 Oktober 2020 Revised : 29 November 2020 Accepted : 15 Desember 2020
SINTESIS NANOPARTIKEL PERAK MELALUI REDUKSI SPONTAN MENGGUNAKAN
REDUKTOR ALAMI EKSTRAK KULIT LEMON SERTA KARAKTERISASINYA SEBAGAI
ANTIFUNGI DAN ANTIBAKTERI
Widya Ernayati Kosimaningrum, Alia Badra Pitaloka
*, Afif Sena Hidayat, Wahidatun
Aisyah, Syahrul Ramadhan, Malik Abdul Rosyid
Jurusan Teknik Kimia, Fakultas Teknik, Universitas Sultan Ageng Tirtayasa
Jl. Jendral Sudirman km. 03, Cilegon, 42435, Banten
*
Email:
[email protected]
Abstrak
Nanopartikel perak, Ag0, merupakan bahan antimikroba spektrum luas dengan resiko resistensi yang sangat rendah. Dalam penelitian ini nanopartikel perak, Ag0, disintesis melalui reduksi spontan larutan Ag+ menggunakan reduktor alami ekstrak kulit lemon. Ekstraksi dilakukan pada suhu 60oC selama 10 menit dalam pelarut air. Ekstraksi kulit lemon melibatkan variasi massa serbuk kulit lemon yaitu 2,5; 5; 7,5; dan 10 gram sehingga menghasilkan konsentrasi zat-zat reduktor dalam ekstrak yang bervariasi. Sintesis nanopartikel perak dilakukan pada suhu 60oC selama 20 menit dengan mencampurkan larutan Ag+ 0,1 M dengan larutan ekstrak kulit lemon dengan berbagai konsentrasi. Hasil sintesis berupa larutan koloidal berwarna cokelat gelap hingga kehitaman yang mengindikasikan pembentukan mikro hingga nanopartikel Ag0 dalam larutan. Gambar SEM dengan perbesaran 5000 kali mengkonfirmasi adanya partikel-partikel speris dengan kisaran ukuran 100 nm hingga 1 µm. Banyaknya Ag0 yang terbentuk, yang dicirikan dengan semakin pekatnya warna larutan, berbanding lurus dengan konsentrasi prekursor ekstrak kulit lemon. Larutan nanopartikel Ag0 menunjukkan efektivitasnya sebagai antifungi dalam pengamatan selama lima hari. Larutan nanopartikel Ag0 juga menunjukkan sifat antibakteri yang sangat efektif berdasarkan pengujian terhadap E. coli.
Kata kunci: Antibakteri, Antifungi, Ektrak Kulit Lemon, Nanopartikel Perak
Abstract
The silver nanoparticle, Ag0, is a broad-spectrum antimicrobial material with a very low risk of resistant. In this study, the silver nanoparticles, Ag0 were synthesized through spontaneous reduction of Ag+ solution using natural reductor lemon peel extract. Extraction was carried out at a temperature of 60oC for 10 minutes in a water solvent. The extraction of lemon peel involved a variation in the mass of lemon peel powder of 2.5; 5; 7.5; and 10 grams resulted in varying concentrations of reductor substances in the extract. Synthesis of silver nanoparticles was carried out at 60oC for 20 minutes by mixing Ag+ 0.1 M solution with lemon peel extract solution with various concentrations. Synthesis resulted in a dark brown to blackish colloidal solution which was indicating the formation of micro to Ag0 nanoparticles in the solution. SEM image with a magnification of 5000 times confirmed the presence of spherical
particles with a size range of 100 nm to 1 μm. The amount of Ag0 formed, which was characterized by the increasing concentrated color of the solution, was directly proportional to the precursor concentration of lemon peel extract. Ag0 nanoparticle solution demonstrated its effectiveness as antifungal in five-day observations. Ag0 nanoparticle solution also showed highly effective antibacterial properties based on testing against E. coli.
Key words: Antibacterial, Antifungal, Lemon Peel Extract, Silver Nanoparticles
JURNAL INTEGRASI PROSES
35
1. PENDAHULUANPerak merupakan logam mulia yang sejak lama telah dikenal memiliki aktivitas antimikroba. Ion perak sangat reaktif bereaksi dengan dinding sel bakteri dan menyebabkan kematian sel (Chernousova and Epple, 2013). Ion perak juga dapat menghambat replikasi bakteri dengan mendenaturasi DNA bakteri yang menyebabkan kerusakan dan kematian bakteri (Rai et al., 2016). Penggunaan perak sebagai antibakteri telah dikenal sejak tahun 1000 SM (Khandelwal et al., 2014). Sebelum antibiotik ditemukan, perak sudah digunakan sebagai obat luka dan luka bakar (Rai et al., 2016).
Nanopartikel perak yang memiliki ukuran antara 1–100 nm lebih menarik perhatian karena memiliki sifat-sifat yang dapat meningkatkan efektivitas dan efisiensinya (Lee and Jun, 2019). Sifat-sifat unggul khas nanopartikel perak antara lain adalah luas permukaan yang tinggi, sehingga dapat memaksimalkan distribusi situs aktif antivirus dan antibakteri (Khandelwal et al., 2014) pada suatu permukaan. Nanopartikel perak dengan ukurannya yang sangat kecil mudah berinteraksi atau menempel pada tubuh bakteri atau virus (Rai et al., 2016). Nanopartikel perak lebih reaktif dan lebih efektif sebagai antimikroba bakteri, virus, dan fungi patogen dengan spektrum luas. Nanopartikel perak juga tahan terhadap perubahan temperatur dan kelembaban dibandingkan dengan antimikroba konvensional serta tidak menginduksi resistensi bakteri (Rai et al., 2014). Selain itu, nanopartikel perak dapat terdeposit atau tertahan pada permukaan sehingga berpotensi sebagai antibakteri yang efektif dalam jangka waktu yang lebih lama (Marassi et al., 2018). Nanopartikel perak telah menunjukkan aplikasi yang menjanjikan dalam bidang-bidang kesehatan, lingkungan, dan industri (Khandelwal et al., 2014) di antaranya sebagai bahan terapi dan antibakteri dalam perangkat medis, bahan aditif antiseptik dalam kemasan atau tekstil, pelapis ubin, dan sistem pemurnian air (Kowalska-Góralska et al., 2015).
Proses pembuatan nanopartikel perak dapat dikelompokkan sebagai metode top-down dan metode bottom-up (Lee and Jun, 2019). Dalam metode top-down, logam perak yang berukuran makro dipecah hingga berukuran nano dengan metode fisika seperti ablasi laser (Suriati et al., 2014). Keuntungan dari metode ini adalah bebas bahan kimia. Namun kekurangannya adalah memerlukan peralatan yang kompleks, memerlukan energi dan biaya yang tinggi. Pembuatan nanopartikel perak umumnya menggunakan metode bottom-up. Dalam metode ini, ion-ion perak Ag+ dalam larutan membentuk atom-atom perak Ag0 yang kemudian mengalami nukleasi dan tumbuh menjadi partikel-partikel Ag yang berukuran nano (García-Barrasa et al., 2011) yang disebut nanopartikel perak. Metode bottom-up
menggunakan metode kimia dengan penambahan zat reduktor dan zat penstabil atau metode biologi melalui biosintesis dengan bakteri. Dalam hal ini, zat reduktor mengubah larutan ion perak Ag+ menjadi larutan koloidal dari partikel-partikel perak Ag0 (Lee and Jun, 2019). Metode bottom-up merupakan metode sintesis nanopartikel yang lebih praktis karena dapat dilakukan secara sederhana.
Metode kimia pembuatan nanopartikel perak menggunakan berbagai macam reduktor seperti senyawa sodium borohidrida (metode Brust-Schiffrin), asam sitrat (metode Turkevich), glukosa, hidrazina, hirazina hidrat, asam askorbat, etilena glikol, polifenol, dan lain sebagainya (Lee and Jun, 2019). Pemilihan reduktor dalam pembuatan nanopartikel perak tidak hanya memperhatikan efektivitasnya saja namun juga perlu memperhatikan sifat-sifat lain seperti ramah lingkungan, keamanan, dan ketersediaannya. Berdasarkan pertimbangan ini, pemilihan senyawa-senyawa reduktor yang bersumber dari bahan alami seperti asam sitrat, asam askorbat, polifenol, dan glukosa menjadi lebih tepat. Ekstrak-ekstrak berbagai jenis tumbuhan dari bagian-bagian seperti buah, kulit buah, biji, daun, batang, kulit batang, atau akar dapat menjadi sumber zat reduktor alami yang melimpah. Beberapa penelitian telah menunjukkan efektivitas reduktor alami berbasis ekstrak buah lemon (Prathna et al., 2011), ekstrak kulit buah jeruk dan anggur (Soto et al., 2019), getah jarak (Jatropa curcas) (Bar et al., 2009) ekstrak daun sirih (Prabha et al., 2014), ekstrak kayu manis (Premkumar et al., 2018), ekstrak aloe vera (Chandran et al., 2006) dan ekstrak daun kelor (El-Khadragy et al., 2018) dalam pembuatan nanopartikel perak. Bahan reduktor alami memiliki sifat yang ramah lingkungan sehingga dapat mengurangi dampak pencemaran zat kimia berbahaya. Selain itu ketersediaan yang melimpah akan membuat sintesis lebih ekonomis dan menjamin sustainabilitasnya.
Dalam penelitian ini, akan dilakukan pembuatan nanopartikel perak dengan metode bottom-up secara kimia dari larutan perak nitrat dengan menggunakan reduktor alami ekstrak kulit lemon (Citrus limon). Buah lemon dan kulitnya mengandung asam sitrat, asam askorbat, senyawa polifenol, dan senyawa-senyawa lain yang dapat bertindak sebagai zat reduktor. Selain itu, ketersediaan limbah kulit lemon yang melimpah dan belum dimanfaatkan secara optimal memotivasi pemilihan material kulit lemon sebagai sumber reduktor alami. Penelitian ini melibatkan tiga tahap utama yaitu 1) ekstraksi kulit lemon menggunakan pelarut air, 2) sintesis nanopartikel dengan ekstrak kulit lemon, dan 3) uji aktivitas larutan koloid nanopartikel perak sebagai antibakteri dan antifungi. Keterbaruan dalam penelitian ini adalah adanya studi pengaruh massa
36
serbuk kulit lemon terhadap konsentrasi zat-zatreduktor dalam ekstrak serta pengaruhnya terhadap kadar dan efektivitas antibakteri dan antifungi nanopartikel perak yang dihasilkan.
2. METODE PENELITIAN 2.1 Bahan
Bahan yang digunakan dalam penelitian ini adalah limbah kulit lemon, perak nitrat (AgNO3), reagen Folin-Ciocalteu, asam galat, kalium iodida (KI), kalium periodat (KIO3), natrium hidroksida, (NaOH), asam oksalat, (H2C2O4), dan natrium tiosulfat (Na2S2O3) yang dibeli dari Merck, serta natrium karbonat (Na2CO3) dari Pudak scientific.
2.2 Prosedur Penelitian
2.2.1 Preparasi serbuk kulit lemon
Kulit lemon dipotong sehingga menjadi ukuran kecil. Kemudian, potongan kulit lemon dikeringkan dalam oven vakum Thermoscientific pada suhu 60oC selama 48 jam. Kulit lemon kering dihaluskan dan diayak dengan menggunakan saringan ukuran 60 mesh.
2.2.2 Ekstraksi serbuk kulit lemon
Ekstraksi serbuk kulit lemon menggunakan metode Soto et al. dengan modifikasi. Sebanyak masing-masing 2,5; 5; 7,5; dan 10 gram serbuk kulit lemon dicampur dengan 100 mL akuades di dalam erlenmeyer. Campuran kemudian dipanaskan pada suhu 60oC selama 10 menit (Soto et al., 2019) dengan pengadukan secara kontinyu. Kemudian campuran disaring menggunakan penyaring Buchner.
2.2.3 Analisis fenolik dalam ekstrak serbuk kulit lemon Setiap ekstrak terlebih dahulu disaring dengan PTFE filter 0,2 mikron. Sebanyak 0,16 mL ekstrak dimasukkan ke dalam labu ukur 50 mL kemudian ditambahkan 30 mL air dan 2,5 mL reagen Folin-Ciocalteu, larutan dikocok dan didiamkan selama 8 menit. Ke dalam larutan kemudian ditambahkan larutan Na2CO3 sebanyak 7,5 mL. Selanjutnya ditambahkan akuades hingga batas tera. Larutan dibiarkan selama 2 jam. Kemudian dilakukan pengukuran absorbansi pada panjang gelombang 765 nm dengan spektrofotometer visible Thermoscientific. Pengukuran dibandingkan terhadap larutan standar asam galat dengan konsentrasi 5,6 mg/L.
2.2.4 Analisis vitamin C dalam ekstrak serbuk kulit lemon
Sampel ekstrak kulit lemon masing-masing sebanyak 2 mL ditambahkan dengan akuades sebanyak 30 mL kemudian ditambahkan10 mL KI 10 %, 8 mL KIO3 0,037 M, dan 2 mL asam sulfat 2 M. Larutan kemudian dititrasi dengan natrium tiosulfat,
Na2S2O3. Titrasi yang sama dilakukan juga terhadap blangko. Pembakuan natrium tiosulfat menggunakan KIO3 untuk menentukan konsentrasinya. Setiap penentuan sampel dan pembakuan dilakukan secara duplo.
2.2.5 Analisis asam sitrat dalam ekstrak serbuk kulit lemon
Penentuan kadar asam sitrat menggunakan metode titrasi asam basa. Sampel ekstrak kulit lemon masing-masing sebanyak 2 mL dimasukkan ke dalam erlenmeyer dan ditambahkan dengan 10 mL akuades. Kemudian ditambahkan indikator fenolftalein sebanyak 3 tetes. Campuran dititrasi menggunakan NaOH. Titrasi yang sama juga dilakukan terhadap blangko. Konsentrasi NaOH ditentukan melalui standarisasi dengan larutan standar asam oksalat. Setiap penentuan sampel dan pembakuan dilakukan secara duplo.
2.2.6 Sintesis nanopartikel perak
Sintesis nanopartikel menggunakan metode yang digunakan oleh Soto et al. dengan modifikasi. Sebanyak 10 mL masing-masing larutan ekstrak (E2.5, E5, E7.5, dan E10) dicampur dengan 10 mL larutan AgNO3 0,1 M. Campuran dipanaskan pada suhu 60oC selama 20 menit (Soto et al., 2019). Setelah pemanasan, campuran disaring dan diperoleh filtrat cokelat gelap kehitaman yang merupakan larutan koloid perak, Ag0, mikro hingga nanopartikel. Larutan Ag0 yang dihasilkan selanjutnya diberi kode Ag0-E2.5, Ag0-E5, Ag0-E7.5, dan Ag0-E10.
2.2.7 Analisis SEM-EDX
Larutan Ag0 hasil sintesis diendapkan dengan sentrifus diikuti dekantasi untuk memperoleh endapan kental Ag0. Endapan dikeringkan pada suhu ruang hingga kering. Kemudian, endapan digerus sehingga menjadi serbuk. Selanjutnya serbuk endapan Ag0 dianalisis menggunakan SEM Jeol JSM-IT 100 dan EDX, Oxford Instruments.
2.2.8 Uji aktivitas antifungi
Uji antifungi menggunakan metode pemaparan media dalam cawan petri pada udara terbuka selama beberapa hari. Media kontrol yang digunakan adalah larutan ekstrak kulit lemon, sedangkan media uji adalah campuran ekstrak kulit lemon dengan larutan nanopartikel Ag0 hasil sintesis dengan rasio volume 10:1. Media kontrol dan media uji, masing-masing, ditempatkan dalam cawan petri. Pengamatan pertumbuhan fungi dilakukan secara visual setiap hari. Set percobaan uji antifungi dicantumkan dalam Tabel 1.
37
Tabel 1. Percobaan uji aktivitas antifungiPerc. Media kontrol Media uji 1 Ekstrak dari 2.5 g serbuk
kulit lemon/ E2.5 E2.5 + Ag 0-E2.5 2 Ekstrak dari 5 g serbuk
kulit lemon/E5 E5 + Ag 0-E5 3 Ekstrak dari 7.5 g serbuk
kulit lemon/E7.5 E7.5 + Ag 0-E7.5 4 Ekstrak dari 10 g serbuk
kulit lemon/E10 E10 + Ag 0-E10
2.2.9 Uji aktivitas antibakteri
Uji antibakteri menggunakan isolat bakteri E. coli yang telah diencerkan 1000 kali sehingga diperoleh jumlah koloni awal sebesar 274 CFU/20 mL. Larutan bakteri awal sebanyak 10 mL selanjutnya dikultur dengan inkubasi pada suhu 37oC selama 48 jam dalam beberapa cawan petri yang berisi medium agar. Uji bakteri dilakukan masing-masing terhadap larutan Ag0 hasil sintesis, ekstrak kulit lemon sebagai kontrol 1 dan air steril sebagai kontrol 2.
3. HASIL DAN PEMBAHASAN
Ekstraksi serbuk kulit lemon dengan pelarut air menghasilkan larutan ekstrak berwarna kuning cerah. Hal ini karena kulit lemon mengandung pigmen kuning yang terlarut dalam air dan cukup stabil (Chen et al., 2019). Dalam penelitian ini, ekstraksi dilakukan pada suhu 60oC selama 10 menit dengan memvariasikan penambahan massa serbuk lemon yaitu 2,5; 5; 7,5 dan 10 gram masing-masing ke dalam 100 mL air. Selanjutnya, ekstrak dari berbagai massa serbuk ini diberi kode berturut-turut E2.5, E5, E7.5, dan E10.
Gambar 1. Ekstrak kulit lemon dari berbagai massa serbuk kulit lemon: a. 2,5, b. 5, c. 7,5, dan d. 10 gram Setiap larutan ekstrak kulit lemon yang dihasilkan menunjukkan intensitas warna kuning yang semakin pekat dengan meningkatnya massa serbuk lemon dalam ekstraksi. Hal ini menunjukkan peningkatan kuantitas zat-zat dalam serbuk kulit lemon yang terlarut/terekstrak dalam pelarut air yang relevan dengan konsentrasi zat-zat terekstrak. Dengan demikian, setiap larutan ekstrak yang dihasilkan mengandung zat-zat terlarut dengan konsentrasi yang
linier dengan peningkatan massa serbuk lemon yang diekstraksi.
3.1 Kandungan Senyawa Fenolik
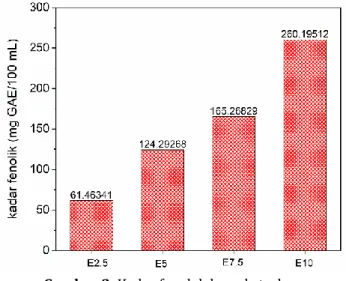
Analisis senyawa fenolik dalam larutan ekstrak kulit lemon menggunakan metode Folin-Ciocalteu dan menggunakan ekuivalensi asam galat yaitu Gallic Acid Equivalence (GAE). Hasil analisa menunjukkan relevansi peningkatan kadar fenol dengan banyaknya serbuk lemon yang diekstraksi. Semakin pekat ekstrak, maka semakin tinggi kadar fenol yang terukur (Gambar 2). Sedangkan kadar fenol larut air rata-rata dalam per gram serbuk kulit lemon adalah sebesar 24,37 ± 1,45 mg GAE/gram serbuk kulit lemon. Penelitian Elkhatim, et al. 2018 menunjukkan kadar senyawa fenolik dalam kulit lemon sebanyak 49,8 mg GAE/gram kulit lemon (Sir Elkhatim et al., 2018). Sedangkan penelitian Li et al. 2006 menunjukkan kadar senyawa fenolik dalam kulit lemon kering adalah 0,4357 mg GAE/gram serbuk kulit lemon (Li et al., 2006). Perbedaan cukup besar ini menunjukkan bahwa kadar total fenolik dalam penelitian ini dan juga penelitian Elkhatim, et al. 2018 adalah kadar total kasar karena pengukuran dilakukan pada crude ekstrak tanpa melakukan pemurnian terlebih dahulu. Sehingga, kandungan gula dan senyawa organik dalam ekstrak dapat ikut bereaksi dengan reagen Folin-Ciocalteu (Li et al., 2006) dan memberikan nilai yang besar.
Gambar 2. Kadar fenol dalam ekstrak
3.2 Kandungan Senyawa Asam Askorbat (Vitamin C) Dan Asam Sitrat
Asam askorbat merupakan zat yang berpotensi terdapat dalam kulit lemon. Dalam penelitian ini, analisis asam askorbat dalam larutan ekstrak kulit lemon menggunakan metode titrasi iodometri. Hasil Analisis menunjukkan kadar asam askorbat dalam larutan ekstrak kulit lemon berkisar antara 0,07–0,38 % w/v (Gambar 3) atau 28–77 mg asam askorbat/100 gram serbuk kulit lemon. Penelitian Elkhatim et al.,
38
2018, menunjukkan kadar asam askorbat dalam kulitlemon adalah sebesar 58,59 mg asam askorbat/100 gram kulit lemon. Perbedaan kadar asam askorbat ini dapat disebabkan oleh jenis atau varietas lemon yang berbeda.
Asam sitrat juga merupakan senyawa yang banyak ditemukan dalam buah lemon terutama dalam daging buahnya (Jamil et al., 2015). Namun penelitian ini menunjukkan bahwa kulit lemon juga mengandung asam sitrat. Analisis asam sitrat menggunakan metode titrasi asam basa. Hasil Analisis menunjukkan kandungan asam sitrat dalam serbuk kulit jeruk rata-rata adalah 10,84 ±1.68 % w/w. sedangkan kadar asam sitrat dalam masing-masing larutan ekstrak berkisar antara 0,33 – 1,02 % w/v (Gambar 3).
Gambar 3. Kadar asam askorbat dan asam sitrat dalam ekstrak
3.3 Sintesis Nanopartikel Perak
Sintesis nanopartikel perak menggunakan metode reduksi spontan ion perak, Ag+, dengan reduktor alami ekstrak kulit lemon berbasis pelarut air yang telah dipreparasi seperti telah dijelaskan sebelumnya. Terdapat 4 variasi larutan nanopartikel Ag0 yang dihasilkan yaitu larutan Ag0-E2.5, larutan Ag0-E5, larutan Ag0-E7.5, dan larutan Ag0-E10 yang berturut-turut dihasilkan dari reaksi reaksi larutan Ag+ dengan larutan E.25, E5, E7.5, dan E10. Reaksi larutan ekstrak kulit lemon dengan larutan Ag+ menghasilkan produk larutan berwarna coklat gelap hingga kehitaman yang mengindikasikan pembentukan mikro hingga nanopartikel Ag0 dalam larutan. Kepekatan warna larutan menunjukkan semakin banyaknya nanopartikel Ag0 yang terbentuk. Dalam hal ini larutan ekstrak kulit lemon dengan kandungan zat-zat terlarut yang tinggi menghasilkan larutan nanopartikel Ag0 paling pekat, larutan Ag0-E10>Ag0-E7.5>Ag0-E5>Ag0 -E2.5, seperti ditunjukkan pada Gambar 4. Kepekatan menurun dengan penurunan konsentrasi ekstrak kulit lemon. Hasil ini menunjukkan hubungan yang linier antara kandungan reduktor dalam ekstrak dengan larutan Ag0 yang dihasilkan.
Gambar 4. Larutan nanopartikel Ag0 hasil reduksi larutan Ag+ dengan ekstrak kulit lemon
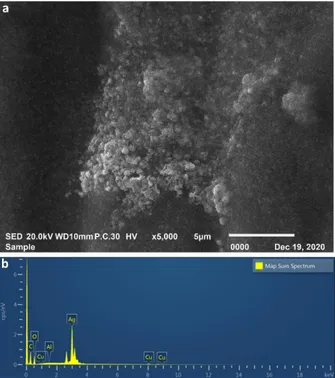
Gambar 5. a. Morfologi serbuk Ag0 yang diperoleh dari larutan nanopartikel Ag0 hasil reaksi antara larutan Ag+ dan ektrak kulit lemon E5, b. spektrum
EDX yang mengonfirmasi keberadaan Ag0 Ekstrak kulit lemon berbasis pelarut air telah dianalisis mengandung senyawa fenolik, asam sitrat, dan askorbat. Senyawa-senyawa ini merupakan reduktor yang mampu mereduksi larutan Ag+ secara spontan. Dari hasil analisis dalam penelitian ini, kadar senyawa fenolik, asam sitrat, dan asam askorbat meningkat secara linier dengan banyaknya massa serbuk lemon yang diekstraksi.
Gambar 5.a. menunjukkan hasil pengukuran SEM yang memberikan konfirmasi pembentukan mikro hingga nanopartikel Ag0 dalam larutan hasil sintesis. Gambar SEM dengan perbesaran 5000 kali menunjukkan partikel-partikel speris berukuran kisaran 100 nm hingga 1 µm yang saling berdekatan satu sama lain (beraglomerasi). Sedangkan Gambar 5.b adalah spektrum EDX yang memberikan informasi komposisi elemental dari serbuk Ag0 yang diukur.
39
Spektrum EDX menunjukkan komposisi beberapaunsur yaitu perak (Ag) 53,98 %, karbon (C) 16,27 %, oksigen (O) 27,84 %, tembaga (Cu) 2,8 %, dan alumunium 1,75 %. Unsur-unsur C, O, Cu, dan Al merupakan unsur-unsur yang dapat berasal dari ekstrak lemon.
3.5 Karakteristik Antifungi
Uji coba aktivitas antifungi dari larutan nanopartikel Ag0 hasil sintesis menggunakan metode observasi pertumbuhan jamur dalam cawan petri. Pengujian ini menggunakan media larutan ekstrak kulit lemon, karena berdasarkan pengamatan, larutan ekstrak kulit lemon sangat mudah ditumbuhi oleh jamur/fungi. Dalam pengujian antifungi, masing-masing ekstrak dicampurkan dengan larutan nanopartikel Ag0 yang bersesuaian dengan rasio volume 10:1. Campuran dimasukkan ke dalam cawan petri dan dipaparkan pada udara terbuka dan suhu ruangan serta dibiarkan selama beberapa hari. Pengamatan terhadap campuran dilakukan setiap hari. Hasil antifungi secara pengamatan visual disajikan dalam Tabel 2.
Hari ke-1 adalah hari pada saat mulai penyiapan, pencampuran, dan penempatan media atau campurannya dalam cawan petri. Pengujian dilakukan terhadap semua ekstrak dengan berbagai konsentrasi dan larutan nanopartikel Ag0 produk sintesisnya. Setiap pengujian melibatkan dua cawan yaitu cawan pertama hanya berisi larutan ekstrak yang merupakan kontrol sedangkan cawan kedua berisi campuran ekstrak dengan larutan nanopartikel Ag0 hasil sintesisnya dalam rasio volume 10:1.
Hasil pengamatan pada hari ke-2 menunjukkan kemunculan titik-titik jamur pada semua larutan ekstrak kontrol. Hal ini menunjukkan bahwa larutan ekstrak kulit lemon merupakan media yang sesuai untuk pertumbuhan jamur. Spora yang hinggap di atas permukaan dapat tumbuh dalam waktu yang relatif singkat. Sedangkan cawan-cawan yang berisi campuran larutan ekstrak dan larutan nanopartikel Ag0 pada percobaan 1 hingga 4 tidak menunjukkan adanya titik-titik jamur. Hal ini menunjukkan bahwa
keberadaan nanopartikel Ag0 dalam media dapat menghambat pertumbuhan jamur atau bahkan mematikan spora sehingga tidak memunculkan pertumbuhan. Pada hari ke-2, warna campuran ekstrak dengan larutan Ag0 mengalami pemekatan, terutama pada percobaan 1 dan 2. Hal ini menunjukan adanya reaksi lanjutan pembentukan nanopartikel Ag0. Pada percobaan 1, larutan nanopartikel Ag0 yang digunakan adalah hasil reaksi antara ekstrak dari 2,5 gram serbuk kulit lemon dengan larutan Ag+ 0,1 M. Dalam hal ini, larutan Ag+ dapat menjadi reagen berlebih karena kandungan zat-zat terlarut dan reduktor dalam ekstrak dari 2,5 gram serbuk kulit lemon diperkirakan paling rendah dibandingkan dengan ekstrak dari 5; 7,5; dan 10 gram serbuk kulit lemon. Pasca sintesis, larutan yang dihasilkan adalah larutan nanopartikel Ag0 yang masih mengandung banyak sisa Ag+. Ketika larutan ini dicampurkan kembali dengan media ekstrak kulit lemon yang fresh untuk uji antifungi dalam percobaan 1, maka kelebihan Ag+ ini akan bereaksi membentuk Ag0 yang ditandai dengan warna campuran menjadi kehitaman. Hal yang sama juga terjadi dalam percobaan 2. Sedangkan warna campuran dalam percobaan 3 dan 4 tidak mengalami perubahan yang signifikan. Hal ini karena larutan nanopartikel Ag0 yang ditambahkan pada media ekstrak kulit lemon tidak mengandung sisa Ag+ sehingga reaksi pembentukan Ag0 lanjutan tidak terjadi. Hasil pengamatan hari ke-3 hingga hari ke-5 menunjukkan pertumbuhan jamur yang semakin meningkat pada semua media kontrol ekstrak kulit lemon dari semua percobaan. Percobaan 1 dan 2 menunjukkan aktivitas anti jamur yang efektif oleh karena kandungan nanopartikel Ag0 yang cukup. Sementara pada percobaan 3 dan 4 menunjukkan adanya pertumbuhan jamur pada media uji yang telah ditambahkan larutan nanopartkel Ag0. Hal ini menunjukkan kuantitas Ag0 yang kurang sehingga jamur tetap dapat tumbuh. Selain itu ekstrak kulit lemon yang pekat menghalangi nanopartikel Ag0 sehingga jamur dapat tumbuh pada permukaan ekstrak kulit lemon.
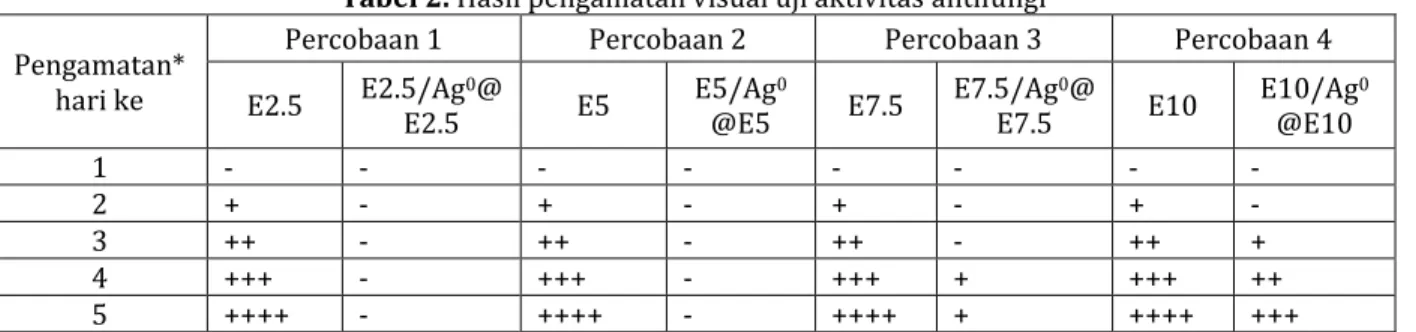
Tabel 2. Hasil pengamatan visual uji aktivitas antifungi Pengamatan*
hari ke
Percobaan 1 Percobaan 2 Percobaan 3 Percobaan 4
E2.5 E2.5/AgE2.5 0@ E5 E5/Ag@E5 0 E7.5 E7.5/AgE7.5 0@ E10 E10/Ag@E10 0
1 - - - -
2 + - + - + - + -
3 ++ - ++ - ++ - ++ +
4 +++ - +++ - +++ + +++ ++
5 ++++ - ++++ - ++++ + ++++ +++
*berdasarkan pengamatan visual
40
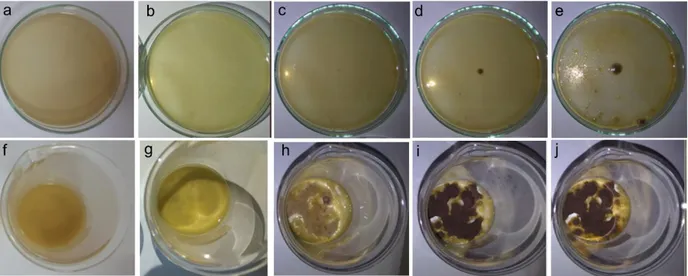
Gambar 6. a. Ekstrak dari 2.5 gram (E2.5) serbuk lemon pada hari ke-1 (media kontrol), b-e. ekstrak padahari ke-2, ke-3, ke-4, dan ke-5 (tumbuh jamur) f. campuran, pada hari ke-1, ekstrak E2.5 dengan larutan nanopartikel Ag0 hasil sintesisnya, g-j. campuran pada hari ke-2, ke-3, ke-4, dan ke-5 (tidak ada jamur,
terbentuk lanjutan nanopartikel Ag0)
Gambar 7. a. Ekstrak dari 5 gram (E5) serbuk lemon pada hari ke-1 (media kontrol), b-e. ekstrak pada hari ke-2, ke-3, ke-4, dan ke-5 (tumbuh jamur) f. campuran, pada hari ke-1, ekstrak E5 dengan larutan nanopartikel Ag0 hasil sintesisnya, g-j. campuran pada hari ke-2, ke-3, ke-4, dan ke-5 (tidak ada jamur,
41
Gambar 8. a. Campuran, pada hari ke-1, ekstrak E7.5 dengan larutan nanopartikel Ag0 hasil sintesisnya, b-c.campuran pada hari ke-2, ke-3 (tidak tumbuh jamur), d-e. campuran pada hari ke-4 dan ke-5 (muncul pertumbuhan jamur), f. Campuran, pada hari ke-1, ekstrak E10 dengan larutan nanopartikel Ag0 hasil
sintesisnya, g-j. campuran pada hari ke-2, ke-3, ke-4, dan ke-5 (tumbuh jamur)
Gambar 9 Koloni bakteri E.Coli yang tumbuh setelah inkubasi 48 jam pada suhu 30oC pada medium agar ternutrisi dengan penambahan a. air steril, b. ekstrak kulit lemon (E7.5), c. larutan nanopartikel Ag0 (Ag0 -E2.5) d. larutan nanopartikel Ag0 (Ag0-E5), e. larutan nanopartikel Ag0 (Ag0-E7.5), dan f. larutan nanopartikel
Ag0 (Ag0-E10) 3.6 Karakteristik Antibakteri
Uji antibakteri larutan nanopartikel Ag0 yang dihasilkan menggunakan metode penghitungan koloni. Dalam metode ini, kultur bakteri E. coli dalam media agar ternutrisi pada suhu 30oC selama 48 jam menghasilkan koloni sebanyak 448 CFU/20 mL yaitu hampir dua kali lipat dari koloni semula (274 CFU/20 mL). Demikian juga, koloni bakteri E coli mengalami peningkatan hingga 342 CFU/20 mL dalam media agar ternutrisi yang mengandung ekstrak kulit lemon. Sedangkan semua media yang mengandung larutan nanopartikel Ag0 menunjukkan jumlah koloni 0 CFU/20 mL setelah inkubasi. Hal ini memberikan konfirmasi efektivitas antibakteri larutan nanopartikel Ag0 yang disintesis dengan reduktor alami ekstrak kulit lemon.
4. KESIMPULAN
Larutan nanopartikel Ag0 dapat disintesis melalui reduksi spontan menggunakan reduktor alami ekstrak kulit lemon. Larutan nanopartikel Ag0 yang dihasilkan menunjukkan aktivitas antifungi dan antibakteri yang efektif.
5. UCAPAN TERIMA KASIH
Penulis mengucapkan terima kasih kepada Universitas Sultan Ageng Tirtayasa atas pendanaan riset melalui penelitian internal dalam skema Penelitian Dosen Madya tahun 2020.
6. DAFTAR PUSTAKA
Bar, H., Bhui, D. K., Sahoo, G. P., Sarkar, P., De, S. P., and Misra, A. (2009). Green synthesis of silver nanoparticles using latex of Jatropha curcas, Colloids and Surfaces A: Physicochemical and
42
Engineering Aspects, 339(1–3), 134–139.https://doi.org/10.1016/j.colsurfa.2009.02.00 8.
Chandran, S. P., Chaudhary, M., Pasricha, R., Ahmad, A., and Sastry, M. (2006). Synthesis of Gold Nanotriangles and Silver Nanoparticles Using Aloevera Plant Extract, Biotechnology Progress, 22(2), 577–583.
https://doi.org/https://doi.org/10.1021/bp05 01423.
Chen, X., Ding, Y., Forrest, B., Oh, J., Boussert, S. M., and Hamann, M. T. (2019). Lemon yellow #15 a new highly stable, water soluble food colorant from the peel of Citrus limon, Food Chemistry, 270, 251–256.
https://doi.org/https://doi.org/10.1016/j.foo dchem.2018.07.055.
Chernousova, S., and Epple, M. (2013). Silver as Antibacterial Agent: Ion, Nanoparticle, and Metal, Angewandte Chemie International Edition, 52(6), 1636–1653.
https://doi.org/https://doi.org/10.1002/anie. 201205923.
Khadragy, M., Alolayan, E. M., Metwally, D. M., El-Din, M. F. S., Alobud, S. S., Alsultan, N. I., Alsaif, S. S., Awad, M. A., and Moneim, A. E. A. (2018). Clinical efficacy associated with enhanced antioxidant enzyme activities of silver nanoparticles biosynthesized using moringa oleifera leaf extract, against cutaneous leishmaniasis in a murine model of leishmania major, International Journal of Environmental Research and Public Health, 15(5). https://doi.org/10.3390/ijerph15051037. García-Barrasa, J., López-de-Luzuriaga, J. M., and
Monge, M. (2011). Silver nanoparticles: synthesis through chemical methods in solution and biomedical applications, Central European Journal of Chemistry, 9(1), 7–19. https://doi.org/10.2478/s11532-010-0124-x Jamil, N., Jabeen, R., Khan, M., Riaz, M., Naeem, T.,
Khan, A., Us Sabah, N., Ghori, S. A., Jabeen, U., Bazai, Z. A., Mushtaq, A., Rizwan, S., and Fahmid, S. (2015). Quantitative Assessment of Juice Content, Citric Acid and Sugar Content in Oranges, Sweet Lime, Lemon and Grapes Available in Fresh Fruit Market of Quetta City, International Journal of Basic & Applied Sciences IJBAS-IJENS, retrieved from internet: www.uwhealth.org/files/uwhealth/docs/pdf/ kidney_citric_acid.pdf, 15(01), 21–24.
Khandelwal, N., Kaur, G., Kumar, N., and Tiwari, A. (2014). Application of silver nanoparticles in viral inhibition: A new hope for antivirals, Digest Journal of Nanomaterials and
Biostructures, 9(1), 175–186.
Kowalska-Góralska, M., Senze, M., Polechoński, R., Dobicki, W., Pokorny, P., and Skwarka, T. (2015). Biocidal Properties of Silver-Nanoparticles in Water Environments, Polish Journal of Environmental Studies, 24(4), 1641– 1647. https://doi.org/10.15244/pjoes/39554. Lee, S. H., and Jun, B. H. (2019). Silver
nanoparticles: Synthesis and application for nanomedicine, International Journal of
Molecular Sciences, 20(4).
https://doi.org/10.3390/ijms20040865. Li, B. B., Smith, B., and Hossain, M. M. (2006).
Extraction of phenolics from citrus peels: I. Solvent extraction method, Separation and Purification Technology, 48(2), 182–188. https://doi.org/10.1016/j.seppur.2005.07.005 .
Marassi, V., Di Cristo, L., Smith, S. G. J., Ortelli, S., Blosi, M., Costa, A. L., Reschiglian, P., Volkov, Y., and Prina-Mello, A. (2018). Silver nanoparticles as a medical device in healthcare settings: A five-step approach for candidate screening of coating agents, Royal Society Open Science, 5(1). https://doi.org/10.1098/rsos.171113. Prabha, P. S., Sundari, J. J., and Jacob, Y. brightson A.
(2014). Synthesis of silver nano particles using piper betle and its antibacterial activity, European Chemical Bulletin, 3(10–12), 1014– 1016.
Prathna, T. C., Chandrasekaran, N., Raichur, A. M., and Mukherjee, A. (2011). Biomimetic synthesis of silver nanoparticles by Citrus limon (lemon) aqueous extract and theoretical prediction of particle size, Colloids and Surfaces B: Biointerfaces, 82(1), 152–159. https://doi.org/10.1016/j.colsurfb.2010.08.03 6.
Premkumar, J., Sudhakar, T., Dhakal, A., Shrestha, J. B., Krishnakumar, S., and Balashanmugam, P. (2018). Synthesis of silver nanoparticles (AgNPs) from cinnamon against bacterial pathogens, Biocatalysis and Agricultural Biotechnology, 15(June), 311–316. https://doi.org/10.1016/j.bcab.2018.06.005. Rai, M., Deshmukh, S. D., Ingle, A. P., Gupta, I. R.,
Galdiero, M., and Galdiero, S. (2016). Metal nanoparticles: The protective nanoshield against virus infection, Critical Reviews in Microbiology, 42(1), 46–56. https://doi.org/10.3109/1040841X.2013.879 849.
Rai, M., Kon, K., Ingle, A., Duran, N., Galdiero, S., and Galdiero, M. (2014). Broad-spectrum bioactivities of silver nanoparticles: The
43
emerging trends and future prospects, AppliedMicrobiology and Biotechnology, 98(5), 1951– 1961. https://doi.org/10.1007/s00253-013-5473-x.
Sir Elkhatim, K. A., Elagib, R. A. A., and Hassan, A. B. (2018). Content of phenolic compounds and vitamin C and antioxidant activity in wasted parts of Sudanese citrus fruits, Food Science and Nutrition, 6(5), 1214–1219. https://doi.org/10.1002/fsn3.660.
Soto, K. M., Quezada-Cervantes, C. T., Hernández-Iturriaga, M., Luna-Bárcenas, G., Vazquez-Duhalt, R., and Mendoza, S. (2019). Fruit peels
waste for the green synthesis of silver nanoparticles with antimicrobial activity against foodborne pathogens, Lwt, 103
(December 2018), 293–300.
https://doi.org/10.1016/j.lwt.2019.01.023. Suriati, G., Mariatti, M., and Azizan, A. (2014).
Synthesis Of Silver Nanoparticles By Chemical Reduction Method: Effect Of Reducing Agent And Surfactant Concentration, International Journal of Automotive and Mechanical Engineering (IJAME), 10(1), 1920–1927. https://doi.org/10.1111/evo.13107.This.