I. Ruang Lingkup
Standar Nasional Indonesia (SNI) 7381:2008 menetapkan persyaratan mutu, metode pengambilan contoh, prosedur uji, persyaratan higiene, dan penandaan untuk Minyak Kelapa Virgin (VCO). Standar ini bertujuan untuk menjamin kualitas VCO yang beredar di Indonesia dan untuk ekspor, serta melindungi keamanan konsumen. SNI ini merujuk pada berbagai peraturan perundang-undangan terkait pangan dan perlindungan konsumen di Indonesia, memastikan VCO yang diproduksi memenuhi standar keamanan dan kualitas yang tinggi.
II. Istilah dan Definisi
SNI 7381:2008 mendefinisikan Minyak Kelapa Virgin (VCO) sebagai minyak yang diekstrak dari daging buah kelapa (Cocos nucifera L.) tua dan segar. Proses ekstraksi dilakukan dengan pemerasan, dengan atau tanpa penambahan air, tanpa pemanasan atau dengan pemanasan tidak lebih dari 60 °C. Produk akhir harus aman untuk dikonsumsi manusia. Singkatan VCO merupakan kependekan dari Virgin Coconut Oil.
III. Komposisi Bahan Baku Utama
Bahan baku utama pembuatan VCO adalah daging buah kelapa tua dan segar. Kualitas daging buah kelapa, terutama tingkat kematangan dan kesegarannya, secara langsung mempengaruhi kualitas VCO yang dihasilkan. Standar ini tidak secara spesifik membahas detail proses seleksi dan persiapan bahan baku, namun kualitas bahan baku ini merupakan faktor kunci dalam mencapai persyaratan mutu yang ditetapkan.
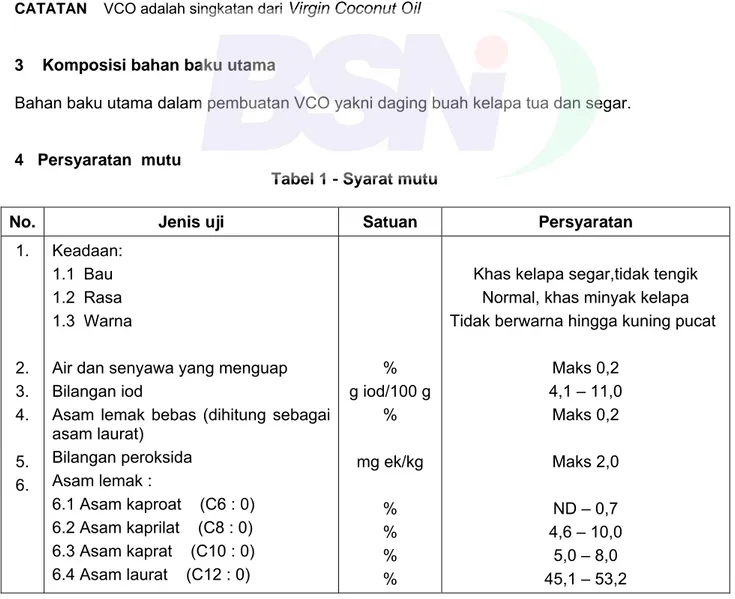
IV. Persyaratan Mutu
Bagian ini merinci persyaratan mutu VCO melalui Tabel 1. Tabel tersebut mencakup berbagai parameter, termasuk karakteristik organoleptik (bau, rasa, warna), kadar air, bilangan iod, kadar asam lemak bebas, bilangan peroksida, profil asam lemak (asam kaproat hingga asam linolenat), cemaran mikroba, dan cemaran logam (timbal, tembaga, besi, kadmium, dan arsen). Setiap parameter memiliki nilai batas maksimum atau rentang yang diizinkan untuk memenuhi standar mutu VCO yang ditetapkan.
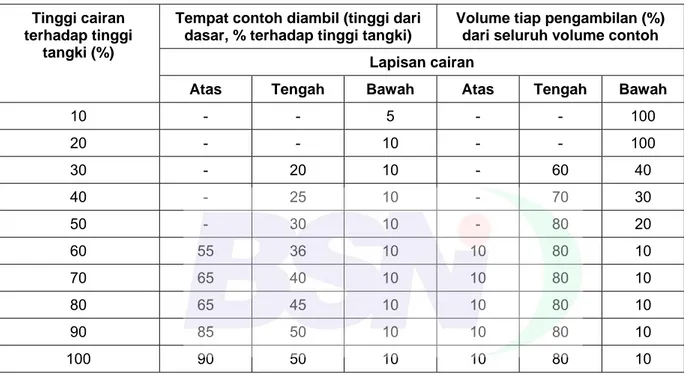
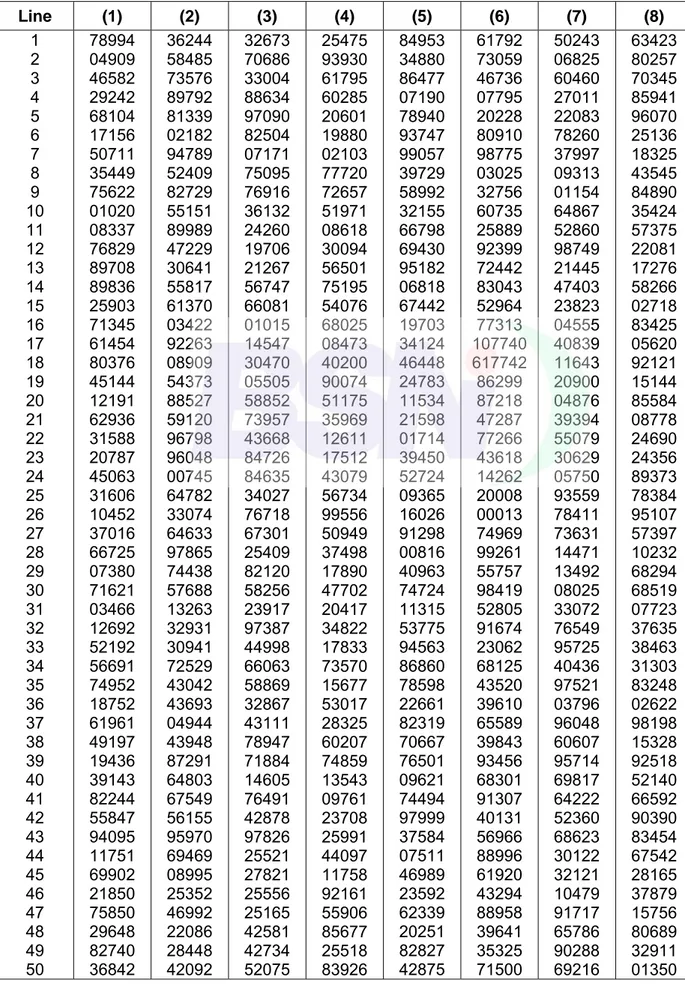
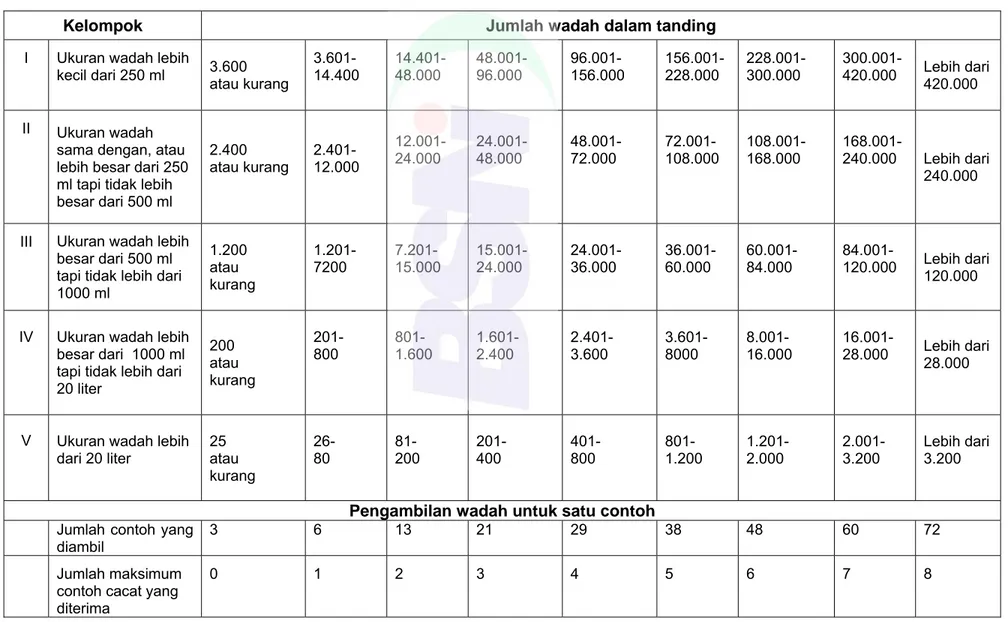
V. Pengambilan Contoh
Metode pengambilan contoh VCO dijelaskan secara rinci di Lampiran A. Prosedur ini bergantung pada bentuk kemasan VCO, baik curah maupun terkemas. Lampiran A memberikan panduan terperinci tentang cara mengambil contoh secara acak dan representatif dari berbagai ukuran dan jenis kemasan, memastikan sampel yang diambil mewakili keseluruhan produk yang akan diuji.
VI. Cara Uji
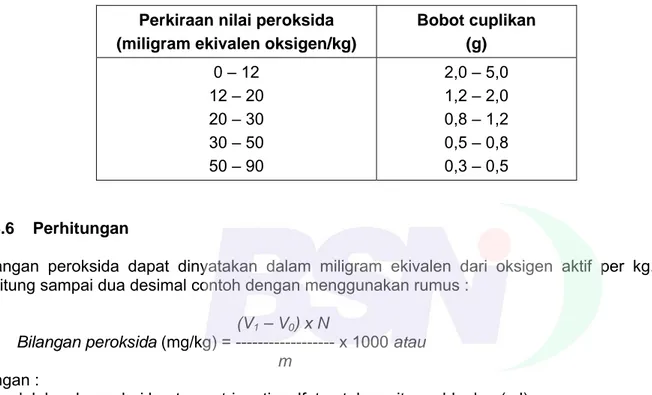
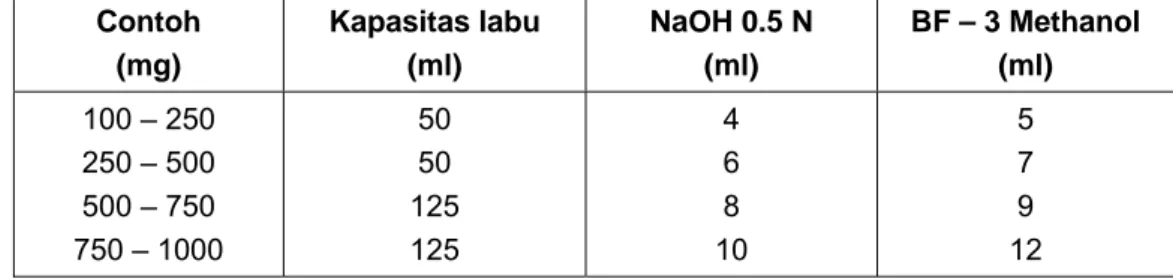
Lampiran B menjelaskan prosedur uji untuk setiap parameter mutu yang tercantum di Tabel 1. Prosedur uji ini meliputi metode organoleptik (bau, rasa, warna), metode kimia (kadar air, bilangan iod, asam lemak bebas, bilangan peroksida, profil asam lemak), dan metode mikrobiologi (angka lempeng total). Prosedur ini merujuk pada standar internasional dan nasional yang relevan, memberikan pedoman detail dan memastikan konsistensi hasil uji.
VII. Syarat Lulus Uji
VCO dinyatakan lulus uji jika memenuhi semua persyaratan mutu yang tertera pada Tabel 1. Kepatuhan terhadap semua parameter yang ditentukan sangat penting untuk memastikan kualitas dan keamanan produk. Jika salah satu parameter tidak memenuhi persyaratan, maka VCO tersebut dinyatakan tidak memenuhi standar SNI 7381:2008.
VIII. Higiene
Proses produksi VCO harus memenuhi Pedoman Cara Produksi yang Baik (CPB) untuk pangan. Hal ini menekankan pentingnya praktik higiene yang ketat selama seluruh tahapan produksi untuk mencegah kontaminasi dan memastikan keamanan produk. Standar ini tidak secara rinci menyebutkan semua CPB, tetapi menekankan perlunya kepatuhan pada peraturan terkait CPB yang berlaku.
IX. Pengemasan
VCO harus dikemas dalam wadah bersih dan tertutup rapat. Bahan kemasan harus inert, tidak bereaksi dengan VCO dan tidak mempengaruhi kualitas atau keamanan produk selama penyimpanan dan pengangkutan. Standar ini menekankan pentingnya memilih bahan kemasan yang sesuai untuk mempertahankan kualitas VCO.
X. Penandaan
Label VCO harus sesuai dengan peraturan perundang-undangan terkait label dan iklan pangan di Indonesia. Informasi yang harus tertera pada label meliputi nama produk, komposisi, berat bersih, tanggal kadaluarsa, instruksi penyimpanan, dan informasi produsen. Kepatuhan terhadap peraturan penandaan memastikan informasi yang jelas dan akurat kepada konsumen.
Referensi Dokumen
- AOAC Official Method 986. 15, Arsenic, Cadmium, Lead, Selenium, and Zinc in Human and Pet Foods, Multielement Method, 17 th Edition, Chapter 9.1.01 ( Association of Official Analytical Chemistry )
- SNI 01-2896 -1998, Cara Uji cemaran logam dalam makanan
- SNI 01 – 4866 – 1998, Cara uji cemaran arsen dalam makanan