PERKEMBANGAN RIBOSOME-INACTIVATING PROTEIN (RIP) SEBAGAI ANTIKANKER
RECENT DEVELOPMENT of RIBOSOME-INACTIVATING PROTEINS (RIPs) as ANTICANCER
Sudjadidan Sismindari
Fakultas Farmasi UGM
ABSTRAK
Ribosome-inactivating protein (RIP) merupakan protein yang umumnya berasal dari tanaman dan bersifat
sitotoksik terhadap sel mamalia. Hal ini karena aktivitas rRNA N-glikosidae dan purin glikosidase sehingga menyebabkan kematian sel mamalis. Selain itu berbagai RIP juga mampu menginduksi apoptosis bagi sel yang rusak, dan bersifat antioksidan, sehingga RIP merupakan kandidat antikanker yang baik. RIP dapat dikonjugasikan dengan antibodi monoklonal sebagai imunotoksin sehingga mempunyai efek yang selekif hanya terhadap sel target.
Kata kunci: Ribosome-inactivating protein (RIP), antikanker, imunotoksin
ABSTRACT
Ribosome-inactivating proteins (RIPs) are a group of ribotoxins widely distributed the plants. The toxicity of RIPs is due to rRNA N-glycosidase and purin glycosidase activities causing mammalian cells death. RIPs are potent candidate as anticancer agents. RIPs are able to induce apoptotic cell death and some RIPs have antioxidant activity. As immunotoxin, RIPs are conjugated with monoclonal antibody to increase selectivity to targeted cells.
Key words: Ribosome-inactivating proteins (RIPs), anticancer, immunotoxin
Alamat Korespondensi: Prof. Dr. Sudjadi., Apt
Bagian Kimia Farmasi, Fakultas Farmasi UGM Sekip Utara, Yogyakarta
PENDAHULUAN
Penggunaan makromolekul pada terapi kanker semakin berkembang. Kemajuan dalam biologi molekular dan bioteknologi akhir-akhir ini telah memungkinkan protein obat dikonjugasikan dengan antibodi sehingga obat selektif menuju ke sel target. Salah satu protein obat tersebut adalah
Ribosome-inactivating protein (RIP).
RIP telah diidentifikasi 100 tahun lalu. Ricin dari biji Ricinus comunis merupakan RIP
yang dikenal sangat toksik dan dapat mengakibatkan abortifasien (Endo et al., 1987).
Istilah Ribosome-inactivating protein (RIP)
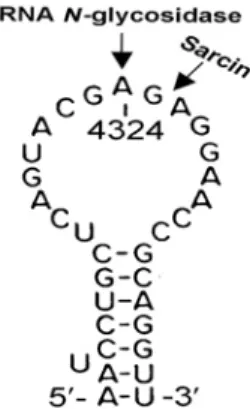
digunakan untuk protein tanaman yang mempunyai aktivitas rRNA N-glikosidase terhadap ribosom hewan. Aktivitas rRNA N-glikosidase ini yang menyebabkan depurinasi Adenin pada posisi 4324 dari 28S rRNA (Gambar 1). Aktivitas ini mencegah pembentukan konfigurasi penting stem-loop, sehingga faktor elongasi 2 (EF2) tidak dapat
berikatan dan berakibat proses translokasi pada sintesis protein terhambat. Hasil akhir dari aktivitas ini adalah penghambatan sempurna sintesis protein. Suatu jenis protease tidak termasuk sebagai RIP waupun dapat menginaktivasi ribosom dan menghentikan sintesis protein (Peumans et al.,
2001). Aktivitas N-glikosidase juga dapat diamati pada daun Carica papaya, Morinda citrifolia dan Mirabilis jalapa (Sismindari and Lord, 2000).
Gambar 1. Situs pemotongan oleh RIP pada ribosom tikus. Aktivitas rRNA-N-glikosidase akan menghidrolisis ikatan glikosidik N-C A4324 16S rRNA (Diadaptasi dari Xu dan Liu, 2004).
RIP dalam tanaman penghasil bersifat sebagai alat pertahanan diri terhadap infeksi virus dan patogen. Beberapa RIP terbukti dapat menghambat infeksi virus dan jamur pada tanaman (Park et al, 2004). RIP telah teridentifikasi pada
famili, yaitu 17 famili tanaman dikotil dan 3 tanaman monokotil. Pada satu tanaman terdapat beberapa RIP baik pada biji, buah, daun maupun akar (Tabel I). Sebagai contoh Mirabiliis jalapa L,
pada biji dan akar mengandung RIP yang dinamakan Mirabilis antiviral protein, MAP 24,2
kDa (Vivanco et al, 1999), dan daunnya
mengandung MJ-30 (30 kDa) yang bersifat basa (Sudjadi et al. 2003) serta MJ-C yang bersifat asam
(Sudjadi et al, 2007). RIP yang bersifat asam masih
sangat sedikit dilaporkan, diantaranya maize b-32 (Mundy et al., 1994)
Konsentrasi RIP pada berbagai tanaman bervariasi mulai kurang dari 1 mg sampai lebih dari 100 mg setiap 100 g bahan (Stirpe and Barbieri, 1986). Pemurnian strandar untuk RIP yang dilakukan dengan menggunakan kolom penukar ion CM-Sepharose yang bermuatan negatif sehingga RIP yang bermuatan positif saja yang terisolasi kemudian dilanjutkan dengan kolom penyaring molekul Sephadex .
JENIS RIP
Berdasarkan strukturnya, RIP dapat dibagi menjadi 3 jenis, yaitu :
1) RIP tipe 1 atau Holo-RIP merupakan polipeptida tunggal, berukuran ~30 kDa dengan aktivitas rRNA N-glikosidase (Gambar 2A). Contoh RIP tipe 1 klasik adalah PAP (Pokeweed Antiviral Protein).
RIP tipe 1 sebagian besar berupa glikoprotein dan berupa basa kuat yang umumnya memiliki pI ≥ 9,5 (Barbieri et al., 1993). Di
samping itu, telah ditemukan protein sejenis RIP tipe 1 yang terdiri dari 2 rantai polipeptida yang lebih pendek yang dihubungkan dengan interaksi nonkovalen (Peumans et al., 2001).
2) RIP tipe 2 atau chimero-RIP terdiri dari dua subunit, rantai A mempunyai aktivitas N-glikosidase dan rantai B yang mengandung lektin yang masing-masing dihubungkan oleh suatu ikatan disulfida. Sebagian besar RIP tipe 2 dengan bobot molekul ~60 kDa dan pI antara 4,8 sampai 8. (Barbieri et al., 1993).
Sedangkan fungsi rantai B adalah untuk membantu RIP masuk ke dalam sel dengan cara berikatan dengan residu gula spesifik dari glikoprotein atau glikolipid dalam membran plasma dan internalisasi secara endositosis (Narayanan et al., 2005). Oleh
3) RIPs tipe 3, terdiri dari domain amino-terminal menyerupai RIP tipe 1 dihubungkan pada unrelated carboxyl-terminal domain
dengan fungsi yang belum diketahui (Gambar 2C). JIP60 (Jasmonate-induced Protein)
dengan ukuran 60 kDa diisolasi dari Hordeum vulgare disebut sebagai RIP tipe 3 (Peumans et al., 2001). Bentuk dari masing-masing tipe
RIP dapat dilihat pada Gambar 2.
Sejauh ini RIP menunjukkan kandidat yang baik sebagai antikanker dan antivirus. Antikanker yang ideal mempunyai sifat sebagai antioksidan, antiproliferasi, menaikkan system perbaikan DNA, menginduksi apoptosis pada sel rusak, menghambat angiogenesis dan menaikkan sistem imun. Ini berarti agen anti-kanker yang ideal dapat beraksi pada tahap penjegahan maupun pengobatan.
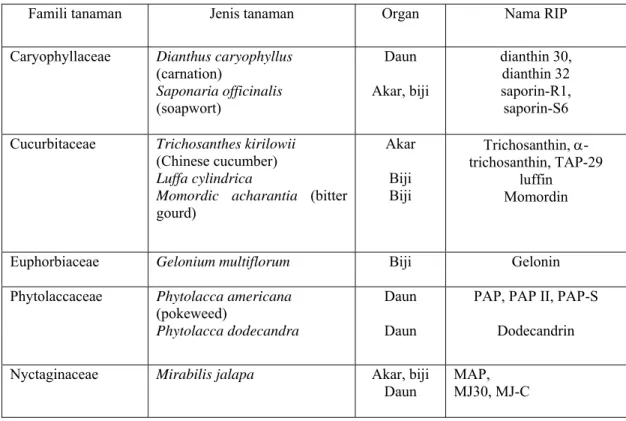
Tabel 1. Sumber tanaman dan nama RIP tipe 1 yang dihasilkan.
Famili tanaman Jenis tanaman Organ Nama RIP Caryophyllaceae Dianthus caryophyllus
(carnation) Saponaria officinalis (soapwort) Daun Akar, biji dianthin 30, dianthin 32 saporin-R1, saporin-S6 Cucurbitaceae Trichosanthes kirilowii
(Chinese cucumber)
Luffa cylindrica
Momordic acharantia (bitter
gourd) Akar Biji Biji Trichosanthin, α-trichosanthin, TAP-29 luffin Momordin
Euphorbiaceae Gelonium multiflorum Biji Gelonin
Phytolaccaceae Phytolacca americana
(pokeweed)
Phytolacca dodecandra
Daun Daun
PAP, PAP II, PAP-S Dodecandrin Nyctaginaceae Mirabilis jalapa
Akar, biji
Daun MAP, MJ30, MJ-C
Gambar 2. Struktur skematik dari tiga tipe RIP yang berbeda
Keterangan gambar A : RIP tipe 1, menunjukkan RIP tipe 1 klasik dan RIP yang serupa RIP tipe 1 yang terdiri dari 2 rantai polipeptida yang lebih pendek (α dan β). Garis yang berupa titik antara rantai α dan β pada RIP tipe 1 mengindikasikan bahwa kedua rantai berinteraksi satu sama lain secara non-kovalen. B: RIP tipe 2, menunjukkan rantai A dan rantai B (mengandung lektin) yang dihubungkan oleh ikatan disulfida. C : RIP tipe 3, mempunyai domain yang tidak diketahui. (Diadaptasi dari Xu and Liu, 2004)
AKTIVITAS BIOLOGIS
Efek antioksidan. RIP yang diisolasi dari biji Cinnamomum camphora dan Cucurbita moshata memiliki aktivitas sebagai penangkap
radikal seperti superoksid dismutase (SOD). Aktivitas SOD ini setara dengan aktivitas SOD
E.coli. (Barbieri et al.,2006). Reaksi RIP sebagai
penangkap radikal:
2O2* + 2H+ O2 + H2O2
2 H2O2 O2 + H2O
Fraksi protein M.jalapa menujukkan
aktivitas antioksidan jauh lebih kuat daripada RIP MJ-30 maupun MJ-C dari daun M.jalapa
(Sismindari et al,. submited). Fraksi protein M.jalapa ini mampu menghambat timbulnya
kanker kulit yang diinduksi dengan penyinaran UV-B. Protein ini juga mampu mereduksi perbanyakan tumor pada fase awal paparan UV-B sampai minggu ke-9. Hal ini diduga karena fraksi protein tersebut mempunyai aktivitas penangkap radikal yang disebabkan oleh penyinaran UV-B sehingga memperkecil kemungkinan terjadinya mutasi DNA (Sismindari et al., submited).
Efek sitotoksik. Beberapa RIP telah
diketahui mempunyai kemampuan membunuh
sel-toksik karena aktivitas rRNA N-glikosidase sehingga sintesis protein berhenti. Selain RNA ribosom, beberapa RIP dapat mengenali RNA dan mRNA sebagai substrat dan kemudian melakukan deadenilasi. Saporin-L1 (suatu RIP tipe I dari
Saponaria officinalis) memiliki kemampuan untuk
memotong beberapa residu adenin dari berbagai substrat asam nukleat seperti herring sperm DNA,
poli-(A), tRNA, bahkan RNA Tobaco Mosaic Virus. (Barbieri et al., 1997). Selain itu beberapa
RIP diketahui mempunyai aktivitas guanosin glikosidase, memotong G4323 rRNA. (Peumans et al., 2001). Hal ini merupakan makanisme lain
kematian sel yang disebabkan oleh RIP (Battelli, 2004). MJ-30 yang bersifat basa dari M.jalapa
bersifat lebih toksik terhadap sel kanker daripada sel normal (Ikawati et al., 2006). Sedangkan MJ-C
yang bersifat asam menunjukkan 13 sampai 495 kali lebih toksik daripada MJ30 (Sudjadi et a.l.,
2007).
Secara in vitro RIP dapat memotong dan
melinearisasi DNA superkoil untai ganda menjadi konformasi nik-sirkuler pada RIP kadar rendah dan menjadi konformasi linier pada kadar tinggi (Ling
et al., 1994; Sismindari et al., 1998). Aktivitas
DNase RIP tidak mengenali adanya sekuen spesifik pada situs pemotongan, tetapi ditentukan oleh struktur 3-D DNA (Ling et al., 1994).
Induksi apoptosis. Beberapa penelitian melaporkan bahwa RIP mampu menginduksi kematian sel melalui apoptosis. Ricin mampu Katalase
diketahui dapat menginduksi apoptosis pada sel HeLa (Ikawati, et al., 2003). RIP tidak secara
langsung dapat menginaktivasi perangkat apoptosis seluler, karena aktivitas primer dari toksin ini adalah menginaktivasi ribosom dan menghentikan sintesis protein sel. Mitokondria akan mensensitisasi stress yang ditimbulkan oleh RIP (disebut stress ribotoksik), titik ini merupakan awal dari proses tranduksi sinyal apoptosis secara intrinsik (Narayanan et al., 2004; Qu dan Qing,
2004).
Adanya RIP menyebabkan terjadinya perubahan pada fungsi mitokondria. Kerusakan mitokondria yang diikuti hilangnya potensial membran mitokondria, mengindikasikan adanya transisi permeabilitas membran mitokondria dalam pembentukan pori-pori untuk melepaskan
cytochrome c. Dimana assosiasi cytochrome c
dengan Apaf-1 dan caspase-9 akan mengaktivasi caspase-3 (Narayanan et al., 2004).
Aktivitas imunosupresif. Semua RIP merupakan imunogen kuat. Aksi alergi terhadap biji tanaman jarak terjadi pada pekerja pembuat minyak jarak. Ricin pada ekstrak biji tanaman jarak menginduksi respon IgE. Pada kelinci respon imun humoral naik oleh induksi berbagai RIP tipe 1. Serum kelinci tersebut menunjukkan reaksi silang terhadap RIP dari tanaman satu famili tetapi tidak menghasilkan reaksi terhadap RIP dari tanaman yang beda famili. Imunogenisitas juga terlihat pada penggunaan imunotoksin yang mengandung RIP pada pemakain berulangkali.
Pada konsentrasi rendah, RIP berpengaruh pada lipopolisakharid dan menginduksi IL-1. Sedangkan pada konsentrasi tinggi RIP menghambat produksi IL-1 dan menekan proliferasi sel. Oleh karena itu RIP menunjukkan efek imunosupresif pada pembentukan antibodi humural dan berbagai respon perantara sel (Battelli, 2004).
RIP memiliki toksisitas yang tinggi terhadap makrofag. PAP, momordin dan gelonin memiliki efek penghambatan yang kuat terhadap sel yang memproduksi antibodi. Dengan adanya PAP dan momordin, sama sekali tidak terbentuk antibodi sebagai respon terhadap antigen T-dependen. Kemungkinan RIP beraksi pada tahap awal proses pembentukan antibodi (Stirpe dan Barbieri, 1986; Barbieri et al., 1993).
PENGGUNAAN
Penggunaan RIP yang menarik adalah dikembangkannya sebagai imunotoksin. Trichokirin, RIP dari Trichosanthes kirilowii, telah
dikonjugasikan dengan antibodi yang mengenal antigen Tyr1.2. Percobaan in vitro menunjukkan
bahwa imunotoksin ini secara selektif mematikan sel leukemia yang mengekspresikan antigen Tyr1.2. (Casellas et al., 1988). Rantai A ricin
banyak dikonjugasikan berbagai antibodi untuk digunakan sebagai imunotoksin dan menghasilkan toksisitas terhadap sel target ( Bolognesi and Polito, 2004).
Beberapa RIP seperti bryodin 2 dari
Bryonia dioica telah dipatenkan dengan paten US
Patent 5597569 pada Januari 1997 (Anonima). Gelonin yang mengandung gugus sulfihidril dikonjugasikan antibodi monoklonal pada gugus NH membentuk imunotoksin dan telah dipatenkan Desember 1989 No. US4888415 (Anonimb). Antibodi spesifik untuk antigen CD40L permukaan sel manusia juga telah dikonjugasikan dengan RIP tipe 1. Imunotoksin ini dapat digunakan untuk penyakit autoimun seperti multiple sclerosis, rheumatoid arthritis dan systemic lupus erythematosus, atau T-cell malignancies
(US6645494) (Anonimc). Perkembangan pembuatan imunotoksin tanpa ikatan kovalen antara antibodi dengan toksin menjadi lebih menarik karena lebih fleksibel. Setelah diperoleh gena suatu RIP maka RIP disintesis in vitro dengan
penanda biotin yang kemudian dikonjugasikan dengan protein A yang tempeli streptavidin. Antibodi monoklonal yang mengenali epitop sel target juga dapat berikatan dengan protein A. Dengan cara ini pembuatan imunotoksin menjadi lebih fleksibel karena dapat menganti RIP ataupun antibodi dengan lebih mudah.
KESIMPULAN
Ribosome-inactivating protein (RIP)
merupakan kandidat yang baik sebagai agen antikanker jika dikonjugasikan dengan antibodi monoklonal yang mengenal sel target. Saat ini berbagai RIP telah dikarakterisasi dan dipatenkan. Walapun demikian belum ditemukan suatu RIP yang mempunyai sifat seperti yang diinginkan sebagai agen antikanker yang ideal. Penapisan untuk mendapatkan RIP dengan sifat sebagai antikanker yang mendekati ideal masih terbuka, terutama RIP yang bersifat asam.
DAFTAR PUSTAKA:
Anonima, US Patent 5597569-Bryodin 2 a ribosome-inactivating protein isolated from the plant Brypnia dioica,
www.patentstrom.us/patents/5597569 .html, 19-11-2008
Anonimb, Gelonin immunotoxin, www.patents.com/Gelonin immunotoxin/ US4888415/en-US/, 19-11-2008
Anonimc, Anti-CD40L immunotoxins for treatment of diseases, www.freepatents online.com/6645494.html, 19-11-2008 Battelli, M.G., 2004, Cytotoxicity and toxicity to
animals and humans of ribosome-inactivating proteins, Mini Rev. Med.Chem,
4, 513-521.
Barbieri L., Battelli, M.G., dan Stirpe F, 1993, Ribosome-inactivating proteins from plants.
Biochim. Biophys. Acta., 1154, 237–282.
Barbieri, L., Valbonesi, P., Bonora, E., Gorini, P., Bolognesi, A., dan Stirpe, F. ,1997, Polynucleotide:adenosine glycosidase activity of ribosome-inactivating proteins: effect on DNA, RNA and poly(A). Nucleic Acids Res, 25, 518-522
Barbieri, L Polito,L., Bolognesi,A., Ciani,M., Pelosi,E., Farini,V., Jha,A.K., Sharma,N., Vivanco,J.M., Chambery,A., Parente,A., and Stirpe,F, 2006, Ribosome-inactivating proteins in edible plants and purification and characterization of a new ribosome-inactivating protein from Cucurbita moshata, Biochim Biophys Acta, 1760,
783-792.
Bolognesi,L., and Polito,L., 2004, Immunotoxins and othe conjugates: Pre-clinical studies,
Mini Rev. Med.Chem, 4, 563-583.
Casselas,P., Dossossoy,D., Falasca,A.J., Barbieri,L., Gullemot,J.C., Ferrara,P., Bolognesi,A., Cenini,P., and Stirpe,F., 1988, Trichokirin, a ribosome-inactivating protein from the seeds of Trichosanthes kirilowii Maximovics: Preparation, partial
characterization and use for preparation of immunotoxins, Eur.J.Biochem., 176,
581-588.
Endo, Y., Mitsui, K., Motizuki, M., dan Tsurugi, K. ,1987, The mechanism of action of ricin and related toxic lectins on eukaryotic ribosomes. The site and the characteristics of the modification in 28S ribosomal RNA caused by the toxins. J. Biol. Chem. 262,
5908-5912.
Hartley, M.R., Chaddock, J. A., dan Bonness, M. S., 1996, The structure and function of ribosome-inactivating proteins. Trends Plant Sci., 1, 254-260.
Ikawati,Z., Sudjadi, Elly,W., Puspitasari,D., and Sismindari, 2003, Induction apoptosis by protein fraction isolated from the leaves of
Mirabilis jalapa L on HeLa and Raji
cell-line, OPEM, 3(3), 151 – 156.
protein isolated from leaves of Mirabilis jalapa L., Malaysian J Parm. Sci., 4(1), 1 -
12
Ling, J., Liu,W.Y., and Wang, T.P., 1994, Cleavage of Supercoiled double stranded DNA by Several Ribosome Inactivating Proteins in vitro, FEBS Lett., 345 (23),
143-146.
Mundy, L. Leach, R., Boston, R, Endo, R., and Stirpe, L., 1994, Gene encoding ribosome inactivating protein, Plant. Mol. Biol. Rep.,
12, 60-62.
Narayanan, S., Surolia, A., and Karande, AA., 2004, Ribosome-inactivating protein and apoptosis: abrin causes cell death via mitochondrial pathway in Jurkat cells,
Biochem. J., 377, 233–240.
Narayanan, S., Surendranatbh, K., Borab, N., and Karandep, A.A., 2005, Ribosome inactivating proteins and apoptosis, FEBS Lett., 579 (6), 1324-1331.
Park, S.W., Vepachedu, R., Sharma, N., dan Vivanco, J.M., 2004, Ribosome-inactivating proteins in plant biology, Planta, 219,
1093-1096.
Peumans, W. J., Hao, Q., and Van-Damme, E.J. ,2001, Ribosome inactivating proteins from plants: more than RNA N-glycosidases.
FASEB J. 15, 1493–1506.
Qu, X., and Qing, L., 2004, Abrin Induces cell Apoptosis by Cytochrome c release and caspase activation, J Biochem. Microbiol.,
37(4), 445-453.
Sismindari, Husaana,A., and Mubarika,S., 1998, In vitro cleavage of supercoiled DNA by
Annona squamosa extract, MFI, 9,4,
146-152.
Sismindari and Lord J.M., 2000, RNA N-glicosidase activity of leave crude extract from Carica papaya, Morinda citrifolia and Mirabilis jalapa, Indon.J. Biotech., special issue, 342-345
Sismindari, Mubarika S., and Sudjadi, 2001, Selective cytotoxic effect on cancer cell-lines of protein fraction isolated from
Annona squamosa L conataining
Ribosome-inactivating proteins, Indon. J. Biotech.,
459-462
Sismindari, Sudjadi, Hussaana,A., Widyarini, S., dan Ikawati,Z., Efek aplikasi topikal fraksi protein Mirabilis jalapa L pada insidenti
kanker kulit yang diinduksi sinar UV-B pada mencit, submitted.
Stirpe, F., and Barbieri, L., 1986, Ribosome Inactivating Protein up to date, FEBS 3269,
195, 1-8.
Sudjadi, Sismindari, Herawati,T., and Prasetyowati,A.T., 2003, Pemurnian
Ribosome-inactivating protein (RIP) dari
daun Mirabilis jalapa L. dengan kolom
CM-Sepharose CL-6B dan Sephacryl S-300HR, MFI, 14(2), 316-321.
Sudjadi, Witasari,L.D., Sadarum,M.T., Natity,N., dan Sismindari, 2007, Efek sitotoksik suatu protein seperti Ribosome-Inactitang protein
yang bersifat asam dari daun Mirabilis jalapaL pada sel kanker, MFI, 18(1), 8-14.
Vivanco, J. M., Querci, M., dan Salazar, L. F. 1999. Antiviral and antiviroid activity of MAP containing extracts from Mirabilis jalapa roots. Plant Dis. , 83,1116-1121.
Xu, H., dan Liu, W.Y., 2004 , Cinnamomin-a Versatile Type II Ribosome-inactivating Protein, Acta Biochimt. Biophys. Sinica,