PERBANDINGAN METODE PENENTUAN
AKTIVITAS ANTIOKSIDAN RIMPANG
TEMULAWAK
IRMA IRAWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
ABSTRAK
IRMA IRAWATI. Perbandingan Metode Penentuan Aktivitas Antioksidan
Rimpang Temulawak. Dibimbing oleh LATIFAH KOSIM DARUSMAN dan
MOHAMAD RAFI.
Temulawak merupakan bahan baku obat tradisional mengandung
kurkuminoid dan xantorhizol yang berpotensi sebagai antioksidan. Antioksidan
secara alami terdapat dalam tubuh sebagai suatu sistem perlindungan tubuh dari
pengaruh radikal bebas. Penelitian ini mengacu pada penelitian sebelumnya
bahwa tidak ada korelasi linear antara kandungan xantorhizol dan aktivitas
antioksidan sehingga diperlukan metode yang sesuai untuk analisis antioksidan
rimpang temulawak. Temulawak yang berasal dari Boyolali diekstraksi dengan
pelarut etanol, tetrahidrofuran (THF), dan metanol. Penentuan aktivitas
antioksidan setiap ekstrak menggunakan metode DPPH
(1,1-difenil-2-pikrilhidrazil) dan metode CUPRAC (reduksi ion tembaga
), kedua metode
tersebut dinyatakan dalam ekuivalen troloks.
Hasil penelitian menunjukkan bahwa ekstrak etanol, THF, dan metanol
rimpang temulawak memiliki kadar kurkuminoid dan xantorizhol berturut-turut
20.10, 26.82, 21.72 dan 0.01, 0.09, 0.004%. Uji aktivitas antioksidan metode
DPPH ekstrak etanol, THF, dan metanol bernilai 0.8953, 0.8818, dan 0.8827 µmol
troloks/g ekstrak. Sementara metode CUPRAC memiliki kapasitas antioksidan
42.5933, 131.5937, dan 30.4542 µmol troloks/g ekstrak. Hasil tersebut
menunjukkan bahwa metode CUPRAC memiliki korelasi linear antara kandungan
komponen aktif dan aktivitas antioksidan. Hal ini dibuktikan pula dengan
menggunakan sampel temulawak yang berasal dari Semarang dengan kadar
kurkuminoid dan xantorhizol 30.77, 33.85, 28.03 dan 0.19, 0.17, 0.02%
berturut-turut untuk ekstrak etanol, THF, dan metanol dengan kapasitas antioksidan
bernilai 97.5599, 68.5104, dan 72.0673 µmol troloks/g ekstrak. Hasil evaluasi
data analisis metode DPPH lebih teliti dibandingkan dengan metode CUPRAC
dengan sensitivitas yang kemungkinan juga lebih tinggi. Uji t dan uji F
menunjukkan hasil analisis dan keragaman kedua metode berbeda nyata karena
nilai t hitung > t tabel dan F hitung > F tabel pada selang kepercayaan 95%.
ABSTRACT
IRMA IRAWATI. Comparison of Antioxidant Activity Determination Methods
for Rhizome of Curcuma xanthorrhiza. Supervised by LATIFAH KOSIM
DARUSMAN and MOHAMAD RAFI.
Temulawak as raw materials for traditional medicine contains curcuminoid
and xanthorrhizol with antioxidant activities. Antioxidant naturally occurs in
human body as protection system from free radical. This study was performed
according to previous research that there was no linear correlation between
xanthorrhizol content and antioxidant activity. So it needed suitable method to
determine antioxidant activities for rhizome of temulawak. Temulawak from
Boyolali was extracted with ethanol, tetrahydrofuran (THF), and methanol.
Antioxidant activity of each extract was determined by DPPH
(1,1-diphenyl-2-picrylhydrazyl)
and CUPRAC methods (cupric ion reducing antioxidant
capacity), they were expressed as µmol trolox equivalents per gram extract.
The result showed that ethanol, THF, and methanol extracts from rhizome
of temulawak contains curcuminoid and xanthorrhizol that were 20.10, 26.82,
21.72 and 0.01, 0.09, 0.004%, respectively. Antioxidant assay of temulawak
rhizome extract using the scavenging DPPH radicals from ethanol, THF, and
methanol extract were 0.8953, 0.8818, dan 0.8827 µmol trolox/g extract,
respectively. Meanwhile antioxidant activity using CUPRAC method gave the
value of 42.5933, 131.5937, dan 30.4542 µmol trolox/g extract, respectively. This
result indicated that CUPRAC method has linear correlation between active
components and antioxidant activity. This was also proved using temulawak
rhizome obtained from Semarang with curcuminoid and xanthorrhizol content of
30.77, 33.85, 28.03 and 0.19, 0.17, 0.02% for ethanol, THF, and methanol extract,
respectively. Antioxidant capacity of the three extracts were 97.5599, 68.5104,
dan 72.0673 µmol trolox/g extract, respectively. Data evaluation indicated that
DPPH method was more precise than CUPRAC method with its sensitivity was
also higher. Significantly difference were given for all t test and F test because t
exp > t table and F exp > F table at 95% significant level.
PERBANDINGAN METODE PENENTUAN
AKTIVITAS ANTIOKSIDAN RIMPANG
TEMULAWAK
IRMA IRAWATI
Skripsi
sebagai salah satu syarat memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
Judul : Perbandingan Metode Penentuan Aktivitas Antioksidan Rimpang
Temulawak
Nama : Irma Irawati
NIM : G44204023
Menyetujui
Pembimbing I,
Pembimbing II,
Prof. Dr. Ir. Latifah K Darusman, MS Mohamad Rafi, S.Si
NIP 130 536 681 NIP 132 321 454
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor,
Dr. drh. Hasim, DEA
NIP 131 578 806
PRAKATA
Puji syukur Penulis panjatkan kepada Allah SWT atas segala rahmat yang
diberikan kepada Penulis sehingga dapat menyelesaikan karya ilmiah ini.
Penelitian ini bertujuan mendapatkan metode yang sesuai dalam penentuan
aktivitas antioksidan rimpang temulawak. Penelitian ini dilaksanakan sejak bulan
Maret–Juli 2008 di Pusat Studi Biofarmaka dan Laboratorium Kimia Analitik.
Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, IPB.
Penulis mengucapkan terima kasih kepada semua pihak yang telah
membantu Penulis selama penelitian dan juga penyusunan karya ilmiah ini,
terutama kepada Ibu Prof. Dr. Ir. Latifah K Darusman, MS dan Bapak Mohamad
Rafi, S.Si selaku pembimbing yang selalu memberikan saran dan meluangkan
waktu selama berkonsultasi; kepada Pusat Studi Biofarmaka yang telah mendanai
sebagian biaya penelitian dan diikutsertakan dalam penelitian temulawak; kepada
Mama, Apa serta adik-adikku tercinta yang selalu memberi dukungan dan doanya,
Ela dan teman-teman Sunda Karya yang selalu setia mendampingi Penulis,
rekan-rekan Analitik 41 dan rekan-rekan-rekan-rekan Kimia 41. Penulis juga mengucapkan terima
kasih kepada Mbak Ina, Bu Nunuk, Endi, Ka Zulhan atas arahannya yang sangat
membangun, Om Eman dan para laboran di Kimia Analitik atas bantuannya
selama Penulis menjalani penelitian.
Akhir kata, semoga karya ilmiah ini dapat bermanfaat.
Bogor, September 2008
RIWAYAT HIDUP
Penulis dilahirkan di Kuningan pada tanggal 14 Februari 1986 sebagai anak
pertama dari tiga bersaudara dari pasangan Mustofa Zaenudin dan Tetin Suhaetin.
Tahun 2004, Penulis lulus seleksi masuk Institut Pertanian Bogor (IPB) melalui
jalur Undangan Seleksi Masuk IPB (USMI) pada Departemen Kimia, Fakultas
Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, Penulis menjadi asisten praktikum Kimia
TPB pada tahun ajaran 2005/2006, Kimia Organik untuk mahasiswa Biokimia
tahun ajaran 2006/2007, Kimia Lingkungan tahun ajaran 2007/2008, Kimia
Analitik I dan II tahun ajaran 2007/2008, dan Spektroskopi D3 Analisis Kimia
pada tahun ajaran 2007/2008. Penulis juga aktif dalam kegiatan organisasi Ikatan
Mahasiswa Kimia (Imasika) pada tahun 2007. Penulis berkesempatan menjalani
Praktik Lapangan di Laboratorium Tanah dan Tanaman, SEAMEO BIOTROP
pada tahun 2007.
DAFTAR ISI
Halaman
DAFTAR TABEL ... ix
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Temulawak ... 1
Xantorizhol... 2
Kurkuminoid ... 2
Tokoferol... 3
Troloks ... 3
Antioksidan ... 3
Mekanisme Kerja Antioksidan ... 3
Uji Aktivitas Antioksidan ... 4
Kromatografi Cair Kinerja Tinggi ... 4
Spektrofotometri UV-Vis... 4
Evaluasi Data Analisis ... 5
BAHAN DAN METODE
Alat dan Bahan ... 5
Lingkup Kerja ... 5
PEMBAHASAN
Ekstraksi... 7
Kadar Kurkuminoid dan Xantorizhol Rimpang Temulawak ... 7
Aktivitas Antioksidan Metode DPPH... 8
Aktivitas Antioksidan Metode CUPRAC ... 9
Evaluasi Data Analisis ... 9
Sensitivitas Metode... 9
Perbandingan Metode Penentuan Aktivitas Antioksidan ... 10
SIMPULAN DAN SARAN
Simpulan ... 11
Saran ... 11
DAFTAR PUSTAKA ... 11
LAMPIRAN ... 14
DAFTAR TABEL
Halaman
1 Perbandingan Kapasitas Antioksidan Rimpang Temulawak Boyolali ... 10
2 Komponen Aktif dan Kapasitas Antioksidan Temulawak Semarang... 11
3
Hasil Pengukuran Kadar Air Rimpang Temulawak Boyolali ... 16
4 Hasil Pengukuran Kadar Air Rimpang Temulawak Semarang. ... 16
5 Rendemen Ekstrak Rimpang Temulawak ... 17
6 Absorbans standar kurkuminoid λ 420 nm... 18
7 Kadar Kurkuminoid Ekstrak Temulawak dengan Spektrofotometer UV-Vis. 18
8 Kadar Xantorhizol Ekstrak Temulawak Boyolali... 19
9 Kadar Xantorhizol Ekstrak Temulawak Semarang... 19
10 Absorbans Kurva Kalibrasi Troloks Metode DPPH ... 22
11 Kapasitas Antioksidan Metode DPPH ... 22
12 Absorbans Kurva Kalibrasi Troloks Metode CUPRAC... 23
13 Kapasitas Antioksidan Sampel Boyolali Metode CUPRAC ... 23
14 Kapasitas Antioksidan Sampel Semarang Metode CUPRAC ... 24
15 Kurva Standar Tokoferol Metode DPPH ... 25
16 Kurva Standar Tokoferol Metode CUPRAC ... 25
17 Hasil Evaluasi Analisis Metode CUPRAC dan DPPH Rimpang Temulawak 26
DAFTAR GAMBAR
Halaman
1 Rimpang Temulawak ... 1
2 Struktur Xantorhizol... 2
3 Struktur Kurkuminoid ... 2
4 Struktur α-Tokoferol ... 3
5 Struktur Troloks ... 3
6 Reaksi Penangkapan H dari Troloks oleh DPPH... 4
7 Reaksi Reduksi Kelat Bis-Neokuproin Tembaga (II) oleh Troloks... 4
8 Kurva Standar Kurkuminoid... 7
9 Kurva Kalibrasi Troloks Metode DPPH... 8
10 Kurva Kalibrasi Troloks Metode CUPRAC ... 9
11 Kurva Sensitivitas Metode DPPH terhadap Tokoferol ... 10
12 Kurva Sensitivitas Metode CUPRAC terhadap Tokoferol... 10
13 Kromatogram Xantorhizol Ekstrak Rimpang Temulawak Boyolali... 20
14 Kromatogram Xantorhizol Ekstrak Rimpang Temulawak Semarang ... 21
DAFTAR LAMPIRAN
Halaman
1 Diagram Alir Penelitian... 15
2 Penentuan Kadar Air Rimpang Temulawak ... 16
3 Penentuan Rendemen Ekstrak Rimpang Temulawak ... 17
4 Penentuan Kadar Kurkuminoid... 18
5 Penentuan Kadar Xantorhizol ... 19
6 Kromatogram KCKT Xantorhizol ... 20
7 Kapasitas Antioksidan Metode DPPH ... 22
8 Kapasitas Antioksidan Metode CUPRAC... 23
9 Sensitivitas Metode ... 25
10 Uji-F dan Uji-t Metode... 26
PENDAHULUAN
Temulawak (Curcuma xanthorrhiza)
merupakan salah satu tanaman obat yang banyak digunakan sebagai bahan baku dalam industri jamu dan farmasi. Temulawak diketahui memiliki banyak manfaat antara lain sebagai antihepatitis, antihiperlipidemia, antiinflamasi, antikarsinogenik, antimikrob, antiviral, detoksifikasi, dan antioksidan (WHO 1999). Salah satu komponen aktif yang bertanggung jawab terhadap respon biologis pada temulawak adalah kurkuminoid dan xantorhizol. Menurut Jayaprakasha et al. (2006) kurkuminoid pada rimpang temulawak berpotensi sebagai antioksidan. Demikian halnya dengan xantorhizol, selain memiliki aktivitas antibakteri paling tinggi juga berpotensi sebagai antioksidan (Hwang et al. 2004).
Antioksidan secara alami sudah terdapat dalam tubuh sebagai suatu sistem perlindungan tubuh dari pengaruh negatif radikal bebas. Jika radikal bebas berlebih dapat berpotensi menonaktifkan berbagai enzim dan mengoksidasi lemak sehingga sistem antioksidan dalam tubuh terganggu serta dapat menyebabkan berbagai penyakit (Anonim 2007). Senyawa antioksidan dalam bentuk tereduksi akan memiliki warna berbeda dengan bentuk teroksidasinya yang stabil sehingga perubahan warna tersebut dapat dideteksi dengan spektrofotometer pada panjang gelombang yang sesuai.
Terdapat beberapa metode penentuan kapasitas antioksidan di antaranya seperti DPPH (1,1-difenil-2-pikrilhidrazil) dan CUPRAC (cupric ion reducing antioxidant
capacity). Pemilihan metode DPPH pada
penentuan aktivitas antioksidan temulawak karena merupakan metode yang sederhana, mudah, cepat, peka, serta hanya memerlukan sedikit contoh. Sementara itu, metode CUPRAC dipilih karena dapat bekerja pada pH fisiologis, stabil, mudah dalam penggunaan, selektif, serta sensitif terhadap oksidan tipe tiol (Apak et al. 2004).
Metode di atas diekspresikan sebagai ekuivalen troloks dan diujikan pada tiga ekstrak, yaitu ekstrak etanol, ekstrak THF, dan ekstrak metanol. Pemilihan ekstrak berhubungan dengan komponen utama yang berperan dalam kapasitas antioksidan. Kurkuminoid dan xantorhizol yang diduga sebagai komponen utama yang berperan dalam aktivitas antioksidan ditentukan kadarnya menggunakan spektrofotometri
UV-Vis untuk kurkuminoid dan kromatografi cair kinerja tinggi (KCKT) untuk xantorizhol.
Berdasarkan penelitian sebelumnya dengan metode ekstraksi maserasi, diperoleh kapasitas antioksidan rimpang temulawak menggunakan metode DPPH dengan nilai konsentrasi penghambatan aktivitas radikal bebas sebanyak 50% (IC50) sebesar 106.58,
103.25, dan 101,66 mg/L berturut-turut untuk kadar xantorhizol 1.90, 1.86, dan 1.78 %(b/b) menggunakan pelarut etanol (Widiastuty 2006). Namun, dari penelitian tersebut tidak menunjukkan adanya korelasi linear antara kandungan xantorhizol terhadap aktivitas antioksidan, semakin tinggi kadar xantorhizol justru menunjukkan aktivitas antioksidan yang rendah. Oleh karena itu, diperlukan suatu metode yang sesuai sehingga terlihat proporsionalitas antara kandungan komponen aktif temulawak yang berperan sebagai antioksidan dan aktivitas antioksidannya.
Tujuan penelitian ini adalah membandingkan dan memilih metode yang sesuai dalam penentuan aktivitas antioksidan pada rimpang temulawak. Pemilihan metode didasarkan pada konsistensi kadar komponen aktif terhadap aktivitas antioksidan dan sensitivitas serta evaluasinya dengan uji statistika, yaitu uji-t dan uji-F untuk memberikan informasi mengenai ketepatan dan ketelitian pengukuran.
TINJAUAN PUSTAKA
TemulawakTemulawak (C. xanthorrhiza) merupakan tanaman yang berasal dari Indonesia khususnya daerah Jawa, Bali, dan Maluku.
Curcuma berasal dari bahasa arab kurkum
yang berarti kuning, sedangkan xanthorrhiza berasal dari bahasa Yunani xantos yang berarti kuning dan rhiza yang berarti akar. Temulawak ditunjukkan pada Gambar 1 telah digunakan oleh nenek moyang bangsa Indonesia untuk makanan, tujuan pengobatan, dan sebagai penambah energi (Hwang et al. 2006).
2
Temulawak atau dikenal juga JavaTurmeric (kunyit dari Jawa) diklasifikasikan
ke dalam kingdom Plantae, divisi Spermatophyta, subdivisi Angiospermae, kelas Monocotyledonae, ordo Zingiberales, famili Zingiberaceae, genus Curcuma, dan spesies Curcuma xanthorrhiza Roxb. Nama lain dari temulawak adalah koneng gede (suku Sunda), temu lawak (suku Jawa), temo labak (Madura), temu lawas dan temu raya (Malaysia), serta wan chakmotluk (Thailand).
Kandungan rimpang temulawak segar dapat dibedakan atas pati (48-59.64%), kurkuminoid (1.6-2.2%) dan minyak atsiri (1.48-1.63%) (Sidik et al. 1995). Temulawak merupakan tumbuhan yang tumbuh tegak dengan tinggi batang bisa mencapai 2 m, berwarna hijau atau cokelat gelap. Akar rimpang terbentuk dengan sempurna, bercabang kuat, dan berwarna hijau gelap. Tiap batang mempunyai daun 2-9 helai dengan bentuk bundar memanjang sampai bangun lanset, warna daun hijau atau coklat keunguan terang sampai gelap, panjang daun 31-84 cm dan lebar 10-18 cm, panjang tangkai daun termasuk helaian 43-80 cm. Daun termasuk tipe daun sempurna artinya tersusun dari pelepah daun, tangkai daun, dan helai daun (Sidik et al. 1995).
Temulawak dilaporkan memiliki berbagai aktivitas biologis seperti antitumor, antiinflamasi, antioksidan, hepatoprotektif, dan antibakteri. Aktivitas tersebut disebabkan komponen aktif temulawak berupa kurkuminoid dan xantorhizol (Hwang et al. 2006).
Xantorhizol
Xantorhizol merupakan komponen khas minyak atsiri yang diisolasi dari famili Zingiberaceae dan Astericeae seperti rimpang temulawak, dan termasuk ke dalam kelompok seskuiterpen tipe bisabolen (Aguilar et al. 2001). Xantorhizol memiliki rumus molekul C15H22O dengan bobot molekul 218.335
g/mol. Nama IUPAC dari xantorhizol adalah 5-(1,5-dimetilheks-4-enil)-2-metilfenol. Xantorhizol tidak berwarna, dan sangat pahit. Struktur xantorhizol ditunjukkan pada Gambar 2. H3C H O C H3 C H3 C H3 H
Gambar 2 Struktur xantorhizol. Xantorhizol memiliki aktivitas sebagai antibakteri, xantorhizol memiliki daya hambat
yang tinggi terhadap bakteri spesies
Streptococcus yang merupakan penyebab
karies pada gigi. Oleh karena itu, xantorhizol dapat digunakan dalam produk makanan dan pasta gigi untuk mencegah penyakit pada gigi. Dalam pasta gigi mengandung xantorhizol dengan konsentrasi 0.001-1.000% (b/b), sedangkan dalam pembersih mulut mengandung xantorhizol dengan konsentrasi 0.0001-0.1000% (b/b). Xantorizhol juga dapat digunakan sebagai agen potensial antibakteri dalam pembentukan biofilm oleh
Streptococcus mutans (Hwang et al. 2004)
Kurkuminoid
Kurkuminoid merupakan komponen yang memberi warna kuning pada rimpang temulawak (Sidik et al. 1995). Kurkuminoid berwarna kuning atau kuning jingga, berbentuk serbuk dengan rasa pahit, larut dalam aseton, alkohol, asam glasial, dan alkali hidroksida. Kurkuminoid mempunyai aroma yang khas dan tidak bersifat toksik (Sidik et
al. 1995). Kurkuminoid rimpang temulawak
terdiri atas dua komponen, yaitu kurkumin dan demetoksikurkumin. Berbeda dengan kurkuminoid pada rimpang kunyit (Curcuma
domestica Vahl.), selain mengandung dua
komponen diatas, juga mengandung bisdemetoksikurkumin. Sifat menarik dari bis-demetoksikurkumin ini adalah aktivitas kerjanya terhadap sekresi empedu antagonis dengan aktivitas kurkumin dan desmetoksikurkumin. Memperhatikan hal tersebut, penggunaan rimpang temulawak sebagai sumber kurkuminoid lebih menguntungkan dibanding dengan rimpang kunyit walaupun kandungan kurkuminoid rimpang temulawak lebih kecil dari rimpang kunyit (Afifah 2003). Struktur kimia kurkuminoid ditunjukkan pada Gambar 3.
Gambar 3 Struktur kurkuminoid Gambar 3 Struktur Kurkuminoid. Keterangan:
R1 R2
-OCH3 -OCH3 = kurkumin
-OCH3 -H = demetoksikurkumin
Kurkumin mempunyai rumus molekul C21H20O6 dengan bobot molekul 368 g/mol,
sedangkan demetoksikurkumin mempunyai
OH
R2
OH
R1
3
rumus molekul C20H18O5 dengan bobotmolekul sebesar 338 g/mol.
Kurkuminoid berkhasiat menetralkan racun, menurunkan kadar kolesterol, dan trigliserida darah, antibakteri, analgetik, dan antiinflamasi. Sekarang sudah banyak diteliti bahwa kurkuminoid dapat digunakan sebagai antioksidan dan inhibitor virus HIV (Anonim 2007).
Tokoferol
Tokoferol dikenal sebagai vitamin E terdiri atas senyawa aromatik tersubstitusi dan rantai isoprena dengan bobot molekul 430.17 g/mol. tokoferol berasal dari kata tokos artinya keturunan/kelahiran, person artinya memelihara dan ol termasuk senyawa golongan alkohol sehingga dapat disimpulkan tokoferol adalah vitamin yang membantu proses kelahiran. Selain berperan dalam proses kelahiran tokoferol juga dikenal sebagai antioksidan. Peranan tokoferol sebagai antiokasidan sangat kuat, tokoferol dapat membantu mencegah oksidasi terhadap vitamin A dengan menerima oksigen dalam sistem pencernaan dan menekan oksidasi asam lemak tak jenuh dalam jaringan (Winarno 1992). O CH3 CH3 HO H3C CH3 CH3 CH3 CH3 CH3
Gambar 4 Struktur α-Tokoferol. Tokoferol merupakan antioksidan alami yang dapat ditemukan hampir disetiap minyak tanaman, tetapi saat ini telah dapat diproduksi secara kimia. Tokoferol memiliki karakteristik berwarna kuning terang, cukup larut dalam lipida karena rantai C panjang. Pengaruh nutrisi secara lengkap dari tokoferol belum diketahui, tetapi α-tokoferol dikenal sebagai sumber vitamin E. Didalam jaringan hidup, aktivitas antioksidan tokoferol cenderung α ->β->γ->δ-tokoferol, tetapi dalam makanan aktivitas tokoferol terbalik δ->γ->β->α -tokoferol. Urutan tersebut kadang bervariasi bergantung pada substrat dan kondisi-kondisi lain seperti suhu (Trilaksani 2003).
Troloks
Troloks merupakan analog vitamin E yang larut dalam air (Davies et al. 1988). Troloks seperti terlihat pada Gambar 5 memiliki nama IUPAC 6-hidroksi-2,5,7,8-tetrametilkroman-2-asam karboksilat.
Berdasarkan metode rasimat troloks memiliki indeks kapasitas antioksidasi (AI) yang tinggi yaitu 4 sehingga senyawa yang berpotensi sebagai antioksidan dapat dinyatakan sebagai ekivalen troloks. Trolox Equivalent
Antioksidant Capacity (TEAC) adalah
konsentrasi troloks yang memiliki kapasitas antioksidan ekuivalen dengan sampel yang dianalisis (Apak et al. 2004).
O CH3 HO H3C CH3 COOH CH3
Gambar 5 Struktur Troloks. Antioksidan
Antioksidan didefinisikan sebagai senyawa yang dalam konsentrasi rendah dibandingkan dengan substrat yang dapat teroksidasi, secara signifikan menghambat dan mencegah oksidasi substrat (Safitri 2000). Antioksidan dalam tubuh bermanfaat untuk mencegah reaksi oksidasi yang ditimbulkan oleh radikal bebas baik berasal dari metabolisme tubuh maupun faktor eksternal lainnya.
Berdasarkan asalnya, antioksidan terdiri atas antioksigen yang berasal dari dalam tubuh (endogen) dan dari luar tubuh (eksogen). Adakalanya sistem antioksidan endogen tidak cukup mampu mengatasi stres oksidatif yang berlebihan. Stres oksidatif merupakan keadaan saat mekanisme antioksidan tidak cukup untuk memecah spesies oksigen reaktif (ROS). Oleh karena itu, diperlukan antioksidan dari luar (eksogen) untuk mengatasinya (Kukic et al. 2006). Antioksidan eksogen dibutuhkan ketika jumlah prooksidan dan antioksidan tubuh tidak seimbang.
Mekanisme Kerja Antioksidan Mekanisme kerja antioksidan secara umum menghambat oksidasi lemak atau disebut juga autooksidan yang terjadi dalam tiga tahap utama, yaitu iniasi, propagasi, dan terminasi. Pada tahap inisiasi terjadi pembentukan radikal asam lemak yaitu turunan asam lemak yang bersifat tidak stabil dan sangat reaktif akibat hilangnya satu atom H. Pada tahap propagasi, radikal asam lemak akan bereaksi dengan oksigen membentuk radikal peroksi. Radikal peroksi lebih lanjut akan menyerang asam lemak menghasilkan
4
hidroperoksida dan radikal asam lemak baru(tahap propagasi). Reaksi inisiasi LH L* + H* Reaksi propagasi L* + O2 LOO* LOO* + LH LOOH + L* Reaksi Terminasi
LOO* + LOO* LOOL + O2
LOO* + L* LOOL Uji Aktivitas Antioksidan
Metode penentuan aktivitas antioksidan diklasifikasikan berdasarkan transfer atom hidrogen dan transfer elektron (TE) (Apak et
al. 2007). Metode elektron transfer pengukurannya berdasarkan kapasitas antioksidan dalam mereduksi senyawa oksidan yang ditandai dengan perubahan warna ketika direduksi. Metode TE meliputi DPPH dan CUPRAC. Setiap metode memiliki pereaksi redoks kromogenik yang berbeda dengan potensial standar yang berbeda pula.
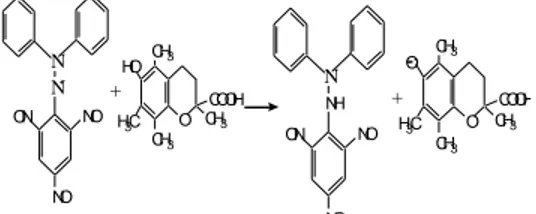
Pengujian antioksidan ekstrak tanaman dengan DPPH (1,1-difenil-2-pikrilhidrazil) pada prinsipnya adalah reaksi penangkapan hidrogen dari antioksidan oleh radikal bebas DPPH dan diubah menjadi 1,1-difenil-2-pikrilhidrazin (Gambar 6) N N. O CH3 HO H3C CH3 COOH CH3 NO NO ON NO NO ON N NH O CH3 O. H3C CH3 COOH CH3 + +
Gambar 6 Reaksi penangkapan atom H dari troloks oleh DPPH.
CUPRAC (cupric ion reducing antioxidant capacity) menggunakan pereaksi
tembaga (II) neokuproin sebagai agen pengoksidasi kromogenik. Metode ini mengukur kemampuan antioksidan dalam mereduksi kompleks Cu2+-Nc menjadi kompleks Cu+-Nc (Gambar 7). O CH3 HO H3C CH3 COOH CH3 N N H3C Cu2+ CH3 N N CH3 H3C N N H3C Cu+ CH3 N N CH3 H3C O CH3 CH3 O H3C COOH CH3 H+ + + +
Gambar 7 Reaksi reduksi kelat bis-neokuproin tembaga(II) oleh troloks.
Kromatografi Cair Kinerja Tinggi Kromatografi Cair Kinerja Tinggi (KCKT) merupakan teknik kromatografi dengan fase gerak berupa cairan (Harvey 2000). Dalam KCKT, sampel sebagai fase diam berupa cairan atau padatan yang dilarutkan dalam pelarut yang cocok. Sampel akan melewati kolom kromatografi bersama dengan fase gerak. Pemisahan teknik ini berdasarkan pada kesetimbangan komponen-komponen campuran diantara fase gerak dan fase diam. Sistem pemisahan pada penentuan kadar xantorhizol menggunakan fase nonpolar seperti kolom C18 dan fase gerak
bersifat polar seperti metanol. Penentuan kadar xantorhizol pada akar Iostephane
heterophylla menggunakan kolom C18,
ukuran partikel kolom 5 mikron, fase gerak asetonitril:air (85:15) dengan elusi isokratik, laju alir 1 mL/menit, menggunakan detektor UV pada panjang gelombang 230 nm dan diperoleh kadar xantorhizol 1.8 to 10.94 mg/g (Aguilar et al. 2007).
Teknik KCKT digunakan untuk memisahkan senyawa-senyawa yang tidak mudah menguap tetapi mudah terurai oleh panas. Selain untuk pemisahan, metode ini juga dapat digunakan untuk analisis kualitatif maupun kuantitatif seperti penentuan kadar xantorhizol dan kurkuminoid yang telah dilakukan pada penelitian sebelumnya. Alat yang digunakan untuk mendeteksi komponen-komponen yang keluar dari kolom adalah detektor. Detektor UV termasuk solute
property detector yang merespon sifat tertentu
dari solut (Skoog et al. 1998). Keuntungan menggunakan KCKT adalah jumlah contoh yang digunakan sedikit (mikroliter), waktu retensi hanya beberapa menit, dan batas deteksi sampai nanogram/liter (Hendayana et
al. 1994).
Spektrofotometri UV-Vis
Spektrofotometri merupakan suatu metode analisis yang mempelajari interaksi antara materi dengan radiasi elektromagnetik. Spektrofotometri serapan sinar tampak dan ultraviolet memanfaatkan sinar dengan panjang gelombang 400-700 nm untuk daerah sinar tampak dan 100-400 nm untuk daerah sinar UV. Bila suatu zat dikenai radiasi maka zat akan menyerap radiasi tersebut untuk berbagai keperluan.
Suatu zat dapat menyerap berbagai panjang gelombang suatu radiasi. Sudah tentu tidak seluruh radiasi yang mengenai zat
5
tersebut akan diserap, sebagian diteruskanatau ditransmisikan. Spektrum absorpsi merupakan gambaran hubungan antara panjang gelombang sinar yang mengenai suatu zat dengan besarnya serapan sinar pada panjang gelombang tersebut oleh zat yang bersangkutan. Pengukuran absorpsi radiasi UV-Vis oleh spesi larutan dapat digunakan sebagai metode analisis kuantitatif. Dasar penentuan kuantitatif teknik spektrofotometri adalah hukum Lambert-Beer.
A = log Io/I = lεc
A merupakan absorbans analat, Io adalah intensitas sinar sebelum melewati analat, I intensitas sinar setelah melewati analat, l ketebalan sampel yang dilalui sinar, ε koefisien absorpsi molekul, dan c adalah konsentrasi analat (Skoog et al. 1998).
Berdasarkan penelitian yang dilakukan oleh Pothitirat, diperoleh kadar kurkuminoid dalam rimpang temulawak asal Thailand Selatan yang diekstraksi menggunakan pelarut etanol dengan spektrofotometer UV-Vis sebesar 14.14 ± 0.87% sampai 26.76 ± 0.17% (b/b).
Evaluasi Data Analisis
Setiap metode yang digunakan untuk pekerjaan analisis pasti mengandung galat (error), baik galat acak maupun galat sistematik yang tidak selalu dapat kita hindarkan. Galat acak muncul akibat adanya sedikit variasi dalam setiap langkah prosedur analisis antara lain disebabkan oleh keterampilan dan kondisi pelaksanaan serta fluktuasi listrik selama analisis. Galat acak dapat dikurangi dengan memperbanyak jumlah pengukuran. Galat sistematik terjadi karena faktor yang tetap sehingga menimbulkan penyimpangan tertentu dari rerata hasil analisis terhadap nilai sebenarnya. Galat sistematik disebabkan oleh kelemahan metode, kesalahan alat, dan kesalahan personal. Oleh karena itu, dibutuhkan suatu evaluasi hasil analisis untuk mengukur sejauh mana suatu metode analisis dapat dipercaya.
Uji-uji statistik sederhana yang dapat dilakukan untuk memberikan informasi mengenai ketepatan dan ketelitian suatu pengukuran meliputi uji-t dan uji-F. Uji-t dilakukan untuk membandingkan efektivitas dan efisiensi metode baik dari segi teoritis maupun dari segi teknis (biaya). Uji ini membandingkan dua nilai rerata untuk melihat perbedaannya terlalu besar atau tidak untuk dijelaskan oleh galat acak. Uji F dilakukan untuk membandingkan hasil analisis dengan
menggunakan metode yang berbeda berdasarkan standar deviasinya, dan untuk melihat perbedaannya terlalu besar atau tidak untuk dijelaskan oleh galat acak (Harvey 2000). Di samping ketelitian dan ketepatan, dalam pemilihan metode analisis harus diperhatikan pula sensitivitas metode. Sensitivitas merupakan ukuran kemampuan metode untuk membedakan dua sampel. Semakin tinggi sensitivitas semakin baik suatu metode analisis (Harvey 2000).
BAHAN DAN METODE
Alat dan BahanPeralatan yang digunakan adalah peralatan gelas, maserator, oven, eksikator, cawan porselen, neraca analitik Precisa XT 220A, pipet mikro, penguap putar Buchi R-114, spektrofotometer UV-Vis model U-2800 Hitachi, kuvet persegi, dan KCKT La Chrome Elite dengan detektor UV-Vis L-2420 Hitachi dan kolom C-18.
Bahan-bahan yang digunakan dalam penelitian ini adalah sampel rimpang temulawak Boyolali dan Semarang, standar tokoferol, standar kurkuminoid, standar xantorizhol, akuades, etanol 96%, metanol 75%, tetrahidrofuran (THF) dari Sigma, etil asetat, larutan DPPH 0.1 mM, troloks(6-hidroksi-2,5,7,8-tetrametilkroman-2-asam karboksilat) dari Sigma, CuCl2·2H2O,
Neokuproin alkoholik 0.0075M dari Sigma, dan bufer amonium asetat pH 7.
Lingkup Kerja Penentuan Kadar Air
Cawan porselen dikeringkan pada suhu 105 °C. Setelah didinginkan dalam eksikator, kemudian ditimbang. Sebanyak 3 g sampel rimpang temulawak ditimbang (dicatat sampai 4 desimal dalam gram), dimasukkan dalam cawan, dan dikeringkan pada temperatur 105 °C. Setelah 6 jam, sampel diambil, didinginkan dalam eksikator, dan ditimbang. Hal ini dilakukan sampai diperoleh bobot yang konstan.
Ekstraksi Etanol Rimpang Temulawak (Metode PSB 2003)
Ekstrak dibuat dengan cara maserasi menggunakan etanol 96%. Sebanyak 100 gram serbuk kering rimpang temulawak dimasukkan ke dalam maserator, ditambah 500 ml etanol 96% direndam selama 24 jam sambil sekali-kali diaduk. Maserat dipisahkan
6
dan proses diulang dua kali dengan jenis danjumlah pelarut yang sama. Semua maserat dikumpulkan dan diuapkan dengan penguap putar kemudian dipekatkan hingga diperoleh ekstrak kental (Metode ekstraksi Korea). Ekstraksi THF Rimpang Temulawak (WHO 1999)
Sebanyak 15 gram sampel dilarutkan dalam 500 ml tetrahidrofuran (THF). Larutan disimpan dalam suhu kamar selama 24 jam. Kemudian disaring dan diambil filtratnya. Larutan dipekatkan dengan penguap putar. Ekstraksi Metanol Rimpang Temulawak (Hwang 2004)
Sebanyak 100 gram rimpang temulawak diekstrak dengan 400 ml metanol 75% pada suhu ruang selama 2 hari, kemudian ekstrak disaring menggunakan kertas saring Whatman No 42. Filtrat dipekatkan dengan penguap putar selanjutnya diekstraksi menggunakan etilasetat (1:4) sebanyak 2 kali ulangan dan dipekatkan kembali dengan penguap putar hingga diperoleh ekstrak pekat etil asetat. Uji Aktivitas Antioksidan dengan Metode DPPH (Wong et al. 2006)
Larutan DPPH 0.1 mM dalam metanol disiapkan. Sebanyak 40 µL larutan ekstrak yang telah diencerkan dengan metanol ditambahkan ke dalam 3 ml larutan DPPH dalam metanol. Larutan diukur pada panjang gelombang 515 nm setelah 30 menit. Blangko yang digunakan adalah pereaksi tanpa penambahan larutan ekstrak. Kurva kalibrasi dibuat menggunakan larutan troloks dengan konsentrasi 1, 3, 5, 7, dan 9 µM. Kapasitas antioksidan berdasarkan kemampuan memecah radikal DPPH dan dinyatakan sebagai µmol troloks /g ekstrak.
Uji Aktivitas Antioksidan dengan Metode CUPRAC (Cupric ion reducing antioxidant capacity) (Apak et al. 2004)
Sebanyak 1 ml larutan CuCl2 0.01 M, 1
ml larutan neokuproin alkoholik 0.0075 M, dan 1 ml larutan buffer ammonium asetat pH 7 ditambahkan ke dalam 0.1 ml akuades dan 1 ml larutan ekstrak yang dilarutkan pada etanol 96%. Volume total sebesar 4.1 ml. Blangko yang digunakan adalah pereaksi tanpa penambahan larutan ekstrak. Larutan diukur pada panjang gelombang 457 nm setelah 30 menit. Kurva kalibrasi dibuat menggunakan larutan troloks dengan konsentrasi 10, 20, 30, 40, 50, 60, 70, dan 80 µM. Kapasitas
antioksidan dinyatakan dalam µmol troloks/g ekstrak .
Penentuan Kadar Xantorizhol
Ekstrak yang diperoleh, ditentukan kadar xantorizholnya dengan menggunakan KCKT. Sistem KCKT dgunakan ialah kolom C-18, etektor UV-Vis, volume injeksi 10 µL, elusi gradien, dan suhu kolom 40 ºC.
Penentuan Kadar Kurkuminoid
Analisis kuantitatif kurkuminoid metode spektrofotometri dibuat dengan cara standar kurkuminoid 100 ppm diencerkan dengan metanol sehingga diperoleh konsentrasi 0.25, 1, 2, 3, 4, dan 5 ppm. Setelah itu serapan diukur menggunakan spektrofotometer Uv-Vis pada panjang gelombang 420 nm sehingga diperoleh kurva standar kurkuminoid. Analisis sampel dibuat dengan cara sebanyak 0.1 g ekstrak pekat dilarutkan dalam 10 ml THF kemudian disimpan selama 24 jam pada suhu kamar dalam keadaan gelap. Setelah 24 jam penyimpanan supernatan temulawak diambil dan diencerkan hingga 1250 kali dengan metanol. Selanjutnya larutan dikocok sempurna dan diukur serapannya pada panjang gelombang 420 nm.
Evaluasi Data Analisis
Data hasil penelitian dievaluasi berdasarkan ketelitian dan sensitivitas (Lampiran 9 dan 10). Ketelitian dinyatakan dengan hasil uji-F sedangkan ketepatan dinyatakan dalam uji-t.
Sensitivitas
Sensitivitas metode dilakukan dengan membuat larutan standar tokoferol konsentrasi 5, 10, 15, 20, dan 25 ppm kemudian dianalisis aktivitas antioksidannya dengan metode DPPH dan CUPRAC sehingga diperoleh nilai koefisien determinasi (R2) paling tinggi, mendekati nilai 1. Nilai slope persamaan regresi linear merupakan koefisien sensitivitas metode.
Uji-t
Uji-t dilakukan dengan hipotesis H0:
kedua metode memiliki hasil analisis yang sama. Penarikan simpulan berdasarkan nilai t hitung, apabila nilai thitung < ttabel maka H0
diterima tetapi jika nilai thitung > ttabel maka H0
ditolak. Nilai ttabel = 2.685 derajat bebas 9
pada selang kepercayaan 95%. Uji-F
7
Uji-F dilakukan dengan hipotesis H0:kedua metode memiliki standar deviasi yang sama. Penarikan simpulan berdasarkan nilai F hitung, apabila nilai Fhitung < Ftabel maka H0
diterima tetapi jika nilai Fhitung > Ftabel maka H0
ditolak. Nilai Ftabel = 6.256 apabila metode 1
sebanyak 5 ulangan dan metode 2 sebanyak 4 ulangan pada selang kepercayaan 95%.
HASIL DAN PEMBAHASAN
EkstraksiSerbuk rimpang temulawak yang diperoleh asal Boyolali dan Semarang ditentukan kadar airnya. Kadar air yang diperoleh sebesar 12.84 ± 0.16% untuk sampel asal Boyolali dan 15.05 ± 0.30% untuk sampel asal Semarang (Lampiran 2). Tujuan pengeringan adalah agar sampel tidak mudah rusak sehingga dapat disimpan dalam waktu yang lama. Dengan mengurangi kadar air, kerusakan sampel oleh mikroba dapat dihindari. Nilai yang diperoleh >10% menandakan masih terdapat air dalam sampel rimpang temulawak dan tidak baik disimpan dalam jangka waktu lama sehingga sampel yang telah diekstrak dan dipekatkan harus segera dianalisis dengan memperhatikan faktor koreksi.
Ekstraksi serbuk rimpang temulawak menggunakan metode maserasi dengan pelarut etanol, THF, dan metanol. Pemilihan pelarut yang berbeda berhubungan dengan komponen utama yang berperan sebagai antioksidan dalam rimpang temulawak. Etanol digunakan karena memiliki kepolaran yang tinggi untuk mengekstrak berbagai komponen termasuk kurkuminoid dan xantorhizol. Metanol digunakan untuk mengekstrak senyawa xantorhizol yang kemudian dipisahkan dengan etil asetat karena kelarutan xantorhizol dalam etil asetat yang tinggi (Hwang 2004). Sementara THF digunakan untuk mengekstrak senyawa kurkuminoid dalam sampel karena kelarutan kurkuminoid dalam THF lebih tinggi dibandingkan dengan etanol maupun metanol.
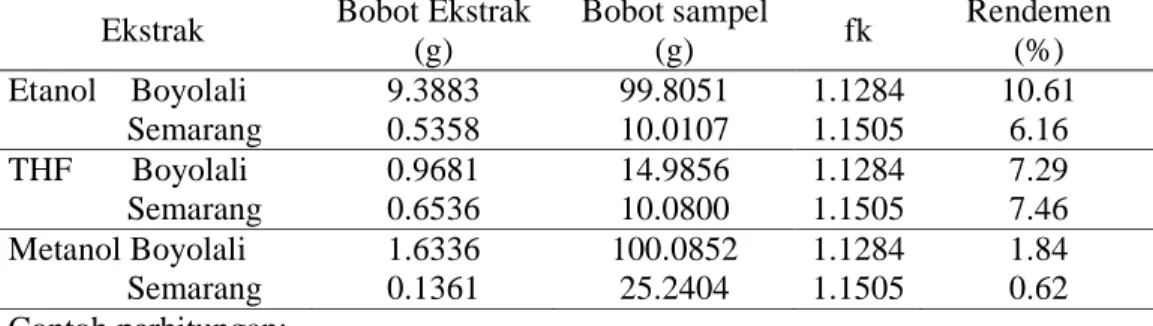
Rendemen ekstrak sampel dari Boyolali yang terdiri atas ekstrak etanol, ekstrak THF, dan ekstrak metanol berturut-turut adalah 10.61%, 7.29%, dan 1.84%. Sementara rendemen ekstrak sampel dari Semarang berturut-turut adalah 6.16%, 7.46%, dan 0.62% (Lampiran 3).
Kadar Kurkuminoid dan Xantorizhol Rimpang Temulawak
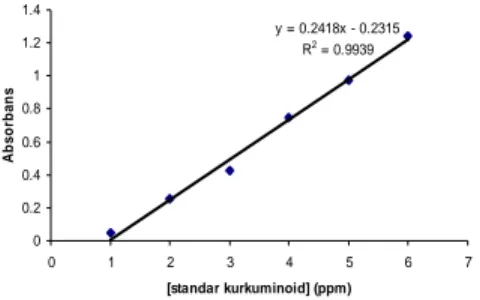
Ekstrak rimpang temulawak ditentukan kadar kurkuminoidnya menggunakan spektrofotometer UV-Vis pada panjang gelombang 420 nm dan diperoleh persamaan kurva standar ditunjukkan pada Gambar 8, yaitu y=0.2418x-0.2315 dengan R2=99.39%. Kadar kurkuminoid rimpang temulawak asal Boyolali dan Semarang, yaitu untuk ekstrak etanol, THF, dan metanol berturut-turut sebesar 20.10%, 26.82%, 21.72% dan 30.77%, 33.85%, 28.03% (Lampiran 4). y = 0.2418x - 0.2315 R2 = 0.9939 0 0.2 0.4 0.6 0.8 1 1.2 1.4 0 1 2 3 4 5 6 7 [standar kurkuminoid] (ppm) A b s o rb a n s
Gambar 8 Kurva standar kurkuminoid. Hasil diatas menunjukkan bahwa pada sampel asal Boyolali dan Semarang diperoleh kadar kurkuminoid ekstrak THF lebih besar dibandingkan dengan ekstrak etanol dan ekstrak metanol karena seperti telah disebutkan sebelumnya bahwa kelarutan kurkuminoid dalam THF lebih tinggi dibandingkan dengan etanol maupun metanol. Sementara pada percobaan sebelumnya diperoleh kadar kurkuminoid ekstrak rimpang temulawak sebesar 1.92% dengan pelarut air (Yulanda 2007), 25.45% dengan pelarut etanol dilanjutkan dengan ekstraksi cair-cair menggunakan heksana untuk nisbah bahan baku-pelarut 1:3 (Afif 2006), dan 29.52% dengan nisbah bahan baku-pelarut aseton sebesar 1:6 pada suhu 70ºC (Supriadi 2008). Selama penyimpanan ekstrak harus terlindung dari cahaya karena kurkuminoid mempunyai sifat sensitif terhadap cahaya. Bila kurkuminoid terkena cahaya akan terjadi dekomposisi struktur berupa siklisasi kurkuminoid. Siklisasi kurkuminoid menyebabkan senyawa kurkuminoid terdegradasi menjadi asam ferulat sehingga kadarnya dalam ekstrak menjadi rendah (Sidik
et al. 1995).
Kadar xantorhizol sampel asal Boyolali dan Semarang ditentukan menggunakan KCKT dan diperoleh kadar xantorizhol untuk ekstrak etanol, THF, dan metanol
berturut-8
turut sebesar 0.01%, 0.09%, dan 0.004%.Sementara kadar xantorhizol sampel asal Semarang untuk ekstrak etanol, THF, dan metanol berturut-turut sebesar 0.19%, 0.17%, dan 0.02% (Lampiran 5). Sementara berdasarkan percobaan sebelumnya diperoleh kadar xantorhizol rimpang temulawak asal Semarang hasil budi daya PSB, Balitro, dan Lokal berturut-turut sebesar 1.78%, 1.86%, dan 1.90% (Widiastuty 2006). Dengan demikian kadar xantorhizol rimpang temulawak asal Boyolali dan Semarang jauh lebih rendah dibandingkan ketiga rimpang diatas. Kadar xantorhizol dipengaruhi pula oleh letak geografis, umur rimpang, jenis rimpang (induk, anak, cucu) dan teknik budi daya (organik dan anorganik). Berdasarkan pustaka ekstrak metanol yang dipisahkan dengan etil asetat seharusnya memiliki kadar xantorhizol paling tinggi tetapi hasil yang diperoleh masih lebih kecil dibandingkan dengan ekstrak THF dan etanol. Hal ini kemungkinan karena xantorhizol pada ekstrak metanol belum larut sempurna sehingga kadar yang diperoleh menjadi lebih kecil.
Aktivitas Antioksidan dengan Metode DPPH
Aktivitas antioksidan dapat ditentukan dengan melihat kemampuan ekstrak rimpang temulawak dalam menghambat radikal bebas DPPH. Radikal DPPH (1,1-difenil-2-pikrilhidrazil) merupakan radikal nitrogen, meskipun tidak sereaktif radikal oksigen seperti RO. atau ROO. tetapi mampu terstabilkan oleh sistem resonansi (Windono
et al. 2003). Aktivitas antioksidan metode
DPPH dinyatakan dalam ekuivalen troloks karena lebih bermakna dan terdeskripsikan dibandingkan dengan aktivitas antioksidan yang dinyatakan dalam persen inhibisi (Wong
et al. 2006). Kapasitas antioksidan rimpang
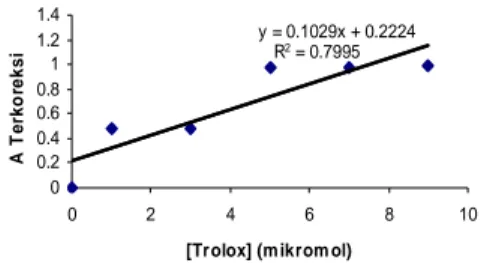
temulawak yang dinyatakan dalam ekuivalen troloks, ditentukan konsentrasi sampel rimpang temulawak ekuivalen troloks melalui persamaan reaksi kurva kalibrasi trolox ditunjukkan pada Gambar 9, yaitu y = 0.2224 + 0.1029x dengan R2 = 79.95%. Nilai R2 menggambarkan korelasi antara konsentrasi analat dan sinyal analat. Semakin tinggi nilai R2 semakin kuat korelasi antara konsentrasi analat dan sinyal analat. Menurut ICH (1995) nilai koefisien korelasi yang memenuhi persyaratan adalah lebih besar dari 0.9972 sedangkan secara statistik 0.80 masih menunjukkan korelasi yang cukup kuat. Nilai R2 hasil percobaan menunjukkan korelasi
kurang kuat antara konsentrasi trolox dan nilai absorbans sehingga dapat dikatakan korelasi antara keduanya nonlinear.
y = 0.1029x + 0.2224 R2 = 0.7995 0 0.2 0.4 0.6 0.8 1 1.2 1.4 0 2 4 6 8 10
[Trolox] (m ikrom ol)
A T e rk o re k s i
Gambar 9 Kurva Kalibrasi Troloks Metode DPPH.
Kapasitas antioksidan ekstrak etanol sebesar 0.8953 µmol troloks/g ekstrak, ekstrak THF 0.8818 µmol troloks/g ekstrak, dan ekstrak metanol 0.8827 µmol troloks/g ekstrak. Berdasarkan kurva kalibrasi terlihat bahwa pada konsentrasi troloks diatas 5 µM sudah menunjukkan aktivitas troloks yang maksimal dalam menghambat radikal DPPH. Hasil yang diperoleh menunjukkan bahwa kapasitas antioksidan ekstrak etanol > ekstrak metanol > ekstrak THF (Lampiran 7). Hal ini tidak sesuai dengan kadar kurkuminoid dalam ekstrak THF > ekstrak metanol > ekstrak etanol dan kadar xantorizol ekstrak THF > ekstrak etanol > ekstrak metanol. Hasil tersebut tidak menunjukkan adanya korelasi linear antara aktivitas antioksidan dan kandungan kurkuminoid atau xantorhizol. Hal ini dimungkinkan karena adanya senyawa lain dalam ekstrak sampel yang bersifat inhibitor atau memiliki peran antagonis terhadap aktivitas antioksidan rimpang temulawak, disamping itu setiap ekstrak memiliki matriks yang berbeda sehingga memiliki kemampuan aktivitas antioksidan yang berbeda (Widiastuty 2006).
Pada saat reaksi antara DPPH dan senyawa antioksidan, terjadi dehidrogenasi pada molekul antioksidan dan DPPH berubah menjadi DPPHn dengan n menunjukkan jumlah atom H yang diterima oleh DPPH dari antioksidan (Windono et al. 2003). DPPH berwarna violet dan DPPHn memiliki warna yang berkurang kepekatannya mendekati kuning sehingga memungkinkan pengukuran dengan spektrofotometri dari perubahan warna DPPH menjadi DPPHn. Absorbans yang rendah menunjukkan kapasitas pemecahan DPPH yang lebih tinggi.
9
Aktivitas Antioksidan dengan MetodeCUPRAC
Aktivitas antioksidan dapat ditentukan pula dengan menambahkan suatu pereaksi kromogenik. Pereksi kromogenik yang digunakan adalah neokuproin (Nc), yang akan membentuk kelat dengan Cu2+ sehingga terbentuk bis-neokuproin tembaga (II) atau Cu2+-Nc yang berwarna biru. Potensial standar Cu(Nc)2
2+/+
sebesar 0.6 V lebih besar dibandingkan dengan Cu2+/+ sebesar 0.17 V sehingga Cu(Nc)2
2+
lebih mudah tereduksi dan antioksidan semakin cepat teroksidasi (Apak
et al. 2004). Aktivitas antioksidan dapat
dilihat dari kemampuannya mereduksi Cu2+ -Nc menjadi Cu+-Nc yang berwarna kuning. Kelat Cu+-Nc ini bersifat stabil karena tidak sensitif terhadap perubahan lingkungan berupa udara, cahaya, ataupun pH seperti radikal kromogenik DPPH.
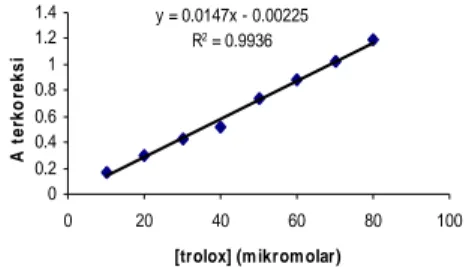
Penentuan kapasitas antioksidan rimpang temulawak dinyatakan dalam ekuivalen troloks. Persamaan reaksi kurva kalibrasi troloks ditunjukkan pada Gambar 10, yaitu y=0.0147x-0.00225 dengan R2= 99.36%. y = 0.0147x - 0.00225 R2 = 0.9936 0 0.2 0.4 0.6 0.8 1 1.2 1.4 0 20 40 60 80 100
[trolox] (m ikrom olar)
A t e rk o re k s i
Gambar 10 Kurva Kalibrasi Troloks Metode CUPRAC.
Berdasarkan persamaan tersebut dapat ditentukan konsentrasi sampel dan ditentukan kapasitas antioksidannya berturut-turut untuk ekstrak etanol, THF, dan metanol sebesar 42.5933 µmol troloks/g ekstrak, 131.5937µmol troloks/g ekstrak, dan 30.4542 µmol troloks/g ekstrak (Lampiran 8). Hasil tersebut menunjukkan adanya linearitas antara kandungan komponen yang berperan sebagai antioksidan terhadap aktivitas antioksidannya. Semakin tinggi kadar xantorhizol semakin tinggi pula aktivitas antioksidannya. Namun berbeda halnya dengan kurkuminoid, kadar kurkuminoid ekstrak metanol lebih besar 1.62% dibandingkan dengan ekstrak etanol tetapi kapasitas antioksidan ekstrak etanol lebih besar 12.1391 µmol troloks/g ekstrak. Hal ini kemungkinan karena sifat
kurkuminoid yang mudah terdegradasi oleh cahaya.
Evaluasi Hasil Analisis
Ketelitian suatu metode dapat dibandingkan melalui %SBR. Penentuan presisi atau ketelitian kedua metode ini ditunjukkan pada Lampiran 10. Hasil yang diperoleh untuk metode DPPH mulai dari ekstrak etanol, THF, dan metanol adalah 1.0095%, 3.1300%, dan 2.6849% yang berarti metode DPPH untuk ekstrak etanol teliti (%SBR 1-2), ekstrak THF dan metanol cukup teliti (%SBR 2-5). Metode CUPRAC memiliki %SBR berturut-turut mulai dari ekstrak etanol, THF, dan metanol sebesar 11.2142%, 3.5838%, dan 3.2304% yang berarti metode CUPRAC untuk ekstrak etanol tidak teliti (%SBR > 5), ekstrak THF dan metanol cukup teliti (%SBR 2-5) menurut AOAC (2003). Untuk membandingkan kedua metode berdasarkan simpangan baku dilakukan uji F dengan selang kepercayaan 95%, F hitung ekstrak etanol, THF, dan metanol sebesar 279296.3627, 29196.4083 dan 1723.1256 Hasil yang diperoleh F hitung > F tabel sehingga simpangan baku kedua metode berbeda nyata, perbedaannya terlalu besar untuk dijelaskan oleh galat acak.
Uji t dilakukan untuk membandingkan hasil analisis kedua metode berdasarkan reratanya. Ekstrak etanol, THF, dan metanol memiliki nilai t hitung sebesar 19.5204, 61.9753, dan 78.3620. Hasil yang diperoleh t hitung > t tabel sehingga kedua metode akan menghasilkan rerata analisis yang berbeda. Metode CUPRAC memberikan hasil analisis yang lebih besar dibandingkan metode DPPH.
Sensitivitas Metode
Respon analat dan komposisi dari matriks sampel merupakan faktor penting dalam menentukan sensitivitas (Willard HH et al 1988). Sensitivitas metode dilakukan terhadap tokoferol karena memiliki sifat lipofilik yang sama dengan analat dalam sampel rimpang temulawak sehingga dimungkinkan memiliki sensitivitas metode yang sama terhadap ekstrak rimpang temulawak. Persamaan regresi linear hubungan antara konsentrasi tokoferol (ppm) dan nilai absorbans metode DPPH dan CUPRAC ditunjukkan pada Gambar 11 dan 12, yaitu y=0.0603x + 0.0442 dan y=0.0402x + 0.0382 (Lampiran 9).
10
y = 0.0603x + 0.0442 R2 = 0.9707 0 0.2 0.4 0.6 0.8 1 1.2 1.4 1.6 1.8 0 5 10 15 20 25 30 [tokoferol] (ppm ) A b s o rb a n s t e rk o re k s iGambar 11 Hubungan [tokoferol] (ppm) dan absorbans metode DPPH. y = 0.0402x - 0.0382 R2 = 0.9914 0 0.2 0.4 0.6 0.8 1 1.2 0 5 10 15 20 25 30 [tokofol] (ppm) A
Gambar 12 Hubungan [tokoferol] (ppm) dan absorbans metode CUPRAC. Persamaan diatas menunjukkan hubungan yang linear antara konsentrasi dan sinyal analat, semakin tinggi konsentrasi semakin tinggi nilai absorbans pada range konsentrasi 5-25 ppm. Kemiringan garis kurva kalibrasi digunakan untuk menentukan koefisien sensitivitas metode. Nilai koefisien sensitivitas metode DPPH terhadap tokoferol 0.0603 dan metode CUPRAC terhadap tokoferol 0.0402. Hasil tersebut menunjukkan metode DPPH lebih sensitif terhadap tokoferol, semakin tinggi nilai koefisien sensitivitas semakin tinggi pula sensitivitas metode tersebut karena sedikit saja perubahan konsentrasi analat mampu memberi respon yang signifikan.
Perbandingan Metode Penentuan Aktivitas Antioksidan
Beragamnya matriks dan kandungan senyawa fitokimia pada ekstrak rimpang temulawak mengakibatkan aktivitas antioksidan ekstrak etanol, THF, maupun metanol penting untuk diperiksa dengan lebih dari satu metode. Penelitian ini menggunakan metode DPPH dan CUPRAC. Penentuan aktivitas antioksidan ekstrak tumbuhan yang dilakukan dengan metode yang berbeda memberikan hasil yang acak, sulit untuk dibandingkan dan terkadang menimbulkan ketidakcocokan (Koleva et al. 2002 dalam Ridwina 2008) sehingga kapasitas antioksidan kedua metode dinyatakan dalam ekuivalen troloks (Tabel 1).
Berdasarkan data pada Tabel 1, kapasitas antioksidan ketiga ekstrak rimpang temulawak tersebut dengan metode CUPRAC lebih tinggi dibandingkan dengan metode DPPH. Hal ini kemungkinan karena kurkuminoid maupun xantorhizol sebagai komponen antioksidan dalam sampel tidak terlalu reaktif terhadap radikal DPPH karena adanya halangan sterik yang tidak mudah dilewati sehingga hanya molekul kecil yang memiliki peluang lebih mudah untuk bereaksi dengan radikal. Dalam hal ini, berarti metode DPPH memiliki linearitas kisaran absorbans dan konsentrasi yang sempit berbeda dengan metode CUPRAC yang mampu bereaksi dengan molekul besar sekalipun sehingga memiliki linearitas kisaran absorbans dan konsentrasi yang luas. Disamping itu, pengukuran kapasitas antioksidan metode DPPH tidak menunjukkan hubungan yang linear antara komponen aktif antioksidan dan kapasitas antioksidannya, sementara metode CUPRAC menunjukkan hubungan yang linear antara kedua hal tersebut. Hal ini dibuktikan kembali terhadap sampel berbeda yang berasal dari Semarang (Tabel 2).
Tabel 1 Perbandingan kapasitas antioksidan rimpang temulawak Boyolali Ekstrak Kadar Kurkuminoid %(b/b) Kadar Xantorizol %(b/b) Kapasitas Antioksidan Metode DPPH (µmol tr/g ekstrak) Kapasitas Antioksidan Metode CUPRAC (µmol tr/g ekstrak) Etanol 20.10 0.010 0.8953 42.5933 THF 26.82 0.086 0.8818 131.5937 Metanol 21.72 0.004 0.8827 30.4542
11
Tabel 2 Kadar komponen aktif dan kapasitas antioksidan rimpang Temulawak SemarangBerdasarkan Tabel 2 kapasitas antioksidan semakin meningkat dengan meningkatnya kadar xantorhizol, berbeda dengan kadar kurkuminoid ekstrak etanol < ekstrak THF tetapi memiliki kapasitas antioksidan ekstrak etanol > ekstrak THF. Seharusnya peranan kurkuminoid sebagai antioksidan lebih dominan dibandingkan dengan xantorizhol karena stabilitas resonansi pada kurkuminoid melibatkan 2 buah cincin aromatik dan ikatan rangkap terkonjugasi sehingga delokalisasi radikal lebih terstabilkan, namun sifat kurkuminoid yang sensitif terhadap cahaya dan mudah terdegradasi sehingga kemungkinan mempengaruhi terhadap aktivitas antioksidannya.
Apabila dilihat berdasarkan ketelitian dan sensitivitas, metode DPPH lebih teliti dan kemungkinan lebih sensitif dalam menganalisis aktivitas antioksidan rimpang temulawak dibandingkan metode CUPRAC, meskipun demikian metode CUPRAC lebih sesuai untuk penentuan aktivitas antioksidan rimpang temulawak karena dapat diterapkan untuk mengatasi berbagai matriks sampel yang terdapat dalam rimpang temulawak
SIMPULAN DAN SARAN
SimpulanPerbandingan metode penentuan aktivitas antioksidan menunjukkan bahwa metode CUPRAC lebih sesuai untuk menganalisis aktivitas antioksidan ekstrak rimpang temulawak berdasarkan kandungan komponen aktifnya, yaitu kurkuminoid dan xantorhizol. Ekstrak etanol, THF, dan metanol memiliki kadar kurkuminoid dan xantorhizol berturut-turut 20.10%, 26.82%, 21.72% dan 0.01%, 0.09%, 004%
.
Kapasitas antioksidan untuk ketiga ekstrak berturut-turut sebesar 42.5933, 131.5937, dan 30.4542 µmol troloks/g ekstrak. Metode DPPH memiliki kapasitas antioksidan untuk ketiga ekstrak berturut-turut sebesar 0.8953, 0.8818, dan 0.8827 µmol troloks/g ekstrak. Sensitivitas metode DPPH > metode CUPRAC terhadap tokoferol yang memiliki sifat lipofilik yang sama dengan kurkuminoid maupun xantorhizol dalamrimpang temulawak. Persentase SBR metode DPPH < metode CUPRAC sehingga metode DPPH lebih teliti dibandingkan dengan metode CUPRAC. Uji t menunjukkan hasil analisis yang berbeda nyata, sedangkan uji F memperlihatkan keragaman yang berbeda nyata antara kedua metode.
Saran
Ekstrak rimpang temulawak mulai dari ekstraksi sampai dengan analisis harus terlindungi dari cahaya karena akan mengurangi kadar kurkuminoid dalam ekstrak. Pada metode CUPRAC komponen yang tidak larut air sebaiknya menggunakan pelarut diklorometana sehingga diharapkan memiliki sensitivitas yang lebih tinggi dalam menganalisis sampel lipofilik.
DAFTAR PUSTAKA
Afif KH. 2006. Peningkatan Kadar Kurkumin Ekstrak Etanol Temulawak Dengan Metode Ekstraksi Cair-cair [Skripsi]. Bogor: Departemen Kimia FMIPA, IPB. Afifah E. 2003. Khasiat dan Manfaat
Temulawak: rimpang penyembuh aneka penyakit. Jakarta: Agromedia Pustaka.
Aguilar MI, Guillermo D, Maria LV. 2001. New bioactive derivatives of xanthorrhizol. J Mex Chem Soc 45:56-59. Anonim. 2007a. Antioksidan penting untuk mencegah sakit jantung. [terhubung berkala] http//www.lizaherbal.com. [21 Desember 2007].
Anonim. 2007b. Peranan antioksidan dalam menjaga kesehatan keluarga. [terhubung berkala] http//www.santamaria.or.id. [21 Desember 2007].
Apak et al.. 2007. Comparative evaluation of various total antioxidant capacity assay applied to phenolic compounds with the CUPRAC assay. Molecules 12:1496-1547.
Ekstrak Kadar Kurkuminoid %(b/b) Kadar Xantorhizol %(b/b) Kapasitas Antioksidan Metode CUPRAC (µmol tr/g ekstrak) Etanol 30.77 0.19 97.5599 THF 33.85 0.17 72.0673 Metanol 28.03 0.02 68.5104
12
Apak R, K Güçlü, M Özyürek, SE Çelik, SEKarademir. 2004. Novel total antioxidant capacity index for dietary polyphenols and vitamins C and E, using their cupric ion reducing capability in the presence of neocuproine: CUPRAC method. J Agric
Food Chem 52:7970-7981.
[AOAC] Association of Official Analytical Chemistry. 2005. Official Methods of
Analysis of AOAC International. Ed-18.
Maryland: AOAC International.
Davies MJ, LG Forni, RL Willson. 1988. Vitamin E analogue Trolox C. Biochem J 255:513-522.
Harvey D. 2000. Modern Analytical Chemistry. Toronto: McGraw-Hill.
Hendayana S, Kadarohman A, Sumarna AA, Supriatna A. 1994. Kimia Analitik
Instrumen. Ed ke-1. Semarang: IKIP
Semarang Press.
Hwang JK, penemu; LG Household & Healthcare. 24 Feb 2004. Antibacterial composition having xanthorrhizol. US Patent 6 696 404.
[ICH] International Conference on Harmonization. 1995. Validation of Analytical Prosedures: Methodology Q2B [terhubung berkala]. www.ich.org [8 Sep 2008].
Jayaprakasha GK, LJ Rao, KK Sakariah. 2006. Antioxidant activities of curcumin, demethoxycurcumin, and bisdemethoxycurcumin. Food Chem
98:720-724.
Kukic J, Silvana P, Marjan N. 2006. Antioxidant activity of four endemic
Stachys Taxa. Biol Pharm Bull
29(4):725-729.
Ridwina G. 2008. Perbandingan Pengukuran Aktivitas Antioksidan dan Ekstrak Etanol dan Minyak Atsiri Lempuyang Gajah [Skripsi]. Bogor: Departeman Kimia FMIPA, IPB.
Safitri R. 2000. Ekstraksi dan Identifikasi dari Tumbuhan Caesalpinia sappan lin.
Bandung: FMIPA UNPAD.
Sidik, Moelyono MW, Mutadi A.1995.
Temulawak (Curcuma xanthorrhiza
Roxb.). Jakarta: Phyto Medika.
Skoog DA, Holler PJ, Nieman TA. 1998.
Principles of Instrumental Analysis. Ed
ke-5. Philadelphia: Harcaurt Brace. Sudjarwo SA. 2002. Efek proteksi dari
kurkumin terhadap sel endothelium pada hiperkholesterolemia. J Pen Med Eks 3:41-48.
Supriadi D. 2008. Optimalisasi Ekstraksi Kurkuminoid Temulawak (Curcuma
xanthorrhiza Roxb.) [Skripsi]. Bogor:
Departemen Kimia, IPB.
Trilaksani W. 2003. Antioksidan: Jenis, Sumber, Mekanisme Kerja dan Peran Terhadap Kesehatan. [terhubung berkala] http://www.poultryindonesia.com [20 Juli 2008].
Widiastuty W. 2006. Teknik Spektroskopi Inframerah Transformasi Fourier untuk Penentuan Profil Kadar Xantorizol dan Aktivitas Antioksidan Temulawak [Skripsi]. Bogor: Departemen Kimia FMIPA, IPB.
Willard HH, LL Merrit Jr, John AD, FA Settle Jr. 1988. Instrumental Methods of Analysis. Ed ke-7. California: A Division of Wodsworth.
Winarno FG. 1992. Kimia Pangan dan Gizi. Jakarta: Gramedia Pustaka Utama Windono T, Budiono R, Sumijani R, Kusuma
D. 2003. Radical Scavenging Capacity Against 1,1-Diphenyl-2-Picryl Hydrazyl (DPPH) of Some Indonesian Medicinal Plants. Didalam: Biodiversity on Tradisional Biomedicine for Human Health and Welfare. Proceedings Symposium of Biomedicines; Bogor, 18-19 Sept 2003. Bogor: Biopharmaca Research Center IPB. hlm 63-70.
[WHO] World Health Organization. 1999. Monograph on selected medicinal plant. Vol 1. Jenewa: WHO.
Wong SP, LP Leong, JH William Koh. 2006. Antioxidant activities of aqueous extracts of selected plants. Food Chem 99:775-783.
13
Yulanda H. 2007. Ekstraksi, Fraksinasi, danPencirian Pati Rimpang Temulawak [Skipsi]. Bogor: Departemen Kimia FMIPA, IPB.

![Gambar 12 Hubungan [tokoferol] (ppm) dan absorbans metode CUPRAC.](https://thumb-ap.123doks.com/thumbv2/123dok/4260059.2882670/20.918.191.774.874.976/gambar-hubungan-tokoferol-ppm-dan-absorbans-metode-cuprac.webp)

![Tabel 9 Kadar xantorhizol serbuk rimpang temulawak Semarang Ekstrak Luas Area [xantorhizol]](https://thumb-ap.123doks.com/thumbv2/123dok/4260059.2882670/29.918.197.816.645.763/tabel-kadar-xantorhizol-rimpang-temulawak-semarang-ekstrak-xantorhizol.webp)