ii
KAJIAN NISBAH LIGNIN-NaHSO
3DAN pH PADA REAKSI
SULFONASI LIGNIN KRAFT UNTUK MENGHASILKAN
NATRIUM LIGNOSULFONAT
JONIZAL DAVID
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2008
i
ABSTRAK
JONIZAL DAVID. Kajian Nisbah Lignin-NaHSO3 dan pH pada Reaksi Sulfonasi Lignin Kraft untuk Menghasilkan Natrium Lignosulfonat. Dibimbing oleh GUSTINI
SYAHBIRIN dan DUDI TOHIR.
Lignin diisolasi dari lindi hitam proses kraft dengan H2SO4 20% lalu disulfonasi menjadi natrium lignosulfonat (NaLS). Pada penelitian ini, lignin disulfonasi oleh NaHSO3 dengan nisbah lignin-NaHSO3 1:0,4; 1:0,5; dan 1:0,6 pada pH awal 5, 6, dan 7. Parameter yang diamati ialah kadar, pH akhir, dan bobot NaLS. Hasil penelitian menunjukkan bahwa nisbah lignin-NaHSO3, pH awal, dan interaksi antara keduanya hanya berpengaruh nyata terhadap kadar NaLS. Kadar NaLS tertinggi didapatkan pada nisbah lignin-NaHSO3 1:0,5 dengan pH awal 7, yaitu 54,96%. Kadar NaLS terendah didapatkan pada nisbah lignin-NaHSO3 1:0,5 dengan pH awal 5, yaitu 28,40%. Kondisi terbaik sintesis NaLS pada perlakuan ini didapatkan pada nisbah lignin-NaHSO3 1:0,5 dengan pH awal 7. Pola spektrum FTIR NaLS menunjukkan adanya vibrasi ulur C-S pada bilangan gelombang 622 cm-1. Hal ini menunjukkan bahwa telah terjadi sulfonasi terhadap lignin.
ABSTRACT
JONIZAL DAVID. Study the Influence of Ratio lignin-NaHSO3 and pH to Kraft Lignin Sulfonation Reaction to produce Sodium Lignosulphonic. Supervised by GUSTINI SYAHBIRIN and DUDI TOHIR.
Lignin was isolated from black liquor kraft processing with H2SO4 20% and was sulfonated onto sodium lignosulphonic (NaLS). In this research, lignin was sulfonated by NaHSO3 with ratio of lignin-NaHSO3 1:0.4; 1:0.5; and 1:0.6, and initial pH 5, 6, and 7. Parameters observed were yield of NaLS level, final pH, and NaLS weight. This result showed that the ratio of lignin-NaHSO3, initial pH, and the interactions only gave a significant effect on NaLS yield. The highest NaLS level occured in the ratio of lignin-NaHSO3 1:0.5 with initial pH 7, was 54.96%. The lowest NaLS level occured in the ratio of lignin-NaHSO3 1:0.5 with initial pH 5, was 28.40%. The best of condition to sinthesis of NaLS this treatment occured in the ratio of lignin-NaHSO3 1:0.5 with initial pH 7. Fourier transformed infrared spectrum of NaLS showed the existence of C-S stretching at wavenumber 622 cm-1. In the case showed the sulfonation of lignin has occured.
iii
NIM : G44202056Menyetujui:
Pembimbing I Pembimbing II
Dra. Gustini Syahbirin, MS NIP 131842414 Drs. Dudi Tohir, MS NIP 131851277 Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. Drh. Hasim, DEA NIP 131578806
iv
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT atas ridho, rahmat, dan karunia-Nya sehingga karya ilmiah dapat diselesaikan. Judul yang dipilih dalam penelitian yang dilaksanakan dari bulan Desember 2006 sampai dengan bulan November 2007 ini ialah Kajian Nisbah Lignin-NaHSO3 dan pH pada Reaksi Sulfonasi Lignin Kraft untuk Menghasilkan Natrium Lignosulfonat.
Penulis ucapkan terima kasih kepada Dra. Gustini Syahbirin, MS dan Drs. Dudi Tohir, MS selaku pembimbing atas bimbingan, ilmu, dan dorongan semangat yang diberikan selama penelitian dan penyusunan karya ilmiah ini. Terima kasih juga disampaikan kepada kedua orang tua, Yogi, Ibu Er, serta seluruh keluarga yang memberikan doa, kasih sayang, dorongan semangat, dan bantuan materi kepada penulis.
Penulis juga tak lupa ucapkan kepada Tesar, Dewi, Ichsan, dan Dicky selaku teman penelitian, serta kepada Bapak Sabur, Ibu Yeni, dan Ibu Aah atas segala fasilitas dan kemudahan yang telah diberikan. Penulis juga ucapkan terima kasih kepada teman-teman penghuni laboratorium Kimia Organik, Obie, Lukmana, Izul, Ijal, dan teman-teman Kimia 39 atas persahabatan dan dukungannya, semoga Allah senantiasa membalas kebaikan semuanya. Amin Ya Robbal ‘alamin.
Semoga karya ilmiah ini bermanfaat.
Bogor, Desember 2007
v
Trimurti. Penulis merupakan putra pertama dari dua bersaudara.Tahun 2002 penulis lulus dari SMU Negeri 29 Jakarta dan pada tahun yang sama lulus seleksi masuk IPB melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB). Penulis memilih Program Studi Kimia, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam.
Selama mengikuti perkuliahan, penulis menjadi asisten praktikum mata kuliah Kimia Dasar I pada tahun ajaran 2004/2005, asisten praktikum mata kuliah Kimia TPB dan asisten dosen mata kuliah Kimia Organik TPB pada tahun ajaran 2004-2005, serta asisten praktikum mata kuliah Kimia Fisik I pada tahun ajaran 2005-2006. Pada Tahun 2006 penulis melaksanakan praktik lapangan di Balai Besar Industri Agro (BBIA) Bogor.
vi
DAFTAR ISI
Halaman
DAFTAR TABEL... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN... viii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Lindi Hitam... 1
Pengertian dan Struktur Lignin ... 2
Kegunaan Lignin ... 3
Natrium Lignosulfonat ... 3
Kegunaan Natrium Lignosulfonat ... 3
BAHAN DAN METODE Bahan dan Alat ... 4
Metode Penelitian ... 4
HASIL DAN PEMBAHASAN Ciri Bahan Baku ... 6
Lignin Isolat ... 6
Natrium Lignosulfonat Sintetik... 7
Kadar NaLS... 8
Derajat Keasaman NaLS ... 9
Bobot NaLS... 9
Spektrum FTIR Lignin dan NaLS ... 9
SIMPULAN DAN SARAN Simpulan... 12
Saran... 12
DAFTAR PUSTAKA ... 12
vii
1 Komposisi lindi hitam kraft pada kayu lunak ... 2
2 Ciri bahan baku... 6
3 Karakteristik lignin isolat ... 7
4 Karakteristik NaLS sintetik ... 7
DAFTAR GAMBAR
Halaman 1 Struktur p-koumaril alkohol, koniferil alkohol, dan sinapil alkohol ... 22 Bagian struktur lignin yang banyak pada kayu lunak dengan 16 unit fenilpropana (Adler 1977)... 2
3 Lignin tersulfonasi pada posisi C-α dan C-γ ... 3
4 Reaksi pengasaman gugus fenolat pada lignin ... 7
5 Reaksi sulfonasi terhadap 1,2-diguaiasilpropana-1,3-diol ... 8
6 Hubungan kadar NaLS terhadap pH awal pada berbagai nisbah lignin- NaHSO3... 8
7 Struktur resonansi lignin pH awal 7 pada penstabilan karbokation C- α... 8
8 Struktur resonansi lignin pH awal 5 dan 6 pada penstabilan karbokation C- α ... 8
9 Hubungan pH NaLS terhadap pH awal pada berbagai nisbah lignin- NaHSO3... 9
10 Hubungan bobot NaLS terhadap pH awal pada berbagai nisbah lignin- NaHSO3... 9
11 Spektrum FTIR lignin isolat ... 10
viii
DAFTAR LAMPIRAN
Halaman
1 Diagram alir isolasi lignin... 14
2 Diagram alir sintesis natrium lignosulfonat ... 15
3 Data kadar air dan padatan total lindi hitam ... 16
4 Data bobot jenis lindi hitam... 16
5 Data rendemen lignin berdasarkan volume lindi hitam ... 16
6 Data rendemen lignin berdasarkan padatan total lindi hitam... 16
7 Data kadar lignin... 17
8 Pengaruh nisbah lignin-NaHSO3 dan pH awal terhadap kadar NaLS ... 17
9 Uji lanjut Duncan pada kadar NaLS ... 19
10 Pengaruh nisbah lignin-NaHSO3 dan pH awal terhadap pH NaLS yang dihasilkan ... 21
11 Pengaruh nisbah lignin-NaHSO3 dan pH awal terhadap bobot NaLS yang dihasilkan ... 23
PENDAHULUAN
Permintaan kertas dari tahun ke tahun semakin meningkat. Permintaan dunia untuk berbagai jenis kertas pada Tahun 1990 sebesar 239.428.000 juta ton dan meningkat menjadi 369.085.000 juta ton pada Tahun 2005 (Pulp and Paper Industry 2006). Meningkatnya permintaan produksi kertas juga diikuti oleh meningkatnya masalah pencemaran lingkungan.
Hasil samping proses pembuatan pulp disebut dengan lindi hitam. Larutan ini merupakan salah satu pencemar bagi lingkungan. Hal ini disebabkan oleh adanya beberapa senyawa kimia seperti metil merkaptan dan hidrogen sulfida yang bersifat racun. Lindi hitam jika tersebar ke seluruh ekosistem dapat menyebabkan penyimpangan reproduktif pada zooplankton dan invertebrata yang merupakan sumber makanan ikan. Hal ini selanjutnya dapat menyebabkan kerusakan genetik dan sistem kekebalan tubuh pada ikan (Rini 2002). Di sisi lain, berbagai jenis produk yang bermanfaat dapat dihasilkan dari isolasi yang terdapat dalam sisa pemasak tersebut. Komponen kimia terbesar yang terkandung dalam lindi hitam proses kraft adalah lignin dan sisanya terdiri atas produk degradasi karbohidrat, zat ekstraktif, dan komponen lain.
Lignin merupakan komponen terbesar dalam lindi hitam proses kraft sekitar 46% dari padatan totalnya (Sjöström 1995). Lignin
kraft atau bentuk-bentuk modifikasinya dapat
digunakan sebagai zat pendispersi dan aditif dalam karet, resin, dan plastik. Penggunaan lignin kraft sebagai bahan mentah masih terbatas. Hal tersebut dikarenakan untuk memurnikan lignin kraft diperlukan biaya yang relatif mahal dan pada saat ini hanya diproduksi dalam jumlah sedikit.
Salah satu pemanfaatan lignin ialah dapat dimodifikasi menjadi natrium lignosulfonat. Natrium lignosulfonat dapat disintesis dari lignin dengan reaksi sulfonasi. Reaksi sulfonasi merupakan reaksi yang melibatkan pemasukan gugus sulfonat ke dalam lignin. Dilling et al. (1990) telah melakukan sulfonasi lignin dengan kondisi pH awal 6-6,3 dan 2,5-3,5 mol bisulfit per 1 gram lignin pada suhu 175 οC menghasilkan natrium
lignosulfonat pH 7. Syahmani (2000) telah melakukan sulfonasi terhadap lignin dari tandan kosong sawit dengan bisulfit pada pH 5 dengan suhu 100 οC selama 4 jam
menghasilkan 2,2490 g natrium lignosulfonat dengan kemurnian 83,95%. Dzikrulloh (2007)
juga telah melakukan sulfonasi terhadap lignin hasil isolasi lindi hitam proses soda menggunakan nisbah lignin-NaHSO3 1:0,4;
1:0,5; dan 1:0,6 dengan pH awal 5, 6, dan 7 pada suhu 100 οC selama 4 jam menghasilkan
natrium lignosulfonat dengan kadar 68,62-83,57% dan pH 6,42-7,11.
Pembuatan natrium lignosulfonat dari lignin kraft ini dapat digunakan sebagai zat pendispersi dan pengikat pada lumpur pengeboran minyak dan juga untuk pewarna tekstil. Natrium lignosufonat juga dapat digunakan sebagai zat aditif yang bersifat pendispersi pada beton. Pemanfaatan lindi hitam juga diharapkan dapat mengurangi lindi hitam yang dibuang begitu saja.
Penelitian ini bertujuan mengisolasi lignin dari lindi hitam proses kraft. Lignin hasil isolasi lalu disulfonasi dengan NaHSO3
untuk menentukan pengaruh nisbah reaktan lignin-NaHSO3 dan pH awal pada kadar, pH
akhir, dan bobot natrium lignosulfonat yang dihasilkan serta mendapatkan kondisi terbaik dalam sintesis natrium lignosulfonat.
TINJAUAN PUSTAKA
Lindi Hitam
Lindi hitam kraft merupakan larutan sisa
pemasak serpih kayu dari pembuatan pulp dengan proses kimia sulfat. Sifat fisik dan kimia dari lindi hitam tersebut berupa cairan yang berwarna hitam, berbau, persen padatan 80%, pH 10-13, bobot jenis 1,20-1,60 g/ml yang dihasilkan dari proses pulping (Weyerhaesuer Company 2004).
Menurut Sjöström (1995), lindi hitam
kraft merupakan campuran kompleks yang
dihasilkan dari pembuatan pulp menggunakan larutan NaOH dan Na2S mengandung
sejumlah besar komponen dengan struktur dan susunan berbeda. Pada pembuatan pulp proses
kraft, lindi hitam mengandung bahan organik.
Namun pada dasarnya lindi hitam ini terdiri atas lignin dan produk-produk degradasi karbohidrat di samping bagian-bagian kecil ekstraktif dan produk-produk lainnya (Tabel 1).
2
Tabel 1 Komposisi lindi hitam kraft pada kayu lunak Komponen Komposisi (% padatan kering) Lignin 46 Asam-asam hidroksi 30 Asam format 8 Asam asetat 5 Ekstraktif 7 Senyawa-senyawa lain 4 Sumber: Sjöström 1995
Pengertian dan Struktur Lignin
Lignin adalah makromolekul atau polimer dengan unit monomer fenilpropana (C-9) yang terikat satu sama lain melalui ikatan eter (C-O-C) dan ikatan karbon ke karbon (C-C) (Sjöström 1993). Menurut Achmadi S (1990), 2/3 bagian unit fenilpropana dalam lignin dihubungkan oleh ikatan eter (C-O-C) sedangkan sisanya sebanyak 1/3 dihubungkan oleh ikatan karbon ke karbon (C-C). Baik lignin alami maupun lignin dari lindi hitam bersifat amorf dan merupakan senyawa aromatik dengan struktur kimia yang kompleks.
Lignin menurut strukturnya, dapat dibagi menjadi 2 kelompok:
1 Lignin guaiasil, yaitu lignin yang terdapat pada hampir semua kayu lunak dan sebagian besar merupakan produk polimerisasi dari koniferil alkohol.
2 Lignin guaiasil-siringil, yaitu lignin khas kayu keras yang merupakan produk polimerisasi dari koniferil alkohol dan sinapil alkohol dengan nisbah bervariasi dari 1:2 sampai 1:3.
Fengel dan Wegener (1995) menyatakan prekursor pembentuk lignin terdiri atas
p-koumaril alkohol, koniferil alkohol, dan
sinapil alkohol. Ketiga struktur tersebut dapat ditunjukkan pada Gambar 1.
CH CH CH2OH OH CH CH CH2OH OH OCH3 CH CH CH2OH OH OCH3 H3CO
Gambar 1 Struktur p-koumaril alkohol, koniferil alkohol, dan sinapil alkohol.
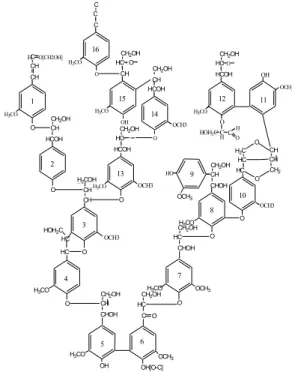
Rumus struktur lignin kayu lunak telah diusulkan oleh Adler (1977) yang ditunjukkan pada Gambar 2. Rumus ini terdiri atas 16 unit fenilpropana dan rumus tersebut hanya menunjukkan sebagian dari makromolekul lignin. Rumus struktur yang dimodelkan oleh Adler ukurannya terbatas sehingga tidak dapat memberikan gambaran kuantitatif secara sempurna. Keterbatasan lainnya, dalam rumus Adler tidak ada ikatan-ikatan antara lignin dan karbohidrat atau konstituen-konstituen lainnya. H3CO OCH3 CH CHOH C OCH3 CH2OH HC O O OH[O-C] H3CO HC O OH O CH2OH HC HOH2C H2COH H3CO HC CHOH CH2OH H3CO O O CH CH O O H3CO OCH3 H3CO CH HCOH CH2OH O CH CH C H3CO OCH3 H O[CH2OH] OCH3 OCH3 CH CHOH CH2OH OCH3 HO HC CH HC CH2 O H2C O CH HC HCOH CH2OH O C HCO H HOH2C O OCH3 OH H3CO HC - O CH CH2OH H3CO C C C HC HCOH CH2OH CH HCOH CH2OH O OH O 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16
Gambar 2 Bagian struktur lignin yang banyak pada kayu lunak dengan 16 unit fenilpropana (Adler 1977).
Lignin sebagai bahan alami, terdapat hampir pada semua jenis kayu dan merupakan komponen kimia utama penyusun kayu selain selulosa. Di dalam sel kayu, kandungan lignin tertinggi terdapat pada dinding sel sekunder yakni sebesar 70% dari semua lignin di dalam kayu walaupun konsentrasi lignin tertinggi terdapat pada ruang antarsel atau lamela tengah. Kayu keras umumnya mengandung lignin 20-25%, sedangkan kayu keras tropika kandungan ligninnya bisa mencapai lebih dari 30%. Kayu lunak umumnya mengandung lignin 26-32% sedangkan pada kayu tekan bisa mencapai 35-40% (Sjöström 1995). Penelitian yang telah dilakukan Lubis (2007)
untuk lindi hitam proses kraft dihasilkan lignin dengan rendemen 25,26% padatan total. Lignin mempunyai bentuk amorf dan berwarna cokelat muda. Lignin tidak larut dalam air, asam, dan hidrokarbon. Karena lignin tak larut dalam asam, penggunakan asam sebagai pereaksi sering digunakan untuk uji kuantitatif lignin. Lignin tidak dapat mencair tetapi akan melunak kemudian menjadi hangus bila dipanaskan. Lignin yang diperdagangkan larut dalam alkali encer dan beberapa senyawa organik (Fengel & Wegener 1995).
Kegunaan Lignin
Lignin berfungsi sebagai pengikat sel-sel kayu satu sama lain, ibarat adukan semen pada susunan batu bata sehingga kayu menjadi keras dan membuat pohon dapat berdiri tegak. Hal inilah yang menyebabkan kayu mampu meredam kekuatan mekanik yang dikenakan terhadapnya. Atas dasar inilah Rudatin (1989) mengembangkan teori, bahwa lignin mampu berfungsi sebagai perekat dalam pembuatan papan partikel dan kayu lapis. Lignin yang terdapat dari lindi hitam, komposisi komponen kimianya bervariasi bergantung pada spesies kayu dan kondisi pemasakannya.
Lignin kraft digunakan sama seperti lignosulfonat tetapi pemurniannya relatif mahal dan pada saat ini hanya diproduksi dalam jumlah sedikit. Lignin kraft atau bentuk-bentuk modifikasinya dapat digunakan sebagai bahan pendispersi dan aditif dalam karet, resin, dan plastik. Kondensasi lignin
kraft dengan formaldehida dan ikatan silang
dengan fenol dapat menghasilkan polimer-polimer termosetting yang berguna sebagai perekat untuk produk-produk berbeda seperti kertas berlapis atau kayu lapis.
Natrium Lignosulfonat
Lignosulfonat merupakan turunan lignin yang mengandung gugus sulfonat pada rantai samping propana (Gambar 3) (Sjöström 1995). Lignosulfonat dapat diisolasi dari lindi hitam proses sulfit dengan ultrafiltrasi yaitu lignin yang berbobot molekul tinggi terkonsentrasi sedangkan senyawa berbobot molekul rendah seperti asam hidroksi dan ekstraktif dilewatkan melalui membran (Jain & Kulkarni 1991). CH2 HC SO3Na NaO3S HC OH R
Gambar 3 Lignin tersulfonasi pada posisi C-α dan C-γ.
Sintesis lignosulfonat dapat dilakukan dengan sulfonasi lignin. Tujuan sulfonasi adalah mengubah hidrofilisitas lignin yang kurang polar (tidak larut dalam air) dengan memasukkan gugus sulfonat yang lebih polar daripada gugus hidroksil lignin sehingga hidrofilisitasnya meningkat (Syahmani 2000). Sulfonasi konvensional umumnya dilakukan dengan sulfometilasi, yaitu dengan mereaksikan lignin dengan formaldehida dan natrium sulfat. Pembuatan lignosulfonat tanpa formaldehida pada dasarnya juga cocok dilakukan sulfonasi kayu dengan bisulfit pada pH 5 dengan suhu 135 οC (Fengel & Wegener
1995). Keberhasilan sulfonasi lignin bergantung pada kondisi larutan lignin, temperatur, dan pH (Dilling et al. 1990).
Kegunaan Natrium Lignosulfonat
Lignosulfonat berguna untuk sejumlah pemakaian terutama karena sifat adhesi dan dispersinya. Sebagai contoh, bila ditambahkan pada beton, lignosulfonat diserap pada permukaan mineral dan hanya membutuhkan sedikit air untuk memberikan kemudahan mengalir dan membuat beton menjadi kuat. Hal ini menyebabkan beton kurang dapat ditembus oleh air sehingga lebih kuat. Demikian juga bila lignosulfonat ditambahkan pada lumpur pengeboran minyak, maka kekentalan lumpur menjadi menurun. Potensi penggunaan lignosulfonat ini sangat besar untuk sumur-sumur minyak di Indonesia (Gargulak & Lebo 2000).
Kategori lain bahan-bahan kimia yang berasal dari lignin diperoleh bila lignosulfonat didegradasi menjadi poduk-poduk bobot molekul rendah. Produk perdagangan yang paling penting adalah vanilin, yang diperoleh dari oksidasi álkali lignosulfonat kayu lunak. Namun lignin pada kayu keras tidak berguna sebagai bahan mentah pembuatan vanilin.
4
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah lindi hitam proses kraft dari industri kertas PT Toba Pulp Lestari, Sumatera Utara, H2SO4 20% (b/v),
H2SO4 72% (b/v), H2SO4 0,01 N, HCl 0,2 N,
NaOH 1 N, NaOH 0,125 N, akuades, kertas saring, dan kertas pH.
Alat-alat yang digunakan adalah pH-meter merk Inolab WTW, sentrifus merk International Equipment Company, Spektrofotometer UV-VIS dan FTIR, dan neraca analitik.
Metode Penelitian
Penelitian ini terdiri atas empat tahap. Tahap pertama adalah pencirian bahan baku lindi hitam yang meliputi warna, bau, pH, kadar air, padatan total, dan bobot jenis. Tahap kedua adalah isolasi lignin dari lindi hitam. Tahap ketiga sintesis natrium lignosulfonat dengan variasi nisbah lignin-NaHSO3 dan pH awal. Nisbah lignin-NaHSO3
yang digunakan 1:0,4; 1:0,5; dan 1:0,6 berdasarkan bobot sedangkan pH awal dilakukan pada pH 5, 6, dan 7. Tahap keempat adalah pencirian natrium lignosulfonat dengan spektrofotometer FTIR, pH, dan kadar NaLS dengan spektrofotometer UV-VIS.
pH
Lindi hitam diukur pH-nya dengan pH-meter.
Kadar Air dan Padatan Total (SNI
06-2235-1991)
Sebanyak 5 gram lindi hitam (W2)
dimasukkan dalam cawan yang telah diketahui bobotnya (W1). Cawan yang berisi sampel
dimasukkan dalam oven pada suhu 105 °C selama 3 jam. Setelah itu, cawan didinginkan dalam eksikator lalu ditimbang. Pengeringan dilakukan sampai cawan yang berisi sampel bobotnya konstan (W3). Kadar air dihitung
dengan persamaan sebagai berikut: Kadar air (%) = (1 - 2 1 3 W W W − ) × 100 Padatan total (%) = 100 – kadar air (%)
Bobot Jenis (SNI 06-2235-1991)
Air dimasukkan dalam piknometer yang telah diketahui bobotnya (m1). Kemudian
piknometer yang telah berisi air ditimbang (m2). Lindi hitam dimasukkan dalam
piknometer kosong yang sama lalu ditimbang (m3). Suhu air diukur dan ditentukan densitas
air pada suhu tersebut (da). Massa jenis
dengan persamaan: Bobot jenis =
(
(
)
)
1 2 1 3 m -m m -m × daIsolasi Lignin dari Lindi Hitam (Kim et al.
1987)
Sebanyak 300 ml larutan lindi hitam yang telah disaring dimasukkan dalam gelas piala. Kemudian ditambahkan dengan larutan H2SO4
20% (b/v) perlahan-lahan hingga pH-nya mencapai 2. Selanjutnya endapan yang terbentuk dipisahkan dari cairan induknya dengan alat sentrifugal.
Endapan dilarutkan kembali dengan menambahkan larutan NaOH 1 N lalu disaring dan diambil filtratnya. Filtrat tersebut diendapkan kembali dengan menambahkan larutan H2SO4 20% (b/v) perlahan-lahan
hingga pH-nya mencapai 2. Selanjutnya endapan yang terbentuk dipisahkan kembali dari cairan induknya dengan alat sentrifugal. Endapan yang dihasilkan dicuci dengan larutan H2SO4 0,01 N sebanyak 5 kali dan
dengan air suling sebanyak 2 kali. Endapan yang telah dicuci, dikeringkan dalam oven pada suhu 50-60 °C (Lampiran 1).
Rendemen Lignin
Rendemen lignin dihitung berdasarkan hasil bagi bobot lignin isolat dengan jumlah padatan total yang digunakan. Rendemen dinyatakan dalam persen bobot.
Rendemen (%) = total padatan bobot isolat lignin bobot × 100 pH Lignin
Sebanyak 1 g lignin isolat dilarutkan
dengan air suling hingga 10 ml. Kemudian larutan tersebut diukur pH-nya dengan pH-meter.
Penentuan Kadar Lignin (Tappi T 222
05-74)
Sebanyak 1 gram lignin isolat (A) dimasukkan dalam gelas piala 100 ml lalu ditambahkan dengan 15 ml H2SO4 72% (b/v)
perlahan-lahan di dalam bak perendam sambil diaduk selama 2-3 jam. Setelah itu, gelas piala ditutup dengan gelas arloji dan dibiarkan (dalam bak perendam) pada suhu 20 °C selama 2 jam dengan sesekali diaduk.
Sebanyak 300-400 ml air suling dimasukkan dalam erlenmeyer 1000 ml. Sampel dari gelas piala juga dimasukkan ke dalam erlenmeyer tersebut kemudian diencerkan sampai volumenya 575 ml dengan air suling sehingga konsentrasi asam sulfat mencapai 3% (b/v). Larutan dipanaskan sampai mendidih selama 4 jam dengan api kecil. Volume dijaga konstan dengan menggunakan pendingin tegak. Setelah itu, endapan lignin yang terbentuk dibiarkan mengendap sempurna. Larutan didekantasi kemudian endapan dipindahkan dalam kertas saring yang telah diketahui bobotnya (B). Endapan lignin dicuci dengan air panas sampai bebas asam diuji dengan kertas lakmus. Selanjutnya endapan tersebut dikeringkan dalam oven pada suhu 105 °C lalu ditimbang sampai bobotnya konstan (C). Kadar lignin dalam lindi hitam dihitung dengan persamaan berikut:
Kadar lignin (%) = A B -C × 100
Pencirian Lignin dengan Metode Spektrofotometri FTIR
Metode analisis lignin secara spektrofotometri FTIR mengacu pada Nada
et al. (1998). Sebanyak 1 mg lignin dicampur
dengan 300 mg KBr, kemudian dibuat pellet dan selanjutnya dianalisis dengan spektrofotometer FTIR.
Sintesis Natrium Lignosulfonat
Sebanyak 5 g lignin dicampurkan dengan NaHSO3 dengan nisbah lignin-NaHSO3
(1:0,4; 1:0,5; dan 1:0,6) (Dzikrulloh 2007) lalu disuspensikan dalam 150 ml air. Kemudian pH suspensi dinaikkan menjadi 5, 6, dan 7 dengan menambahkan NaOH 1 N (Dilling et al. 1990). Campuran selanjutnya
direfluks pada suhu 100 °C sambil diaduk selama 4 jam (Syahmani 2000). Hasil refluks didestilasi untuk menghilangkan air. Setelah itu, destilat disaring lalu diambil filtratnya
(mengandung natrium lignosulfonat dan bisulfit sisa reaksi). Kemudian filtrat ditambahkan dengan metanol dan dikocok kuat untuk mengendapkan sisa bisulfit. Endapan yang terbentuk disaring dan diambil filtratnya. Selanjutnya filtrat dikeringkan dalam oven pada suhu 60 °C. Serbuk yang dihasilkan merupakan natrium lignosulfonat (Lampiran 2).
Penentuan Kadar NaLS (Wesco 1995)
Sebanyak 0,1 g NaLS sintetik kering dilarutkan dalam 100 ml air deionisasi. Kemudian dari larutan tersebut dipipet 5 ml dan dimasukkan ke dalam gelas piala 250 ml. Setelah itu, diencerkan sampai volume larutan menjadi 200 ml. pH larutan diatur antara 4-5 dengan penambahan NaOH 0,1250 N atau HCl 0,2 N. Selanjutnya larutan tersebut dipindahkan ke dalam labu takar 250 ml, dan diencerkan sampai volume 250 ml dengan air deionisasi. Absorbans larutan diukur pada λ= 232,5 nm dalam kuvet 1 cm. Kadar NaLS ditentukan dengan persamaan sebagai berikut: Kadar NaLS (%) = 10 sampel g 35 n vol.laruta FP A × × × × Keterangan: 35 = faktor NaLS
pH NaLS
Sebanyak 1 g NaLS sintetik dilarutkan
dengan air suling hingga 10 ml. Kemudian larutan tersebut diukur pH-nya dengan pH-meter.
Pencirian NaLS dengan Metode Spektrofotometri FTIR
Sebanyak 1 mg NaLS dicampur dengan 300 mg KBr, kemudian dibuat pellet dan selanjutnya dianalisis dengan spektrofotometer FTIR.
Rancangan Percobaan (Mattjik &
Sumertajaya 2002)
Pengaruh nisbah lignin-NaHSO3 dan pH
awal terhadap kadar, pH, bobot NaLS sintetis dianalisis secara statistik dengan metode rancangan acak lengkap (RAL) lalu dilanjutkan dengan uji Duncan. Model rancangan tersebut adalah
6
Keterangan:
Yijk = kadar NaLS atau pH akhir atau bobot NaLS pada nisbah lignin-NaHSO3 ke-i, pH awal ke-j, serta
ulangan ke-k, dengan i = 1, 2, 3, j = 1, 2, 3, dan k = 1, 2.
µ = rataan umum
τi = pengaruh nisbah lignin-NaHSO3
ke-i
βj = pengaruh pH awal ke-j
τβij = pengaruh interaksi antara nisbah
lignin-NaHSO3 ke-i dan pH awal
ke-j
εijk = pengaruh acak dari perlakuan
nisbah lignin-NaHSO3 ke-i, pH awal
ke-j, serta ulangan ke-k
Hipotesis yang diuji
1 Pengaruh nisbah lignin-NaHSO3
Ho : τ1 = τ2 = τ3 = 0 (nisbah
lignin-NaHSO3 memberikan pengaruh yang
sama terhadap kadar NaLS atau pH akhir atau bobot NaLS)
H1 : minimal ada satu i dengan τi ≠ 0,
i = 1, 2, 3
2 Pengaruh pH awal
Ho : β1 = β2 = β3 = 0 (pH awal
memberikan pengaruh yang sama terhadap kadar NaLS atau pH akhir atau bobot NaLS)
H1 : minimal ada satu j dengan βj ≠ 0,
j = 1, 2, 3
3 Pengaruh interaksi antara nisbah lignin-NaHSO3 dan pH awal
Ho : (τβ)ij = 0 untuk semua ij
H1 : minimal ada satu (τβ)ij ≠ 0
HASIL DAN PEMBAHASAN
Ciri Bahan Baku
Fungsi pencirian bahan baku ialah mengetahui karakteristik bahan secara fisik dan kimia pada lindi hitam. Hasil pencirian disajikan pada Tabel 2.
Tabel 2 Ciri bahan baku
Pencirian Pengamatan
Warna hitam pekat
Bau telur busuk
pH 13,74 Kadar air (%) 81,09
Bobot jenis (g/ml) 1,11 Padatan total (%) 18,91
Warna dan bau dapat menggambarkan komposisi limbah cair. Limbah cair segar
biasanya berwarna cokelat keabu-abuan dan apabila kondisinya dalam keadaan anaerob warna pun akan berubah menjadi abu-abu gelap sampai hitam. Warna yang terlihat pada lindi hitam yaitu hitam pekat. Secara kualitatif warna tersebut disebabkan oleh adanya formasi logam-logam sulfida (Goldman & Horne 1983). Adanya logam-logam sulfida ini dikarenakan lindi hitam yang dihasilkan dari pembuatan pulp proses kraft dilakukan dengan
menggunakan larutan yang terdiri atas NaOH dan Na2S (Sjöström 1995). Bau telur busuk
pada lindi hitam ini juga disebabkan oleh senyawaan sulfida.
Derajat keasaman (pH) pada lindi hitam sebesar 13,74. Nilai pH ini cukup tinggi dan bersifat basa kuat. Hal ini disebabkan pada pembuatan pulp proses kraft digunakan
larutan yang terdiri atas NaOH dan Na2S.
Pada keadaan basa, gugus fenol pada lignin terionisasi menjadi gugus fenolat sehingga lignin dapat larut dalam air.
Kadar air yang diperolah pada lindi hitam sebesar 81,09% (Lampiran 3). Kadar air yang diperoleh Lubis (2007) sebesar 94,12%. Hal ini menunjukkan bahwa kadar air pada lindi hitam proses kraft relatif tinggi sehingga dapat
melarutkan senyawaan yang dapat larut dalam air.
Bobot jenis yang diperoleh pada lindi hitam sebesar 1,11 g/ml (Lampiran 4). Nilai ini sedikit melebihi dari bobot jenis air. Hal ini dapat dikatakan bahwa selain air, masih terdapatnya komponen kimia yang terkandung dalam lindi hitam, salah satunya adalah lignin. Padatan total merupakan residu yang diperoleh dari hasil penguapan lindi hitam pada suhu tertentu. Padatan total yang diperoleh pada lindi hitam sebesar 18,91% (Lampiran 3). Padatan total tersebut secara kualitatif, terdapat komponen kimia yang terkandung dalam lindi hitam. Padatan total dihitung untuk mengetahui rendemen lignin hasil isolasi dari lindi hitam.
Lignin Isolat
Lignin dapat diisolasi dari lindi hitam menggunakan H2SO4 20% dengan
mengendapkannya hingga pH 2 (Kim et al.
1987). Pada pH 2, gugus fenolat pada lignin menerima ion hidrogen secara maksimum menjadi gugus fenol (Gambar 4). Hal tersebut menyebabkan kelarutan lignin dalam air berkurang sehingga lignin dapat dipisahkan dari senyawaan yang larut dalam air. Tujuan melarutkan kembali endapan lignin dengan NaOH 1 N ialah memisahkan endapan putih
yang merupakan garam dari senyawaan organik yang tak larut bersama lignin ketika pH dinaikkan (Kim et al. 1987).
HC HC CH2OH OH R OCH3 O -H+ HC HC CH2OH OH R OCH3 OH
Gambar 4 Reaksi pengasaman gugus fenolat pada lignin.
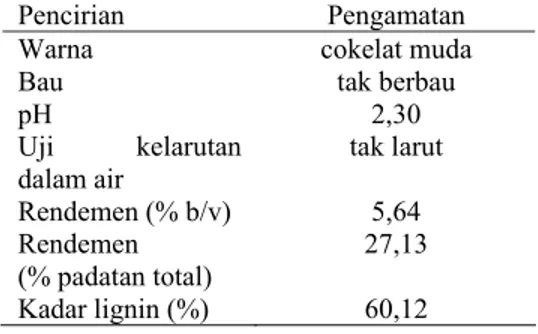
Lignin isolat merupakan lignin yang diperoleh dari isolasi lindi hitam. Karakteristik lignin isolat disajikan pada Tabel 3.
Tabel 3 Karakteristik lignin isolat
Pencirian Pengamatan
Warna cokelat muda
Bau tak berbau
pH 2,30 Uji kelarutan
dalam air tak larut Rendemen (% b/v) 5,64 Rendemen
(% padatan total) 27,13 Kadar lignin (%) 60,12
Lignin isolat yang diperoleh berwarna cokelat muda, tidak berbau, dan tak larut dalam air. Tak larutnya lignin dalam air disebabkan pada struktur lignin (Gambar 2) gugus hidrofobik lignin lebih meruah dibandingkan dengan gugus hidrofilik. Secara kualitatif, dapat dikatakan lignin telah terisolasi dari lindi hitam. Secara kuantitatif jumlah lignin dihitung dengan rendemennya. Rendemen lignin terhadap volume lindi hitam atau terhadap padatan total berturut-turut diperoleh 5,64% (Lampiran 5) atau 27,13% (Lampiran 6). Rendemen lignin terhadap padatan total yang diperoleh mendekati dengan yang diperoleh Lubis (2007) yaitu 25,26%.
Penentuan kadar lignin isolat digunakan metode Klason. Pereaksi yang digunakan ialah H2SO4 72% yang berfungsi
menghidrolisis ikatan eter antara lignin dengan selulosa/produk degradasi selulosa. Pada proses hidrolisis, selulosa larut dalam H2SO4 72% sedangkan lignin tidak larut.
Kadar lignin yang diperoleh dari isolasi sebesar 60,12% (Lampiran 7). Nilai ini tidak terlalu tinggi karena perlakuan isolasi lignin
dilakukan pada suhu kamar. Hal ini menunjukkan bahwa proses hidrolisis eter pada lignin dengan selulosa pada suhu kamar belum mencapai sempurna.
Natrium Lignosulfonat Sintetik
Menurut Sjöström (1995), gugus sulfonat lebih mudah masuk ke dalam lignin menggantikan gugus hidroksil pada karbon-α pada rantai samping propana. Karakteristik natrium lignosulfonat yang dihasilkan disajikan pada Tabel 4. Natrium lignosulfonat (NaLS) yang dihasilkan pada penelitian ini berbentuk serbuk berwarna cokelat kekuningan. Perubahan warna tersebut yang semula lignin berwarna cokelat muda menunjukkan adanya tambahan gugus sulfonat berupa ikatan rangkap. NaLS yang dihasilkan dapat larut dalam air. Hal ini menunjukkan bahwa hidrofilisitas lignin meningkat setelah mengalami sulfonasi. Tabel 4 Karakteristik NaLS sintetik
Pencirian NaLS sintetik NaLS* Warna cokelat
kekuningan kekuningan cokelat Uji kelarutan dalam air Larut Larut Kadar NaLS (%) 28,40-54,96 80,00 pH 6,58-7,24 7,00
Keterangan: * = Wesco Technology (1995) Reaksi sulfonasi terhadap lignin menurut Sjöström (1995) berlangsung serupa dengan
reaksi sulfonasi lignin terhadap 1,2-guaiasilpropana-1,3-diol (Gambar 5) yang
merupakan penggabungan karbon-β dengan karbon-1 salah satu dilignol. Langkah pertama terjadi pembentukan kuinon metida dengan pemutusan gugus α-hidroksil (eliminasi air), dilanjutkan dengan reaksi adisi nukleofilik terhadap kuinon metida dengan ion bisulfit menghasilkan
natrium-1,2-diguaiasilpropana-α-sulfonat-γ-ol. Kemudian dilanjutkan dengan
pemutusan gugus γ-hidroksil (eliminasi air) yang dikuti oleh adisi dengan ion bisulfit menghasilkan produk natrium-1,2-diguaiasilpropana-α-γ-disulfonat (Gambar 5).
8
HC HCOH CH2OH OCH3 -H2O OH HC CH CH2OH OCH3 OH NaHSO3 OCH3 OH OCH3 O HC OH HCSO3Na CH2OH OCH3 OCH3 OH -H2O NaHSO3 NaO3SCH2 HC OH HCSO3Na OCH3 OCH3 OHGambar 5 Reaksi sulfonasi terhadap 1,2-diguaiasilpropana-1,3-diol.
Kadar NaLS
Kadar NaLS merupakan ukuran jumlah natrium lignosulfonat yang dihasilkan reaksi sulfonasi dengan NaHSO3. Kadar NaLS yang
diperoleh pada perlakuan ini berkisar 28,40-54,96% (Lampiran 8). Hasil yang diperoleh pada perlakuan tersebut belum mencapai sempurna jika dibandingkan dengan yang diperoleh Wesco (1995) yaitu 80,00%. Walaupun kadar tersebut tidak tinggi, secara kuantitatif reaksi sulfonasi pada suhu 100 °C telah terjadi pemasukan gugus sulfonat ke dalam lignin.
Ketiga nisbah lignin-NaHSO3 1:0,4;
1:0,5; dan 1:0,6 pada selang pH awal 5 sampai 7 terjadi peningkatan kadar NaLS (Gambar 6).
Gambar 6 Hubungan kadar NaLS terhadap pH awal pada berbagai nisbah lignin-NaHSO3.
Kadar NaLS tertinggi diperoleh pada nisbah lignin-NaHSO3 1:0,5 dengan pH awal 7. Hal
ini dapat dikatakan bahwa pada nisbah lignin-NaHSO3 1:0,5 dengan pH awal 7, pemasukan
gugus sulfonat ke dalam lignin terjadi secara maksimum. Hal tersebut disebabkan pada pH 7, lignin lebih mudah terionisasi daripada pH 5 atau 6 sehingga lignin lebih mudah larut dengan NaHSO3 dan air. Sedangkan pada
nisbah lignin-NaHSO3 1:0,5 diduga terjadi
tumbukan antarmolekul lignin dan NaHSO3
paling efektif daripada nisbah 1:0,4 dan 1:0,6. Hal ini dapat dikatakan bahwa interaksi antara pH awal 7 dan nisbah lignin-NaHSO3 1:0,5
lebih efektif untuk menghasilkan NaLS. Struktur resonansi lignin pada pH awal 7 juga memberikan pengaruh pada kadar NaLS.
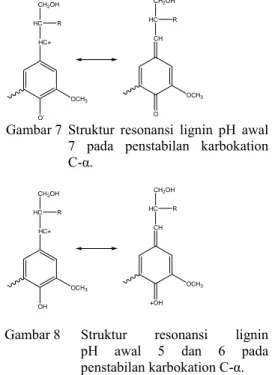
Hal tersebut dikarenakan pembentukan karbokation C-α (setelah eliminasi air) pada pH 7 lebih stabil daripada struktur resonansi lignin pada pH awal 5 dan 6 (Gambar 7 dan 8). Hal ini menyebabkan pada pH awal 7, gugus sulfonat lebih mudah masuk pada posisi C-α. HC+ HC CH2OH R OCH3 O -CH HC CH2OH R OCH3 O
Gambar 7 Struktur resonansi lignin pH awal 7 pada penstabilan karbokation C-α. HC+ HC CH2OH R OCH3 OH CH HC CH2OH R OCH3 +OH
Gambar 8 Struktur resonansi lignin pH awal 5 dan 6 pada penstabilan karbokation C-α. Hasil analisis ragam pada α = 5% menunjukkan bahwa nisbah lignin-NaHSO3,
pH awal, serta interaksi antara keduanya memberikan pengaruh yang nyata terhadap kadar NaLS (Lampiran 8). Hal ini menunjukkan bahwa kadar NaLS dipengaruhi oleh nisbah lignin-NaHSO3 dan pH awal.
Uji lanjut Duncan pada α = 5% menunjukkan bahwa pada pH awal 5, ketiga nisbah lignin-NaHSO3 memberikan pengaruh
yang berbeda satu sama lain (Lampiran 9). Nisbah lignin-NaHSO3 1:0,4 menghasilkan
kadar NaLS 31,33% berbeda nyata dengan nisbah lignin-NaHSO3 1:0,5 dengan kadar
NaLS 28,40%. Nisbah lignin-NaHSO3 1:0,5
juga berbeda nyata dengan nisbah lignin-NaHSO3 1:0,6 dengan kadar NaLS 35,11%.
Hal tersebut juga terjadi antara nisbah lignin-NaHSO3 1:0,4 dengan 1:0,6 yang
menghasilkan kadar NaLS berbeda nyata. Uji lanjut Duncan pada pH awal 6 dan 7 menunjukkan kesimpulan yang sama dengan pH awal 5, yaitu ketiga nisbah lignin-NaHSO3
(1:0,4; 1:0,5; dan 1:0,6) memberikan pengaruh yang berbeda satu sama lain (Lampiran 9). 0 10 20 30 40 50 60 4,5 5 5,5 6 6,5 7 7,5 pH awal Ka da r N aL S (% ) Nisbah 1:0.4 Nisbah 1:0.5 Nisbah 1:0.6
Derajat Keasaman NaLS
Derajat keasaman (pH) NaLS merupakan ukuran jumlah ion hidrogen dalam natrium lignosulfonat yang dihasilkan dari reaksi sulfonasi lignin. pH NaLS yang diperoleh pada perlakuan ini berkisar 6,58-7,24 (Lampiran 10). Kisaran pH NaLS yang diperoleh mendekati pH NaLS standar yaitu 7. Kisaran pH NaLS yang diperoleh juga relatif sama dengan yang diperoleh Dzikrulloh (2007) yaitu 6,42-7,11. Kisaran pH NaLS yang diperoleh pada perlakuan ini bersifat netral akibat naiknya hidrofilisitas lignin menjadi NaLS. Naiknya hidrofilisitas lignin disebabkan oleh adanya tambahan gugus sulfonat yang masuk ke dalam lignin sehingga NaLS yang dihasilkan dapat larut dalam air.
Baik pada nisbah lignin-NaHSO3 1:0,4
maupun 1:0,6, pada selang pH awal 5 sampai 7 sedikit menaikkan pH NaLS sedangkan pada nisbah lignin-NaHSO3 1:0,5 sedikit
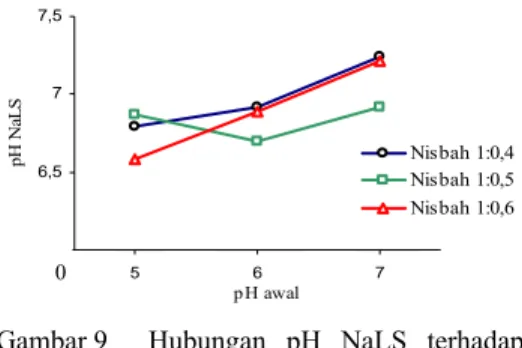
menurun pada selang pH awal 5 sampai 6 dan meningkat pada pH awal 7 (Gambar 9).
Gambar 9 Hubungan pH NaLS terhadap pH awal pada berbagai nisbah lignin-NaHSO3.
pH NaLS tertinggi didapatkan pada nisbah lignin-NaHSO3 1:0,4 dengan pH awal 7.
Walaupun pada kondisi nisbah lignin-NaHSO3 1:0,4 dengan pH awal 7 dihasilkan
pH NaLS tertinggi, perlakuan tersebut bukan merupakan kondisi terbaik untuk menghasilkan NaLS. Hal tersebut dikarenakan pada uji analisis ragam pada α = 5% menunjukkan bahwa nisbah lignin-NaHSO3,
pH awal, serta interaksi antara keduanya tidak memberikan pengaruh yang nyata terhadap pH NaLS (Lampiran 10). Hal ini menunjukkan bahwa pH NaLS tidak dipengaruhi oleh nisbah lignin-NaHSO3 dan
pH awal.
Bobot NaLS
Bobot NaLS yang diperoleh pada perlakuan ini berkisar 2,9778-5,1269 g (Lampiran 11). Baik pada nisbah lignin-NaHSO3 1:0,4 maupun 1:0,5, bobot NaLS
meningkat tajam pada selang pH awal 5 sampai 6 dan menurun pada selang pH awal 6 sampai 7 sedangkan pada nisbah lignin-NaHSO3 1:0,6, bobot NaLS sedikit menurun
pada selang pH awal 5 sampai 6 dan meningkat tajam pada selang pH awal 6 sampai 7 (Gambar 10).
Gambar 10 Hubungan bobot NaLS terhadap pH awal pada berbagai nisbah lignin-NaHSO3.
.
Bobot NaLS tertinggi didapatkan pada nisbah lignin-NaHSO3 1:0,6 dengan pH awal 7.
Walaupun pada kondisi nisbah lignin-NaHSO3 1:0,6 dengan pH awal 7 dihasilkan
bobot NaLS tertinggi, perlakuan tersebut bukan merupakan kondisi terbaik untuk menghasilkan NaLS. Hal tersebut dikarenakan pada uji analisis ragam pada α = 5% menunjukkan bahwa nisbah lignin-NaHSO3,
pH awal, serta interaksi antara keduanya tidak memberikan pengaruh yang nyata terhadap bobot NaLS (Lampiran 11). Hal ini menunjukkan bahwa bobot NaLS tidak dipengaruhi oleh nisbah lignin-NaHSO3 dan
pH awal.
Spektrum FTIR Lignin dan NaLS
Tujuan pencirian gugus fungsi lignin dan NaLS adalah melihat perubahan serapan antara lignin dengan NaLS hasil sulfonasi. Spektrum FTIR lignin (Gambar 11) memperlihatkan serapan pada bilangan gelombang 3432,6 cm-1 menunjukkan adanya
gugus hidroksil (-OH), pada bilangan gelombang 2933,2 cm-1 merupakan uluran
C-H, pada bilangan gelombang 1613,2 cm-1
merupakan gugus karbonil (C=O), pada bilangan gelombang 1515,4 cm-1 dan
1459,3 cm-1 merupakan gugus C-C aril, dan
pada bilangan gelombang 1112,6 cm-1
merupakan C-O eter.
6 6,5 7 7,5 4,5 5 5,5 6 6,5 7 7,5 pH awal pH Na L S Nisbah 1:0,4 Nisbah 1:0,5 Nisbah 1:0,6 0 0 1 2 3 4 5 6 4,5 5 5,5 6 6,5 7 7,5 pH awal B obot N aL S ( gr am ) Nisbah 1:0,4 Nisbah 1;0,5 Nisbah 1:0,6
10
Walaupun tidak ada cara pasti mempresentasikan spektrum FTIR, dalam penelitian ini menunjukkan perubahan serapan yang signifikan antara lignin dengan NaLS hasil sulfonasi. Perubahan tersebut terlihat pada spektrum FTIR NaLS terdapat serapan uluran C-S pada bilangan gelombang 622 cm-1
(Gambar 12) sedangkan pada spektrum FTIR lignin tidak terdapat serapan uluran C-S pada bilangan gelombang tersebut (Gambar 11). Hal ini menunjukkan bahwa secara kualitatif pada penelitian ini telah terjadi reaksi sulfonasi lignin dengan cara pemasukan gugus sulfonat pada lignin.
Gambar 11 Spektrum FTIR lignin isolat. O-H C-H C=O C-C aril C-O Bilangan gelombang (cm-1)
Gambar 12 Spektrum FTIR NaLS sintetik. Bilangan gelombang (cm-1) C-H O-H C=O C-C aril C-S C-O
12
SIMPULAN DAN SARAN
Simpulan
Lignin isolat yang diperoleh memiliki rendemen 5,64% (b/v) atau 27,13% padatan total. Kadar lignin yang diperoleh sebesar 60,12%.
Reaksi sulfonasi lignin dengan NaHSO3
pada suhu 100 °C dengan nisbah lignin-NaHSO3 (1:0,4; 1:0,5; dan 1:0,6) dan pH awal
5, 6, dan 7 dihasilkan NaLS dengan kadar 28,40-54,96%, pH (10% larutannya) 6,58-7,24, dan bobot 2,9778-5,1269 g.
Pada penelitian ini telah terjadi reaksi sulfonasi lignin. Nisbah lignin-NaHSO3 dan
pH awal pada reaksi sulfonasi hanya berpengaruh terhadap kadar NaLS dan tidak berpengaruh terhadap pH dan bobot NaLS. Kondisi terbaik sulfonasi lignin pada perlakuan ini didapatkan pada nisbah lignin-NaHSO3 1:0,5 dengan pH awal 7 dihasilkan
NaLS dengan kadar 54,96% dan pH 6,92 dengan bobot 3,7629 g.
Saran
Pengaruh suhu sebaiknya dilakukan juga terhadap NaLS yang dihasilkan dan perlu dilakukan penelitian lanjutan mengenai aplikasi NaLS yang dihasilkan.
DAFTAR PUSTAKA
Achmadi SS. 1990. Bahan Pengajaran Kimia Kayu. Departemen Pendidikan dan Kebudayaan Direktorat Jendral Pendidikan Tinggi. Bogor: PAU Ilmu
Ilmu Hayat IPB.
Adler E. 1977. Lignin Chemistry-past, present, and future Wood Sci. Technology. 11: 169-218.
Dilling et al., penemu. 1990. Production of
Lignosulphonate Aditives. 9 Jan 1990. US Patent. 4 892 588.
Dzikrulloh T. 2007. Pengaruh Nisbah Reaktan Lignin-NaHSO3 dan pH terhadap Produk
Natrium Lignosulfonat [skripsi]. Bogor: Institut pertanian Bogor.
Fengel D, Wegener G. 1995. Kayu: Kimia, Ultrastruktur, dan Reaksi-Reaksi.
Sastrohamidjojo H, penerjemah; Yogyakarta: UGM Pr. Terjemahan dari:
Wood: Chemistry, Ultrastructure, and Reactions.
Gargulak JD, Lebo SE. 2000. Commercial Use of Lignin Based Materials. In: Glaser W.G., Northey, R.A., Schultz, T.P (Eds), Lignin: Historical, biological, and Material Perspectives. Washington;
Oxford University Pr. Hlm. 304-320. Goldman CR dan Horne AJ. 1983. Limnology.
New York: Mc Graw-Hill.
Jain RK, Kulkarni AG.1991. Utilization of Alkaline Spent Pulping Liquor from Bagasse as Source of Industrial Dispersant. Di dalam: Pant R, editor.
Bagasse Newsprint, Lignin Utilization and Cellulose Derivatives; Proceedings of the Woorkshop on Wood Pulping Refining, Bandung, 10-13 Nov 1991.
Bandung: Departemen Perindustrian. Hlm 199-218.
Lubis AA. 2007. Isolasi dari Lindi Hitam (Black Liquor) Proses Pemasakan Soda dan Proses Sulfat (Kraft) [skripsi]. Bogor:
Institut Pertanian Bogor.
Kim H, Hill MK, Fricke AL. 1987. Preparation of Kraft Lignin From Black Liquor. Tappi Journal 12: 112-115.
Mattjik AA, Sumertajaya IM. 2002.
Perancangan Percobaan dengan Aplikasi SAS dan Minitab. Jilid I. Bogor: IPB Pr.
Nada AM, Sakhawi ME, Kamel SM. 1998. Infrared Spectroscopic Study of Lignin.
Polimer Degradation and Stability 60:
247-251.
[Pulp and Paper Industry]. 2006. World and Paper Demand by Grade 1980-2010. [terhubung berkala] http;//www. pulpandpaper-technology.com/projects/ silao/silao3.html [21 Agustus 2006]. Rini DS. 2002. Minimasi Limbah Dalam
Industri Pulp and Paper. [terhubung berkala]. http;//www.terranet.or.id/ tulisandetil.php/id=1306 [4 Juli 2004
Rudatin S. 1989. Potensi dan Prospek Pemanfaatan Lignin dari Limbah Industri Pulp dan Kertas di Indonesia. Berita Selulosa(25)1: 14-17. Departemen Perindustrian RI. Balai Besar Penelitian
dan Pengembangan Industri Selulosa. Bandung.
[SNI] Standar Nasional indonesia. 1991. Cara Uji Massa Jenis, Senyawa-Senyawa Organik dan Anorganik dalam Lindi Hitam. SNI 06-2235-1991.
Sjöström E. 1993. Kimia Kayu, Dasar-Dasar,
dan Penggunaanya. Ed ke-2.
Sastrohamidjojo H, penerjemah. Yogyakarta: UGM pr. Terjemahan dari:
Wood Chemistry, Fundamental, and Application.
Sjöström E. 1995. Kimia Kayu, Dasar-Dasar,
dan Penggunaanya. Ed ke-2.
Sastrohamidjojo H, penerjemah. Yogyakarta: UGM pr. Terjemahan dari:
Wood Chemistry, Fundamental, and Application.
Syahmani. 2000. Isolasi, Sulfonasi, dan Asetilasi Lignin dari Tandan Kosong Sawit dan Studi Pengaruhnya Terhadap Proses Pelarutan Urea [Tesis]. Program Pascasarjana, Institut Teknologi Bandung.
[TAPPI] Technical of the Pulp and Paper Industry. Lignin Content of Pulp and Wood. T222 05-74.
[Weyerhaeuser Company]. 2004. Material Safety Data Sheet of Lignin. [terhubung berkala]. http; /www.weyerhaeuser.com/ environment/msds/pdfs/074.pdf [7 Juli 2006].
[WTL] Wesco Technologies, Ltd. 1995. Typical properties of Weschem Ammonium Lignosulphonat, Sodium Lignosulphonat, Zinc Lignosulphonat, San Clemente, CA. 92674-3880.USA. [Terhubung Berkala]. http: /www.wtl.com/aprops.htm [12 sept 2005].
14
Lampiran 1 Diagram alir isolasi lignin
disaring
* ditambahkan H2SO4 20% (b/v) hingga pH 2
* disentrifus 3000 rpm, 20 menit
* dilarutkan dengan NaOH 1 N * disaring
* ditambahkan H2SO4 20% (b/v) hingga pH 2
* disentrifus 3000 rpm, 20 menit
* dicuci dengan H2SO4 0,01 N 5 kali
* dicuci dengan air deionisasi 2 kali * dikeringkan dalam oven 50-60 °C
Lindi Hitam
Sisa-sisa padatan
Larutan lindi hitam
Endapan lignin Larutan lignin Larutan non-lignin Padatan non-lignin Endapan lignin Larutan non-lignin Lignin isolat
Lampiran 2 Diagram alir sintesis natrium lignosulfonat
direfluks selama 4 jam
didestilasi Air * ditambah metanol * disaring NaHSO3 Penguapan metanol MeOH Isolat lignin
Sintesis natrium lignosulfonat (NaLS) Nisbah lignin-NaHSO3 : 1:0,4; 1:0,5; 1:0,6 pH: 5, 6, 7 suhu: 100°C Hasil reaksi NaLS+ NaHSO3
NaLS + MeOH NaLS Pencirian NaLS
16
Lampiran 3 Data kadar air dan padatan total lindi hitam
Ulangan A (g) B (g) Kadar air (%) Padatan total (%) 1 5,0007 0,9480 81,04 18,96 2 5,0005 0,9450 81,10 18,90 3 5,0000 0,9440 81,12 18,88
Rerata 81,09 18,91
Keterangan:
A = bobot contoh sebelum pengeringan B = bobot contoh setelah pengeringan Lampiran 4 Data bobot jenis lindi hitam
Ulangan m1 (g) m2 (g) m3 (g) da (g/cm3) Bobot jenis (g/cm3)
1 14,7244 20,1088 20,6923 0,9998 1,11
2 14,7244 20,1086 20,6925 0,9998 1,11
3 14,7244 20,1087 20,6923 0,9998 1,11
Rerata 1,11
Keterangan:
m1 = bobot piknometer kosong
m2 = bobot piknometer + air
m3 = bobot piknometer + contoh
da = bobot jenis air pada 26 οC
Lampiran 5 Data rendemen lignin berdasarkan volume lindi hitam
Ulangan Volume contoh (ml) Bobot lignin (g) Rendemen (%)
1 300,00 17,2494 5,75
2 300,00 16,8327 5,61
3 300,00 16,7085 5,57
Rerata 5,64
Lampiran 6 Data rendemen lignin berdasarkan padatan total lindi hitam Ulangan Volume
contoh (ml) Bobot jenis contoh (g/ml)
Bobot
contoh (g) Padatan Bobot total (g) Bobot lignin isolat (g) Rendemen lignin (%) 1 300 1,11 330 62,4030 17,2494 27,64 2 300 1,11 330 62,4030 16,8327 26,97 3 300 1,11 330 62,4030 16,7085 26,78 Rerata 27,13
Lampiran 7 Data kadar lignin
Ulangan Bobot contoh (g) Bobot lignin (g) Kadar lignin (%)
1 1,0002 0,5974 59,73
2 0,9998 0,6011 60,12
3 1,0003 0,6053 60,51
Lampiran 8 Pengaruh nisbah lignin-NaHSO3 dan pH awal terhadap kadar NaLS pH awal Nisbah lignin-NaHSO3 Ulangan 5 6 7 1 30,93 43,36 47,75 1 : 0,4 2 31,73 44,10 48,43 Rerata µ = 31,33 µ = 43,73 µ = 48,09 1 28,00 46,50 55,10 1 : 0,5 2 28,80 47,22 54,82 Rerata µ = 28,40 µ = 46,86 µ = 54,96 1 36,03 39,33 52,40 1 : 0,6 2 34,19 39,21 52,12 Rerata µ = 35,11 µ = 39,27 µ = 52,26 Hipotesis yang diuji
1 Pengaruh nisbah lignin-NaHSO3
H0 : τ1 = τ2 = τ3 = 0 (nisbah lignin-NaHSO3 memberikan pengaruh yang sama terhadap kadar
NaLS)
H1 : minimal ada satu i dengan τi ≠ 0, i = 1,2,3
2 Pengaruh pH awal
H0 : β1 = β2 = β3 = 0 (pH awalmemberikan pengaruh yang sama terhadap kadar NaLS)
H1 : minimal ada satu j dengan βj ≠ 0, j = 1,2,3
3 Pengaruh interaksi antara nisbah lignin-NaHSO3 dan pH awal
H0 : (τβ)ij = 0 untuk semua ij (interaksi antara nisbah lignin-NaHSO3 dan pH awal
memberikan pengaruh yang sama terhadap kadar NaLS) H1 : minimal ada satu (τβ)ij ≠ 0
Langkah-langkah perhitungan: FK = a.b.r Y...2 ∑ ∑ ∑ =
(
)
2 . 3 . 3 02 , 760 2 = 32.090,5778 JKT = ∑ Yijk2 – FK = (30,932 + 43,362 + ... + 52,122) – 32.090,5778 = 1.383,6122 JKA = b.r Yi..2 ∑ ∑ - FK = 2 . 3 ) 28 , 253 44 , 260 30 , 246 ( 2+ 2+ 2 - 32.090,5778 = 16,6625 JKB = a.r Y.j.2 ∑ ∑ - FK = 2 . 3 ) 62 , 310 72 , 259 68 , 189 ( 2+ 2+ 2 - 32.090,5778 = 1.229,0497 JKP = r Yij.2 ∑ - FK = 2 ) 52 , 104 ... 46 , 87 66 , 62 ( 2+ 2+ + 2 - 32.090,5778 = 1.380,4296 JKAB = JKP – JKA – JKB = 1.380,4296 – 16,6625 – 1.229,0497 = 134,7174 JKG = JKT – JKP = 1.383,6122 – 1.380,4296 = 3,182618
Lanjutan Lampiran 8 dbA = a–1 = 3 - 1 = 2 dbB = b–1 = 3 - 1 = 2 dbAB = (a-1)(b-1) = 4 dbG = ab(r-1) = (3)(3)(2-1) = 9 dbT = abr-1 = (3)(3)(2)-1 = 17 KTA = A db JKA = 2 6625 , 16 = 8,3313 KTB = B db JKB = 2 0497 , 229 . 1 = 614,5249 KTAB = AB db JKAB = 4 7174 , 134 = 33,6794 KTG = G db JKG = 9 1826 , 3 = 0,3536 Fhit A = KTG KTA = 3536 , 0 3313 , 8 = 23,5614 Fhit B = KTG KTB = 3536 , 0 5249 , 614 = 1.737,9098 Fhit AB = KTG KTAB = 3536 , 0 6794 , 33 = 95,2472 Tabel ANOVASumber keragaman Derajat bebas (db) Jumlah Kuadrat (KT) Kuadrat Tengah (KT) Fhitung Ftabel Nisbah 2 16,6625 8,3313 23,5614 F0,05(2,9)=4,256 pH awal 2 1.229,0497 614,5249 1.737,9098 F0,05(2,9)=4,256 Nisbah vs pH awal 4 134,7174 33,6794 95,2472 F0,05(4,9)=3,633 Galat 9 3,1826 0,3536 Total 17 1.383,6122 Kesimpulan:
1 Karena Fhitung nisbah > F0,05(2,9) maka tolak H0
Artinya: Nisbah lignin-NaHSO3 memberikan pengaruh yang nyata terhadap kadar NaLS.
2 Karena Fhitung pH awal > F0,05(2,9) maka tolak H0
Artinya: pH awal memberikan pengaruh yang nyata terhadap kadar NaLS. 3 Karena Fhitung interaksi nisbah vs pH awal > F0,05(4,9) maka tolak H0
Artinya: Interaksi antara nisbah lignin-NaHSO3 dan pH awal memberikan pengaruh yang
Lampiran 9 Uji lanjut Duncan pada kadar NaLS A Uji Duncan untuk masing-masing pH awal
Nilai kritis Duncan: Rp = rα (p,dbg)
r KTG , p = 2,3 R2 = r0,05 (2,9) 2 3536 , 0 = 1,3455 R3 = r0,05 (3,9) 2 3536 , 0 = 1,4044 1 Pada pH awal 5
Nisbah lignin-NaHSO3 Rata-rata
1;0,4 31,33 1:0,5 28,40 1:0,6 35,11 µ1 = 28,40; µ2 = 31,33; µ3 = 35,11
|
µ1- µ2| =
2,93>R2 = 1,3455|
µ2- µ3| =
3,78>R2 = 1,3455 Tolak H0|
µ1- µ3| =
6,71>R3 = 1,4044Artinya: Pada pH awal 5, masing-masing nisbah lignin-NaHSO3 memberikan pengaruh yang
berbeda satu sama lain. 2 Pada pH awal 6
Nisbah lignin-NaHSO3 Rata-rata
1;0,4 43,73 1:0,5 46,86 1:0,6 39,27 µ1 = 39,27; µ2 = 43,73; µ3 = 46,86
|
µ1- µ2| =
4,46>R2 = 1,3455|
µ2- µ3| =
3,13>R2 = 1,3455 Tolak H0|
µ1- µ3| =
7,59>R3 = 1,4044Artinya: Pada pH awal 6, masing-masing nisbah lignin-NaHSO3 memberikan pengaruh yang
berbeda satu sama lain. 3 Pada pH awal 7
Nisbah lignin-NaHSO3 Rata-rata
1;0,4 48,09 1:0,5 54,96 1:0,6 52,26 µ1 = 48,09; µ2 = 52,26; µ3 = 54,96
|
µ1- µ2| =
4,17 >R2 = 1,3455|
µ2- µ3| =
2,70>R2 = 1,3455 Tolak H0|
µ1- µ3| =
6,87>R3 = 1,4044Artinya: Pada pH awal 7, masing-masing nisbah lignin-NaHSO3 memberikan pengaruh yang
20
Lanjutan Lampiran 9
B Uji Duncan untuk masing-masing nisbah lignin-NaHSO3
Nilai kritis Duncan: Rp = rα (p,dbg)
r KTG , p = 2,3 R2 = r0,05 (2,9) 2 3536 , 0 = 1,3455 R3 = r0,05 (3,9) 2 3536 , 0 = 1,4044
1 Pada nisbah lignin-NaHSO3 1;0,4
pH awal Rata-rata 5 31,33 6 43,73 7 48,09 µ1 = 31,33; µ2 = 43,73; µ3 = 48,09
|
µ1- µ2| =
12,40>R2 = 1,3455|
µ2- µ3| =
4,36>R2 = 1,3455 Tolak H0
|
µ1- µ3| =
16,76>R3 = 1,4044Artinya: Pada nisbah lignin-NaHSO3 1:0,4, masing-masing pH awal memberikan pengaruh yang
berbeda satu sama lain. 2 Pada nisbah lignin-NaHSO3 1:0,5
pH awal Rata-rata 5 28,40 6 46,86 7 54,96 µ1 = 28,40; µ2 = 46,86; µ3 = 54,96
|
µ1- µ2| =
18,46>R2 = 1,3455|
µ2- µ3| =
8,10>R2 = 1,3455 Tolak H0
|
µ1- µ3| =
26,56>R3 = 1,4044Artinya: Pada nisbah lignin-NaHSO3 1:0,5, masing-masing pH awal memberikan pengaruh yang
berbeda satu sama lain. 3 Pada nisbah lignin-NaHSO3 1:0,6
pH awal Rata-rata 5 35,11 6 39,27 7 52,26 µ1 = 35,11; µ2 = 39,27; µ3 = 52,26
|
µ1- µ2| =
4,16>R2 = 1,3455
|
µ2- µ3| =
12,99>R2 = 1,3455 Tolak H0|
µ1- µ3| =
17,15>R3 = 1,4044Artinya: Pada nisbah lignin-NaHSO3 1:0,6, masing-masing pH awal memberikan pengaruh yang
Lampiran 10 Pengaruh nisbah lignin-NaHSO3 dan pH terhadap pH NaLS yang dihasilkan pH awal Nisbah lignin-NaHSO3 Ulangan 5 6 7 1 6,93 7,19 7,60 1 : 0,4 2 6,64 6,65 6,88 Rerata µ = 6,79 µ = 6,92 µ = 7,24 1 6,84 6,61 6,81 1 : 0,5 2 6,89 6,79 7,03 Rerata µ = 6,87 µ = 6,70 µ = 6,92 1 6,36 7,00 7,42 1 : 0,6 2 6,79 6,77 7,00 Rerata µ = 6,58 µ = 6,89 µ = 7,21 Hipotesis yang diuji
1 Pengaruh nisbah lignin-NaHSO3
H0 : τ1 = τ2 = τ3 = 0 (nisbah lignin-NaHSO3 memberikan pengaruh yang sama terhadap pH
NaLS yang dihasilkan)
H1 : minimal ada satu i dengan τi ≠ 0, i = 1,2,3
2 Pengaruh pH awal
H0 : β1 = β2 = β3 = 0 (pH awalmemberikan pengaruh yang sama terhadap pH NaLS yang
dihasilkan)
H1 : minimal ada satu j dengan βj ≠ 0, j = 1,2,3
3 Pengaruh interaksi antara nisbah lignin-NaHSO3 dan pH awal
H0 : (τβ)ij = 0 untuk semua ij (interaksi antara nisbah lignin-NaHSO3 dan pH awal
memberikan pengaruh yang sama terhadap pH NaLS yang dihasilkan) H1 : minimal ada satu (τβ)ij ≠ 0
Langkah-langkah perhitungan: FK = a.b.r Y...2 ∑ ∑ ∑ =
(
)
2 . 3 . 3 20 , 124 2 = 856,9800 JKT = ∑ Yijk2 – FK = (6,932 + 6,642 + ... + 7,002) – 856,9800 = 1,4414 JKA = b.r Yi..2 ∑ ∑ - FK = 2 . 3 ) 34 , 41 97 , 40 89 , 41 ( 2+ 2+ 2 - 856,9800 = 0,0714 JKB = a.r Y.j.2 ∑ ∑ - FK = 2 . 3 ) 74 , 42 01 , 41 45 , 40 ( 2+ 2+ 2 - 856,9800 = 0,4750 JKP = r Yij.2 ∑ - FK = 2 ) 42 , 14 ... 84 , 13 57 , 13 ( 2+ 2+ + 2 - 856,9800 = 0,7456 JKAB = JKP – JKA – JKB = 0,7456 – 0,0714 – 0,4750 = 0,199222
Lanjutan Lampiran 10 JKG = JKT – JKP = 1,4414 – 0,7456 = 0,6958 dbA = a–1 = 3 - 1 = 2 dbB = b–1 = 3 - 1 = 2 dbAB = (a-1)(b-1) = 4 dbG = ab(r-1) = (3)(3)(2-1) = 9 dbT = abr-1 = (3)(3)(2)-1 = 17 KTA = A db JKA = 2 0714 , 0 = 0,0357 KTB = B db JKB = 2 4750 , 0 = 0,2375 KTAB = AB db JKAB = 4 1992 , 0 = 0,0498 KTG = G db JKG = 9 6958 , 0 = 0,0773 Fhit A = KTG KTA = 0773 , 0 0357 , 0 = 0,4618 Fhit B = KTG KTB = 0773 , 0 2375 , 0 = 3,0724 Fhit AB = KTG KTAB = 0773 , 0 0498 , 0 = 0,6442 Tabel ANOVASumber keragaman Derajat
bebas (db) Kuadrat (KT) Jumlah Tengah (KT) Kuadrat Fhitung Ftabel Nisbah 2 0,0714 0,0357 0,4618 F0,05(2,9)=4,256 pH awal 2 0,4750 0,2375 3,0724 F0,05(2,9)=4,256 Nisbah vs pH awal 4 0,1992 0,0498 0,6442 F0,05(4,9)=3,633 Galat 9 0,6958 0,0773 Total 17 1,4414 Kesimpulan:
1 Karena Fhitung nisbah < F0,05(2,9) maka terima H0
Artinya: Nisbah lignin-NaHSO3 tidak memberikan pengaruh yang nyata terhadap pH NaLS.
2 Karena Fhitung pH awal < F0,05(2,9) maka terima H0
Artinya: pH awal tidak memberikan pengaruh yang nyata terhadap pH NaLS. 3 Karena Fhitung interaksi nisbah vs pH awal < F0,05(4,9) maka terima H0
Artinya: Interaksi antara nisbah lignin-NaHSO3 dan pH awal tidak memberikan pengaruh
Lampiran 11 Pengaruh nisbah lignin-NaHSO3 dan pH terhadap bobot NaLS yang dihasilkan pH awal Nisbah lignin-NaHSO3 Ulangan 5 6 7 1 3,3418 5,1484 4,2557 1 : 0,4 2 2,8322 4,6928 5,3395 Rerata µ = 3,0870 µ = 4,9206 µ = 4,7976 1 3,4436 3,4975 3,9935 1 : 0,5 2 2,5120 5,5477 3,5323 Rerata µ = 2,9778 µ = 4,5226 µ = 3,7629 1 5,2019 4,4872 4,5096 1 : 0,6 2 3,6919 4,1679 5,7441 Rerata µ = 4,4469 µ = 4,3276 µ = 5,1269 Hipotesis yang diuji
1 Pengaruh nisbah lignin-NaHSO3
H0 : τ1 = τ2 = τ3 = 0 (nisbah lignin-NaHSO3 memberikan pengaruh yang sama terhadap bobot
NaLS yang dihasilkan)
H1 : minimal ada satu i dengan τi ≠ 0, i = 1,2,3
2 Pengaruh pH awal
H0 : β1 = β2 = β3 = 0 (pH awalmemberikan pengaruh yang sama terhadap bobot NaLS yang
dihasilkan)
H1 : minimal ada satu j dengan βj ≠ 0, j = 1,2,3
3 Pengaruh interaksi antara nisbah lignin-NaHSO3 dan pH awal
H0 : (τβ)ij = 0 untuk semua ij (interaksi antara nisbah lignin-NaHSO3 dan pH awal
memberikan pengaruh yang sama terhadap bobot NaLS yang dihasilkan) H1 : minimal ada satu (τβ)ij ≠ 0
Langkah-langkah perhitungan: FK = a.b.r Y...2 ∑ ∑ ∑ =
(
)
2 . 3 . 3 9396 , 75 2 = 320,3790 JKT = ∑ Yijk2 – FK = (3,34182 + 5,1484+ ... + 5,74412) – 320,3790 = 15,0902 JKA = b.r Yi..2 ∑ ∑ - FK = 2 . 3 ) 8026 , 27 5266 , 22 6104 , 25 ( 2+ 2+ 2 - 320,3790 = 2,3418 JKB = a.r Y.j.2 ∑ ∑ - FK = 2 . 3 ) 3747 , 27 5415 , 27 0234 , 21 ( 2+ 2+ 2 - 320,3790 = 4,6030 JKP = r Yij.2 ∑ - FK = 2 ) 2537 , 10 ... 8412 , 9 1740 , 6 ( 2+ 2+ + 2 - 320,3790 = 9,6743 JKAB = JKP – JKA – JKB = 9,6743 – 2,3418 – 4,6030 = 2,729524
Lanjutan Lampiran 11 JKG = JKT – JKP = 15,0902 – 9,6743 = 5,4159 dbA = a–1 = 3 - 1 = 2 dbB = b–1 = 3 - 1 = 2 dbAB = (a-1)(b-1) = 4 dbG = ab(r-1) = (3)(3)(2-1) = 9 dbT = abr-1 = (3)(3)(2)-1 = 17 KTA = A db JKA = 2 3418 , 2 = 1,1709 KTB = B db JKB = 2 6030 , 4 = 2,3015 KTAB = AB db JKAB = 4 7295 , 2 = 0,6824 KTG = G db JKG = 9 4159 , 5 = 0,6018 Fhit A = KTG KTA = 6018 , 0 1709 , 1 = 1,9457 Fhit B = KTG KTB = 6018 , 0 3015 , 2 = 3,8244 Fhit AB = KTG KTAB = 6018 , 0 6824 , 0 = 1,1339 Tabel ANOVASumber keragaman Derajat
bebas (db) Kuadrat (KT) Jumlah Tengah (KT) Kuadrat Fhitung Ftabel Nisbah 2 2,3418 1,1709 1,9457 F0,05(2,9)=4,256 pH awal 2 4,6030 2,3015 3,8244 F0,05(2,9)=4,256 Nisbah vs pH awal 4 2,7295 0,6824 1,1339 F0,05(4,9)=3,633 Galat 9 5,4159 0,6018 Total 17 15,0902 Kesimpulan:
1 Karena Fhitung nisbah < F0,05(2,9) maka terima H0
Artinya: Nisbah lignin-NaHSO3 tidak memberikan pengaruh yang nyata terhadap bobot NaLS
yang dihasilkan.
2 Karena Fhitung pH awal < F0,05(2,9) maka terima H0
Artinya: pH awal tidak memberikan pengaruh yang nyata terhadap bobot NaLS yang dihasilkan.
3 Karena Fhitung interaksi nisbah vs pH awal < F0,05(4,9) maka terima H0
Artinya: Interaksi antara nisbah lignin-NaHSO3 dan pH awal tidak memberikan pengaruh