NEFRITIS LUPUS
PENDAHULUAN
Nefritis lupus merupakan salah satu manifestasi Sistemik Lupus Eritematosus (SLE) yang paling serius, biasanya timbul dalam waktu 5 tahun diagnosis, namun jarang terjadi
gagal ginjal.
Gejala nefritis lupus umumnya terkait dengan hipertensi, proteinuria, dan gagal ginjal. Dengan munculnya terapi imunosupresif, keterlibatan ginjal dan kelangsungan hidup pasien dengan nefritis lupus membaik.1
PATOGENESIS
Eritematosus sistemik lupus (SLE) adalah suatu gangguan autoimun yang ditandai dengan keterlibatan multisistem dan beragam autoantibodies dengan target komponen sel. Di antaranya antibodi terhadap DNA dan protein yang berperan dalam pembentukan deposits komplek imun yang menyebabkan respons inflamasi yang selanjutnya dapat menyebabkan gagal ginjal. 1 Reaksi autoimun mempunyai peranan penting dalam pathogenesis nefritis lupus. Reaksi imunologi meliputi produksi autoantibodi secara langsung terhadap elemen sel. Autoantibodi membentuk komplek imun pathogen. Pengendapan kompleks imun pada ginjal menyebabkan respon inflamasi melalui aktivasi kaskade komplemen dan rekruitmen sel inflamasi yang dapat dilihat saat biopsi. Trombosis glomerulus merupakan mekanisme lain yang berperan dalam pathogenesis nefritis lupus, terutama pada pasien dengan sindrom antiphospholipid antibody yang merupakan respon terhadap kompleks phospholipid-protein.1,2 Nukleosom mempunyai peranan penting dalam patogenesis nefritis lupus. Meningkatnya apoptosis menyebabkan munculnya antibodi anti-DNA dan kompleks imun. Nukleosom juga berperanan untuk memicu lesi jaringan, termasuk lesi glomerulus. Terdapat dua mekanisme yang menjelaskan bagaimana autoantibodi menyebabkan kerusakan jaringan: (a) pengendapan preformed kompleks imun di ginjal atau pembentukan kompleks in situ
melalui interaksi antara nukleosom yang sebelumnya sudah terdapat dalam glomerulus dan anti-dsDNA atau (b) reaksi silang antibodi dengan komponen membran basal glomerulus. Actinin telah diidentifikasi sebagai target cross-reaktif yang terikat oleh nephritogenic- anti dsDNA. Actinin adalah protein aktin-bundling yang terdapat pada podosit, monosit, kapiler, dan pembuluh darah besar. Terjadinya mutasi gen yang mengkode isoform actinin-4 telah
diidentifikasi dalam fokal dan segmental glomerulosklerosis familial. Actinin juga menjadi target anti-dsDNA pada manusia. Permukaan sel dan reseptor matriks pada berbagai tipe sel, termasuk sel mesangial, fibroblas, dan monosit, dapat mengikat nukleosom di ginjal.2,3,4,5
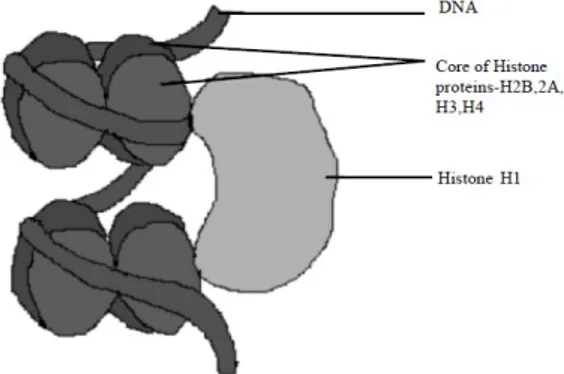
Gambar 1. Struktur nukleosom3
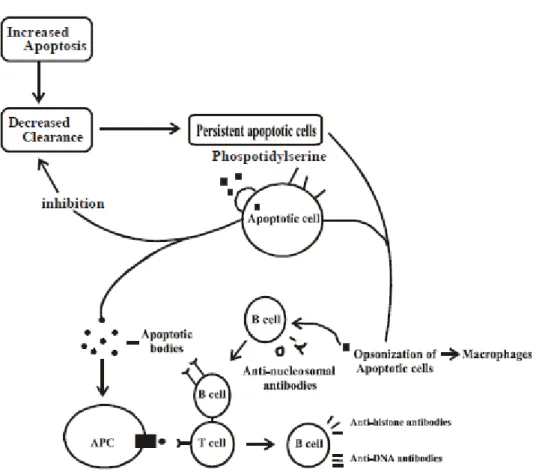
Pada awal penyakit, sebelum anti-Antibodi DNA muncul, antibodi spesifik nukleosom dapat memulai lesi ginjal. Perkembangan nukleosom memerlukan apoptosis. Sel yang mengalami apoptosis merupakan autoantigens SLE (gambar 2).3
Gambar 2. Pengaruh apoptosis dan nukleosom pada pathogenesis SLE3
PERJALANAN PENYAKIT
Klasifikasi nefritis lupus telah mengalami banyak revisi. Saat ini klasifikasi yang digunakan adalah klasifikasi the International Society of Pathology/Renal Pathology Society (ISN/RPS)
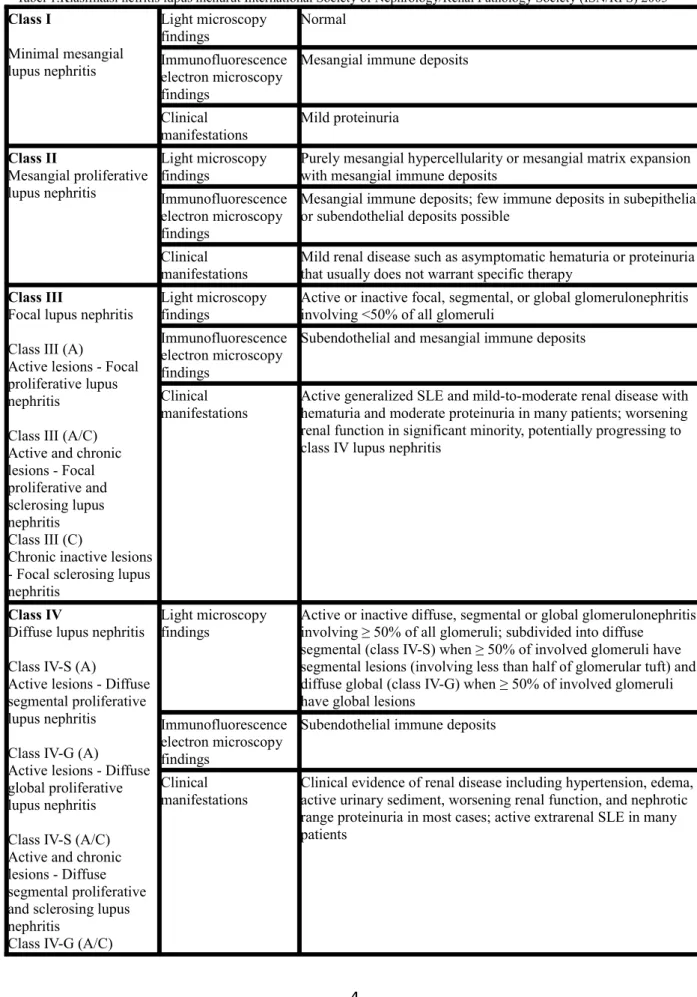
tahun 2003 berdasarkan pemeriksaan dengan mikroskop cahaya, imunofluoresen, dan pemeriksaan dengan mikroskop elektron yang berasal dari biopsi ginjal, yang dirangkum pada tabel 1.1,4
Tabel 1.Klasifikasi nefritis lupus menurut International Society of Nephrology/Renal Pathology Society (ISN/RPS) 2003 Class I Minimal mesangial lupus nephritis Light microscopy findings Normal Immunofluorescence electron microscopy findings
Mesangial immune deposits
Clinical
manifestations Mild proteinuria Class II
Mesangial proliferative lupus nephritis
Light microscopy findings
Purely mesangial hypercellularity or mesangial matrix expansion with mesangial immune deposits
Immunofluorescence electron microscopy findings
Mesangial immune deposits; few immune deposits in subepithelial or subendothelial deposits possible
Clinical
manifestations Mild renal disease such as asymptomatic hematuria or proteinuria that usually does not warrant specific therapy Class III
Focal lupus nephritis Class III (A)
Active lesions - Focal proliferative lupus nephritis
Class III (A/C) Active and chronic lesions - Focal proliferative and sclerosing lupus nephritis Class III (C)
Chronic inactive lesions - Focal sclerosing lupus nephritis
Light microscopy
findings Active or inactive focal, segmental, or global glomerulonephritis involving <50% of all glomeruli Immunofluorescence
electron microscopy findings
Subendothelial and mesangial immune deposits
Clinical manifestations
Active generalized SLE and mild-to-moderate renal disease with hematuria and moderate proteinuria in many patients; worsening renal function in significant minority, potentially progressing to class IV lupus nephritis
Class IV
Diffuse lupus nephritis Class IV-S (A)
Active lesions - Diffuse segmental proliferative lupus nephritis
Class IV-G (A)
Active lesions - Diffuse global proliferative lupus nephritis Class IV-S (A/C) Active and chronic lesions - Diffuse segmental proliferative and sclerosing lupus nephritis
Class IV-G (A/C)
Light microscopy
findings Active or inactive diffuse, segmental or global glomerulonephritis involving ≥ 50% of all glomeruli; subdivided into diffuse segmental (class IV-S) when ≥ 50% of involved glomeruli have segmental lesions (involving less than half of glomerular tuft) and diffuse global (class IV-G) when ≥ 50% of involved glomeruli have global lesions
Immunofluorescence electron microscopy findings
Subendothelial immune deposits
Clinical manifestations
Clinical evidence of renal disease including hypertension, edema, active urinary sediment, worsening renal function, and nephrotic range proteinuria in most cases; active extrarenal SLE in many patients
Active and chronic lesions - Diffuse global proliferative and sclerosing lupus nephritis Class IV-S (C)
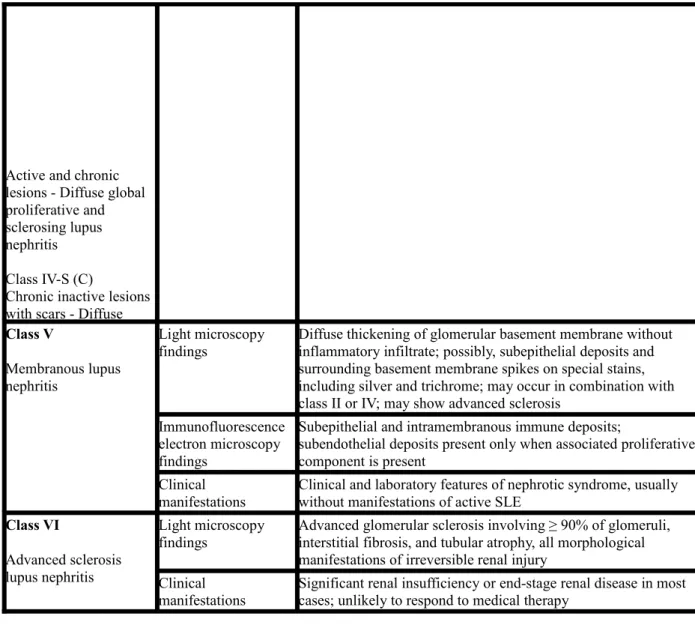
Chronic inactive lesions with scars - Diffuse Class V
Membranous lupus nephritis
Light microscopy findings
Diffuse thickening of glomerular basement membrane without inflammatory infiltrate; possibly, subepithelial deposits and surrounding basement membrane spikes on special stains, including silver and trichrome; may occur in combination with class II or IV; may show advanced sclerosis
Immunofluorescence electron microscopy findings
Subepithelial and intramembranous immune deposits;
subendothelial deposits present only when associated proliferative component is present
Clinical
manifestations Clinical and laboratory features of nephrotic syndrome, usually without manifestations of active SLE Class VI
Advanced sclerosis lupus nephritis
Light microscopy
findings Advanced glomerular sclerosis involving ≥ 90% of glomeruli, interstitial fibrosis, and tubular atrophy, all morphological manifestations of irreversible renal injury
Clinical
manifestations Significant renal insufficiency or end-stage renal disease in most cases; unlikely to respond to medical therapy
Selain klasifikasi berdasarkan patologis, terdapat indeks aktivitas dan indeks kronisitas yang dapat memprediksi prognosis ginjal (progresivitas penyakit ginjal). Indeks aktivitas mencerminkan keadaan peradangan aktif diamati pada biopsi, yang mungkin reversibel dengan terapi medis. Indeks kronisitas mencerminkan jumlah fibrosis dan jaringan parut, yang tidak respon terhadap terapi. Lesi ginjal dengan indeks aktivitas yang tinggi memerlukan terapi agresif (pemberian obat sitostatika) karena bersifat reversibel, sedangkan lesi ginjal dengan kronisitas tinggi harus dipikirkan untuk transplantasi ginjal karena bersifat ireversibel. Indeks tersebut berfungsi sebagai alat prognostik dan panduan umum untuk terapi.1
Tabel 2. Indeks aktivitas dan kronisitas glomerulus1
Activity Index Chronicity Index
• Endocapillary hypercellularity with or without leukocyte
• Karyorrhexis • Fibrinoid necrosis
• Rupture of glomerular basement membrane • Cellular or fibrocellular crescents
• Subendothelial deposits on light microscopy • Intraluminal immune aggregates
• Fibrous adhesion • Fibrous crescents
PREVALENSI
Prevalensi SLE di Eropa dan Amerika Utara adalah 40 per 100.000. Kejadian SLE 3 kali lebih besar pada ras kulit hitam dibandingkan kulit putih,kecuali pada negro Afrika. Pada survei yang dilakukan di Inggris (UK) didapatkan risiko relatif SLE pada populasi Asia adalah 6,7 dan 6,1 pada kulit hitam dibandingkan dengan kulit putih. Lebih dari 80% kasus SLE terjadi pada perempuan setelah masa pubertas. Pada masa prepubertas kejadian SLE adalah 2:1 pada anak perempuan dan laki-laki, meningkat pada remaja 4,5:1 dan dewasa 8:1. Pada anak SLE terjadi setelah usia 5 tahun dengan puncak pada akhir masa kanak-kanak dan remaja. Dua puluh persen kasus SLE terjadi pada masa kanak-kanak. 3 Perkiraan keterlibatan ginjal pada penderita SLE adalah 30-90% pada penelitian yang dipublikasikan. Prevalensi nefritis lupus pada penderita SLE adalah sekitar 50% pada kelompok etnis tertentu dan pada anak-anak. Anak-anak dengan SLE mempunyai risiko penyakit ginjal yang lebih tinggi daripada orang dewasa 1,2,4
FAKTOR RISIKO
Terdapat beberapa faktor risiko terjadinya nefritis lupus, yaitu faktor genetik, lingkungan,hormonal, toksin dan infeksi.2
Tabel 3. Lokus gen yang berhubungan dengan SLE1
Lokus gen Nama gen Produk gen
1q21-q23 CRP C-reactive protein
1q23 FCGR2A, FCGR2B Fc γ RIIA (R131), Fc γ RIIB 1q23 FCGR3A, FCGR3B Fc γ RIIIA (V176), Fc γ RIIIB
1q31-q32 IL10 Interleukin-10 (IL–10)
1q36.12 C1QB Complement component 1, q subcomponent (C1q) deficiency
2q33 CTLA4 Cytotoxic T-lymphocyte-associated protein 4 (CTLA-4)
6p21.3 HLA-DRB1 HLA-DRB1: DR2/*1501, DR3/*0301C1q deficiency
6p21.3 C2, C4A, C4B C2, C4 deficiencies
6p21.3 TNF Tumor necrosis factor (TNF)–alpha (promoter, -308)
PENATALAKSANAAN1,2,3
• Umum
o Tujuan utama terapi nefritis lupus adalah mengoptimalkan fungsi ginjal dan
mencegah progresivitas kelainan ginjal.
o Biopsi ginjal pada pasien dengan nefritis lupus. o Asesmen indeks aktivitas dan kronisitas.
o Pengobatan manifestasi ekstrarenal dan factor lain yang dapat mempengaruhi
ginjal. • Pengobatan
o Terapi kortikosteroid diberikan apabila terdapat kelainan ginjal. Penggunaan
obat imunosupresif seperti cyclophosphamide, azathioprine, atau mofetil mycophenolate diberikan jika terdapat kelainan ginjal proliferatif agresif/ difus, dapat digunakan juga pada pasien yang tidak berespon dengan kortikosteroid atau terdapat kontra indikasi kortikosteroid.
o Terapi hipertensi dengan angiotensin-converting enzyme (ACE) inhibitor atau angiotensin II receptor blockers (ARBs) jika terdapat proteinuria tanpa insufiensi ginjal yang jelas.
o Restriksi diit lemak atau dengan menggunakan statin untuk hiperlipidemia.. o Restriksi diit protein apabila terdapat gangguan fungsi ginjal.
o Pemberian suplementasi kalsium untuk mencegah osteoporosis jika pasien
mendapatkan kortikosteroid jangka panjang dan penambahan biposponat sebagai binder pospat.
o Menghindari obat yang mempengaruhi fungsi ginjal, seperti NSAIDs,
terutama pada pasien dengan peningkatan kreatinin.
o Pasien dengan gagal ginjal terminal, sklerosis dan indeks kronisitas tinggi
berdasarkan biopsi ginjal tidak akan berespon dengan terapi agresif. Pada kasus seperti ini, terapi difokuskan terhadap manifestasi ekstra renal dan kemungkinan untuk transplantasi ginjal.
Pilihan terapi untuk pasien dengan nefritis lupus bervariasi tergantung pada kelainan histologis berdasarkan hasil biopsi ginjal.
Pasien dengan glomerulonefritis proliferatif mesangial II tidak memerlukan terapi khusus, karena mempunyai kemungkinan kecil untuk berkembang menjadi progresif. Meskipun demikian harus tetap dilakukan pemantauan rutin pada pasien agar kelainan ginjal tidak bertambah berat.
Terapi pasien dengan glomerulonefritis fokal segmental
Pasien dengan glomerulonefritis fokal segmental dengan kelainan glomerulus <20% memiliki prognosis jangka panjang yang baik. Pasien-pasien ini mungkin memerlukan pengobatan untuk kelainan di luar ginjal , tetapi tidak memerlukan terapi spesifik untuk kelainan ginjal. Sebaliknya jika terjadi kelainan glomerulus > 40% , perjalanan penyakit ini mirip dengan glomerulonefritis proliferatif difus, dengan terapi yang sama.
Terapi pasien dengan glomerulonefritis proliferatif difus
Pasien dengan glomerulonefritis proliferatif fokal aktif dan glomerulonefritis proliferatif difus mempunyai risiko tinggi menjadi penyakit ginjal stadium akhir apabila tidak mendapatkan terapi yang adekuat. Menurut Pollak dkk dosis tinggi kortikosteroid (prednison 1 sampai 2 mg / kg / hari) dapat memperbaiki glomerulonefritis proliferatif difus, sedangkan dosis rendah tidak efektif. Namun, dosis tinggi prednison oral dapat memberikan hasil jangka panjang yang buruk dan sering dikaitkan dengan efek samping yang serius. Banyak penulis telah mengusulkan terapi awal dengan pulse metilprednisolon intravena yang memiliki efek antiinflamasi dan imunosupresif yang lebih kuat dan cepat. Setelah pemberian pulse metilprednisolon, gejala ekstrarenal dan serum kreatinin mengalami perbaikan lebih cepat, sehingga dapat mengurangi komplikasi pengobatan steroid jangka panjang. Beberapa penelitian menunjukkan perbaikan secara signifikan jika siklofosfamid atau azathioprine ditambahkan ke kortikosteroid. Penambahan siklofosfamid atau azathioprine dapat menurunkan insiden gagal ginjal sebesar 40% dibandingkan dengan kortikosteroid saja. Tidak ada perbedaan dalam hal mortalitas antara kedua kelompok. Pada penelitian yang dilakukan Institut Kesehatan Nasional dari 111 pasien dengan nefritis lupus tidak terdapat perbedaan kejadian gagal ginjal selama 5 tahun pertama, setelah 5 tahun didapatkan kejadian gagal ginjal lebih tinggi secara signifikan pada kelompok yang menerima prednison saja dibandingkan dengan pasien yang diberi siklofosfamid intravena. Terdapat kecenderungan untuk hasil yang lebih baik pada pasien yang mendapatkan siklofosfamid intravena dibandingkan dengan siklofosfamid oral tunggal atau dengan kombinasi azathioprine, meskipun perbedaan tersebut secara statistik tidak signifikan. Terapi agresif dengan sitotoksik diindikasikan pada pasien yang berisiko tinggi menjadi gagal ginjal, peningkatan kreatinin
tubulointerstitial berat dan perubahan vascular. Cyclophosphamide diberikan secara pulse tiap bulan dengan dosis awal 750 mg/m2, dosis menjadi 1000 mg/m2 jika jumlah sel darah putih > 3000/mm3. Berdasarkan penelitian National Institute of Health dari 65 pasien dengan nefritis lupus berat didapatkan bahwa cyclophosphamide pulse lebih efektif dibandingkan dengan metilprednisolon pulse dalam mempertahankan fungsi ginjal dan penggunaan cyclophosphamide pulse dapat mengurangi risiko kekambuhan. Penelitian terbaru menunjukkan bahwa kombinasi metilprednisolon pulse dan cyclophosphamide pulse lebih efektif dalam jangka panjang dan kurang toksik dibandingkan dengan terapi tunggal. Terapi pada pasien dengan nefritis lupus berat adalah mulai dengan 3 kali metil prednisolon pulse dilanjutkan dengan prednison oral 1,5 mg / kg / hari dan 6 kali siklofosfamid pulse tiap bulan. Pada anak dengan penyakit ringan, pengobatan yang diberikan adalah metil prednisolon pulse intravena dilanjutkan dengan prednison oral dosis 1,0-1,5 mg/kg berat badan per hari. Setelah biopsi ginjal kedua dilakukan dan jika penyakit dapat dikendalikan, dapat diberikan azathioprine atau mikofenolat dengan tapering off prednison. Preparat tersebut menurunkan risiko neoplasia dan toksisitas kelenjar gonad dibandingkan dengan terapi siklofosfamid jangka panjang. Terdapat risiko kambuh jika terapi imunosupresif dihentikan sebelum 2 tahun jika terdapat proteinuria, karena itu kortikosteroid dan imunosupresif hanya boleh dihentikan setelah 3 tahun jika laju filtrasi glomerulus normal, proteinuria<1g/hari, dan sedimen urin inaktif.
Terapi relaps
Relaps didefinisikan sebagai memburuknya gejala ginjal. Beberapa pasien menunjukkan peningkatan kreatinin yang berhubungan dengan sedimen urin aktif dan proteinuria. Terdapatnya silinder eritrosit dan lekosit merupakan prediksi relaps ginjal. Peningkatan titer antibodi anti-DNA dan penurunan komplemen (C4 dan C3) sering dikaitkan dengan flare
ginjal, sehinggan parameter ini harus diperiksa secara berkala. Apabila fungsi ginjal mengalami perburukan, biopsi ginjal ulang dapat dilakukan mungkin untuk memutuskan penggantian terapi.
Terapi pasien dengan nefropati membranosa
Pasien dengan nefropati membrane murni, proteinuria ringan, dan fungsi ginjal normal memiliki prognosis baik, dan tanpa pengobatan khusus . Pengobatan pasien dengan sindrom nefrotik masih menjadi kontroversi. Pasien ini berisiko mempunyai komplikasi trombotik. Pasien dengan fungsi ginjal menurun harus dilakukan ulangan biopsi ginjal karena nefropati membran
Pendekatan terapi Lain
Plasmafaresis tidak dianjurkan karena tidak membantu pasien nefritis lupus. Immunoglobulin intravena efektif pada pasien, termasuk pasien dengan nefritis lupus proliferatif .
Dietetik
Pengelolaan diit spesifik pada tiap penderita tergantung dari penyakit yang menyertai, seperti jika terdapat hipertensi diberikan diit rendah garam, pada keadaan hiperlipidemia diberikan pembatasan lemak dan pada kelainan ginjal kronis diberikan protein 0,8-1,3 gram/kgbb/hari .
Prognosis
1,5• Prognosis buruk SLE pada
o Keterlambatan terapi lebih dari 5 bulan dari onset nefritis. o Usia muda saat onset nefritis
o Jenis kelamin laki-laki o Ras negro
o Hipertensi
o Sindrom Nefrotik
o Peningkatan kreatinin >3 mg/dL saat awal
o Peningkatan anti-dsDNA persisten, C3 dan C4 rendah.
o Biopsi ginjal nefritis lupus difus atau dengan indeks kronisitas tinggi
• Prognosis sangat baik pada Minimal mesangial lupus nephritis dan mesangial proliferative lupus nephritis (kelas I dan II).
• Prognosis baik : Focal lupus nephritis (kelas III), hanya sedikit pasien yang berkembang menjadi gagal ginjal terminal.
• Prognosis cukup baik
o Diffuse lupus nephritis (kelas IV) memberikan prognosis cukup baik, dengan sejumlah besar pasien berkembang menjadi gagal ginjal progresif..
o Membranous lupus nephritis (kelas V) dengan sejumlah besar pasien
mengalami kerusakan ginjal progresif secara bertahap
DAFTAR PUSTAKA
1. Brent L, Karhadkar A, Bloom E. Nefritis Lupus. Diunduh dari : http://emedicine.medscape.com/article/330369-print
2. Avner, Ellis D, Harmon, William E, Niaudet, Patrick. Systemic Lupus Erythematosus. Dalam: Barratt TM, Avner ED, Harmon WE, Penyunting. Pediatric Nephrology. Edisi 5. Baltimore Williams & Wilkins, 2004: 866-81.
3. Agrawal S. Lupus Nephritis : an Update on Pathogenesis. J Indian Rheumatol Assoc 2004 : 12:11-15
4. Weening J,dkk. The Classification of Glomerulonephritis in Systemic Lupus Erythematosus Revisited. J Am Soc Nephrol 15: 241–250, 2004
5. Schwartz M, Korbet S, Lewis E. The prognosis and pathogenesis of severe lupus glomerulonephritis. Nephrol Dial Transplant (2008) 23: 1298–1306