PEMANFAATAN Streptomyces spp. SEBAGAI AGEN
PENGENDALI HAYATI MIKROB PATOGEN PADA
TANAMAN TOMAT (Solanum lycopersicum)
ADI SASONO
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2010
ABSTRAK
ADI SASONO. Pemanfaatan Streptomyces spp. sebagai Agen Pengendali Hayati Mikrob Patogen pada Tanaman Tomat (Solanum lycopersicum). Dibimbing oleh YULIN LESTARI dan CHAERANI.
Streptomyces spp. merupakan salah satu bakteri antagonis yang dapat dimanfaatkan sebagai pengendali hayati mikrob patogen tanaman. Penelitian ini bertujuan mengkaji kemampuan dua isolat Streptomyces spp. (LSW05 dan PS4-16) dalam mengendalikan mikrob patogen tular tanah pada tanaman tomat di lapangan dan mendapatkan metode aplikasi Streptomyces spp. yang efektif. Kedua isolat diaplikasikan secara tunggal dan dikombinasikan antar keduanya dengan metode seed coating, penyiraman dan penyemprotan. Streptomyces spp. yang diaplikasikan efektif menekan keparahan penyakit, meningkatkan tinggi dan bobot kering tanaman serta bobot dan jumlah buah yang dihasilkan. Isolat LSW05 yang diaplikasikan secara penyiraman mampu menekan keparahan penyakit secara lebih baik dengan menurunkan nilai LADKP hingga 24% dan meningkatkan bobot kering tanaman hingga mencapai 187,10 %. Sementara itu, isolat LSW05 yang diaplikasikan secara seed coating mampu meningkatkan tinggi tanaman dengan meningkatkan nilai LADKT hingga 47,5% serta meningkatkan bobot dan jumlah buah total tertinggi berturut-turut 794 g/tanaman dan 14,3 buah/tanaman dibandingkan kontrol. Aplikasi Streptomyces isolat LSW05 secara seed coating memberikan keuntungan terbesar dibandingkan dengan perlakuan lain maupun tanpa aplikasi hingga mencapai Rp 75.244.600 per hektar lahan. Hasil penelitian ini memberikan prospek yang cerah dari Streptomyces sebagai agen biokontrol untuk diterapkan pada sistem pertanian organik.
Kata kunci: Streptomyces spp., pengendali hayati, mikrob patogen, tanaman tomat.
ABSTRACT
ADI SASONO. The Utilization of Streptomyces spp. as Biological Control Agent of Microbial Pathogens in Tomato Plants (Solanum lycopersicum). Supervised by YULIN LESTARI and CHAERANI.
Streptomyces spp. is one of the bacterial antagonists, which can be used to control microbial plant pathogens. Aims of this study were to examine the ability of two Streptomyces spp. isolates (LSW05 and PS4-16) in reducing tomato diseases in field and to obtain an effective application method. Both isolates were applied singly and in combination using three application methods (seed coating, soil drenching and spraying). Streptomyces spp. effectively suppressed disease severity, increased plant height, dry weight, fruit weight and fruit number per plant. LSW05 isolate applied as soil drenching suppressed disease severity by lowering the Area Under Disease Progress Curve (AUDPC) value up to 24% and increased the plant dry weight up to 187.10%. On the other hand, LSW05 isolate applied as seed coating improved plant height as measured by Area Under Height Growth Curve (AUHGC) up to 47.5% and increased fruit weight (794 g/plant) and fruit number (14,3 fruit/plant) as compared with control. Seed coating with Streptomyces LSW05 gave the highest benefit compared to the other treatments and non treatment up to Rp 75.244.600/ha. The results of this study provide a good prospect of Streptomyces based biocontrol agent to be applied to organic farming system.
PEMANFAATAN Streptomyces spp. SEBAGAI AGEN
PENGENDALI HAYATI MIKROB PATOGEN PADA
TANAMAN TOMAT (Solanum lycopersicum)
ADI SASONO
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2010
Judul Skripsi : Pemanfaatan Streptomyces spp. sebagai Agen Pengendali Hayati Mikrob
Patogen pada Tanaman Tomat (Solanum lycopersicum)
Nama : ADI SASONO NIM : G 3405 3723
Menyetujui :
Mengetahui : Ketua Departemen Biologi
Institut Pertanian Bogor
Tanggal Lulus :
Pembimbing I
(Dr. Ir. Yulin Lestari) NIP. 19620710 198803 2 002
Pembimbing II
(Dr. Ir. Chaerani, M.Sc) NIP. 19670406 199303 2 002
(Dr. Ir. Ence Darmo Jaya Supena M.Si) NIP. 19641002 198903 1 002
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah SWT yang telah melimpahkan rahmat, kesehatan dan kekuatan sehingga penulis dapat menyelesaikan karya ilmiah yang berjudul Pemanfaatan Streptomyces spp. sebagai Agen Pengendali Hayati Mikrob Patogen pada Tanaman Tomat (Solanum lycopersicum).Penelitian ini dilaksanakan dari bulan Januari hingga September 2009 di Laboratorium Mikrobiologi Departemen Biologi, FMIPA IPB dan Lahan Pertanian Organik Resor Permata Hati, Cisarua, Bogor.
Terima kasih sebesar-besarnya penulis ucapkan kepada Dr. Ir. Yulin Lestari dan Dr. Ir. Chaerani, M.Si yang telah memberikan bimbingan, saran, motivasi dan fasilitas selama penelitian dan penyusunan karya ilmiah ini serta Dr. Ir. Tatik Chikmawati, MSi. selaku Wakil Komisi Pendidikan yang telah memberikan saran dan kritikannya.Penulis juga mengucapkan terima kasih kepada kedua orang tua, kakak dan adik yang telah memberikan kasih sayang yang melimpah dan dorongan materil maupun moril sehingga penulis dapat menyelesaikan pendidikan.Terima kasih secara khusus penulis ucapkan kepada Bapak Asep Miswan yang telah membantu teknis pelaksanaan penelitian di lapangan dan informasi-informasi yang telah diberikan, Ibu Tini dari Laboratorium Mikroteknik atas bantuannya dalam menggunakan fotomikroskop, Mba Asti dari Laboratorium Mikologi yang telah mengajari penulis dalam pembuatan preparat cendawan patogen, segenap staf dan laboran di Laboratorium Mikrobiologi, Ibu Ratih DH, Pak S. Pujianto, Yohanna AW, Ika Rezza R, Dmitry & Ester, Femi AZ, Vina V, Hirmas FP, Akbar AP, serta teman-teman dari Laboratorium Mikrobiologi atas bantuan dan kerja samanya.
Semoga karya ilmiah ini bermanfaat. Amin.
Bogor, Februari 2010
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 21 Mei 1987 sebagai anak ketiga dari lima bersaudara, putra pasangan Adi Purwanto dan Siti Alifah. Tahun 2005 penulis lulus dari SMA Negeri 84 Jakarta dan pada tahun yang sama penulis diterima di IPB melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB).
Selama mengikuti perkuliahan, penulis aktif menjadi asisten praktikum, diantaranya Biologi Dasar (2007/2008, 2008/2009 dan 2009/2010), Mikrobiologi Dasar (2009/2010) dan Fisiologi Tumbuhan (2009/2010). Pada tahun 2007, proposal penulis lolos dalam Program Kreativitas Mahasiswa Ilmiah (PKMI) dengan judul “Isolasi dan Karakterisasi Bakteri Selulolitik dan Xilanolitik Asal Wana Wisata Cangkuang, Sukabumi”. Penulis melaksanakan praktek kerja lapang pada bulan Juli - Agustus 2008 dengan judul “Analisis Mutu Mikrobiologis Bir Bintang di PT. Multi Bintang Indonesia, Tbk”. Pada tahun 2009, proposal penulis lolos dalam Program Kreativitas Mahasiswa Penelitian (PKMP) dengan judul “Prospek Pemanfaatan Streptomyces spp. sebagai Agen Pengendali Hayati Penyakit Tular Tanah pada Tanaman Tomat (Solanum lycopersicum) dan Cabai Besar (Capsicum anuum).
DAFTAR ISI
HalamanDAFTAR TABEL ... viii
DAFTAR GAMBAR ... viii
DAFTAR LAMPIRAN ... viii
PENDAHULUAN Latar Belakang ... 1
Tujuan ... 1
Waktu dan Tempat ... 1
BAHAN DAN METODE Bahan dan Alat ... 1
Metode ... 1
Peremajaan dan Produksi Inokulum Streptomyces spp ... 1
Persiapan Tanam dan Lahan ... 2
Aplikasi Streptomyces spp ... 2
Rancangan Percobaan ... 2
Pengamatan ... 2
Analisis Statistik ... 3
Analisis Usaha Tani Tomat ... 3
Analisis Kandungan NPK Tanah Percobaan ... 3
Penghitungan Populasi Aktinomiset dan Identifikasi Keragaman Aktinomiset Lokal ... 3
Isolasi dan Identifikasi Cendawan yang Diduga Patogen Tanaman ... 3
HASIL Keparahan Penyakit pada Daun ... 3
Tinggi Tanaman ... 4
Produksi Buah ... 4
Bobot Kering Tanaman ... 6
Analisis Usaha Tani Tomat ... 6
Analisis Kandungan NPK Tanah Percobaan ... 7
Penghitungan Populasi Aktinomiset dan Identifikasi Keragaman Aktinomiset Lokal ... 7
Isolasi dan Identifikasi Cendawan yang Diduga Patogen Tanaman ... 8
PEMBAHASAN ... 8
SIMPULAN ... 10
SARAN ... 10
DAFTAR TABEL
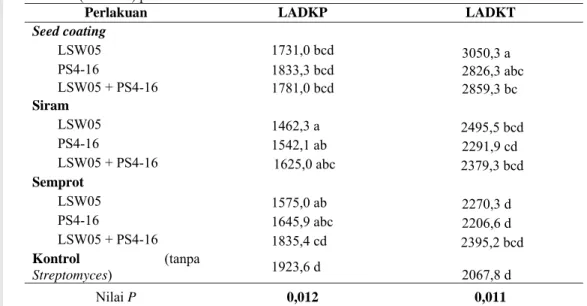
Halaman 1 Pengaruh aplikasi Streptomyces terhadap luasan area di bawah kurva perkembangan
penyakit (LADKP) dan luasan area di bawah kurva perkembangan tinggi tanaman
(LADKT) pada tanaman tomat berumur 70 HST ... 5
2 Pengaruh aplikasi Streptomyces terhadap bobot buah grade A, B, dan C serta bobot buah total per tanaman ... 5
3 Pengaruh aplikasi Streptomyces terhadap jumlah buah grade A, B, dan C serta jumlah buah total per tanaman... 6
4 Pengaruh aplikasi Streptomyces terhadap bobot kering tanaman ... 6
5 Analisis usaha tani tomat per hektar ... 7
DAFTAR GAMBAR
Halaman 1 Sampel daun yang terinfeksi penyakit. Daun tanaman kontrol tanpa Streptomyces (a), daun tanaman yang diberi Streptomyces isolat LSW05 dengan metode seed coating (b), penyiraman (c) dan penyemprotan (d) ... 42 Perbedaan kualitas buah tomat; grade A (a), grade B (b) dan grade C (c) ... 4
3 Populasi aktinomiset ... 7
4 Koloni aktinomiset pada media HV agar (a) dan isolat murni aktinomiset pada media ISP 2 (b) ... 7
5 Gejala penyakit yang menyerang tanaman. Tanaman yang terserang penyakit (a), gejala pada batang (b) : batang berwarna coklat (b1), batang membusuk dan patah (b2), gejala pada daun (c) dan gejala pada buah (d) ... 8
DAFTAR LAMPIRAN
Halaman 1 Tabel komposisi media per liter ... 132 Pengaruh aplikasi Streptomyces terhadap luasan area di bawah kurva perkembangan penyakit (LADKP) pada tanaman tomat pada tujuh periode pengamatan ... .... 14
3 Pengaruh aplikasi Streptomyces terhadap luasan area di bawah kurva perkembangan tinggi tanaman (LADKT) pada tanaman tomat pada tujuh periode pengamatan ... 14
4 Analisis biaya usaha tani tanaman tomat per hektar ... 15
5 Hasil analisis NPK tanah percobaan ... 17
6 Tata letak plot percobaan ... 17
7 Deskripsi tanaman tomat varietas Arthaloka ... 18
8 Keragaman aktinomiset di Lahan Pertanian Organik Resor Permata Hati Cisarua ... 19
9 Keragaman koloni (a) dan mikroskopis (b) aktinomiset di Lahan Pertanian Organik Resor Permata Hati Cisarua ... 20
PENDAHULUAN
Latar BelakangTomat (Solanum lycopersicum) merupakan salah satu komoditas hortikultura yang penting dan bernilai ekonomi tinggi namun produksinya masih rendah (Wijayani & Widodo 2005). Rata-rata produksi tomat Indonesia tahun 2008 mencapai 689.420 ton/tahun dengan produktivitas 13,82 ton/ha (BPS dan Dirjen BPH 2008). Produksi ini masih sangat rendah bila dibandingkan dengan produksi tomat di negara Cina, Amerika dan India yang masing-masing mencapai 37,5 juta ton (USDA FAS 2008), 36,84 juta ton (USDA ERS 2007) dan 25 juta ton (IPNI 2008).
Salah satu penyebab rendahnya produktivitas tanaman tomat di Indonesia adalah serangan mikrob patogen. Menurut Semangun (1994), beberapa mikrob patogen yang menyerang tanaman tomat antara lain: Fusarium oxysporum (layu Fusarium), Phytophthora infestans (hawar daun), Sclerotium rolfsii dan Rhizoctonia solani (rebah kecambah), Colletotrichum capsici (antraknosa) dan Rasltonia solanacearum (layu bakteri). Kehilangan hasil produksi tomat yang disebabkan oleh penyakit layu Fusarium diperkirakan mencapai 10-40%, hawar daun 10-100% (Suryaningsih et al. 1999), antraknosa 5-20% dan layu bakteri 4-10% (Adiyoga et al. 2007).
Mikrobisida kimiawi efektif membasmi mikrob patogen namun penggunaannya telah dibatasi karena dampak negatif yang ditimbulkan (Widarto 2008). Pada pertanian organik, penggunaan mikrobisida kimiawi tersebut sangat dihindari. Salah satu cara alternatif pengendalian mikrob patogen adalah secara hayati dengan mikrob antagonis yang berasal dari tanah, antara lain dengan Streptomyces spp. Streptomyces dikenal memiliki kemampuan yang tinggi dalam menghasilkan berbagai senyawa bioaktif yang potensial untuk menghambat pertumbuhan mikrob patogen (Lestari 2006).
Beberapa peneliti melaporkan kemampuan Streptomyces spp. sebagai pengendali mikrob patogen tanaman, antara lain Rhizoctonia sp. pada tomat (Sabaratnam & Traquaira 2002), P. dreschsleri pada kenari (Bonjar et al. 2006), F. solani pada gula bit (Moussa & Rizk 2002) dan C. gloeosporioides pada anggrek (Prapagdee et al. 2008). Streptomyces isolat lokal juga dilaporkan mampu menghambat serangan S.
rolfsii pada tomat (Yusniawati 2009) dan cabai (Papuangan 2009), R. solanacearum pada tanaman cabai (Muthahanas 2004) dan Xanthomonas axonopodis pada kedelai (Ifdal 2003, Andri 2004). Berdasarkan kemampuannya tersebut, maka pemanfaatan Streptomyces spp. isolat lokal sebagai agen pengendali hayati mikrob patogen tular tanah di lapangan perlu dilakukan.
Tujuan
Penelitian bertujuan mengkaji kemampuan Streptomyces spp. dalam mengendalikan mikrob patogen pada tanaman tomat di lapangan dan mendapatkan metode aplikasi Streptomyces spp. yang efektif.
Waktu dan Tempat
Penelitian berlangsung dari bulan Januari hingga September 2009 bertempat di Laboratorium Mikrobiologi Departemen Biologi, FMIPA, IPB dan Lahan Pertanian Sayuran Organik Resor Permata Hati, Cisarua.
BAHAN DAN METODE
Bahan dan AlatBahan yang digunakan adalah dua isolat Streptomyces spp. (LSW05 dan PS4-16), benih tomat varietas Arthaloka (deskripsi pada Lampiran 7), media modifikasi molase-kedelai, Humic Acid Vitamin-B Agar (HV Agar), Oatmeal Agar (OA), International Streptomyces Project (ISP) no.2, Potato Dextrose Agar (PDA) (Lampiran 1), antibiotik cycloheximide dan nalidixic acid, alkohol 70%, NaOCl 0,5%, larutan NaCl 0,85 % dan tepung kanji.
Alat yang digunakan adalah inkubator bergoyang, autoklaf, mikroskop cahaya, centrifuge, laminar air flow, handsprayer, timbangan, meteran, kamera digital dan peralatan umum di laboratorium mikrobiologi.
Metode
Peremajaan dan Produksi Inokulum Streptomyces spp.
Streptomyces isolat LSW05 dan PS4-16 diremajakan berturut-turut pada media ISP no.2 dan OA selama 14 hari pada suhu ruang. Inokulum Streptomyces diproduksi dalam 1,8 liter media modifikasi molase-kedelai dalam botol bekas air mineral berkapasitas 19 liter. Media diinokulasi dengan 144 bulatan koloni Streptomyces spp. berdiameter 8 mm yang diambil dengan sedotan steril. Inkubasi dilakukan pada suhu ruang menggunakan
inkubator bergoyang dengan kecepatan 120 rpm selama 10 hari.
Persiapan Tanam dan Lahan
Benih tomat disemai di bak persemaian selama 21 hari sebelum ditanam di lahan percobaan. Tiga hari sebelum tanam, tanah diolah dan dicampur dengan kompos dengan perbandingan 3:1. Plot percobaan berupa bedengan berukuran 1 m x 3,5 m berisi 8 tanaman dengan jarak tanam antar barisan 70 cm dan jarak di dalam barisan 50 cm. Jarak antar plot diisi dengan 2 tanaman tanpa perlakuan Streptomyces yang berfungsi sebagai border. Tata letak plot percobaan dapat dilihat pada lampiran 6.
Aplikasi Streptomyces spp.
Kedua isolat diaplikasikan secara tunggal dan dikombinasikan antar keduanya dengan metode seed coating, penyiraman dan penyemprotan.
Seed coating. Kultur isolat Streptomyces spp. disentrifugasi dengan kecepatan 4000 rpm pada suhu 4 oC selama 20 menit. Dua
gram massa sel Streptomyces disuspensikan dalam 10 ml larutan kanji 2% steril (konsentrasi akhir 0,2 g massa sel/ml) dengan bantuan magnetic stirer selama lima menit untuk memperoleh konsistensi yang seragam. Biji tomat (100 biji) yang telah disterilisasi permukaan dengan alkohol 70% selama 1 menit, NaOCl 0,5% 1 menit dan dibilas tiga kali dengan akuades steril, direndam dalam 2 ml suspensi Streptomyces spp. dan larutan kanji selama 30 menit kemudian dikering-anginkan dalam laminar air flow. Biji kemudian disemai. Aplikasi dengan kombinasi isolat menggunakan massa sel Streptomyces separuh dari konsentrasi masing-masing isolat, yaitu 0,1 g massa sel/ml isolat LSW05 ditambah 0,1 g massa sel/ml isolat PS4-16.
Penyiraman. Kultur Streptomyces spp. disiramkan di sekitar perakaran sebanyak 25 ml per tanaman.
Penyemprotan. Kultur Streptomyces spp. disemprotkan pada permukaan daun dan batang sebanyak 25 ml per tanaman.
Pada metode penyiraman dan penyemprotan Streptomyces spp. diaplikasikan seminggu sekali dimulai pada saat tanaman berumur 28 hari setelah tanam (HST) hingga tanaman berumur 56 HST.
Rancangan Percobaan
Percobaan disusun berdasarkan Rancangan Acak Kelompok (RAK) dengan 9 perlakuan yang terdiri dari:
1.
Seed coating dengan Streptomyces isolat LSW052. Seed coating dengan Streptomyces isolat PS4-16
3. Seed coating dengan kombinasi Streptomyces isolat LSW05 dan PS4-16
4. Penyiraman dengan Streptomyces isolat LSW05
5. Penyiraman dengan Streptomyces isolat PS4-16
6. Penyiraman dengan kombinasi Streptomyces isolat LSW05 dan PS4-16
7. Penyemprotan dengan Streptomyces isolat LSW05
8. Penyemprotan dengan Streptomyces isolat PS4-16
9. Penyemprotan dengan kombinasi Streptomyces isolat LSW05 dan PS4-16
Tanaman yang tidak diberi perlakuan Streptomyces digunakan sebagai kontrol. Tiap perlakuan dan kontrol diulang tiga kali. Keterbatasan lahan tidak memungkinkan percobaan dilaksanakan dalam satu hamparan, tetapi terbagi dalam tiga hamparan. Tiap hamparan merupakan satu ulangan.
Pengamatan
Pengamatan dilakukan setiap minggu dimulai saat tanaman berumur 28 HST hingga 70 HST dengan parameter yang diamati berupa keparahan penyakit pada daun, tinggi tanaman, bobot kering tanaman dan produksi buah meliputi bobot dan jumlah buah grade A (>100 g/buah), B (50-100 g/buah), C (<50 g/buah) serta produksi buah total.
Keparahan penyakit pada daun dinilai berdasarkan sistem skoring sebagai berikut (Christ 1991):
0 = tidak ada gejala 1 = 1% kanopi terinfeksi 2 = 2-5 % kanopi terinfeksi 3 = 6-10% kanopi terinfeksi 4 = 11-25% kanopi terinfeksi 5 = 26-50% kanopi terinfeksi 6 = 51-75% kanopi terinfeksi 7 = 76-100% kanopi terinfeksi
Skor penyakit digunakan untuk menghitung intensitas penyakit (Ri) dengan
menggunakan rumus (Kuswinanti 2006) :
Ri = intensitas penyakit
a = nilai skor penyakit tiap tanaman N = jumlah tanaman dengan nilai skor
tertentu
Intensitas penyakit kumulatif dikonversi menjadi luasan area di bawah kurva perkembangan penyakit (LADKP) dengan rumus (Christ & Haynes 2001) :
Ri = intensitas penyakit
ti = waktu pengamatan
n = jumlah pengamatan
Rata-rata tinggi tanaman diperoleh dengan rumus :
TT = Tinggi tanaman
Tinggi tanaman kumulatif dikonversi menjadi luasan area di bawah kurva perkembangan tinggi tanaman (LADKT) menggunakan rumus sama seperti perhitungan LADKP.
Analisis Statistik
Data hasil pengamatan dianalisis menggunakan prosedur Generalized Linier Model (GLM) dari software SPSS 12,0. Beda nyata antar perlakuan diuji menggunakan uji jarak berganda Duncan pada taraf 5%.
Analisis Usaha Tani Tomat
Analisis biaya dilakukan untuk mengetahui pengaruh perlakuan Streptomyces spp. terhadap keuntungan yang diperoleh.
Analisis Kandungan NPK Tanah Percobaan
Sampel tanah diambil sebelum tanam menggunakan sekop pada kedalaman 5-10 cm pada lima titik dalam tiap plot percobaan kemudian dicampurkan. Analisis dilakukan di Laboratorium Biokimia/Kimia, BB Biogen.
Penghitungan Populasi Aktinomiset dan Identifikasi Keragaman Aktinomiset Lokal
Sebanyak 50 g sampel tanah dari setiap plot percobaan diambil kemudian dicampur hingga merata. Sampel tanah diambil pada masa sebelum tanam, setelah aplikasi dan setelah panen untuk mengetahui dinamika populasi mikroorganisme tanah.
Satu gram sampel tanah diencerkan serial sampai seri 10-4 menggunakan tabung reaksi
berisi 9 ml larutan NaCl 0,85% kemudian 0,1 ml suspensi disebar pada media Humic Acid Vitamin-B Agar (HV Agar). Media diinkubasi pada suhu ruang selama 14 hari. Jumlah koloni aktinomiset yang tumbuh dihitung kemudian dimurnikan pada media ISP 2 untuk diidentifikasi dan disimpan sebagai kultur koleksi. Identifikasi dilakukan melalui pengamatan mikroskopis dan makroskopis serta karakterisasi koloni dengan berpedoman padaAtlas of Actinomycetes (Miyadoh 1997).
Isolasi dan Identifikasi Cendawan yang Diduga Patogen Tanaman
Jaringan yang terinfeksi disterilisasi permukaan dengan NaOCl 0,5% 1 menit kemudian dibilas dengan akuades steril 1 menit. Jaringan yang sudah steril dipotong (2 mm x 2 mm) dan ditanam pada media PDA. Media diinkubasi pada suhu ruang selama 3 hari (Windels 1993). Cendawan yang tumbuh dimurnikan kembali pada media PDA dan disimpan sebagai kultur koleksi.
Identifikasi cendawan dilakukan melalui pengamatan langsung terhadap gejala yang muncul pada tanaman yang terinfeksi dan pengamatan mikroskopis morfologi koloni pada media PDA dengan berpedoman pada Barnett & Hunter (1972).
HASIL
Keparahan Penyakit pada DaunSerangan penyakit mulai terlihat saat tanaman berumur 21 HST. Perlakuan Streptomyces berpengaruh nyata (P<0,05) menekan tingkat keparahan penyakit mulai 49 hingga 70 HST (Tabel 1, Lampiran 2). Semua perlakuan dapat menekan penyakit dibandingkan kontrol dengan nilai LADKP yang bervariasi. Penyiraman dengan Streptomyces isolat LSW05 merupakan perlakuan terbaik dalam menekan keparahan penyakit dengan menurunkan nilai LADKP hingga 24% pada 70 HST (Tabel 1).
Penurunan nilai LADKP pada metode penyiraman dengan Streptomyces isolat LSW05 lebih tinggi bila dibandingkan dengan Ri = a1N1 + a2N2 + … + anNn x 100%
7 x jumlah tanaman
TT = ∑ tinggi tanaman x 100% ∑ jumlah tanaman
nilai LADKP pada metode seed coating dan semprot menggunakan isolat yang sama. Hal serupa juga ditunjukkan oleh nilai LADKP pada metode penyiraman menggunakan isolat yang berbeda. Kemampuan Streptomyces isolat LSW05 dalam menekan keparahan penyakit menurun jika diaplikasikan secara kombinasi dengan isolat PS4-16. Perbedaan intensitas penyakit antara tanaman kontrol dengan tanaman yang diberi Streptomyces spp. dapat dilihat pada Gambar 1.
Tinggi Tanaman
Perlakuan Streptomyces berpengaruh nyata (P=0,011) dalam meningkatkan tinggi tanaman dibandingkan kontrol pada 70 HST (Tabel 1). Pada semua periode pengamatan, tanaman tomat yang diberi perlakuan secara nyata lebih tinggi daripada tanaman kontrol (Lampiran 3). Streptomyces isolat LSW05 yang diaplikasikan dengan metode seed coating mampu meningkatkan tinggi tanaman secara lebih baik dengan meningkatkan nilai LADKT hingga 47,5% pada 70 HST.
Peningkatan nilai LADKT oleh isolat LSW05 dengan metode seed coating menurun jika diaplikasikan dengan metode penyiraman dan penyemprotan. Hasil ini berbeda dengan parameter keparahan penyakit dimana isolat LSW05 mampu menekan keparahan penyakit secara lebih baik jika diaplikasikan dengan metode penyiraman. Sementara itu, kemampuan isolat PS4-16 dan kombinasi isolat LSW05+PS4-16 yang diaplikasikan dengan metode seed coating ternyata lebih rendah dalam meningkatkan tinggi tanaman bila dibandingkan dengan isolat LSW05 pada metode yang sama dengan nilai LADKT
berturut-turut sebesar 2826,3, 2859,3 dan 3050,3.
Produksi Buah
Pemanenan dilakukan saat tanaman berumur 70 hingga 93 HST. Buah yang dipanen berwarna kuning kemerahan. Buah kemudian dikelompokkan ke dalam tiga tipe kualitas, yaitu grade A, B dan C. Buah grade A dijual dengan harga Rp 10.000/kg, grade B Rp 7.000/kg dan grade C Rp 2.000/kg.
Perlakuan Streptomyces tidak berpengaruh nyata terhadap bobot buah pada kelompok kualitas manapun dan bobot buah total namun cenderung lebih baik dibandingkan kontrol (Tabel 2). Rata-rata tanaman yang diberi perlakuan Streptomyces menghasilkan bobot buah grade A yang lebih tinggi 25-52% dibandingkan kontrol (77 g per tanaman) kecuali perlakuan penyiraman dengan Streptomyces isolat PS4-16 (70 g per tanaman) dan penyemprotan dengan kombinasi Streptomyces isolat LSW05+PS4-16 (46 g per tanaman).
Semua perlakuan menghasilkan buah grade B dan buah total dengan bobot yang lebih tinggi daripada kontrol. Namun beberapa perlakuan menghasilkan buah dengan grade C yang lebih rendah daripada kontrol, antara lain perlakuan seed coating dengan Streptomyces isolat PS4-16 dan kombinasi Streptomyces isolat LSW05+PS4-16, penyiraman dengan Streptomyces isolat PS4-16, penyemprotan dengan Streptomyces isolat LSW05 dan isolat PS4-16. Perlakuan seed coating dengan Streptomyces isolat LSW05 menghasilkan bobot buah dengan grade A, B, C dan buah total tertinggi berturut-turut sebesar 118 g, 487`g, 188 g dan
794 g per tanaman.
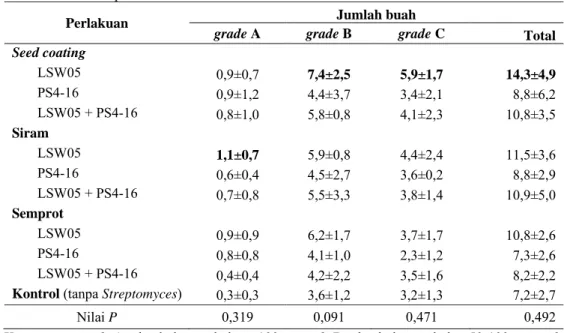
Pada parameter jumlah buah perlakuan juga tidak berpengaruh nyata, baik terhadap jumlah buah grade A, B, dan C maupun jumlah buah total. Namun demikian, meskipun secara statistik tidak berpengaruh nyata, semua perlakuan menghasilkan jumlah buah dengan grade A, B, dan C serta buah Gambar 1 Sampel daun yang terinfeksi
penyakit. Daun tanaman kontrol tanpa Streptomyces (a), daun tanaman yang diberi Streptomyces isolat LSW05 dengan metode seed coating (b), penyiraman (c) dan penyemprotan (d).
c
d
b
a
Gambar 2 Perbedaan kualitas buah tomat ; grade A (a), grade B (b) dan grade C (c).
total yang lebih banyak dibandingkan kontrol (Tabel 3).
Untuk buah dengan grade A, jumlah buah terbanyak dihasilkan pada perlakuan penyiraman dengan Streptomyces isolat LSW05 yaitu sebanyak 1,1 buah per tanaman. Sementara untuk jumlah buah grade B, grade C dan jumlah buah total terbanyak dihasilkan pada perlakuan seed coating dengan
Streptomyces isolat LSW05, berturut-turut sebanyak 7,4 buah, 5,9 buah dan 14,3 buah per tanaman. Jumlah buah dengan grade C paling sedikit dihasilkan pada perlakuan penyemprotan dengan Streptomyces isolat PS4-16, yaitu sebanyak 2,3 buah per tanaman. Jumlah ini lebih kecil dibandingkan kontrol yang mencapai 3,2 buah per tanaman. Tabel 1 Pengaruh aplikasi Streptomyces terhadap luasan area di bawah kurva perkembangan
penyakit (LADKP) dan luasan area di bawah kurva perkembangan tinggi tanaman (LADKT) pada tanaman tomat berumur 70 HST
Perlakuan LADKP LADKT Seed coating LSW05 1731,0 bcd 3050,3 a PS4-16 1833,3 bcd 2826,3 abc LSW05 + PS4-16 1781,0 bcd 2859,3 bc Siram LSW05 1462,3 a 2495,5 bcd PS4-16 1542,1 ab 2291,9 cd LSW05 + PS4-16 1625,0 abc 2379,3 bcd Semprot LSW05 1575,0 ab 2270,3 d PS4-16 1645,9 abc 2206,6 d LSW05 + PS4-16 1835,4 cd 2395,2 bcd Kontrol (tanpa Streptomyces) 1923,6 d 2067,8 d Nilai P 0,012 0,011
Keterangan : Angka yang diikuti oleh huruf yang sama pada kolom yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan pada taraf 5%.
Tabel 2 Pengaruh aplikasi Streptomyces terhadap bobot buah grade A, B, dan C serta bobot buah total per tanaman
Perlakuan Bobot buah (g)
grade A grade B grade C Total Seed coating LSW05 118±106 487±178 188±44 794±308 PS4-16 98±136 317±295 124±84 539±483 LSW05 + PS4-16 100±109 381±91 122±81 604±257 Siram LSW05 105±75 347±81 128±61 581±182 PS4-16 70±50 329±228 129±8 529±279 LSW05 + PS4-16 75±81 348±237 113±51 537±358 Semprot LSW05 97±107 316±25 116±11 530±124 PS4-16 97±99 250±75 94±38 442±186 LSW05 + PS4-16 46±41 273±149 133±58 453±194
Kontrol (tanpa Streptomyces) 77±93 215±220 126±60 420±363
Nilai P 0,489 0,291 0,626 0,921 Keterangan: grade A = buah dengan bobot >100 g; grade B = buah dengan bobot 50-100 g; grade
Tabel 3 Pengaruh aplikasi Streptomyces terhadap jumlah buah grade A, B, dan C serta jumlah buah total per tanaman
Perlakuan Jumlah buah
grade A grade B grade C Total Seed coating LSW05 0,9±0,7 7,4±2,5 5,9±1,7 14,3±4,9 PS4-16 0,9±1,2 4,4±3,7 3,4±2,1 8,8±6,2 LSW05 + PS4-16 0,8±1,0 5,8±0,8 4,1±2,3 10,8±3,5 Siram LSW05 1,1±0,7 5,9±0,8 4,4±2,4 11,5±3,6 PS4-16 0,6±0,4 4,5±2,7 3,6±0,2 8,8±2,9 LSW05 + PS4-16 0,7±0,8 5,5±3,3 3,8±1,4 10,9±5,0 Semprot LSW05 0,9±0,9 6,2±1,7 3,7±1,7 10,8±2,6 PS4-16 0,8±0,8 4,1±1,0 2,3±1,2 7,3±2,6 LSW05 + PS4-16 0,4±0,4 4,2±2,2 3,5±1,6 8,2±2,2
Kontrol (tanpa Streptomyces) 0,3±0,3 3,6±1,2 3,2±1,3 7,2±2,7
Nilai P 0,319 0,091 0,471 0,492 Keterangan: grade A = buah dengan bobot >100 g; grade B = buah dengan bobot 50-100 g; grade
C = buah dengan bobot <50 g.
Bobot Kering Tanaman
Bobot kering tanaman diukur setelah panen yaitu pada saat tanaman berumur 93 HST. Perlakuan secara nyata (P=0,000) meningkatkan bobot kering tanaman dibandingkan kontrol (Tabel 4).
Tabel 4 Pengaruh aplikasi Streptomyces terhadap bobot kering tanaman
Perlakuan Bobot kering (g)* Seed coating LSW05 38,4±4,2 bc PS4-16 32,3±6,4 cde LSW05+PS4-16 37,2±4,4 bcd Siram LSW05 53,4±9,0 a PS4-16 44,8±9,2 ab LSW05+ PS4-16 46,7±9,1 ab Semprot LSW05 29,0±2,7 c-f PS4-16 24,3±5,3 ef LSW05+ PS4-16 25,4±4,4 def Kontrol (tanpa Streptomyces) 18,6±5,1 f Nilai P 0,000
* Angka yang diikuti oleh huruf yang sama tidak berbeda nyata berdasarkan uji jarak berganda Duncan pada taraf 5%.
Bobot kering tanaman tertinggi diperoleh pada perlakuan penyiraman dengan Streptomyces isolat LSW05 sebesar 53,4 g. Perlakuan ini meningkatkan bobot kering tanaman hingga mencapai 187,10 %
dibandingkan kontrol (18,6 g). Peningkatan bobot kering tanaman yang diberi perlakuan Streptomyces berbanding terbalik dengan tingkat keparahan penyakit. Tanaman kontrol dengan tingkat keparahan penyakit paling tinggi menghasilkan bobot kering paling rendah.
Analisis Usaha Tani Tomat
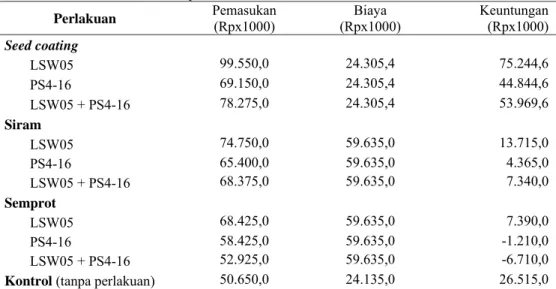
Keuntungan per tanaman dikonversi ke dalam satu hektar lahan berisi 20.000 tanaman. Rata-rata Streptomyces yang diaplikasikan dengan metode seed coating mampu meningkatkan keuntungan yang diperoleh 69-183% dibandingkan tanpa aplikasi Streptomyces (Tabel 5). Keuntungan terbesar diperoleh dari perlakuan seed coating dengan Streptomyces isolat LSW05 yang mencapai Rp 75.244.600 per hektar atau meningkat 183% dibandingkan tanpa aplikasi Streptomyces yang hanya memperoleh keuntungan sebesar Rp 26.515.000 per hektar.
Sementara itu, Streptomyces yang diaplikasikan dengan dua metode lainnya ternyata kurang menguntungkan bahkan keuntungan yang diperoleh pada kedua metode aplikasi ini masih lebih rendah daripada tanpa aplikasi. Hal ini disebabkan oleh tingginya biaya yang harus dikeluarkan selama aplikasi dibandingkan tanpa aplikasi, antara lain biaya produksi inokulum Streptomyces dan biaya tenaga kerja untuk aplikasi tersebut (Lampiran 4).
Tabel 5 Analisis usaha tani tomat per hektar*
Perlakuan Pemasukan (Rpx1000) (Rpx1000) Biaya Keuntungan (Rpx1000) Seed coating LSW05 99.550,0 24.305,4 75.244,6 PS4-16 69.150,0 24.305,4 44.844,6 LSW05 + PS4-16 78.275,0 24.305,4 53.969,6 Siram LSW05 74.750,0 59.635,0 13.715,0 PS4-16 65.400,0 59.635,0 4.365,0 LSW05 + PS4-16 68.375,0 59.635,0 7.340,0 Semprot LSW05 68.425,0 59.635,0 7.390,0 PS4-16 58.425,0 59.635,0 -1.210,0 LSW05 + PS4-16 52.925,0 59.635,0 -6.710,0
Kontrol (tanpa perlakuan) 50.650,0 24.135,0 26.515,0
* Hasil konversi dari keuntungan yang diperoleh per tanaman ke dalam satu hektar lahan berisi 20.000 tanaman.
Analisis Kandungan NPK Tanah Percobaan
Jenis tanah percobaan tergolong anisol dengan kandungan nitrogen (N) pada ulangan 1 dan 2 tergolong tinggi, berturut-turut 0,589% dan 0,603%, sedangkan pada ulangan 3 tergolong sedang (0,477%). Kandungan fosfor (P) pada ketiga ulangan sangat rendah, berturut-turut 8,337 mg/100g, 8,066 mg/100g dan 7,877 mg/100g. Kandungan kalium (K) pada ketiga ulangan sangat tinggi berturut-turut sebesar 73,229 mg/100g, 75,969 mg/100g dan 80,129 mg/100g. Hasil analisis tanah percobaan dapat dilihat di Lampiran 5.
Penghitungan Populasi Aktinomiset dan Identifikasi Keragaman Aktinomiset Lokal
Populasi aktinomiset meningkat selama aplikasi dari 5,98x105 sel/g tanah sebelum
aplikasi menjadi 2,69x106 sel/g tanah setelah
aplikasi dan 2,91x106 sel/g setelah panen
(Gambar 3).
Dari hasil isolasi dan pemurnian aktinomiset dari tanah diperoleh 40 isolat yang sangat beragam. Keragaman aktinomiset hasil isolasi tampak jelas pada konsistensi, pigmentasi, permukaan dan elevasi koloni serta penghasilan pigmen di sekeliling koloni beberapa isolat aktinomiset (Lampiran 8 dan 9).
Pengamatan morfologi menunjukkan bahwa hampir semua isolat memiliki elevasi timbul dengan konsistensi keras, lunak hingga sangat lunak. Permukaan koloni bervariasi dari halus, berkerut, bersisik, berbukit-bukit dan seperti butiran. Warna koloni yang dihasilkan sangat beragam namun secara garis besar dapat dikelompokkan dalam 4 warna yaitu putih, abu-abu, hitam dan coklat. Pembentukan pigmen warna juga terlihat pada media pertumbuhan di sekeliling koloni dari isolat. Isolat Csr 1-1, Csr 1-6, Csr 4, Csr 2-6 dan Csr 3-1 menghasilkan pigmen berwarna coklat di sekeliling koloni.
Gambar 4 Koloni aktinomiset pada media HV agar (a) dan isolat murni aktinomiset pada media ISP 2 (b).
b
a
Isolasi dan Identifikasi Cendawan yang Diduga Patogen Tanaman
Gejala penyakit muncul saat tanaman berumur 21 HST dimulai pada daun berupa bercak berwarna coklat berbentuk tidak teratur, muncul pada bagian tepi atau tengah daun kemudian meluas membentuk daerah nekrotik (jaringan nekrosis). Jaringan nekrosis ini dikelilingi oleh daerah berwarna kuning (klorosis) kemudian mengering dan mati. Bercak pada batang berwarna coklat yang lama kelamaan melingkari batang sehingga batang membusuk dan patah. Pada buah gejala penyakit berupa bercak coklat. Bercak pada buah terus meluas sampai ke seluruh daging buah dan permukaan buah menghitam (Gambar 5).
Berdasarkan gejala yang ditunjukkan, diduga penyakit pada daun disebabkan oleh bakteri, sedangkan penyakit pada batang dan buah diduga adalah antraknosa yang disebabkan oleh cendawan Colletotrichum sp. Setelah dilakukan isolasi dan identifikasi, mikroba yang didapatkan adalah tujuh isolat Fusarium sp. dan satu isolat Curvularia sp. (Lampiran 10).
PEMBAHASAN
Streptomyces spp. yang diaplikasikan secara nyata mampu menekan tingkat keparahan penyakit dan meningkatkan pertumbuhan tanaman (tinggi dan bobot kering tanaman) serta secara tidak nyata meningkatkan bobot dan jumlah buah baik buah grade A, B, dan C maupun buah total.
Terjadinya penekanan keparahan penyakit terlihat dari rendahnya nilai LADKP perlakuan dibandingkan kontrol (tanpa Streptomyces).
Streptomyces isolat LSW05 dan PS4-16 mampu menghambat pertumbuhan mikrob patogen dengan kemampuan yang beragam bergantung pada cara aplikasi. Kemampuan Streptomyces isolat LSW05 lebih tinggi dalam menekan keparahan penyakit dibandingkan isolat PS4-16 dan kombinasi keduanya. Hal ini terlihat dari nilai LADKP kombinasi aplikasi kedua isolat yang lebih rendah dibandingkan dengan aplikasi isolat LSW05 secara tunggal. Hasil ini didukung oleh penelitian Yusniawati (2009) secara in vitro dimana isolat LSW05 mampu menghambat pertumbuhan miselium S. rolfsii hingga 84% sementara isolat PS4-16 hanya mampu menghambat pertumbuhan miselium S. rolfsii sebesar 33%. Di lapangan, isolat LSW05 juga mampu meningkatkan tinggi dan bobot kering tanaman serta produksi buah lebih baik dibandingkan isolat PS4-16 dan kombinasi keduanya.
Perbedaan kemampuan isolat Streptomyces diduga disebabkan oleh keragaman senyawa bioaktif yang dihasilkan. Streptomyces dikenal memiliki kemampuan yang tinggi dalam menghasilkan berbagai senyawa bioaktif yang potensial untuk menghambat pertumbuhan mikrob patogen (Lestari 2006). Senyawa bioaktif yang dihasilkan isolat LSW05 diduga lebih efektif dibandingkan isolat PS4-16 sehingga kemampuannya lebih tinggi dalam menekan keparahan penyakit. Kemampuan kombinasi isolat LSW05+PS4-16 yang lebih rendah dalam menekan keparahan penyakit kemungkinan disebabkan karena terjadi antagonisme antar isolat Streptomyces.
Aplikasi Streptomyces secara penyiraman lebih mampu menekan keparahan penyakit dibandingkan metode aplikasi lainnya. Diduga frekuensi aplikasi secara penyiraman sebanyak lima kali dapat meningkatkan populasi Streptomyces di dalam tanah sehingga lebih efektif dalam menekan serangan patogen. Streptomyces yang diaplikasikan dengan metode penyemprotan pada permukaan tanaman kurang efektif kemungkinan karena kurang tercukupinya kelembaban pada permukaan tanaman sehingga Streptomyces kurang dapat bertahan lama. Sementara itu, pada metode seed coating Streptomyces spp. yang dilapiskan secara dini pada permukaan biji tidak cukup menekan serangan patogen lebih lanjut. Untuk Gambar 5 Gejala penyakit yang menyerang
tanaman. Tanaman yang terserang penyakit (a), gejala pada batang (b) : batang berwarna coklat (b1), batang membusuk dan patah (b2), gejala pada daun (c) dan gejala pada buah (d).
b1
b2
c
d
aplikasi Streptomyces di lapangan dengan kondisi telah terjadi kolonisasi oleh patogen yang beragam, seed coating satu kali mungkin tidak cukup melindungi tanaman yang lebih dewasa.
Mekanisme kerja Streptomyces sebagai agen pengendali hayati dapat secara tidak langsung melalui peningkatan kebugaran tanaman. Penekanan keparahan penyakit dapat terjadi melalui induksi ketahanan sistemik tanaman dan produksi senyawa bioaktif, antara lain senyawa antibiotik, siderofor dan beberapa enzim litik seperti kitinase, glukanase dan selulase (Compant et al. 2005). Induksi ketahanan sistemik berkembang setelah tanaman diinokulasi lebih awal dengan Streptomyces spp. sehingga tanaman lebih tahan terhadap serangan patogen berikutnya. Antibiotik seperti oligomisin A, kanosamin, zwittermisin A dan xantobasin dan beberapa enzim litik seperti kitinase, glukanase dan selulase diketahui berperan dalam mekanisme penghambatan mikrob patogen. Enzim kitinase dan β-1,3-glukanase yang disintesis Streptomyces sp. strain 385 mampu mendegradasi dinding sel Fusarium oxysporum f.sp. cucumerinum dan menggunakannya sebagai sumber karbon (Compant et al. 2005). Senyawa siderofor yang disekresikan dapat menghambat pertumbuhan mikrob patogen. Ion Fe sangat diperlukan oleh spora Fusarium sp. untuk berkecambah. Dengan tidak tersedianya ion Fe maka infeksi Fusarium sp. pada tanaman akan berkurang sehingga tanaman tumbuh lebih sehat (Haas & Defago 2005). Hal ini ditunjukkan oleh peningkatan beberapa parameter pertumbuhan tanaman seperti tinggi dan bobot kering tanaman serta produksi buah setelah diaplikasikan Streptomyces spp. Produksi siderofor oleh Streptomyces telah dilaporkan oleh Macagnan et al. (2008) yang mendeteksi produksi siderofor oleh Streptomyces albovinaceus, S. caviscabies, S. griseus, S. setonii dan S. virginiae.
Mekanisme peningkatan pertumbuhan tanaman juga disebabkan oleh adanya fitohormon yang dihasilkan bakteri antagonis (Yuen & Schroth 1986), dalam hal ini adalah Streptomyces. Dimkpa et al. (2008) melaporkan produksi indole-3-acetic acid (IAA) oleh Streptomyces acidiscabies E13, S. avermitilis, S. tendae F4, S. tanashiensis, S. coelicolor A3(2) dan W13. Streptomyces isolat lokal juga diketahui dapat menghasilkan fitohormon seperti auksin (Hastuti, komunikasi pribadi). Peningkatan bobot kering, bobot basah, jumlah dan ukuran daun
tanaman tomat setelah pemberian Streptomyces juga dilaporkan oleh Romeiro et al. (1997). Berdasarkan kemampuannya dalam memacu pertumbuhan tanaman, Streptomyces digolongkan sebagai plant growth-promoting bacteria (PGPB) yang pada beberapa penelitian juga dilaporkan dapat meningkatkan ketahanan sistemik tanaman melawan patogen tanaman (Compant et al. 2005).
Pada aplikasi secara penyiraman dan penyemprotan penekanan penyakit oleh Streptomyces diduga bekerja melalui mekanisme produksi antibiotik, enzim litik dan siderofor sehingga lebih efektif dalam menekan keparahan penyakit. Sementara itu, pada metode seed coating, aplikasi Streptomyces yang dilakukan saat tanaman masih berupa biji diduga dapat menginduksi ketahanan tanaman terhadap infeksi patogen. Namun metode ini ternyata kurang mampu menekan serangan patogen lebih lanjut dibandingkan dengan metode penyiraman dan penyemprotan. Walaupun demikian, metode seed coating ternyata mampu memacu produksi tanaman secara lebih baik. Diduga senyawa bioaktif seperti antimikrob dan senyawa fitohormon yang dihasilkan oleh Streptomyces spp. yang dilapiskan secara dini pada permukaan biji mampu memacu pertumbuhan tanaman sejak dini, sehingga tinggi tanaman serta bobot dan jumlah buah yang dihasilkan lebih tinggi.
Kesuburan tanah juga memegang peranan penting dalam penelitian ini. Hasil analisis tanah menunjukkan bahwa tanah yang digunakan dalam penelitian tergolong subur sehingga dapat diketahui bahwa gejala penyakit yang ditunjukkan pada tanaman bukan disebabkan oleh kekurangan unsur hara tetapi karena tanaman terserang oleh patogen.
Hasil isolasi dan pemurnian aktinomiset dari sampel tanah komposit menunjukkan bahwa sebelumnya sudah terdapat beragam jenis aktinomiset lokal dalam tanah percobaan. Namun demikian, beragam jenis aktinomiset ini belum mampu menekan keparahan penyakit.
Berdasarkan hasil isolasi dan identifikasi cendawan yang diduga patogen tanaman, cendawan yang didapatkan adalah Fusarium sp. dan Curvularia sp. Fusarium merupakan salah satu patogen tular tanah yang dapat menyebabkan penyakit layu Fusarium pada tanaman. Gejala umum yang ditunjukkan berupa menjadi pucatnya tulang-tulang daun, terutama daun-daun sebelah atas, kemudian diikuti dengan merunduknya tangkai, dan
akhirnya tanaman menjadi layu secara keseluruhan. Namun, gejala umum yang disebabkan oleh Fusarium patogen tidak ditemukan dalam penelitian, yang ditemukan adalah gejala penyakit karena bakteri dan Colletotrichum. Oleh karena itu, Fusarium yang ditemukan kemungkinan bukan dari jenis patogen. Beberapa spesies Fusarium diketahui dapat hidup di dalam jaringan tanaman dan bersifat non-patogenik terhadap tanaman (Bao et al. 2002). Curvularia biasa ditemukan pada gejala nekrosis yang telah lanjut oleh patogen primer.
Dari sisi ekonomi, aplikasi Streptomyces mempengaruhi keuntungan yang diperoleh. Tanpa aplikasi keuntungan yang diperoleh hanya sebesar Rp 26.515.000 per ha sementara bila Streptomyces spp. diaplikasikan dengan metode seed coating, keuntungan meningkat hingga 183%. Aplikasi Streptomyces dengan metode penyiraman dan penyemprotan kurang menguntungkan karena tingginya biaya yang harus dikeluarkan selama aplikasi.
Hasil penelitian ini memberikan gambaran bahwa aplikasi Streptomyces memiliki prospek yang cerah untuk diterapkan pada lahan pertanian yang lebih luas, terutama pada lahan pertanian organik tanpa penggunaan bahan-bahan kimiawi baik pupuk maupun mikrobisida kimiawi.
SIMPULAN
Streptomyces spp. yang diaplikasikan efektif menekan keparahan penyakit, meningkatkan tinggi dan bobot kering tanaman serta bobot dan jumlah buah yang dihasilkan.
Seed coating dengan Streptomyces isolat LSW05 merupakan perlakuan terbaik dalam meningkatkan tinggi tanaman, bobot dan jumlah buah serta merupakan perlakuan yang paling menguntungkan untuk diterapkan.
SARAN
Perlu kajian lebih lanjut tentang dosis aplikasi seed coating. Juga perlu dilakukan pengkajian terhadap penambahan metode lain setelah seed coating seperti perendaman akar bibit tanaman dalam kultur Streptomyces spp. sebelum dilakukan penanaman.
DAFTAR PUSTAKA
Adiyoga W, Gunadi N, Moekasan TK, Subhan. 2007. Identifikasi potensi dan
kendala produksi paprika di rumah plastik. J Hort 17(1): 88-100.
Andri C. 2004. Kajian potensi Streptomyces sp. PS1-4 sebagai penghasil senyawa bioaktif pengendali bakteri patogen tanaman kedelai [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Bao JR, Fravel DR, O’Neil NR, Lazarovits G, van Berkum P. 2002. Genetic analysis of pathogenic and nonpathogenic Fusarium oxysporum from tomato plants. Can J Bot 80: 271-279.
Barnett HL, Hunter BB. 1972. Illustrated Genera of Imperfect Fungi. Minnesota: Burgess Publishing Company.
Bonjar GHS et al. 2006. Biological control of Phytophthora drechsleri Tucker, the causal agent of pistachio gummosis, under greenhouse condition by use of Actinomyces. Plant Pathol J 5 (1): 20-23. [BPS dan Dirjen BPH] Badan Pusat Statistik
dan Direktorat Jendral Bina Produksi Hortikultura. 2008. Produksi Tanaman Sayuran di Indonesia Periode 2003-2007. [BPT] Balai Penelitian Tanah. 2005. Analisis Kimia Tanah, Tanaman, Air dan Pupuk. Jakarta: Agro Inovasi.
Christ BJ. 1991. Effect of disease assessment method on ranking potato cultivar for resistance to early blight. Plant Disease 75: 353-356.
Christ BJ, Haynes KG. 2001. Inheritance of resistance to early blight disease in a diploid potato population. Plant Breed 120: 169-172.
Compant S, Duffy B, Nowak J, Clement C, Barka EA. 2005. Use of plant growth-promoting bacteria for biocontrol of plant diseases: principles, mechanisms of action, and future prospects. Appl Environ Microbiol 71 (9): 4951–4959.
Dimkpa CO et al. 2008. Involvement of siderophores in the reduction of metal-induced inhibition of auxin synthesis in Streptomyces spp. Chemosphere (74): 19– 25.
Haas D, Défago G. 2005. Biological control of soil-borne pathogens by Pseudomonads fluorescent. Nat Rev.
Ifdal. 2003. Interaksi antara Streptomyces sp. dengan Bacillus subtilis, Xanthomonas campestris pv glycine, Rhizobia dan Pseudomonas sp. [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
[IPNI] International Plant Nutrional Institut. 2008. Potassium Improves Yield and Quality of Tomato in the Red & Lateritic Soils of West Bengal with Low Inherent Fertility [terhubung berkala] http://www.ipni.net [15 Agustus 2009].
Kuswinanti 2006. Efektivitas Trichoderma harzianum dan Gliocladium virens dalam menekan pertumbuhan Sclerotium rolfsii penyebab penyakit busuk pangkal batang pada tanaman kacang tanah. Bul Penel 9(1): 10-17.
Lestari Y. 2006. Identification of indigenous Streptomyces spp. producing antibacterial compound. J Mikrobiol Indones 11(2): 99-101.
Macagnan D, Romeiro RS, Pomella AWV, deSouza JT. 2008. Production of lytic enzymes and siderophores, and inhibition of germination of basidiospores of Moniliophthora (ex Crinipellis) perniciosa by phylloplane actinomycetes. Biol Control (47): 309–314.
Miyadoh S. 1997. Atlas of Actinomycetes. Japan: Asakura Publishing Co, Ltd. Moussa TAA, Rizk MA. 2002. Biocontrol of
sugarbeet pathogen Fusarium solani (Mart.) Sacc. by Streptomyces aureofaciens. Pak J Biol Sci 5(5): 556-559.
Muthahanas I. 2004. Potensi Streptomyces agens pengendali biologi Raltsonia solanacearum penyebab penyakit layu tanaman cabai [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor. Papuangan N. 2009. Aktivitas penghambatan
senyawa antimikrob Streptomyces spp. terhadap mikrob patogen tular tanah secara in vitro dan in planta [tesis]. Bogor: Program Pascasarjana, Institut Pertanian Bogor.
Prapagdee B, Akrapikulchart U, Mongkolsuk S. 2008. Potential of a soil-borne Streptomyces hygroscopicus for biocontrol of anthracnose disease caused by Colletotrichum gloeosporioides in orchid. J Biol Sci 8(7): 1187-1192.
Romeiro RS, Moura AB, Matsuoka K, Fernandes MC. 1997. Actinomycetes selected for biological control of tomato wilt (Ralstonia solanacearum) and growth promotion after seed microbialization.
Sabaratnam S, Traquaira JA. 2002. Formulation of Streptomyces biocontrol agent for suppression of Rhizoctonia damping-off in tamato transplants. Biol Cont 23(3):245-253.
Semangun H. 1994. Penyakit-penyakit Tanaman Hortikultura di Indonesia. Yogyakarta: UGM Press.
Suryaningsih E, Chujoi E, Kusmana. 1999. Identification of potato cultivars resistance to late blight through a Standard International Field Trial (SIFT) in Indonesia. In Potato Research in Indonesia. Research Result in a Series of Working Papers, 1999. Collaborative Research between The RIV and CIP. P. 37-44.
[USDA ERS] United States Department of Agriculture Economic Research Service. 2007. US Tomato Statistics [terhubung berkala] http://usda.mannlib.cornell.edu [15 Agustus 2009].
[USDA FAS] United States Department of Agriculture Foreign Agricultural Service. 2008. World Markets and Trade
[terhubung berkala] http://www.fas.usda.gov [15 Agustus
2009].
Widarto HT. 2008. Mendongkrak Kinerja Mikroorganisme Antagonis terhadap Patogen Tular Tanah. Direktorat Perlindungan Perkebunan.
Wijayani A, Widodo W. 2005. Usaha meningkatkan kualitas beberapa varietas tomat dengan sistem budidaya hidroponik. Ilmu Pertanian 12(1).
Windels CE. 1993. Methods Research on Soilborne Phytopathogenic Fungi: Fusarium. Minnesota: APS Press.
Yuen GY, Schroth MN. 1986. Interactions of Pseudomonas fluorescens strain E6 with ornamental plant and its effect on the composition of root-colonizing microflora. Phytopathol 76: 176-180.
Yusniawati RD. 2009. Potensi Streptomyces spp. sebagai penghambat cendawan tular tanah Sclerotium rolfsii secara in vitro dan in planta pada tanaman tomat (Solanum lycopersicum) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Lampiran 1 Tabel komposisi media per liter Media ISP no.2 Agar
Komposisi Jumlah Yeast extract 4 g Malt extract 10 g Dextrose 4 g Agar 20 g Akuades sampai 1000 ml
Media modifikasi molase-kedelai
Komposisi Jumlah Molase 1 % (v/v) CaCO3 2 g Urea 1 g SP-18 1 g KCl 1 g MgSO4.7H2O 1 g NaCl 1 g FeSO4.7H2O 0,001 g MnCl2.4H2O 0,013 g ZnSO4.7H2O 0,001 g Bubuk kedelai 0,5 % (g/v) Akuades sampai 1000 ml Media PDA Komposisi Jumlah PDA 39 g Akuades sampai 1000 ml Media Oatmeal Agar
Komposisi Jumlah Oatmeal agar 23 g
Akuades sampai 1000 ml
Media HV Agar
Komposisi Jumlah Humic acid sol.1) 40 ml CaCO3 0,02 g KCl 1,71 g Na2HPO4 0,5 g MgSO4.7H2O 0,05 g FeSO4.7H2O 0,01 g Vitamine B sol. 200x2) 5 ml Cycloheximide 50 mg Nalidixid acid sol.3) 4 ml
Akuades sampai 1000 ml 1) 1 g humic acid dilarutkan semalam dalam 40 ml NaOH 0,4 %.
2) 5 ml vitamin B (masing-masing mengandung 0,5 mg thiamine-HCl, riboflavin, niacin, pyridoxin-HCl, inositol, Ca- panthothenate, p-aminobenzoic acid, dan 0,25 mg biotin). 3) 20 mg dilarutkan dalam campuran 1 ml NaOH 0,4 % steril dan 3 ml akuades steril.
Lampiran 2 Pengaruh aplikasi Streptomyces terhadap luasan area di bawah kurva perkembangan penyakit (LADKP) pada tanaman tomat pada tujuh periode pengamatan
Perlakuan Hari setelah tanam (HST)
28 35 42 49 56 63 70 Seed coating LSW05 83,3 168,8 348,0 635,5 ab 987,5 ab 1352,1 a-d 1731,0 bcd PS4-16 83,3 172,9 389,6 720,8 ab 1087,5 b 1458,3 cd 1833,3 bcd LSW05+ PS4-16 141,7 252,1 447,9 731,3 b 1064,6 ab 1412,5 bcd 1781,0 bcd Siram LSW05 58,3 116,7 268,8 518,8 a 810,0 a 1133,4 a 1462,3 a PS4-16 50,0 116,7 270,9 522,9 a 846,0 a 1187,9 ab 1542,1 ab LSW05+ PS4-16 66,7 141,7 320,9 597,9 ab 920,9 a 1262,5 a-d 1625,0 abc Semprot LSW05 66,7 137,5 314,6 589,6 a 895,9 a 1227,1 abc 1575,0 ab PS4-16 100,0 183,4 368,8 641,7 ab 951,9 ab 1287,4 a-d 1645,9 abc LSW05+ PS4-16 66,7 156,3 362,5 683,3 ab 1060,4 ab 1441,4 cd 1835,4 cd Kontrol 116,7 222,9 432,6 737,0 b 1107,6 b 1498,6 d 1923,6 d Nilai P 0,268 0,177 0,089 0,048 0,037 0,031 0,012
Keterangan: Angka yang diikuti oleh huruf yang sama pada setiap kolom tidak berbeda nyata berdasarkan uji jarak berganda Duncan pada taraf 5 %.
Lampiran 3 Pengaruh aplikasi Streptomyces terhadap luasan area di bawah kurva perkembangan tinggi tanaman (LADKT) pada tanaman tomat pada tujuh periode pengamatan
Perlakuan Hari setelah tanam (HST)
28 35 42 49 56 63 70
Seed coating
LSW05 392,6 a 611,6 a 900,5 a 1282,6 a 1763,7 a 2335,1 a 3050,3 a PS4-16 376,9 a 582,5 ab 847,0 ab 1208,4 ab 1662,5 ab 2185,8 ab 2826,3 abc LSW05+ PS4-16 340,1 ab 530,5 abc 776,9 abc 1105,9abc 1522,1 abc 2012,2 abc 2859,3 ab
Siram LSW05 280,6 bc 437,9 cd 651,9 bcd 952,0 cd 1347,1 bcd 1841,6 abc 2495,5 bcd PS4-16 283,0 bc 434,4 cd 632,2 bcd 907,7 cd 1267,9 cd 1711,5 cd 2291,9 cd LSW05+ PS4-16 275,9 bc 429,0 cd 638,0 bcd 926,8 cd 1299,8 bcd 1762,6 abc 2379,3 bcd Semprot LSW05 283,5 bc 449,3 cd 640,5 bcd 967,0 bcd 1346,2 bcd 1799,0 abc 2270,3 d PS4-16 249,7 c 391,1 d 575,8 bcd 829,3 cd 1167,8 cd 1602,8 cd 2206,6 d LSW05+ PS4-16 296,9 bc 458,2 bcd 674,0 bcd 975,8 bcd 1365,9 bcd 1836,0 abc 2395,2 bcd Kontrol 236,3 c 373,2 d 553,6 d 801,6 d 1135,5 d 1550,9 d 2067,8 d Nilai P 0,004 0,007 0,012 0,012 0,012 0,013 0,011
Keterangan: Angka yang diikuti oleh huruf yang sama pada setiap kolom tidak berbeda nyata berdasarkan uji jarak berganda Duncan pada taraf 5 %.
Lampiran 4 Analisis biaya usaha tani tanaman tomat per hektar Komponen biaya umum (tanpa Streptomyces)
Uraian Satuan Volume Harga per satuan (Rpx1000)
Total harga (Rpx1000) A. Sarana Produksi
- Benih gram 300 6 1.800 - Pupuk kandang ton 20 450 9.000 - Kapur dolomit ton 20 30 6.000 - Ajir batang 30.000 0,2 600
- Tali rafia gulung 5 15 75
Jumlah 17.475
B. Tenaga Kerja
- Penyemaian HOK 3 20 60
- Pengolahan tanah HOK 100 20 2.000 - Penanaman dan pemupukan HOK 35 20 700 - Pemeliharaan HOK 75 20 1.400 - Pemanenan dan pengangkutan HOK 25 20 500 Jumlah 4.660 C. Biaya Lain-lain
- Sewa lahan hektar 1 2.000 2.000
Total Biaya A+B+C 24.135
Keterangan : HOK = hari orang kerja Metode Seed coating
Uraian Satuan Volume Harga per satuan (Rpx1000)
Total Harga (Rpx1000) A. Komponen biaya umum 24.135 B. Produksi inokulum
Streptomyces liter 12 14,2 170,4
Total Biaya A+B 24.305,4
Metode Penyiraman dan Penyemprotan
Uraian Satuan Volume Harga per satuan (Rpx1000)
Total Harga (Rpx1000) A. Komponen biaya umum 24.135 B. Produksi inokulum
Streptomyces liter 2.500 14,2 35.500
Lampiran 4 (Lanjutan)
Perhitungan produksi inokulum Streptomyces
Metode Seed coating
Aplikasi hanya dilakukan satu kali berupa pelapisan isolat Streptomyces pada benih yang akan ditanam. Isolat terlebih dahulu disuspensikan dalam larutan kanji 2%, kemudian dilapiskan pada benih.
# Kebutuhan suspensi Streptomyces + larutan kanji 2%
1 hektar lahan dapat ditanami sekitar 20.000 tanaman = 20.000 benih. 100 benih butuh 2 ml suspensi Streptomyces + larutan kanji 2%. 20.000 benih = 20.000 benih x 2 ml = 400 ml
100 benih
Maka, untuk 20.000 benih dibutuhkan 400 ml suspensi Streptomyces + larutan kanji 2%. # Kebutuhan inokulum Streptomyces
10 ml suspensi = 2 g massa sel Streptomyces + 10 ml larutan kanji 2% 400 ml suspensi = 40 x (2 g massa sel Streptomyces + 10 ml larutan kanji 2%)
= 80 g massa sel Streptomyces + 400 ml larutan kanji 2%
Maka, untuk membuat 400 ml suspensi Streptomyces + larutan kanji 2% dibutuhkan 80 g massa sel Streptomyces dan 400 ml larutan kanji 2%.
300 ml inokulum Streptomyces menghasilkan 2 g massa sel Streptomyces
80 g massa sel Streptomyces = 80 g massa sel x 300 ml = 12.000 ml = 12 liter 2 g massa sel
Maka, untuk aplikasi seed coating dibutuhkan 12 liter inokulum Streptomyces. Metode Penyiraman dan Penyemprotan
Aplikasi diberikan sebanyak 25 ml inokulum per tanaman, maka jumlah inokulum Streptomyces yang dibutuhkan setiap aplikasi per hektar
= 20.000 x 25 ml inokulum = 500.000 ml inokulum
= 500 liter inokulum Streptomyces
# Kebutuhan inokulum Streptomyces selama 5 kali aplikasi per hektar
Aplikasi dilakukan sebanyak 5 kali dimulai saat tanaman berumur 28 HST hingga tanaman berumur 56 HST, maka jumlah total inokulum Streptomyces yang dibutuhkan selama 5 kali aplikasi per hektar
= 5 x 500 liter inokulum = 2500 liter inokulum
Jadi, mulai dari proses penanaman hingga panen dibutuhkan inokulum sebanyak 2500 liter inokulum Streptomyces per hektar.
Lampiran 5 Hasil analisis NPK tanah percobaan
Ulangan Kandungan unsur hara dan kualitasnya
N% P (mg/100g) K (mg/100g) 1 0,589 (tinggi) 8,337 (sangat rendah) 73,229 (sangat tinggi) 2 0,603 (tinggi) 8,066 (sangat rendah) 75,969 (sangat tinggi) 3 0,477 (sedang) 7,877 (sangat rendah) 80,129 (sangat tinggi) Rata-rata 0,556 (tinggi) 8,093 (sangat rendah) 76,442 (sangat tinggi) Sumber : Laboratorium Biokimia/Kimia BB-Biogen
Keterangan : Kriteria kualitas tanah diambil dari BPT (2005)
Lampiran 6 Tata letak plot percobaan
Keterangan :
= Tanaman yang diberi perlakuan Streptomyces
x
= Tanaman bordera, b, c = Jenis perlakuan Streptomyces
1 m 3,5 m
x
x
x
x
a
b
c
Lampiran 7 Deskripsi tanaman tomat varietas Arthaloka
Umur mulai berbunga : 3 – 4 minggu setelah pindah tanam Umur panen : 108 hari setelai semai
Tipe tanaman : indeterminate Warna daun : hijau agak tua Warna batang : hijau
Warna mahkota bunga : kuning Bentuk buah : oval – lonjong
Warna buah muda : hijau mengkilap dengan bahu buah hijau tua Warna buah tua : merah merata
Potensi hasil : 3 – 4 kg/tanaman
Ketahanan terhadap penyakit : Tahan terhadap layu bakteri (Ralstonia), bacterial canker, TMV
Lampiran 8 Keragaman aktinomiset di Lahan Pertanian Organik Resor Permata Hati Cisarua
Isolat Konsistensi Pigmentasi Permukaan Elavasi Kelompok
Koloni Media
Csr 1-1 keras putih coklat halus timbul Streptomyces
Csr 1-2 sangat lunak putih halus timbul Streptomyces
Csr 1-4 sangat lunak putih bersisik timbul Streptomyces
Csr 1-5 sangat lunak putih halus datar Streptomyces
Csr 1-8 keras putih berbukit-bukit timbul Streptomyces
Csr 2-1 sangat lunak putih bersisik datar Streptomyces
Csr 2-2 sangat lunak putih berkerut timbul Streptomyces
Csr 3-4 lunak putih halus timbul Streptomyces
Csr 3-8 keras putih bersisik timbul Streptomyces
Csr 3-14 keras putih berkerut datar Streptomyces
Csr 3-15 sangat lunak putih halus timbul Streptomyces
Csr 3-16 keras putih seperti butiran timbul Streptomyces
Csr 3-19 lunak putih halus timbul Streptomyces
Csr 1-3 lunak abu-abu berkerut timbul Streptomyces
Csr 1-6 lunak abu-abu coklat halus datar Streptomyces
Csr 1-9 keras abu-abu berbukit-bukit timbul Streptomyces
Csr 1-10 sangat lunak abu-abu berkerut timbul Streptomyces
Csr 1-11 lunak abu-abu berbukit-bukit timbul Streptomyces
Csr 2-3 lunak abu-abu berbukit-bukit timbul Streptomyces
Csr 2-4 sangat lunak abu-abu coklat berkerut timbul Streptomyces
Csr 2-5 lunak abu-abu bersisik timbul Streptomyces
Csr 2-6 lunak abu-abu coklat halus timbul Streptomyces
Csr 2-7 keras abu-abu berbukit-bukit timbul Streptomyces
Csr 3-1 sangat lunak abu-abu coklat seperti butiran timbul Streptomyces
Csr 3-2 sangat lunak abu-abu berkerut timbul Streptomyces
Csr 3-3 lunak abu-abu halus timbul Streptomyces
Csr 3-5 keras abu-abu seperti butiran timbul Streptomyces
Csr 3-6 lunak abu-abu halus datar Streptomyces
Csr 3-7 sangat lunak abu-abu halus timbul Streptomyces
Csr 3-9 lunak abu-abu halus timbul Streptomyces
Csr 3-10 keras abu-abu halus timbul Streptomyces
Csr 3-11 keras abu-abu halus timbul Streptomyces
Csr 3-12 keras abu-abu halus timbul Streptomyces
Csr 1-7 lunak hitam berbukit-bukit timbul Streptomyces
Csr 1-12 lunak hitam berkerut timbul Streptomyces
Csr 3-13 lunak coklat berkerut timbul Non- Streptomyces
Csr 3-17 keras coklat berbukit-bukit timbul Non- Streptomyces
Csr 3-18 keras coklat bersisik timbul Non- Streptomyces
Csr 3-20 keras coklat berbukit-bukit timbul Non- Streptomyces
Csr 3-21 keras coklat berbukit-bukit timbul Non- Streptomyces
Csr 3-22 lunak coklat bersisik datar Non- Streptomyces
Lampiran 9 Keragaman koloni (a) dan mikroskopis (b) aktinomiset di Lahan Pertanian Organik Resor Permata Hati Cisarua
a
Csr 1-1 Csr 1-2 Csr 1-3 Csr 1-4 Csr 1-5 Csr 1-6 Csr 1-7 Csr 1-9 Csr 1-10 Csr 1-11 Csr 2-1 Csr 2-2 Csr 2-3 Csr 2-4 Csr 2-5 Csr 2-6 Csr 2-7 Csr 3-1 Csr 3-2 Csr 3-3 Csr 3-4 Csr 3-5 Csr 3-6 Csr 3-7Lampiran 9 (Lanjutan)
b
Csr 3-8 Csr 3-9 Csr 3-10 Csr 3-11 Csr 3-12 Csr 3-13 Csr 3-15 Csr 3-16 Csr 3-18 Csr 3-19 Csr 3-20 Csr 3-22Csr3-20
Csr2-5
Csr1-7
Csr1-3
Lampiran 10 Cendawan hasil isolasi dari tanaman yang terinfeksi 1 2 3 4 5
a
d
f
a
e
a
b
c
d
e
a
a
d
g
Lampiran 10 (Lanjutan) 6 7 8
Keterangan : Koloni (a), konidiofor (b), konidia (c), hifa (d), makrokonidia (e), mikrokonidia (f), klamidospora (g) dari Culvularia D1-2 (1), Fusarium A1-1 (2), Fusarium Bh1-1 (3), Fusarium Bh1-2 (4), Fusarium Bt1-1 (5), Fusarium Bt1-2 (6), Fusarium Bt2-1 (7), Fusarium D1-1, Fusarium D1-1 (8) perbesaran 400x.