ANALISIS
ANALISIS
FARMASI
ANORGANIK
Sophi Damayanti 11Analisis Kuantitatif
TOPIK
• Prinsip Analisis Kuantitatif • Titrasi Asam Basa
T
UJUANI
NSTRUKSIONAL| Mahasiswa mampu menetapkan kadar atau
konsentrasi ion penyusun sampel sekaligus kandungan senyawa anorganik dalam sampel kandungan senyawa anorganik dalam sampel | Memahami prinsip dan teori yang melandasi
analisis kuantitatif (titrasi asam basa dan titrasi analisis kuantitatif (titrasi asam basa dan titrasi pengendapan)
| Menyusun prosedur analisis untuk penetapan | Menyusun prosedur analisis untuk penetapan
kadar secara metode kimia klasik (tanpa instrumen)
TIPS
TIPS
1. Mencatat: Mind Map
2 Berlatih soal soal 2. Berlatih soal-soal
3. Membaca buku-buku pustaka
P ktik
P
USTAKA| R th HJ d Bl hk G “A li i F i” t j h | Roth HJ dan Blaschke G, “Analisis Farmasi”, terjemahan
S. Kisman dan S. Ibrahim, Cetakan III, Gadjah Mada University
| Cairns D “Essential of Pharmaceutical Chemistry” 2nd ed | Cairns D, Essential of Pharmaceutical Chemistry , 2 ed,
Pharm Press London, 2005
| Day RA and Underwood AL, “Quantitative Analysis”, 6th ed, Practice Hall, New Jersey, 1991
ed, Practice Hall, New Jersey, 1991
| Connors KA, “A Textbook of Pharmaceutical Chemistry”, 3rd ed. John Willey and Sons, New York, 1982
| Skoog DA West DM and Holler FJ “Fundamental of | Skoog DA, West DM and Holler FJ, Fundamental of
Analytical Chemistry”, 5th ed, Saunder Coll. Publ. New York, 1988
| Christian GD, “Analytical Chemistry”, 6C st a G , a yt ca C e st y , 6 ed, Joth ed, John Wiley W ey and Sons, New York, 2004
PRINSIP ANALISIS
PRINSIP ANALISIS
KUANTITATIF
A
NALISISF
ARMASI/
P
HARMACEUTICALA
NALYSISIlmu dan teknik analisis yang diterapkan atau
diaplikasikan pada senyawa kimia dan bahan-bahan
di k d l b
Ki i
Kimia Organik Kimia
| Hal yang diukur:
K i i Ki i i B h Al H il
• Komposisi Kimiawi Bahan Alam maupun Hasil
Sintesis
T k ik di k
| Teknik yang digunakan:
• Identitas
D j k i
• Derajat kemurnian
B
AHAN YANG DIGUNAKAN DALAMF
ARMASI| Bahan Farmasi Aktif
5 TAHAP UTAMA ANALISIS
KUANTITATIF
1.
Sampling (pengambilan sampel)
2.Pelarutan sampel
3.
Pengubahan analit ke dalam bentuk
4. Pengukuran
ANALISIS KUALITATIF
ANALISIS KUANTITATIF
KUALITATIF KUANTITATIF KUALITATIF KUANTITATIF
Berkaitan dengan identifikasi Berkaitan dengan kadar
Menjawab pertanyaan “Apa” Menjawab pertanyaan “Berapa” What chemicals are present How much of one or more
1. SKALA SAMPEL ANALISIS
KUANTITATIF
| Skala Operasional Sampel Jumlah (g) Makro ≥ 0,100 Semimikro 0,01 – 0,10 Mikro 0,001-0,10 Ultramikro ≤ 0 001 Ultramikro ≤ 0,001P
RINSIPA
NALISISK
UANTITATIF| Konsentrasi Komponen yang dianalisis
Konstituen Konsentrasi
Mayor 1 – 100 % Minor 0,01 - 1 % Runut ≤ 0,01 %
2. METODE PENETAPAN KADAR
A. Metode Analisis Kimia
Penambahan R ke A
Berdasarkan stoikiometri Dalam bentuk larutan
B. Metode Analisis Fisikokimia
- Didasari pada pengukuran sifat fisika
- Reaksi kimia diperlukan bisa diperlukan
b h (d i i i)
perubahan (derivatisasi)
APA PERBEDAANNYA?
ANALISIS ANALISIS KIMIA? FISIKOKIMIA? J l h l Jumlah sampel K Komponen Langsung/Tidak Langsung/TidakINDIKATOR Peniter Aliquot
Terminologi
TITRASI
?
?
S
YARATR
EAKSIT
ITRASI1. Stoikiometri diketahui dan tetap 2. Arah reaksi diketahui
3. Kesetimbangan harus cepat 4. Tidak ada reaksi samping
P
ERHITUNGAN STOIKIOMETRI| Bobot Molekul | Bobot Atom
S
ISTEMK
ONSENTRASIM l it | Molaritas
Hitung molaritas larutan yang mengandung 6 g NaCl dalam 200 ml larutan?
NaCl dalam 200 ml larutan? | Normalitas
Hitung normalitas larutan nikel nitrat yang Hitung normalitas larutan nikel nitrat yang
dibuat dari 2 g nikel murni dalam asam nitrat 500 ml (BM Nikel 58.70)
| Persen bobot P = w x 100
w+wo
1. Sampel NaOH seberat 5 g, dilarutkan dalam 45 l air. Hitung persen bobot NaOH
2. HCl pekat (BM 36.5) mempunyai kerapatan 1,19 g/ml dan 37 % bobot HCl. Berapa ml untuk
| Bagian per juta ppm P = w x 106 w+wo mg/L | Miliekivalen 1000 mekivelen = 1 ekivalen Milimol
R
EAKSIT
ITRASIU
MUM| aA + b R pP + qQ
| Keq = [P]p [Q]q [A]a [R]b
K
URVAT
ITRASI E -log A TS TS TS ml peniter ml peniterJenis jenis titrasi
Reaksi Titrasi Peniter a) Netralisasi (proton
transfer) transfer) - Asidimetri
Medium Air AsamHCl H
2SO TBA
-Alkalimetri
HCl, H2SO4
Reaksi Titrasi Peniter b) Redoks (perpindahan elektron - Serimetri C 4+ - Serimetri - Permanganometri - Kromometri Ce4+ MNO4 -Cr2O7 2-- Bromometri - Iodimetri Cr2O7 Br2 (BrO3-/Br-) I2 - Iodometri - Iodatometri Nit it t i 2 S2O3 2-IO3 -- Nitritometri NaNO
Reaksi Titrasi Peniter c) Pengendapan - Argentometri M k i t i Ag+ H + - Merkurimetri d) Kompleksometri Hg+ EDTA
B
AHANB
AKUP
RIMERPeniter: Tergantung reaksi kimia, bila tidak stabil, harus dibakukan oleh baku primer
• Tersedia dalam bentuk murni, mudah dikeringkan dan dimurnikang
• Stabil
• Cemaran harus bisa ditentuken (0.02 %)
l if b k i l
• BM relatif besar untuk mengurangi galat penimbangan.
• Larut dalam air atau kondisi yang • Larut dalam air atau kondisi yang
Media Titrasi
| Umumnya dalam air
| Apabila dalam lingkungan bukan air, alasan apa yang mendasari?
TUGAS
| Cari macam-macam baku primer dan
penggunaannya
C i l h t t h d b k
| Cari salah satu contoh prosedur pembakuan peniter
| Pelarut pelarut dalam titrimetri dan aplikasinya | Pelarut pelarut dalam titrimetri dan aplikasinya | Cari satu prosedur titrasi di Farmakope, jangan
sama ya! sama ya!
Penetapan Titik Akhir Titrasi
p
| Dengan indikator | Golongan indikator:
- Indikator asam basa - Indikator redoks
- Indikator logam - Indikator adsorpsi
Perhitungan titrasi
| mek peniter = mek analit mek analit = Vt.Nt
Vs.Ns = Vt. Nt
Vt.Nt = berat sampel (mg) BM
Soal
1. 0.8168 g baku primer K Biftalat (BM 204,2)
dititrasi terhadap indikator fenolftalein membutuhkan 41 03 ml larutan NaOH membutuhkan 41,03 ml larutan NaOH. Berapakah normalitas NaOH?
2 0 2212 g KHCO3 (BM 100 1) dititrasi dengan 2. 0,2212 g KHCO3 (BM 100,1) dititrasi dengan
20,23 ml larutan HCL 0,1091 N. Hitunglah % kemurnian KHCO33
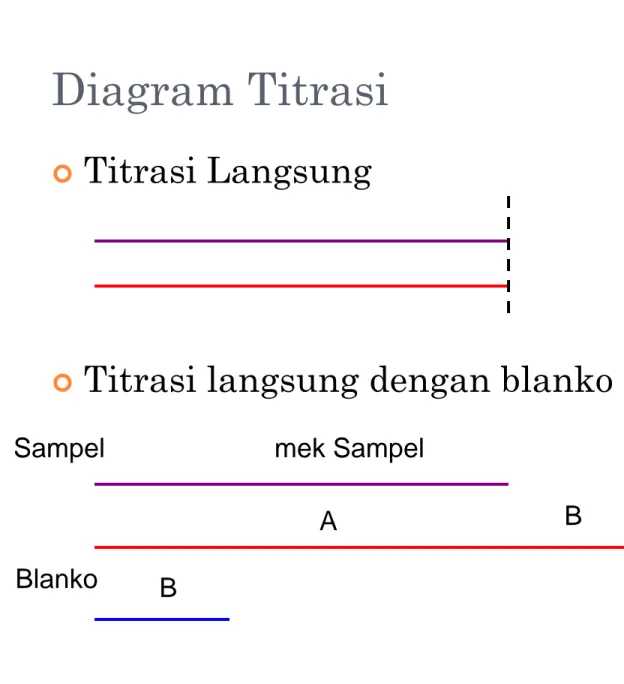
Diagram Titrasi
| Titrasi Langsung
| Titrasi langsung dengan blanko
mek Sampel Sampel p
A B
p
| Titrasi kembali
C pelarut yang lain A berlebih
C
p y g
menitrasi kelebihan A
C
Penyiapan sampel
| Sampel harus dalam bentuk larutan
| Jenis sampel
a. Gas: dilarutkan/diserap
b. Cairan: Langsung, bila suspensi oksidasi,
reduksi, pembentukan kompleks, ekstraksi,
d k i i/d k t k i
dekomposisi/dekstruksi
c. Sampel berbentuk padat: pelarutan/filtrasi atau
sentrifuga ekstraksi analit dan sentrifuga, ekstraksi analit dan
| Digesti dan dekomposisi
- Sampel digerus
- Pemanasan
- Pembakaran
- Digesti asam (ditambahkan asamd an katalis) - Pemijaran
| Penyiapan sampel untuk meningkatkan selektivitas
P i h litik ( k t k i d til i
1. Pemisahan analitik (ekstraksi, destilasi,
kromatografi)
2 Reaksi Kimia Khusus (pengendapan selektif 2. Reaksi Kimia Khusus (pengendapan selektif,
oksidasi/reduksi, masking-demasking, pengaturan pH
pengaturan pH
3. Pengubahan Kondisi titrasi (reaksi titrasi,
lingkungan/medium titrasi dan metode g g penunjukan titik akhir)
Keunggulan metode titrimetri
| Penentuan kadar secara absolut
| Mudah diimplementasi/diinterpretasi | Cepat dalam pelaksanaan
| Cermat dan tepat ulang
| Murah