MAKALAH KIMIA FISIKA
PROBLEM BASED LEARNING - 4
KELOMPOK 2
Disusun oleh:
Jervis Sinto 1406531681 Maulina Cahya Indah S 1406531845 Merisa Aulia 1406531731 Muhammad Irfan Raharjo 1406604531 Stella Faustine L 1406564830
UNIVERSITAS INDONESIA DEPOK
KATA PENGANTAR
Puji dan syukur penulis panjatkan ke hadirat Tuhan Yang Maha Esa, karena atas berkat, karunia, dan rahmat-Nya, penulis dapat menyelesaikan makalah ini sesuai dengan waktunya. Ucapan terima kasih penulis sampaikan kepada berbagai pihak yang telah mendukung dalam proses penyusunan makalah ini. Penulis juga mengucapkan terima kasih kepada Ibu Eny Kusrini dan Ibu Rita Arbianti sebagai dosen pembimbing kelas Kimia Fisika. Makalah ini disusun dalam rangka untuk menyelesaikan tugas mata kuliah Kimia Fisika mengenai Kesetimbangan Kimia.
Penulis menyadari bahwa makalah yang penulis susun ini masih jauh dari kesempurnaan. Oleh karena itu, kritik dan saran yang membangun sangat penulis harapkan agar dapat membuat makalah yang lebih baik dari sebelumnya di masa mendatang. Penulis mengucapkan terima kasih yang telah membantu proses pembuatan makalah ini. Akhir kata, penulis mohon maaf apabila dalam penyusunan makalah ini masih terdapat banyak kesalahan. Semoga makalah ini dapat bermanfaat bagi penulis dan pembaca sehingga dapat meningkatkan pengetahuan mengenai materi-materi yang terdapat dalam makalah ini.
Depok, Desember 2015
DAFTAR ISI
KATA PENGANTAR... ii
DAFTAR ISI ... iii
BAB I: DASAR TEORI ... 1
Pemicu A: Koloid ... 1
1. Definisi dan Jenis-Jenis Koloid... 1
2. Pembuatan Koloid ... 2
3. Penjernihan Air ... 3
Pemicu B: Emulsi ... 4
1. Definisi Emulsi ... 4
2. Komponen Emulsi ... 4
3. Faktor-Faktor yang Mempengaruhi Kestabilan Emulsi ... 5
4. Tipe-Tipe Emulsi ... 6
5. Metode Destabilisasi Emulsi ... 7
Pemicu C: Emulsifier ... 7
1. Proses Pembuatan Emulsifier Food Grade ... 7
2. Cara Memperoleh Kondisi Emulsi yang Stabil ... 8
3. Definisi dan Jenis-Jenis Emulsifier ... 8
4. Hukum Stokes ... 12
BAB II: PEMBAHASAN ... 13
KESIMPULAN ... 39
BAB I
DASAR TEORI
Bagian A: Koloid
1. Definisi dan Jenis-Jenis Koloid
Sistem koloid (koloid) merupakan suatu bentuk campuran (sistem dispersi) dua atau lebih zat yang bersifat homogen namun memiliki ukuran partikel terdispersi yang cukup besar (1 - 100 nm), sehingga menyebabkan efek Tyndall. Bersifat homogen, artinya partikel terdispersi tidak terpengaruh oleh gaya gravitasi atau gaya lain yang dikenakan kepadanya; sehingga tidak terjadi pengendapan. Sifat homogen ini juga dimiliki oleh larutan, namun tidak dimiliki oleh
campuran biasa (suspensi). Koloid mudah dijumpai dimana-mana. Susu, agar-agar, tinta, sampo, serta awan merupakan contoh-contoh koloid yang dapat dijumpai sehari-hari. Sitoplasma dalam sel juga merupakan sistem koloid. Koloid menjadi kajian tersendiri dalam kimia industri karena kepentingannya. Di dalam larutan koloid secara umum, terdapat 2 zat sebagai berikut:
1. Zat terdispersi, yakni zat yang terlarut di dalam larutan koloid. 2. Zat pendispersi, yakni zat pelarut di dalam larutan koloid. Jenis-jenis koloid:
2. Pembuatan Koloid
Dalam proses pembuatannya, koloid mampu dibuat baik secara manual maupun alami yang terdiri dari berbagai macam cara, seperti:
a. Kondensasi
Pembuatan sistem koloid dengan cara kondensasi dilakukan dengan cara menggumpalkan partikel yang sangat kecil. Penggumpalan partikel ini dapat dilakukan dengan cara sebagai berikut:
1) Reaksi Pengendapan
Pembuatan sistem koloid dengan cara ini dilakukan dengan mencampurkan larutan elektrolit sehingga menghasilkan endapan.
Contoh: AgNO3 (aq) + NaCl (aq) —> AgCl (s) + NaNO3 (aq)
2) Reaksi Hidrolisis
Reaksi hidrolisis adalah reaksi suatu zat dengan air. Sistem koloid dapat dibuat dengan mereaksikan suatu zat dengan air.
Contoh: AlCl3 (aq) + H2O (l) —> Al(OH)3 (s) + HCl (aq)
3) Reaksi Redoks
Pembuatan koloid dapat terbentuk dari hasil reaksi redoks.
Contoh: Pemurnian emas
Reaksi: AuCl3 + HCOH —> Au + HCl + HCOOH
4) Reaksi Pergeseran
Contoh: Pembuatan sol As2S3 dengan cara mengalirkan gas H2S kedalam
larutan H3AsO3 encer pada suhu tertentu.
Reaksi: 2 H3AsO3 + 3 H2S —> 6 H2O + As2S3
5) Reaksi Pergantian Pelarut
b. Dispersi
Pembuatan sistem koloid dengan cara dispersi dilakukan dengan memperkecil partikel suspensi yang terlalu besar menjadi partikel koloid, pemecahan partikel-partikel kasar menjadi koloid.
Ada 3 cara dalam pembuatan koloid dengan dispersi, yaitu secara mekanik, peptisasi, dan Busur Bredig.
3.
Penjernihan AirPenjernihan air adalah proses pengolahan air kotor menjadi bersih dan sehat. Proses penjernihan/penyediaan air bersih merupakan proses perubahan sifat fisik, kimia dan biologi air agar memenuhi syarat untuk digunakan sebagai air minum.
Tujuan dari kegiatan pengolahan air minum adalah sebagai berikut: 1. Menurunkan kekeruhan.
2. Mengurangi bau, rasa dan warna.
3. Menurunkan dan mematikan mikroorganisme.
4. Mengurangi kadar bahan-bahan yang terlarut dalam air. 5. Menurunkan kesadahan.
6. Memperbaiki derajat keasaman (pH).
Syarat-syarat kualitas air yang harus dipenuhi diantaranya:
a. Syarat fisik, antara lain:
Air harus bersih dan tidak keruh. Tidak bewarna.
Tidak berasa. Tidak berbau.
Suhu antara 100-250 C (sejuk).
b. Syarat kimia, antara lain :
Tidak mengandung bahan kimia yang mengandung racun. Tidak mengandung zat-zat kimia yang berlebihan.
pH air antara 6,5 – 9,2.
Prinsip penjernihan air dibedakan menjadi 2 yaitu: 1. Prinsip penjernihan air secara fisika
Saringan kapas
Saringan Pasir Lambat (SPL) Saringan Pasir Cepat (SPC) Gravity-Fed Filtering System Saringan Arang
Saringan Air Sederhana Pengendepan (sedimentasi) 2. Prinsip penjernihan air secara kimia
Aerasi
Metode koagulasi
Bagian B: Emulsi
1. Definisi Emulsi
Emulsi merupakan suatu sistem yang tidak stabil, sehingga dibutuhkan zat
pengemulsi atau emulsifier untuk menstabilkannya sehingga antara zat yang
terdispersi dengan pendispersinnya tidak pecah atau keduanya tidak terpisah.
Ditinjau dari segi kepolaran, emulsi merupakan campuran cairan polar dan cairan
non-polar. Salah satu emulsi yang kita kenal sehari-hari adalah susu, di mana lemak
terdispersi dalam air. Dalam susu terkandung kasein suatu protein yang berfungsi
sebagai zat pengemulsi. Beberapa contoh emulsi yang lain adalah pembuatan es
krim, sabun, deterjen, yang menggunakan pengemulsi gelatin.
2. Komponen Emulsi
A. Komponen Dasar
Fase dispersi/fase internal/fase diskontinyu yaitu zat cair terbagi-bagi menjadi
butiran kecil kedalam zat cair lain.
Fase kontinyu/ fase eksternal yaitu zat cair dalam emulsi yang berfungsi
sebagai bahan dasar (pendukung).
Emulgator adalah zat yang berfungsi untuk menstabilkan emulsi.
B. Komponen Tambahan
Colouris
Antioksidant: Asam askorbat, asam sitrat dll.
Preservatif: Asam benzoat, fenol, kresol, klorobutanol.
3. Faktor-Faktor yang Mempengaruhi Kestabilan Emulsi Kestabilan emulsi dipengaruhi oleh berbagai faktor, diantaranya:
Rendahnya tegangan antarmuka
Tidak bercampurnya dua fase cairan dikarenakan tingginya tegangan antarmuka antar kedua fase yang dalam keadaan normal tidak bercampur. Oleh karena itu, diperlukan emulsifier untuk menstabilkan emulsi yang akan terbentuk. Cara emulsifier menstabilkan emulsi yaitu dengan menurunkan tegangan antarmuka antara dua fase yang dalam keadaan normal tidak bercampur. Turunnya tegangan antarmuka pada salah satu fase akan membuat fase terdispersi dapat menyebar dan menjadi fase kontinyu.
Tolakan lapisan rangkap listrik (Electric double layer repulsion)
Terjadinya emulsi karena adanya susunan listrik yang menyelubungi partikel sehingga terjadi tolak-menolak antara partikel sejenis. Terjadinya muatan listrik disebabkan oleh salah satu dari cara berikut:
a. Terjadinya ionisasi dari molekul pada permukaan partikel. b. Terjadinya absorpsi ion oleh partikel dari cairan sekitarnya. c. Terjadinya gesekan partikel dengan cairan sekitarnya.
Adanya tolakan lapisan rangkap listrik mengurangi laju agregasi dan coalescence. Semakin besar tolakan lapisan rangkap listrik, semakin stabil emulsi.
Kecilnya perbedaan densitas antara dua fase
Semakin besar perbedaan densitas antara kedua fase, maka kedua fase akan semakin sulit bercampur dan salah satu fasenya semakin sulit terdispersi. Kecilnya perbedaan densitas antara dua fase dapat menurunkan laju creaming dan agregasi. Semakin kecil perbedaan densitas dua fase, semakin stabil emulsi.
Kecilnya ukuran droplet dan volume fase terdispersi
Viskositas fase pendispersi
Tingginya viskositas fase pendispersi dapat mengurangi laju creaming dan agregasi. Hal ini dikarenakan tingginya viskositas fase pendispersi akan membuat fase yang terdispersi dalam campuran semakin sulit bergerak. Gerak yang dimaksud adalah gerak partikel fase terdispersi yang cenderung berkumpul dengan partikel cairan sejenis dan membuat emulsi tidak stabil. Jadi, semakin tinggi viskositas fase pendispersi, maka semakin stabil emulsi.
Gaya tarik-menarik fase terdispersi
Seperti yang telah dijelaskan sebelumnya, salah satu gaya yang menentukan kestabilan emulsi adalah gaya tarik-menarik antar fase terdispersi (gaya Van Der Waals). Semakin besar gaya tarik-menarik antar partikel fase terdispersi, maka akan semakin membuat emulsi tidak stabil. Hal ini dikarenakan gaya tarik-menarik antar partikel fase terdispersi akan meningkatkan laju agregasi dan coalescence.
4. Tipe-Tipe Emulsi
Pada umumnya dikenal dua tipe emulsi yaitu:
1. Tipe water in oil atau w/o (water/oil)
Emulsi ini mengandung air yang merupakan fase internalnya (diskontinyu) dan minyak merupakan fase eksternalnya (kontinyu). Emulsi tipe w/o umumnya mengandung kadar air yang kurang dari 10–25% dan mengandung sebagian besar fase minyak. Emulsi jenis ini dapat diencerkan atau bercampur dengan minyak, akan tetapi sangat sulit bercampur/dicuci dengan air.
2. Tipe oil in water atau o/w (oil/water)
Merupakan suatu jenis emulsi yang fase terdispersinya berupa minyak yang terdistribusi dalam bentuk butiran-butiran kecil didalam fase kontinyu yang berupa air. Emulsi tipe ini umumnya mengandung kadar air yang lebih dari 31 – 41% sehingga emulsi o/w dapat diencerkan atau bercampur dengan air dan sangat mudah dicuci.
Metode untuk membedakan emulsi o/w dan w/o:
5. Metode Destabilisasi Emulsi
Sistem emulsi dapat didestabilisasi melalui beberapa metode, yaitu:
a. Creaming
Creaming menunjukkan adanya kecenderungan dua fase dalam emulsi untuk memisah karena adanya perbedaan densitas. Dalam creaming, ada kecenderungan fase yang densitasnya lebih kecil untuk terkonsentrasi di atas sistem emulsi. Creaming hanya terjadi pada emulsi yang encer dan kedua fasenya mempunyai densitas yang berbeda, serta medium pendispersinya adalah cairan yang mudah mengalir.
b. Flocculation
Flocculation diartikan sebagai proses dimana dua atau lebih droplet saling menempel tanpa kehilangan identitas. Pada flocculation tidak terjadi penggabungan butiran-butiran kecil menjadi butiran-butiran yang lebih besar.
c. Coalescence
Coalescence adalah proses ketika dua atau lebih droplet bergabung dan membentuk droplet yang lebih besar.
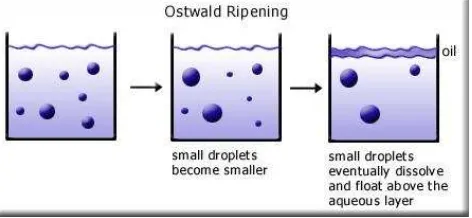
d. Ostwald Ripening
Ostwald ripening terjadi pada emulsi dimana droplet bertabrakan dengan yang lain membentuk droplet yang lebih besar dan lebih kecil. Droplet yang berukuran kecil cenderung menjadi semakin kecil.
Bagian C: Emulsifier
1. Proses Pembuatan Emulsifier Food Grade
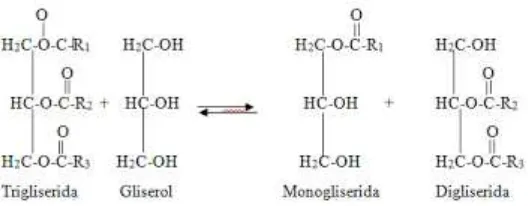
Emulsifier food grade adalah emulsifier yang biasa digunakan dalam industri makanan atau minuman. Salah satu contoh dari emulsifier ini adalah golongan cake emulsifier yang umumnya mempunyai komposisi kimia dari monogliserida dan digliserida.
Gambar 1. Reaksi Pembentukan Monogliserida
2. Cara Memperoleh Kondisi Emulsi yang Stabil
Kondisi emulsi yang stabil dapat diperoleh dengan cara:
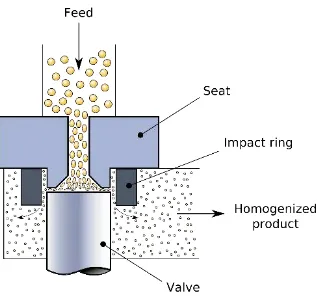
a. Menggunakan kondisi homogenisasi yang optimum untuk memperoleh ukuran partikel terkecil. Proses homogenisasi dapat dilakukan dengan menggunakan alat yang disebut homogenizer. Prinsip alat homogenizer adalah memaksa suatu zat untuk melewati celah yang sempit sehingga ukuran molekul menjadi kecil.
Gambar 2. Homogenizer tipe Valve
b. Menggunakan kombinasi hidrokoloid (stabilizer) yang sesuai untuk memodifikasi viskositas emulsi. Hidrokoloid dapat menstabilkan emulsi dengan membentuk lapisan yang rigid/kaku, bersifat viskoelastik pada permukaan minyak-air. Terbentuknya lapisan ini akan menaikkan viskostas emulsi. Yang termasuk hidrokoloid contohnya adalah gom arab, agar-agar, alginate, caragen, metilselulosa, gelatin, polimer sintetik, protein, dll.
3. Definisi dan Jenis-Jenis Emulsifier
permukaan menjadi hal menarik karena emulsifier memiliki keunikan struktur kimia yang mampu menyatukan dua senyawa berbeda polaritasnya.
Daya kerja emulsifier mampu menurunkan tegangan permukaan yang dicirikan oleh bagian lipofilik (non-polar) dan hidrofilik (polar) yang terdapat pada struktur kimianya. Ukuran relatif bagian hidrofilik dan lipofilik zat pengemulsi menjadi faktor utama yang menentukan perilakunya dalam pengemulsian.
Emulsifier apabila lebih terikat pada air atau lebih larut dalam air (polar) maka dapat lebih membantu terjadinya dispersi minyak dalam air sehingga terjadilah emulsi minyak dalam air (o/w), misalnya pada susu. Emulsifier yang lebih larut dalam minyak (non-polar) menyebabkan terjadinya emulsi air dalam minyak (w/o), contohnya pada mentega dan margarin.
Secara umum emulsifier dapat dibedakan menjadi dua macam, yaitu emulsifier alami dan emulsifier buatan.
1. Emulsifier Alami
Pengemulsi alami dibuat dari bahan-bahan yang berasal dari alam. a. Telur
Telur mengandung lipoprotein dan fosfolipid seperti lesitin yang dikenal sebagai misel. Struktur misel pada lesitin tersebut adalah bagian yang membuat emulsifier tersebut bekerja dengan baik.
b. Kuning dan putih telur
Gelatin dan albumin pada putih telur adalah protein yang bersifat sebagai emulsifier dengan kekuatan biasa dan kuning telur merupakan emulsifier yang paling kuat. Paling sedikit sepertiga kuning telur merupakan lemak, tetapi yang menyebabkan daya emulsifier kuat adalah kandungan lesitin dalam bentuk kompleks sebagai lesitin protein.
c. Gelatin
9 asam amino essensial, satu asam amino essensial yang hampir tidak terkandung dalam gelatin yaitu triptofan.
Penggunaan gelatin sangatlah luas dikarenakan gelatin bersifat serba bisa, yaitu bisa berfungsi sebagai bahan pengisi, pengemulsi (emulsifier), pengikat, pengendap, pemerkaya gizi, sifatnya juga luwes yaitu dapat membentuk lapisan tipis yang elastis, membentuk film yang transparan dan kuat, kemudian sifat penting lainnya yaitu daya cernanya yang tinggi.
d. Kedelai
Kedelai sebagai bahan makanan mempunyai nilai gizi cukup tinggi. Di antara jenis kacang-kacangan, kedelai merupakan sumber protein, lemak, vitamin, mineral dan serat yang paling baik. Di dalam biji kedelai terdapat minyak yang cukup tinggi, di samping air. Keduanya dihubungkan oleh suatu zat yang disebut lecithin. Bahan inilah yang kemudian diambil atau diekstrak menjadi bahan pengemulsi yang bisa digunakan dalam produk-produk olahan.
e. Lesitin
Lesitin (Fosfatidil Kolina) ialah suatu fospolipid yang menjadi komponen utama fraksi fospatida pada ekstrak kuning tel atau kacang kedelai yang diisolasi secara mekanik, maupun kimiawi dengan menggunakan heksana. Lesitin merupakan bahan penyusun alami pada hewan maupun tanaman. Lesitin paling
banyak diperoleh dari kedelai. Penggunaan lesitin yang paling awal adalah pada tahun 1890-an sebagai pengemulsi pada margarin, berupa kuning telur (mengandung lesitin tinggi), dan fosfatida lainnya. Lesitin merupakan bagian integral membran sel, dan bisa sepenuhnya dicerna, sehingga dapat dipastikan aman bagi manusia. Lesitin digunakan secara komersil untuk keperluan pengemulsi dan/atau pelumas, dari farmasi hingga bahan pengemas. Sebagai contoh, lesitin merupakan pengemulsi yang menjaga cokelat dan margarin pada permen tetap menyatu.
f. Tepung Kanji
dipertukarkan. Emulsifier tepung kanji dapat menghasilkan tekstur yang lunak pada zat terdispersi, selain itu juga menghasilkan butiran-butiran yang halus, serta dapat menyatu dengan zat terdispersi. Tepung kanji adalah salah satu tepung yang tidak membentuk gel. Gel yang terbentuk akan membuat bahan makanan tidak dapat teraduk rata serta memiliki viskositas tinggi. Tepung ini sering digunakan untuk membuat makanan dan untuk bahan perekat. Banyak makanan tradisional yang menggunakan tepung kanji atau tapioka sebagai bahan bakunya, seperti bakso, batagor, siomay, comro, misro, cireng, dan pempek.
g. Susu Bubuk
Susu bubuk adalah bubuk yang dibuat dari susu kering yang solid. Susu bubuk mempunyai daya tahan yang lebih lama dari pada susu cair dan tidak perlu disimpan di lemari es karena kandungan uap airnya sangat rendah. Susu bubuk selain sebagai pelengkap gizi, dapat pula berperan sebagai emulsifier dalam proses emulsi suatu bahan pangan yang sangat bagus. Susu bubuk merupakan emulsifier yang baik dari segi tekstur, kemantapan emulsi, ukuran dispersi, maupun rasa. Hal ini dikarenakan susu bubuk merupakan emulsifier yang lebih terikat pada air atau lebih larut dalam air (polar) sehingga dapat lebih membantu terjadinya dispersi minyak dalam air dan menyebabkan terjadinya emulsi minyak dalam air. Bahan pangan yang dalam pembuatannya ditambahkan susu sebagai emulsifier akan
menghasilkan tekstur, aroma, dan rasa yang lebih bagus dibandingkan dengan bahan pangan yang sama yang tidak ditambahkan emulsifier susu. Emulsifier susu bubuk dapat membuat tekstur zat terdispersi menjadi lunak, butiran zat terdispersi menjadi halus, dan meningkatkan kemantapan emulsi.
2. Emulsifier Buatan
Contoh lain dari emulsifier buatan yaitu ester dari asam lemak sorbitan yang dikenal sebagai SPANS yang dapat membentuk emulsi air dalam minyak, dan ester dari polioksietilena sorbitan dengaan asam lemak yang di kenal sebagai TWEEN yang dapat membentuk emulsi minyak dari air. Pada kue-kue, penggunaan SPANS membentuk serta memperbaiki tekstur dan volume, sedang TWEEN membantu mengurangi atau mencegah kekeringan, sehingga kue tetap lunak. Jenis emulsifier lain seperti gliseril laktopalmitat, merupakan emulsifier yang banyak di gunakan dalam pembuatan cakes mixes.
4. Hukum Stokes
Hukum Stokes berbunyi sebagai berikut: “Jika sebuah bola bergerak dalam suatu fluida yang diam maka terhadap bola itu akan bekerja gaya geser dalam
bentuk gaya gesekan yang arahnya berlawanan dengan arah gerak bola tersebut.
Jika sebuah benda padat berbentuk bola dilepas pada permukaan zat cair, bola
tersebut akan mendapatkan percepatan.”
Dengan bertambah besarnya kecepatan bola, maka gaya Stokes yang bekerja pada bola juga bertambah besar sehingga akhirnya bola akan bergerak dengan kecepatan tetap, yaitu setelah terjadi keseimbangan antara gaya-gaya berat, Archimedes, dan Stokes pada bola tersebut.
Syarat-syarat yang diperlukan agar Hukum Stokes dapat berlaku adalah: 1. Ruang tempat fluida terbatas.
2. Tidak ada turbulensi di dalam fluida.
3. Kecepatan v tidak besar sehingga aliran masih linier. Berikut ini adalah penurunan Hukum Stokes.
BAB II
PEMBAHASAN
Bagian A
Air bersih adalah kebutuhan penting dalam kehidupan manusia. Penyediaan kebutuhan air bersih bagi masyarakat merupakan tugas dari PDAM, yang merupakan perusahaan milik daerah yang bergerak di bidang pengolahan dan pendistribusian air bersih. Proses pengolahan air bersih di PDAM dilakukan secara fisika dan kimia. Koagulasi, flokulasi dan sedimentasi merupakan beberapa proses yang terjadi di unit aselator, yang dilakukan untuk mendapatkan air bersih dengan memanfaatkan prinsip sifat-sifat koloid. Bahan-bahan yang biasa digunakan adalah tawas (Al2(SO4)3), karbon aktif, klorin/kaporit, kapur tohor dan pasir.
Pertanyaan:
1. Jelaskan apa yang Anda ketahui tentang koloid, dan jelaskan juga jenis-jenis dari dispersi koloid, serta berikan contoh nya. Tuliskan rujukan anda berdasarkan buku Kimia Fisika yang anda gunakan.
Jawab:
Klasifikasi Koloid a. Koloid Sol
Sol padat (padat dalam padat)
Zat fase padat terdispersi dalam zat fase padat.
Contoh: Logam paduan, kaca berwama, intan hitam, dan baja. Sifat-sifat:
1) Kekerasan dapat ditingkatkan dari kekerasan logam asalnya. 2) Kekuatan tarik dapat diperbesar.
3) Daya pemuaian dapat dikurangkan.
4) Titik lebur dapat diturunkan atau dinaikkan dibanding logam-logam asalnya.
Sol cair (padat dalam cair)
Zat fase padat terdispersi dalam zat fase cair. Berarti, Hal ini berarti zat terdispersi fase padat dan medium fase cair. Contoh: Cat, tinta, dan kanji.
Sol gas (padat dalam gas)
b. Koloid Emulsi
Koloid emulsi terbagi menjadi tiga jenis, yakni sebagai berikut: Emulsi padat (cair dalam padat)
Emulsi padat (gel) ialah koloid dengan zat fase cair terdispersi dalam zat fase padat. Hal ini berarti zat terdispersi fase cair dan medium fase padat. Contoh: mentega, keju, jeli/agar-agar, dan mutiara.
Emulsi cair (cair dalam cair)
Emulsi cair (emulsi) ialah koloid dengan zat fase cair terdispersi dalam zat fase cair. Hal ini berarti zat terdispersi fase cair dan medium fase cair. Contoh: susu, minyak ikan, dan santan kelapa.
Emulsi gas (cair dalam gas)
Emulsi gas (aerosol cair) ialah koloid dengan zat fase cair terdispersi dalam zat fase gas. Hal ini berarti zat terdispersi fase cair dan medium fase gas. Contoh: obat-obat insektisida (semprot), kabut, dan hair spray.
c. Koloid Buih
Kolodi buih terdiri atas dua jenis, yaitu sebagai berikut: Buih padat (gas dalam padat)
Buih padat ialah koloid dengan zat fase gas terdispersi dalam zat fase padat. Hal ini berarti zat terdispersi fase gas dan medium fase padat. Contoh: busa jok dan batu apung.
Buih cair (gas dalam cair)
Buih cair (buih) ialah koloid dengan zat fase gas terdispersi dalam zat fase cair. Berarti, zat terdispersi fase gas dan medium fase cair. Contoh: buih sabun, buih soda, dan krim kocok.
2. Flokulasi merupakan proses reversibel, sedangkan koagulasi adalah ireversibel. Dapatkah Anda menjelaskan tentang proses koagulasi dan flokulasi pada pengolahan air bersih?
Jawab:
a. Koagulasi
Partikel-partikel koloid dapat bersifat stabil karena memiliki muatan listrik sejenis. Apabila muatan listrik itu hilang, maka partikel koloid tersebut akan bergabung membentuk gumpalan. Proses penggumpalan partikel koloid dan pengendapannya disebut koagulasi.
b. Flokulasi
Flokulasi adalah proses penggumpalan bahan terlarut, bersifat koloid, dan yang tidak dapat mengendap dalam air. Flokulasi merupakan proses pembentukan flok yang pada dasarnya menggunakan pengelompokkan aglomerasi antara partikel dengan koagulan (menggunakan proses pengadukkan lambat atau slow mixing). Pada flokulasi terjadi proses penggabungan beberapa partikel menjadi flok yang berukuran besar. Partikel yang ukurannya besar akan lebih mudah diendapkan daripada yang kecil.
3. Proses pembuatan koloid dapat dilakukan dengan dua cara, yaitu cara kondensasi dan cara dispersi. Jelaskan perbedaan antara kedua cara tersebut. Akan lebih baik jika Anda dapat memberikan penjelasan secara visual. Jawab:
Dispersi
Dispersi adalah suatu cara pembuatan larutan koloid dengan mengubah partikel-partikel kasar menjadi partikel koloid yang lebih kecil.
Cara dispersi ini dapat dilakukan dengan cara kimia atau cara mekanik: a. Cara Mekanik
Materi yang besar dihaluskan dengan cara menggunakan penggilingan koloid. Karbon kasar dijadikan halus lalu didispersikan ke dalam air.
b. Cara Peptisasi
pembentukan Al(OH)3 dalam jumlah yang banyak. Endapan tersebut dapat berubah
menjadi koloid apabila ditambah AlCl3. Jika Gas H2S dialirkan ke endapan CaS
atau endapan NiS, maka akan terbentuk sol S yang terdispersi. Endapan ini membentuk sol sulfida.
Kondensasi
Kondensasi adalah cara pembuatan koloid dari partikel kecil (larutan) menjadi partikel koloid. Proses kondensasi ini didasarkan atas reaksi kimia; yaitu melalui reaksi redoks, reaksi hidrolisis, dekomposisi rangkap, dan pergantian pelarut.
a. Reaksi Redoks
Reaksi redoks adalah reaksi yang disertai perubahan bilangan oksidasi. Contoh:
Pembuatan sol belerang dari reaksi antara hidrogen sulfida (H2S) dengan
belerang dioksida (SO2), yaitu dengan mengalirkan gas H2S ke dalam larutan SO2.
H2S(g) + SO2(aq) ⎯⎯→ 2 H2O(l) + 3 S (koloid)
b. Hidrolisis
Hidrolisis adalah reaksi suatu zat dengan air. Contoh:
Pembuatan sol Fe(OH)3 dari hidrolisis FeCl3. Apabila ke dalam air mendidih
ditambahkan larutan FeCl3, maka akan terbentuk sol Fe(OH)3.
FeCl3(aq)+ 3 H2O(l) ⎯⎯→ Fe(OH)3 (koloid) + 3 HCl (aq)
c. Dekomposisi Rangkap Contoh:
Sol As2S3 dapat dibuat dari reaksi antara larutan H3AsO3 dengan larutan
H2S.
2 H3AsO3(aq) + 3 H2S(aq) ⎯⎯→ As2S3(koloid) + 6 H2O(l)
d. Penggantian Pelarut
Contoh:
Apabila larutan jenuh kalsium asetat dicampur dengan alkohol, maka akan terbentuk suatu koloid berupa gel.
4. Partikel koloid dapat bermuatan listrik yang disebabkan oleh sifat-sifat partikel koloid seperti adsorpsi, elektroforesis dan koagulasi. Dapatkah Anda menjelaskan sifat-sifat koloid tersebut, dan sifat koloid lainnya? Berikan contoh untuk setiap sifat yang Anda jelaskan.
Jawab:
Efek Tyndall :
Proses penghamburan cahaya pada partikel koloid.
Dalam kehidupan sehari-hari, contoh efek Tyndall diterapkan pada:
a. Penggunaan lampu sorot mobil pada kondisi cuaca berkabut. Lampu mobil akan lebih terang pada kondisi berkabut daripada kondisi cuaca cerah;
b. Sorot lampu mercusuar yang terlihat lebih terang pada kondisi malam yang berkabut dibandingkan pada malam yang cerah; dan
c. Pada saat ada orang yang merokok di dalam bioskop, sorot lampu proyektor akan terlihat jelas, sedangkan gambar film yang ada di layar tidak terlihat jelas.
Koagulasi
Koagulasi adalah proses penggumpalan partikel koloid dengan menambahkan bahan elektrolit yang berbeda muatan. Dalam kehidupan sehari-hari, contoh penerapan koagulasi dapat ditemukan pada proses-proses berikut.
a. Proses penjernihan air
Pada proses penjernihan air, kita dapat menambahkan tawas KAl(SO ) ke dalam air. Tawas akan membentuk koloid Al(OH) yang akan menggumpalkan
kotoran-kotoran di air, lalu mengendapkannya sehingga kotoran-kotoran tersebut terpisah dari air.
b. Pengolahan karet
c. Proses pembuatan tahu
Tahu dibuat dengan menghaluskan kacang kedelai yang bercampur dengan air, kemudian disaring sehingga diperoleh filtrat susu kedelai. Susu kedelai ditambahkan zat elekrolit CaSO .2H O yang dikenal di kehidupan sehari-hari sebagai batu tahu. Penambahan batu tahu berfungsi untuk menggumpalkan protein
yang ada pada susu kedelai sehingga menjadi tahu. Adsorpsi
Permukaan koloid memiliki kemampuan menyerap ion. Hal ini yang menyebabkan partikel koloid memiliki muatan. Proses penyerapan ion pada permukaan koloid disebut adsorpsi. Dalam kehidupan sehari-hari, sifat adsorpsi dapat dimanfaatkan untuk hal-hal berikut.
a. Pemutihan gula pasir
Gula pasir atau gula tebu yang masih mengandung partikel pengotor akan berwarna cokelat atau berwarna kuning. Gula pasir dapat diputihkan dengan melarutkannya dengan air panas, kemudian dialirkan melalui tanah diatom yang berasal dari rangka tumbuhan air. Gula pasir juga dapat diputihkan dengan menambahkan karbon. Karbon adalah adsorben yang dapat mengikat partikel-partikel zat pengotor gula.
b. Obat sakit perut (norit)
Norit mengandung serbuk karbon yang berasal dari arang kayu tertentu. Norit digunakan sebagai obat sakit perut. Norit di dalam perut akan bercampur dengan cairan yang ada di usus membentuk koloid. Koloid yang terbentuk akan menyerap zat racun atau bakteri patogen yang berada di dalam usus.
c. Deodorant
Deodorant dalam kehidupan sehari-hari digunakan untuk menghilangkan
Koloid Pelindung
Koloid pelindung adalah koloid yang memiliki kemampuan untuk menstabilkan koloid yang lain. Penerapannya dalam kehidupan sehari-hari diantaranya sebagai berikut.
a. Gelatin digunakan dalam pembuatan es krim. Gelatin berfungsi mencegah terjadinya pengkristalan pada es krim agar diperoleh es krim yang lembut.
b. Kasein adalah koloid pelindung yang secara alami terdapat pada susu. Dialisis
Dialisis adalah proses pemisahan koloid dengan larutan sejati melalui selaput membran semipermiabel. Prinsip dialisis dalam kehidupan sehari-hari digunakan untuk membantu pasien yang mengalami masalah dengan ginjal (gagal
ginjal). Pada penderita gagal ginjal, fungsi ginjalnya tidak sempurna. Ginjal berfungsi untuk menyaring darah yang mengandung urea sisa metabolisme tubuh. Seharusnya jika ginjal masih baik, darah yang keluar dari ginjal sudah bersih tidak mengandung urea. Pasien gagal ginjal harus menjalani proses cuci darah dengan menggunakan dialisator sebagai pengganti ginjal.
Elektroforesis
Elektroforesis adalah peristiwa terjadinya pergerakan partikel koloid bermuatan yang dipengaruhi oleh medan listrik. Jenis muatan partikel koloid dapat ditentukan dengan elektroforesis. Penerapan elektroforesis dalam kehidupan sehari-hari adalah untuk mengurangi pencemaran udara. Asap pabrik hasil buangan industri dapat dibersihkan dengan menggunakan alat yang bernama Cottrell. Alat ini menggunakan prinsip elektroforesis. Asap pabrik adalah jenis koloid aerosol padat. Cerobong asap yang dilengkapi plat kawat listrik dialiri asap pabrik. Partikel padat (zat pengotor) yang terdapat dalam asap memiliki muatan. Ketika dialirkan
ke dalam cerobong, partikel ini akan tertarik oleh plat kawat listrik yang berbeda muatan dengan zat pengotor. Kemudian zat pengotor ini akan menggumpal, selanjutnya mengendap ke bawah sehingga asap yang keluar dari cerobong tidak mengandung partikel pengotor lagi.
seperti dengan penambahan tawas, Al2(SO4)3. Jelaskan proses penjernihan
air berdasarkan konsep koloid dari pemicu di atas. Sertakan gambar ataupun video untuk melengkapi penjelasan Anda.
Jawab:
Syarat fisika, antara lain:
Air harus bersih dan tidak keruh. Tidak bewarna.
Tidak berasa. Tidak berbau.
Suhu anta 100-250 C (sejuk).
Proses Penjernihan Air dibedakan menjadi 2 yaitu: 1. Penjernihan air secara fisika (metode penyaringan)
a. Saringan Kain Katun
Merupakan teknik penyaringan air yang paling sederhana. Air keruh disaring dengan menggunakan kain katun yang bersih, bertujuan untuk membersihkan air dari kotoran dan organisme kecil yang ada dalam air keruh.
b. Saringan Kapas
Air disaring dengan kapas yang diletakkan di dasar wadah yang diberi lubang. Bertujuan untuk membersihkan air dari kotoran dan organisme kecil yang ada dalam air keruh.
c. Saringan Pasir Lambat (SPL)
Saringan pasir lambat merupakan saringan air yang dibuat dengan menggunakan lapisan pasir
d. Saringan Pasir Cepat (SPC)
Saringan pasir cepat seperti halnya dengan saringan pasir lambat, terdiri atas lapisan pasir pada bagian atas dan kerikil pada bagian bawah. Tetapi arah penyaringan air terbalik bila dibandingkan dengan saringan pasir lambat, yakni dari bawah ke atas (up flow). Air bersih didapatkan dengan jalan menyaring air baku melewati lapisan kerikil terlebih dahulu baru kemudian melewati lapisan pasir.
e. Grafity-Fed Filtering System
Grafity-Fed Filtering System merupakan gabungan dari SPC dan SPL. Air bersih dihasilkan melalui dua tahap. Pertama-tama air disaring menggunakan SPC. Air hasil penyaringan tersebut kemudian disaring kembali hasilnya dengan menggunakan SPL. Dengan dua tahap penyaringan tersebut diharapkan kualitas air bersih yang dihasilkan
tersebut dapat lebih baik. f. Saringan Arang
g. Saringan Air Sederhana / Tradisional
Saringan Air Sederhana / Tradisional merupakan modifikasi dari saringan arang dengan saringan pasir lambat. Pada saringan tradisional ini selain menggunakan pasir, kerikil, batu dan arang juga ditambahkan satu buah lapisan injik/ijuk yang berasal dari sabut kelapa.
h. Pengendepan (sedimentasi)
Sedimentasi merupakan proses pengendapan bahan padat dari air olahan. Proses sedimentasi bisa terjadi bila air limbah mempunyai berat jenis lebih besar daripada air sehingga mudah tenggelam. Proses pengendapan ada yang bisa terjadi langsung, tetapi adapula yang memerlukan proses pendahuluan, seperti koagulasi atau reaksi kimia. Prinsip sedimentasi adalah pemisahan bagian padat dengan memanfaatkan gaya gravitasi sehingga bagian
yang padat berada di dasar kolam pengendapan, sedangkan air dibagian atas.
i. Prinsip penjernihan air dengan absorpsi dan adsorpsi
Absorpsi merupakan proses penyerapan bahan-bahan tertentu. Dengan penyerapan tersebut air dapat menjadi jernih karena zat-zat di dalamnya diikat oleh absorben.
untuk mengurangi warna serta menghilangkan bau dan rasa. Proses kerja penyerapan (absorpsi) yaitu penyerapan ion-ion bebas di dalam air yang dilakukan oleh absorben. Sebagai contoh, penyerapan ion oleh karbon aktif.
Aplikasi absorpsi yaitu dengan mencampurkan absorben dengan serbuk karbon aktif dengan cara menjadikan karbon aktif sebagai media filtrasi. Apabila absorben dicampurkan dengan serbuk karbon aktif, selanjutnya larutan disaring. Namun apabila karbon aktif digunakan sebagai media penyaring, dipilih karbon aktif yang berbentuk granula dan secara berkala harus dicuci atau diganti dengan yang baru. Disamping dapat mengabsorpsi fenol, karbon aktif juga dapat mengabsorpsi racun dan mikroorganisme.
Adsorpsi merupakan penangkapan/ pengikatan ion-ion bebas di dalam air oleh adsorben. Contoh zat yang digunakan untuk proses adsorpsi adalah zeolit dan resin yang merupakan polimerasi dari polihidrik fenol dengan formaldehid. Contohnya pengikatan ion Ca2+ dan
Na+. Setiap gram resin dapat mengadsorpsi asam 4 – 9 mev. Banyaknya
adsorben yang diperlukan tergantung konsentrasi larutan. Semakin tinggi konsentrasi larutan, semakin besar pula adsorben yang diperlukan untuk
menjernihkan air.
2. Penjernihan air secara Kimia a. Metode Koagulasi
Koagulasi merupakan proses penggumpalan melalui reaksi kimia, reaksi koagulasi dapat berjalan dengan membubuhkan zat pereaksi (koagulan) sesuai dengan zat yang terlarut. Koagulan yang banyak digunakan adalah kapur, tawas dan kaporit.
air limbah maka dilakukan pengadukan dengan mixer statis maupun rapid mixer.
Contoh skema instalasi koagulasi:
b. Metode Aerasi
Aerasi merupakan proses penjernihan air dengan cara mengisikan oksigen ke dalam air. Dengan diisikannya oksigen ke dalam air maka zat-zat
seperti karbon dioksida serta hidrogen sulfida dan metana yang mempengaruhi rasa dan bau dari air dapat dikurangi atau dihilangkan. Selain itu, partikel mineral yang terlarut dalam air seperti besi dan mangan akan teroksidasi dan secara cepat akan membentuk lapisan endapan yang nantinya dapat dihilangkan melalui proses sedimentasi atau filtrasi.
Bagian B
Pertanyaan:
1. Campuran berdasarkan ukuran partikelnya, dibedakan menjadi 3 golongan utama, jelaskan apa saja dan uraikan secara singkat perbedaannya.
Jawab:
Campuran berdasarkan ukuran partikel, dapat dibedakan menjadi tiga golongan yaitu larutan, suspensi, dan koloid. Berikut ini masing-masing penjelasannya:
a. Larutan
Pada larutan, ukuran partikel pelarut (solvent) dan zat terlarut (solute) sebesar molekul tunggal kecil (ion) karena distribusi yang merata (serba sama), maka sifat fisik larutan berbeda dengan pelarutnya, sehingga disebut campuran homogen. Contohnya larutan gula, larutan garam, larutan teh, dan sebagainya.
b. Suspensi
Suspensi adalah campuran heterogen karena masih dapat dibedakan dari zat-zat penyusunnya. Pada suspensi, salah satu komponen partikelnya relatif lebih besar dan terdistribusi dalam partikel lainnya. Contohnya pasir halus dalam air, asap di udara, dan endapan dalam reaksi campuran.
c. Koloid
Koloid juga disebut sistem dispersi, yaitu suatu campuran heterogen yang terbagi rata dan sulit terlihat oleh mata. Koloid dapat diamati dengan menggunakan
ultramikroskop untuk membedakan komponen-komponen penyusunnya. Koloid pada umumnya keruh, tetapi tidak dapat memisah. Susu merupakan contoh dari
koloid.
2. Mayo merupakan salah satu contoh emulsi cair dalam pendispersi cair. Jelaskan apa maksud dari kalimat tersebut. Jelaskan juga jenis emulsi lain yang Anda ketahui. Bagaimana dua fase cairan yang saling tidak menyukai bisa bercampur selama penyimpanan? Jelaskan faktor-faktor apa saja yang dapat mempengaruhi kestabilan emulsi dan bagaimana faktor-faktor tersebut dapat mempengaruhi kestabilan emulsi. Berikan gambaran visual untuk memperjelas keterangan Anda.
Jawab:
pendispersi) asam cuka atau lemon juice juga berwujud cair, dan bagian emulsifiernya adalah kuning telur. Oleh karena itu mayonaise disebut emulsi cair karena medium pendispersinya cair.
Jenis-jenis Emulsi (fase terdispersi cair) Emulsi dibagi menjadi 3, yaitu:
1. Emulsi Padat (Gel)
Emulsi Padat merupakan koloid dengan fase terdipersi cair dan medium
pendispersi padat. Contoh: jelly, keju, mentega, nasi.
2. Emulsi Cair (Emulsi)
Emulsi Cair merupakan koloid dengan fase terdispersi cair dan medium
pendispersi cair. Contoh: susu, mayones, krim.
3. Emulsi gas (Aerosol Cair)
Emulsi Gas merupakan koloid dengan fase terdispersi cair dan medium
pendispersi gas. Contoh: awan, kabut, hairspray, obat nyamuk semprot.
Untuk mencampurkan dua fase cair yang tidak saling menyukai (tidak bercampur) itu karena sifat kepolarannya maka digunakanlah emulsifier atau emulgator. Emulgator merupakan zat yang dapat menstabilkan emulsi sehingga dua cairan yang tidak bercampur akan bercampur seteah penambahan adanya emulgator. Contohnya: sabun, kuning telur, gelatin, kasein dan lain-lain. Emulgator ini memiliki gugus hidrofilik dan gugus hidrofobik. Misalnya antara air dan minyak dimana air bersifat polar sedangkan minyak non-polar, maka
keduanya tidak akan pernah bercampur karena berbeda kepolarannya tapi dengan adanya penambahan emulgator maka keduanya akan bercampur menjadi satu karena bagian yang suka air akan terikat pada bagian hidrofilik sedangkan yang bagian suka minyak akan terikat dengan gugus hidrofobik. Emulgator ini juga menurunkan tegangan permukaan cairan sehingga dua fase zat cair yang berbeda jenis akan mudah bercampur.
Faktor-faktor yang mempengaruhi kestabilan emulsi: Rendahnya tegangan antarmuka
normal tidak bercampur. Oleh karena itu, diperlukan emulsifier untuk menstabilkan emulsi yang akan terbentuk. Cara emulsifier menstabilkan emulsi yaitu dengan menurunkan tegangan antarmuka antara dua fase yang dalam keadaan normal tidak bercampur. Turunnya tegangan antarmuka pada salah satu fase akan membuat fase terdispersi dapat menyebar dan menjadi fase kontinyu. Rendahnya tegangan antarmuka membuat terbentuk dan terjaganya wilayah antarmuka yang besar lebih mudah. Jadi, semakin rendah tegangan antarmuka, semakin stabil emulsi.
Tolakan lapisan rangkap listrik (Electric double layer repulsion) Terjadinya emulsi karena adanya susunan listrik yang menyelubungi partikel sehingga terjadi tolak-menolak antara partikel sejenis. Terjadinya muatan listrik disebabkan oleh salah satu dari cara berikut:
a. Terjadinya ionisasi dari molekul pada permukaan partikel. b. Terjadinya absorpsi ion oleh partikel dari cairan sekitarnya. c. Terjadinya gesekan partikel dengan cairan sekitarnya.
Apabila gaya tolak-menolak antar partikel sejenis lebih besar daripada gaya tarik-menariknya (gaya Van Der Waals), maka emulsi yang terbentuk stabil. Adanya tolakan lapisan rangkap listrik mengurangi laju agregasi dan coalescence. Jadi, semakin besar tolakan lapisan rangkap listrik, semakin stabil emulsi.
Kecilnya perbedaan densitas antara dua fase
Agar terbentuk emulsi yang stabil, densitas antara dua fase tidak boleh terpaut terlalu jauh. Semakin besar perbedaan densitasnya, maka dua fase akan semakin sulit bercampur dan salah satu fasenya semakin sulit terdispersi. Kecilnya perbedaan densitas antara dua fase dapat menurunkan laju creaming dan agregasi. Jadi, semakin kecil perbedaan densitas dua fase, semakin stabil emulsi.
Kecilnya ukuran droplet dan volume fase terdispersi
Ukuran droplet dan volume fase terdispersi berpengaruh terhadap kestabilan emulsi. Semakin besar ukuran droplet dan semakin banyaknya volume fase terdispersi, maka akan semakin besar juga peluang terbentuknya agregat. Oleh karena itu, semakin kecil ukuran droplet dan volume fase terdispersi maka semakin berkurang laju agregasi. Dengan demikian dapat disimpulkan bahwa kecilnya ukuran droplet dan volume fase terdispersi, maka semakin stabil emulsi.
Viskositas fase pendispersi
Gaya tarik-menarik fase terdispersi
Seperti yang telah dijelaskan sebelumnya, salah satu gaya yang menentukan kestabilan emulsi adalah gaya tarik-menarik antar fase terdispersi (gaya Van Der Waals). Semakin besar gaya tarik-menarik antar partikel fase terdispersi, maka akan semakin membuat emulsi tidak stabil. Hal ini dikarenakan gaya tarik-menarik antar partikel fase terdispersi akan meningkatkan laju agregasi dan coalescence.
Sebagai gambaran, perhatikan gambar berikut:
(a) Emulsi Stabil (b) Emulsi Tidak Stabil
Faktor-faktor yang mempengaruhi kestabilan emulsi yang telah disebutkan di atas akan menentukan kondisi emulsi stabil (a) ataupun tidak stabil (b). Contohnya pengaruh dari tegangan antarmuka, tingginya tegangan antarmuka akan membuat suatu emulsi menjadi tidak stabil (b), terlihat dari bagaimana campuran dua fase terlihat jelas terpisah. Namun, ketika ditambahkan emulsifier yang berfungsi menurunkan tegangan antarmuka maka fase terdispersi suatu emulsi dapat menyebar secara merata dalam fase pendispersi. Meratanya sebaran fase terdispersi (tidak berkumpul lagi seperti gambar b) ini yang mengindikasikan bahwa emulsi telah menjadi stabil (a). Contoh lainnya yaitu pengaruh viskositas fase pendispersi dan gaya antar partikel fase terdispersi yang bekerja dalam emulsi. Viskositas fase pendispersi yang tinggi akan membuat partikel fase terdispersi sulit untuk bergerak dalam emulsi dan sulit untuk berkumpul seperti gambar b. Sehingga dengan adanya viskositas fase pendispersi yang tinggi akan membuat partikel terdispersi stabil menyebar merata seperti yang ditunjukkan pada gambar a. Sementara gaya antar partikel fase terdispersi yang bekerja dalam emulsi dibagi menjadi dua yaitu gaya tolak-menolak dan gaya tarik-menarik (gaya Van Der Waals). Apabila gaya tarik-menarik lebih besar daripada gaya tolak-menolak, hal yang terjadi adalah partikel fase terdispersi cenderung berkumpul dan membentuk emulsi tidak stabil (b). Sementara apabila gaya tolak-menolak lebih besar daripada gaya tarik-menariknya maka patikel fase terdispersi cenderung tidak berkumpul, tetapi menyebar secara merata membentuk emulsi stabil (a).
3. Ada 2 tipe pembentukan emulsi, yaitu oil in water emulsion dan water in oil emulsion. Jelaskan ke dua tipe tersbut dalam bentuk diagram, simbol, karakteristik dan juga contohnya. Adakah metode yang dapat digunakan untuk membedakan antara emulsi o/w dan emulsi w/o? Jelaskan.
Pada umumnya dikenal dua tipe emulsi yaitu:
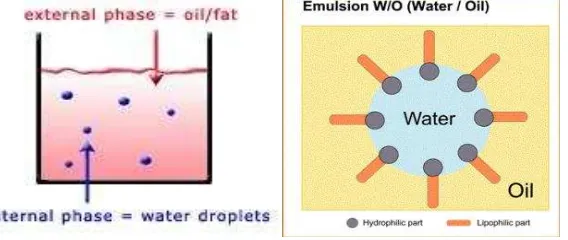
1. Tipe water in oil atau w/o (water/oil)
Emulsi ini mengandung air yang merupakan fase internalnya (diskontinyu) dan minyak merupakan fase eksternalnya (kontinyu). Emulsi tipe w/o umumnya mengandung kadar air yang kurang dari 10 – 25% dan mengandung sebagian besar fase minyak. Emulsi jenis ini dapat diencerkan atau bercampur dengan minyak, akan tetapi sangat sulit bercampur/dicuci dengan air.
Emulsi jenis ini bersifat non-polar, maka molekul–molekul emulsifier tersebut akan teradsorpsi lebih kuat oleh minyak dibandingkan oleh air. Akibatnya tegangan permukaan minyak menjadi lebih rendah sehingga mudah menyebar menjadi fase kontinyu.
Karakteristik dari emulsi tipe ini adalah terasa greasy (berminyak) dan dapat dengan minyak atau pelarut non polar. Contohnya: mentega, cream, selai kacang, semir, margarine, lipstick, coklat batangan.
Gambar 3. Diagram emulsi water in oil (Sumber: Suryani, Ani. Emulsi)
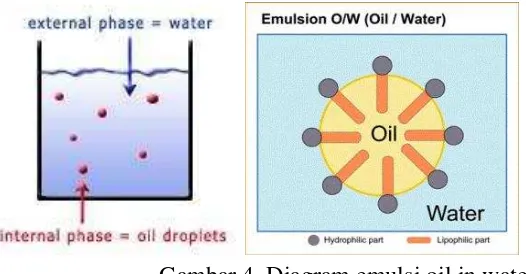
2. Tipe oil in water atau o/w (oil/water)
Merupakan suatu jenis emulsi yang fase terdispersinya berupa minyak yang terdistribusi dalam bentuk butiran-butiran kecil di dalam fase kontinyu yang berupa air. Emulsi tipe ini umumnya mengandung kadar air yang lebih dari 31 – 41% sehingga emulsi o/w dapat diencerkan atau bercampur dengan air dan sangat mudah dicuci.
Emulsi ini bersifat polar maka molekul–molekul emulsifier tersebut akan teradsorpsi lebih kuat oleh air dibandingkan minyak. Akibatnya tegangan permukaan air menjadi lebih rendah sehingga mudah menyebar menjadi fase kontinyu.
Gambar 4. Diagram emulsi oil in water (Sumber: Suryani, Ani. Emulsi)
Metode untuk membedakan emulsi o/w dan w/o a. Metode penampakan visual
Emulsi tipe o/w biasanya berwarna putih dan agak creamy. Sedangkan emulsi w/o berwarna lebih gelap dan menunjukkan tekstur minyak.
b. Metode pengenceran tetesan
Metode ini berdasarkan prinsip bahwa suatu emulsi akan bercampur dengan zat yang sesuai dengan kepolaran fase kontinyunya. Misalnya suatu emulsi tipe o/w akan lebih mudah diencerkan dengan penambahan air, begitu juga sebaliknya dengan tipe w/o.
c. Metode kelarutan pewarna
Metode ini berdasarkan prinsip keseragaman dispersi pewarna dalam emulsi. Misalnya amaranth, yang merupakan pewarna yang larut dalam air, maka akan terdispersi seragam pada emulsi tipe o/w. Sudan III, merupakan pewarna yang larut dalam minyak, maka akan terdispersi seragam pada emulsi tipe w/o.
d. Metode penyerapan
Metode ini menggunakan kertas filter yang berdasarkan sifat kapilaritas air yang lebih tinggi daripada minyak (misalnya CoCl2). Benda dengan permukaan
licin dapat digunakan untuk mengamati kecepatan alir emulsinya. Jika tetesan emulsi ini tersebar merata, berarti emulsi ini bertipe o/w. jika emulsi tidak tersebar merata, berarti emulsi bertipe w/o.
e. Metode konduktivitas elektrik
f. Metode fluorosensi
Sangat banyak minyak yang dapat berfluorosensi jika terpapar sinar UV. Jika setetes emulsi diuji di bawah paparan sinar UV dan diamati di bawah mikroskop menunjukkan seluruh daerah berfluorosensi, maka tipe emulsi itu adalah w/o. Jika emulsi bertipe w/o, maka fluorosensi hanya berupa noda.
4. Bahan dasar mayo adalah minyak nabati, tapi rasa minyak nabati dalam mayo ini sudah tidak ada. Dapatkah anda menjelaskan secara saintifik dan bagaimana setiap molekul minyak dapat dikelilingi oleh mikromolekul dari larutan asam?
Jawab:
Mayonnaise adalah salah satu jenis saus yang dibuat dari bahan utama minyak nabati, telur ayam, dan cuka. Mayonnaise biasanya digunakan sebagai perasa pada makanan seperti salad atau sandwich. Secara ilmiah, mayonnaise termasuk dalam campuran koloid jenis emulsi permanen. Untuk mencapai kestabilan emulsi yang tinggi, diperlukan bahan ketiga yang mampu membentuk sebuah selaput (film) di sekeliling butiran yang terdispersikan sehingga mencegah bersatunya kembali butir-butir zat terdispersi tersebut. Bahan ketiga inilah yang disebut sebagai emulsifier atau stabilizer.
Dalam sistem mayonnaise, yang berfungsi sebagai emulsifier adalah kuning telur. Dalam kuning telur, terkandung zat lesitin dalam bentuk kompleks sebagai lesitoprotein dan berfungsi sebagai surfaktan. Surfaktan adalah zat aktif permukaan yang diadsorpsi pada antar muka suatu cairan, dalam hal ini adalah permukaan antara minyak dan air lemon (asam). Surfaktan berfungsi untuk menurunkan tegangan permukaan antar muka sehingga kedua zat tersebut dalam saling larut satu dengan yang lainnya.
5. Sistem emulsi dapat didestabilisasi melalui beberapa metode, yaitu creaming, flocculation, coalescence dan Ostwald Ripening. Jelaskan secara prinsip metode-metode tersebut, dan gunakan rujukan yang sesuai.
Jawab:
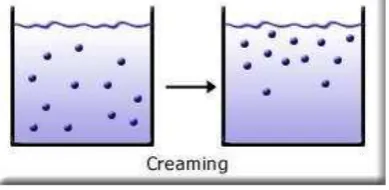
Creaming
Creaming menunjukkan adanya kecenderungan dua fase dalam emulsi untuk memisah karena adanya perbedaan densitas. Dalam creaming, ada kecenderungan fase yang densitasnya lebih kecil untuk terkonsentrasi di atas sistem emulsi. Creaming hanya terjadi pada emulsi yang encer dan kedua fasenya mempunyai densitas yang berbeda, serta medium pendispersinya adalah cairan yang mudah mengalir. Jika fase terdispersinya memiliki densitas yang lebih besar dari medium pendispersinya, maka proses creaming akan berlangsung di bawah sistem emulsi.
Gambar 5. Creaming Flocculation
Flocculation diartikan sebagai proses dimana dua atau lebih droplet saling menempel tanpa kehilangan identitas. Pada flocculation tidak terjadi penggabungan butiran-butiran kecil menjadi butiran-butiran yang lebih besar. Butir-butir yang mengelompok dapat didispersikan kembali dengan pengadukan atau pengocokan apabila gaya Van Der Waalsnya lemah.
Gambar 6. Flocculation Coalescence
Gambar 7. Coalescense Ostwald Ripening
Ostwald ripening terjadi pada emulsi dimana droplet bertabrakan dengan yang lain membentuk droplet yang lebih besar dan lebih kecil. Droplet yang berukuran kecil cenderung menjadi semakin kecil.
Gambar 8. Ostwald Ripening
Bagian C
Belakangan ini perkembangan ilmu dan teknologi pangan kian pesat. Berbagai produk pangan olahan mampu dihasilkan guna memenuhi permintaan konsumen yang makin beragam. Sekarang ini tidak lah sulit menemukan es krim, saus, roti yang teksturnya lembut, mayonaise, margarin, mentega, dan berbagai produk olahan lainnya. Pengembangan produk pangan baru berbasis emulsi ini tidak lepas dari peran ganda si emulsifier, yang dapat menggabungkan antara minyak dengan air, dan juga menjaga agar kestabilan emulsi dapat berlangsung dalam waktu yang lama.
Pertanyaan:
1. Benarkah penggunaan emulsifier dapat digunakan untuk menstabilisasi emulsi? Jelaskan dan berikan rujukan sebagai dasar penjelasan Anda. Berikan satu contoh emulsifier food grade, dan jelaskan proses pembuatan emulsifier tersebut.
Alasan Emulsifier dapat Menstabilisasi Emulsi
Benar, penggunaan emulsifier dapat digunakan untuk menstabilisasi emulsi. Emulsifier merupakan bahan yang digunakan untuk mengurangi tegangan permukaan antara dua fase yang dalam keadaan normal tidak bercampur, sehingga keduanya dapat teremulsi. Emulsifier diperlukan untuk memfasilitasi terbentuknya emulsi, sebab dispersi minyak dan air tidak stabil (secara termodinamik). Emulsifier dapat digunakan untuk menstabilkan emulsi karena memiliki kedua gugus penting, yaitu gugus hidrofilik dan gugus lipofilik.
Adanya gugus hidrofilik dan gugus lipofilik menyebabkan emulsifier memiliki kemampuan untuk menyatukan dua jenis bahan yang tidak saling larut. Dalam emulsifier, salah satu gugus harus lebih dominan jumlahnya. Bila gugus hidrofiliknya (polar) yang lebih dominan, maka molekul-molekul emulsifier tersebut akan diadsorpsi lebih kuat oleh air dibandingkan dengan minyak. Akibatnya tegangan permukaan air menjadi lebih rendah sehingga mudah menyebar dan menjadi fase kontinyu.
Secara umum, emulsifier akan diadsorpsi oleh medium pendispersi lebih besar dari zat yang terdispersi. Kemudian proses adsorpsi emulsifier ini akan menurunkan tegangan permukaan dari medium pendispersi yang lebih besar daripada zat yang terdispersi, sehingga terbentuklah suatu lapisan terpisah dan terjadi emulsi. Lapisan ini akan menyelimuti partikel dan akan mencegah partikel tersebut bersatu dengan partikel sejenis.
Proses Pembuatan Emulsifier Food Grade
Emulsifier food grade adalah emulsifier yang biasa digunakan dalam industri makanan atau minuman. Salah satu contoh dari emulsifier ini adalah golongan cake emulsifier. Umumnya, komposisi kimia dari cake emulsifier adalah monogliserida dan digliserida. Oleh karena itu, berikut ini akan dijelaskan mengenai proses pembuatan emulsifier monogliserida.
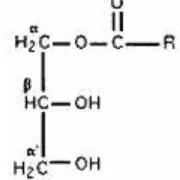
Gambar 9. Struktur Kimia Monogliserida
Gambar 10. Reaksi Pembentukan Monogliserida
Pada proses pembuatan monogliserida, lemak, atau minyak dicampur dengan gliserol berlebih pada kenaikan temperatur (220-240oC atau 425-440oF)
dengan melibatkan katalis alkali, biasanya berupa natrium atau kalsium hidroksida (0,1% berat minyak). Namun sebelumnya, reaktan didehidrasi dahulu pada temperatur 220-240oF selama 30 menit. Selama proses reaksi, campuran reaksi tetap dipertahankan sampai radikal asam lemak trigliserida didistribusikan kembali secara acak di antara grup hidroksil gliserol yang tersedia. Reaksi dilakukan dengan pengadukan selama 30 sampai 60 menit.
Campuran reaksi kemudian didinginkan dengan pengadukan sampai kesetimbangan dicapai dan kemudian katalis dideaktivasi dengan menambahkan asam fosfor (0,1%). Garam fosfat yang dihasilkan dari netralisasi katalis harus dikeluarkan dengan filtrsi. Gliserol berlebih akan dipisahkan, sebagai lapisan bawah selama pendinginan, secara parsial dengan dekantasi. Sedangkan gliserol yang tersisa dalam campuran reaksi dapat dikeluarkan melalui distilasi vakum yang sementara itu juga dilakukan steam stripping untuk mengurangi kandungan asam lemak bebas dan memindahkan material oksidasi yang menyebabkan rasa dan bau yang tidak diinginkan.
Reaksi gliserolisis menggunakan katalis asam maupun alkali basa, berlangsung pada temperatur yang tinggi (200-240oC). Hasilnya merupakan suatu campuran kasar dari monogliserida dan digliserida (tampak hampir sama) serta trigliserida yang tidak terkonversi (konversi overall 90%). Proses pemisahan lebih lanjut biasanya dilakukan dengan distilasi molekular yang menghasilkan kemurnian monogliserida di atas 90%.
2. Bagaimana cara memperoleh kondisi emulsi yang stabil? Perlukah anda tahu ukuran dan densitas partikel untuk menjaga kestabilan emulsi? Jelaskan.
Jawab:
Cara memperoleh kondisi emulsi yang stabil:
alat yang disebut homogenizer. Prinsip alat homogenizer adalah memaksa suatu zat untuk melewati celah yang sempit sehingga ukuran molekul menjadi kecil.
Gambar 11. Homogenizer tipe Valve
b. Menggunakan kombinasi hidrokoloid (stabilizer) yang sesuai untuk memodifikasi viskositas emulsi. Hidrokoloid dapat menstabilkan emulsi dengan membentuk lapisan yang rigid/kaku, bersifat viskoelastik pada permukaan minyak-air. Terbentuknya lapisan ini akan menaikkan viskositas emulsi.
Untuk mendapatkan kondisi emulsi yang stabil, maka perlu diketahui terlebih dahulu faktor-faktor apa saja yang mempengaruhi kestabilan emulsi. Faktor-faktor tersebut di antaranya adalah ukuran dan densitas partikel, sehingga penting untuk mengetahui kedua faktor tersebut untuk menjaga kestabilan emulsi. Ukuran partikel fase terdispersi berpengaruh terhadap kestabilan emulsi. Semakin besar ukuran partikel, maka akan semakin besar juga peluang terbentuknya agregat. Oleh karena itu, semakin kecil ukuran partikel maka semakin berkurang laju agregasi. Dengan demikian kecilnya ukuran partikel akan menjaga kestabilan emulsi.
Densitas partikel baik fase terdispersi maupun medium pendispersi berpengaruh terhadap kestabilan emulsi. Agar terbentuk emulsi yang stabil, densitas antara dua fase tidak boleh terpaut terlalu jauh. Semakin besar perbedaan densitasnya, maka dua fase akan semakin sulit bercampur dan salah satu fasenya semakin sulit terdispersi. Kecilnya perbedaan densitas antara dua fase dapat menurunkan laju creaming dan agregasi. Jadi, semakin kecil perbedaan densitas dua fase, semakin terjaga kestabilan emulsi.
Jawab:
Sedimentasi (pengendapan) merupakan salah satu cara pemisahan padatan yang tersuspensi dalam suatu cairan di mana akan terjadi peristiwa turunnya partikel–partikel padat yang semula tersebar atau tersuspensi dalam cairan karena adanya gaya berat atau gaya gravitasi. Selama proses sedimentasi ini berlangsung, terdapat tiga gaya yang berpengaruh gaya gravitasi, gaya apung, gaya dorong.
Proses sedimentasi terjadi karena zat-zat sedimen mengalami penurunan kecepatan atau berhenti sama sekali. Selain itu, sedimentasi juga dapat terjadi karena gaya
berat benda lebih besar dari gaya tekan ke atas (gaya apung). Partikel-partikel pada sistem emulsi di bawah pengaruh gaya gravitasi biasanya memiliki kecepatan rendah karena perbedaan densitas yang kecil antara partikel dengan medium emulsi. Laju sedimentasi atau laju creaming partikel-partikel bulat yang tersuspensi berbanding terbalik dengan viskositas, sesuai dengan hukum Stoke. Bila semua variabel dijaga konstan, kenaikan viskositas umumnya meminimumkan creaming atau terjadi pengendapan.
4. Laju pergerakan partikel dalam sedimentasi dapat ditentukan dengan Hukum STOKE. Jelaskan prinsip-prinsip dari hukum Stoke dan berikan contoh penggunaan hukum tersebut.
Jawab:
Prinsip dari Hukum Stokes adalah gaya yang menghambat bola bergerak melalui cairan kental berbanding lurus dengan kecepatan bola, jari-jari bola, dan viskositas fluida.
5. Secara prinsip aplikasi emulsifier sangat meluas untuk berbagai produk makanan ataupun produk lain. Adakah keuntungan ataupun kerugian dalam penggunaan emulsifier? Jelaskan!
Jawab:
Keuntungan dari penggunaan emulsifier adalah:
1. Membantu mencegah pemisahan dari bahan-bahan yang digunakan (contohnya air dan minyak).
2. Mencegah pembentukkan jamur jika lemak dan minyak terpisah.
Kelemahan dari penggunaan emulsifier adalah:
1. Dapat menimbulkan alergi kepada beberapa orang, sehingga dapat berbahaya.
KESIMPULAN
Koloid merupakan suatu bentuk campuran (sistem dispersi) dua atau lebih zat yang bersifat homogen namun memiliki ukuran partikel terdispersi yang cukup besar (1-100 nm). Koloid mudah ditemukan dan banyak digunakan dalam kehidupan sehari-hari. Hal ini tidak terlepas dari manfaat yang dimiliki koloid. Contohnya yaitu proses pengolahan dan penjernihan air yang menerapkan prinsip dari sifat-sifat koloid. Contoh lainnya yaitu mayonnaise, koloid yang digunakan sebagai salah satu penyedap makanan.
DAFTAR PUSTAKA
Aimyaya. 2015. Kumpulan Teknik Penyaringan Sederhana. [ONLINE] Available at: http://aimyaya.com/id/tag/saringan/. [Accessed 22 November 2015].
Anief, M. 2000. Sistem Dispersi, Formulasi Suspensi dan Emulsi. Gadjah Mada
UniversityPress: Yogyakarta.
Anonym. 2015. Hukum Stokes. [ONLINE] Available at: https://www.scribd.com/doc/84239809/Hukum-Stokes. [Accessed 30 November 2015].
Anonym. 2015. Stokes' law | Define Stokes' law at Dictionary.com. [ONLINE] Available at: http://dictionary.reference.com/browse/stokes--law. [Accessed 30 November 2015].
Ansel, C.Howard. 2005. Pengantar Bentuk Sediaan Edisi keempat. Jakarta: UI Press.
Atkins, Peter Julia. 2006. Physical Chemistry 8th ed. Great Britain: Oxford University Press.
Brown, Amy. 2014. Understanding Food: Principles and Preparation, Fifth Edition. Stamford: Cengage Learning.
Levine, I. 1983. Physical Chemistry. Second Edition. Mcgraw-Hill Book Company: NewYork.
Liiy Dyaa. 2015. Sedimen Febri - Documents. [ONLINE] Available at: http://documents.tips/documents/sedimen-febri.html. [Accessed 30 November 2015].
Moechtar. 1989. Farmasi Fisika Bagian Larutan Dan Sistem Dispers. Universitas
GadjahMada: Yogyakarta.
Pages, Ramadhani. 2014. Tegangan Permukaan Proses Pembuatan Mayonaise. [ONLINE] Available at:
https://www.academia.edu/9643813/Aplikasi_Tegangan_Permukaan_pada_ Pembuatan_Mayones. [Accessed 20 November 2015].
Paye, et al. 2001. Handbook of Cosmetic Science and Technology. New York: Marcel Dekker, Inc.
Schramm, Laurier L. 2009. Surfactants Fundamentals and Apllications in the Petroleum Industry. 1st ed. Cambridge: Cambridge University Press.
Sukardjo. 1989. Kimia Fisika. Penerbit Rineka Cipta: Yogyakarta.
Tirto Prakoso, dkk. 2009. Pembuatan Monogliserida. [ONLINE] Available at: http://citation.itb.ac.id/pdf/JURNAL/JTKI/JTKI%202007%203%20DES/JT KI%206(3)%20689-698%20PEMBUATAN%20MONOGLISERIDA.pdf. [Accessed 21 November 2015].
Zaka. 2013. Jenis Campuran Berdasarkan Ukuran Partikel. [ONLINE] Available