INTISARI
Ekstrak kulit buah manggis (Garcinia mangostana L.) diketahui memiliki banyak manfaat salah satunya sebagai antioksidan. Sifat fisik suatu sediaan krim dapat dipengaruhi oleh emolien dan humektan dalam formula yang digunakan. Parafin cair berperan sebagai emolien yang menjaga stabilitas campuran antara fase minyak dan fase air dalam sediaan krim, sedangkan gliserol digunakan sebagai humektan yang menjaga kelembapan kulit ketika sediaan diaplikasikan ke kulit. Penelitian ini bertujuan untuk mengetahui pengaruh komposisi parafin cair dan gliserol pada daerah optimum, pengaruhnya terhadap sifat fisik dan stabilitas fisik setelah 6 siklus freeze-thaw sediaan krim serta mengetahui aktivitas antioksidan sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.).
Penelitian ini merupakan penelitian eksperimental dengan menggunakan rancangan penelitian desain faktorial yang menggunakan dua faktor yang berbeda yaitu parafin cair dan gliserol dengan dua level yaitu level tinggi dan level rendah. Respon sifat fisik dan stabilitas fisik sediaan krim diketahui dengan menguji organoleptis, pH, daya sebar, viskositas dan pemisahan fase sediaan krim ekstrak kulit buah manggis. Data viskositas dan daya sebar dianalisis dengan menggunakan Design Expert® versi 10 dan R Studio.
Hasil penelitian menunjukkan parafin cair memberikan efek dominan pada respon daya sebar sebesar 68,39% sedangkan gliserol memberikan efek dominan pada respon viskositas 29,19%. Area komposisi optimum parafin cair dan gliserol ditentukan dengan superimposed contourplot respon viskositas dan daya sebar sediaan krim ekstrak kulit buah manggis. Sediaan krim ekstrak kulit buah manggis stabil secara organoleptis, pH, daya sebar, viskositas dan pemisahan fase, serta memiliki nilai aktivitas antioksidan yang sangat lemah yaitu ditunjukkan dengan penurunan aktivitas antioksidan > 100%.
ABSTRACT
Mangosteen rind extract (Garcinia mangostana L.) is known to has a lot of benefits, one of them is as an antioxidant. Physical properties of cream can be affected by emollient and humectant in the formula. Mineral Oil or Liquid Paraffin is an emollient that can maintain the mixture stability between oil phase and water phase in cream, while Glycerol is a humectant which maintain the humidity when applied to the skin. This research aims to know the effect of Mineral Oil and Glycerol composition at optimum areas, their effect on the physical stability and properties after 6 cycles of freeze-thaw stability testing and to find out the antioxidant activiy of Mangosteen rind (Garcinia mangostana L.) extract in cream formulation.
This research is a design factorial experimental research that use two different factors which are Mineral Oil and Glycerol and two levels whish are high and low. Physical properties and stability of cream were knew by looking at organoleptic, pH, spreadability, viscosity and sedimentation of Mangosteen rind (Garcinia mangostana L.) extract in cream formulation. The spreadability and viscosity respons of cream are analyzed by Design Expert® 10th version and R studio.
The result shows that Mineral Oil contribute a dominant effect in 68,39% of cream’s spreadability respon and the otherwise, Glycerol contribute a dominant effect in 29,19% of cream’s viskosity response. The optimum area of Mineral Oil and Glycerol is found by superimposed contourplot of viskosity and spreadability responses. Cream is stable in organoleptic, pH, spreadability, viskosity and sedimentation, and also cream has a very weak antioksidan activity which is showed by > 100% antioxidant activity reduction..
OPTIMASI PARAFIN CAIR SEBAGAI EMOLIEN DAN GLISEROL SEBAGAI HUMEKTAN DALAM SEDIAAN KRIM EKSTRAK KULIT
BUAH MANGGIS (Garcinia mangostana L.) SERTA UJI AKTIVITAS
ANTIOKSIDAN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Vinsensia Septima Ria Yovita
NIM : 128114123
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
OPTIMASI PARAFIN CAIR SEBAGAI EMOLIEN DAN GLISEROL SEBAGAI HUMEKTAN DALAM SEDIAAN KRIM EKSTRAK KULIT
BUAH MANGGIS (Garcinia mangostana L.) SERTA UJI AKTIVITAS
ANTIOKSIDAN
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Vinsensia Septima Ria Yovita
NIM : 128114123
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
Halaman Persembahan
Mengejar tujuan dengan sungguh-sungguh dengan disertai
niat yang tulus serta bantuan dari Tuhan merupakan kunci utama supaya cepat LULUS.
vii PRAKATA
Puji Syukur kehadirat Tuhan Yang Maha Esa karena berkat rahmat dan kasih setia-Nya, penulis dapat menyelesaikan skripsi yang berjudul “Optimasi Parafin Cair Sebagai Emolien dan Gliserol Sebagai Humektan dalam Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia Mangostana L.) Serta Uji Aktivitas Antioksidan” dengan baik. Skripsi ini disusun untuk memenuhi salah satu syarat mendapat gelar sarjana Farmasi (S.Farm.) program studi Farmasi.
Selama proses perkuliahan, penelitian hingga selesai penyusunan skripsi, penulis banyak mendapat dukungan dan bantuan dari berbagai pihak. Dengan penuh syukur, penulis mengucapkan terimakasih kepada:
1. Tuhan Yesus, Bunda Maria dan Roh Kudus yang selalu memberikan kekuatan, kesabaran, semangat dan berkat yang selama ini talah diberikan kepada penulis. 2. Keluargaku yang terkasih, Papa, Mama, Oma (alm.), Opa (alm.), Kungkung (alm.), Pho-pho, Ooh Steven, Bella, Tony dan Mbak Widji yang telah memberikan semangat, doa, nasehat dan dukungan kepada penulis.
3. Ibu Aris Widyawati, M. Si., Ph.D., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
viii
5. Ibu Agustina Setyawati, M. Si., Apt., selaku kepala laboratorium Fakultas Farmasi atas segala kesabaran, semangat dan bantuan selama proses penelitian skripsi.
6. Segenap tim dosen penguji atas waktu dan kesediaan untuk menguji penulis. 7. Segenap dosen Fakultas Farmasi Universitas Sanata Dharma Yogyakarta yang
telah memberikan ilmu, pengalaman serta nasehat selama perkuliahan penulis. 8. Bapak Musrifin, Mas Agung, Pak Kayatno, Pak Kunto, Pak Parlan, Pak
Wagiran dan laboran Fakultas Farmasi lainnya atas segala bantuan dan semangat selama penelitian berlangsung.
9. Linda Evelina Larisa, Lotmi Sabaretnam Barasa, Clarisa Dian, Agatha Riona Oktavianus, Adriana Cindy Salim, Desion Sudi, Buana Cahya Wijaya, Giovani Anggasta Febrinda, Vicky Wijoyo dan Bernardus Anggi P., atas dukungan, kerjasama serta suka-duka yang dialami selama proses penyusunan skripsi. 10. Semua teman-teman angkatan 2012, khususnya FST B 2012 dan FSM C 2012
atas kebahagian, canda-tawa dan kebersamaan selama perkuliahan.
11. Semua pihak yang penulis tidak dapat sebutkan satu persatu, yang telah membantu dalam proses penyususnan skripsi
Penulis menyadari bahwa masih banyak kekurangan dalam penyusunan skripsi ini, sehingga penulis mengharapkan adanya kritik dan saran yang membangun. Semoga skripsi ini dapat berguna, terutama di bidang kesehatan.
Yogyakarta, 20 Juni 2016
ix DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
PERSETUJUAN PUBLIKASI ... vi
PRAKATA ... vii
DAFTAR ISI ... ix
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvii
INTISARI ... xviii
ABSTRACT ... xix
BAB I. PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Rumusan Masalah ... 3
C. Keaslian Penelitian ... 4
D. Manfaat Penelitian ... 5
E. Tujuan Penelitian ... 5
BAB II. PENELAAHAN PUSTAKA... 7
x
B. Antioksidan ... 8
C. Manggis ... 9
1. Taksonomi Tanaman ... 9
2. Deskripsi Umum ... 10
3. Manfaat dan Kegunaan ... 10
D. Krim ... 12
E. Paraffin Cair ... 14
F. Gliserol ... 14
G. Bahan-Bahan dalam Formulasi ... 15
1. Asam Stearat ... 15
2. Setil Alkohol ... 15
3. Metil Paraben ... 16
4. Trietanolamin ... 16
H. Desain Faktorial ... 17
I. Pengujian Efek Antioksidan dengan Metode DPPH ... 19
J. Landasan Teori ... 21
K. Hipotesis ... 23
BAB III. METODE PENELITIAN... 24
A. Jenis dan Rancangan Penelitian ... 24
B. Variabel Penelitian dan Definisi Operasional ... 24
1. Variabel Penelitian ... 24
2. Definisi Operasional... 25
xi
1. Alat Penelitian ... 26
2. Bahan Penelitian... 27
D. Tata Cara Penelitian ... 27
1. Verifikasi Ekstrak Kulit Buah Manggis ... 27
2. Uji Aktivitas Antioksidan Ekstrak Kulit Buah Manggis... 27
a. Pembuatan Ekstrak Kental ... 27
b. Penyiapan Ekstrak Uji ... 28
c. Pembuatan Larutan DPPH ... 28
d. Penentuan Panjang Gelombang Maksimum ... 28
e. Penetapan Operating Time ... 29
f. Pengukuran Aktivitas Antioksidan Ekstrak ... 29
3. Formulasi Krim Ekstrak Kulit Buah Manggis ... 29
a. Formula ... 29
b. Pembuatan Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) ... 30
4. Uji Sifat Fisika Kimia Sediaan Krim Antioksidan Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) ... 31
a. Uji Organoleptis dan pH ... 31
b. Uji Daya Sebar ... 31
c. Uji Viskositas ... 31
d. Uji Sifat Alir ... 32
5. Uji Stabilitas Krim Ekstrak Kulit Buah Manggis ... 32
xii
b. Uji Daya Sebar ... 33
c. Uji Viskositas ... 33
d. Uji pH ... 33
e. Uji Sentrifugasi ... 34
6. Uji Aktivitas Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) dengan Metode DPPH ... 34
E. Analisis Data ... 35
BAB IV. HASIL DAN PEMBAHASAN ... 36
A. Verifikasi Ekstrak Kulit Buah Manggis ... 36
B. Pembuatan dan Uji Aktivitas Antioksidan Ekstrak Kental ... 36
1. Pembuatan Ekstrak Kental Kulit Buah Manggis (Garcinia mangostana L.) ... 36
2. Penentuan Panjang Gelombang Maksimum ... 37
3. Penentuan Operating Time (OT) ... 38
4. Pengukuran Aktivitas Antioksidan Ekstrak Kulit Buah Manggis.. 39
C. Pengujian Sifat Fisik Krim ... 40
1. Uji Organoeptis dan pH ... 40
2. Uji Daya Sebar ... 41
3. Uji Viskositas ... 46
4. Uji Rheologi (Sifat Alir) ... 49
5. Optimasi Formula ... 51
D. Uji Aktivitas Antioksidan Krim Ekstrak Kulit Buah Manggis ... 53
xiii
1. Uji Organoleptis dan pH ... 55
2. Uji Daya Sebar ... 55
3. Uji Viskositas ... 56
F. Uji Sentrifugasi ... 57
BAB V. KESIMPULAN DAN SARAN ... 59
A. Kesimpulan ... 59
B. Saran ... 60
DAFTAR PUSTAKA ... 61
LAMPIRAN ... 65
xiv
DAFTAR TABEL
Tabel I. Nilai Kekuatan Antioksidan ... 11
Tabel II. Rancangan Penelitian Desain Faktorial dengan Dua Faktor dan level ... 18
Tabel III. Formula Krim Ekstrak Kulit Buah Manggis ... 30
Tabel IV. Hasil Verifikasi Ekstrak Kulit Buah Manggis ... 36
Tabel V. Data Penetapan Operating Time Rkstrak Kulit Buah Manggis ... 38
Tabel VI. Hasil Pengukuran Aktivitas Antioksidan Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) ... 39
Tabel VII. Hasil Pengujian Organoleptis dan pH Sediaan Krim ... 41
Tabel VIII. Hasil Uji Daya Sebar Setelah Didiamkan Selama 48 Jam ... 42
Tabel IX. Pengaruh Parafin Cair, Gliserol dan Interaksi Keduanya Terhadap Respon Daya Sebar ... 44
Tabel X. Hasil Uji Viskositas Krim Ekstrak Kulit Buah Manggis ... 46
Tabel XI. Pengaruh Parafin Cair, Gliserol dan Interaksi Keduanya Terhadap Respon Viskositas ... 48
Tabel XII. Sifat Alir Sediaan Krim Ekstrak Kulit Buah Manggis ... 50
Tabel XIII. Hasil Validasi Counterplot Superimposed ... 53
Tabel XIV. Nilai IC50 Peredaman Radikal Bebas ... 54
xv
DAFTAR GAMBAR
Gambar 1. Diagram Pembentukan Radikal Bebas ... 8
Gambar 2. Buah Manggis (Garcinia mangostana L.)... 9
Gambar 3. Struktur Molekul Xanthone ... 11
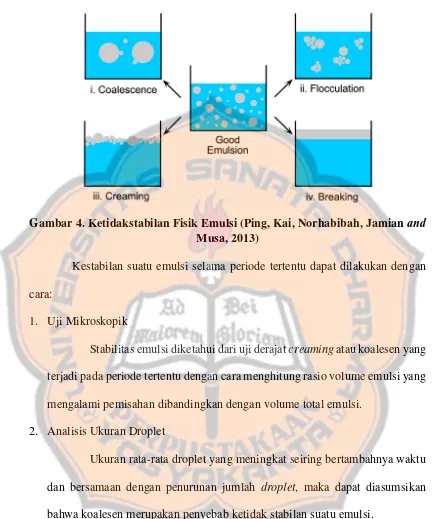
Gambar 4. Ketidakstabilan Fisik Emulsi ... 13
Gambar 5. Struktur Molekul Gliserol... 14
Gambar 6. Struktur Molekul Asam Stearat ... 15
Gambar 7. Struktur Molekul Cetyl Alcohol... 15
Gambar 8. Struktur Molekul Metil Paraben ... 16
Gambar 9. Struktur Molekul Trietanolamin ... 16
Gambar 10. Mekanisme Penghambatan Radikal Bebas DPPH ... 20
Gambar 11. Peak λ Maksimum Larutan DPPH ... 38
Gambar 12. Counterplot Respon Daya Sebar Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.)... 43
Gambar 13. Grafik Pengaruh Parafin Cair Terhadap Daya Sebar ... 44
Gambar 14. Grafik Pengaruh Gliserol Terhadap Daya Sebar ... 45
Gambar 15. Counterplot Respon Viskositas Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.)... 47
Gambar 16. Grafik Pengaruh Parafin Cair Terhadap Viskositas ... 48
Gambar 17. Grafik Pengaruh Gliserol Terhadap Viskositas ... 49
Gambar 18. Rheogram Formula I Krim Ekstrak Kuli Buah Manggis ... 50
xvi
Gambar 20. Rheogram Formula B Krim Ekstrak Kuli Buah Manggis ... 51 Gambar 21. Rheogram Formula AB Krim Ekstrak Kuli Buah Manggis ... 51 Gambar 22. Counterplot Superimposed Ekstrak Kuli Buah Manggis ... 52 Gambar 23. Grafik Perubahan Respon Daya Sebar Krim Ekstrak Kulit Buah
Manggis Tiap Siklus Freeze Thaw ... 56 Gambar 24. Grafik Perubahan Respon Viskositas Krim Ekstrak Kulit Buah
xvii
DAFTAR LAMPIRAN
Lampiran 1. Certificate of Analysis (COA) Ekstrak Kering Kulit Buah Manggis ... 66 Lampiran 2. Material Safety Data Sheet (MSDS) Kering Kulit Buah Manggis
... 67 Lampiran 3. Ekstraction Flow Chart Mangosteen... 69 Lampiran 4. Foto Ekstrak Kulit Buah Manggis ... 70 Lampiran 5. Data Sifat Fisik Organoleptis Sediaan Krim Ekstrak Kulit Buah
Manggis ... 71 Lampiran 6. Aktivitas Antioksidan Ekstrak Kulit Buah Manggis ... 74 Lampiran 7. Data Pengukuran Viskositas Krim Ekstrak Kulit Buah Manggis
(Garcinia mangostana L.) ... 75 Lampiran 8. Data Pengukuran Daya Sebar Krim Ekstrak Kulit Buah Manggis
(Garcinia mangostana L.) ... 79 Lampiran 9. Data Sifat Alir Sediaan Krim Ekstrak Kulit Buah Manggis
(Garcinia mangostana L.) ... 83 Lampiran 10. Data Hasil Uji Sentrifugasi Sediaan Krim Ekstrak Kulit Buah
Manggis (Garcinia mangostana L.) ... 84 Lampiran 11. Data Hasil Uji Aktivitas Antioksidan Sediaan Krim Ekstrak Kulit
Buah Manggis (Garcinia mangostana L.)... 85 Lampiran 12. Data Persen Penurunan Aktivitas Antioksidan Ekstrak Kulit Buah
xviii INTISARI
Ekstrak kulit buah manggis (Garcinia mangostana L.) diketahui memiliki banyak manfaat salah satunya sebagai antioksidan. Sifat fisik suatu sediaan krim dapat dipengaruhi oleh emolien dan humektan dalam formula yang digunakan. Parafin cair berperan sebagai emolien yang menjaga stabilitas campuran antara fase minyak dan fase air dalam sediaan krim, sedangkan gliserol digunakan sebagai humektan yang menjaga kelembapan kulit ketika sediaan diaplikasikan ke kulit. Penelitian ini bertujuan untuk mengetahui pengaruh komposisi parafin cair dan gliserol pada daerah optimum, pengaruhnya terhadap sifat fisik dan stabilitas fisik setelah 6 siklus freeze-thaw sediaan krim serta mengetahui aktivitas antioksidan sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.).
Penelitian ini merupakan penelitian eksperimental dengan menggunakan rancangan penelitian desain faktorial yang menggunakan dua faktor yang berbeda yaitu parafin cair dan gliserol dengan dua level yaitu level tinggi dan level rendah. Respon sifat fisik dan stabilitas fisik sediaan krim diketahui dengan menguji organoleptis, pH, daya sebar, viskositas dan pemisahan fase sediaan krim ekstrak kulit buah manggis. Data viskositas dan daya sebar dianalisis dengan menggunakan Design Expert® versi 10 dan R Studio.
Hasil penelitian menunjukkan parafin cair memberikan efek dominan pada respon daya sebar sebesar 68,39% sedangkan gliserol memberikan efek dominan pada respon viskositas 29,19%. Area komposisi optimum parafin cair dan gliserol ditentukan dengan superimposed contourplot respon viskositas dan daya sebar sediaan krim ekstrak kulit buah manggis. Sediaan krim ekstrak kulit buah manggis stabil secara organoleptis, pH, daya sebar, viskositas dan pemisahan fase, serta memiliki nilai aktivitas antioksidan yang sangat lemah yaitu ditunjukkan dengan penurunan aktivitas antioksidan > 100%.
xix ABSTRACT
Mangosteen rind extract (Garcinia mangostana L.) is known to has a lot of benefits, one of them is as an antioxidant. Physical properties of cream can be affected by emollient and humectant in the formula. Mineral Oil or Liquid Paraffin is an emollient that can maintain the mixture stability between oil phase and water phase in cream, while Glycerol is a humectant which maintain the humidity when applied to the skin. This research aims to know the effect of Mineral Oil and Glycerol composition at optimum areas, their effect on the physical stability and properties after 6 cycles of freeze-thaw stability testing and to find out the antioxidant activiy of Mangosteen rind (Garcinia mangostana L.) extract in cream formulation.
This research is a design factorial experimental research that use two different factors which are Mineral Oil and Glycerol and two levels whish are high and low. Physical properties and stability of cream were knew by looking at organoleptic, pH, spreadability, viscosity and sedimentation of Mangosteen rind (Garcinia mangostana L.) extract in cream formulation. The spreadability and viscosity respons of cream are analyzed by Design Expert® 10th version and R studio.
The result shows that Mineral Oil contribute a dominant effect in 68,39%
of cream’s spreadability respon and the otherwise, Glycerol contribute a dominant effect in 29,19% of cream’s viskosity response. The optimum area of Mineral Oil
and Glycerol is found by superimposed contourplot of viskosity and spreadability responses. Cream is stable in organoleptic, pH, spreadability, viskosity and sedimentation, and also cream has a very weak antioksidan activity which is showed by > 100% antioxidant activity reduction..
1 BAB I PENDAHULUAN
A.Latar Belakang Penelitian
Radikal bebas merupakan salah satu faktor eksternal penyebab proses penuaan dini. Proses penuaan dini ini ditandai dengan munculnya noda hitam atau flek, keriput, kondisi kulit kering bersisik dan kasar. Proses penuaan dini ini dapat
dicegah dengan menggunakan senyawa antioksidan (Swastika, Mufrod dan Purwanto, 2013). Antioksidan merupakan senyawa yang mampu mencegah dan mengurangi kerusakan kulit yang diakibatkan dari reaksi oksidasi oleh radikal bebas (Senja, Issusilaningtyas, Nugroho dan Setyowati, 2014).
Manggis (Garcinia mangostana L.) merupakan tanaman yang sering digunakan sebagai obat tradisional masyarakat, yang dapat mengobati sakit perut, diare, disentri, luka terbuka yang terinfeksi, nanah dan maag akut. Buah manggis memiliki kandungan Xanton terutama dibagian kulit buahnya yang merupakan sumber senyawa Xanton pada manggis. Xanton merupakan senyawa antioksidan yang sudah terbukti dapat menghambat senyawa radikal bebas (Chaverri, Rodriguez, Ibarra and Rojas, 2008).
(A/M). Tipe krim minyak dalam air (M/A) memiliki kelebihan yaitu mudah dicuci dengan air.
Emolien merupakan bahan yang memiliki fungsi untuk menutup lapisan permukaan stratum korneum kulit sehingga menahan air yang hendak menguap pada stratum korneum (Ifnudin, 2011). Parafin cair merupakan cairan viskos yang memiliki bentuk transparan dan tidak berwarna. Parafin cair digunakan secara luas dalam berbagai produk topikal sebagai emolien (Sheng, 2009).
Humektan merupakan senyawa yang berfungsi untuk menjaga dan meningkatkan kelembapan kulit dengan cara menyerap uap air dari lingkungan sekitar (Ifnudin, 2011). Gliserol merupakan humektan yang tidak berwarna, bening dan berbentuk cairan viskos yang tidak memiliki bau (Nunez and Medina, 2009).
itu juga menurut Ifnudin (2011) “gliserol memiliki kemampuan menyerap air
hampir sama dengan Natural Moisturizing Factor (NMF) yaitu pengikat uap air
alami yang ada pada kulit”.
Dari hasil formulasi yang dilakukan tersebut, penulis ingin mengetahui bagaimana pengaruh optimasi parafin cair sebagai emolien dan gliserol sebagai humektan dalam stabilitas krim serta pengaruhnya terhadap efek antioksidan dari ekstrak kulit buah manggis (Garcinia mangosta L.) yang telah dicampurkan ke dalam sediaan krim. Selain itu, penulis juga ingin mengetahui berapa komposisi parafin cair sebagai emolien dan gliserol sebagai humektan dalam stabilitas dan efek antioksidan yang diberikan dari ekstrak kulit buah manggis (Garcinia mangosta L.) dalam nilai IC50.
B.Rumusan Masalah
Berdasarkan latar belakang yang telah dijabarkan, permasalahan yang diajukan dalam penelitian ini adalah:
1. Bagaimana pengaruh parafin cair dan gliserol terhadap sifat fisik dan stabilitas fisik sediaan krim ekstrak kulit buah manggis (Garcinia mangstana L.)? 2. Berapa komposisi parafin cair dan gliserol pada daerah optimum sehingga
dihasilkan sediaan krim ekstrak kulit buah manggis (Garcinia mangstana L.) dengan sifat fisik yang baik?
3. Bagaimana aktivitas antioksidan buah manggis (Garcinia mangstana L.)? 4. Bagaimana stabilitas fisik sediaan krim ekstrak kulit buah manggis (Garcinia
5. Bagaimana aktivitas antioksidan ekstrak kulit buah manggis (Garcinia mangstana L.) setelah diformulasi dalam sediaan krim?
C.Keaslian Penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian tentang “Optimasi Parafin Cair Sebagai Emolien dan Gliserol Sebagai Humektan
dalam Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) Serta Uji Aktivitas Antioksidan” belum pernah dilakukan. Berikut beberapa penelitian pendukung yang penulis ambil, diantaranya:
Harun, 2014, Formulasi dan Uji Aktivitas Antioksidan Krim Anti-Aging Ekstrak Etanol 50% Kulit Buah Manggis (Garcinia mangostana L.) dengan Metode DPPH (1,1-Diphenyl-2-Pricil Hydrazil).
Terjadi pergeseran viskositas menjadi lebih viskos setelah dilakukan penyimpanan selama 10 hari pada ruang dengan suhu 250C.
Puspitasari, 2014, Optimasi Parafin Cair Sebagai Emolien dan Gliserin Sebagai Humektan dalam Krim Sunscreen Ekstrak Daun Jambu Biji (Psidium guajava L.)
D.Manfaat Penelitian 1. Manfaat Teoritis
Penelitian ini diharapkan dapat menambah informasi bagi ilmu pengetahuan kefarmasian mengenai pengaruh parafin cair sebagai emolien dan gliserol sebagai humektan terhadap sifat fisik dan stabilitas fisik sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.), serta bagaimana aktivitas antioksidan sediaan krim ekstrak kulit buah manggis.
2. Manfaat Praktis
Penelitian ini diharapkan mampu menghasilkan suatu formula sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.) yang memiliki sifat fisik dan stabilitas fisik yang baik serta aman untuk digunakan masyarakat.
E.Tujuan Penelitian 1. Tujuan Umum
Tujuan umum dari penelitian ini adalah untuk menghasilkan krim antioksidan dari ekstrak kulit buah manggis (Garcinia mangostana L.) dengan sifat fisik dan stabilitas fisik yang sesuai dengan persyaratan yang ditentukan serta dapat diterima di masyarakat.
2. Tujuan Khusus
a. Mengetahui pengaruh parafin cair sebagai emolien dan gliserol sebagai humektan terhadap sifat fisik sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.).
sehingga dihasilkan sediaan krim ekstrak kulit buah manggis dengan sifat fisik yang baik.
c. Mengetahui aktivitas antioksidan ekstrak kulit buah manggis (Garcinia mangostana L.).
d. Mengetahui stabilitas fisik sediaan krim ekstrak kulit buah manggis (Garcinia mangstana L.) setelah dilakukan pengujian sentrifugasi dan freeze-thaw cycle.
7 BAB II
PENELAAHAN PUSTAKA
A.Radikal Bebas
Radikal bebas merupakan suatu atom ataupun gugus atom yang memiliki satu atau lebih elektron yang tak berpasangan (Fessenden and Fessenden, 1999). Adanya elektron yang tidak berpasangan menyebabkan senyawa tersebut sangat reaktif untuk mencari pasangan dengan cara menyerang dan mengikat elektron molekul lain yang berada disekitarnya. Senyawa radikal bebas memiliki reaktivitas yang tinggi dan akan mengakibatkan terbentuknya senyawa radikal baru sehingga terjadi reaksi berantai (chain reactions). Reaksi berantai tersebut akan berlanjut dan baru akan berhenti apabila reaktivitasnya diredam (qunched) oleh senyawa yang memiliki sifat sebagai antioksidan (Winarsi, 2007).
harus dapat dinetralkan oleh antioksidan yang ada di dalam tubuh (Holistic Heath Solution, 2011).
Gambar 1. Diagram Pembentukan Radikal Bebas (Zander, 2013)
B.Antioksidan
Antioksidan merupakan senyawa yang berperan menetralkan radikal bebas yang menjadi racun (toksik) bagi tubuh. Bila radikal bebas yang dihasilkan tubuh berlebihan (karena olahraga terlalu berlebihan, infeksi, peradangan, kedinginan, keracunan dan kehilangan pasokan oksigen) dapat merusak sistem enzim, membran sel dan DNA (Holistic Heath Solution, 2011).
Antioksidan bekerja dengan cara mendonorkan elektron senyawa antioksidan pada senyawa yang bersifat oksidan (Musarofah, 2015). Berdasarkan sumbernya antioksidan dibagi menjadi dua yaitu:
2. Antioksidan alami yaitu antioksidan yang didapat dari bahan-bahan alami misalnya dari buah-buahan ataupun sayuran. Contohnya adalah tomat, apel, semangka, apel, kembang kol, kentang, dan manggis (Swastika, Mufrod dan Purwanto, 2013).
Antioksidan alami biasanya lebih diminati karena tingkat keamanan yang lebih baik dan manfaatnya yang lebih luas di bidang makanan, kesehatan dan kosmetik (Musarofah, 2015).
[image:31.595.85.515.244.735.2]C.Manggis
Gambar 2. Buah Manggis (Garcinia mangostana Linn.) (Paramawati, 2010)
1. Taksonomi tanaman
Klasifikasi tanaman manggis menurut United State Departement of Agruculture (2010), sebagai berikut:
Kingdom : Plantae (tumbuhan),
Ordo : Theales, Famili : Clusiaceae, Genus : Garcinia,
Spesies : Garcinia mangostana L. 2. Deskripsi umum
Manggis merupakan salah satu tanaman kelas Dicotyledonae, keluarga Guttiferae dan genus Garcinia (Paramawati, 2010). Buah manggis dapat ditemukan pada hutan hujan tropis pada beberapa negara kawasan Asia Tenggara seperti Indonesia, Malaysia, Sri Lanka, Filipina dan Thailand (Chaverri, et al., 2008). Buah manggis terdiri dari tiga bagian yaitu:
a. Bagian kulit (pericarp atau rind). Kulit berwarna hijau (ketika masih mentah) dan ungu gelap (ketika sudah matang). Di dalam kulit buah manggis terkandung senyawa kelompok antosianin yang memiliki kemampuan sebagai antioksidan yang cukup kuat yaitu Xanton.
b. Bagian daging buah (pulp) yang memiliki warna putih susu dan memiliki rasa yang khas.
c. Bagian biji (seed) merupakan lapisan luarnya yang merupakan selaput tipis yang sedikit mengandung Xanton dan bagian dalam biji berwarna kuning kecoklatan dengan tektur keras (Paramawati, 2010).
3. Manfaat dan kegunaan
Gambar 3. Struktur molekul Xanthone (Miryanti, 2011)
Xanton merupakan senyawa keton siklik polifenol dengan rumus molekul C13H8O2. Struktur dasar Xanton terdiri dari tiga benzena, dengan satu
benzena di tengahnya yang merupakan keton. Hampir semua molekul turunan Xanton sering disebut Polifenol. Xanton memiliki 200 jenis zat turunan dan 40 diantaranya terdapat dalam kulit manggis. Xanton dalam buah manggis terdapat di bagian kulit buah (pericarp) dan sedikit dalam kulit biji (hull) (Chaverri, Rodriguez, Ibarra and Rojas., 2008).
Kekuatan antioksidan dihitung dari kemampuannya dalam menetralisasi gugus radikal bebas. Kemampuan tersebut dihitung dengan satuan ORAC (Oxygen Radical Absorbance Capacity), yaitu kemampuan dalam menyerap radikal oksigen (Dewi, 2014). Pada tabel 1 dapat dilihat nilai kekuatan antioksidan beberapa bahan makanan setiap 100 ons atau setara dengan 3 kg.
Tabel I. Nilai Kekuatan Antioksidan (Dewi, 2014)
Buah Kemampuan menyerap radikal oksigen
Manggis Tomat Pisang dan mangga
Anggur Apel Jeruk Stroberi
D.Krim
Krim merupakan bentuk sediaan setengah padat berupa emulsi yang mengandung satu atau lebih bahan obat yang terlarut atau terdispersi dalam bahan dasar yang sesuai dan mengandung air tidak kurang dari 60%. Krim yang dapat dicuci dengan air (M/A) ditujukan untuk penggunaan kosmetik dan estetika (Syamsuni, 2005).
Ketidakstabilan suatu sediaan krim ada tiga yaitu creaming, koalesen dan inversi. Creaming merupakan pemisahan emulsi menjadi dua bagian dimana bagian yang satu memiliki fase dispersi yang lebih banyak daripada bagian yang lain. Koalesen merupakan penggabungan gelembung droplet yang saling berdekatan menjadi lebih besar, yang merupakan kelanjutan dari creaming (Aulton, 2002). Inversi merupakan berubahnya tipe emulsi M/A ke tipe A/M atau sebaliknya (Anief, 2000). Kerusakan yang terjadi pada sediaan krim adalah:
1. Cracking, yaitu pemisahan fase terdispersi.
2. Creaming, yaitu terbentuknya emulsi yang terkonsentrasi sehingga membentuk krim pada permukaan emulsi
3. Flokulasi/agregasi, yaitu terbentuknya partikel-partikel yang saling berkumpul yang bersifat reversibel.
Gambar 4. Ketidakstabilan Fisik Emulsi (Ping, Kai, Norhabibah, Jamian and Musa, 2013)
Kestabilan suatu emulsi selama periode tertentu dapat dilakukan dengan cara:
1. Uji Mikroskopik
Stabilitas emulsi diketahui dari uji derajat creaming atau koalesen yang terjadi pada periode tertentu dengan cara menghitung rasio volume emulsi yang mengalami pemisahan dibandingkan dengan volume total emulsi.
2. Analisis Ukuran Droplet
Ukuran rata-rata droplet yang meningkat seiring bertambahnya waktu dan bersamaan dengan penurunan jumlah droplet, maka dapat diasumsikan bahwa koalesen merupakan penyebab ketidak stabilan suatu emulsi.
3. Perubahan Viskositas
E.Parafin Cair
Parafin cair yang juga disebut mineral oil merupakan minyak kental yang transparan, tidak berwarna dan tidak memiliki rasa. Memiliki titik didih > 3600C dan larut dalam aseton, benzena, kloroform, karbon disulfida eter, petroleum eter, serta praktis tidak larut dalam air. Penggunaan parafin cair pada emulsi topikal yaitu 1,0 % - 32,0 %. Viskositas parafin cair pada 200C sebesar 110-230 mPa.s dan parafin cair inkompatibel dengan agen pegoksidasi yang kuat. Parafin cair biasanya digunakan pada emulsi minyak dalam air (M/A) (Sheng, 2009).
[image:36.595.85.513.215.618.2]F. Gliserol
Gambar 5. Struktur molekul gliserol (Nunez and Medina, 2009).
Gliserol atau gliserin (C3H8O3) merupakan cairan higroskopis kental, tidak
berwarna, tidak berbau, bening, dan inkompatibel dengan agen pengoksidasi kuat. Gliserol berfungsi sebagai pengawet, humektan, kosolven, pelarut, pemanis, plasticizer dan agen tonisistas. Gliserol sebagai humektan digunakan ≤ 30%.
G.Bahan-Bahan dalam Formulasi 1. Asam stearat
Gambar 6. Struktur molekul asam stearat (Allen, 2009)
Asam stearat merupakan serbuk padat, berwarna putih atau kekuningan dan sedikit mengkilap. Asam stearat memiliki fungsi sebagai agen pengemulsi, solubilizing agent, serta sebagai lubrikan tablet dan kapsul. Dalam formulasi
sediaan topikal dapat berfungsi sebagai pengemulsi dan solubilizing agent. Asam stearat memiliki nilai keasaman sebesar 195-212, asam stearat dinetralkan keasamannya dengan senyawa alkali atau trietanolamin (TEA) pada formulasi sediaan topikal agar tidak mengiritasi kulit ketika diaplikasikan pada kulit serta agar membentuk konsistensi creamy. Asam stearat sangat larut dalam benzen, karbon tetraklorida, kloroform dan eter. Larut dalam etanol 95%, hexane dan propylene glycol. Tidak larut parsial dalam air, serta memiliki titik lebur 69-700C. Asam stearat inkompatibel terhadap basa, agen pereduksi dan agen pengoksidasi. Penggunaan asam stearat pada sediaan krim sebesar 1 hingga 20% (Allen, 2009). 2. Setil Alkohol
Setil alkohol digunakan dalam sediaan krim untuk meningkatkan stabilitas, meningkatkan tektur dan meningkatkan konsistensi sediaan. Setil alkohol memiliki titik leleh 45-520C. Setil akhohol mudah larut dalam alkohol 96% dan eter, larut sebagian dalam air dan tercampur ketika dilelehkan dengan lemak, parafin cair atau padat dan isopropil miristat (Unvala, 2009).
[image:38.595.87.514.225.683.2]3. Metil paraben
Gambar 8. Struktur molekul metil paraben (Haley, 2009)
Metil paraben merupakan suatu agen antibakteri atau pengawet yang banyak digunakan dalam sediaan kosmetik dan dalam berbagai macam bentuk sediaan farmasi. Metil paraben memiliki bentuk kristal atau serbuk kristal. Metil paraben tidak berwarna serta tidak berbau. Metil paraben dapat menunjukkan aktivitas antibakteri pada pH 4-8, akan tetapi lebih aktif mencegah jamur daripada bakteri (Haley, 2009). Penggunaan metil paraben untuk sediaan topial yaitu 0,02-0,3% (Winarti, 2013).
4. Trietanolamin (TEA)
TEA berbentuk cairan kental tidak berwarna hingga kuning pucat serta memiliki bau amonia yang ringan. Titik leleh dari TEA sebesar 20-210C dan pH
sebesar 10,5 dalam larutan 0,1 N. TEA memiliki titik didih sebesar 3350C dan viskositas sebesar 590 mPa.s pada 300C. TEA bersifat higroskopis. TEA dapat bercampur dengan aseton, karbon tetraklorida, metanol dan air. TEA inkompatibel terhadap tionil kloridan dan asam mineral (Goskonda, 2009).
H.Desain Faktorial
Desain faktorial merupakan aplikasi persamaan regresi yaitu teknik untuk memberikan model hubungan antara varabel respon dengan satu atau lebih variabel bebas, model yang diperoleh berupa persamaan matematika. Desain faktorial dua level berarti ada dua faktor (A dan B) yang masing-masing faktor diuji pada dua
tingkatan yang berbeda, yaitu level rendah dan tinggi (Bolton and Bon, 2010). Pada desain faktorial dapat dilihat hubungan antara respon variabel dengan dua atau lebih faktor untuk menentukan efek dari faktor yang diteliti beserta interaksinya yang berpengaruh signifikan (Wijoyo, 2016).
Optimasi campuran dua bahan (dua faktor) dengan desain faktorial (two level factorial design) dilakukan berdasarkan rumus:
Y = b0 + b1(Xa) + b2(Xb) + b12(Xa)( Xb)...(1)
Keterangan:
Y = respon hasil atau sifat yang diamati. (A), (B) = level bagian A, level bagian B.
b0, b1, b2, b12 = koefisien yang dapat dihitung dari percobaan.
rendah, (b) A pada level rendah dan B pada level tinggi, (ab) A dan B masing-masing pada level tinggi. Dari rumus dan data yang diperoleh dapat dibuat contourplot dan superimposed contourplot suatu respon tertentu yang sangat berguna dalam memilih kondisi yang optimum pada level faktor yang diteliti (Bolton and Bond, 2010).
Tabel II. Rancangan Penelitian Desain Faktorial dengan Dua Faktor dan Level (Bolton and Bon, 2010)
Formula Faktor A Faktor B Interaksi
I - - +
a + - -
b - + -
ab + + +
Keterangan:
(-) = level rendah (+) = level tinggi
Formula I = faktor A level rendah, faktor B level rendah Formula a = faktor A level tinggi, faktor B level rendah Formula b = faktor A level rendah, faktor B level tinggi Formula ab = faktor A level tinggi, faktor B level tinggi
Istilah-istilah desain faktorial yaitu:
1. Faktor yaitu variabel yang telah ditetapkan pada suatu penelitian yang dapat bersifat kualitatif maupun kuantitatif. Faktor ini harus dapat dinyatakan dalam suatu harga atau nilai.
2. Level yaitu harga yang ditetapkan untuk faktor.
3. Respon yaitu hasil terukur yang didapat dari suatu penelitian dan harus dapat dikuantifikasi.
4. Interaksi yaitu akibat dari penambahan efek-efek faktor yang dapat bersifat antagonis atau sinergis. Antagonis berarti memiliki efek yang memperkecil efek faktor sedangkan sinergis berarti memiliki efek memperbesar efek faktor (Kurniawan dan Sulaiman, 2009).
I. Pengujian Efek Antioksidan dengan Metode DPPH
Ada beberapa metode umum yang sering digunakan untuk pengujian kapasitas antioksidan yaitu metal reducing power atau ferric reducing antioxidant power (FRAP), organic radical scavenging
(2,2-Azino-bis(3-ethylbenz-thiazoline-6-sulfonic acid) (ABTS), trolox equivalent antioxidant capacity (TEAC), DPPH (2,2-diphenyl-1-picrylhydrazyl) dan peroxy radical scavenging (oxygen radical absorbance capacity ) (ORAC) (Marinova and Batchvarov, 2011). Salah satu
menjadi memudar (warna kuning). Pemudaran warna akan mengakibatkan penurunan nilai absorbansi sinar tampak dari spektrofotometer. Semakin pudar warna DPPH setelah direaksikan dengan antioksidan menunjukkan kapasitas antioksidan yang semakin besar pula (Dewi, 2014). Elektron ganjil pada radikal bebas DPPH memberikan absorbansi maksimum yang kuat pada panjang gelombang 517 nm dan memberikan warna ungu. Metode ini tergolong cepat, sederhana, tidak mahal dan banyak digunakan untuk mengukur kemampuan komponen sebagai pemerangkap radikal bebas serta dapat mengevaluasi aktivitas antioksidan dari makanan (Prakash, Rigelhof and Miller 2001).
Kelebihan dari metode ini adalah DPPH akan beraksi dengan sampel secara keseluruhan dalam waktu tertentu dan DPPH dapat bereaksi secara perlahan meskipun dengan antioksidan yang lemah (Prakash, et al., 2001). Mekanisme penghambatan radikal DPPH dapat dilihat pada Gambar 10.
Gambar 10. Mekanisme Penghambatan Radikal Bebas DPPH (Miryanti, 2011)
Pendekatan sederhana untuk intepretasi data adalah membandingkan absorbansi dengan konsentrasi substrat. Metode alternatif lain yang sering digunakan adalah persentase reduksi DPPH (Q) yang dikenal dengan “inhibition” atau “quenching”
yang dihitung dengan rumus :
Q = 100 (A0 – Ac) / A0 ... (2)
Lambang A0 adalah absorbansi awal dan Ac adalah nilai absorbansi
terhadap penambahan sampel dengan konsentrasi c (Molyneux, 2004).
J. Landasan Teori
Radikal bebas merupakan senyawa yang memiliki elektron ganjil yang bersifat reaktif dan dapat merusak sel tubuh sehingga menyebabkan penyakit. Senyawa radikal ini bersifat sangat reaktif, akan tetapi kereaktifan dari senyawa radikal bebas ini dapat dihentikan oleh senyawa antioksidan. Senyawa antioksidan merupakan senyawa yang berfungsi untuk mendonorkan elektron kepada senyawa radikal bebas.
2002). Inversi merupakan berubahnya tipe emulsi M/A ke tipe A/M atau sebaliknya (Anief, 2000).
Salah satu komponen penyusun sediaan krim adalah emolien dan humektan. Dalam penelitian ini digunakan emolien parafin cair yang berfungsi untuk menutup permukaan stratum korneum sehingga menahan air yang hendak menguap pada stratum korneum. Humektan yang digunakan dalam penelitian ini adalah gliserol yang merupakan humektan yang paling umum digunakan di berbagai produk kosmetik. Humektan merupakan bahan yang digunakan untuk meningkatkan kelembaban kulit. Emolien dan humektan merupakan komponen penting dalam suatu sediaan krim terkait aseptabilitas, sehingga dihasilkan suatu sediaan krim yang lembut dan tidak kering ketika diaplikasikan pada kulit.
Kulit buah manggis (Garcinia mangostana L.) diketahui memiliki kandungan antioksidan yang berupa senyawa Xanton yang paling banyak terdapat pada kulit buahnya. Xanton merupakan suatu senyawa antioksidan golongan polyphenolic yang digolongkan kebeberapa bagian diantaranya adalah α -mangostin, -mangostin, -mangostin, garcinon E, 8-deoxygartanin dan gartanin (Chaverri, et al., 2008).
karena DPPH merupakan senyawa radikal bebas yang cukup stabil (Molyneux ,2004).
Maka dari itu penulis hendak melihat bagaimana pengaruh parafin cair dan gliserol terhadap sifat fisik dan stabilitas fisik sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.), berapa komposisi optimum parafin cair dan gliserol dalam sediaan krim sehingga dihasilkan suatu sediaan krim denga sifat fisik yang baik, bagaimana aktivitas antioksidan dari ekstrak kulit buah manggis (Garcinia mangostana L.) yang digunakan dalam penelitian, bagaimana stabilitas sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.) setelah diuji sentrifugasi dan freeze-thaw cycle serta bagaimana pengaruhnya terhadap aktivitas antioksidan ekstrak kulit buah manggis yang dicampurkan ke dalam sediaan krim.
K.Hipotesis
1. Parafin cair dan gliserol memiliki pengaruh yang signifikan terhadap sifat fisik sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.) yang meliputi respon daya sebar dan viskositas.
2. Diperoleh area optimum parafin cair dan gliserol pada superimpozed counter plot sehingga diperoleh formula krim ektrak kulit buah manggis (Garcinia
mangostana L.) optimum.
3. Ekstrak kulit buah manggis memiliki aktivitas antioksidan yang kuat.
4. Sediaan krim antioksidan ekstrak kulit buah manggis (Garcinia mangostana L.) dapat menjaga stabilitas setelah diuji sentrifugasi dan siklus freeze thaw. 5. Ekstrak kulit buah manggis dalam sediaan krim memiliki aktivitas antioksidan
24 BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian eksperimental murni menggunakan desain faktorial dengan dua faktor dan dua level berbeda, untuk membandingkan sifat fisik serta stabilitas fisik sediaan krim.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel Penelitian
a. Variabel bebas dalam penelitian ini adalah penggunaan parafin cair sebagai emolien dan gliserol sebagai humektan.
b. Variabel tergantung dalam penelitian ini adalah organoleptis, viskositas, daya sebar, pH, stabilitas fisik dan aktivitas antioksidan sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.).
c. Variabel pengacau terkendali dalam penelitian ini adalah alat dan bahan- bahan yang digunakan, lama pengadukan, prosedur pembuatan dan pengujian sediaan krim, lama penyimpanan serta wadah penyimpanan sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.). d. Variabel pengacau tak terkendali dalam penelitian ini adalah suhu dan
2. Definisi Operasional
a. Krim antioksidan ekstrak kulit buah manggis (Garcinia mangostana L.) merupakan suatu sediaan semisolid yang memiliki aktivitas antioksidan dengan parafin cair sebagai emolien dan gliserol sebagai humektan.
b. Ekstrak kulit buah manggis (Garcinia mangostana L.) merupakan ekstrak yang yang terbuat dari kulit buah manggis (Garcinia mangostana L.) dan berasal dari PT. Borobudur Industri Jamu. Ekstrak kental kulit buah manggis didapat dari hasil filtrasi dan evaporasi dari pelarut etanol 96%. c. Antioksidan merupakan senyawa penangkal radikal bebas dengan cara
menyumbangkan 1 atom hidrogen untuk berikatan dan menetralkan senyawa radikal bebas. Dalam penelitian senyawa antioksisan yang digunakan adalah Xanton yang merupakan senyawa antioksidan dari ekstrak kulit buah manggis (Garcinia mangostana L.).
d. Radikal bebas merupakan senyawa yang kehilangan 1 elektronnya sehingga menjadi sangat reaktif. Senyawa radikal bebas yang digunakan dalam penelitian ini adalah DPPH.
e. Emolien merupakan senyawa merupakan senyawa yang dapat menjaga stabilitas sediaan emulsi minyak dan air. Dalam penelitian ini digunakan emollien yaitu parafin cair.
yang banyak digunakan dalam kosmetik dan sediaan farmasi lainnya sebagai humektan.
g. Sifat fisik krim meliputi pengujian pH, organoleptis, viskositas dan daya sebar krim.
h. Stabilitas fisik krim meliputi pengujian daya sebar dan fiskositas selama siklus freeze thaw, uji sentrifugasi dan pH.
i. Daya sebar merupakan kemampuan krim untuk menyebar pada permukaan kulit ketika diaplikasikan. Daya sebar berkaitan erat dengan kenyamanan pasien dalam menggunakan sediaan.
j. Viskositas merupakan tahanan dari suatu fluida, semakin tinggi viskositas maka semakin tinggi pula tahanannya. Semakin besar tahanan maka semakin sukar pula sediaan krim untuk mengalir.
k. Formula gel optimum didapat area optimum yang berwarna kuning pada counterplot superimposed.
C. Alat dan Bahan Penelitian 1. Alat Peneltian
Alat yang digunakan dalam penelitian ini meliputi alat-alat gelas (Pyrex® Germany), timbangan analitik, spektrofotometer UV-Vis Single Beam, waterbath, viscometer seri VT 04 (Rion® Japan), horizontal double plate,
sentrifugator, tabung sentrifugasi, cawan porselen, kertas indikator pH (Merck® Germany), kertas saring, termometer, oven, pendingin (kulkas), pipet volume, glassfinn, batang pengaduk, pipet tetes, toples kaca (net @200 gram dan @100
2. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah ekstrak kulit manggis (Garcinia mangostana L.) yang diperoleh dari PT. Borobudur Semarang, aquadest, gliserol (kualitas farmasetis), parafin cair (kualitas farmasetis), metil paraben (kualitas farmasetis), asam stearat, trietanolamine, cetyl alcohol, etanol 96% (teknis) dan DPPH .
D. Tata Cara Penelitian
1. Verifikasi Ekstrak Kulit Manggis (Garcinia mangostana L.)
Bentuk, warna serta bau dari ekstrak kulit manggis (Garcinia mangostana L.) yang digunakan dalam penelitian ini diamati dan dibandingkan
dengan Certificate of Analysis (CoA) ekstrak kulit buah manggis. Ekstrak kulit buah manggis diperoleh dari PT. Borobudur Semarang yang telah teridentifikasi jenis dan kandungannya melalui Certificate of Analysis (CoA) yang diberikan oleh PT. Borobudur Semarang.
2. Uji Aktivitas Antioksidan Ekstrak Kulit Buah Manggis a. Pembuatan Ekstrak Kental
didapatkan ekstrak kental dengan bobot 85% dari ekstrak kering kulit buah manggis yang ditimbang.
b. Penyiapan Ekstrak Uji
Ekstrak kulit buah manggis sebanyak 100,0 mg dilarutkan menggunakan etanol 96% dalam beaker glass dengan dibantu pengadukan, dimasukkan ke dalam labu ukur 100 ml dan di ad hingga tanda batas sehingga didapatkan konsentrasi 1000,0 ppm. Dibuat lima larutan seri dengan cara mengambil sebanyak 0,3; 0,4; 0,5; 0,75 dan 1,5 mL larutan stok dan ad dengan etanol 96% hingga batas tanda pada labu ukur 25 mL sehingga diperoleh konsentrasi larutan intermediet sebesar 12,0; 16,0; 20,0; 30,0 dan 60,0 ppm.
c. Pembuatan Larutan DPPH
DPPH sebanyak 2,0 mg dilarutkan dengan menggunakan etanol 96% dalam labu ukur 100,0 mL yang telah ditutup dengan alumunium foil (larutan dilindungi dari cahaya), sehingga diperoleh konsentrasi 20,0 ppm. d. Penentuan Panjang Gelombang Maksimum
e. Penetapan Operating Time
Larutan DPPH 20,0 ppm diambil sebanyak 4,0 ml dan ditambah dengan ekstrak uji dengan konsentrasi 20,0 ppm sebanyak 2,0 mL, kemudian diamati absorbansinya pada panjang gelombang maksimum yang telah diperoleh dalam interval waktu 5, 10, 15, 20, 25 dan 30 menit. Blangko yang digunakan dalam penetapan OT (operating time) berupa larutan DPPH dengan konsentrasi 20,0 ppm sebanyak 4,0 mL dan etanol 96% sebanyak 2,0 ml.
f. Pengukuran Aktivitas Antioksidan Ekstrak Kulit Buah Manggis Larutan uji pada masing-masing konsentrasi seri sebanyak 2,0 ml diambil dan ditambah dengan larutan DPPH 20,0 ppm sebanyak 4,0 ml, kemudian didiamkan selama OT (operating time) yang diperoleh dan diamati absorbansinya pada panjang gelombang maksimum yang telah diperoleh. Blangko yang digunakan berupa larutan DPPH dengan konsentrasi 20,0 ppm sebanyak 4,0 mL, yang telah dicampur dengan etanol 96% sebanyak 2,0 mL. Dari absorbansi diperoleh persamaan regresi yang kemudian digunakan untuk menghitung nilai IC50.
3. Formulasi Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) a. Formula
Tabel III. Formula Krim Ekstrak Kulit Buah Manggis
Bahan Formula
I A B AB
Asam stearat (g) 15,000 15,000 15,000 15,000 Setil alkohol (g) 2,000 2,000 2,000 2,000 Parafin cair (g) 7,500 14,500 7,500 14,500
Ekstrak (g) 0,015 0,015 0,015 0,015 Gliserol (g) 4,625 4,625 11,875 11,875 Metil paraben (g) 0,200 0,200 0,200 0,200
TEA (g) 0,327 0,327 0,327 0,327 Aquadest (mL) 60,000 60,000 60,000 60,000
b. Pembuatan Sediaan Krim Ekstrak Kulit Manggis (Garcinia mangostana L.)
kemudian dicek dengan menggunakan stik indikator pH universal (pH sediaan yang diinginkan dalam rentang antara 4,8 hingga 6,5).
4. Uji Sifat Fisika Kimia Sediaan Krim Antioksidan Ekstrak Kulit Manggis (Garcinia mangostana L.)
a. Uji organoleptis dan pH
Dilakukan dengan mengamati bentuk, warna, dan bau sediaan krim yang dihasilkan. Untuk uji pH, dilakukan dengan mengukur pH sediaan krim menggunakan indikator pH universal stick, nilai pH dilihat dengan membandingkan warna yang dihasilkan dengan warna pada standar. Kriteria pH yang diinginkan adalah 4,5-6,5 yang merupakan pH kulit manusia.
b. Uji daya sebar
Sebanyak 1 g sediaan krim diletakkan di atas bagian tengah suatu kaca bulat. Kemudian diberikan beban pemberat sebesar 125 gram (kaca bulat penutup dan beban tambahan) diatas sediaan krim dan dibiarkan selama 1 menit. Kemudian diukur diameternya dari empat sisi yang berbeda. Dilakukan replikasi sebanyak 3 kali untuk tiap-tiap formula (formula A, B, AB dan I).
c. Uji viskositas
dalam cup viscometer dan dipasang pada rotor viscometer. Nilai viskositas ditunjukkan oleh jarum penunjuk saat viscometer dinyalakan, skala rotor yang digunakan yaitu dua.
d. Uji sifat alir
Uji sifat alir dilakukan dengan menggunakan Rheosys Merlyn dengan menggunakan cone and plate pada suhu 250C. Parameter kecepatan awal 0,1 rpm dan kecepatan akhir 100 rpm. Kecepatan meningkat 10 tahap dengan peningkatan kecepatan berturut-turut yaitu 1,0 rpm; 12,0 rpm; 23,0 rpm; 34,0 rpm; 45,0 rpm; 56,0 rpm; 67,0 rpm; 78,0 rpm; 89,0 rpm dan 100,0 rpm. Sediaan krim antioksidan diletakkan ditengah plate, kemudian cone diatur sedemikian rupa hingga menempel sediaan krim. Selanjutnya, Rheosys Merlyn dijalankan dengan menggunakan bantuan software Rheosys
Micra, sehingga didapatkan tipe sifat alir dari sediaan krim antioksidan yang
diuji. Sifat alir sediaan krim mengikuti model Non-Newtonian pseudoplastis.
5. Uji Stabilitas Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.) a. Freeze-Thaw Cycle
Uji Freeze-Thaw dilakukan dengan cara menyimpan masing-masing formula pada suhu -40C selama 24 jam pada freezer, kemudian
disimpan kembali pada suhu 450C selama 24 jam pada oven (1 siklus freeze-thaw). Penyimpanan dilakukan hingga 6 siklus dan pada akhir tiap siklus
b. Uji daya sebar
Dilakukan uji daya sebar pada akhir siklus freeze thaw, dengan 3 kali replikasi untuk tiap-tiap formula (formula A, B, AB dan I). Sebanyak 1 g sediaan krim diletakkan di atas bagian tengah suatu kaca bulat. Kemudian diberikan beban pemberat sebesar 125 gram (kaca bulat penutup dan beban tambahan) diatas sediaan krim dan dibiarkan selama 1 menit. Kemudian diukur diameternya dari empat sisi yang berbeda.
c. Uji Viskositas
Uji viskositas dilakukan pada akhir siklus freeze thaw dan dilakukan 3 kali replikasi untuk formula A, B, AB dan I. Pengukuran viskositas dilakukan dengan menggunakan viscometer Rion seri VT 04. Pengukuran viskositas dilakukan dengan cara memasukkan sediaan krim ke dalam cup viscometer dan dipasang pada rotor viscometer. Nilai viskositas ditunjukkan oleh jarum penunjuk saat viscometer dinyalakan, skala rotor yang digunakan yaitu dua.
d. Uji PH
Uji pH dilakukan pada formula A, B, AB, dan I dengan menggunakan indikator pH universal stick pada setiap akhir siklus freeze thaw. Pengujian dilakukan dengan cara mengoleskan sedikit sediaan krim
pada kemasan pH universal. Nilai pH yang diinginkan antara 4,5 hingga 6,5 yang merupakan pH kulit.
e. Uji sentrifugasi
Uji sentriugasi dilakukan pada masing-masing formula (formula A, B, AB dan 1) sebanyak 3 kali replikasi. Pengujian sentrifugasi dilakukan dengan cara memasukkan sediaan krim yang sudah didiamkan terlebih dahulu selama 48 jam dari hari pembuatan ke dalam tabung sentrifugasi kemudian tabung sentrifugasi yang telah terisi dengan sediaan krim dimasukkan ke dalam sentrifuge. Kecepatan mesin sentrifugasi diatur hingga kecepatan 3750 rpm selama 5 jam, kemudian diamati pemisahan yang terjadi pada sediaan krim setelah di sentrifugasi.
6. Uji Aktivitas Sediaan Krim Ekstrak Kulit Manggis (Garcinia mangostana L.) dengan Metode DPPH
Sediaan krim sebanyak 100,0 mg dilarutkan dalam etanol 96% dalam beaker glass dan dibantu pengadukan menggunakan batang pengaduk agar
Masing-masing konsentrasi larutan seri uji pada tiap formula diambil sebanyak 2,0 mL kemudian ditambah dengan larutan DPPH 20,0 ppm sebanyak 4,0 mL. Campuran larutan ini kemudian didiamkan selama OT (Operating Time) dan dibaca absorbansinya pada panjang gelombang maksimum dengan
menggunakan spektrofotometer. Blangko yang digunakan marupakan campuran 4,0 mL DPPH 20,0 ppm dan etanol 96% sebanyak 2 mL.
E. Analisis Data
Data yang diperoleh berupa sifat fisik sediaan krim, stabilitas fisik sediaan krim dan aktivitas antioksidan krim ekstrak kulit buah manggis. Data yang diperoleh dianalisis menggunakan “R Studio” untuk mengetahui
signifikansi perbedaan data yang diperoleh.
Data sifat fisik sediaan krim dihitung rata-rata dan dicari standar deviasinya dari tiap replikasinya. Data sifat fisik viskositas dan daya sebar juga dianalisis menggunakan Design Expert® 10 sehingga didapatkan data pengaruh serta interaksi dari kedua faktor pada dua level untuk masing-masing respon. Analisis statistiknya dalam Design Expert® 10 menggunakan uji ANOVA dengan taraf kepercayaan 95%.
Data stabilitas fisik dihitung rata-rata dan dan dicari standar deviasinya dari tiap replikasinya. Data stabilitas fisik viskositas dan daya sebar dianalisis sebaran normal dan homogenitas data dengan menggunakan “R Studio” dengan
36 BAB IV
HASIL DAN PEMBAHASAN
A. Verifikasi Ekstrak Kulit Buah Manggis
[image:58.595.94.512.235.613.2]Verifikasi ekstrak kulit buah manggis dalam penelitian ini dilakukan dengan tujuan untuk membuktikan kebenaran bahwa ekstrak yang digunakan dalam penelitian ini merupakan ekstrak kulit buah manggis (Garcinia mangostana L.) yang berasal dari PT. Borobudur Industri Jamu Semarang. Verifikasi dilakukan dengan cara membandingkan ekstrak kering kulit buah manggis yang diterima dengan Certificate of Analysis (CoA) yang tertera dalam kemasan ekstrak kering.
Tabel IV. Hasil Verifikasi Ekstrak Kulit Buah Manggis
Kriteria Hasil Pengamatan Data Certificate of Analysis (CoA)
Bentuk Granul Granul
Warna Coklat Coklat
Bau Khas aromatis Khas aromatis
Dari hasil pengamatan yang tertera pada tabel 4, dapat dikatakan bahwa ekstrak yang digunakan telah sesuai dengan CoA yang dicantumkan.
B. Pembuatan dan Uji Aktivitas Antioksidan Ekstrak Kental
Pelarut yang digunakan dalam pembuatan ekstrak kental kulit buah manggis ini merupakan etanol 96%. Setelah ekstrak kering dilarutkan dalam etanol 96%, dilakukan penyaringan dengan tujuan ntuk memisahkan ekstrak yang terlarut dalam etanol 96% dengan maltodekstrin yang mengendap. Jumlah ekstrak kental yang didapatkan dari penimbangan 10,0 gram ekstrak kering yaitu:
Ekstrak kental = × , gram = , gram
Pelarut diuapkan pada suhu 500C untuk menjaga agar senyawa
antioksidan dalam ekstrak kulit buah manggis (Garcinia mangostana L.) tidak rusak, dan untuk mendapatkan aktivitas antioksidan yang maksimal dari senyawa antioksidan (Husni, Putra dan Lelana, 2014). Alasan lain pelarut diuapkan pada suhu 600C karena sebagian besar senyawa antioksidan mulai rusak pada suhu > 600C (Barasa, 2014).
2. Penentuan Panjang Gelombang Maksimum
Gambar 11. Peak λ Maksimum Larutan DPPH
Dari hasil pengukuran panjang gelombang maksimum menggunakan spektrofotometer UV-Vis didapatkan λ maksimum 517 nm. Pada penelitian Tjahjani, Widowati, Khiong, Suhendra dan Tjokropranoto (2014) panjang gelombang maksimum yaitu 517 nm. Sehingga pada penelitian digunakan panjang gelombang 517 nm.
3. Penentuan Operating Time (OT)
Penentuan operating time (OT) dikakukan dengan tujuan untuk mendapatkan waktu dimana reaksi antara senyawa antioksidan dan larutan DPPH telah berjalan sempurnan hal tersebut ditunjukkan dengan absorbansi yang stabil.
Tabel V. Data Penetapan Operating Time Ekstrak Kulit Buah Manggis Waktu (menit) Absorbansi (A)
5 0,874
10 0,749
15 0,726
20 0,725
25 0,717
[image:60.595.87.510.107.726.2]Berdasarkan tabel data penetapan OT ekstrak kulit buah manggis didapatkan absorbansi yang stabil pada menit ke-25 dan 30. Hal tersebut menunjukkan bahwa reaksi antara senyawa antioksidan pada ekstrak kulit buah manggis dengan larutan DPPH telah berjalan sempurna, maka dari itu digunakan operating time 25 menit.
4. Pengukuran Aktivitas Antioksidan Ekstrak Kulit Buah Manggis
[image:61.595.86.513.230.622.2]Tujuan pengukuran aktivitas antioksidan ekstrak kulit buah manggis yaitu untuk mengetahui aktivitas antioksidan yang diberikan oleh ekstrak kulit buah manggis yang akan digunakan dalam formulasi sediaan krim.
Tabel VI. Hasil Pengukuran Aktivitas Antioksidan Ekstrak Kulit Buah Manggis (Garcinia mangostana L.)
Konsentrasi (ppm) Absorbansi (A) Inhibisi (%)
Persamaan regresi linier (konsentrasi vs inhibisi (%))
12 0,828 5,263
y = 0,9172 x - 5,7279 R2 = 0,9981
16 0,801 8,352
20 0,753 13,844
30 0,690 21,053
60 0,442 49,428
sampel. IC50 berarti konsentrasi penghambatan oleh senyawa antioksidan yang
mampu menghambat 50% aktivitas senyawa radikal bebas. Nilai x pada persamaan menunjukkan konsentrasi (ppm) sedangkan nilai y menunjukkan peredaman yang diberikan oleh larutan sampel sehingga untuk menghitung IC50
dilakukan dengan cara memasukkan nilai 50 pada varibel y dalam persamaan regreasi linier yang telah didapat. Nilai IC50 sampel uji yang berupa ekstrak kulit
buah manggis (Garcinia mangostana L.) sebesar 60,7584 ppm (60,7584 ��⁄ ) yang tergolong dalam antioksidan kuat. Senyawa antioksidan dikatakan sangat kuat apabila memiliki IC50 < 50 ppm, tergolong kuat apabila IC50 memiliki nilai
antara 50-100 ppm, tergolong sedang apabila IC50 memiliki nilai antara
101-150 ppm, dan tergolong lemah apabila IC50 memiliki nilai 151-200 ppm
(Barasa, 2015).
C. Pengujian Sifat Fisik Krim Ekstrak Kulit Buah Manggis
Pengujian sifat fisik suatu sediaan memiliki peran penting pada aspek acceptability obat pada pasien maka dari itu pengujian sifat fisik ini sangat diperlukan. Pengujian sifat fisik sediaan krim ekstrak kulit buah manggis dalam penelitian ini meliputi pengujian organoleptis sediaan, pH, daya sebar, viskositas dan rheologi (sifat alir) sediaan krim.
1. Uji Organoleptis dan pH
Tabel VII. Hasil Pengujian Organoleptis dan pH Sediaan Krim
Kriteria Formula
1 A B AB
Bau Bau khas Bau khas Bau khas Bau khas Warna Putih
kecoklatan Putih kecoklatan Putih kecoklatan Putih kecoklatan
Tekstur Halus Halus Halus Halus
pH 5,5 5,5 5,5 5,5
Homogenitas Homogen Homogen Homogen Homogen Sediaan krim pada tabel hasil pengujian organoleptis menunjukkan bahwa sediaan krim berbau khas dan tidak berbau tengik. Warna sediaan krim ekstrak kulit buah manggis putih kecoklatan, warna kecoklatan sediaan krim berasal dari ekstrak kental yang dicampurkan ke dalam sediaan krim. Sediaan krim yang terbentuk memiliki tektur halus dan tidak ada pertikel-partikel kecil yang menggumpal. Pengujian pH sediaan krim berpengaruh pada penetrasi senyawa aktif yang memiliki aktivitas antioksidan ke dalam kulit. Selain itu terkait aseptabilitas atau peneriamaan pada pasien, pH sediaan disesuaikan dengan pH kulit manusia yaitu antara 4-6 (Premjeet, Ajay, Sunil, Bhawana, Sahil, Divashish and Sudeep, 2012) agar tidak mengiritasi kulit ketika diaplikasikan.
2. Uji Daya Sebar
dioleskan, maka semakin besar luas permukaan kulit yang kontak dengan krim (Suwandi, Pramono dan Mufrod, 2012).
Tabel VIII. Hasil Uji Daya Sebar Setelah Didiamkan Selama 48 Jam Formula Daya Sebar (cm2) Viskositas (dPa.s)
I 14,81 ± 0,39 236,67 ± 5,77 A 19,12 ± 0,22 220,00 ± 10,00 B 17,66 ± 0,43 226,67 ± 11,5 AB 21,79 ± 0,73 186,67 ± 5,77
Nilai hasil uji daya sebar dipengaruhi oleh nilai hasil uji viskositas, karena nilai hasil uji daya sebar berbanding terbalik dengan nilai hasil uji viskositas. Jika nilai hasil uji viskositas suatu sediaan semakin besar, maka nilai hasil uji daya sebar sediaan tersebut akan semakin kecil dan sebaliknya. Dari tabel 8 didapatkan hasil formula AB memiliki nilai hasil uji daya sebar yang paling besar yang kemudiaan diikuti oleh formula A, formula B dan formula I yang memiliki nilai hasil uji daya sebar yang paling kecil.
Persamaan desain faktorial untuk respon daya sebar sediaan krim ekstrak kulit buah manggis (Garcinia mangostana L.) terdapat pada persamaan (3) berikut:
Y = 8,237 + 0,633 (X1) + 0,421 (X2) – 3,658 (X1)(X2) ... (3)
Y merupakan daya sebar, X1 merupakan parafin cair, X2 merupakan
gliserol, serta X1 X2 merupakan interaksi antara parafin cair dan gliserol. Dari
dengan penambahan parafin cair dan gliserol dapat memberikan perubahan nilai respon daya sebar yang signifikan sehingga dapat dilakukan optimasi.
Dari persamaan (3) didapatkan counterplot respon daya sebar yang dapat dilihat pada gambar 12.
Gambar 12. Counterplot Respon Daya Sebar Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.)
[image:65.595.87.512.195.627.2]Tabel IX. Pengaruh Parafin Cair, Gliserol dan Interaksi Keduanya Terhadap Respon Daya Sebar
Faktor Efek p-value
Parafin cair 4,22 < 0,0001
Gliserol 2,76 < 0,0001
Interaksi -0,093 0,7447
Parafin cair dan gliserol memiliki efek positif yang berarti kedua faktor tersebut mampu meningkatkan respon daya sebar sediaan krim ekstrak kulit buah manggis. Sedangkan interaksinya memiliki nilai efek negatif, yang berati interaksi antara parafin cair dan gliserol menurunkan respon daya sebar sediaan krim antioksidan ekstrak kulit buah manggis. Parafin cair dan gliserol memiliki efek yang signifikan terhadap perubahan respon daya sebar sediaan krim (p-value < 0,05), sedangkan interaksi keduanya tidak memiliki efek yang
[image:66.595.85.512.207.671.2]signifikan terhadap perubahan respon daya sebar sediaan krim (p-value > 0,05). Dari efek serta persamaan daya sebar krim yang diperoleh, didapatkan faktor dominan yang menentukan respon daya sebar adalah parafin cair.
Berdasarkan gambar 13 menunjukkan parafin cair pada level tinggi ataupun rendah gliserol menyebabkan peningkatan respon daya sebar krim ekstrak kulit buah manggis (Garcinia mangostana L.).
3. Uji Viskositas
[image:68.595.82.516.216.656.2]Pengujuan viskositas bertujuan untuk mengetahui kekentalan sediaan krim dengan variasi konsentrasi parafin cair dan gliserol yang digunakan. Sediaan krim tidak boleh terlalu viskos dan terlalu encer karena berkaitan dengan efek terapi yang diinginkan serta kenyamanan penggunaan pasien (acceptability pasien) (Shovyana dan Zulkarnain, 2013).
Tabel X. Hasil Uji Viskositas Krim Ekstrak Kulit Buah Manggis Formula Daya Sebar (cm2) Viskositas (dPa.s)
I 14,81 ± 0,39 236,67 ± 5,77 A 19,12 ± 0,22 220,00 ± 10,00 B 17,66 ± 0,43 226,67 ± 11,5 AB 21,79 ± 0,73 186,67 ± 5,77
Dari data hasil uji viskositas pada tabel 10 menunjukkan bahwa formula AB memiliki hasil uji viskositas dengan nilai terendah yang kemudian diikuti oleh formula A, formula B dan formula I yang memiliki hasil uji viskositas dengan nilai tertinggi. Semakin banyak penambahan parafin cair dan gliserol dalam sediaan menyebabkan nilai viskositas semakin kecil. Nilai viskositas sediaan krim yang dikendaki yaitu antara 170-220 dPa.s.
Persamaan desain faktorial untuk respon viskositas sediaan krim dapat dilihat pada persamaan (4):
Y = 244,955 - 0,255 (X1) + 2,069 (X2) – 0,460 (X1)(X2) ... (4)
Y merupakan respon viskositas, X1 merupakan parafin cair, X2
merupakan gliserol, serta X1X2 merupakan interaksi antara parafin cair dan
dengan p-value < 0,05 (signifikan). Hasil uji viskositas tersebut menunjukkan bawa dengan penambahan parafin cair dan gliserol dapat memberikan perubahan nilai respon viskositas yang signifikan sehingga dapat dilakukan optimasi.
Dari persamaan (4) didapatkan counterplot respon viskositas sediaan krim yang dapat dilihat pada gambar 15.
Gambar 15. Counterplot Respon Viskositas Sediaan Krim Ekstrak Kulit Buah Manggis (Garcinia mangostana L.)
Daerah counterplot yang berwarna biru menunjukkan daerah dengan respon viskositas yang paling rendah, sedangkan counterplot yang berwarna merah menunjukkan daerah dengan respon viskositas yang paling tinggi. Dari grafik counterplot didapatkan bahwa semakin banyak penggunaan parafin cair maupun gliserol pada sediaan krim akan menyebabkan semakin menurunnya respon viskositas.
[image:69.595.87.512.224