ILMU RESEP TEORI
Jilid II ( untuk kelas II )
Cetakan Kedua
Disusun Berdasarkan Kurikulum SMF 2001
KHUSUS DIPERGUNAKAN UNTUK SEKOLAH MENENGAH FARMASI
Departemen Kesehatan RI
Badan Pengembangan Dan Pemberdayaan
Sumber Daya Manusia Kesehatan
Pusdiknakes
2004
375.615 1 Ind i
ILMU RESEP TEORI
Jilid II ( untuk kelas II ) Cetakan Kedua
Disusun Berdasarkan Kurikulum SMF 2001
KHUSUS DIPERGUNAKAN UNTUK SEKOLAH MENENGAH FARMASI
Tim Penyusun :
1. Drs. Seno Soetopo, Apt. 2. Dra. Siti Atifah Wardiyati, Apt. 3. Dra. Russie Rohadiyatie, Apt. 4. Purwitaningsih, S.Pd.
Tim Pembahas / Editor :
1. Drs. Abd. Karim Zulkarnaen, Apt. M.Si. 2. Drs. Fery Norhendy, Apt.
3. Drs. Hendra Nanto, Apt. 4. Dra. Zubaedah, Apt.
5. Fahleni, S.Si., Apt. 6. Yugo Susanto, S.Si., Apt. 7. I. Wayan Sueta, B.A 8. Yulie, Amd.
KATA PENGANTAR
Dengan memanjatkan puji dan syukur kehadirat Tuhan Yang Maha Esa, atas segala rahmat dan petunjukNya, buku pegangan untuk siswa Sekolah Menengah Farmasi telah dapat disusun kembali. Penyusunan kembali ini disesuaikan dengan kurikulum baru yakni Kurikulum Sekolah Menengah Farmasi 2001.
Kami sangat menghargai usaha Tim Penyusun buku pegangan ini yang dikoordinir oleh Sekretariat Bersama Sekolah Menengah Farmasi Se Indonesia dan telah melibatkan seluruh unsur SMF Se Indonesia.
Kami harapkan buku ini sangat bermanfaat bagi siswa / peserta didik, guru / tenaga pendidik di sekolah dalam upaya peningkatan pengetahuan dan keterampilannya, selanjutnya dapat meningkatkan pelayanan kepada masyarakat di bidang farmasi khususnya dan dibidang kesehatan umumnya.
Akhirnya untuk penyempurnaan cetakan selanjutnya kami harapkan adanya saran perbaikan dan kritik dari semua pembaca.
PENGANTAR DARI SEKBER
Cepatnya perkembangan ilmu pengetahuan terutama dalam bidang farmasi telah diikuti dengan perombakan kurikulum Sekolah Menengah Farmasi 1987 dengan kurikulum Sekolah Menengah Farmasi 2001. Dalam kurikulum baru ini telah diperjelas kompetensi seorang Asisten Apoteker berdampingan dengan peran tenaga farmasi lainnya.
Dengan mengucap syukur kehadirat Tuhan yang Maha Esa,
Buku Ilmu Resep Jilid II untuk siswa kelas II Sekolah
Menengah Farmasi dapat terbit pada waktunya. Buku Ilmu Resep ini disusun kembali untuk disesuaikan dengan
perkembangan jenis obat dan teknologinya disertai dengan harapan akan menjadi buku pegangan yang sangat bermanfaat bagi siswa Sekolah Menengah Farmasi.
Kami sangat berterima kasih kepada Tim Penyusun, Tim Pembahas dan Editor yang telah bekerja keras sehingga buku ini dapat terbit pada waktunya.
DAFTAR ISI
BAB I BAB II BAB III BAB IV BAB V KATA PENGANTARPENGANTAR DARI SEKBER DAFTAR ISI SOLUTIO ( LARUTAN ) SUSPENSI EMULSI PILULAE GALENIKA Halaman ii iii iv 1 16 22 36 41
BAB I
SOLUTIO (LARUTAN)
A.
PengertianLarutan adalah sediaan cair yang mengandung satu atau lebih zat kimia yang terlarut. Misal : terdispersi secara molekuler dalam pelarut yang sesuai atau campuran pelarut yang saling bercampur.
Karena molekul-molekul dalam larutan terdispersi secara merata, maka penggunaan larutan sebagai bentuk sediaan, umumnya memberikan jaminan keseragaman dosis dan memiliki ketelitian yang baik jika larutan diencerkan atau dicampur.
Bila zat A dilarutkan dalam air atau pelarut lain akan terjadi tipe larutan sebagai berikut :
1. Larutan encer, yaitu larutan yang mengandung sejumlah kecil zat A yang terlarut. 2. Larutan, yaitu larutan yang mengandung sejumlah besar zat A yang terlarut.
3. Larutan jenuh, yaitu larutan yang mengandung jumlah maksimum zat A yang dapat larut dalam air pada tekanan dan temperatur tertentu.
4. Larutan lewat jenuh, yaitu larutan yang mengandung jumlah zat A yang terlarut melebihi batas kelarutannya di dalam air pada temperatur tertentu.
Zat pelarut disebut juga solvent, sedangkan zat yang terlarut disebut solute. Solvent yang biasa dipakai adalah :
1. Air untuk macam-macam garam
2. Spiritus , misalnya untuk kamfer, iodium , menthol. 3. Gliserin, misalnya untuk tannin, zat samak, borax, fenol. 4. Eter, misalnya untuk kamfer, fosfor , sublimat.
5. Minyak, misalnya untuk kamfer dan menthol.
6. Parafin Liquidum, untuk cera, cetaceum, minyak-minyak, kamfer, menthol, chlorobutanol. 7. Eter minyak tanah , untuk minyak-minyak lemak.
B. Faktor – Faktor Yang Mempengaruhi Kelarutan
1. Sifat dari solute atau solvent.
Solute yang polar akan larut dalam solvent yang polar pula. Misalnya garam-garam anorganik larut dalam air.
Solute yang nonpolar larut dalam solvent yang nonpolar pula. Misalnya alkaloid basa (umumnya senyawa organik) larut dalam chloroform.
2. Cosolvensi.
Cosolvensi adalah peristiwa kenaikan kelarutan suatu zat karena adanya penambahan pelarut lain atau modifikasi pelarut. Misalnya Luminal tidak larut dalam air, tetapi larut dalam campuran air – gliserin atau solutio petit
3. Kelarutan.
Zat yang mudah larut memerlukan sedikit pelarut , zat yang sukar larut memerlukan banyak pelarut. Kelarutan zat anorganik yang digunakan dalam farmasi umumnya adalah :
a. Dapat larut dalam air.
Semua garam klorida larut , kecuali AgCl, PbCl2, Hg2Cl2.
Semua garam nitrat larut, kecuali nitrat base, seperti bismuthi subnitras.
Semua garam sulfat larut, kecuali BaSO4, PbSO4, CaSO4 (sedikit larut)
b. Tidak larut dalam air.
Semua garam karbonat tidak larut , kecuali K2CO3, Na2CO3, (NH4) 2CO3.
Semua oksida dan hidroksida tidak larut , kecuali KOH, NaOH, NH4OH, BaO, dan Ba(OH)2.
Semua garam posphat tidak larut, kecuali K3PO4, Na3PO3, (NH4)3PO4 4. Temperatur.
Zat padat umumnya bertambah larut bila suhunya dinaikkan, zat tersebut dikatakan bersifat endoterm, karena pada proses kelarutannya membutuhkan panas.
Zat terlarut + pelarut + panas Larutan
Beberapa zat yang lain justru kenaikan temperatur menyebabkan tidak larut, zat tersebut dikatakan bersifat eksoterm, karena pada proses kelarutannya menghasilkan panas.
Zat terlarut + pelarut Larutan + panas
Contoh : K2SO4, KOH, CaHPO4, Calsium gliseropospat,
minyak atsiri, gas-gas yang larut.
Berdasarkan pengaruh ini maka beberapa sediaan farmasi tidak boleh dipanaskan, misalnya :
a. Zat-zat yang atsiri, misalnya etanol, minyak atsiri b. Zat yang terurai, misalnya Natrii bicarbonas c. Saturatio
d. Senyawa – senyawa calsium, misalnya aqua calcis 5. Salting Out.
Salting out adalah peristiwa adanya zat terlarut tertentu yang mempunyai kelarutan lebih besar di banding zat utama, akan menyebabkan penurunan kelarutan zat utama atau terbentuknya endapan karena ada reaksi kimia.
Contoh :
a. Kelarutan minyak atsiri dalam air akan turun bila kedalam air tersebut ditambahkan larutan NaCl jenuh. Disini kelarutan NaCl dalam air lebih besar dibanding kelarutan minyak atsiri dalam air, maka minyak atsiri akan memisah.
b. Reaksi antara papaverin Hcl dengan solutio charcot menghasilkan endapan papaverin base.
6. Salting In.
Salting in adalah adanya zat terlarut tertentu yang menyebabkan kelarutan zat utama dalam solvent menjadi lebih besar. Contohnya : riboflavin (vitamin B2) tidak larut dalam
air, tetapi larut dalam larutan yang mengandung nicotinamidum (terjadi penggaraman riboflavin + basa NH4 ).
7. Pembentukan kompleks
Pembentukan kompleks adalah peristiwa terjadinya interaksi antara senyawa tak larut dengan zat yang larut dengan membentuk garam kompleks.
Contohnya : Iodium larut dalam larutan KI atau NaI jenuh. KI + I2 KI3
Kecepatan kelarutan dipengaruhi oleh :
Ukuran partikel ; makin halus solute, makin kecil ukuran partikel ; makin luas permukaan solute yang kontak dengan solvent, solute makin cepat larut.
Suhu ; umumnya kenaikan suhu menambah kelarutan solute.
Pengadukan.
C. Cara Mengerjakan Obat Dalam Larutan
Beberapa bahan obat memerlukan cara khusus dalam melarutkannya. diantaranya adalah :
1. Natrium bicarbonas, harus dilakukan dengan cara gerus tuang (aanslibben)
2. Natrium bicarbonas + Natrium salicylas, Bic natric digerus tuang , kemudian ditambah natrium salicylas.Untuk mencegah terjadinya perubahan warna pada larutan harus ditambahkan Natrium pyrophosphat sebanyak 0,25 % dari berat larutan.
3. Sublimat (HgCl2), untuk obat tetes mata harus dilakukan dengan pemanasan atau
dikocok-kocok dalam air panas, kemudian disaring setelah dingin. NaCl dapat meningkatkan kelarutan sublimat, tetapi menurunkan daya baktericidnya. Kadar Sublimat dalam obat mata 1 :4000
4. Kalium permanganat (KMnO4), KMnO4 dilarutkan dengan pemanasan . Pada proses
pemanasan akan terbentuk batu kawi ( MnO2) , oleh sebab itu setelah dingin tanpa
dikocok – kocok dituangkan ke dalam botol atau bisa juga disaring dengan gelas wol . 5. Seng klorida,, melarutkan seng klorid harus dengan air sekaligus, kemudian disaring .
Karena jika airnya sedikit demi sedikit maka akan terbentuk seng oksi klorid yang sukar larut dalam air. Bila terdapat asam salisilat larutkan seng klorid dengan sebagian air kemudian tambahkan asam salisilat dan sisa air baru disaring.
6. Kamfer, kelarutan dalam air 1: 650. Dilarutkan dengan spiritus fortior ( 96 % ) 2 X berat kamfer dalam botol kering kocok-kocok kemudian tambahkan air panas sekaligus , kocok lagi.
7. Tanin, tanin mudah larut dalam air dan dalam gliserin. Tetapi tanin selalu mengandung hasil oksidasi yang larut dalan air, tetapi tidak larut dalam gliserin sehingga larutannya dalam gliserin harus disaring dengan kapas yang dibasahkan. Jika ada air dan gliserin, larutkan tanin dalam air kocok baru tambahkan gliserin.
8. Extract opii dan extract ratanhiae, dilarutkan dengan cara ditaburkan ke dalam air sama banyak, diamkan selama ¼ jam.
9. Perak protein, dilarutkan dalam air suling sama banyak, diamkan selama ¼ jam , di tempat yang gelap.
10. Succus liquiritiae,
a. dengan gerus tuang (aanslibben), bila jumlahnya kecil. b. dengan merebus atau memanaskannya hingga larut. 11. Calcii Lactas dan Calcii Gluconas, kelarutan dalam air 1 : 20
Bila air tidak cukup disuspensikan dengan penambahan PGS dibuat mixtura agitanda. 12. Codein :
a. direbus dengan air 20 X nya, setelah larut diencerkan sebelumdingin. b. dengan alkohol 96 % sampai larut ,lalu segera encerkan dengan air. c. diganti dengan HCl Codein sebanyak 1,17 X-nya.
13. Bahan-bahan obat yang bekerja keras harus dilarutkan tersendiri.
14. Bila terdapat bahan obat yang harus diencerkan dengan air, hasil pengenceran yang diambil paling sedikit adalah 2 CC
15. Pepsin, tidak larut dalam air tapi larut dalam HCl encer.
Pembuatan : pepsin disuspensikan dengan air 10 X nya kemudian tambahkan HCl encer. Larutan pepsin hanya tahan sebentar dan tidak boleh disimpan.
16. Nipagin dan Nipasol, kelarutan 1 : 2000
Nipagin berfungsi sebagai pengawet untuk larutan air Nipasol berfungsi sebagai pengawet untuk larutan minyak a. dilarutkan dengan pemanasan sambil digoyang-goyangkan
b. dilarutkan dulu dengan sedikit etanol baru dimasukkan dalam sediaan yang diawetkan. 17. Fenol, diambil fenol liquefactum yaitu larutan 20 bagian air dalam 100 bagian fenol.
Jumlah yang diambil 1,2 x jumlah yang diminta.
D. Macam – Macam Sediaan Larutan Obat
Bentuk sediaan larutan berdasarkan cara pemberiannya dibedakan atas :
Larutan oral
Yaitu sediaan cair yang dibuat untuk pemberian oral , mengandung satu atau lebih zat dengan atau tanpa bahan pengaroma, pemanis atau pewarna yang larut dalam air atau campuran kosolven-air.
1. Potiones (obat minum)
Adalah solutio yang dimaksudkan untuk pemakaian dalam ( per oral ). Selain berbentuk larutan potio dapat juga berbentuk emulsi atau suspensi.
2. Elixir
Adalah sediaan larutan yang mengandung bahan obat dan bahan tambahan (pemanis, pengawet, pewarna, pewangi) sehingga memiliki bau dan rasa yang sedap dan sebagai pelarut digunakan campuran air - etanol.
Disini etanol berfungsi mempertinggi kelarutan obat . Pada elixir dapat pula ditambahkan glycerol, sorbitol atau propilenglikol. Sedangkan untuk pengganti gula bisa digunakan sirup gula.
3. Sirup.
Ada 3 macam sirup yaitu :
a. sirup simplex mengandung 65 % gula dalam larutan nipagin 0,25 % b/v
b. sirup obat mengandung satu atau lebih jenis obat dengan atau tanpa zat tambahan digunakan untuk pengobatan
c. sirup pewangi tidak mengandung obat tetapi mengandung zat pewangi atau penyedap lain. Penambahan sirup ini bertujuan untuk menutup rasa atau bau obat yang tidak enak.
4. Netralisasi, Saturatio dan Potio Effervescent.
a. Netralisasi adalah obat minum yang dibuat dengan mencampurkan bagian asam dan bagian basa sampai reaksi selesai dan larutan bersifat netral Contoh : Solutio Citratis Magnesici, Amygdalas Ammonicus
Pembuatan : Seluruh bagian asam direaksikan dengan bagian basanya bila perlu reaksi dipercepat dengan pemanasan.
b. Saturatio adalah obat minum yang dibuat dengan mereaksikan asam dengan basa tetapi gas yang terjadi ditahan dalam wadah sehingga larutan jenuh dengan gas. Pembuatan :
1. Komponen basa dilarutkan dalam 2/3 bagian air yang tersedia. Misalnya NaHCO3
digerus tuang kemudian masuk botol.
2. Komponen asam dilarutkan dalam 1/3 bagian air yang tersedia.
3. 2/3 bagian asam masuk basa, gas dibuang seluruhnya. Sisa asam dituang hati-hati lewat tepi botol, segera tutup dengan sampagne knop sehingga gas yang terjadi tertahan.
c. Potio Effervescent adalah saturatio yang CO2nya lewat jenuh.
Pembuatan :
Langkah 1 dan 2 sama dengan pada saturatio.
Langkah ke 3 Seluruh bagian asam dimasukkan kedalam basa dengan hati-hati, segera tutup dengan sampagne knop.
Gas CO2 umumnya digunakan untuk pengobatan, menjaga stabilitas obat, dan
kadang-kadang dimaksudkan untuk menyegar-kan rasa minuman ( corrigensia).
Hal yang harus diperhatikan untuk sediaan saturatio dan potio effervescent adalah : - diberikan dalam botol yang kuat , berisi kira-kira 9/10 bagian dan tertutup kedap
dengan tutup gabus atau karet yang rapat. Kemudian diikat dengan sampagne knop. - Tidak boleh mengandung bahan obat yang tidak larut , karena tidak boleh dikocok.
Pengocokan menyebabkan botol pecah karena botol berisi gas dalam jumlah besar. Penambahan Bahan –bahan.
Zat – zat yang dilarutkan dalam bagian asam a. Zat netral dalam jumlah kecil.
Bila jumlahnya banyak, sebagian dilarutkan dalam asam sebagian dilarutkan dalam basa, berdasarkan perbandingan jumlah airnya.
b. Zat-zat mudah menguap.
c. Ekstrak dalam jumlah kecil dan alkaloid d. Sirup
Zat- zat yang dilarutkan dalam bagian basa.
a. Garam dari asam yang sukar larut . misalnya natrii benzoas, natrii salisilas.
b. Bila saturasi mengandung asam tartrat maka garam-garam kalium dan ammonium harus ditambahkan kedalam bagian basanya, bila tidak, akan terbentuk endapan kalium atau ammonium dari asam tartrat.
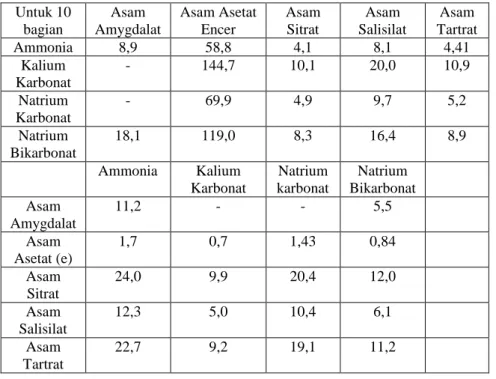
Untuk melihat berapa bagian asam atau basa yang diperlukan dapat melihat tabel penjenuhan ( saturasi dan netralisasi ) dalam Farmakope Belanda edisi V berikut ini :
Tabel saturasi dan netralisasi (Farmakope Belanda V) Untuk 10 bagian Asam Amygdalat Asam Asetat Encer Asam Sitrat Asam Salisilat Asam Tartrat Ammonia 8,9 58,8 4,1 8,1 4,41 Kalium Karbonat - 144,7 10,1 20,0 10,9 Natrium Karbonat - 69,9 4,9 9,7 5,2 Natrium Bikarbonat 18,1 119,0 8,3 16,4 8,9 Ammonia Kalium Karbonat Natrium karbonat Natrium Bikarbonat Asam Amygdalat 11,2 - - 5,5 Asam Asetat (e) 1,7 0,7 1,43 0,84 Asam Sitrat 24,0 9,9 20,4 12,0 Asam Salisilat 12,3 5,0 10,4 6,1 Asam Tartrat 22,7 9,2 19,1 11,2 5. Guttae ( drop)
Guttae atau obat tetes adalah sediaan cair berupa larutan, emulsi atau suspensi , apabila tidak dinyatakan lain dimaksudkan untuk obat dalam. Digunakan dengan cara meneteskan menggunakan penetes yang menghasilkan tetesan yang setara dengan tetesan yang dihasilkan penetes baku yang disebutkan oleh Farmakope Indonesia. Biasanya obat diteteskan ke dalam makanan atau minuman atau dapat diteteskan langsung kedalam mulut.
Dalam perdagangan dikenal pediatric drop yaitu obat tetes yang digunakan untuk anak-anak atau bayi .
Obat tetes sebagai obat luar, biasanya disebutkan tujuan pemakaiannya misalnya : eye drop untuk mata, ear drop untuk telinga.
Larutan topikal
Larutan topikal ialah larutan yang biasanya mengandung air tetapi seringkali juga pelarut lain, misalnya etanol untuk penggunaan topikal pada kulit dan untuk penggunaan topikal pada mukosa mulut. Larutan topikal yang berupa suspensi disebut lotio
Sedian-sedian termasuk larutan topical : 1. Collyrium
Adalah sediaan berupa larutan steril, jernih, bebas zarah asing, isotonus, digunakan untuk membersihkan mata.dapat ditambahkan zat dapar dan zat pengawet.
Kolirium dibuat dengan melarutkan obat dalam air, saring hingga jernih,masukkan kedalam wadah, tutup dan sterilkan.
Penyimpanan : Dalam wadah kaca atau plastik tertutup kedap. Catatan :
Pada etiket harus tertera :
a. Masa penggunaan setelah tutup dibuka. b. “ Obat cuci mata”
Kolirium yang tidak mengandung zat pengawet hanya boleh digunakan paling lama 24 jam setelah botol dibuka tutupnya. Kolirium yang mengandung pengawet dapat digunakan paling lama tujuh hari setelah botol dibuka tutupnya.
2. Guttae Ophthalmicae.
Tetes mata adalah larutan steril bebas partikel asing merupakan sediaan yang dibuat dan dikemas sedemikian rupa hingga sesuai digunakan pada mata. Tetes mata juga tersedia dalam bentuk suspensi, partikel halus dalam bentuk termikronisasi agar tidak menimbulkan iritasi atau goresan pada kornea.
Hal –hal yang perlu diperhatikan pada pembuatan obat tetes mata : a. Nilai isotonisitas.
Secara ideal obat tetes mata harus memiliki nilai isotonis sama dengan larutan NaCl 0,9 % b/v. Tetapi mata masih dapat tahan terhadap nilai isotonis rendah yang setara dengan larutan NaCl 0,6 % b/v dan tertinggi yang setara dengan larutan NaCl 2, 0 % b/v.
b. Pendaparan
Salah satu maksud pendaparan larutan obat mata adalah untuk mencegah kenaikan pH yang disebabkan oleh pelepasan lambat ion hidroksil oleh wadah kaca. Hal tersebut dapat mengganggu kelarutan dan stabilitas obat. Selain itu penambahan dapar juga dimaksudkan untuk menjaga stabilitas obat tertentu misalnya : garam – garam alkaloid.
Air mata normal memiliki pH 7,4 secara ideal obat tetes mata memiliki pH seperti pada air mata, tetapi karena beberapa bahan obat tidak stabil (tidak larut/ rusak/ mengendap) pada pH tersebut maka sebaiknya obat tetes mata di dapar pada pH sedekat mungkin dengan pH air mata supaya tidak terlalu merangsang mata.
Pada larutan yang digunakan pada mata, terlebih pada mata yang luka sterilitas adalah yang paling penting, untuk mencegah terjadinya infeksi lebih lanjut.
c. Pengawet
Wadah larutan obat mata harus tertutup rapat dan disegel untuk menjamin sterilitas pada pemakaian pertama. Larutan harus mengandung zat atau campuran zat yang sesuai untuk mencegah pertumbuhan atau memusnahkan bakteri yang mungkin masuk pada waktu wadah dibuka pada saat digunakan.
Pengawet yang dianjurkan :
nipagin dan nipasol
fenil merkuri nitrat, timerosol
benzalkonium klorid
klorbutanol, fenil etil alcohol
Untuk penggunaan pada pembedahan , selain steril larutan obat mata tidak boleh mengandung antibakteri karena dapat menimbulkan iritasi pada jaringan mata. d. Pengental
Ditambahkan untuk meningkatkan kekentalan sehingga obat lebih lama kontak dengan jaringan. Larutan obat mata yang dikentalkan harus bebas dari partikel yang dapat terlihat. Contoh : metil selulosa, hidroksi propil selulosa, polivinil alcohol
Cara pembuatan obat tetes mata
a. Obat dilarutkan kedalam sal;ah satu zat pembawa yang mengandung salah satu zat pengawet , dijernihkan dengan cara penyaringan, masukkan kedalam wadah, tutup wadah dan sterilkan menggunakan autoklaf pada suhu 115-116oC selama 30 menit.
b. Obat dilarutkan kedalam cairan pembawa berair yang mengandung salah satu zat pengawet dan disterilkan menggunakan bakteri filter masukkan kedalam wadah secara tehnik aseptis dan tutup rapat
c. Obat dilarutkan kedalam cairan pembawa berair yang mengandung salah satu zat pengawet, dijernihkan dengan cara penyaringan, masukkan kedalam wadah, tutup rapat dan sterilkan dengan penambahan bakterisid , dipanaskan pada suhu 98- 100oC selama 30 menit.
3. Gargarisma (Gargle)
Gargarisma atau obat kumur mulut adalah sediaan berupa larutan umumnya dalam keadaan pekat yang harus diencerkan dahulu sebelum digunakan. Dimaksudkan untuk digunakan sebagai pencegahan atau pengobatan infeksi tenggorokan.
Penandaan.
1. Petunjuk pengenceran sebelum digunakan 2. “ Hanya untuk kumur, tidak ditelan “ Contoh : Betadin Gargle.
4. Litus Oris.
Oles Bibir adalah cairan agak kental dan pemakaiannya secara disapukan dalam mulut.
Contoh : Larutan 10 % borax dalam gliserin. 5. Guttae Oris
Tetes mulut adalah obat tetes yang digunakan untuk mulut dengan cara mengencerkan lebih dahulu dengan air untuk dikumur-kumurkan, tidak untuk ditelan. 6. Guttae Nasales
Tetes hidung adalah obat yang digunakan untuk hidung dengan cara meneteskan obat ke dalam rongga hidung, dapat mengandung zat pensuspensi, pendapar dan pengawet. Minyak lemak atau minyak mineral tidak boleh digunakan sebagai cairan pembawa. 7. Inhalationes
Sediaan yang dimaksudkan untuk disedot hidung atau mulut, atau disemprotkan dalam bentuk kabut kedalam saluran pernafasan . Tetesan butiran kabut harus seragam dan sangat halus sehingga dapat mencapai bronkhioli. Inhalasi merupakan larutan dalam air atau gas. ( akan dibahas lebih lanjut dikelas III)
Penandaan : Jika mengandung bahan yang tidak larut pada etiket harus tertera “ Kocok dahulu”
8. Injectiones / obat suntik. (dibahas dikelas III) 9. Lavement / Clysma / Enema.
Cairan yang pemakaiannya per rectum/colon yang gunanya untuk membersihkan atau menghasilkan efek terapi setempat atau sistemik Enema yang digunakan untuk membersihkan atau penolong pada sembelit atau pembersih faeces sebelum operasi,
tidak boleh mengandung zat lendir. Selain untuk membersihkan enema juga berfungsi sebagai karminativa, emolient, diagnostic, sedative, anthelmintic dan lain-lain. Dalam hal ini untuk mengurangi kerja obat yang bersifat merangsang terhadap usus , dipakai basis berlendir misalnya mucilago amyli. Pada pemakaian per rectal berlaku dosis maksimal.
Enema diberikan dalam jumlah variasi tergantung pada umur dan keadaan penderita. Umumnya 0,5 sampai 1 liter, tetapi ada juga yang diperpekat dan diberikan sebanyak 100 – 200 ml.
10. Douche.
Adalah larutan dalam air yang dimasukkan dengan suatu alat ke dalam vagina, baik untuk pengobatan maupun untuk membersihkan. Karenanya larutan ini mengandung bahan obat atau antiseptik. Untuk memudahkan, kebanyakan douche ini dibuat dalam bentuk kering/padat (serbuk, tablet yang kalau hendak digunakan dilarutkan dalam sejumlah air tertentu, dapat juga diberikan larutan kental yang nantinya diencerkan seperlunya. Contoh Betadin Vaginal Douche (dikemas beserta aplikatornya)
11. Epithema /Obat kompres
Adalah cairan yang dipakai untuk mendatangkan rasa dingin pada tempat tempat yang sakit dan panas karena radang atau berdasarkan sifat perbedaan tekanan osmose digunakan untuk mengeringkan luka bernanah. Contoh : Liquor Burowi, Solutio Rivanol, campuran Borwater - Rivanol.
E. Hitungan Farmasi
Farmakope Indonesia Edisi IV memberikan 3 bentuk persen yaitu : 1. Persen bobot per bobot (b/b)
Menyatakan jumlah gram zat dalam 100 gram campuran atau larutan. 2. Persen bobot per volume (b/v)
Menyatakan jumlah gram zat dalam 100 ml larutan, sebagai pelarut dapat digunakan air atau pelarut lain.
3. Persen volume pervolume (v/v)
Menyatakan jumlah ml zat dalam 100 ml larutan. Pernyataan persen tanpa penjelasan lebih lanjut untuk campuran padat atau setengah padat , yang dimaksud adalah b/b, untuk larutan dan suspensi suatu zat padat dalam cairan yang dimaksud adalah b/v dan untuk larutan cair di dalam cairan yang dimaksud adalah v/v dan untuk larutan gas dalam cairan yang dimaksud adalah b/v.
Perhitungan Etanol.
Yaitu mengubah atau mengencerkan kadar etanol yang lebih tinggi menjadi kadar yang lebih rendah .
Perlu diketahui bahwa apabila kita mencampur 2 larutan yang berbeda berat jenisnya (termasuk etanol/spiritus ) akan terjadi penyusutan volume yang disebut dengan kontraksi.
Spiritus atau etanol adalah campuran alkohol absolut dengan air. Umumnya dinyatakan dalam persen b/b atau v/v, sehingga :
alkohol absolute
100 0
x 100 gram = 0 gram air 100 gram – 0 gram = 100 gram 2. 200 cc etanol 70 % v/v artinya larutan mengandung
alkohol absolute
100 70
x 200 cc = 140 cc
air bukan 200 cc – 140 cc = 60 cc, tetapi lebih besar dari 60 cc (hal ini dapat dihitung)
3. 200 cc etanol 70 % b/b, jumlah alkohol absolute tidak bisa langsung dihitung. Disini harus kita sejeniskan terlebih dahulu. Untuk mengetahuinya dapat dipergunakan tabel pada Farmakope edisi IV etanol 70 % b/b = etanol 76,91 % v/v = BJ 0,8658 Volume larutan = 200 cc alkohol absolut = 100 91 , 76 x 200 cc = 153,82 cc Berat larutan = 0,8658 x 200 cc = 173,16 gram Alkohol absolut =
100 70
x 173,16 g = 121,21 gram Berat air = 173,16 g – 121,21 g = 51,95 gram
Latihan .
1. 500 gram etanol 95 % b/b , berapa cc dan gram alkohol absolutnya ? Jawab : alkohol absolute = 100 95 x 500 gram = 475gram 95 % b/b = 96,79 % v/v = BJ 0,8020 500/0,8020 = 623,44 cc, alkohol absolut = 100 79 , 96 x 623,44 cc = 603,42 cc
2. 1 liter etanol 77,79 % v/v, berapa cc dan gram alkohol absolutnya ? Jawab : Alkohol absolute = 100 79 , 77 x 1000 cc = 777,9 cc
77,79 % v/v = 71 % b/b = BJ 0,8634 Berat larutan = 0.8634 x 1000 = 863,4 gram Alk. absolute =
100 71
x 863,44 gram = 613,04gram
3. 500 gram etanol 73,3 % v/v berapa gram dan cc alkohol absolutnya ? Jawab : 73,3 % v/v = 66 % b/b = 0,8753 alkohol absolute = 100 66 x 500 gram = 330 gram volume larutan = 8753 , 0 500 = 571,23 cc alkohol absolute = 100 3 , 73 x 571,23 cc = 418,71 cc
4. 1 liter etanol 57 % b/b berapa cc dan gram alkohol absolutnya Jawab : 57 % b/b = 64,8 % v/v = BJ 0,8964 alkohol absolut = 100 8 , 64 x 1000 cc = 648 cc Berat larutan = 1000 x 0,8964 = 896,4 gram Alkohol absolut = 100 57 x 896,4 g = 510,95 gram 5. 800 cc etanol BJ 0,8364 Jawab : BJ 0,8364 = 87,8 % v/v = 82 % b/b Alkohol absolut = 100 8 , 87 x 800 cc = 702,4 cc Berat larutan = 800 x 0,8364 = 669, 12 gram Alkohol absolut =
100 82
x 669,12 g = 548,68gram
Kegunaan menghitung alkohol absolut adalah untuk mencari kadar.
Contoh soal :
Berapa % b/b kadar etanol yang diperoleh kalau kita mencampurkan 100 gram etanol 70 % v/v dengan air 200 cc ?
100 gram etanol 70 % v/v = 62,44 % b/b alkohol abs. 62,44/100 x 100 = 62,44 g Kadar campuran = 200 100 44 , 62 x 100 % = 20,81 % b/b
Atau menggunakan rumus : B1 x K1 + B2 x K2 = B3 x K3 100 x 62,44 + 200 x 0 = 300 x K3 K3 = 300 44 , 62 x 100 % = 20, 81 %
Apabila tabel yang dimaksud tidak ada dalam daftar maka harus dilakukan interpolasi . Cara :
Misalkan yang hendak diketahui % b/b dan BJ etanol 90,5 % v/v.
Ambil 1 tabel yang terdekat diatasnya. Dengan perbandingan biasa kita dapat membuat tabel baru. BJ 0,8271 b/b 85,69 v/v 90 0,5 1 0,0066 1,3 90,5 0,8337 86,99 91 Perbandingan 0,5/1 =1/2 % b/b= 85,69 + ( ½ x 1,3 ) = 85,69 + 0 65 = 86,34 BJ = 0,8271 + ( ½ x 0,0066 ) = 0,8271 + 0,0033 = 0,8304
Jadi etanol 90,5 % v/v = etanol 86,34 % b/b; Bj = 0,8304. Latihan soal.
1. Interpolasi dari BJ 0,9003 2. Interpolasi dari 66,5 % b/b
3. Tentukan % b/b, % v/v dan BJ dari campuran : 1200 gram etanol 60 % v/v + 200 cc air 4. Hitunglah % b/b, % v/v dan BJ campuran :
100 gram spiritus dilutus + 100 gram air
5. Hitung berapa gram air yang ditambahkan pada campuaran 500 cc spiritus 96 % v/v + air samapi 1 liter
6. Dibutuhkan 1 liter spiritus 60 % b/b. Dalam persediaan kita mempunyai spiritus fortior. Berapa cc air yang diperlukan
7. Dibutuhkan etanol 40 % v/v dalam persediaan terdapat 300 cc spiritus fortior dan 200 cc spiritus dilutus.
8. Tentukan BJ dari campuran sama berat spiritus dilutus dan air 9. Tentukan BJ dari campuran sama volume spiritus dilutus dan air. Contoh soal kontraksi.
Dicampurkan 100 cc spiritus dilutus dengan 100 cc air.
Berapa cc hasil yang akan didapat dan hitungkan kontraksinya! 100 cc x 70 % v/v + 100 cc 0% v/v ? Berat campuran : = (100 x 0,8837) g + 100 g 88,37 + 100 = 188,37 g (x) % b/b Etanol absolut : = 100 44 , 62 x 88,37 = 55,18 g Kadar = 37 , 188 18 , 55 x 100 % = 29,29 % b/b
BJ 0,9545 (hasil interpolasi), maka volume sebenarnya (Volume praktis) =
9545 , 0 37 , 188 = 197,35 ml Volume teoritis = Vt = V1 + V2 = 100 ml + 100 ml = 200 ml Kontraksi = Vt - Vp = 200 ml - 197,35 ml = 2,65 ml % kontraksi = 200 65 , 2 x 100 % = 1,33 %. kontraksi tidak boleh lebih dari 3,6 %
Latihan soal
2. Hitunglah kontraksi dalam % jika dicampur 200 ml spiritus dilutus dengan 300 ml spiritus 95 % v/v
3. Hitunglah kontraksi bila dicampur masing-masing 100 g spiritus 95 % v/v, 100 g spiritus dilutus dan 200 g air.
Hitungan Pengenceran Bukan Etanol.
Hendak dibuat 300 gram larutan yang mengandung 10 % NaCl dengan mempergunakan larutan yang mengandung 50 % NaCl. Berapa jumlah larutan 50 % yang harus dipakai dan berapa air yang harus ditambahkan ?
Untuk menyelesaikan soal ini , tentukan dulu :
1. Mana bagian yang membentuk dan mana yang terbentuk. 2. Komponen yang belum kita ketahui kita misalkan X 3. Zat aktif yang membentuk sama dengan yang terbentuk
4. Berat zat yang membentuk harus sama dengan yang terbentuk.
5. Kalau terdapat selisih berat antara zat terbentuk dengan yang membentuk maka selisihnya adalah zat penambah.
Jawab.
X gram 50 % = 300 gram 10 % Zat aktif (za) =
100 50 x X = 0,5 X Z.A = 100 10 x 300 = 30 gram 0,5 X = 30 X = 5 , 0 30 g = 60 gram
Zat penambah (air) = 300 - 60 = 240 gram
Latihan soal
1. Hitung berapa gram zat penambah diperlukan pada pembuatan 400 gram campuran dengan kadar 20 %, bila yang tersedia 200 gram zat 25 % dan zat 15% yang belum diketahui jumlahnya. Jawab. X g x 15 % + 200 g x 25 % 400 g x 20 % Z.A (15/100 x X ) + ( 25/100 x 200) 20/100 x 400 Z.A 0,15 X + 50 = 80 0,15 X = 80 - 50 X = 15 , 0 30 = 200 Zat 15 % diambil sebanyak 200 gram
Zat penambah sebanyak 400 – ( 200 + 200 ) = 0 gram
2. Hitung berapa gram larutan NaCl 40 % harus ditambahkan pada 10 gram larutan NaCl 10 % supaya diperoleh 100 gram larutan NaCl 20 % !
Jawab : ( 10 g x 10 % ) + ( X g x 40 % ) 100 g x 20 % Z.A( 100 10 x 10 ) + ( 100 40 x X ) 20/100 x 100 1 + 0,4 X = 20 X = 20 - 4 , 0 1 X = 47,5 g Larutan NaCl 40 % yang diambil 47,5 gram
Zat penambah 100 - ( 10 + 47,5 ) = 42,5 gram
3. Hitunglah berapa gram larutan glukosa 15 % dan glukosa 25 % harus ditambahkan pada 200 gram larutan glukosa 20 % supaya diperoleh 600 gram larutan glukosa 18 % Jawab : Glukosa 15 % = X Glukosa 25 % = (600 – 200 ) – X X x 15 % + (400-X) x 25 % + 200 x 20 % 600 x 18 % 0,15 X + 100 - 0,25 X + 40 = 108 0,15 X - 0,25 X = 108 - ( 100 + 40) - 0,1 X = - 32 X = 1 , 0 32 = 320
Jumlah glukosa 15 % 320 gram
Jumlah glukosa 25 % 400 – 320 = 80 gram
4. 50 mg alkaloid belladon dicampur dengan 1 gram extract belladon yang mengandung 1,5 % alkaloid belladon. Berapa gram campuran extract belladon 1,3 % yang diperoleh dan berapa gram zat penambahnya.
Jawab : 50 x 100 % + 1000 x 1,5 % X x 1,3 % 50 + 15 = 0, 013 X X = 013 , 0 65 = 5000 mg = 5 g Campuran yang diperoleh 5000 mg = 5 gram
BAB II
SUSPENSI
A. Pengertian
Suspensi adalah sediaan cair yang mengandung partikel padat tidak larut yang terdispersi dalam fase cair.
Suspensi oral adalah sediaan cair mengandung partikel padat yang terdispersi dalam pembawa cair dengan bahan pengaroma yang sesuai dan ditujukan untuk penggunaan oral. Beberapa suspensi yang diberi etiket sebagai susu atau magma termasuk dalam kategori ini. Beberapa suspensi dapat langsung digunakan , sedangkan yang lain berupa campuran padat yang harus dikonstitusikan terlebih dahulu dengan pembawa yang sesuai segera sebelum digunakan. Sediaan seperti ini disebut “ Untuk Suspensi oral”
Suspensi topikal adalah sediaan cair mengandung partikel padat yang terdispersi dalam pembawa cair yang ditujukan untuk penggunaan pada kulit. Beberapa suspensi yang diberi etiket sebagai “lotio” termasuk dalam kategori ini.
Suspensi tetes telinga adalah sediaan cair mengandung partikel-partikel halus yang ditujukan untuk diteteskan telinga bagian luar.
Suspensi optalmik adalah sediaan cair steril yang mengandung partikel-partikel yang terdispersi dalam cairan pembawa untuk pemakaian pada mata. Obat dalam suspensi harus dalam bentuk termikronisasi agar tidak menimbulkan iritasi atau goresan pada kornea. Suspensi obat mata tidak boleh digunakan bila terjadi massa yang mengeras atau penggumpalan.
Suspensi untuk injeksi adalah sediaan berupa suspensi serbuk dalam medium cair yang sesuai dan tidak disuntikkan secara intravena atau kedalam larutan spinal .
Suspensi untuk injeksi terkonstitusi adalah sediaan padat kering dengan bahan pembawa yang sesuai untuk membentuk larutan yang memenuhi semua persyaratan untuk suspensi steril setelah penambahan bahan pembawa yang sesuai.
B. Stabilitas Suspensi
Salah satu problem yang dihadapi dalam proses pembuatan suspensi adalah cara memperlambat penimbunan partikel serta menjaga homogenitas dari partikel. Cara tersebut merupakan salah satu tindakan untuk menjaga stabilitas suspensi. Beberapa faktor yang mempengaruhi stabilitas suspensi ialah :
1. Ukuran partikel.
Ukuran partikel erat hubungannya dengan luas penampang partikel tersebut serta daya tekan keatas dari cairan suspensi itu. Hubungan antara ukuran partikel merupakan perbandingan terbalik dengan luas penampangnya. Sedangkan antara luas penampang dengan daya tekan keatas merupakan hubungan linier. Artinya semakin besar ukuran partikel semakin kecil luas penampangnya. (dalam volume yang sama) .Sedangkan semakin besar luas penampang partikel daya tekan keatas cairan akan semakin memperlambat gerakan partikel untuk mengendap, sehingga untuk memperlambat gerakan tersebut dapat dilakukan dengan memperkecil ukuran partikel.
2. Kekentalan (viscositas)
Kekentalan suatu cairan mempengaruhi pula kecepatan aliran dari cairan tersebut, makin kental suatu cairan kecepatan alirannya makin turun (kecil).
Kecepatan aliran dari cairan tersebut akan mempengaruhi pula gerakan turunnya partikel yang terdapat didalamnya. Dengan demikian dengan menambah viskositas cairan, gerakan turun dari partikel yang dikandungnya akan diperlambat. Tetapi perlu
diingat bahwa kekentalan suspensi tidak boleh terlalu tinggi agar sediaan mudah dikocok dan dituang.
Hal ini dapat dibuktikan dengan hukum “ STOKES “.
d 2 ( - 0 ) g
V = ---
Keterangan : V = kecepatan aliran d = diameter dari partikel = berat jenis dari partikel 0 = berat jenis cairan
g = gravitasi = viskositas cairan 3. Jumlah partikel (konsentrasi)
Apabila didalam suatu ruangan berisi partikel dalam jumlah besar , maka partikel tersebut akan susah melakukan gerakan yang bebas karena sering terjadi benturan antara partikel tersebut.
Benturan itu akan menyebabkan terbentuknya endapan dari zat tersebut, oleh karena itu makin besar konsentrasi partikel, makin besar kemungkinan terjadinya endapan partikel dalam waktu yang singkat.
4. Sifat/muatan partikel
Dalam suatu suspensi kemungkinan besar terdiri dari beberapa macam campuran bahan yang sifatnya tidak selalu sama. Dengan demikian ada kemungkinan terjadi interaksi antar bahan tersebut yang menghasilkan bahan yang sukar larut dalam cairan tersebut. Karena sifat bahan tersebut sudah merupakan sifat alam, maka kita tidak dapat mempe-ngaruhinya.
Stabilitas fisik suspensi farmasi didefinisikan sebagai kondisi suspensi dimana partikel tidak mengalami agregasi dan tetap terdistribusi merata. Bila partikel mengendap mereka akan mudah tersuspensi kembali dengan pengocokan yang ringan. Partikel yang mengendap ada kemungkinan dapat saling melekat oleh suatu kekuatan untuk membentuk agregat dan selanjutnya membentuk compacted cake dan peristiwa ini disebut caking .
Kalau dilihat dari faktor-faktor tersebut diatas, faktor konsentrasi dan sifat dari partikel merupakan faktor yang tetap, artinya tidak dapat diubah lagi karena konsentrasi merupakan jumlah obat yang tertulis dalam resep dan sifat partikel merupakan sifat alam. Yang dapat diubah atau disesuaikan adalah ukuran partikel dan viskositas.
Ukuran partikel dapat diperkecil dengan menggunakan pertolongan mixer, homogeniser, colloid mill dan mortir. Sedangkan viskositas fase eksternal dapat dinaikkan dengan penambahan zat pengental yang dapat larut kedalam cairan tersebut. Bahan-bahan pengental ini sering disebut sebagai suspending agent (bahan pensuspensi), umumnya bersifat mudah berkembang dalam air (hidrokoloid).
Bahan pensuspensi atau suspending agent dapat dikelompokkan menjadi dua, yaitu : 1. Bahan pensuspensi dari alam
Bahan pensuspensi alam dari jenis gom sering disebut gom/hidrokoloid. Gom dapat larut atau mengembang atau mengikat air sehingga campuran tersebut membentuk mucilago atau lendir. Dengan terbentuknya mucilago maka viskositas cairan tersebut bertambah dan akan menambah stabilitas suspensi. Kekentalan mucilago sangat dipengaruhi oleh panas, pH dan proses fermentasi bakteri .
Hal ini dapat dibuktikan dengan suatu percobaan : - Simpan 2 botol yang berisi mucilago sejenis .
- Satu botol ditambah dengan asam dan dipanaskan, kemudian keduanya disimpan ditempat yang sama.
- Setelah beberapa hari diamati ternyata botol yang ditambah dengan asam dan dipanaskan mengalami penurunan viskositas yang lebih cepat dibanding dengan botol tanpa pemanasan.
Termasuk golongan gom adalah :
Acasia ( pulvis gummi arabici)
Didapat sebagai eksudat tanaman akasia sp, dapat larut dalam air, tidak larut dalam alkohol, bersifat asam. Viskositas optimum dari mucilagonya antara pH 5 – 9. Dengan penambahan suatu zat yang menyebabkan pH tersebut menjadi diluar 5 – 9 akan menyebabkan penurunan viskositas yang nyata.
Mucilago gom arab dengan kadar 35 % kekentalannya kira-kira sama dengan gliserin. Gom ini mudah dirusak oleh bakteri sehingga dalam suspensi harus ditambahkan zat pengawet ( preservative).
Chondrus
Diperoleh dari tanaman chondrus crispus atau gigartina mamilosa, dapat larut dalam air, tidak larut dalam alkihol, bersifat alkali. Ekstrak dari chondrus disebut caragen, yang banyak dipakai oleh industri makanan. Caragen merupakan derivat dari saccharida, jadi mudah dirusak oleh bakteri, jadi perlu penambahan bahan pengawet untuk suspensi tersebut.
Tragacanth
Merupakan eksudat dari tanaman astragalus gumnifera. Tragacanth sangat lambat mengalami hidrasi, untuk mempercepat hidrasi biasanya dilakukan pemanasan, Mucilago tragacanth lebih kental dari mucilago dari gom arab. Mucilago tragacanth baik sebagai stabilisator suspensi saja, tetapi bukan sebagai emulgator.
Algin
Diperoleh dari beberapa species ganggang laut. Dalam perdagangan terdapat dalam bentuk garamnya yakni Natrium Alginat. Algin merupakan senyawa organik yang mudah mengalami fermentasi bakteri sehingga suspensi dengan algin memerlukan bahan pengawet. Kadar yang dipakai sebagai suspending agent umumnya 1-2 %.
Golongan bukan gom
Suspending agent dari alam bukan gom adalah tanah liat.Tanah liat yang sering dipergunakan untuk tujuan menambah stabilitas suspensi ada 3 macam yaitu bentonite,
hectorite dan veegum. Apabila tanah liat dimasukkan ke dalam air mereka akan
mengembang dan mudah bergerak jika dilakukan penggojokan. Peristiwa ini disebut
Karena peristiwa tersebut, kekentalan cairan akan bertambah sehingga stabilitas dari suspensi menjadi lebih baik.
Sifat ketiga tanah liat tersebut tidak larut dalam air, sehingga penambahan bahan tersebut kedalam suspensi adalah dengan menaburkannya pada campuran suspensi. Kebaikan bahan suspensi dari tanah liat adalah tidak dipengaruhi oleh suhu/panas dan fermentasi dari bakteri, karena bahan-bahan tersebut merupakan senyawa anorganik, bukan golongan karbohidrat.
2. Bahan pensuspensi sintetis
Derivat selulosa
Termasuk dalam golongan ini adalah metil selulosa (methosol, tylose), karboksi metil selulosa (CMC), hidroksi metil selulosa.
Dibelakang dari nama tersebut biasanya terdapat angka/nomor, misalnya methosol 1500. Angka ini menunjukkan kemampuan menambah viskositas dari cairan yang dipergunakan untuk melarutkannya. Semakin besar angkanya berarti kemampuannya semakin tinggi. Golongan ini tidak diabsorbsi oleh usus halus dan tidak beracun , sehingga banyak dipakai dalam produksi makanan. Dalam farmasi selain untuk bahan pensuspensi juga digunakan sebagai laksansia dan bahan penghancur/disintregator dalam pembuatan tablet.
Golongan organik polimer
Yang paling terkenal dalam kelompok ini adalah Carbophol 934 (nama dagang suatu pabrik) .Merupakan serbuk putih bereaksi asam, sedikit larut dalam air,tidak beracun dan tidak mengiritasi kulit, serta sedikit pemakaiannya.Sehingga bahan tersebut banyak digunakan sebagai bahan pensuspensi. Untuk memper-oleh viskositas yang baik diperlukan kadar 1 %.
Carbophol sangat peka terhadap panas dan elektrolit. Hal tersebut akan mengakibatkan penurunan viskositas dari larutannya.
C. Cara Mengerjakan Obat Dalam Suspensi
1. Metode pembuatan suspensi. Suspensi dapat dibuat secara :
Metode dispersi
Dengan cara menambahkan serbuk bahan obat kedalam mucilago yang telah terbentuk kemudian baru diencerkan.
Perlu diketahui bahwa kadang-kadang terjadi kesuka-ran pada saat mendispersi serbuk dalam vehicle, hal tersebut karena adanya udara, lemak, atau kontaminan pada serbuk. Serbuk yang sangat halus mudah kemasukan udara sehingga sukar dibasahi. Mudah dan sukarnya serbuk terbasahi tergantung besarnya sudut kontak antara zat terdispers dengan medium. Bila sudut kontak 90o serbuk akan mengambang diatas cairan. Serbuk yang demikian disebut memiliki sifat hidrofob. Untuk menurunkan tegangan antar muka antara partikel zat padat dengan cairan tersebut perlu ditambahkan zat pembasah atau wetting agent.
Metode praesipitasi.
Zat yang hendak didispersi dilarutkan dahulu dalam pelarut organik yang hendak dicampur dengan air. Setelah larut dalam pelarut organik diencer- kan dengan larutan pensuspensi dalam air. Akan terjadi endapan halus dan tersuspensi dengan bahan pensuspensi.
2. Sistem pembentukan suspensi
Sistem flokulasi
Dalam sistem flokulasi, partikel terflokulasi terikat lemah,cepat mengendap dan pada penyimpanan tidak terjadi cake dan mudah tersuspensi kembali
Sistem deflokulasi
Dalam sistem deflokulasi partikel deflokulasi mengendap perlahan dan akhirnya membentuk sedimen, dimana terjadi agregasi akhirnya terbentuk cake yang keras dan sukar tersuspensi kembali.
Secara umum sifat-sifat dari partikel flokulasi dan deflokulasi adalah : Deflokulasi :
1. Partikel suspensi dalam keadaan terpisah satu dengan yang lain.
2. Sedimentasi yang terjadi lambat masing - masing partikel mengendap terpisah dan ukuran partikel adalah minimal
3. Sedimen terbentuk lambat
4. Akhirnya sedimen akan membentuk cake yang keras dan sukar terdispersi lagi
5. Ujud suspensi menyenangkan karena zat tersuspensi dalam waktu relatif lama. Terlihat bahwa ada endapan dan cairan atas berkabut.
Flokulasi :
1. Partikel merupakan agregat yang bebas. 2. Sedimentasi terjadi cepat.
3. Sedimen terbentuk cepat.
4. Sedimen tidak membentuk cake yang keras dan padat dan mudah terdispersi kembali seperti semula
5. Ujud suspensi kurang menyenangkan sebab sedimentasi terjadi cepat dan diatasnya terjadi daerah cairan yang jernih dan nyata.
D. Formulasi Suspensi
Membuat suspensi stabil secara fisis ada 2 kategori :
Penggunaan “structured vehicle” untuk menjaga partikel deflokulasi dalam suspensi
structured vehicle, adalah larutan hidrokoloid seperti tilose, gom, bentonit, dan
lain-lain.
Penggunaan prinsip-prinsip flokulasi untuk membentuk flok, meskipun terjadi cepat pengendapan, tetapi dengan penggojokan ringan mudah disuspensikan kembali.
Pembuatan suspensi sistem flokulasi ialah :
1. Partikel diberi zat pembasah dan dispersi medium
2. Lalu ditambah zat pemflokulasi, biasanya berupa larutan elektrolit, surfaktan atau polimer.
3. Diperoleh suspensi flokulasi sebagai produk akhir.
4. Apabila dikehendaki agar flok yang terjadi tidak cepat mengendap, maka ditambah
structured vehicle
5. Produk akhir yang diperoleh ialah suspensi flokulasi dalam
structured vehicle
Bahan pemflokulasi yang digunakan dapat berupa larutan elektrolit, surfaktan atau polimer. Untuk partikel yang bermuatan positif digunakan zat pemflokulasi yang bermuatan
negatif, dan sebaliknya. Contohnya suspensi bismuthi subnitras yang bermuatan positif digunakan zat pemflokkulasi yang bermuatan negatif yaitu kalium fosfat monobase. Suspensi sulfamerazin yang bermuatan negatif digunakan zat pemflokulasi yang bermuatan positif yaitu AlCl3 (Aluminium trichlorida)
Bahan Pengawet
Penambahan bahan lain dapat pula dilakukan untuk menambah stabilitas suspensi, antara lain penambahan bahan pengawet. Bahan ini sangat diperlukan terutama untuk suspensi yang menggunakan hidrokoloid alam, karena bahan ini sangat mudah dirusak oleh bakteri.
Sebagai bahan pengawet dapat digunakan butil p. benzoat (1 : 1250), etil p. benzoat (1 : 500 ), propil p. benzoat (1 : 4000), nipasol, nipagin 1 %
Disamping itu banyak pula digunakan garam komplek dari mercuri untuk pengawet, karena memerlukan jumlah yang kecil, tidak toksik dan tidak iritasi. Misalnya fenil mercuri nitrat, fenil mercuri chlorida, fenil mercuri asetat.
E. Penilaian Stabilitas Suspensi
1. Volume sedimentasi
Adalah suatu rasio dari volume sedimentasi akhir (Vu) terhadap volume mula-mula dari
suspensi (Vo) sebelum mengendap.
2. Derajat flokulasi
Adalah suatu rasio volume sedimen akhir dari suspensi flokulasi (Vu) terhadap volume
sedimen akhir suspensi deflokulasi ( Voc)
Derajat Flokulasi =
Voc Vu
3. Metode reologi
Berhubungan dengan faktor sedimentasi dan redispersibilitas, membantu menentukan perilaku pengendapan, mengatur vehicle dan susunan partikel untuk tujuan perbandingan.
4. Perubahan ukuran partikel
Digunakan cara Freeze – thaw cycling yaitu temperatur diturunkan sampai titik beku, lalu dinaikkan sampai mencair kembali. Dengan cara ini dapat dilihat pertumbuhan kristal, yang pokok menjaga tidak terjadi perubahan ukuran partikel dan sifat kristal.
F = o u
V V
BAB III
EMULSI
A. Pengertian Emulsi
Menurut FI Edisi IV, emulsi adalah sistem dua fase yang salah satu cairannya terdispersi dalam cairan yang lain, dalam bentuk tetesan kecil. Stabilitas emulsi dapat dipertahankan dengan penambahan zat yang ketiga yang disebut dengan emulgator (emulsifying agent)
Emulsi berasal dari kata emulgeo yang artinya menyerupai milk, warna emulsi adalah putih. Pada abad XVII hanya dikenal emulsi dari biji-bijian yang mengandung lemak, protein dan air. Emulsi semacam ini disebut emulsi vera atau emulsi alam, sebagai emulgator dipakai protein yang terdapat dalam biji tersebut.
Pada pertengahan abad ke XVIII, ahli farmasi Perancis memperkenalkan pembuatan emulsi dari oleum olivarum, oleum anisi dan eugenol oil dengan menggunakan penambahan gom arab, tragacanth, kuning telur. Emulsi yang terbentuk karena penambahan emulgator dari luar disebut emulsi spuria atau emulsi buatan.
B. Komponen Emulsi
Komponen dari emulsi dapat digolongkan menjadi 2 macam yaitu : 1. Komponen dasar
Adalah bahan pembentuk emulsi yang harus terdapat didalam emulsi. Terdiri atas :
Fase dispers / fase internal / fase diskontinue
Yaitu zat cair yang terbagi- bagi menjadi butiran kecil ke dalam zat cair lain.
Fase kontinue / fase external / fase luar
Yaitu zat cair dalam emulsi yang berfungsi sebagai bahan dasar (pendukung) dari emulsi tersebut.
Emulgator.
Adalah bagian dari emulsi yang berfungsi untuk menstabilkan emulsi.
2. Komponen tambahan
Bahan tambahan yang sering ditambahkan pada emulsi untuk memperoleh hasil yang lebih baik. Misalnya corrigen saporis, odoris, colouris, preservative (pengawet), anti oksidan.
Preservative yang digunakan antara lain metil dan propil paraben, asam benzoat, asam sorbat, fenol, kresol dan klorbutanol, benzalkonium klorida, fenil merkuri asetas dan lain – lain.
Antioksidan yang digunakan antara lain asam askorbat, L.tocopherol, asam sitrat, propil gallat , asam gallat.
C. Tipe Emulsi
Berdasarkan macam zat cair yang berfungsi sebagai fase internal ataupun external, maka emulsi digolongkan menjadi dua macam yaitu :
1. Emulsi tipe O/W ( oil in water) atau M/A ( minyak dalam air). Adalah emulsi yang terdiri dari butiran minyak yang tersebar kedalam air. Minyak sebagai fase internal dan air sebagai fase external.
2. Emulsi tipe W/O ( water in oil ) atau A/M ( air dalam minyak) Adalah emulsi yang terdiri dari butiran air yang tersebar kedalam minyak. Air sebagai fase internal dan minyak sebagai fase external.
D. Tujuan pemakaian emulsi
Emulsi dibuat untuk diperoleh suatu preparat yang stabil dan rata dari campuran dua cairan yang saling tidak bisa bercampur. Tujuan pemakaian emulsi adalah :
1. Dipergunakan sebagai obat dalam / per oral. Umumnya emulsi tipe o/w
2. Dipergunakan sebagai obat luar.
Bisa tipe o/w maupun w/o tergantung banyak faktor misalnya sifat zatnya atau jenis efek terapi yang dikehendaki.
E. Teori Terjadinya Emulsi
Untuk mengetahui proses terbentuknya emulsi dikenal 4 macam teori , yang melihat proses terjadinya emulsi dari sudut pandang yang berbeda-beda. Teori tersebut ialah :
1. Teori Tegangan Permukaan (Surface Tension)
Molekul memiliki daya tarik menarik antara molekul yang sejenis yang disebut daya kohesi. Selain itu molekul juga memiliki daya tarik menarik antara molekul yang tidak sejenis yang disebut daya adhesi.
Daya kohesi suatu zat selalu sama, sehingga pada permukaan suatu zat cair akan terjadi perbedaan tegangan karena tidak adanya keseim -bangan daya kohesi. Tegangan yang terjadi pada permukaan tersebut dinamakan tegangan permukaan (surface tension).
Dengan cara yang sama dapat dijelaskan terjadinya perbedaan tegangan bidang batas dua cairan yang tidak dapat bercampur (immicible liquid). Tegangan yang terjadi antara dua cairan tersebut dinamakan tegangan bidang batas (interfacial tension).
Semakin tinggi perbedaan tegangan yang terjadi pada bidang mengakibatkan antara kedua zat cair itu semakin susah untuk bercampur. Tegangan yang terjadi pada air akan bertambah dengan penambahan garam-garam anorganik atau senyawa elektrolit, tetapi akan berkurang dengan penambahan senyawa organik tertentu antara lain sabun (sapo).
Dalam teori ini dikatakan bahwa penambahan emulgator akan menurunkan menghilangkan tegangan yang terjadi pada bidang batas sehingga antara kedua zat cair tersebut akan mudah bercampur.
2. Teori Orientasi Bentuk Baji (Oriented Wedge)
Setiap molekul emulgator dibagi menjadi dua kelompok yakni :
Kelompok hidrofilik, yaitu bagian dari emulgator yang suka pada air.
Kelompok lipofilik , yaitu bagian yang suka pada minyak. Masing-masing kelompok akan bergabung dengan zat cair yang disenanginya, kelompok hidrofil kedalam air dan kelompok lipofil kedalam minyak. Dengan demikian emulgator seolah-olah
menjadi tali pengikat antara air dan minyak. Antara kedua
kelompok tersebut akan membuat suatu keseimbangan.
Setiap jenis emulgator memiliki harga keseimbangan yang besarnya tidak sama.Harga keseimbangan itu dikenal dengan istilah H.L.B. (Hydrophyl Lipophyl Balance) yaitu angka yang menunjukkan perbandingan antara kelompok lipofil dengan kelompok hidrofil .
Semakin besar harga HLB berarti semakin banyak kelompok yang suka pada air, itu artinya emulgator tersebut lebih mudah larut dalam air dan demikian sebaliknya.
Dalam tabel dibawah ini dapat dilihat keguaan suatu emulgator ditinjau dari harga HLB-nya.
HARGA HLB K E G U N A A N
1 - 3 Anti foaming agent 4 – 6 Emulgator tipe w/o
7 – 9 Bahan pembasah ( wetting agent) 8 – 18 Emulgator tipe o/w
13 - 15 Detergent
10 – 18 Kelarutan (solubilizing agent)
Untuk menentukan komposisi campuran emulgator sesuai dengan nilai HLB yang dikehendaki , dapat dilakukan dengan contoh perhitungan seperti tersebut dibawah ini.
Contoh :
Pada pembuatan 100 ml emulsi tipe o/w diperlukan emulgator dengan harga HLB 12. Sebagai emulgator dipakai campuran Span 20 (HLB 8,6) dan tween 20 (HLB 16,7) sebanyak 5 gram. Berapa gram masing-masing berat Span 20 dan Tween 20 ?
Jawab : Rumus I A % b = HLBb HLBa HLBb x ) ( x 100 % B % a = ( 100% - A%) Keterangan :
x = Harga HLB yang diminta ( HLB Butuh) A = Harga HLB tinggi B = Harga HLB rendah % Tween = 6 , 8 7 , 16 ( ) 6 , 8 12 ( X 100% = 42% 100 42 X 5 gram = 2,1 gram % Span = 100 % - 42 % = 58 % 100 58 X 5 gram = 2,9 gram
Rumus II.
(B1 x HLB1) + (B2 x HLB2) = (B campuran x HLB campuran)
B = Berat emulgator Misalnya berat tween = X Berat span = 5 – X (X x 16,7) + (5-X) x 8,6 = 5 x 12 16,7 X + 43 – 8,6 X = 60 8,1X = 60 – 43 X = 1 , 8 17 = 2,1 gram ( tween) Berat span = 5 – 2,1 = 2,9 gram
Cara menghitung nilai HLB dari campuran surfaktan Contoh : R/ Tween 80 70% HLB = 15 Span 80 30% HLB = 4,5 Perhitungan : Cara I Tween 80 = 100 70 x 15 = 10,5 Span 80 = 100 30 x 4,5 = 01,35 HLB Campuran 11,85
Cara II. (Cara Aligatie) Tween 80 15 (X – 4,5) (X – 4,5) : (15 – X) = 70 : 30 = 7 : 3 (X – 4,5) 3 = 7 (15 – X) 3X – 13,5 = 105 – 7X 10X = 118,5 X = 11,85 X Span 80 4,5 (15 – X) Jadi HLB Campuran = 11,85
Nilai HLB beberapa surfaktan
Zat HLB Zat HLB Tween 20 Tween 40 Tween 80 Tween 60 Tween 85 Tween 65 16,7 15,6 15,0 14,9 11,0 10,5 Span 20 Span 60 Span 80 Arlacel 83 Gom Trietanolamin 8,6 4,7 4,3 3,7 8,0 12,0
Nilai HLB Butuh beberapa zat yang sering dipakai. Nama Zat HLB butuh
(type a/m) HLB butuh (type m/a) Asam stearat Setil alcohol Paraffin Vaselin Cera alba 6 5 5 4 15 15 12 12 12
3. Teori Interparsial Film
Teori ini mengatakan bahwa emulgator akan diserap pada batas antara air dan minyak, sehingga terbentuk lapisan film yang akan membungkus partikel fase disper.
Dengan terbungkusnya partikel tersebut maka usaha antara partikel yang sejenis untuk bergabung menjadi terhalang. Dengan kata lain fase disper menjadi stabil.
Untuk memberikan stabilitas maksimum pada emulsi, syarat emulgator yang dipakai adalah :
dapat membentuk lapisan film yang kuat tapi lunak
jumlahnya cukup untuk menutup semua permukaan partikel fase- dispers
dapat membentuk lapisan film dengan cepat dan dapat menutup semua permukaan partikel dengan segera.
4. Teori electric double layer ( lapisan listrik rangkap)
Jika minyak terdispersi ke dalam air, satu lapis air yang langsung berhubungan dengan permukaan minyak akan bermuatan sejenis, sedangkan lapisan berikutnya akan mempunyai muatan yang berlawanan dengan lapisan didepannya. Dengan demikian seolah-olah tiap partikel minyak dilindungi oleh 2 benteng lapisan
listrik yang saling berlawanan. Benteng tersebut akan menolak
setiap usaha dari partikel minyak yang akan mengadakan penggabungan menjadi satu molekul yang besar, karena susunan listrik yang menyelubungi setiap partikel minyak mempunyai susunan yang sama. Dengan demikian antara sesama partikel akan tolak-menolak , dan stabilitas emulsi akan bertambah.
Terjadinya muatan listrik disebabkan oleh salah satu dari ke tiga cara dibawah ini,
terjadinya ionisasi dari molekul pada permukaan partikel
terjadinya absorbsi ion oleh partikel dari cairan disekitarnya.
terjadinya gesekan partikel dengan cairan disekitarnya.
F. Bahan Pengemulsi (Emulgator)
Emulgator alam
Yaitu emulgator yang diperoleh dari alam tanpa proses yang rumit. Dapat digolongkan menjadi tiga golongan yaitu :
1. Emulgator alam dari tumbuh-tumbuhan.
Pada umumnya termasuk karbohydrat dan merupakan emulgator tipe o/w, sangat peka terhadap elektrolit dan alkohol kadar tinggi, juga dapat dirusak bakteri. Oleh sebab itu pada pembuatan emulsi dengan emulgator ini harus selalu ditambah bahan pengawet.
a. Gom Arab
Sangat baik untuk emulgator tipe o/w dan untuk obat minum. Emulsi yang terbentuk sangat stabil dan tidak terlalu kental. Kestabilan emulsi yang dibuat dengan gom arab berdasarkan 2 faktor yaitu
kerja gom sebagai koloid pelindung (teori plastis film)
terbentuknya cairan yang cukup kental sehingga laju pengendapan cukup kecil sedangkan masa mudah dituang (tiksotropi)
Bila tidak dikatakan lain maka emulsi dengan gom arab menggunakan gom arab sebanyak ½ dari jumlah minyaknya.
Untuk membuat corpus emulsi diperlukan air 1,5 X berat gom, diaduk keras dan cepat sampai putih , lalu diencerkan dengan air sisanya. Selain itu dapat disebutkan :
Lemak-lemak padat : PGA sama banyak dengan lemak padat
Cara pembuatan .
Lemak padat dilebur lalu ditambahkan gom, buat corpus emulsi dengan air panas 1,5 X berat gom . Dinginkan
dan encerkan emulsi dengan air dingin. Contoh : cera, oleum cacao, parafin solid
Minyak atsiri : PGA sama banyak dengan minyak atsiri
Minyak lemak : PGA ½ kali berat minyak, kecuali oleum ricini karena memiliki gugus OH yang bersifat hidrofil sehingga untuk membuat emulsi cukup dibutuhkan 1/3 nya saja. Contoh : Oeum amygdalarum
Minyak Lemak + minyak atsiri + zat padat larut dalam minyak lemak
Kedua minyak dicampur dulu, zat padat dilarutkan dalam minyaknya, tambahkan gom ( ½ x myk lemak + aa x myk atsiri + aa x zat padat )
Bahan obat cair BJ tinggi, contohnya chloroform, bromoform :
Ditambah minyak lemak 10 x beratnya, maka BJ campuran mendekati satu. Gom sebanyak ¾ kali bahan obat cair.
Balsam-balsam
Gom sama banyak dengan balsam.
Oleum Iecoris Aseli
Menurut Fornas dipakai gom 30 % dari berat minyak. b. Tragacanth
Dispersi tragacanth dalam air sangat kental sehingga untuk memperoleh emulsi dengan viskositas yang baik hanya diperlukan trgacanth sebanyak 1/10 kali gom arab. Emulgator ini hanya bekerja optimum pada pH 4,5 – 6. Tragacanth dibuat corpus emulsi dengan menambahkan sekaligus air 20 x berat tragacanth. Tragacanth hanya
berfungsi sebagai pengental tidak dapat membentuk koloid pelindung.
c. Agar-agar
Emulgator ini kurang efektif apabila dipakai sendirian. Pada umumnya zat ini ditambahkan untuk menambah viskositas dari emulsi dengan gom arab.
Sebelum dipakai agar-agar tersebut dilarutkan dengan air mendidih Kemudian didinginkan pelan-pelan sampai suhu tidak kurang dari 45oC (bila suhunya kurang dari 45oC
larutan agar-agar akan berbentuk gel). Biasanya digunakan 1-2 %
d. Chondrus
Sangat baik dipakai untuk emulsi minyak ikan karena dapat menutup rasa dari minyak tersebut. Cara mempersiapkan dilakukan seperti pada agar.
e. Emulgator lain
Pektin, metil selulosa, karboksimetil selulosa 1-2 %. 2. Emulgator alam dari hewan
a. Kuning telur
Kuning telur mengandung lecitin (golongan protein / asam amino) dan kolesterol yang kesemuanya dapat berfungsi sebagai emulgator. Lecitin merupakan emulgator tipe o/w. Tetapi kemampuan lecitin lebih besar dari kolesterol sehingga secara total kuning telur merupakan emulgator tipe o/w. Zat ini mampu mengemulsikan minyak lemak empat kali beratnya dan minyak menguap dua kali beratnya. b. Adeps Lanae
Zat ini banyak mengandung kholesterol , merupakan emulgator tipe w/o dan banyak dipergunakan untuk pemakaian luar. Penambahan emulgator ini akan menambah
kemampuan minyak untuk menyerap air. Dalam keadaan kering dapat menyerap air 2 X beratnya.
Contoh resep emulsi dengan adeps lanae : R/ Adeps lanae 100 Ol. Olivarum 400 ml Zinc. Oxyd 100 Talc. 100 Sol. Pb. Acet. 28 ml Aq. Calcis ad 1000 ml
3. Emulgator alam dari tanah mineral.
a. Magnesium Aluminium Silikat/ Veegum
Merupakan senyawa anorganik yang terdiri dari garam - garam magnesium dan aluminium. Dengan emulgator ini, emulsi yang terbentuk adalah emulsi tipe o/w. Sedangkan pemakaian yang lazim adalah sebanyak 1 %. Emulsi ini khusus untuk pemakaian luar.
b. Bentonit
Tanah liat yang terdiri dari senyawa aluminium silikat yang dapat mengabsorbsikan sejumlah besar air sehingga membentuk massa sepert gel. Untuk tujuan sebagai emulgator dipakai sebanyak 5 %.
Emulgator buatan 1. Sabun.
Sangat banyak dipakai untuk tujuan luar, sangat peka terhadap elektrolit. Dapat dipergunakan sebagai emulgator tipe o/w maupun w/o, tergantung dari valensinya. Bila sabun tersebut bervalensi 1, misalnya sabun kalium, merupakan emulgator
tipe o/w, sedangkan sabun dengan valensi 2 , missal sabun kalsium, merupakan emulgator tipe w/o.
2. Tween 20 : 40 : 60 : 80 3. Span 20 : 40 : 80
Emulgator dapat dikelompokkan menjadi :
Anionik : sabun alkali, natrium lauryl sulfat
Kationik : senyawa ammmonium kuartener
Non Ionik : tween dan span.
Amfoter : protein, lesitin.
G. Cara Pembuatan Emulsi
Dikenal 3 metode dalam pembuatan emulsi , secara singkat dapat dijelaskan :
1. Metode gom kering atau metode kontinental.
Dalam metode ini zat pengemulsi (biasanya gom arab) dicampur dengan minyak terlebih dahulu, kemudian ditambahkan air untuk pembentukan corpus emulsi, baru diencerkan dengan sisa air yang tersedia.
2. Metode gom basah atau metode Inggris.
Zat pengemulsi ditambahkan ke dalam air (zat pengemulsi umumnya larut) agar membentuk suatu mucilago, kemudian perlahan-lahan minyak dicampurkan untuk mem-bentuk emulsi, setelah itu baru diencerkan dengan sisa air.
3. Metode botol atau metode botol forbes.
Digunakan untuk minyak menguap dan zat –zat yang bersifat minyak dan mempunyai viskositas rendah (kurang kental). Serbuk gom dimasukkan ke dalam botol kering, kemudian ditambahkan 2 bagian air, tutup botol kemudian campuran
tersebut dikocok dengan kuat. Tambahkan sisa air sedikit demi sedikit sambil dikocok.
Alat – alat yang digunakan dalam pembuatan emulsi Untuk membuat emulsi biasa digunakan :
1. Mortir dan stamper
Mortir dengan permukaan kasar merupakan mortir pilihan untuk pembuatan emulsi yang baik.
2. Botol
Mengocok emulsi dalam botol secara terputus-putus lebih baik daripada terus menerus, hal tersebut memberi kesempatan pada emulgator untuk bekerja sebelum pengocokan berikutnya. 3. Mixer, blender
Partikel fase disper dihaluskan dengan cara dimasukkan kedalam ruangan yang didalamnya terdapat pisau berputar dengan kecepatan tinggi , akibat putaran pisau tersebut, partikel akan berbentuk kecil-kecil.
4. Homogeniser
Dalam homogenizer dispersi dari kedua cairan terjadi karena campuran dipaksa melalui saluran lubang kecil dengan tekanan besar.
5. Colloid Mill
Terdiri atas rotor dan stator dengan permukaan penggilingan yang dapat diatur. Coloid mill digunakan untuk memperoleh derajat dispersi yang tinggi cairan dalam cairan
H. Cara Membedakan Tipe Emulsi
Dikenal beberapa cara membedakan tipe emulsi yaitu : 1. Dengan pengenceran fase.
Setiap emulsi dapat diencerkan dengan fase externalnya. Dengan prinsip tersebut, emulsi tipe o/w dapat diencerkan dengan air sedangkan emulsi tipe w/o dapat diencerkan dengan minyak.
2. Dengan pengecatan/pemberian warna.
Zat warna akan tersebar rata dalam emulsi apabila zat tersebut larut dalam fase external dari emulsi tersebut. Misalnya (dilihat dibawah mikroskop)
- Emulsi + larutan Sudan III dapat memberi warna merah pada emulsi tipe w/o, karena sudan III larut dalam minyak - Emulsi + larutan metilen blue dapat memberi warna biru
pada emulsi tipe o/w karena metilen blue larut dalam air. 3. Dengan kertas saring.
Bila emulsi diteteskan pada kertas saring , kertas saring menjadi basah maka tipe emulsi o/w, dan bila timbul noda minyak pada kertas berarti emulsi tipe w/o.
4. Dengan konduktivitas listrik
Alat yang dipakai adalah kawat dan stop kontak, kawat dengan K ½ watt lampu neon ¼ watt semua dihubung- kan secara seri. Lampu neon akan menyala bila elektroda dicelupkan dalam cairan emulsi tipe o/w, dan akan mati dicelupkan pada emulsi tipe w/o
I. KESTABILAN EMULSI.
Emulsi dikatakan tidak stabil bila mengalami hal-hal seperti dibawah ini :
1. Creaming yaitu terpisahnya emulsi menjadi 2 lapisan, dimana yang satu mengandung fase dispers lebih banyak daripada lapisan yang lain. Creaming bersifat reversible artinya bila digojok perlahan-lahan akan terdispersi kembali.
2. Koalesen dan cracking (breaking) adalah pecahnya emulsi karena film yang meliputi partikel rusak dan butir minyak akan koalesen(menyatu).Sifatnya irreversible ( tidak bisa diperbaiki). Hal ini dapat terjadi karena :
Peristiwa kimia, seperti penambahan alkohol, perubahan pH, penambahan CaO/CaCl2 exicatus.
Peristiwa fisika, seperti pemanasan, penyaringan, pendinginan, pengadukan.
3. Inversi adalah peristiwa berubahnya sekonyong-konyong tipe emulsi w/o menjadi o/w atau sebaliknya. Sifatnya irreversible.