SINTESIS DAN KARAKTERISASI TiO2 TERDADAH NITROGEN MELALUI METODE HIDROTERMAL DENGAN VARIASI
SUHU DAN KALSINASI
SKRIPSI
Diajukan Kepada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta Untuk Mememenuhi
Sebagian Persyaratan Guna Memperoleh Sarjana Sains Bidang Kimia
Oleh:
Purdiana Susilowati
12307141038
PROGRAM STUDI KIMIA
JURUSAN PENDIDIKAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
PERSEMBAHAN
Karya ini kupersembahkan untuk…
Bapak Tugiyo dan Ibu Murharyani
yang selama ini telah mencurahkan segala usaha, doa dan kasih sayangnya untukku
Kakak-kakakku dan adikku
terimakasih atas segala dukungan kalian
Sahabat-sahabatku Fitri, Vina, Asri, Ratna, Elsa
terimakasih untuk waktu kalian selama ini
Teman-teman Kimia Subsidi 2012
KATA PENGANTAR
Puji syukur saya panjatkan kehadirat Allah SWT atas limpahan rahmat, karunia, taufiq dan hidayah-Nya sehingga penulis dapat menyeleaikan skripsi yang berjudul “Sintesis dan Karakterisasi TiO2 Terdadah Nitrogen Melalui Metode Hidrotermal dengan Variasi Suhu dan Kalsinasi”. Penulis menyadari bahwa dalam menyelesaikan penelitian dan penyusunan laporan penelitian ini telah mendapat bimbingan, bantuan, arahan dan kerjasama dari berbagai pihak. Oleh karena itu, pada kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak Dr. Hartono, selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta.
2. Bapak Jaslin Ikhsan, Ph.D selaku Ketua Jurusan Pendidikan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta. 3. Bapak Prof. A.K. Prodjosantoso, Ph.D selaku dosen pembimbing utama yang
telah memberikan bimbingan, pengarahan, saran, dan masukan dalam menyelesaikan skripsi ini.
4. Ibu Dr. Cahyorini Kusumawardani, M.Si selaku pembimbing pendamping yang telah memberikan bimbingan, arahan, motivasi serta masukan dalam penyelesaian skripsi ini.
5. Bapak Dr. Hari Sutrisno dan Bapak M. Pranjoto Utomo, M.Si selaku dosen penguji yang telah memberikan saran dan masukan guna memperbaiki penulisan skripsi ini.
6. Kedua orang tuaku yang selalu memberikan dukungan dan motivasi dalam penulisan skripsi ini.
7. Sahabat-sahabatku Vina, Asri, Fitri, Ratna, Elsa yang selalu membantu dalam penyelesaian penulisan skripsi ini.
8. Teman-teman satu kelompok penelitian Hary, Saiful, Muhaimin, Eti, Fia, Yuza yang membantu dalam pelaksanaan penelitian ini.
10. Semua pihak yang telah membantu dan memberikan dukungan secara moral maupun material dalam penyelesaian tugas akhir skripsi ini yang tidak dapat penulis sebut satu per satu.
Penulis menyadari bahwa penulisan ini masih jauh dari kesempurnaan, oleh karena itu penulis mengharapkan kritik dan saran dari berbagai pihak yang bersifat membangun untuk kesempurnaan laporan ini. Semoga laporan ini dapat bermanfaat bagi kita semua. Amin.
Yogyakarta, 29 September 2016
DAFTAR ISI
JUDUL ... i
PERSETUJUAN ... ii
PERNYATAAN ... iii
PENGESAHAN ... iv
PERSEMBAHAN ... v
KATA PENGANTAR ... vi
DAFTAR ISI ... viii
DAFTAR TABEL ... x
DAFTAR GAMBAR ... xi
DAFTAR LAMPIRAN ... xii
ABSTRAK ... xii
ABSTRACT ... xiv
BAB I PENDAHULUAN A. Latar Belakang Masalah ... 1
B. Identifikasi Masalah ... 3
C. Pembatasan Masalah ... 3
D. Perumusan Masalah... 4
E. Tujuan Penelitian ... 4
F. Manfaat Penelitian ... 5
BAB II KAJIAN PUSTAKA A. Deskripsi Teori ... 6
1. Semikonduktor TiO2 ... 6
2. TiO2 Terdadah Nitrogen (N-TiO2) ... 8
3. Sintesis N-TiO2 dengan Metode Hidrotermal ... 10
4. Metode X-Ray Diffraction (XRD) ... 12
5. Metode FTIR ... 13
6. Metode UV-Vis ... 14
7. Isoterm Adsorpsi-Desorpsi N2 ... 15
B. Penelitian yang Relevan ... 17
BAB III METODE PENELITIAN
A. Alat dan Bahan Penelitian ... 20
1. Alat-alat Penelitian ... 20
2. Bahan-bahan`Penelitian ... 20
B. Subjek dan Objek Penelitian ... 20
1. Subjek Penelitian ... 20
2. Objek Penenlitian ... 20
C. Waktu dan Tempat Penelitian ... 21
D. Prosedur Penelitian ... 21
1. Sintesis nanopartikel N-TiO2 dengan Metode Hidrotermal ... 21
2. Karakterisasi dan Analisis ... 22
3. Bagan Penelitian ... 25
BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Sintesis N-TiO2 dengan Metode Hidrotermal ... 26
B. Karakterisasi N-TiO2 Hasil Sintesis dengan Metode Hidrotermal ... 27
1. Karakterisasi Menggunakan X-Ray Diffraction (XRD) ... 27
2. Karakterisasi Menggunakan FTIR ... 33
3. Kakaterisasi N-TiO2 dengan UV-Vis ... 34
4. Isoterm Adsorpsi-Desorpsi ... 35
BAB V KESIMPULAN DAN SARAN A. Kesimpulan ... 38
B. Saran ... 39
DAFTAR PUSTAKA ... 40
LAMPIRAN ... 44
DAFTAR TABEL
Tabel 1 Data Hasil XRD Sampel N-TiO2 Setelah Dikalsinasi ... 29
Tabel 2 Hasil Perbandingan Fraksi Rutile dan Anatase ... 31
Tabel 3 Ukuran Kristalit N-TiO2 Setelah Dikalsinasi ... 31
Tabel 3 Hasil U-Fit Parameter Kisi Sampel Setelah Dikalsinasi ... 32
DAFTAR GAMBAR
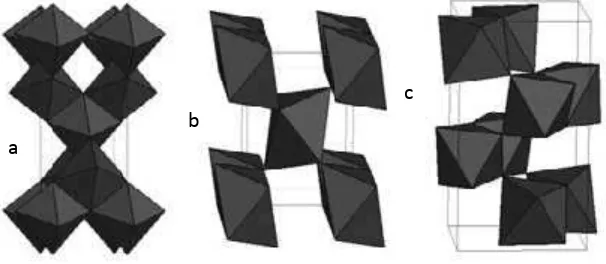
Gambar 1 Struktur Kristal Anatase, Rutile dan Broockite ... 7
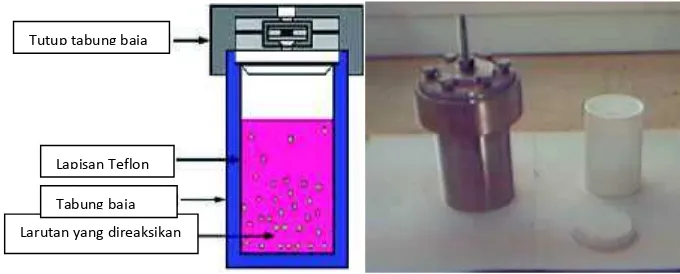
Gambar 2 Bagian Autoclave, Baja dan Tabung Teflon ... 11
Gambar 3 Ilustrasi Hukum Bragg ... 13
Gambar 4 Klasifikasi Isoterm Adsorpsi Desorpsi ... 16
Gambar 5 Klasifikasi Alur Histeresis ... 17
Gambar 6 Skema Kerja Penelitian ... 25
Gambar 7 Difraktogram XRD Senyawa N-TiO2 pada Temperatur Hidrotermal 110°C, 120°C dan 150°C Sebelum Dikalsinasi ... 28
Gambar 8 Difraktogram XRD Senyawa N-TiO2 yang Disintesis pada Temperatur Hidrotermal 110°C, 120°C dan 150°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam... 30
Gambar 9 Spektra FTIR Sampel N-TiO2 yang Disintesis pada Temperatur 110°C Sebelum Kalsinasi dan Sesudah Kalsinasi Selama 3 Jam pada Temperatur 450°C ... 33
Gambar 10 Spektra UV Senyawa N-TiO2 dengan Variasi Temperatur Hidrotermal Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam ... 34
Gambar 11 Grafik Energi Celah Pita Senyawa N-TiO2 pada Suhu Hidrotermal 110°C, 120°C, 150°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam ... 35
Gambar 12 Isoterm Adsorpsi Desorpsi Senyawa N-TiO2 Temperatur Hidrotermal 110°C dan 120°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam ... 36
DAFTAR LAMPIRAN
Lampiran 1 Difraktogram XRD ... 44
Lampiran 2 Hasil Perhitungan Ukuran Partikel N-TiO2 ... 50
Lampiran 3 Perhitungan Rasio Fasa Rutile:Anatase ... 55
Lampiran 4 Perhitungan Parameter Kisi dengan U-Fit ... 56
Lampiran 5 Spektra FTIR N-TiO2 yang Disintesis pada Suhu 110°C ... 61
Lampiran 6 Spektra Absorbansi dan Reflektansi ... 64
Lampiran 7 Grafik Perhitungan Energi Celah Pita ... 70
Lampiran 8 Proses Sintesis dan Hasil Sintesis ... 72
SINTESIS DAN KARAKTERISASI TiO2 TERDADAH NITROGEN MELALUI METODE HIDROTERMAL DENGAN
VARIASI SUHU DAN KALSINASI
Oleh:
Purdiana Susilowati 12307141038
Pembimbing:
Prof. A.K. Prodjosantoso, Ph.D Dr. Cahyorini Kusumawardani, M.Si
ABSTRAK
Penelitian ini bertujuan untuk mensintesis nanopartikel N-TiO2 melalui metode hidrotermal dengan variasi temperatur untuk mengetahui pengaruh temperatur hidrotermal diikuti dengan kalsinasi terhadap struktur, ukuran partikel, karakter elektronik dan porositas N-TiO2.
Nanopartikel N-TiO2 disintesis dengan cara mencampurkan akuades dengan HCl 36% dan diaduk selam 10 menit, kemudian ke dalam larutan tersebut ditambahkan larutan dodesilamin sambil dilakukan pengadukan selama 30 menit hingga diperoleh larutan homogen. Setelah itu, ke dalam larutan tersebut ditambahkan sedikit demi sedikit larutan TiCl4 sambil dilakukan pengadukan selama 30 menit. Larutan tersebut kemudian dimasukkan ke dalam tablung teflondan dioven selama 12 jam pada temperatur 110°C, 120°C dan 150°C. Hasil dari pengovenan tersebut kemudian digerus dan dikalsinasi selama 3 jam pada temperatur 450°C. Karakterisasi sampel dilakukan menggunakan X-Ray
Diffraction (XRD), FTIR, UV-Vis dan analisa isoterm adsorpsi-desorpsi
menggunakan alat Quantachrome NovaWin2
Hasil penelitian ini menunjukkan bahwa kenaikan temperatur hidrotermal yang diikuti dengan kalsinasi pada temperatur 450°C mempengaruhi ukuran partikel N-TiO2 antara lain adanya peningkatan ukuran partikel pada fase rutile dan adanya penurunan ukuran partikel pada fase anatase. Selain itu, kenaikan temperatur hidrotermal juga menyebabkan perubahan rasio fase anatase dan
rutile. Rasio fase rutile mengalami penurunan pada sintesis dengan temperatur
SYNTHESIS AND CHARACTERIZATION OF NITROGEN-DOPED TiO2 THROUGH HYDROTHERMAL METHOD WITH TEMPERATURE
VARIATION AND CALCINATION
By:
Purdiana Susilowati 12307141038
Advisor:
Prof. A.K. Prodjosantoso, Ph.D Dr. Cahyorini Kusumawardani, M.Si
ABSTRACT
This research aims to synthesize N-TiO2 nanoparticles through hydrothermal method with temperature variations and calcination to determine the influence of hydrothermal temperature on the structure, size of particles, electronic character and porosity N-TiO2.
N-TiO2 nanoparticlessynthesized by mixing distilled water with HCl 36% and stirred 10 minutes, then dodesylamine is added to the solution while stirring for 30 minutes to obtain a homogeneous solution. Thereafter, to the solution was added TiCl4 while stirring for 30 minutes. The solution is then inserted into teflon tube and oven for 12 hours at 110°C, 120°C and 150°C. Results of the oven was then crushed and calcined for 3 hours at a temperature of 450°C. Characterization of the samples was performed using X-Ray Diffraction (XRD), FTIR, UV-Vis and analysis of isotherm adsorption-desorption using a Quantachrome NovaWin2.
The results of this study indicate that the rise in temperature hydrothermal followed by calcination at a temperature of 450°C affect the particle size of the N-TiO2, among others, the increase in the size of particles in rutile phase and a decrease in particle size on the anatase phase. In addition, the increase in temperature hydrothermal also cause changes in the ratio of anatase and rutile phase. Ratio of rutile phase decreased in the hydrothermal synthesis temperature of 120°C but an increase in the hydrothermal synthesis temperature of 150°C, while the ratio of anatase phase decreases with increasing temperature hydrothermal. Rising hydrothermal temperatures also cause lattice parameter tends to rise, the energy band gap tends to decrease, becoming more uniform pore size, and specific surface area increases.
PERSEMBAHAN
Karya ini kupersembahkan untuk
Bapak Tugiyo dan Ibu Murharyani
yang selama ini telah mencurahkan segala usaha, doa dan kasih sayangnya untukku
Kakak-kakakku dan adikku terimakasih atas segala dukungan kalian
Sahabat-sahabatku Fitri, Vina, Asri, Ratna, Elsa terimakasih untuk waktu kalian selama ini
Teman-teman Kimia Subsidi 2012
KATA PENGANTAR
Puji syukur saya panjatkan kehadirat Allah SWT atas limpahan rahmat,
karunia, taufiq dan hidayah-Nya sehingga penulis dapat menyeleaikan skripsi yang
berjudul “Sintesis dan Karakterisasi TiO2 Terdadah Nitrogen Melalui Metode
Hidrotermal dengan Variasi Suhu dan Kalsinasi”.Penulis menyadari bahwa dalam
menyelesaikan penelitian dan penyusunan laporan penelitian ini telah mendapat
bimbingan, bantuan, arahan dan kerjasama dari berbagai pihak. Oleh karena itu,
pada kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak Dr. Hartono, selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan
Alam Universitas Negeri Yogyakarta.
2. Bapak Jaslin Ikhsan, Ph.D selaku Ketua Jurusan Pendidikan Kimia Fakultas
Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta.
3. Bapak Prof. A.K. Prodjosantoso, Ph.D selaku dosen pembimbing utama yang
telah memberikan bimbingan, pengarahan, saran, dan masukan dalam
menyelesaikan skripsi ini.
4. Ibu Dr. Cahyorini Kusumawardani, M.Si selaku pembimbing pendamping yang
telah memberikan bimbingan, arahan, motivasi serta masukan dalam
penyelesaian skripsi ini.
5. Bapak Dr. Hari Sutrisno dan Bapak M. Pranjoto Utomo, M.Si selaku dosen
penguji yang telah memberikan saran dan masukan guna memperbaiki
penulisan skripsi ini.
6. Kedua orang tuaku yang selalu memberikan dukungan dan motivasi dalam
penulisan skripsi ini.
7. Sahabat-sahabatku Vina, Asri, Fitri, Ratna, Elsa yang selalu membantu dalam
penyelesaian penulisan skripsi ini.
8. Teman-teman satu kelompok penelitian Hary, Saiful, Muhaimin, Eti, Fia, Yuza
yang membantu dalam pelaksanaan penelitian ini.
10. Semua pihak yang telah membantu dan memberikan dukungan secara moral
maupun material dalam penyelesaian tugas akhir skripsi ini yang tidak dapat
penulis sebut satu per satu.
Penulis menyadari bahwa penulisan ini masih jauh dari kesempurnaan, oleh
karena itu penulis mengharapkan kritik dan saran dari berbagai pihak yang bersifat
membangun untuk kesempurnaan laporan ini. Semoga laporan ini dapat bermanfaat
bagi kita semua. Amin.
Yogyakarta, 29 September 2016
DAFTAR ISI A. Latar Belakang Masalah...1
B. Identifikasi Masalah ...3
C. Pembatasan Masalah ...3
D. Perumusan Masalah ...4
E. Tujuan Penelitian...4
F. Manfaat Penelitian ...5
BAB II KAJIAN PUSTAKA A. Deskripsi Teori...6
1. Semikonduktor TiO2...6
2. TiO2Terdadah Nitrogen (N-TiO2) ...8
3. Sintesis N-TiO2dengan Metode Hidrotermal ...10
4. Metode X-Ray Diffraction (XRD) ...12
5. Metode FTIR ...13
6. Metode UV-Vis ...14
7. Isoterm Adsorpsi-Desorpsi N2...15
B. Penelitian yang Relevan ...17
BAB III METODE PENELITIAN
A. Alat dan Bahan Penelitian...20
1. Alat-alat Penelitian ...20
2. Bahan-bahan`Penelitian...20
B. Subjek dan Objek Penelitian ...20
1. Subjek Penelitian ...20
2. Objek Penenlitian ...20
C. Waktu dan Tempat Penelitian ...21
D. Prosedur Penelitian ...21
1. Sintesis nanopartikel N-TiO2dengan Metode Hidrotermal...21
2. Karakterisasi dan Analisis ...22
3. Bagan Penelitian ...25
BAB IV HASIL PENELITIAN DAN PEMBAHASAN A. Sintesis N-TiO2dengan Metode Hidrotermal ...26
B. Karakterisasi N-TiO2Hasil Sintesis dengan Metode Hidrotermal...27
1. Karakterisasi Menggunakan X-Ray Diffraction (XRD) ...27
2. Karakterisasi Menggunakan FTIR ...33
3. Kakaterisasi N-TiO2dengan UV-Vis ...34
4. Isoterm Adsorpsi-Desorpsi ...35
BAB V KESIMPULAN DAN SARAN A. Kesimpulan ...38
B. Saran ...39
DAFTAR PUSTAKA ...40
DAFTAR TABEL
Tabel 1 Data Hasil XRD Sampel N-TiO2Setelah Dikalsinasi ...29
Tabel 2 Hasil Perbandingan Fraksi Rutile dan Anatase...31
Tabel 3 Ukuran Kristalit N-TiO2Setelah Dikalsinasi ...31
Tabel 3 Hasil U-Fit Parameter Kisi Sampel Setelah Dikalsinasi...32
DAFTAR GAMBAR
Gambar 1 Struktur Kristal Anatase, Rutile dan Broockite ...7
Gambar 2 Bagian Autoclave, Baja dan Tabung Teflon...11
Gambar 3 Ilustrasi Hukum Bragg ...13
Gambar 4 Klasifikasi Isoterm Adsorpsi Desorpsi ...16
Gambar 5 Klasifikasi Alur Histeresis...17
Gambar 6 Skema Kerja Penelitian ...25
Gambar 7 Difraktogram XRD Senyawa N-TiO2 pada Temperatur Hidrotermal 110°C, 120°C dan 150°C Sebelum Dikalsinasi ...28
Gambar 8 Difraktogram XRD Senyawa N-TiO2yang Disintesis pada Temperatur Hidrotermal 110°C, 120°C dan 150°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam ...30
Gambar 9 Spektra FTIR Sampel N-TiO2yang Disintesis pada Temperatur 110°C Sebelum Kalsinasi dan Sesudah Kalsinasi Selama 3 Jam pada Temperatur 450°C ...33
Gambar 10 Spektra UV Senyawa N-TiO2dengan Variasi Temperatur Hidrotermal Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam...34
Gambar 11 Grafik Energi Celah Pita Senyawa N-TiO2 pada Suhu Hidrotermal 110°C, 120°C, 150°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam...35
Gambar 12 Isoterm Adsorpsi Desorpsi Senyawa N-TiO2Temperatur Hidrotermal 110°C dan 120°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam...36
DAFTAR LAMPIRAN
Lampiran 1 Difraktogram XRD...44
Lampiran 2 Hasil Perhitungan Ukuran Partikel N-TiO2...50
Lampiran 3 Perhitungan Rasio Fasa Rutile:Anatase...55
Lampiran 4 Perhitungan Parameter Kisi dengan U-Fit...56
Lampiran 5 Spektra FTIR N-TiO2yang Disintesis pada Suhu 110°C...61
Lampiran 6 Spektra Absorbansi dan Reflektansi...64
Lampiran 7 Grafik Perhitungan Energi Celah Pita ...70
Lampiran 8 Proses Sintesis dan Hasil Sintesis...72
SINTESIS DAN KARAKTERISASI TiO2TERDADAH NITROGEN
MELALUI METODE HIDROTERMAL DENGAN VARIASI SUHU DAN KALSINASI
Oleh:
Purdiana Susilowati 12307141038
Pembimbing:
Prof. A.K. Prodjosantoso, Ph.D Dr. Cahyorini Kusumawardani, M.Si
ABSTRAK
Penelitian ini bertujuan untuk mensintesis nanopartikel N-TiO2 melalui
metode hidrotermal dengan variasi temperatur untuk mengetahui pengaruh temperatur hidrotermal diikuti dengan kalsinasi terhadap struktur, ukuran partikel,
karakter elektronik dan porositas N-TiO2.
Nanopartikel N-TiO2disintesis dengan cara mencampurkan akuades dengan
HCl 36% dan diaduk selam 10 menit, kemudian ke dalam larutan tersebut ditambahkan larutan dodesilamin sambil dilakukan pengadukan selama 30 menit hingga diperoleh larutan homogen. Setelah itu, ke dalam larutan tersebut
ditambahkan sedikit demi sedikit larutan TiCl4 sambil dilakukan pengadukan
selama 30 menit. Larutan tersebut kemudian dimasukkan ke dalam tablung teflondan dioven selama 12 jam pada temperatur 110°C, 120°C dan 150°C. Hasil dari pengovenan tersebut kemudian digerus dan dikalsinasi selama 3 jam pada
temperatur 450°C. Karakterisasi sampel dilakukan menggunakan X-Ray
Diffraction (XRD), FTIR, UV-Vis dan analisa isoterm adsorpsi-desorpsi
menggunakan alat Quantachrome NovaWin2
Hasil penelitian ini menunjukkan bahwa kenaikan temperatur hidrotermal
yang diikuti dengan kalsinasi pada temperatur 450°C mempengaruhi ukuran
partikel N-TiO2antara lain adanya peningkatan ukuran partikel pada fase rutile dan
adanya penurunan ukuran partikel pada fase anatase. Selain itu, kenaikan temperatur hidrotermal juga menyebabkan perubahan rasio fase anatase dan rutile. Rasio fase rutile mengalami penurunan pada sintesis dengan temperatur
hidrotermal 120°C namun mengalami kenaikan pada sistesis dengan temperatur
hidrotermal 150°C, sedangkan rasio fase anatase menurun seriring dengan naiknya
SYNTHESIS AND CHARACTERIZATION OF NITROGEN-DOPED TiO2
THROUGH HYDROTHERMAL METHOD WITH TEMPERATURE VARIATION AND CALCINATION
By:
Purdiana Susilowati 12307141038
Advisor:
Prof. A.K. Prodjosantoso, Ph.D Dr. Cahyorini Kusumawardani, M.Si
ABSTRACT
This research aims to synthesize N-TiO2 nanoparticles through
hydrothermal method with temperature variations and calcination to determine the influence of hydrothermal temperature on the structure, size of particles, electronic
character and porosity N-TiO2.
N-TiO2nanoparticles synthesized by mixing distilled water with HCl 36%
and stirred 10 minutes, then dodesylamine is added to the solution while stirring for 30 minutes to obtain a homogeneous solution. Thereafter, to the solution was added
TiCl4 while stirring for 30 minutes. The solution is then inserted into teflon tube
and oven for 12 hours at 110°C, 120°C and 150°C. Results of the oven was then crushed and calcined for 3 hours at a temperature of 450°C. Characterization of the samples was performed using X-Ray Diffraction (XRD), FTIR, UV-Vis and analysis of isotherm adsorption-desorption using a Quantachrome NovaWin2.
The results of this study indicate that the rise in temperature hydrothermal followed by calcination at a temperature of 450°C affect the particle size of the
N-TiO2, among others, the increase in the size of particles in rutile phase and a
decrease in particle size on the anatase phase. In addition, the increase in temperature hydrothermal also cause changes in the ratio of anatase and rutile phase. Ratio of rutile phase decreased in the hydrothermal synthesis temperature of 120°C but an increase in the hydrothermal synthesis temperature of 150°C, while the ratio of anatase phase decreases with increasing temperature hydrothermal. Rising hydrothermal temperatures also cause lattice parameter tends to rise, the energy band gap tends to decrease, becoming more uniform pore size, and specific surface area increases.
BAB I PENDAHULUAN
A. Latar Belakang Masalah
Permasalahan energi sedang hangat dibicarakan saat ini. Di Indonesia,
sebagian besar kebutuhan energi masih bergantung pada energi fosil, terutama
energi minyak dan gas bumi. Kebutuhan sumber energi semakin hari semakin
meningkat seiring dengan kemajuan teknologi dan meningkatnya populasi
manusia. Harga energi fosil dari hari ke hari juga semakin mahal seiring dengan
semakin menipisnya cadangan energi fosil. Hal tersebut mendorong banyak ahli
berusaha mengembangkan sumber energi alternatif baru yang murah dan ramah
lingkungan. Salah satu bentuk pengembangan energi terbarukan yang murah dan
ramah lingkungan adalah sel surya.
Energi surya merupakan sumber energi terbesar yang tidak akan pernah
habis ketersediaanya. Energi surya dapat dikonversi menjadi energi listrik
menggunakan sel surya dan dapat dimanfaatkan sebagai energi alternatif untuk
memenuhi kebutuhan manusia di masa sekarang dan di masa yang akan datang.
Sel surya mampu beroperasi dengan baik hampir di seluruh belahan bumi yang
tersinari matahari tanpa menghasilkan polusi sehingga lebih ramah lingkungan.
Mekanisme prinsip kerja sel surya berdasarkan efek fotovoltaik, yaitu foton dari
radiasi diserap kemudian dikonversi menjadi energi listrik. Efek fotovoltaik
adalah suatu peristiwa terciptanya muatan listrik di dalam bahan sebagai akibat
Material berbasis titanium dioksida (TiO2) mulai banyak dikembangkan
untuk aplikasi di bidang fotovoltaik dan fotokatalis sejak kristal tunggal TiO2
digunakan sebagai fotoanoda sel fotoelektrokimia oleh Fujishima dan Honda
(1972). TiO2 memiliki energi celah pita yang cukup lebar, tidak beracun, mudah
disintesis, mempunyai kemampuan fotoaktivitas tinggi, luas permukaan tinggi dan
dapat diregenerasi (Wade, 2005). TiO2mempunyai energi celah pita yang berkisar
antara 3-3,2 eV yang menjadikan TiO2 hanya aktif di daerah sinar ultraviolet
(200-400 nm). Hal ini tentunya menjadi masalah karena hanya 3-5% dari sinar
matahari yang teremisi pada daerah ultraviolet (Mikhalow et al., 2009).
Usaha-usaha untuk meningkatkan respon TiO2terhadap sinar tampak banyak dilakukan,
diantaranya dengan penggunaan sensitizer, pendadahan logam, pendadahan non
logam, modifikasi struktur dan lain-lain.
TiO2 dapat disintesis dengan beberapa metode, antara lain seperti metode
sol-gel (Manseki et al., 2003), teknik sputtering (Asahi et al., 2001), kalsinasi
suhu tinggi pada atmosfer yang mengandung nitrogen (Nakamura et al., 2004) dan
metode hidrotermal. Metode hidrotermal merupakan metode yang lebih
menguntungkan jika dibandingkan dengan proses lainnya karena proses ini lebih
sederhana dan biayanya pun cukup murah. Selain itu, hasil dari metode hidrotemal
lebih homogen karena prosesnya terjadi secara perlahan-lahan (Yanagisawa &
Ovenstone, 1999).
Peningkatan kemampuan fotoaktivitas TiO2 dapat ditingkatkan dengan
cara melakukan pendadahan. Salah satu pendadah yang paling efektif adalah
tampak. Pada penelitian ini, sumber nitrogen yang digunakan berasal dari
surfaktan yang bersifat netral, yaitu dodesilamin. Dodesilamin selain berfungsi
sebagai sumber nitrogen juga berfungsi sebagai pencetak pori. Sintesis material
TiO2 yang terdadah nitrogen dengan metode hidrotermal ini nantinya diharapkan
dapat meningkatkan respon TiO2di daerah sinar tampak.
B. Identifikasi Masalah
Berdasarkan latar belakang masalah yang telah diuraikan, dapat
diidentifikasi masalah sebagai berikut.
1. Metode yang digunakan dalam preparasi TiO2terdadah nitrogen (N-TiO2).
2. Sumber Ti yang digunakan.
3. Sumber N yang digunakan.
4. Temperatur yang digunakan untuk mensintesis nanopartikel N-TiO2.
C. Pembatasan Masalah
Berdasarkan identifikasi masalah yang diuraikan, dapat ditentukan batasan
masalah sebagai berikut.
1. Metode yang digunakan dalam preparasi TiO2 terdadah nitrogen adalah
metode hidrotermal.
2. Sumber Ti yang digunakan adalah TiCl4.
3. Sumber N yang digunakan adalah dodesilamin.
D. Perumusan Masalah
Berdasarkan batasan masalah di atas, perumusan masalah penelitian ini
adalah sebagai berikut.
1. Bagaimana pengaruh variasi temperatur hidrotermal yang diikuti dengan
kalsinasi pada temperatur 450°C terhadap struktur dan ukuran partikel
N-TiO2?
2. Bagaimana pengaruh variasi temperatur hidrotermal yang diikuti dengan
kalsinasi pada temperatur 450°C terhadap karakter elektronik N-TiO2?
3. Bagaimana pengaruh variasi temperatur hidrotermal yang diikuti dengan
kalsinasi pada temperatur 450°C terhadap porositas N-TiO2?
E. Tujuan Penelitian
Berdasarkan perumusan masalah yang diuraikan di atas, tujuan dari
penelitian ini adalah sebagai berikut.
1. Mengetahui pengaruh variasi temperatur hidrotermal yang diikuti dengan
kalsinasi pada temperatur 450°C terhadap struktur dan ukuran partikel N-TiO2.
2. Mengetahui pengaruh temperatur hidrotermal terhadap yang diikuti dengan
kalsinasi pada temperatur 450°C karakter elektronik N-TiO2.
3. Mengetahui pengaruh variasi temperatur hidrotermal yang diikuti dengan
F. Manfaat Penelitian
Manfaat dari penelitian ini adalah:
1. Memberikan informasi tentang peningkatan fotorespon N-TiO2.
2. Menambah wawasan dalam upaya pengembangan energi baru terbarukan
BAB II
KAJIAN PUSTAKA
A. Deskripsi Teori
1. Semikonduktor TiO2
Titanium dioksida (TiO2) merupakan salah satu bahan semikonduktor
yang mempunyai sifat stabil terhadap fotokorosi dan korosi oleh bahan kimia,
inert, dan merupakan senyawa semikonduktor yang bersifat fotokatalis. TiO2
berupa padatan ionik yang terdiri dari Ti4+dan O2-dalam konfigurasi oktahedron.
Padatan ini memiliki 11 bentuk polimorf, dan dari sebelas polimorf tersebut tiga
diantaranya terdapat di alam dan bersifat stabil yaitu anatase, rutile dan broockite
(Sutrisno, 2009).
Rutile merupakan salah satu bentuk polimorf TiO2yang cenderung lebih stabil
pada suhu tinggi sehingga polimorf ini sering ditemukan dalam batuan igneous
(beku karena pengapian). Rutile mempunyai sistem kristal tetragonal dan
memiliki energi celah pita 3,0 eV (Grant., 1959).
Anatase merupakan bentuk polimorf TiO2 yang cenderung lebih stabil pada
suhu rendah. Bentuk kristal anatase terjadi pada pemanasan TiO2 serbuk mulai
dari temperatur 120-500°C (Ollis & Elkabi, 1991). Struktur anatase memiliki
eneri celah pita sebesar 3,2 eV yang setara dengan energi gelombang sinar UV
dengan panjang gelombang 388 nm. Anatase mempunyai sistem kristal tetragonal
(Asahi et al., 2001).
Broockite sangat sulit diamati karena tidak stabil dan umumnya hanya terdapat
dalam mineral. Broockite memiliki struktur kristal orthorombik dan memiliki
Struktur dari ketiga tipe kristal TiO2tersebut ditunjukkan pada Gambar 1.
Gambar 1. Struktur Kristal (a) Anatase, (b) Rutile dan (c) Broockite
Secara umum, anatase dan rutile merupakan fasa kristal dari TiO2 yang
banyak diaplikasikan dalam proses fotokatalis, sel fotovoltaik, fotoinduksi
superhidrofilik dan pemurnian lingkungan seperti pemurnian udara dan air (Shifu
& Gengyu, 2005). Fase anatase memiliki fotoaktivitas yang lebih tinggi
dibandingkan dengan rutile (Yates et al., 1995). Menurut Su et al. (2004)
fotoaktivitas TiO2 dipengaruhi oleh beberapa faktor, antara lain seperti luas
permukaan spesifik, ukuran kristalit, distribusi ukuran pori dan metode preparasi.
TiO2 yang berukuran nano dengan stuktur mesopori mempunyai fotoaktivitas
yang paling optimal. Kartini (2004) juga menyatakan aplikasi TiO2 sebagai
semikonduktor pada sistem DSSC dimana TiO2mesopori dengan luas permukaan
yang tinggi dan domain fase kristal anatase dapat meningkatkan efisiensi sel
surya. Luas permukaan yang tinggi mengakibatkan adsorpsi senyawa sensitiser
yang lebih besar sehingga dapat meningkatkan penyerapan sinar, dan domain fase
anatase menyebabkan efisiensi perpindahan elektron yang lebih tinggi.
a b
2. TiO2terdadah Nitrogen (N-TiO2)
Pemanfaatan TiO2 sebagai semikonduktor fotokimia diawali dengan
penemuan sel fotoelektrokimia pertama untuk dekomposisi air dengan
menggunakan elektroda TiO2 yang dilapisi Pt oleh Fujishima & Honda (1972).
Sejak saat itu, penelitian di bidang fotokatalis didominasi studi fotokatalitik
oksidasi berbasis TiO2. Gratzel & O’Regan (1991) menggunakan TiO2 sebagai
semikonduktor fotoanoda pada dye-sensitized solar cells/DSSC. DSSC
mengundang banyak perhatian karena menghasilkan efisiensi konversi yang tinggi
dengan biaya produksi yang rendah. DSSC mampu menghasilkan konversi energi
sinar menjadi energi listrik sekitar 11% (Gratzel dan Zakeeruddin, 2008).
TiO2merupakan semikonduktor yang mempunyai energi celah pita (Eg)
3-3,2 eV dan bersifat transparan di daerah sinar tampak. Dengan harga Eg pada
kisaran tersebut, TiO2mengadsorpsi energi foton pada daerah ultraviolet dengan
kisaran panjang gelombang 290-400 nm (Gratzel dan Gerfin, 1997). Oleh karena
itu TiO2 hanya memiliki respon optis aktif di daerah sinar ultraviolet. Dengan
demikian dapat dikatakan TiO2tidak mempunyai respon di daerah sinar tampak
karena absorpsi energi foton pada daerah visibel dengan kisaran panjang
gelombang 400-900 nm kurang efektif untuk proses transisi elektron dari pita
valensi ke pita konduksi TiO2. Respon TiO2 terhadap cahaya matahari sangat
rendah karena hanya 5% dari cahaya matahari yang dipancarkan pada daerah
ultraviolet (Yates et al., 1995).
Salah satu usaha yang cukup efektif untuk meningkatkan fotoaktivitas TiO2
logam yang paling efektif adalah nitrogen, karena memiliki ukuran yang hampir
sama dengan oksigen dan memiliki energi ionisasi yang kecil (Park et al., 2002).
TiO2yang terdadah nitrogen menghasilkan aktivitas fotokatalik yang lebih tinggi
jika dibandingkan dengan TiO2murni pada reaksi dekomposisi senyawa organik.
Peningkatan fotoaktivitas TiO2 tersebut juga dipengaruhi oleh karakter
fisikokimia material TiO2 seperti ukuran partikel, kristalinitas dan porositas
(Wade, 2005). Aplikasi TiO2 terdadah nitrogen pada sistem DSSC juga
memberikan efisiensi sel surya dengan kestabilan yang tiggi jika dibandingkan
dengan TiO2murni. Efisiensi yang dihasilkan pada DSSC berbasis N-TiO2adalah
sekitar 8% dengan kestabilan selama 2000 jam, sedangkan pada TiO2 murni
efisiensi yang dihasilkan adalah 3,8% dengan kestabilan selama 680 jam (Ma et
al., 2005).
Pendadahan nitrogen pada permukaan TiO2bertujuan untuk menghasilkan
material yang aktif pada daerah sinar tampak. Penerapan pendadahan pada
semikonduktor berarti penambahan pengotor pada material semikonduktor dengan
tujuan untuk memodifikasi karakteristik elektroniknya sehingga dapat
menurunkan energi celah pita.
Sintesis N-TiO2 telah dilakukan oleh Sato (1986) dengan cara melakukan
kalsinasi Ti(OH)4 yang dihasilkan dari proses hidrolisis TiCl4 dengan adanya
NH4Cl. Proses kalsinasi dilakukan pada temperatur 400°C dan menghasilkan
material N-TiO2 yang menunjukkan peningkatan fotoaktivitas pada daerah sinar
kecepatan dekomposisi pada gas asetaldehida lima kali lebih cepat jika
dibandingkan dengan TiO2 murni. Sintesis dengan metode sol-gel pernah
dilakukan oleh Burda et al. (2003) untuk menghasilkan material N-TiO2mesopori.
Dodesilamin digunakan sebagai pencetak pori dan sumber nitrogen. Nitrogen
yang terdadah pada TiO2memberikan peningkatan respon di daerah sinar tampak
yang ditunjukkan dengan adanya pergeseran serapan pada panjang gelombang 600
nm.
3. Sintesis N-TiO2dengan Metode Hidrotermal
Sintesis dengan metode hidrotermal merupakan metode yang melibatkan
penggunaan air pada suhu dan tekanan yang tinggi dengan tujuan untuk merubah
stuktur kristal dan juga membentuk material nanostruktur. Metode hidrotermal
merupakan metode preparasi material mikropori yang telah dikembangkan oleh
Rouxel dari Universite de Nantes Perancis yaitu dengan menggunakan air sebagai
media pelarut. Metode ini dilakukan dengan menggunakan tekanan uap dan suhu
di atas titik didih normal yang bertujuan untuk mempercepat reaksi antar zat
padat. Metode hidrotermal dapat digunakan untuk pembentukan/pertumbuhan
kristal tunggal (West, 1984).
Metode hidrotermal lebih menguntungkan dibandingkan dengan proses
lainnya, antara lain menghemat enegi, proses sederhana, bebas polusi (karena
dilakukan pada sistem tertutup), biaya cukup efisien, tingkat dispersi lebih tinggi,
kontrol nukleasi yang lebih baik, tingkat reaksi yang tinggi, dan temperatur
mengontrol bentuk (Pujianto, 2009). Material hasil sintesis melalui metode
hidrotermal juga lebih homogen karena prosesnya terjadi secara perlahan lahan
(Yanagisawa & Ovenstone, 1999). Teknik ini juga memudahkan fabrikasi, bahkan
pada material kompleks dengan sifat fisik maupun kimia yang ekstrim.
Pertumbuhan kristal dengan metode hidrotermal terjadi dalam sebuah alat
yang terbuat dari tabung baja yang disebut autoclave. Pada umumnya, alat ini
berbentuk tabung silinder yang berdinding tebal yang memiliki hermetic seal yang
bertujuan agar tahan terhadap suhu tinggi dan tekanan dalam periode tertentu.
Autoclave ini harus inert terhadap larutan untuk mencegah terjadinya reaksi antara
dinding dan bagian yang dimasukkan ke dalamnya. Selain itu juga harus
diperhatikan apabila zat yang dimasukkan bersifat korosi. Untuk mencegah
terjadinya korosi, pada umumnya autoclave diberi tambahan berupa protective
insert. Bagian ini dapat terbuat dari tembaga, emas, perak, titanium, kaca, kuarsa
atau teflon tergantung temperatur yang akan digunakan (Akhmad et al., 2004).
Bagian dari autoclave, baja dan tabung teflon dapat dilihat pada Gambar 2.
Gambar 2. Bagian Autoclave, Baja dan Tabung Teflon Lapisan Teflon
Tutup tabung baja
4. Metode X-Ray Diffraction (XRD)
Spektroskopi X-Ray Diffraction atau XRD merupakan salah satu metode
karakterisasi material kristalin untuk menentukan parameter kisi dan struktur
kristal (Handayani & Haryadi, 1998). Difraktogram XRD dapat digunakan untuk
melakukan identifikasi dan analisis struktur kristal berdasarkan puncak-puncak
difraksi yang muncul. Fase kristal dapat diidentifikasi berdasarkan jarak antar
bidang (dhkl) atau sudut refleksi puncak (2 ) yang berhubungan. Pola difraksi
standar yang umumnya digunakan adalah JCPDS file (Join Commite on Powder
Diffraction Standard) atau ASTM (American Society for Testing Materials).
Cara kerja XRD yaitu cahaya monokromatik sinar-X ttembakkan pada
kristal, satu pantulan atau difraksi dari variasi sudut sinar-X akan menunjukkan
sinar mula-mula, jika seberkas sinar-X menumbuk partikel berukuran atom maka
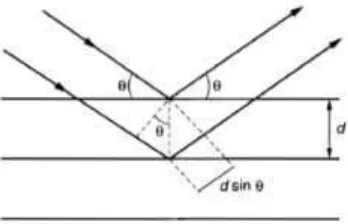
sinar tersebut akan dipantulkan oleh partikel atomik yang ditumbuknya. Bragg
menunjukkan bahwa lebih mudah untuk memperhatikan sinar-X yang direfleksi
dari setumpuk bidang dalam kristal karena hanya bergantung pada sudut tertentu
yang ditentukan oleh panjang gelombang sinar-X dan ruang antar bidang dalam
kristal itu. Variabel ini dapat dihubungkan melalui persamaan Bragg (Smallman,
1991) pada Persamaan 1.
…...(1)
Dimana, n = orde
λ = panjang gelombang sinar monokromatis
d = jarak antar bidang kristal
Gambar 3. Ilustrasi Hukum Bragg
5. Metode FTIR
Spektroskopi infra merah merupakan metode analisis yang dapat
digunakan untuk mengidentifikasi gugus organik maupun gugus anorganik.
Analisis FTIR digunakan untuk analisis kualitatif gugus fungsional suatu material.
Spektrum serapan infra merah suatu senyawa bersifat khas, artinya senyawa yang
berbeda akan mempunyai spektrum yang berbeda pula. Serapan infra merah
berkaitan dengan vibrasi molekul atau atom, dan hanya radiasi dengan frekuensi
yang sama dengan frekuensi vibrasi tersebut akan diserap. Atom dan molekul
dalam suatu senyawa berisolasi atau bervibrasi dengan frekuensi sekitar 1013-1014
hitungan per detik (hpd). Vibrasi molekul atau atom menyebabkan jarak antar
atom berubah karena pergerakan atom menyebabkan atom-atom mengalami
pergantian berkala satu sama lain. Sampel analisis FTIR padat dapat berupa
kristal, gel, amorf, serbuk dan lain-lain. Ada tiga cara yang dapat dilakukan untuk
mencatat spektra bentuk padatan antara lain metode pellet KBr, metode mull dan
bentuk film/lapis tipis (Sastrohamidjojo, 2007). Analisis FTIR pada penelitian ini
6. Metode Uv-Vis
Spektroskopi UV-Vis digunakan untuk mengukur panjang gelombang dan
intensitas penyerapan sinar UV dan sinar tampak. Analisis yang digunakan pada
spektroskopi ini didasarkan pada interaksi antara molekul dengan sinar. Nilai
energi celah pita dapat ditentukan dengan menggunakan teknik Kubelka Munk
(Morales & Pena, 2007) dengan cara menghubungkan energi celah pita (Eg)
dengan nilai reflektansi dari sampel. Nilai energi celah pita dapat digunakan untuk
mengetahui perubahan sifat elektronik dari material hasil sintesis.
Energi celah pita N-TiO2 dapat ditentukan energi celah pita yang
dihasilkan dengan menggunakan metode spektrofotometri UV-Vis Diffuse
Reflectance. Metode ini didasarkan pada pengukuran intensitas UV-Vis yang
direfleksikan oleh sampel. Reflektansi yang terukur dinyatakan dalam persmaan
berikut (Morales & Pena, 2007):
…...(2)
Nilai ini akan digunakan untuk mengetahui persamaan Kubelka Munk:
…...(3)
Persamaan ini memiliki hubungan dengan parameter k (koefisien absorbansi) dan
s (koefisien hamburan reflektansi difusi), F(R’∞)=k/s , sehingga persamaan
selanjutnya dapat ditulis:
Dimana k= A (E-Eg)γ dengan A adalah tetapan dan nilai γ = 2 adat ½, sehingga
persamaan tersebut kemudian dapat dijabarkan lagi menjadi Persamaan 5:
…...(5)
…...(6)
Dimana E= hv maka dengan metode ini energi celah pita diperoleh dari grafik
hubungan antara hv (eV) vs (F(R’∞)hv) . Energi celah pita semikonduktor adalah
besarnya hv pada saat (F(R’∞) hv) =0, yang diperoleh dari persamaan regresi
linier kurva tersebut.
7. Isoterm Adsorpsi-Desorpsi N2
Isoterm adsorpsi-desorpsi N2digunakan untuk mengkarakterisasi porositas
material. Jika suatu padatan dilewati gas dengan tekanan tertentu, gas akan
mengalami penetrasi ke dalam pori padatan. Grafik jumlah gas yang teradsorp (V)
versus tekanan (P) saat proses adsorpsi pada temperatur konstan disebut isoterm
adsorpsi. Proses adsorpsi diklasifikasikan dalam dua kategori: adsorpsi fisika dan
adsorpsi kimia. Adsorsi fisika yang sering juga disebut adsorpsi Van der Waals
dihasilkan dari interaksi molekuler, sedangkan adsorpsi kimia dihasilkan dari
interaksi-interaksi kimia yang spesifik antara adsorbat dengan adsorben dengan
energi yang menyertai terjadinya ikatan kimia.
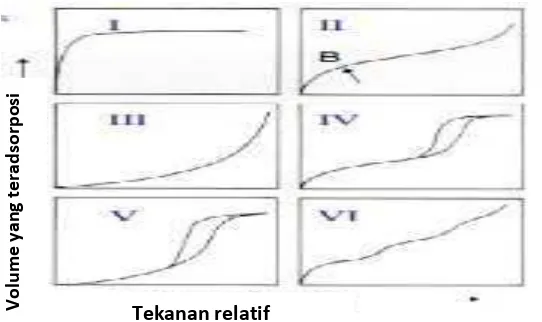
Isoterm adsorpsi menurut klasifikasi Brunair-Deming-Teller (BDDT)
Gambar 4. Klasifikasi Isoterm Adsorpsi Desorpsi
Isoterm adsorpsi tipe I dihasilkan dari adsorpsi mikropori. Isoterm adsorpsi tipe II
dihasilkan dari isoterm adsorpsi padatan non pori atau makropori yang heterogen,
adsorpsinya bersifat reversibel. Isoterm adsorpsi tipe III terjadi karena interaksi
adsorben-adsorbat yang lemah. Isoterm adsorpsi tipe IV memiliki histeresis loop
atau peristiwa dimana kurva proses isoterm adsorpsi dan isoterm desorpsi tidak
berimpit/sudut kontak adsorben-adsorbat pada proses adsorpsi biasanya lebih
besar daripada sudut kontak pada proses desorpsi karena jalan isoterm adsorpsi
berbeda dengan isoterm desorpsi sampai tekanan relatif P/P0 mendekati 0,4.
Histeresis ini disebabkan oleh adanya retakan kapiler pada adsorben dan
karakteristik pada material mesopori. Isoterm adsorpsi tipe V dihasilkan dari
interaksi adsorben-adsorbat yang lemah seperti halnya isoterm adsorpsi tipe III.
Jalan isoterm adsorpsi berbeda dengan jalan isoterm desorpsi seperti pada tipe IV.
Isoterm adsorpsi tipe VI karakteristik untuk multilayer adsorpsi pada material non
pori yang seragam (Allen, 1997).
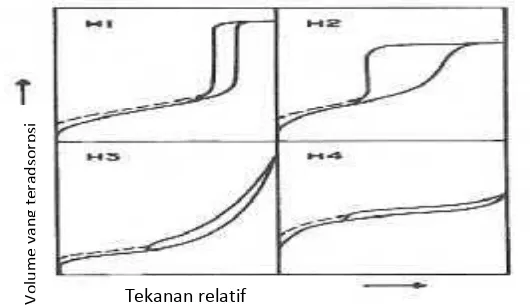
Alur histeresis pada isoterm adsorpsi desorpsi menunjukkan adanya
kondensasi kapiler dalam mesopori. Menurut IUPAC alur histeresis
diklasifikasikan dalam empat tipe (Gambar 5) yang masing-masing berkaitan
dengan bentuk dan struktur porositas dalam mesopori. Alur histeresis tipe H1
merupakan karakteristik untuk material mesopori yang mengalami aglomerasi
dengan ukuran yang seragam (distribusi pori sempit). Tipe H2 menunjukkan
adanya pori yang berbentuk leher sempit dengan ruang yang luas di dalamnya.
Tipe H3 menunjukkan pori dengan bentuk slit-like, dan tipe H4 menunjukkan
karakter mikropori yang dominan (Allen, 1997).
Gambar 5. Klasifikasi Alur Histeresis
B. Penelitian yang Relevan
Azmi (2014) menggunakan teknik basah untuk preparasi N-TiO2 dengan
mencampur TTIP, etilendiamin, akuades dan etanol. Sensitisasi senyawa N-TiO2
menggunakan CdS dengan metode SILAR (Succesive Layer Adsorption) dapat
menurunkan energi celah pita N-TiO2 menjadi 1,95 eV pada 50x pencelupan
dengan CdS. Pencelupan yang semakin banyak menghasilkan pergeseran absorpsi
ke arah visibel pada spektra UV-Vis.
2000) tetapi TiO2 terdadah logam tidak stabil secara termal. Usaha baru yang
intensif juga dilakukan untuk memperoleh TiO2aktif di daerah sinar tampak yaitu
dengan subtitusi unsur non logam seperti N, C, S, P dan B terhadap sisi oksigen
pada kisi TiO2 (Asahi et al., 2001; Gole et al., 2003). Menurut Xie et al. (2000)
diantara beberapa unsur non logam tersebut yang paling efektif digunakan sebagai
pendadah untuk meningkatkan respon TiO2 di daerah sinar tampak adalah
nitrogen.
Pendadahan nitrogen sebagai bahan pencetak pori betujuan untuk
menghasilkan nanopartikel TiO2 mesopori. Seperti yang telah dilaporkan oleh
Gratzel (2005), nanopartikel TiO2 mesopori memiliki kelebihan sifat seperti luas
permukaan yang tinggi dan perpindahan muatan karena induksi foton yang lebih
mudah terjadi.
Metode hidrotermal konvensional digunakan untuk mensintesis TiO2
dengan waktu yang cukup singkat jika dibandingkan dengan metode sol-gel.
Seperti yang telah dilakukan oleh Manseki et al. (2003) yang menggunakan
metode hidrotermal dengan bantuan gelombang mikro untuk mensintesis
nanopartikel TiO2 dengan waktu yang lebih singkat dibandingkan metode
hidrotermal konvensional.
C. Kerangka Berpikir
Titanium oksida (TiO2) merupakan bahan semikonduktor yang memiliki
kemampuan fotoaktivitas di daerah sinar ultraviolet, sedangkan intensitas sinar
modifikasi TiO2agar memiliki respon di daerah sinar tampak untuk meningkatkan
efektivitas pemanfaatan energi matahari. Salah satu cara yang dapat dilakukan
untuk meningkatkan aktivitas TiO2 di daerah sinar tampak antara lain modifikasi
permukaan TiO2 dengan pendadahan, salah satunya dengan pendadahan nitrogen.
Sintesis TiO2 terdadah nitrogen dapat dilakukan melalui metode hidrotermal.
Sumber nitrogen didapatkan dari dodesilamin. Selain sebagai sumber nitrogen
dodesilamin juga digunakan sebagai templat pencetak pori. Sintesis dengan
metode hidrotermal diharapkan dapat menghasilkan N- TiO2dengan lebih cepat.
Kristal dari hasil sintesis ini diharapkan dapat menghasilkan energi celah pita
yang aktif di daerah sinar tampak sehingga dapat digunakan untuk aplikasi sel
BAB III
METODE PENELITIAN
A. Alat dan Bahan Penelitian
1. Alat-alat Penelitian
Peralatan utama yang digunakan dalam penelitian meliputi alat-alat gelas
untuk proses sintesis, stirrer dan magnetic stirrer, tabung teflon, oven, muffle
furnace, dan alat-alat instrumentasi analisis karakter senyawa seperti XRD Rigaku
Multiflex dengan radiasi Cu Kα (λ =1,5405981 Å), UV 1700 Pharmaspec UV-Vis
Spectrophotometer Specular Reflectance, Fourrier Transform Infra-Red (FTIR)
dan Quantachrome NovaWin2.
2. Bahan-bahan Penelitian
Bahan-bahan utama yang digunakan meliputi TiCl4 (Aldrich), HCl 36%
dan etanol (Merck), akuades (General), dan dodesilamin (Aldrich).
B. Subjek dan Objek Penelitian
1. Subjek Penelitian
Subjek penelitian ini adalah senyawa nanopartikel N-TiO2.
2. Objek Penelitian
Objek penelitian ini adalah gugus fungsional, fase kristal, ukuran partikel,
parameter kisi, energi celah pita dan luas permukaan dari senyawa nanopartikel
C. Waktu dan Tempat Penelitian
1. Waktu penelitian
Waktu penelitian: 3 bulan
2. Tempat penelitian
Tempat penelitian: Laboratorium penelitian kimia FMIPA UNY
D. Prosedur Penelitian
1. Sintesis nanopartikel N-TiO2dengan metode hidrotermal
a. Sebanyak 4 mL akuades ditambahkan pada 4 mL larutan HCl (36%),
kemudian diaduk dengan pengaduk magnet selama 10 menit sampai larutan
homogen.
b. Ke dalam larutan 1.a, ditambahkan 2 mL dodesilamin dan diaduk dengan
pengaduk magnet selama 30 menit hingga terbentuk struktur misel.
c. Ke dalam larutan 1.b, ditambahkan 4 mL TiCl4dan diaduk selama 30 menit
dengan menggunakan pengaduk magnet sampai larutan homogen.
d. Larutan yang telah homogen dimasukkan ke dalam tabung teflon dan ditutup
dengan rapat.
e. Tabung teflon yang berisi larutan dipanaskan selama 12 jam pada temperatur
110°C.
f. Padatan yang berada dalam tabung teflon dikeluarkan dan dikalsinasi selama 3
jam pada temperatur 450°C.
2. Karakterisasi dan Analisis
a. Difraksi Sinar-X Serbuk (Powder X-Ray Diffraction/XRD)
Analisis XRD dilakukan untuk menentukan struktur kristal, ukuran
partikel, dan parameter kisi. Pola difraksi standar yang digunakan adalah JCPDS
file (Join Commite on Powder Diffraction Standard). Analisis dilakukan pada
kondisi 2 = 20-90º dengan kecepatan scanning 2º/detik. Instrumen XRD
menggunakan sumber radiasi sinar X dari CuKα (λ = 1,54060 Å). Fase kristal
diidentifikasi berdasarkan jarak antar bidang (dhkl) atau sudut refleksi puncak (2 )
yang berhubungan. Perhitungan ukuran partikel dapat ditentukan dengan
menggunakan persamaan Debye-Scherrer (Sutanding, 2008):
…...(9)
Perbandingan rasio fase anatase (A) terhadap fase rutile (R) dihitung secara relatif
dengan membandingkan intensitas puncak difraksi kedua bidang tersebut dengan
persamaan (Gonzales, 1996):
…...(10)
Dengan I101 adalah intensitas refleksi bidang anatase dan I110 adalah intensitas
bidang rutile. Perhitungan parameter kisi kristal dilakukan dengan menggunakan
progam Universal Filter (U-Fit).
b. Spektroskopi Infra Merah
Analisis FTIR dalam penelitian ini digunakan untuk menentukan
Sampel N-TiO2 berupa serbuk, serbuk dari sampel dicampur dengan KBr dan
ditekan untuk menghasilkan pelet. Pelet kemudian discan pada kisaran panjang
gelombang 4000-400 cm-1menggunakan FTIR Termo Nicolet Avatar 360 IR. KBr
murni digunakan sebagai standar untuk setiap analisis.
c. Spektroskopi UV-Vis
Analisis UV-Vis dilakukan untuk karakterisasi absorpsi sampel untuk
menentukan jenis transisi elektronik dari sampel N-TiO2. Analisis UV-Vis juga
digunakan untuk menentukan energi celah pita (Eg) dari sampel N-TiO2.
Karakterisasi dilakukan dengan UV Pharmaspec UV-Vis Spectrophotometer
Specular Refectance dengan sumber sinar halogen. Pada penelitian ini analisis
dilakukan terhadap lapis tipis pada kaca substrat dengan standar kaca substrat.
Karakter absorpsi dilakukan pada kisaran 200-800 nm dengan kecepatan scanning
2 nm/detik.
Energi celah pita N-TiO2 dapat ditentukan dengan menggunakan metode
spektrofotometri UV-Vis Diffuse Reflectance. Data spektrum UV-Vis Diffuse
Reflectance berupa kurva hubungan antara reflektansi (R) dengan panjang
gelombang (λ ) atau absorbansi (A) dengan panjang gelombang (λ ). Energi celah
pita dapat ditentukan dengan menggunakan grafik hubungan antara energi foton
(hv) dengan (F(R’∞)hv)1/2yang terdapat pada Persamaan 6. Grafik yang diperoleh
disinggunggkan dengan garis linier untuk mengetahui besar energi celah pita.
d. Isoterm Adsorpsi Desorpsi
Analisis luas permukaan dan distribusi ukuran pori dilakukan dengan
Quantachrome NovaWin2 terhadap sampel serbuk dengan berat sekitar 0,1 gram.
Sebelum dilakukan analisis, sampel di-degassing pada 180°C dengan kondisi
vakum selama 3 jam. Luas permukaan spesifik ditentukan menggunakan metode
Brunauer-Emmet-Teller (BET) pada P/Po 0-0,3. Pada penentuan luas permukaan
spesifik menggunakan BET adsorbat yang digunakan adalah gas nitrogen dan
proses adsorpsi isotermisnya berlangsung pada suhu 77 K dengan tekanan relative
dibatasi pada rentang 0,005-0,350. Sedangkan distribusi ukuran pori ditentukan
3. Bagan Penelitian
Akuades 4 mL HCL (36%) 4 mL
Aduk 10 menit
Campuran
homogen 1 Dodesilamin 2 mL
Aduk 30 menit
Campuran
homogen 2 TiCl44 mL
Campuran homogen 3
Aduk 30 menit
Dimasukkan teflon
Oven 12 jam (110°, 120°dan 150° C)
Kalsinasi 3 jam pada temperatur 450°C
Karakterisasi
• XRD
• FTIR
• UV-Vis
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Sintesis N-TiO2dengan metode hidrotermal
Pada penelitian ini nanopartikel TiO2 yang terdadah nitrogen disintesis.
Pendadahan nitrogen diharapkan mampu meningkatkan aktivitas fotokatalik TiO2
dengan penurunan energi celah pita, sehingga elektron mampu pindah ke pita
konduksi dengan lebih mudah. Sintesis dilakukan dengan metode hidrotermal
menggunakan dodesilamin sebagai sumber nitrogen, TiCl4 sebagai sumber Ti,
akuades sebagai pelarut dan HCl sebagai pengarah struktur untuk mendapatkan
nanosferis TiO2. Reaksi hidrotermal (penggunaan air sebagai pelarut di atas titik
didihnya) harus dilakukan pada sistem tertutup, hal ini dilakukan untuk mencegah
hilangnya pelarut saat proses pemanasan.
Pada proses hidrotermal yang pertama dilakukan adalah mencampurkan 4
mL akuades dengan 4 mL HCl 36% dan diaduk selama 10 menit. Setelah itu, ke
dalam larutan tersebut ditambahkan larutan dodesilamin 2 mL tetes demi tetes
sambil dilakukan pengadukan selama 30 menit hingga diperoleh larutan homogen.
Pada proses ini akan terjadi pembentukan misel dodesilamin. Setelah itu, ke dalam
larutan tersebut ditambahkan sedikit demi sedikit larutan TiCl4 sambil dilakukan
pengadukan selama 30 menit. Penambahan ini dimaksudkan untuk menghindari
terjadinya penggumpalan partikel. Campuran dari semua larutan tersebut
merupakan larutan prekursor. Larutan prekursor tersebut kemudian dimasukkan
ke dalam tablung teflon. Teflon ditutup dengan rapat agar ketika dilakukan
jam pada temperatur 110°C, 120°C dan 150°C. Hasil dari perlakuan tersebut
berupa gumpalan berwarna putih. Gumpalan tersebut kemudian digerus dan
dikalsinasi selama 3 jam pada temperatur 450°C. Karakterisasi sampel dilakukan
menggunakan X-Ray Diffraction (XRD) untuk menentukan struktur kristal,
ukuran partikel dan parameter kisi. Selain itu juga dilakukan karakterisasi dengan
menggunakan spektroskopi infra merah untuk mempelajari perubahan gugus
fungsional dan efektivitas kalsinasi pada N-TiO2, spektroskopi UV-Vis untuk
menganalisis besarnya energi celah pita (Eg), dan analisa isoterm
adsorpsi-desorpsi untuk menentukan luas permukaan spesifik dan distribusi ukuran pori.
B. Karakterisasi N-TiO2Hasil Sintesis dengan Metode Hidrotermal
1. Karakterisasi Menggunakan X-Ray Diffraction (XRD)
Analisis struktur dan parameter kisi kristal dari nanopartikel N-TiO2
dilakukan dengan menggunakan X-Ray Diffraction (XRD) dengan sumber radiasi
Cu-Kα (λ =1,5406 Å), pada kisaran 20-90°. Pola difraksi XRD sampel N-TiO2
(Gambar 7) menunjukkan bahwa senyawa N-TiO2yang disintesis pada temperatur
110°C, 120°C dan 150°C sebelum dikalsinasi menunjukkan adanya fase rutile
pada ketiga sampel dan fase anatase pada sampel yang disintesis pada temperatur
120°C dan 150°C. Selain terdapat fase rutile dan anatase juga muncul
puncak-puncak yang berasal dari fase organik dari dodesilamin. Hail dari XRD ini
Meas. data:213-xrd-2016/Data 1
Gambar 7. Difraktogram XRD Senyawa N-TiO2pada Temperatur Hidrotermal
110°C (a), 120°C (b) dan 150°C (c) Sebelum Dikalsinasi
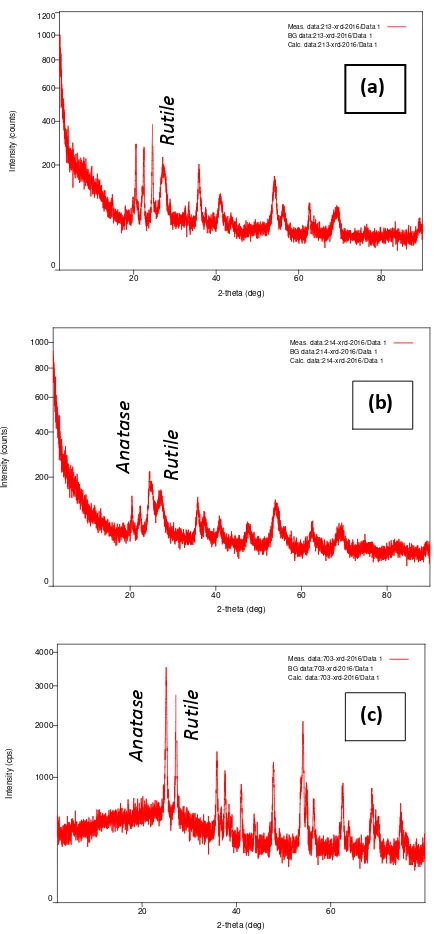
Analisis XRD yang dilakukan terhadap N-TiO2 hasil kalsinasi disajikan
pada Gambar 8. Difraktogram pada Gambar 8 menunjukkan posisi puncak utama
fase kristal rutile dari senyawa N-TiO2 yang disintesis secara berurutan pada
temperatur 110°C, 120°C dan 150°C setelah kalsinasi pada temperature 450°C
selama 3 jam sebesar 27,259°, 27,158° dan 27,141°. Puncak utama dari fase
kristal anatase senyawa N-TiO2 yang disintesis pada temperatur 120°C dan
temperatur 150°C setelah dikalsinasi muncul pada 2 sebesar 25,002° dan
25,070°. Hasil analisis XRD juga menunjukkan bahwa perlakuan kalsinasi selama
3 jam pada temperatur 450°C menghasilkan nanokristal N-TiO2.
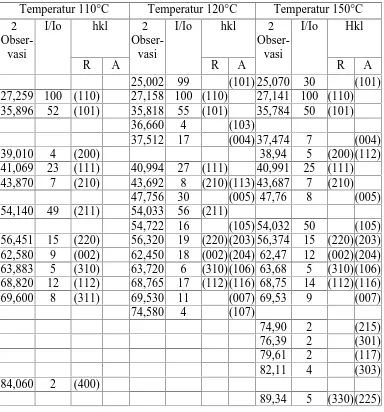
Tabel 1. Data Hasil XRD Sampel N-TiO2Setelah Kalsinasi
Temperatur 110°C Temperatur 120°C Temperatur 150°C
2θ
25,002 99 (101) 25,070 30 (101)
27,259 100 (110) 27,158 100 (110) 27,141 100 (110)
35,896 52 (101) 35,818 55 (101) 35,784 50 (101)
36,660 4 (103)
37,512 17 (004) 37,474 7 (004)
39,010 4 (200) 38,94 5 (200)(112)
41,069 23 (111) 40,994 27 (111) 40,991 25 (111)
43,870 7 (210) 43,692 8 (210)(113) 43,687 7 (210)
47,756 30 (005) 47,76 8 (005)
54,140 49 (211) 54,033 56 (211)
54,722 16 (105) 54,032 50 (105)
56,451 15 (220) 56,320 19 (220)(203) 56,374 15 (220)(203)
62,580 9 (002) 62,450 18 (002)(204) 62,47 12 (002)(204)
63,883 5 (310) 63,720 6 (310)(106) 63,68 5 (310)(106)
68,820 12 (112) 68,765 17 (112)(116) 68,75 14 (112)(116)
69,600 8 (311) 69,530 11 (007) 69,53 9 (007)
dikalsinasi pada temperatur 450°C selama 3 jam dengan menggunakan Persamaan
10.
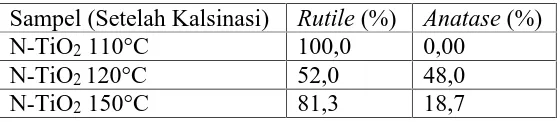
Hasil perbandingan fase rutile dan anatase disajikan dalam Tabel 2.
Perubahan rasio fase rutile dan anatase terjadi karena perlakuan sintesis secara
hidrotermal pada temperatur yang berbeda.
Tabel 2. Hasil Perbandingan Fase Rutile dan Anatase
Sampel (Setelah Kalsinasi) Rutile (%) Anatase (%)
N-TiO2110°C 100,0 0,00
N-TiO2120°C 52,0 48,0
N-TiO2150°C 81,3 18,7
Ukuran kristalit dari sampel yang telah dikalsinasi dihitung berdasarkan
full width at a half of the maximum height (FWHM) dengan formula
Debye-Scherrer (Persamaan 9) menunjukkan ukuran kristalit N-TiO2(Tabel 3):
Tabel 3. Ukuran Kristalit N-TiO2Setelah Dikalsinasi
Sampel Rutile (nm) Anatase (nm)
N-TiO2110°C 35,79
-N-TiO2120°C 33,94 28,35
N-TiO2150°C 31,02 29,34
Ukuran kristal sampel N-TiO2 yang dihitung berdasarkan puncak bidang
anatase dan rutile pada difraktogram XRD menyatakan bahwa ukuran kristal
rutile mengalami penurunan seiring dengan meningkatnya temperatur
hidrotermal, berbeda dengan ukuran kristal fase anatase yang meningkat seiring
dengan peningkatan temperatur hidrotermal.
dengan menggunakan program Universal Filter (U-Fit). Adapun parameter kisi
N-TiO2dapat dilihat pada Tabel 4.
Tabel 4. Hasil U-Fit Parameter Kisi Sampel Setelah Dikalsinasi
Sampel Rutile Anatase
N-TiO2110°C a= 4,5943
c= 2,9598
z= -0,1687 D= 0,0061 R= 0,0008
-N-TiO2120°C a= 4,6156
c= 3,0005
N-TiO2150°C a= 4,6395
c= 3,0019
Perhitungan parameter kisi kristal dihitung dengan formula yang
menghubungkan jarak antar bidang dhkl dengan konstanta kisi a, b, dan c, nilai
parameter kisi fraksi rutile berdasarkan standar JCPDS No. 01-076-0322 untuk
konstanta kisi a= 4,6344 Å dan c= 2,9919 Å sedangkan untuk fraksi anatase
konstanta kisi a= 3,7850 Å dan c= 9,5100 Å (JCPDS No.01-083-2243). Perbedaan
parameter kisi a dan c terhadap JCPDS menunjukkan bahwa peningkatan
temperatur hidrotermal dalam sintesis TiO2 menyebabkan terjadinya ekspansi
pada sumbu a dan sumbu c, sehingga mengakibatkan parameter kisi dari sampel
2. Karakterisasi menggunakan FTIR
Pengaruh perlakuan kalsinasi terhadap karakter N-TiO2 diamati dengan
analisis FTIR. Perubahan gugus fungsional yang terjadi selama proses kalsinasi
dapat dilihat pada Gambar 9. Berdasarkan analisis FTIR terlihat bahwa perlakuan
kalsinasi cukup efektif untuk menghilangkan molekul dodesilamin yang ditandai
dengan hilangnya gugus-gugus organik residu dari molekul dodesilamin.
Gambar 9. Spektra FTIR Sampel N-TiO2yang Disintesis pada Temperatur 110°C
Sebelum Kalsinasi dan Sesudah Kalsinasi Selama 3 Jam pada Temperatur 450°C
Gugus-gugus organik terlepas dari N-TiO2 yang ditunjukkan dengan
menghilangnya pita vibrasi C-H dari dodesilamin pada daerah sekitar ~1390 cm-1,
~2849 cm-1 dan ~2917 cm-1. Pita lebar pada ~3438 cm-1 yang timbul dari
rentangan O-H dan serapan C-O di daerah 1300-1000 cm-1tidak lagi muncul. Hal
ini menunjukkan bahwa gugus-gugus organik dari molekul dodesilamin sudah
hilang dari material hasil sintesis. Meskipun demikian masih terdapat serapan kuat
3. Kakaterisasi N-TiO2dengan UV-Vis
Material hasil sintesis kemudian dikarakterisasi menggunakan UV 1700
Pharmaspec Uv-Vis Spectrophotometer Specular Reflectance untuk mengetahui
aktivitas absorbsi lapis tipis N-TiO2yang disintesis pada temperatur 110°C, 120°C
dan 150°C. Spektra absorbsi N-TiO2dapat dilihat pada Gambar 10.
Gambar 10. Spektra UV Senyawa N-TiO2dengan Variasi Temperatur
Hidrotermal Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam
Dari Gambar 10 terlihat bahwa terjadi perubahan transisi elektronik di
daerah ultraviolet. N-TiO2 disintesis pada temperatur 110°C, 120°C dan 150°C
dan dikalsinasi selama 3 jam pada temperatur 450°C memberikan nilai λ maks330
nm dan 333 nm yang merupakan transisi metal to ligand transfer (MLCT) yang
bertumpang tindih dengan transisi d-d.
Besar energi celah pita yang terdapat pada senyawa N-TiO2 dapat
ditentukan dengan menggunakan Persamaan 6. Berdasarkan persamaan tersebut,
dapat diperoleh grafik hubungan antara hv (eV) vs (F ( )hv)1/2. Gambar 11
menunjukkan cara perhitungan energi celah pita dari N-TiO2. Sedangkan besarnya
Tabel 5. Nilai Energi Celah Pita Sampel N-TiO2Setelah Dikalsinasi
Temperatur Hidrotermal Eg
110°C 3,34 eV
120°C 3,02 eV
150°C 3,06 eV
Gambar 11. Grafik Energi Celah Pita Senyawa N-TiO2pada Temperatur
Hidrotermal (a) 110°C, (b) 120°C dan (c) 150°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam
Berdasarkan hasil pada Tabel 5 telihat bahwa kenaikan temperatur
hidrotermal yang digunakan saat sintesis menyebabkan nilai energi celah pita
cenderung menurun. Namun pada saat sampel disintesis pada temperatur 150°C
terjadi sedikit kenaikan nilai energi celah pita yaitu 3,06 eV.
4. Isoterm Adsorpsi-Desorpsi
Analisis adsorpsi desorpsi isotermis N dilakukan untuk mengkarakterisasi
Eg(eV)
disintesis pada temperatur 110°C dan temperatur 120°C ditunjukkan pada Gambar
12. Dari kedua kurva tersebut terlihat bahwa adsorpsi desorpsi yang terjadi pada
material hasil sintesis termasuk dalam tipe III. Isoterm adsorpsi tipe III terjadi
karena interaksi antara adsorben dan adsorbat yang lemah. Kurva tersebut juga
menunjukkan alur histeresis yang berdasarkan klasifikasi dari IUPAC material
hasil sintesis tersebut termasuk dalam alur histeresis tipe H3. Alur histeresis tipe
H3 ini mengindikasikan pori yang berbentuk slit-like (Allen, 1997). Gambar 12
juga menunjukkan bahwa material N-TiO2 yang disintesis pada temperatur 120°C
menyerap gas N2 dengan volum yang lebih banyak yaitu ~77cc/g jika
dibandingkan dengan material N-TiO2 yang disintesis pada temperatur 110°C
yaitu ~41cc/g. Penyerapan gas N2 tersebut dipengaruhi oleh luas permukaan
spesifik masing-masing material. Material N-TiO2yang disintesis pada temperatur
temperatur 120°C memiliki luas permukaan spesifik yang lebih tinggi yaitu 17
m2/g sedangkan material N-TiO2 yang disintesis pada temperatur temperatur
110°C memiliki luas permukaan spesifik 8 m2/g.
Gambar 12. Isoterm Adsorpsi Desorpsi Senyawa N-TiO2pada Temperatur
Hidrotermal (a) 110°C dan (b) 120°C Setelah Dikalsinasi pada Temperatur 450°C Selama 3 Jam
Distribusi ukuran pori rata-rata dari material N-TiO2 yang disintesis pada
temperatur 110°C dan 120°C dihitung berdasarkan metode
Barrett-Joyner-Halenda (BJH) yang hasilnya ditampilkan pada Gambar 13. Material N-TiO2yang
disintesis pada temperatur 120°C mempunyai distribusi pori yang lebih seragam
jika dibandingkan dengan material yang disintesis pada temperatur 110°C, hal ini
menunjukkan bahwa variasi suhu yang lebih tinggi mengakibatkan adanya
penataan struktur menjadi lebih teratur sehingga kristal yang dihasilkan memiliki
ukuran pori yang lebih seragam. Distribusi ukuran pori untuk material yang
disintesis pada temperatur 110°C dan 120°C secara berurut-turut 1,7038 nm dan
1,5295 nm.
Gambar 13. Distribusi Ukuran Pori N-TiO2Temperatur Hidrotermal 110°C dan
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil penelitian dan pembahasan yang telah diuraikan, maka
dapat ditarik kesimpulan sebagai berikut:
1. Kenaikan temperatur hidrotermal yang diikuti dengan kalsinasi pada
temperatur 450°C mempengaruhi ukuran partikel N-TiO2 antara lain adanya
peningkatan ukuran partikel pada fase rutile dan adanya penurunan ukuran
partikel pada fase anatase. Selain itu, kenaikan temperatur hidrotermal yang
diikuti dengan kalsinasi pada temperatur 450°C juga menyebabkan perubahan
rasio fase anatase dan rutile. Rasio fase rutile mengalami penurunan pada
sintesis dengan temperatur hidrotermal 120°C namun mengalami kenaikan
pada sistesis dengan temperatur hidrotermal 150°C, sedangkan rasio fase
anatase menurun seriring dengan naiknya temperature hidrotermal. Kenaikan
temperatur hidrotemal yang diikuti dengan proses kalsinasi pada temperatur
450°C juga menyebabkan parameter kisi cenderung naik.
2. Kenaikan temperatur hidrotermal yang diikuti dengan kalsinasi pada
temperatur 450°C menyebabkan energi celah pita cenderung menurun.
3. Kenaikan temperatur hidrotermal yang diikuti dengan kalsinasi pada
temperatur 450°C menyebabkan ukuran pori menjadi lebih seragam, selain itu
kenaikan temperatur hidrotermal juga menyebabkan luas permukaan spesifik
B. Saran
Penelitian ini masih berada dalam lingkup ruang sederhana dan masih
membutuhkan pengembangan lebih lanjut. Untuk itu peneliti mengajukan saran,
yaitu perlu dilakukan penelitian lebih lanjut untuk mempelajari sintesis senyawa