6 BAB II
TINJAUAN PUSTAKA
2.1 Tinjauan Nyeri
Nyeri adalah pengalaman sensori dan emosional yang tidak menyenangkan akibat dari adanya kerusakan jaringan yang aktual atau potensial. Nyeri muncul sebagai bentuk respon sensori setelah menerima rangsangan nyeri. Nyeri bisa disebabkan karena ada kerusakan jaringan dalam tubuh akibat dari adanya cedera, kecelakaan, maupun tindakan medis seperti operasi (Ratnasari, 2013).
Nyeri terjadi bisa bersamaan karena adanya penyakit atau beberapa pemeriksaan diagnostik maupun pengobatan lain (Brunner & Suddarth’s, 2010).
Nyeri dapat berasal dari setiap bagian tubuh manusia seperti kulit, otot, ligament, sendi, tulang (nyeri nociceptive), jaringan terluka (nyeri inflamasi), saraf (nyeri neuropatik), organ internal (nyeri viseral) atau kombinasi dari jenis rasa sakit (nyeri campuran) (The British Pain Society, 2010).
2.2 Tinjauan Analgesik
Analgesik adalah senyawa yang secara selektif dapat menekan fungsi sistem saraf pusat. Analgesik merupakan zat yang dapat mengurangi rasa nyeri tanpa mengurangi kesadaran (Tjay dan Rahardja, 2015). Dimana analgesik bekerja dengan cara meningkatkan nilai ambang persepsi rasa sakit. Berdasarkan kerja farmakologinya, analgesik dibagi menjadi dua kelompok besar, yaitu analgesik narkotik dan analgesik perifer (non narkotik) (Tjay dan Raharja, 2015).
Analgesik narkotik dapat menekan fungsi sistem saraf pusat secara selektif juga untuk mengurangi rasa sakit. Analgesik non narkotik hanya digunakan untuk mengurangi rasa sakit yang ringan sampai moderat, sehingga aktivitas analgesik dari narkotik jauh lebih besar dibandingkan dengan golongan analgesik non narkotik, maka disebut dengan analagesik kuat (Purwanto dan Susilowati, 2016).
2.3 Tinjauan Analgesik Non Narkotik
Obat analgesik non narkotik atau obat analgesik perifer cenderung mampu menghilangkan atau meringankan rasa sakit tanpa berpengaruh pada sistem saraf pusat bahkan hingga efek menurunkan tingkat kesadaran. Obat analgesik non
narkotik/obat analgesik perifer juga tidak mengakibatkan efek adiksi pada penggunanya. Obat golongan ini mengadakan potensisasi dengan obat-obatan penekan sistem saraf pusat (Siswandono dan Purwanto, 2016).
Analgesik non-narkotik mengurangi nyeri dengan dua aksi yaitu di sistem saraf pusat dan perifer. Tempat aksi utama yaitu di sistem saraf perifer dan pada level nosiseptor dapat mengurangi penyebab nyeri. Sensasi nyeri berhubungan dengan pelepasan substansi endogen seperti prostaglandin, bradikinin (Katzung, 2007).
2.3.1 Tinjauan Asam Salisilat
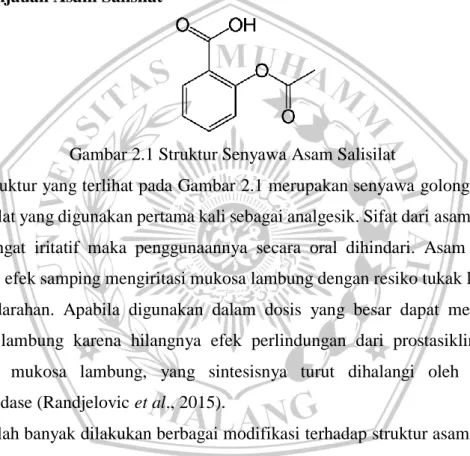
Gambar 2.1 Struktur Senyawa Asam Salisilat
Struktur yang terlihat pada Gambar 2.1 merupakan senyawa golongan asam karboksilat yang digunakan pertama kali sebagai analgesik. Sifat dari asam salisilat yaitu sangat iritatif maka penggunaannya secara oral dihindari. Asam salisilat memiliki efek samping mengiritasi mukosa lambung dengan resiko tukak lambung dan perdarahan. Apabila digunakan dalam dosis yang besar dapat mengiritasi mukosa lambung karena hilangnya efek perlindungan dari prostasiklin (PgI2) terhadap mukosa lambung, yang sintesisnya turut dihalangi oleh blokade siklooksidase (Randjelovic et al., 2015).
Telah banyak dilakukan berbagai modifikasi terhadap struktur asam salisilat untuk memperkecil efek samping serta meningkatkan aktivitasnya disamping itu agar dapat menghasilkan senyawa yang dapat digunakan per oral. Modifikasi struktur yang telah dilakukan yaitu pada gugus karboksil, gugus hidroksi fenolik maupun pada cincin benzene. Senyawa hasil modifikasi pada cincin benzene ialah diflusinal. Sedangkan senyawa hasil modifikasi gugus hidroksi fenolik antara lain adalah asetosal atau asam asetil salisilat yang berkhasiat sebagai analgesik- antipiretik, antiinflamasi dan antiplatelet (Siswandono dan Soekardjo, 2000).
2.3.2 Tinjauan Asam Asetil Salisilat (Asetosal)
Gambar 2.2 Struktur Senyawa Asetosal
Struktur pada Gambar 2.2 adalah sejenis obat turunan dari salisilat yang sering digunakan sebagai analgesik (antinyeri), antipiretik (penurun panas), dan anti inflamasi (antiperadangan) (Saleh, 2011). Asetosal dapat menyebabkan beberapa efek dalam tubuh terutama efek anti inflamasi, analgesik, pencegahan dalam proses pembekuan darah hingga penurun panas. Efek ini didapat akibat dari adanya proses penurunan produksi prostaglandin dan tromboxan (Ekinci, et al., 2011).
2.4 Tinjauan Modifikasi Molekul
Modifikasi molekul merupakan suatu metode yang digunakan untuk mendapatkan obat baru dengan aktivitas yang dikehendaki, antara lain yitu seperti meningkatkan aktivitas obat, menurunkan efek samping dan toksisitas obat, meningkatkan selektivitas obat, memperpanjang masa kerja obat, meningkatkan kenyamanan penggunaan obat dan meningkatkan aspek ekonomis obat (Siswandono, 2008).
Modifikasi molekul umumnya dilakukan dengan cara menyeleksi atau mensintesis obat, pembuatan pra-obat dan obat target, dan modifikasi molekul obat yang telah diketahui aktifitas biologisnya. Tujuan dari modifikasi molekul obat salah satunya adalah untuk menurunkan efek samping serta toksisitasnya atau disebut juga untuk mendapatkan obat dengan indeks terapeutik atau batas keamanannya yang besar (Siswandono, 2000).
2.5 Tinjauan Reaksi Esterifikasi
Reaksi esterifikasi antara asam karboksilat dengan alkohol bersifat reversible, sehingga untuk membuat kesetimbangan reaksi berjalan ke arah pembentukan ester dapat dilakukan dengan memakai jumlah alkohol berlebih. Kecepatan reaksi antara asam karboksilat dengan alkohol tergantung pada jenis alkoholnya dengan urutan yaitu : alkohol primer > alkohol sekunder > alkohol tersier (Hoydonckx, dkk, 2004).
Mekanisme reaksi pembentukan ester seperti pada Gambar 2.3 adalah dengan substitusi nukleofilik pada atom karbonil yang bersifat kekurangan elektron.
Sehingga dengan adanya bantuan dari katalisator membuat atom karbon menjadi lebih rentan terhadap serangan nukleofil (McMurry, 2012).
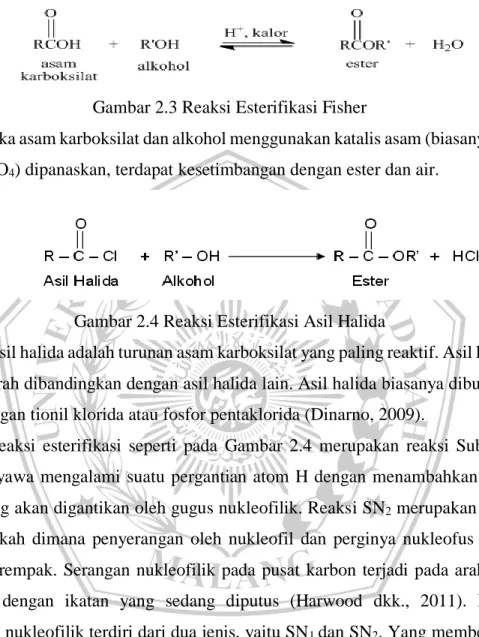
Gambar 2.3 Reaksi Esterifikasi Fisher
Jika asam karboksilat dan alkohol menggunakan katalis asam (biasanya HCl atau H2SO4) dipanaskan, terdapat kesetimbangan dengan ester dan air.
Gambar 2.4 Reaksi Esterifikasi Asil Halida
Asil halida adalah turunan asam karboksilat yang paling reaktif. Asil klorida lebih murah dibandingkan dengan asil halida lain. Asil halida biasanya dibuat dari asam dengan tionil klorida atau fosfor pentaklorida (Dinarno, 2009).
Reaksi esterifikasi seperti pada Gambar 2.4 merupakan reaksi Substitusi SN2, senyawa mengalami suatu pergantian atom H dengan menambahkan gugus pergi yang akan digantikan oleh gugus nukleofilik. Reaksi SN2 merupakan proses satu langkah dimana penyerangan oleh nukleofil dan perginya nukleofus terjadi secara serempak. Serangan nukleofilik pada pusat karbon terjadi pada arah yang kolinear dengan ikatan yang sedang diputus (Harwood dkk., 2011). Reaksi substitusi nukleofilik terdiri dari dua jenis, yaitu SN1 dan SN2. Yang membedakan dari kedua jenis reaksi tersebut yaitu pengaruh substrat dan nukleofil terhadap laju reaksi. Pada reaksi SN1 hanya substrat yeng mempengaruhi laju reaksi sehingga mengikuti reaksi orde satu dengan persamaan kecepatan reaksi = k.[RX].
Sedangkan pada reaksi SN2 yang mempengaruhi laju rekasi adalah substrat dan reaktan sehingga reaksi substitusi berlangsung dengan mengikuti orde dua dengan persamaan reaksi k = [RX] [Nu-] dimana terjadi inversi pada atom karbon pusat alkil halida primer dan sekunder (McMurry, 2008).
2.6 Tinjauan Bahan Sintesis
2.6.1 Tinjauan Senyawa Asam 5-klorosalisilat
Gambar 2.5 Struktur Senyawa Asam 5-klorosalisilat
Struktur senyawa pada Gambar 2.5 adalah C7H5ClO3 yang merupakan turunan dari senyawa asam salisilat. Berat molekul senyawa ini yaitu 172,56 g/mol.
Senyawa asam 5-klorosalisilat memiliki log P sebesar 3,03 dengan titik leleh 171- 172 ℃, serta memiliki kelarutan dalam alkohol. Dengan adanya gugus kloro pada senyawa asam salsilat diposisi 5, dapat meningkatkan kelarutan pada membran karena dalam senyawa 5–kloro salisilat menjadi senyawa yang bersifat lipofilik (SigmaAldrich, 2020).
2.6.2 Tinjauan Senyawa Asetil Klorida
Gambar 2.6 Struktur Senyawa Asetil Klorida
Struktur pada Gambar 2.6 merupakan senyawa organik turunan dari asam asetat dimana gugus hidroksilnya diganti dengan klor. Senyawa ini berbentuk cair, tidak berwarna, memiliki titik didih 50°-52°C, larut dalam eter, aseton, dan asam asetat, mudah bereaksi dengan air dan alkohol. Asetil klorida mudah terbakar, beracun, korosif terhadap kulit dan menyebabkan iritasi pada mata. Struktur kimia dari asetil klorida yaitu C3H3OCl dengan berat molekul 78.50 g/mol (Sigma Aldrich, 2016).
2.6.3 Tinjauan Aseton
Gambar 2.7 Struktur Senyawa Aseton
Aseton memiliki sifat zat cair yang tidakberwarna, berbau tajam, mudah menguap, mudahterbakar, dan mudah larut dalam pelarut polar dengan struktur kimia C3H6O, memiliki berat molekul 58,08 g/mol dan massa jenisnya 0,79 g/cm³.
Titik didih yang dimiliki yaitu 56,53 °C. Kelarutannya dalam air larut dalam berbagai perbandingan (Sigma Aldrich, 2016).
2.5.4 Tinjauan Triethylamine
Gambar 2.8 Struktur Senyawa Triethylamine (TEA)
Pada Gambar 2.8 memiliki struktur kimia C6H15N dengan berat molekul 101,19 g/mol. Sediaan ini berbentuk cair, tidak berwarna dan berbau seperti amina.
pH dari sediaan ini 12,7 pada 100 g/l dengan suhu 15°C. Memiliki titik lebur -115°C dan titik didih 88,8°C. Kelarutan dalam air 112 g/l pada suhu 20°C. cairan dan uap dari sediaan ini sangat mudah terbakar, bahaya bila ditelan, toksik terhadap kulit, dapat menyebabkan luka bakar kulit yang parah dan juga kerusakan mata. Fatal apabila terhirup dan dapat menyebabkan iritasi pada pernafasan (Sigma Aldrich, 2016).
2.7 Tinjauan Uji Kemurnian Senyawa Hasil Modifikasi 2.7.1 Tinjauan Titik Lebur
Titik lebur adalah temperatur dimana zat padat berubah wujud menjadi zat cair pada tekanan satu atmosfer. Dengan kata lain, merupakan suhu ketika fase padat dan cair sama-sama berada dalam kesetimbangan. Ketajaman jarak titik lebur dipengaruhi oleh beberapa hal, yaitu seperti ukuran kristal kecepatan pemanasan dan karena adanya pengotor lain. Adanya pengotor akan menyebabkan jarak lebur turun dan memperlebar jarak leburnya (O’Bryan, 2009).
Uji jarak lebur menggunakan alat electrothermal melting point apparatus stuart. Alat ini di atur supaya termperatur naik secara perlahan-lahan. Temperatur tersebut di catat apabila mengalami perubahan wujud dari serbuk sampai menjadi cair dan meleleh secara sempurna. Senyawa dikatakan murni apabila memiliki rentang jarak lebur 1-2oC (Ifada, dkk., 2013).
2.7.2 Tinjauan Kromatografi Lapis Tipis
Kromatografi lapis tipis (KLT) digunakan secara luas, umumnya digunakan untuk menentukan efektifitas pemurnian, menentukan banyaknya komponen dalam campuran, dan juga identifikasi senyawa (Gandjar dan Rohman, 2016).
Kromatografi lapis tipis merupakan bentuk kromatografi planar, selain kromatografi kertas dan elektroforesis. Pada KLT, fase diamnya berupa lapisan yang seragam (uniform) pada permukaan bidang datar yang didukung oleh lempeng kaca, pelat aluminium, atau pelat plastic (Rohman, 2007).
Fase gerak pada KLT yang dikenal dengan pelarut pengembang akan bergerak sepanjang fase diam karena pengaruh kapiler pada pengembangan secara menaik (ascending), atau karena pengaruh gravitasi pada pengembangan secara menurun (descending) (Rohman, 2007). Keuntungan KLT sebagai metode pemisahan antara lain sangat mudah dilakukan, peralatan yang digunakan cukup sederhana dan biaya yang relatif terjangkau (Gandjar dan Rohman, 2016).
Pada Kromatografi Lapis Tipis dikenal istilah Rf ( Retardation factor ).
Harga Rf didapat dengan membandingkan jarak yang ditempuh oleh komponen dengan jarak yang ditempuh oleh eluen ( Watson, 2009 ).
Rf = 𝑗𝑎𝑟𝑎𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑚𝑝𝑢ℎ 𝑠𝑜𝑙𝑢𝑡𝑒 𝑗𝑎𝑟𝑎𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑚𝑝𝑢ℎ 𝑠𝑜𝑙𝑣𝑒𝑛𝑡
Keuntungan KLT sebagai metode pemisahan antara lain sangat mudah dilakukan, peralatan yang digunakan cukup sederhana dan biaya yang relatif terjangkau (Gandjar dan Rohman, 2016).
2.8 Tinjauan Identifikasi Struktur 2.8.1 Tinjauan Spektrofotometer UV-Vis
Spektrofotometer UV merupakan salah satu metode yang digunakan dalam penentuan struktur molekul organik, metode ini digunakan karena informasi yang diberikan mengenai adanya struktur terkonjugasi dalam senyawa (McMurry, 2015).
Ultraviolet jauh memiliki rentang panjang gelombang ± 10 – 200 nm, sedangkan ultraviolet dekat memiliki rentang panjang gelombang ± 200-400 nm. Cahaya UV tidak bisa dilihat oleh manusia, namun beberapa hewan, termasuk burung, reptil dan serangga seperti lebah dapat melihat sinar pada panjang gelombang UV.
Interaksi senyawa organik dengan sinar ultraviolet dan sinar tampak, dapat digunakan untuk menentukan struktur molekul senyawa organik. Bagian dari molekul yang paling cepat bereaksi dengan sinar tersebut adalah elektron-elektron ikatan dan elektron-elektron nonikatan (elektron bebas). Sinar ultra lembayung dan sinar tampak merupakan energi, yang bila mengenai elektron-elektron tersebut, maka elektron akan tereksitasi dari keadaan dasar ke tingkat energi yang lebih tinggi, eksitasi elektron-elektron ini, direkam dalam bentuk spektrum yang dinyatakan sebagai panjang gelombang dan absorbansi, sesuai dengan jenis elektron-elektron yang terdapat dalam molekul yang dianalisis (Suhartati, 2017).
Spektrofotometri UV-Visible dapat digunakan untuk penentuan terhadap sampel yang berupa larutan, gas, atau uap. Pada umumnya sampel harus diubah menjadi suatu larutan yang jernih untuk sampel yang berupa larutan perlu diperhatikan beberapa persyaratan pelarut yang dipakai antara lain: 1. Harus melarutkan sampel dengan sempurna. 2. Pelarut yang dipakai tidak mengandung ikatan rangkap terkonjugasi pada struktur molekulnya dan tidak berwarna (tidak boleh mengabsorpsi sinar yang dipakai oleh sampel) 3. Tidak terjadi interaksi dengan molekul senyawa yang dianalisis 4. Kemurniannya harus tinggi (Suhartati, 2017).
2.8.2 Tinjauan Spektrofotometer Inframerah (IR)
Spektrofotometer Inframerah (IR) adalah salah satu alat yang digunakan untuk menganalisa senyawa kimia. Spektra IR dapat dihasilkan dengan mengukur absorbsi radiasi, refleksi atau emisi di daerah IR. Penggunaan spektrofotometer IR berdasarkan pada perbedaan molekul dalam menyerap radiasi inframerah yang diinterpretasikan dalam kenaikan amplitudo getaran pada atom-atom yang terikat atau dalam keadaan vibrasi tereksitasi sehingga suatu senyawa akan membentuk sidik jari yang unik pada daerah sidik jari yaitu pada 1500 cm-1 sampai 400 cm-1. Dengan mempelajari absorbs yang terjadi terhadap gugus fungsi tertentu, maka
kemungkinan akan didapatkan informasi tentang struktur senyawa dari spektra IR (McMurry, 2015).
2.8.3 Tinjauan Spektrometer Resonansi Magnet Inti 1H-NMR
Spektrofotometer NMR (Nuclear Magnetic Resonance) merupakan metode penentuan struktur paling bernilai dalam kimia organik. Metode ini dilakukan dengan mapping terhadap kerangka molekul hydrogen dari suatu senyawa (McMurry, 2015). Spektroskopi ini didasarkan pada setiap kelompok proton (H) dalam molekul organikyang akan beresonansi pada frekuensi yang tidak identik atau beresonansi pada frekuensi spesifik. Hal ini disebabkan karena kelompok proton suatu molekul dikelilingi oleh electron yang berbeda (lingkungan elektroniknya berbeda). Semakin besar kerapatan elektron yang mengelilingi inti maka semakin besar pula medan magnet yang digunakan. Karena pada setiap atom proton (H) suatu molekul organik mempunyai lingkungan elektronik (kimia) yang berbeda makan akan menyebabkan frekuensi resonansi berbeda (Sitorus, 2009).
2.9 Tinjauan Metode Uji Aktivitas Analgesik
2.9.1 Tinjauan Metode Stimulasi Kimia (Writhing test)
Metode Writhing Test dilakukan dengan cara menginduksi nyeri untuk memberikan respon geliat. Metode ini sering digunakan untuk skrining obat analgesik yaitu dengan cara menyuntikkan ke dalam rongga perut hewan, adanya respon geliat merupakan kontraksi dari perut hewan dan juga berkurangnya aktivitas motorik. Rasa nyeri pada mencit diperlihatkan dengan respon gerakan menggeliat yaitu kedua pasang kaki kiri ke depan dan ke belakang serta perut menekan lantai (Tasleem et al., 2014).
2.9.2 Tinjauan Metode Stimulasi Listrik
Metode ini dilakukan untuk menimbulkan respon rasa nyeri. Prinsip kerjanya yaitu dengan cara ekor hewan diletakkan pada tempat yang dapat dialiri listrik, kemudian diberi aliran listrik. Respon yang akan diberikan oleh hewan setelah ekor dialiri dengan aliran listrik yaitu akan menunjukkan gerakan atau cicitan. Arus listrik dapat ditingkatkan dengan kekuatan analgesik yang diberikan. Metode ini dapat dilakukan terhadap kera, anjing, kucing, kelinci, tikus, dan mencit (Manihuruk, 2000).
2.9.3 Tinjauan Metode Stimulasi Panas
Metode Panas (Hot plate) dilakukan dengan cara meletakkan mencit ke dalam hot plate yang telah ditentukan suhunya. Waktu dihitung mulai dari mencit dimasukkan ke dalam hot plate sampai mencit memberikan respon berupa meloncat, menarik telapak kaki, dan menjilat telapak kaki (Cannon, 2007). Zat yang diujikan diharapkan dapat merubah nilai ambang batas yang ada sehingga terjadi kemungkinan keseringan untuk menjilat atau melompat jadi bertambah atau bisa juga berkurang (Vogel,2006).
2.9.4 Tinjauan Metode Stimulasi Tekanan (Tail flick)
Metode Tail flick Test menggunakan panas sebagai penginduksi nyeri. Rasa nyeri diperlihatkan dalam bentuk respon yaitu gerakan pada mencit yang menjentikkan ekor ketika ekor mencit diinduksi panas dengan air pada penangas suhu 50±2°C. Suhu diatas 48°C dapat menyebabkan perangsangan kuat pada reseptor nyeri sehingga menghasilkan sensasi nyeri yang hebat (Nair dan Peate, 2015). Waktu yang dibutuhkan oleh mencit untuk menjentikkan ekornya kemudian diukur (Goyal el al., 2013).
2.10 Tinjauan Penentuan ED50
ED50 adalah dosis efektif yang menghasilkan respons tertentu pada 50%
hewan coba dalam kelompok. Nilai ED50 berbeda-beda untuk setiap cara pemberiannya. Apabila responnya adalah kematian, maka ED50 menjadi LD50 atau dosis kematian untuk 50% hewan coba. ED50 dan LD50 dapat dihitung dengan metode grafik. Nilai ED50 pada efek akan akan bertingkat yang diperoleh dengan cara mengukur efek obat pada dosis yang bervariasi. Dosis yang digunakan pada umumnya berkelipatan dua (Siswandono dan Soekardjo, 2016).