KUALITAS SPERMATOZOA CAUDA EPIDIDIMIDIS SAPI
PERANAKAN ONGOLE (PO) SETELAH PENYIMPANAN
EPIDIDIMIS PADA 5
°C
(Quality of Cauda Epididymides Spermatozoa of Ongole Crossbred Bull
after Epididymal Storage at 5
°C
NURCHOLIDAH SOLIHATI1,E.W.ADIKARTA1,R.SETIAWAN1,DIAN A.YANI1danM.RIZAL2
1
Fakultas Peternakan Universitas Padjadjaran Bandung 2
Fakultas Pertanian Universitas Pattimura Ambon
ABSTRACT
The purpose of this research was to examine the quality of PO bull epididymal sperm collected from fresh
cauda epididymides (H-O) or after storage in low temperature (5°C, in refrigerator) for one (H-1), two (H-2),
and three (H-3) days. Collected-sperm were diluted with fisiological NaCl then centrifuged at 3000 rpm for 20 minutes. The supernatant was removed and sperm was diluted with Tris-Egg Yolk extender. Quality of collected-sperm including motility, percentage of live sperm, abnormality, and intact plasma membrane (IPM). This research was designed by using completely randomized design (CRD) with four treatments and six replications. Data was analyzed by using ANOVA, and the difference between treatments were tested by Duncan's Multiple Range Test. It was concluded that storage of epididymides significantly affected motility, percentage of live sperm, intact plasma membrane (IPM), and abnormality. Spermatozoa that was collected from cauda epididymides of slaughtered PO bull could be used for artificial insemination (AI) programs as long as epididymal storage not more than two days.
Key Words: Epididymal Storage, Quality of Sperma, PO Bull
ABSTRAK
Tujuan penelitian ini yaitu menguji kualitas spermatozoa cauda epididimidis sapi PO yang dikoleksi dari epididimis segar (H-O) atau epididimis yang telah disimpan di dalam lemari es (suhu SOC) selama satu (H-I), dua (H-2) dan tiga (H-3) hari. Spermatozoa dikoleksi dengan cara membuat sayatan-sayatan pacta cauda epididimidis kemudian dibilas-tekan dengan larutan NaCl fisiologis. Spermatozoa hasil koleksi disentrifugasi dengan kecepatan 3000 rpm selama 20 menit, supernatan dibuang dan spermatozoa diencerkan dengan pengencer Tris - Kuning Telur. Penilaian kualitas spermatozoa meliputi konsentrasi, motilitas, persentase spermatozoa hidup, abnormalitas dan membran plasma utuh (MPU). Penelitian ini dirancang menggunakan Rancangan Acak Lengkap (RAL), dengan empat perJakuan dan enam kali ulangan. Data yang diperoleh dianalisis menggunakan Sidik Ragam, perbedaan antar perlakuan diuji menggunakan Uji Jarak Berganda Duncan. Disimpulkan bahwa penyimpanan epididimis pada 5°C berpengaruh nyata terhadap motilitas, persentase spermatozoa hidup, membran plasma utuh (MPU) dan abnormalitas; Spermatozoa yang dikoleksi dari cauda epididimidis sapi PO yang telah dipotong memenuhi persyaratan kualitas untuk digunakan dalam program inseminasi buatan (IB) sampai dengan penyimpanan epididimis selama dua hari.
Kata Kunci: Penyimpanan Epididimidis, Kualitas Spermatozoa, sapi PO
PENDAHULUAN
Cauda epididimidis merupakan sumber
alternatif spermatozoa yang belum banyak mendapatkan perhatian. Spermatozoa yang berasal dari cauda epididimidis telah mengalami pematangan pada bagian caput
epididimidis dan corpus epididimidis, sehingga diharapkan memiliki kualitas yang sama dengan spermatozoa yang dikoleksi dari semen hasil ejakulasi. Apabila terjadi kematian ternak unggul secara mendadak dan jauh dari tempat pengolahan semen, maka penyimpanan cauda epididimidis menjadi solusi dalam upaya
pelestarian sumber genetik unggul yang dimiliki sapi jantan tersebut.
Hasil percobaan awal yang dilakukan penulis dkk. menunjukkan bahwa spermatozoa hasil koleksi dari cauda epididimidis sapi PO segera setelah pemotongan (± 1 jam) layak untuk diolah menjadi semen cair dan semen beku, dengan nilai rata-rata konsentrasi total sekitar 4.000 juta sel/ml, motilitas ≥ 70%, membran plasma utuh (MPU) > 80% dan abnormalitas 13%. Semen yang layak digunakan dalam program inseminasi buatan (IB) harus memiliki persentase motilitas spermatozoa paling sedikit sebesar 40% (TOELIHERE, 1993; HAFEZ dan HAFEZ, 2000) dan MPU spermatozoa segar tidak kurang dari 60% (REVELL dan MRODE, 1994).
Permasalahan yang dihadapi adalah bagaimanakah kualitas sperma cauda epididimidis yang diperoleh dari epididimis yang telah mengalami penyimpanan pada suhu 5oC. Tujuan penelitian ini yaitu menguji kualitas spermatozoa cauda epididimidis sapi PO yang dikoleksi dari epididimis segar dan dari epididimis yang telah disimpan di dalam lemari es (suhu 5oC), sehingga diharapkan dapat diketahui sampai berapa lama epididimis dapat disimpan supaya dapat mempertahan kualitas spermatozoa cauda epididimidis yang layak digunakan untuk IB.
MATERI DAN METODE
Materi penelitian yang digunakan adalah epididimis sapi PO sebanyak 24 buah dari 24 ekor sapi yang dipotong di rumah pemotongan hewan (RPH). Pengambilan epididimis dilakukan segera setelah sapi dipotong. Epididimis dipisahkan dari testis dengan menggunakan gunting steril dan dimasukkan ke dalam toples yang berisi larutan NaCl fisiologis untuk dibawa ke laboratorium dan disimpan di lemari es pada suhu 5oC sesuai dengan perlakuan lama penyimpanan epididimis.
Koleksi spermatozoa dari cauda epididimidis
Koleksi spermatozoa cauda epididimidis dilakukan dengan cara memotong bagian
cauda dari epididimis, lalu disayat dengan
menggunakan gunting steril sampai terlihat
cairan kental berwarna putih (sperma) yang keluar dari cauda epididimidis tersebut dan teteskan pada cawan petri, lalu hisap dengan menggunakan pipet haemocytometer. Segera setelah itu lakukan penghitungan konsentrasi total (keadaan segar). Cauda epididimidis yang telah disayat kemudian dibilas-tekan dengan menggunakan larutan NaCl fisiologis, selanjutnya larutan spermatozoa tersebut disimpan di dalam tabung reaksi, kemudian disentrifugasi dengan kecepatan 3000 rpm selama 20 menit. Supernatan dibuang dan bagian yang mengendap merupakan spermatozoa yang akan dievaluasi.
Perlakuan yang dicobakan
Perlakuan yang dicobakan dalam penelitian ini adalah lama penyimpanan epididimis pada suhu 5°C, yaitu:
1. Sperma langsung dikoleksi dari cauda epididimidis langsung segera setelah ternak dipotong (±1 jam): H-0
2. Sperma dikoleksi dari cauda epididimidis setelah epididimis disimpan selama satu hari (24 jam): H-1
3. Sperma dikoleksi dari cauda epididimidis setelah epididimis disimpan selama dua hari (48 jam): H-2
4. Sperma dikoleksi dari cauda epididimis setelah epididimis disimpan selama tiga hari (72 jam) : H-3
Pengenceran
Spermatozoa hasil koleksi kemudian diencerkan dengan menggunakan larutan Tris kuning telur kemudian dievaluasi.
Rancangan percobaan dan analisis data
Penelitian ini menggunakan metode eksperimental dengan Rancangan Acak Lengkap, terdiri dari 4 perlakuan dan 6 kali ulangan. Setiap ulangan menggunakan satu buah epididimidis, sehingga setiap perlakuan menggunakan enam ekor sapi. Parameter yang diukur adalah kualitas spermatozoa, terdiri dari motilitas (%), spermatozoa hidup (%), membran plasma utuh (MPU) (%), dan abnormalitas (%).
HASIL DAN PEMBAHASAN
Kualitas spermatozoa cauda epididimidis sapi PO berdasarkan lama penyimpanan epididimis disajikan pada Tabel 1.
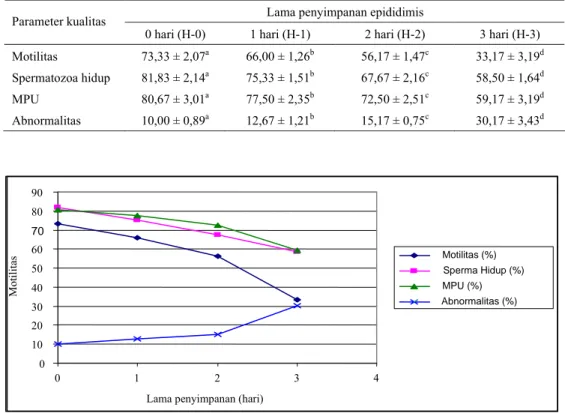
Berdasarkan Tabel 1. tampak bahwa terjadi penurunan kualitas seiring bertambahnya lama penyimpanan. Gambaran penurunan kualitas spermatozoa cauda epididimidis diperlihatkan pada Gambar 1.
Tabel 1. Kualitas sperma cauda epididimidis sapi PO berdasarkan lama penyimpanan epididimis Lama penyimpanan epididimis
Parameter kualitas
0 hari (H-0) 1 hari (H-1) 2 hari (H-2) 3 hari (H-3) Motilitas 73,33 ± 2,07a 66,00 ± 1,26b 56,17 ± 1,47c 33,17 ± 3,19d
Spermatozoa hidup 81,83 ± 2,14a 75,33 ± 1,51b 67,67 ± 2,16c 58,50 ± 1,64d
MPU 80,67 ± 3,01a 77,50 ± 2,35b 72,50 ± 2,51c 59,17 ± 3,19d
Abnormalitas 10,00 ± 0,89a 12,67 ± 1,21b 15,17 ± 0,75c 30,17 ± 3,43d
Gambar 1. Kualitas spermatozoa cauda epididimidis sapi PO berdasarkan lama penyimpanan epididimis
Motilitas yang tertinggi diperoleh dari perlakuan H-0 (73%) diikuti berturut-turut oleh perlakuan H-1 (66%), H-2 (56%), dan H-3 (33,17%). Hasil analisis sidik ragam menunjukkan bahwa perlakuan lama penyimpanan epididimis berpengaruh nyata (P < 0,05) terhadap motilitas sperma cauda epididimidis. Hasil uji jarak berganda Duncan menyatakan bahwa motilitas perlakuan H-0 nyata (P<0,05) lebih tinggi daripada perlakuan H-1, H-2 dan H-3. H-1 nyata lebih tinggi daripada H-2 dan H-3, serta H-2 nyata lebih tinggi daripada H-3.
Motilitas sperma cauda epididimidis menurun seiring bertambahnya lama penyimpanan. Hal ini disebabkan karena daya
hidup sel-sel gamet dipengaruhi oleh lama dan suhu tempat hewan tersebut mati sebelum gamet dikoleksi. Semakin lama penyimpanan epididimis, akan semakin menurunkan kualitas senyawa-senyawa yang terdapat di dalam cairan cauda epididimidis yang berfungsi mendukung kelangsungan hidup sperma.
Terjadinya penurunan kualitas sperma seiring dengan bertambahnya waktu penyimpanan epididimis pada suhu 5oC diduga disebabkan kondisi lingkungan mikro cauda epididimidis mengalami perubahan dari kondisi alami seperti yang terjadi pada hewan hidup. Kondisi lingkungan mikro yang dimaksud bukan hanya faktor suhu, tetapi seluruh kondisi fisiologik di dalam epididimis
0 10 20 30 40 50 60 70 80 90 0 1 2 3 4
Lama penyimpanan (hari)
Motilitas (%) Sperma Hidup (%) MPU (%) Abnormalitas (%) Mot ilitas
akan mengalami perubahan. Semakin lama penyimpanan epididimis akan semakin menurunkan kualitas seluruh senyawa-senyawa kimia yang ada di dalamnya, yang pada akhirnya menurunkan daya preservasinya terhadap sperma yang terkandung di dalam
cauda epididimidis. Dengan demikian, sperma
akan mengalami proses degenerasi, baik morfologi maupun fungsional selama berada di dalam epididimis setelah hewan tersebut mati. Menurut BEARDEN dan FUQUAY (1997) kondisi ideal yang terjadi di dalam cauda epididimidis pada hewan yang masih hidup merupakan perpaduan dari hasil kerja sekian banyak mekanisme yang kompleks, yang tidak mungkin dapat dipenuhi pada perlakuan penyimpanan epididimis secara in vitro. Hasil penelitian NAZLIE (2004) menunjukkan bahwa
kerusakan sel-sel yang menyusun cauda epididimidis kucing mulai terjadi pada hari kedua setelah penyimpanan epididimis pada suhu 4oC, dan kerusakan semakin meluas seiring dengan bertambahnya waktu penyimpanan. Hal ini juga mengindikasikan bahwa kualitas senyawa-senyawa kimia yang terkandung di dalam cauda epididimidis menurun seiring dengan bertambahnya waktu penyimpanan. Dengan demikian, kemampuan senyawa-senyawa kimia tersebut dalam mempreservasi sperma juga mengalami penurunan dan menyebabkan kualitas sperma menurun. Beberapa penelitian melaporkan bahwa persentase sperma motil asal cauda epididimidis setelah diencerkan sebesar 50 – 80% pada domba (SENGER, 1999), 70,83%
pada domba garut (RIZAL, 2004), 70 – 75%
pada badak (LUBBE et al., 1999), 38 – 77% pada kuda (SQUIRES et al., 2000), rata-rata 64% pada monyet ekor panjang (FERADIS et
al., 2001), 57,6% pada rusa merah (SOLER et
al., 2003), 78 – 77% pada kuda (SQUIRES et al.,
2000), 51,7% pada sapi (BRANTON, 1946
dalam SALISBURY dan VANDEMARK, 1985)
dan 48,7% (GOOVAERTS et et al., 2006).
Pada suhu 5oC aktivitas metabolisme yang diukur dengan perubahan-perubahan kimia akan berkurang, namun masih tetap berlangsung (SALISBURY dan VANDEMARK,
1985). Pada penelitian ini penyimpanan cauda epididimidis sapi PO suhu 5oC menghasilkan motilitas yang masih layak untuk IB hingga penyimpanan selama dua hari, karena standar motilitas yang banyak digunakan dalam
program IB harus memiliki persentase motilitas paling sedikit sebesar 40% (TOELIHERE, 1993). Setelah dua hari penyimpanan epididimis, motilitas sperma
cauda epididimidis sapi PO tidak layak untuk
IB karena motilitas yang didapat kurang dari 40%. Hal ini disebabkan pendinginan semen dari suhu tubuh ke suhu lemari es dapat menyebabkan sperma kehilangan motilitas secara gradual sampai pergerakan terhenti sama sekali (TOELIHERE, 1993).
Sperma hidup tertinggi diperoleh dari perlakuan H-0 (81,83%) diikuti berturut-turut oleh perlakuan H-1 (75,33%), H-2 (67,66%), dan H-3 (58,50%). Hasil analisis sidik ragam menyatakan bahwa perlakuan lama penyimpanan epididimis berpengaruh nyata (P < 0,05) terhadap jumlah sperma hidup cauda epididimidis. Hasil uji jarak berganda Duncan menyatakan bahwa motilitas perlakuan H-0 nyata (P < 0,05) lebih tinggi daripada perlakuan H-1, H-2 dan H-3. Perlakuan H-1 nyata lebih tinggi daripada H-2 dan H-3, serta H-2 nyata lebih tinggi daripada H-3.
Jumlah sperma hidup di dalam epididimis hewan yang telah mati akan mengalami penurunan seiring dengan bertambahnya waktu dan suhu lingkungan. Banyaknya sperma yang mati juga akan menjadi racun bagi sperma yang masih hidup selama proses penyimpanan. Menurut SOLER et al. (2003) daya hidup sel-sel
gamet dipengaruhi oleh periode waktu dan suhu tempat hewan tersebut mati sebelum gamet dikoleksi. Walaupun menurut GARDE et
al. (1998) sperma cauda epididimidis rusa
merah masih memiliki daya hidup yang baik setelah setelah rusa tersebut mati dan dibiarkan pada suhu ruang (sekitar 20oC) selama 24 jam. Lebih lanjut dilaporkan bahwa sperma cauda epididimidis domba mouflon yang dikoleksi dari hewan yang telah mati selama 40 jam masih memiliki kemampuan membuahi oosit secara in vivo. Menurut NAZLIE (2004) semakin
lama penyimpanan epididimis semakin meluas kerusakan pada sel-sel penyususun epididimis, yang berakibat menurunnya daya preservasi epididimis terhadap sperma yang terkandung di dalamnya. Dengan demikian sperma akan mengalami proses degenerasi baik morfologi maupun fungsional selama berada di dalam epididimidis setelah hewan tersebut mati.
Membran plasma utuh (MPU) diperoleh dari perlakuan H-0 (80,67%) diikuti
berturut-turut oleh perlakuan H-1 (77,5%), H-2 (72,5%), dan H-3 (59,17%). Hasil analisis sidik ragam menyatakan bahwa perlakuan lama penyimpanan epididimis berpengaruh nyata (P < 0,01) terhadap terhadap jumlah sperma hidup
cauda epididimidis. Hasil uji berganda Duncan
menyatakan bahwa motilitas perlakuan H0 nyata (P < 0,05) lebih tinggi daripada perlakuan H-1, H-2 dan H-3. H-1 nyata lebih tinggi daripada H-2 dan H-3, serta H-2 nyata lebih tinggi daripada H-3.
Hal yang menyebabkan menurunnya kualitas membran plasma sperma cauda epididimidis yaitu karena membran plasma sperma cauda epididimidis tidak mendapatkan perlindungan berupa glikoprotein yang disintesis oleh kelenjar vesikularis. Glikoprotein ini sangat penting dalam melindungi keutuhan membran plasma sperma dari kerusakan akibat pengaruh kejutan dingin dan serangan radikal bebas akibat kontak dengan oksigen saat sperma dikoleksi (NOLAN
dan HAMMERSTEDT, 1997). Hal ini
menyebabkan menurunnya daya hidup sperma dan meningkatnya persentase reaksi akrosom yang prematur akibat rusaknya membran plasma sperma.
NOLAN dan HAMMERSTEDT (1997) menyatakan bahwa sperma yang terdapat di dalam cauda epididimidis yang disimpan pada suhu 5oC akan mengalami perubahan susunan komponen senyawa-senyawa penyusun membran plasma sperma. Membran plasma sperma akan kehilangan sebagian kolesterol, sehingga terjadi peningkatan nisbah antara asam lemak tak jenuh dan kolesterol. Hal ini menyebabkan membran plasma menjadi lebih “rapuh” (fragile) dan produksi ATP juga menurun, sehingga mengganggu motilitas sperma karena sumber energi (ATP) tidak tersedia dengan cukup. Larutan NaCl sebagai media penyimpanan epididimis rupanya tidak cukup mampu menyediakan energi untuk sperma dalam waktu yang lama. Pada penelitian ini nilai MPU yang masih layak untuk IB diperoleh sampai hari kedua sedangkan pada hari ketiga nilai MPU tidak memenuhi syarat karena nilai MPU yang diperoleh 59,17%. Menurut REVELL dan
MRODE (1994), nilai MPU semen segar yang kurang dari 60% dikategorikan sebagai semen yang infertil.
Abnormalitas terendah yang diperoleh dari perlakuan H-0 (10,00%) diikuti berturut-turut oleh perlakuan H-1 (12,67%), H-2 (15,17%), dan H-3 (30,17%). Hasil analisis sidik ragam menyatakan bahwa perlakuan lama penyimpanan epididimis berpengaruh nyata (P < 0,05) terhadap jumlah sperma hidup cauda epididimidis. Hasil uji berganda Duncan menyatakan bahwa abnormalitas perlakuan H-0 nyata (P < H-0,H-05) lebih rendah daripada perlakuan H-1, H-2 dan H-3. H-1 nyata lebih rendah daripada H-2 dan H-3, serta H-2 nyata lebih rendah daripada H-3.
Pada penyimpanan epididimis secara in
vitro di dalam lemari es, kondisi lingkungan
mikro cauda epididimidis mengalami
perubahan dari kondisi alami seperti yang terjadi pada hewan hidup. Kondisi mikro ini memang tidak dapat dikontrol sehingga tercipta lingkungan yang persis sama dengan kondisi alami epididimis hewan hidup. Pada kondisi penyimpanan epididimis secara in vitro pada suhu 5oC diduga bahwa seluruh mekanisme fisiologik yang kompleks tidak akan berjalan lagi sebagaimana yang terjadi pada hewan hidup. Dengan tidak berjalannya mekanisme fisiologik sebagaimana mestinya, akan berpengaruh buruk terhadap integritas sperma. Abnormalitas sperma pun disebabkan karena adanya gangguan dalam proses produksi sperma (spermatogenesis) di dalam tubuli seminiferi testis serta kerusakan selama koleksi dan pengolahan semen.
Pada penelitian ini nilai abnormalitas sperma cauda epididimidis sapi PO yang masih layak untuk IB diperoleh sampai hari ke-2 dengan rata-rata nilai <20%, karena abnormalitas pada hari ketiga lebih dari 30%. Menurut TOELIHERE (1993), apabila
abnormalitas sperma lebih dari 20% maka sperma tersebut tidak layak untuk inseminasi. Pendapat lain dikemukakan oleh PARTODIHARDJO (1992), yang menyatakan
bahwa apabila abnormalitas sperma sampai 25% belum berpengaruh terhadap fertilitas sperma, artinya masih baik untuk diinseminasikan. Semakin lama waktu penyimpanan maka semakin tinggi persentase abnormalitas. Kejadian ini disebabkan oleh kejutan suhu dingin dan ketidakseimbangan tekanan osmotik akibat dari proses metabolik yang terus berlangsung selama penyimpanan
pada 5oC. Hasil akhir proses metabolik dalam suasana anaerob adalah asam laktat.
Pada penelitian ini, abnormalitas sperma yang ditemukan didominasi oleh abnormalitas sekunder, seperti: kepala tanpa ekor, ekor terputus dan ekor melingkar. Abnormalitas ini diduga terjadi pada saat pengolahan sperma dan pembuatan preparat ulas untuk pemeriksaan abnormalitas sperma.
KESIMPULAN DAN SARAN
Berdasarkan hasil penelitian yang telah dilakukan, secara umum dapat disimpulkan sebagai berikut:
1. Perlakuan penyimpanan epididimis sapi PO pada suhu 5oC berpengaruh nyata (P < 0,05) terhadap motilitas, persentase sperma hidup, persentase MPU dan abnormalitas sperma. 2. Motilitas spermatozoa cauda epididimidis
dapat dipertahankan sampai minimal 40% pada penyimpanan epididimis hingga dua hari di dalam larutan NaCl fisiologis pada suhu 5oC.
Penyimpanan epididimidis sebagai sumber spermatozoa hendaknya tidak lebih dari dua hari agar memperoleh kualitas spermatozoa yang layak untuk IB.
DAFTAR PUSTAKA
BEARDEN,H.J. and J.W.FUQUAY. 2000. The Male
Reproductive System. In: Applied Animal
Reproduction, 5th Edition. Prentice Hall, New
Jersey. p. 29.
FERADIS,D.PAWITRI,I.K.SUATHA,M.RIZAL AMIN, T.L.YUSUF,D.SAJUTHI,I.N.BUDIARSA and
E.S. HAYES. 2001. Cryopreservation of epididymal spermatozoa collected by needle biopsy from cynomolgus monkeys (Macaca fascicularis). J. Med.. Primatol. 30: 100 – 106. GARDE,J.,E.ANEL,A.GARCIA-DIAZ,J.C.BOIXO,A. SOLER.,P.DE PAZ,A.LOPEZ-SAEZ,C.GUERRA
and L. ANEL. 2000. Evaluation of two glycerol concentrations in freezing of electroejaculated and epididymal spermatozoa from Iberian red deer (Cervus elaphus
hispanicus). Proc. 14th International Congress
on Animal Reproduction. Stockholm, 2 – 6
July 2000. 17: 14, p. 142. Abstract Vol. 2.
GOOVERTS,I.G.,G.G.HOFLACK and A.VAN SOOM.
2006. Evaluation of Epididiymal Semen Quality Using the Hamilton-Thorne Analyser Indicates Variation Between the two Caudae Epididymides of the Same Bull.
Theriogenology. 15; 66(2): 323 – 330.
HAFEZ, E.S.E. 2000. Preservation and
Criopreservation of Gamets and Embrios. In:
Reproduction in Farm Animals. 7th Ed. HAFEZ,
B. and E.S.E. HAFEZ (Eds.). Lippincott
Williams and Wilkins. Philadelphia. pp. 432 – 441.
LUBBE, K., R.L. SMITH, P. BARTELS and R.A.
GODKE. 1999. Freezing epididymal sperm
from white rhinoceros (Ceratotherium simum) treated with different cryodiluents.
Theriogenology. 51: 288 (Abstract).
NAZLIE, C.S. 2004. Kajian Kualitas Spermatozoa Kucing Asal Epididimis dan Ductus Deferens Setelah Proses Preservasi Selama 7 Hari pada Suhu 4oC. Tesis. Sekolah Pascasarjana,
Institut Pertanian Bogor, Bogor.
NOLAN, J.P. and R.H. HAMMERSTEDT. 1997.
Regulation of membrane stability and the acrosome reaction in mammalian sperm. FASEB J. 11: 670 – 682.
PARTODIHARDJO,S. 1980. Ilmu Reproduksi Hewan.
Mutiara. Jakarta. hlm. 33 – 36.
REVELL,S.G. and R.A.MRODE. 1994. An osmotic
resistance test for bovine semen. Animal
Reproduction Sci. 36: 77 – 86.
RIZAL, M. 2004. Pengaruh Waktu Penyimpanan
Epididimis pada Suhu 5°C Terhadap Kualitas Spermatozoa Epididimis Domba Garut. J.
Veteriner. 5(3): 95 – 103.
SALISBURRY, G.W. and N.L. VANDEMARK. 1985.
Fisiologi Reproduksi dan Inseminasi Buatan pada Sapi. Yogyakarta: Gadjah Mada University
Press. hlm. 207 – 210, 243.
SENGER,P.L. 1999. The organization and function of the male reproduction system. In: Pathways to Pregnancy and Parturition. Current Conception, Inc., Pullman. pp. 32 – 57.
SOLER,A.J.,M.D.PEREZ GUZMAN and J.J.GARDE. 2003. Storage of red deer epididymides for four days at 5oC: Effects on Sperm Motility,
Viability, and Morphology Integrity. J. Exp.
SQUIRES E.L., C. GOMEZ-CUETARA and J.K.
GRAHAM. 2000. Effect of seminal plasma on cryopreserving epididymal and ejaculated stallion spermatozoa. Proc. 14th International
Congress on Animal Reproduction.
Stockholm, 2 – 6 July 2000. 17: 38, p. 166. Abstract Vol. 2.
TOELIHERE, M.R. 1993. Inseminasi Buatan Pada
Ternak. Angkasa. Bandung. hlm. 50 – 60, 98 –