PENGARUH PEMBERIAN MADU HUTAN TERHADAP AKTIVITAS DAN KAPASITAS FAGOSITOSIS MAKROFAG PADA HEWAN UJI
TIKUS JANTAN GALUR WISTAR
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Perthy Melati Kasih
NIM : 088114004
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENGARUH PEMBERIAN MADU HUTAN TERHADAP AKTIVITAS DAN KAPASITAS FAGOSITOSIS MAKROFAG PADA HEWAN UJI
TIKUS JANTAN GALUR WISTAR
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh : Perthy Melati Kasih
NIM : 088114004
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
LEMBAR PERSEMBAHAN
Kebahagiaan dapat ditemukan, bahkan di saat-saat paling
kelam, asalkan seseorang ingat untuk menghidupkan sisi
terangnya.
-J.K.
Rowling-Sebuah karya kecil kupersembahkan kepada :
TUHAN YESUS KRISTUS sebagai wujud rasa syukurku.
Mamah Yukesih & Papah Medio
, ungkapan terima kasih, cinta, dan sayangku.
Tanpa kalian aku tidak bisa menjadi seperti ini, kalian tidak pernah lelah dan bosan untuk selalu mengingatkan dan mendengar keluh kesahku. Kalianlah orang yang paling setia menemaniku saat kuatku dan lemahku. Tidak akan ada yang bisa membalas semua jasa kalian.
Adikku
Curtina Melati Kasih
sebagai tanda sayangku dan motivasi buatmu.
Yohanes Hermawan
yang selalu menghadirkan cinta dan kebahagiaan dalam hidupku.
Seorang
sahabat
yang selalu memberi warna dan rasa tersendiri dalam hidupku.
vi
PRAKATA
Puji syukur dan terima kasih penulis panjatkan kepada Sang Maha Kasih Tuhan Yesus Kristus, atas segala berkat dan anugerah-Nya yang Ia limpahkan sehingga penulis dapat menyelesaikan skripsi ini. Skripsi dengan judul “Pengaruh Pemberian Madu Hutan terhadap Aktivitas dan Kapasitas Fagositosis Makrofag pada Hewan Uji Tikus Jantan Galur Wistar” merupakan karya ilmiah penulis untuk memenuhi syarat memperoleh gelar Sarjana Farmasi (S. Farm.) di Fakultas Farmasi Universitas Sanata Dharma.
Penulis mengucapkan terima kasih kepada semua pihak yang telah ikut membantu, memberikan dukungan, bimbingan, kritik, dan saran selama proses penyelesaian skripsi ini. Semoga kebaikan yang telah diberikan dibalas oleh Tuhan yang Maha Kuasa. Dalam kesempatan ini penulis mengucapkan terima kasih kepada :
1. Bapak Ipang Djunarko, M.Sc., Apt selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Yunita Linawati, M.Sc., Apt selaku Dosen Pembimbing dan Dosen Penguji yang telah banyak memberi bimbingan, arahan, dan masukan dalam penyusunan skripsi ini sehingga dapat menjadi lebih baik.
3. Bapak Prof. Dr. C.J. Soegihardjo, Apt selaku Dosen Penguji yang telah m em berikan m asukan yan g berart i terhadap skripsi ini.
4. Bapak Drs. Ag. Yuswanto, S.U., PhD, Apt selaku Dosen Penguji yang telah m em berikan kri t ik sert a saran terhadap skripsi ini.
5. Ibu C.M. Ratna Rini Nastiti, M.Pharm., Apt selaku Ketua Program Studi sekaligus Ketua Tim Panitia Skripsi Fakultas Farmasi Universitas Sanata Dharma.
6. Pimpinan dan staff LPPT UGM : Ibu Istini dan Pak Sutari yang telah mengijinkan penulis untuk melakukan penelitian serta membantu selama masa penelitian.
vii
8. Para sahabat yang tak pernah bosan menjadi tempat berbagi tawa dan air mata : Mezcovits Team, Adityawarman, Primaboti Nurwidaningrum, Christina Putranti Rose Widani, Wiria Sende Paiman, Eureka Gracia Letitia, Agatha Novita Ika Hayuningtyas, Ketut Ary Widiasih, Liani, Alfonsus Rosario Heppy Dwi Yoga, Incipit Vita Nova Marthadiwangsa dan Brigita Ivana Amanda Susilo.
9. Teman-teman angkatan 2008, khususnya FKK A 2008 yang sudah mengajarkan aku untuk menertawakan hidup.
Semua pihak yang tidak dapat penulis sebutkan satu persatu, yang telah membantu dalam kelancaran penyelesaian skripsi ini.
Penulis menyadari bahwa skripsi ini jauh dari sempurna. Oleh karena itu, segala kritik dan saran yang membangun sangat penulis harapkan demi sempurnanya skripsi ini. Semoga skripsi ini dapat bermanfaat dan memberi informasi bagi pembaca.
ix
DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
HALAMAN PERSETUJUAN PUBLIKASI ... v
PRAKATA ... vi
PERNYATAAN KEASLIAN KARYA ... viii
DAFTAR ISI ... ix
2. Keaslian penelitian... 3
3. Manfaat penelitian ... 3
BAB II. PENELAAHAN PUSTAKA... 5
A.Madu ... 5
B.Sistem Imun ... 8
C.Makrofag ... 11
D.Imunomodulator ... 13
x
F. Hipotesis ... 15
BAB III. METODE PENELITIAN... 16
A.Jenis dan Rancang Penelitian ... 16
B.Variabel dan Definisi Operasional ... 17
1. Variabel penelitian ... 17
2. Definisi operasional ... 17
C.Bahan Penelitian ... 18
1. Bahan utama ... 18
2. Hewan uji ... 18
3. Bahan untuk uji fagositosis makrofag ... 18
D.Alat Penelitian ... 18
1. Preparasi sampel ... 18
2. Pengujian aktivitas dan kapasitas fagositosis makrofag ... 19
E. Tata Cara Penelitian ... 19
1. Tahap penentuan dosis madu hutan ... 19
2. Tahap praperlakuan hewan uji ... 19
3. Tahap orientasi dosis madu hutan... 20
4. Tahap percobaan ... 21
5. Pengukuran aktivitas dan kapasitas fagositosis makrofag ... 22
F. Analisis Hasil ... 23
BAB IV. HASIL DAN PEMBAHASAN ... 24
A.Uji Fagositosis Makrofag ... 24
B.Tahap Orientasi Dosis Madu Hutan ... 28
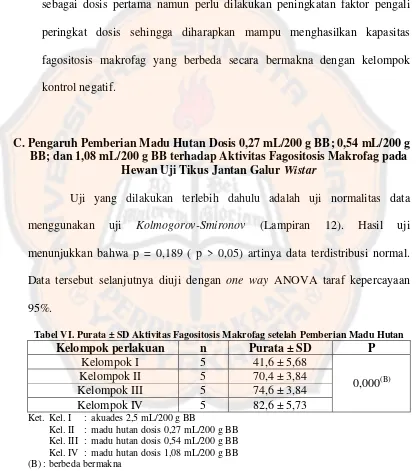
C.Pengaruh Pemberian Madu Hutan Dosis 0,27 ml/200 g BB; 0,54 ml/200 g BB; dan 1,08 ml/200 g BB terhadap Aktivitas Fagositosis Makrofag pada Hewan Uji Tikus Jantan Galur Wistar ... 34
D.Pengaruh Pemberian Madu Hutan Dosis 0,27 ml/200 g BB; 0,54 ml/200 g BB; dan 1,08 ml/200 g BB terhadap Kapasitas Fagositosis Makrofag pada Hewan Uji Tikus Jantan Galur Wistar ... 37
BAB V. KESIMPULAN DAN SARAN ... 41
xi
B.Saran ... 41
DAFTAR PUSTAKA ... 42
LAMPIRAN ... 45
xii
DAFTAR TABEL
Tabel I. Purata ± SD Aktivitas Fagositosis Makrofag setelah Pemberian Madu Hutan pada Tahap Orientasi Dosis ... 28 Tabel II. Hasil Analisis Uji Post-Hoc Tukey Aktivitas Fagositosis
Makrofag setelah Pemberian Madu Hutan pada Tahap Orientasi Dosis ... 29 Tabel III. Peningkatan Aktivitas Fagositosis Makrofag setelah Pemberian
Madu Hutan Dibanding Kontrol Negatif ... 29 Tabel IV. Purata ± SD Kapasitas Fagositosis Makrofag setelah Pemberian
Madu Hutan pada Tahap Orientasi Dosis ... 32 Tabel V. Peningkatan Aktivitas Fagositosis Makrofag setelah Pemberian
Madu Hutan Dibanding Kontrol Negatif ... 32 Tabel VI. Purata ± SD Aktivitas Fagositosis Makrofag setelah Pemberian
Madu Hutan ... 34 Tabel VII. Hasil Analisis Uji Post-Hoc Tukey Aktivitas Fagositosis
Makrofag setelah Pemberian Madu Hutan ... 35 Tabel VIII. Peningkatan Aktivitas Fagositosis Makrofag setelah Pemberian
Madu Hutan Dibanding Kontrol Negatif ... 35 Tabel IX. Purata ± SD Kapasitas Fagositosis Makrofag setelah Pemberian
Madu Hutan ... 37 Tabel X. Hasil Analisis Uji Post-Hoc Tukey Kapasitas Fagositosis
Makrofag setelah Pemberian Madu Hutan ... 38 Tabel XI. Peningkatan Kapasitas Fagositosis Makrofag setelah Pemberian
xiii
DAFTAR GAMBAR
Gambar 1. Gambaran Umum Sistem Imun ... 8 Gambar 2. Mekanisme Pertahanan Sistem Imun Non-Spesifik ... 10 Gambar 3. Makrofag ... 12 Gambar 4. Sel Makrofag Peritoneal dengan Pengecatan Giemsa
Perbesaran 100x ... 25 Gambar 5. Hasil Pengamatan Mikroskopis Sel Makrofag dengan
Pengecatan Giemsa Perbesaran 100x ... 26 Gambar 6. Perbandingan Morfologi Makrofag Tikus dengan Pengecatan
Giemsa Perbesaran 100x ... 27 Gambar 7. Grafik Rata-rata ± SD Aktivitas Fagositosis Makrofag setelah
Pemberian Madu Hutan pada Tahap Orientasi ... 29 Gambar 8. Grafik Rata-rata ± SD Kapasitas Fagositosis Makrofag setelah
Pemberian Madu Hutan pada Tahap Orientasi ... 32 Gambar 9. Grafik Rata-rata ± SD Aktivitas Fagositosis Makrofag setelah
Pemberian Madu Hutan ... 35 Gambar 10. Grafik Rata-rata ± SD Kapasitas Fagositosis Makrofag setelah
xiv
DAFTAR LAMPIRAN
Lampiran 1. Surat Keterangan Kelaikan Etik (Ethical Clearance) ... 46 Lampiran 2. Surat Keterangan Penelitian ... 47 Lampiran 3. Foto Perbandingan Warna antara Madu Hutan dengan Madu
Ternak ... 48 Lampiran 4. Komposisi Media Tumbuh Makrofag ... 49 Lampiran 5. Perhitungan Dosis Pemberian Madu Hutan pada Hewan Uji
Tahap Orientasi Dosis ... 50 Lampiran 6. Data Aktivitas Fagositosis Makrofag Tahap Orientasi
Dosis ... 51 Lampiran 7. Data Kapasitas Fagositosis Makrofag Tahap Orientasi
Dosis ... 52 Lampiran 8. Hasil Analisis Aktivitas Fagositosis Makrofag Tahap
Orientasi Dosis ... 53 Lampiran 9. Hasil Analisis Kapasitas Fagositosis Makrofag Tahap
Orientasi Dosis ... 55 Lampiran 10. Perhitungan Dosis Pemberian Madu Hutan pada Hewan Uji
Tahap Percobaan ... 56 Lampiran 11. Penimbangan Berat Badan Hewan Uji untuk Tahap
Percobaan ... 57 Lampiran 12. Data Aktivitas Fagositosis Makrofag Tahap Percobaan ... 58 Lampiran 13. Data Kapasitas Fagositosis Makrofag Tahap Percobaan... 59 Lampiran 14. Hasil Analisis Aktivitas Fagositosis Makrofag Tahap
Percobaan ... 60 Lampiran 15. Hasil Analisis Kapasitas Fagositosis Makrofag Tahap
xv
INTISARI
Penyakit disebabkan oleh banyak hal salah satunya diantaranya terjadi karena penurunan sistem kekebalan tubuh. Madu hutan mengandung beberapa senyawa organik, salah satunya flavonoid. Flavonoid memiliki aktivitas sebagai antioksidan dan antibakteri serta dapat pula meningkatkan sistem kekebalan tubuh terhadap infeksi penyakit sehingga madu hutan berpotensi sebagai imunomodulator. Tujuan penelitian adalah memperoleh informasi mengenai pengaruh pemberian madu hutan terhadap aktivitas dan kapasitas fagositosis makrofag.
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan penelitian acak pola searah. Sebanyak 20 ekor tikus dibagi menjadi 4 kelompok, yaitu kelompok perlakuan diberikan madu hutan dengan dosis 0,27 ml/200 g BB tikus; 0,54 mL/200 g BB tikus; dan 1,08 ml/200 g BB tikus; serta kelompok kontrol negatif diberikan aquadest 2,5 mL/200 g BB tikus. Aktivitas fagositosis makrofag dinyatakan sebagai ratio fagositik, yaitu persentase sel makrofag yang melakukan fagositosis tiap 100 sel. Kapasitas fagositosis makrofag ditetapkan berdasarkan jumlah bakteri yang difagositosis oleh 100 sel makrofag. Respon imun seluler ditandai dengan peningkatan kemampuan fagositosis makrofag berdasarkan peningkatan jumlah makrofag yang memfagositosis lateks dan peningkatan jumlah lateks yang difagositosis oleh makrofag.. Data dianalisis dengan uji one way ANOVA taraf kepercayaan 95% yang dilanjutkan dengan uji
Tukey.
Hasil penelitian menunjukkan bahwa pemberian madu hutan berpengaruh terhadap aktivitas dan kapasitas fagositosis makrofag berupa peningkatan aktivitas dan kapasitas fagositosis makrofag.
xvi ABSTRACT
Many factor contribute to disease, one of them due to weakenning of immune system. Forest honey contains some organic compounds, true of the active compounds are the flavonoids. Flavonoids have antioxidant and antibacterial activity and can also boost the immune system against infectious diseases so that the honey of forest has a potential as immunomodulator. The aim of this research was to obtain information on the effect of forest honey on the phagocytic activity and phagocytic capacity of macrophages.
This research is experimental with one way randomized complete design. Each group was given honey forest with dose of 0,27 ml/200 g BW; 0,540 mL/200 g BW; 1,080 ml/200 g BW, and negative control group was given aquadest 2,5 mL/200 g BW. Phagocytic activity of macrophages, expressed as a phagocytic ratio, the percentage of cells that perform phagocytosis of macrophages per 100 cells. Phagocytic capacity of macrophages determined based on number of engulfed bacteria per 100 macrophages. Cellular immune response was used to evaluate the increasing capability of macrophage phagocyte (the amount of latex that was phagocyted by macrophage). Data were analyzed by one way ANOVA test with a confidence level of 95%, followed by Tukey test.
The result showed that administration of forest honey has an effect on activity and capacity phagocytosis of macrophages.
1
BAB I PENGANTAR
A.Latar Belakang
Penyakit disebabkan oleh berbagai hal, seperti infeksi bakteri atau virus dan dapat pula disebabkan kondisi tertentu seperti penurunan pertahanan tubuh. Saat kondisi pertahanan tubuh tidak baik maka zat asing yang berasal dari luar tubuh (xenobiotic) maupun dari dalam tubuh mudah menginfeksi sehingga menimbulkan penyakit. Sistem imun merupakan salah satu bagian dari sistem pertahanan tubuh. Senyawa alam maupun sintetik yang meningkatkan sistem pertahanan tubuh tidak bekerja secara langsung menghadapi penyebab penyakit seperti halnya antibiotik. Sistem pertahanan tubuh akan dipacu oleh senyawa tersebut melalui mekanisme efektor sistem imun, sehingga digolongkan sebagai imunomodulator (Munawaroh, 2008). Salah satu bahan alam yang telah digunakan masyarakat Indonesia untuk meningkatkan daya tahan tubuh dan mengatasi alergi adalah madu (Aden, 2010).
Madu poliflora merupakan madu yang berasal dari nektar beberapa jenis tumbuhan bunga. Madu ini biasanya berasal dari hutan yang diproduksi oleh lebah-lebah liar. Madu hutan bersifat alamiah, dalam arti terbebas dari pengaruh pupuk, pestisida, dan polusi (Ambrosio, 2010). Madu hutan yang berbeda sumber nektarnya ini dimungkinkan memiliki aktivitas terhadap sistem imun yang lebih baik daripada madu yang hanya berasal dari satu jenis bunga saja, sebab mengandung antibiotik alami yang diproduksi lebah-lebah liar (Hariyati, 2010).
Madu mengandung flavonoid, zat fitokimia yang berperan sebagai antioksidan (Cahanar dan Irwan, 2006). Menurut Krell (1996) kandungan flavonoid dapat meningkatkan sistem kekebalan tubuh. Senyawa flavonoid diketahui dapat meningkatkan kemampuan fagositosis makrofag peritoneum pada tikus galur Wistar (Arsani, 2010).
Makrofag merupakan sel yang berperan dalam respon imun baik peran fungsional dalam fagositosis maupun perannya sebagai antigen presenting cells
(APC) (Baratawidjaja dan Rengganis, 2010). Fagositosis makrofag lebih aktif dalam menghadapi patogen seperti mikroorganisme maupun antigen lain bahkan sel atau jaringan sendiri yang mengalami kerusakan atau mati, sehingga makrofag merupakan sel efektor utama pada respon imun alamiah (Abbas, Lichtman, and Pober, 2000).
dengan menggunakan latex beads, sehingga dapat diperoleh informasi penggunaan madu hutan sebagai imunomodulator untuk meningkatkan respon imun.
1. Permasalahan
Apakah madu hutan berpengaruh terhadap aktivitas dan kapasitas fagositosis makrofag pada hewan uji tikus jantan galur Wistar?
2. Keaslian penelitian
Berdasarkan pengetahuan dan penelusuran pustaka yang dilakukan oleh penulis penelitian mengenai “Pengaruh Pemberian Madu Hutan terhadap Aktivitas dan Kapasitas Fagositosis Makrofag pada Hewan Uji Tikus Jantan Galur Wistar” belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis
1) Memberikan informasi ilmiah bagi pengembangan ilmu pengetahuan mengenai manfaat madu hutan sebagai imunomodulator.
2) Menjadi dasar dalam pengembangan penelitian di bidang ilmu kefarmasian khususnya tentang madu hutan untuk meningkatkan kesehatan masyarakat.
b. Manfaat praktis
1. Tujuan umum
Memperoleh informasi mengenai pengaruh pemberian madu hutan pada hewan uji tikus jantan galur Wistar sebagai imunomodulator.
2. Tujuan khusus
Memperoleh informasi mengenai pengaruh pemberian madu hutan terhadap aktivitas dan kapasitas fagositosis makrofag pada hewan uji tikus jantan galur Wistar.
5
BAB II
PENELAAHAN PUSTAKA
A.Madu
Madu adalah cairan alami yang umumnya memiliki rasa manis, dari sari bunga tanaman (floral nectar) atau bagian lain dari tanaman (extra floral
nectar) atau ekskresi serangga. Madu merupakan hasil sekresi lebah, karena
madu ditempatkan dalam bagian khusus di perut lebah yang disebut perut madu
yang terpisah dari perut besar (Sambodo, 2009).
1. Jenis madu
Jenis madu berdasarkan sumber nektarnya dapat dibagi menjadi dua, yaitu madu monoflora dan madu poliflora. Madu monoflora merupakan madu yang diperoleh dari satu tumbuhan utama, seperti madu kelengkeng, madu rambutan, dan madu randu, sedangkan madu poliflora adalah madu yang berasal dari nektar beberapa jenis tumbuhan bunga, contoh dari madu jenis ini adalah madu hutan (Aden, 2010).
tanaman atau pohon yang sengaja ditanam untuk perternakan lebah (Suranto, 2007).
2. Kualitas madu
Madu yang berkualitas ditentukan oleh beberapa hal, yaitu waktu pemanenan madu, kadar air, warna, rasa, dan aroma madu. Ketika madu telah matang dan sel-sel madu mulai ditutup oleh lebah maka saat tersebut sangat tepat untuk memanen madu. Warna madu cenderung akan mengikuti tanaman penghasil nektarnya. Rasa dan aroma madu yang paling enak adalah ketika madu baru dipanen dari sarangnya (Sambodo, 2009).
Menurut Sumoprastowo dan Suprapto (1980), kualitas madu secara sensoris biasanya ditentukan oleh warna, aroma khas madu, dan keadaannya (kekentalan dan penampakan). Beberapa ahli menyatakan bahwa madu yang berwarna gelap mengandung banyak mineral, terutama Fe, Cu, dan Mn. Oleh karena itu madu yang berwarna gelap sebagai bahan makanan tidak kalah pentingnya dengan madu yang berwarna terang. Biasanya untuk madu yang berwarna gelap ini terjadi pada madu hutan.
3. Komposisi madu
Zat-zat yang terkandung dalam madu sangatlah kompleks dan kini
telah diketahui tidak kurang dari 181 macam zat yang terkandung dalam madu.
Karbohidrat merupakan komponen terbesar yang terkandung dalam madu, yaitu
berkisar lebih dari 75%. Jenis karbohidrat yang paling dominan dalam hampir
semua madu adalah dari golongan monosakarida yang biasanya terdiri fruktosa
dan glukosa. Fruktosa dan glukosa mencakup 85%-90% dari total karbohidrat
adalah air. Jumlahnya biasanya berkisar dari 15%-25%. Bervariasinya kadar air
dalam madu disebabkan oleh beberapa hal, diantaranya kelembapan udara,
jenis nektar, proses produksi dan penyimpanan (Suranto, 2007).
Madu mengandung beberapa senyawa organik, yang telah
terindentifikasi antara lain seperti polifenol, flavonoid, dan glikosida. Madu
juga mengandung berbagai jenis enzim, antara lain enzim glukosa oksidase dan
enzim invertase yang dapat membantu proses pengolahan sukrosa untuk diubah
menjadi glukosa dan fruktosa yang keduanya mudah diserap dan dicerna
(Aljady et al., 2000).
Menurut Febrita (2011), penapisan fitokimia yang dilakukan pada madu hutan menunjukkan adanya kandungan senyawa flavonoid. Flavonoid bermanfaat sebagai antibiotik, bekerja dengan mengganggu fungsi dari mikroorganisme dari bakteri atau virus. Efek lainnya adalah mencegah alergi karena flavonoid mampu mencegah lepasnya zat utama penyebab alergi yaitu histamin dan serotonin (Suranto, 2007). Flavonoid dalam tubuh manusia berfungsi sebagai antioksidan untuk mencegah kanker dan melindungi sel. Hal inilah yang menyebabkan flavonoid sebagai zat yang sangat kuat menetralisir radikal bebas, mendukung sistem kekebalan tubuh alami manusia pada tingkat seluler dan membantu regenerasi sel (Kusmardi, Kumala, dan Triana, 2007).
4. Manfaat madu
berbeda pula (Haviva, 2011). Manfaat madu hutan antara lain meningkatkan daya tahan tubuh, mengatasi susah tidur, mengatasi alergi, mengobati reumatik, memperlancar fungsi otak, dan menyembuhkan luka bakar (dioles pada bagian yang luka) (Aden 2010).
B.Sistem Imun
Imunitas adalah resistensi terhadap penyakit, terutama penyakit infeksi. Gabungan sel, molekul, jaringan yang berperan dalam resistensi terhadap mikroba serta bahan lainnya disebut respon imun. Sistem imun diperlukan tubuh untuk mempertahankan keutuhannya terhadap bahaya yang dapat ditimbulkan dari berbagai bahan dalam lingkungan hidup (Baratawidjaja dan Rengganis, 2010).
Gambar 1. Gambaran Umum Sistem Imun (Baratawidjaja dan Rengganis, 2010)
membangkitkan reaksi yang tepat untuk mengeliminasi sumber antigen bersangkutan. Respon imun akan diberikan oleh tubuh jika terdeteksi adanya benda asing yang masuk ke dalam tubuh. Benda asing tersebut dapat berupa mikroorganisme eksogenous seperti bakteri, virus atau jamur dapat pula zat-zat kimia eksogenous (polen atau racun tanaman) atau sel-sel endogenous (sel maligna). Respon imun mempunyai tiga fungsi utama, yaitu pertahanan tubuh terhadap infeksi organisme asing, menjaga keseimbangan pergantian sel (homeostasis) dengan mengeliminasi sel-sel tubuh yang sudah tua, dan pengawasan (surveillance) untuk mengawasi sel-sel abnormal yang selalu timbul dalam tubuh. Respon imun merupakan suatu sistem pertahanan agar tubuh dapat menjaga keseimbangan antara lingkungan luar dan di dalam tubuh (Mardilah, Zakaria, dan Asydhah, 2006).
Sistem imun yang mempertahankan keutuhan tubuh terdiri atas sistem imun bawaan (natural/ nonspesifik/ innate/ native immunity) dan sistem imun perolehan (spesifik/ adaptive/ acquired immunity) (Baratawidjaja dan Rengganis, 2010).
1. Sistem imun non-spesifik
Gambar 2. Mekanisme Pertahanan Sistem Imun Non-Spesifik (Baratawidjaja dan Rengganis, 2010)
Bila ada antigen yang masuk, misalnya antigen bakteri, maka bakteri akan melakukan invasi disertai proses inflamasi pada tempat infeksi. Inflamasi bertujuan memusatkan agen pertahanan tubuh ke lokasi yang terinfeksi. Selama inflamasi sel-sel fagosit seperti neutrofil dan makrofag meninggalkan aliran darah dan berpindah menuju tempat infeksi sebagai respon terhadap kemikal (chemoattractants) yang dilepas di tempat infeksi. Tugas sel-sel fagosit adalah menghancurkan bakteri tersebut secara non-spesifik dengan proses fagositosis (Basuki, 2005).
2. Sistem imun spesifik
sel memori sehingga respon yang diberikan lebih cepat dan lebih baik terhadap antigen yang telah masuk sebelumnya ke dalam tubuh (Abbas and
Lichtman, 2005). Benda asing yang pertama kali muncul dalam tubuh akan segera dikenal oleh sistem imun spesifik sehingga terjadi sensitisasi sel-sel sistem imun. Bila sel imun yang sudah tersensitisasi tersebut terpapar kembali dengan benda asing yang sama, maka benda asing ini akan dikenal dengan cepat kemudian dihancurkan (Baratawidjaja dan Rengganis, 2010).
C.Makrofag
Makrofag berasal dari promonosit sumsum tulang lalu mengalami diferensiasi menjadi monosit darah dan akhirnya tinggal di jaringan sebagai makrofag dewasa serta membentuk sistem fagosit mononuklear (Roitt, 2002). Makrofag merupakan sel fagosit yang hampir ditemui di setiap organ di seluruh tubuh, terutama pada jaringan ikat longgar.
Makrofag berukuran 10-30 µm, bentuk tidak teratur, inti lonjong, mengandung granula azurofilik, dan bertahan berbulan-bulan dalam jaringan. Makrofag kadang-kadang mempunyai bentuk yang sangat tidak teratur dengan kaki-kaki palsu yang terjulur keseluruh arah, membran plasma yang melipat-lipat dan bertonjolan kecil-kecil. Keadaan permukaan demikian itu membantu perluasan fagositosis dan gerakan sel. Sel-sel sistem makrofag terdapat pada jaringan ikat longgar berupa makrofag jaringan atau histiosit, di dalam darah berupa monosit, di dalam hepar melapisi sinusoid yang dikenal sebagai sel
tulang, sedangkan pada susunan saraf pusat berupa makroglia berasal dari mesoderm (Efendi, 2003).
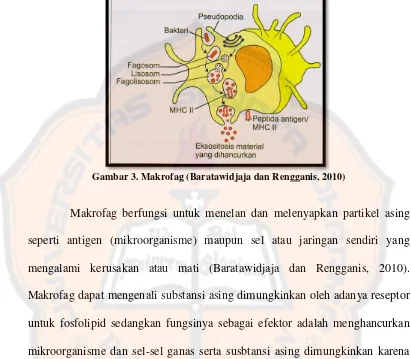
Gambar 3. Makrofag (Baratawidjaja dan Rengganis, 2010)
Makrofag berfungsi untuk menelan dan melenyapkan partikel asing seperti antigen (mikroorganisme) maupun sel atau jaringan sendiri yang mengalami kerusakan atau mati (Baratawidjaja dan Rengganis, 2010). Makrofag dapat mengenali substansi asing dimungkinkan oleh adanya reseptor untuk fosfolipid sedangkan fungsinya sebagai efektor adalah menghancurkan mikroorganisme dan sel-sel ganas serta susbtansi asing dimungkinkan karena sel ini, antara lain mempunyai sejumlah lisosom yang mengandung enzim perusak seperti hidrolase dan peroksidase. Kemampuan fagositosis dalam menghancurkan substansi asing yang telah dilapisi (opsonisasi) antibodi atau komplemen dapat meningkat karena makrofag mempunyai reseptor terhadap Fc (Fragment crystallizable), Ig (immunoglobulin) G1, dan IgG3 serta IgE, dan reseptor terhadap komplemen (Kresno, 2010). Fungsi lain makrofag adalah sebagai antigen presenting cells (APC) dengan cara mengekspresikan MHC
ekspresi MHC II meningkat bila ada makrofag yang teraktivasi. Makrofag menampilkan antigen asing pada sel T yang dilakukannya bersama ekspresi MHC II (Abbas et al., 2000).
Fagositosis merupakan suatu proses atau cara untuk memakan bakteri atau benda asing (Efendi, 2003). Proses fagositosis oleh makrofag secara berurutan berlangsung dalam lima fase, yaitu : fase pergerakan, perlekatan, penelanan (ingestion), degranulasi, dan pembunuhan (killing). Proses penelanan bakteri terjadi karena fagosit membentuk tonjolan pseudopodia, sehingga bakteri tertangkap dalam vakuola yang disebut fagosom. Selanjutnya lisosom yang berisi berbagai jenis enzim dan protein lain bergabung dengan fagosom membentuk fagolisosom, lalu terjadi degranulasi dan respiratory
burst. Enzim dan protein yang terdapat dalam lisosom mampu membunuh
bakteri, baik dengan proses oksidatif maupun non-oksidatif (Abbas et al., 2000).
D.Imunomodulator
1. Imunostimulan
Imunostimulan adalah senyawa tertentu yang dapat meningkatkan mekanisme pertahanan tubuh baik secara spesifik maupun non-spesifik, dan terutama terjadi pada induksi non-spesifik, baik mekanisme pertahanan seluler maupun humoral. Pertahanan non-spesifik terhadap antigen ini disebut paramunitas, dan zat berhubungan dengan penginduksi disebut paraimunitas. Induktor semacam ini biasanya tidak atau sedikit sekali kerja antigennya, akan tetapi sebagian besar bekerja sebagai mitogen yaitu meningkatkan proliferasi sel yang berperan pada imunitas. Sel tujuan adalah makrofag, granulosit, limfosit-T dan limfosit-B, karena induktor paramunitas ini bekerja menstimulasi mekanisme pertahanan seluler. Mitogen ini dapat bekerja langsung maupun tak langsung untuk meningkatkan fagositosis mikro dan makro. Mekanisme pertahanan spesifik maupun non spesifik umumnya saling berpengaruh (Widianto, 1987). 2. Imunosupresan
E.Landasan Teori
Madu hutan merupakan salah satu jenis madu, berasal dari sumber nektar yang berbeda, diproduksi oleh lebah-lebah liar. Madu hutan mengandung banyak senyawa organik, salah satu kandungan senyawa organik yang telah teridentifikasi adalah flavonoid. Flavonoid merupakan senyawa fitokimia yang dapat meningkatkan sistem kekebalan tubuh karena memiliki kandungan antioksidan yang tinggi dan merupakan antibiotik alamiah. Beberapa penelitian terdahulu juga telah membuktikan bahwa senyawa flavonoid mampu meningkatkan kemampuan fagositosis makrofag. Salah satunya penelitian yang dilakukan oleh Arsani (2010) membuktikan bahwa senyawa flavonoid dapat meningkatkan kemampuan fagositosis makrofag peritoneum pada tikus galur Wistar.
F. Hipotesis
16
BAB III
METODE PENELITIAN
A.Jenis dan Rancangan Penelitian
B.Variabel dan Definisi Operasional
1. Variabel penelitian
a. Variabel utama
1) Variabel bebas : dosis madu hutan
2) Variabel tergantung : aktivitas dan kapasitas fagositosis makrofag b. Variabel pengacau
1) Variabel yang dikendalikan : jenis makanan, variasi genetik, jenis kelamin, berat badan, galur tikus, dan umur tikus.
2) Variabel yang tidak terkendali : kondisi psikologis dan patofisiologis tikus.
2. Definisi operasional
a. Madu hutan
Madu poliflora yang berasal dari nektar beberapa jenis tumbuhan bunga di hutan yang diproduksi oleh lebah-lebah liar. Madu hutan yang digunakan diperoleh dari salah satu distributor madu di Yogyakarta. b. Aktivitas fagositosis makrofag
Aktivitas fagositosis makrofag dinyatakan sebagai ratio fagositik, yaitu persentase sel makrofag yang melakukan fagositosis tiap 100 sel (Maqsood, Singh, Samoon, and Balange, 2010).
c. Kapasitas fagositosis makrofag
C.Bahan Penelitian
1. Bahan utama
Madu hutan berasal dari hutan Kalimantan yang diperoleh dari salah satu distributor madu di Yogyakarta, yaitu Madu Pramuka.
2. Hewan uji
Tikus jantan galur Wistar umur 2-3 bulan berat 100-300 g diperoleh dari Unit Praklinik Laboratorium Pengembangan dan Penelitian Terpadu Universitas Gadjah Mada Yogyakarta. Tikus dipelihara dalam ruangan berventilasi cukup dengan suhu ruangan 25-28oC, diberi pakan AD-II (Comfeed) dan akuades sebagai minum secara ad libitum.
3. Bahan untuk uji fagositosis makrofag
Akuades, akuabides, klorofom, Roswell Park Memorial Institute Medium
(RPMI 1640) (Sigma), metanol, alkohol 70%, Phosphate Buffer Saline
(PBS) steril, coverslips bulat, latex beads diameter 3 µm (Sigma Chem. Co), Giemsa 20%, medium komplit yang terdiri dari RPMI 1640, Fetal Bovine
Serum (FBS) (Gibco) 10%, Penisilin-Streptomisin 2% (Gibco) dan
fungizon 1% (Gibco).
D.Alat Penelitian
1. Preparasi sampel
2. Pengujian aktivitas dan kapasitas fagositosis makrofag
Inkubator CO2 5%; 37oC (Heraeus), plate 24 well (Nunc), sentrifus
eppendorf (Sorfall MC 12 V, Dupont), Effendorf tube, Laminar Air Flow
(Labquib), hemositometer (Nebaeur), mikropipet (Eppendorf), neraca elektronik (Sartorius), filter 0,22 µm (Sartorius), tabung sentrifus 15 mL (Nunc), spuit injeksi 10 mL (Terumo), mesin Vortex, pipet Pasteur, yellow
dan blue tip, Inverted Microscope (Olympus), mikroskop binokuler, lampu spiritus, pinset, gunting, tabung reaksi, dan alat-alat gelas yang telah disterilkan.
E.Tata Cara Penelitian
1. Tahap penentuan dosis madu hutan
Besarnya dosis madu hutan ditentukan berdasarkan dosis yang dianjurkan pada manusia adalah 1-2 kali/hari 1 sendok makan (15 mL) (Suranto, 2007). Konversi dosis pada manusia yang berat badannya 70 kg ke tikus yang berat badannya 200 g adalah 0,018 (Ngatidjan, 1991). Dosis madu hutan untuk tikus 200 g adalah :
Faktor konversi x dosis = 0,018 x 15 mL = 0,27 mL/200 g BB
2. Tahap praperlakuan hewan uji
3. Tahap orientasi dosis madu hutan
Tahap orientasi dosis dilakukan untuk mengetahui dosis madu hutan yang dapat menyebabkan peningkatan aktivitas dan kapasitas fagositosis makrofag. Tikus jantan sejumlah 12 ekor dari galur Wistar, umur 2-3 bulan, berat badan 100-300 g. Tikus tersebut dibagi secara random menjadi 4 kelompok, dengan masing-masing kelompok berjumlah 3 ekor. Kelompok-kelompok tersebut antara lain :
a. Kelompok kontrol negatif : kelompok tikus yang diberi akuades sebagai kontrol pelarut dengan volume pemberian 2,5 mL/200 g BB.
b. Kelompok perlakuan 1 : kelompok tikus yang diberi larutan madu hutan
dengan dosis 0,27 mL/200 g BB, dengan volume pemberian 1,35 mL/200 g BB.
c. Kelompok perlakuan 2 : kelompok tikus yang diberi larutan madu hutan
dengan dosis 0,405 mL/200 g BB, dengan volume pemberian 2,03 mL/200 g BB.
d. Kelompok perlakuan 3 : kelompok tikus yang diberi larutan madu hutan
dengan dosis 0,54 mL/200 g BB, dengan volume pemberian 2,7 mL/200 g BB.
4. Tahap percobaan
Tikus jantan sejumlah 20 ekor dari galur Wistar, umur 2-3 bulan, berat badan 100-300 g. Tikus tersebut dibagi secara random menjadi 4 kelompok, dengan masing-masing kelompok berjumlah 5 ekor tikus, sesuai dengan ketentuan WHO (1993), jumlah minimal hewan uji tiap kelompok adalah 5 ekor. Dosis madu hutan pada tahap orientasi yang menyebabkan peningkatan signifikan aktivitas dan kapasitas fagositosis makrofag pada hewan uji digunakan sebagai dosis pertama. Kelompok dosis kedua dan ketiga, yang ditetapkan dengan faktor pengali adalah dua dari dosis pertama. Kelompok-kelompok tersebut antara lain :
a. Kelompok kontrol negatif : kelompok tikus yang diberi akuades sebagai kontrol pelarut dengan volume pemberian 2,5 mL/200 g BB.
b. Kelompok perlakuan 1 : kelompok tikus yang diberi larutan madu hutan dengan dosis 0,27 mL/200 g BB, dengan volume pemberian 0,675 mL/200 g BB.
c. Kelompok perlakuan 2 : kelompok tikus yang diberi larutan madu hutan dengan dosis 0,54 mL/200 g BB, dengan volume pemberian 1,35 mL/200 g BB.
d. Kelompok perlakuan 3 : kelompok tikus yang diberi larutan madu hutan dengan dosis 1,08 mL/200 g BB, dengan volume pemberian 2,7 mL/200 g BB.
Pada hari ke-18, tikus dibunuh dengan narkose menggunakan kloroform. Tikus diletakkan diposisi terlentang, kulit bagian perut dibuka dan dibersihkan selubung peritoneumnya dengan alkohol 70%. Kemudian disuntikan 10 mL RPMI dingin ke rongga peritoneum, tunggu ± 3 menit sambil diguling-gulingkan secara perlahan. Cairan peritoneal dikeluarkan dari rongga peritoneum dengan cara menekan organ dalam dengan dua jari, cairan diaspirasi dengan jarum suntik, dipilih bagian yang tidak berlemak dan jauh dari usus. Jarum yang berisi bahan aspirasi diletakkan dalam gelas beker berisi es, kemudian suspensi tersebut dimasukkan ke tabung sentrifus. Aspirat yang sudah terkumpul disentrifugasi pada kecepatan 3000 rpm selama 5 menit. Supernatan dibuang kemudian ditambahkan 3 mL medium komplit pada pellet yang didapat. Jumlah sel dihitung dengan hemositometer kemudian diresupensikan dengan medium komplit sehingga didapat suspensi sel dengan kepadatan 2,5 x 106/mL. Suspensi sel yang dikultur pada plate 24 yang diberi coverslips bulat, setiap sumuran 200 µL (5 x 105 sel), inkubasi dalam inkubator CO2 5%, 37oC selama 30 menit,
kemudian ditambahkan medium komplit 1 mL/sumuran dan diinkubasi selama 2 jam, sel dicuci dengan RPMI dua kali kemudian ditambahkan medium komplit 1 mL/sumuran dan inkubasi dilanjutkan sampai 24 jam.
5. Pengukuran aktivitas dan kapasitas fagositosis makrofag
Tahap ini dilakukan uji fagositosis sel makrofag terhadap lateks
beads (Leijh et al., 1986). Lateks beads yang digunakan berdiameter 3 µm
Makrofag peritoneum yang dikultur sehari sebelumnya dicuci dua kali dengan RPMI, kemudian tambahkan suspensi lateks beads 200 µL/sumuran dan diinkubasikan selama 60 menit pada 37oC dalam inkubator CO2 5%.
Sel kemudian dicuci dengan PBS tiga kali untuk menghilangkan partikel yang tidak difagositosis dan dikeringkan pada suhu ruangan dan difiksasi dengan metanol absolut. Setelah kering coverslips dipopulasi dengan Giemsa 20% selama 30 menit. Dicuci dengan akuades, diangkat dari sumuran kultur dikeringkan pada suhu ruangan. Presentasi sel yang memfagosit partikel lateks dihitung dari 100 sel fagosit yang diperiksa dengan mikroskop cahaya.
F. Analisis Hasil
24
BAB IV
HASIL DAN PEMBAHASAN
Tujuan penelitian ini adalah untuk mengetahui pengaruh pemberian madu hutan terhadap aktivitas dan kapasitas fagositosis makrofag serta untuk mengetahui seberapa besar pengaruh pemberian madu hutan terhadap aktivitas dan kapasitas fagositosis makrofag. Kemampuan fagositosis makrofag dapat dilihat dari jumlah makrofag yang mampu memfagositosis partikel lateks selain itu ditunjukkan pula dari jumlah lateks yang dapat difagositosis oleh makrofag. Data yang diperoleh dari uji fagositosis dianalisis secara statistik menggunakan uji
Kolmogorov-Smirnov untuk mengetahui normalitas data, selanjutnya dilakukan
analisis one way ANOVA dengan taraf kepercayaan 95%.
A.Uji Fagositosis Makrofag
komplit yang mengandung medium RPMI, FBS (Fetal Bovine Serum) yang merupakan serum untuk memacu pertumbuhan sel dan menjaga kelangsungan hidup sel, ada pula penisilin-streptomisin (penstrep) dan fungison yang berfungsi sebagai antimikroba. Cairan peritoneum yang diambil, selain terdapat sel makrofag juga ditemukan sel-sel lain seperti limfosit dan sel granulosit dan saling berdekatan sehingga sulit dibedakan antara sel makrofag dengan sel lain. Kemampuan sel makrofag untuk menempel pada coverslip membedakan sel makrofag dengan sel yang lain.
b a
Gambar 4. Sel Makrofag Peritoneal dengan Pengecatan Giemsa Perbesaran 100x
Ket. (a). Pembentukan kaki semu (pseudopodia); (b). pembentukan fagosom
Kemampuan sel makrofag pada tahap yang paling awal untuk memfagositosis zat asing dimulai dengan membentuk kaki semu (pseudopodia)
Perbedaan aktivitas dan kapasitas fagositosis makrofag antara kelompok perlakuan dengan kelompok kontrol dapat dilihat dari kemampuan sel makrofag memfagositosis partikel lateks secara in vitro (Leijh et al, 1986). Lateks merupakan makromolekul yang dianggap benda asing yang sangat direspon baik oleh sistem imun tubuh. Oleh karena itu, dengan adanya lateks diharapkan dapat memacu aktivitas makrofag dalam memfagositosis lateks (Sheehan, 1997).
c a
b
Gambar 5. Hasil Pengamatan Mikroskopis Sel Makrofag dengan Pengecatan Giemsa Perbesaran 100x
Ket. (a). Lateks berwarna putih; (b). sel makrofag berwarna ungu; (c). partikel lateks yang difagositosis oleh sel makrofag
dengan Giemsa sehingga tidak berwarna, hal ini dikarenakan metanol akan memperkecil pori-pori lateks sehingga akan mengkerut. Pengamatan menggunakan mikroskop akan memperlihatkan makrofag yang berwarna ungu dan lateks yang berwarna putih (Gambar 5) sehingga dapat dibedakan antara lateks dan sel makrofag yang difagositosis dan lateks yang tidak difagositosis. Kemampuan fagositosis sel makrofag dapat dilihat dari aktivitas dan kapasitas fagositosis makrofag.
KELOMPOK I KELOMPOK II
KELOMPOK III KELOMPOK IV
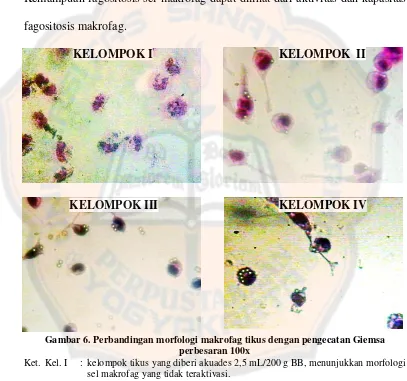
Gambar 6. Perbandingan morfologi makrofag tikus dengan pengecatan Giemsa perbesaran 100x
Ket. Kel. I : kelompok tikus yang diberi akuades 2,5 mL/200 g BB, menunjukkan morfologi sel makrofag yang tidak teraktivasi.
Kel. II : kelompok tikus yang diberi madu hutan dosis 0,27 mL/200 g BB menunjukkan morfologi sel makrofag yang teraktivasi dengan membentuk kaki semu maupun fagososom.
Kel. III : kelompok tikus yang diberi madu hutan madu hutan dosis 0,54 mL/200 g BB menunjukkan morfologi sel makrofag yang teraktivasi dengan membentuk kaki semu maupun fagososom.
Morfologi sel makrofag di bawah mikroskop menunjukkan sel yang berbentuk bulat, besar, populasi jarang dengan inti sel yang besar. Sel
makrofag peritoneal dari tikus yang diberi lateks beads sebagian menunjukkan morfologi teraktivasi dan sebagian lagi menunjukkan morfologi tidak
teraktivasi (Gambar 6).
B.Tahap Orientasi Dosis Madu Hutan
Tahap orientasi dosis madu hutan dilakukan untuk mengetahui dosis madu hutan yang memberikan pengaruh terhadap aktivitas dan kapasitas fagositosis makrofag. Data yang diperoleh pada tahap orientasi dosis dianalisis secara statistik menggunakan uji Kolmogorov-Smirnov selanjutnya dilakukan analisis one way ANOVA dengan taraf kepercayaan 95%.
1. Uji aktivitas fagositosis makrofag
Hasil uji Kolmogorov-Smirnov pada data aktivitas fagositosis makrofag (Lampiran 8) menunjukkan bahwa data terdistribusi normal dengan nilai signifikansi 0,782 (p > 0,05).
Tabel II. Hasil Analisis Uji Post-Hoc Tukey Aktivitas Fagositosis Makrofag setelah Pemberian Madu Hutan pada Tahap Orintasi
Kelompok Perlakuan I II III IV (B) : Berbeda bermakna; (TB) : Berbeda tidak bermakna
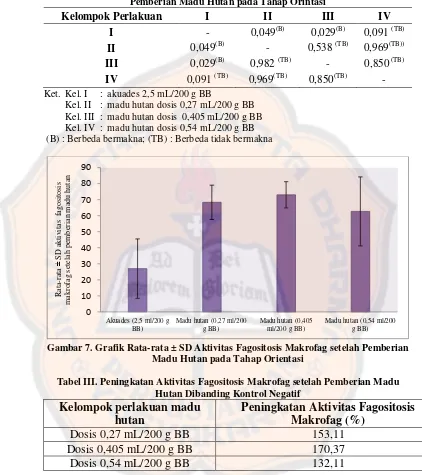
Gambar 7. Grafik Rata-rata ± SD Aktivitas Fagositosis Makrofag setelah Pemberian Madu Hutan pada Tahap Orientasi
Tabel III. Peningkatan Aktivitas Fagositosis Makrofag setelah Pemberian Madu Hutan Dibanding Kontrol Negatif
Hasil uji statistik one way ANOVA (Tabel I) menunjukkan nilai p = 0,026 (p < 0,05), hal ini berarti bahwa kelompok kontrol maupun perlakuan mempunyai aktivitas fagositosis makrofag yang berbeda bermakna. Pada Tabel II menunjukkan bahwa terdapat perbedaan yang
bermakna (p < 0,05) antara kelompok kontrol negatif (akuades 2,5 mL/200 g BB) terhadap kelompok madu hutan dosis 0, 27 mL/200 g BB dan kelompok madu hutan dosis 0,405 mL/200 g BB. Namun, tidak terdapat perbedaan yang bermakna antara kelompok kontrol negatif (akuades 2,5 mL/200 g BB) terhadap kelompok madu hutan dosis 0,54 mL/200 g BB.
Berdasarkan hasil uji statistik tersebut dapat dibuktikan bahwa pemberian madu hutan pada dosis 0, 27 mL/200 g BB dan dosis 0,405 mL/200 g BB berpengaruh terhadap aktivitas fagositosis, yaitu berupa peningkatan aktivitas fagositosis makrofag sebesar 153,11% dan 170,37% (Tabel III). Pada madu hutan dosis 0,54 mL/200 g BB, meskipun secara uji statistik tidak berbeda bermakna terhadap kontrol negatif, namun bila dilihat dari Gambar 7 dan Tabel III menunjukkan bahwa madu hutan dosis 0,54 mL/200 g BB mampu meningkatan aktivitas fagositosis makrofag dibanding kelompok kontrol negatif, yaitu sebesar 132,11%. Berdasarkan hasil analisis ini, maka dapat dibuktikan bahwa madu hutan pada dosis terendah (0,27 mL/200 g BB) sudah mampu memberi pengaruh berupa peningkatan aktivitas fagositosis makrofag, sehingga pada tahap percobaan dosis ini digunakan sebagai dosis pertama.
madu hutan dosis 0,405 mL/200 g BB. Namun, pada kelompok madu hutan dosis 0,54 mL/200 g BB terdapat penurunan aktivitas fagositosis makrofag dibanding kelompok madu hutan dosis 0,27 mL/200 g BB dan dosis 0,405 mL/200 g BB. Hal ini mungkin disebabkan oleh beberapa hal, yaitu : 1) penurunan aktivitas fagositosis makrofag disebabkan oleh mekanisme madu hutan sebagai imunomodulator yang akan meningkatkan respon imunitas dalam tubuh hanya sampai batas tertentu, yang apabila batas itu sudah tercapai, maka efeknya akan menurun. 2) Efek imunomodulator dari madu hutan sudah habis sebelum sampai pada masa pengujian aktivitas makrofag disebabkan pemberian madu hutan hanya pada tujuh hari saja dari masa tahap orientasi dosis selama 29 hari, sehingga pada tahap percobaan perlu dilakukan pemberian madu hutan selama tahap percobaan berlangsung. 3) Faktor pengali peringkat dosis madu hutan pada ketiga kelompok yang terlalu dekat, yaitu 1,5 dan 2 kali dari dosis pertama (0,27 mL/200 g BB) sehingga hasil yang didapat tidak menunjukkan hasil yang berbeda signifikan. Oleh karena itu, pada tahap percobaan perlu dilakukan peningkatan faktor pengali peringkat dosis madu hutan yang lebih besar lagi.
2. Uji kapasitas fagositosis makrofag
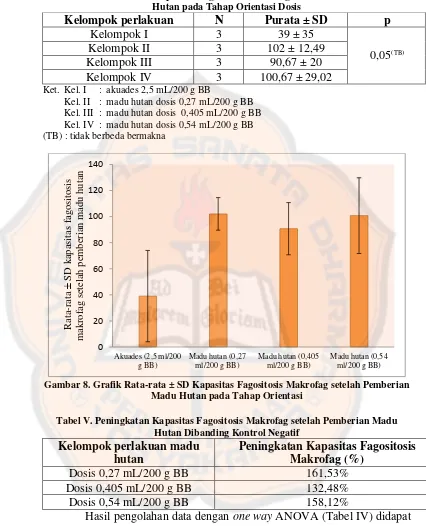
Tabel IV. Purata ± SD Kapasitas Fagositosis Makrofag setelah Pemberian Madu Hutan pada Tahap Orientasi Dosis
Kelompok perlakuan N Purata ± SD p (TB) : tidak berbeda bermakna
Gambar 8. Grafik Rata-rata ± SD Kapasitas Fagositosis Makrofag setelah Pemberian Madu Hutan pada Tahap Orientasi
Tabel V. Peningkatan Kapasitas Fagositosis Makrofag setelah Pemberian Madu Hutan Dibanding Kontrol Negatif
Hasil pengolahan data dengan one way ANOVA (Tabel IV) didapat nilai p = 0,05 (p < 0,05), artinya bahwa tidak ada perbedaan yang bermakna antara kapasitas fagositosis makrofag pada kelompok kontrol dengan kelompok perlakuan madu hutan. Penelitian ini berbeda dengan yang
dilakukan oleh Hasanah (2005), yang menunjukkan bahwa peningkatan aktivitas fagositosis makrofag sebanding dengan peningkatan kapasitas fagositosis makrofag. Hal ini mungkin terjadi karena beberapa faktor antara lain: 1) kendala teknis dalam pelaksanaan perhitungan jumlah partikel lateks yang difagositosis yang dilakukan secara manual sehingga sulit menghitung secara tepat dalam medan pandang mikroskop. Oleh karena itu, pada tahap percobaan sangat dibutuhkan kecermatan dan ketepatan dalam pengamatan dan perhitungan kapasitas fagositosis makrofag. 2) Dosis madu hutan belum mampu memberikan nilai kapasitas fagositosis makrofag yang berbeda bermakna dengan kelompok kontrol. Hal ini diperkuat oleh penelitian Sriningsih dan Wibowo (2006) yang menyatakan bahwa hasil uji fagositosis sangat tergantung dari dosis uji, dimana efek imunosupresan bisa saja muncul manakala pengujian dilakukan dalam dosis besar, sementara efek imunostimulan akan terlihat pada dosis rendah.
mL/200 g BB sebesar 161,53%, madu hutan dosis 0,405 mL/200 g BB sebesar 132,48%, dan 0,54 mL/200 g BB sebesar 158,12%.
Berdasarkan hasil ini, maka dimungkinkan pada tahap percobaan dosis terendah, yaitu madu hutan dosis 0,27 mL/200 g BB dapat digunakan sebagai dosis pertama namun perlu dilakukan peningkatan faktor pengali peringkat dosis sehingga diharapkan mampu menghasilkan kapasitas fagositosis makrofag yang berbeda secara bermakna dengan kelompok kontrol negatif.
C.Pengaruh Pemberian Madu Hutan Dosis 0,27 mL/200 g BB; 0,54 mL/200 g BB; dan 1,08 mL/200 g BB terhadap Aktivitas Fagositosis Makrofag pada
Hewan Uji Tikus Jantan Galur Wistar
Uji yang dilakukan terlebih dahulu adalah uji normalitas data menggunakan uji Kolmogorov-Smironov (Lampiran 12). Hasil uji menunjukkan bahwa p = 0,189 ( p > 0,05) artinya data terdistribusi normal. Data tersebut selanjutnya diuji dengan one way ANOVA taraf kepercayaan 95%.
Tabel VI. Purata ± SD Aktivitas Fagositosis Makrofag setelah Pemberian Madu Hutan
Tabel VII. Hasil Analisis Uji Post-hoc Tukey Aktivitas Fagositosis Makrofag setelah (B) : Berbeda bermakna; (TB) : Berbeda tidak bermakna
Gambar 9. Grafik Rata-rata ± SD Aktivitas Fagositosis Makrofag setelah Pemberian Madu Hutan
kelompok perlakuan dan antara kelompok perlakuan dan kelompok kontrol negatif. Pada Tabel VII menunjukkan bahwa terdapat perbedaan yang bermakna antara kelompok kontrol negatif (akuades 2,5 mL/200 g BB) terhadap kelompok madu hutan dosis 0,27 mL/200 g BB, kelompok madu hutan dosis 0,54 mL/200 g BB dan kelompok madu hutan dosis 1,08 mL/200 g BB. Hal ini menunjukkan bahwa pemberian madu hutan memberikan pengaruh terhadap aktivitas fagositosis makrofag, yaitu berupa peningkatan aktivitas fagositosis makrofag (Gambar 9). Pada Tabel VIII menunjukkan bahwa peningkatan aktivitas fagositosis makrofag seiring meningkatnya peringkat dosis madu hutan, yaitu pada madu hutan dosis 0,27 mL/200 g BB sebesar 69,23 %, madu hutan dosis 0,54 mL/200 g BB sebesar 79, 33%, dan madu hutan dosis 1,08 mL/200 g BB sebesar 98,55%.
mL/200 g BB begitu pula pada dosis madu hutan 1,08 mL/200 g BB peningkatan peringkat dosis hanya dua kali dari madu hutan dosis 0,54 mL/200 g BB, sehingga hasil uji statistik tidak menunjukkan hasil yang berbeda bermakna. Namun, bila dilihat dari grafik rata-rata aktivitas fagositosis makrofag (Gambar 9) terdapat peningkatan aktivitas fagositosis makrofag seiring naiknya peringkat dosis madu hutan.
Berdasarkan hasil penelitian yang didapat maka dapat dibuktikan bahwa pemberian madu hutan mampu memberikan pengaruh berupa peningkatan aktivitas fagositosis makrofag. Aktivitas fagositosis makrofag meningkat seiring peningkatan dosis madu hutan yang diberikan pada hewan uji (Tabel VII).
D.Pengaruh Pemberian Madu Hutan Dosis 0,27 mL/200 g BB; 0,54 mL/200 g BB; dan 1,08 mL/200 g BB terhadap Kapasitas Fagositosis Makrofag pada
Hewan Uji Tikus Jantan Galur Wistar
Hasil uji Kolmogorov-Smirnov (Lampiran 13), didapat nilai p = 0,927 (p > 0,05) sehingga dapat dinyatakan bahwa data kapasitas fagositosis makrofag terdistribusi normal.
Tabel IX. Purata ± SD Kapasitas Fagositosis Makrofag setelah Pemberian Madu Hutan
Tabel X. Hasil Analisis Uji Post-hoc Tukey Kapasitas Fagositosis Makrofag setelah (B) : Berbeda bermakna; (TB) : Berbeda tidak bermakna
Gambar 10. Grafik Rata-rata ± SD Kapasitas Fagositosis Makrofag setelah Pemberian Madu Hutan
menunjukkan bahwa kelompok kontrol negatif (akuades 2,5 mL/200 g BB) berbeda bermakna dengan kelompok madu hutan dosis 0,27 mL/200 g BB, kelompok madu hutan dosis 0,54 mL/200 g BB dan madu hutan dosis 1,08 mL/200 g BB. Hal ini menunjukkan bahwa pemberian madu hutan mampu memberikan pengaruh berupa peningkatan terhadap kapasitas fagositosis makrofag (Gambar 10). Kapasitas fagositosis makrofag antara kelompok perlakuan madu hutan dibanding kontrol negatif (Gambar 10 dan Tabel XI) meningkat seiring kenaikan peringkat dosis, yaitu pada madu hutan dosis 0,27 mL/200 g BB sebesar 65,34%, dosis madu hutan dosis 0,54 mL/200 g BB sebesar 94,97%, dan madu hutan dosis 1,08 mL/200 g BB sebesar 105,56%.
Hasil kapasitas fagositosis makrofag meningkat sesuai dengan peningkatan aktivitas fagositosis makrofag, hasil ini sesuai dengan penelitian Hasanah (2005) yang menyatakan bahwa peningkatan aktivitas fagositosis makrofag sebanding dengan peningkatan kapasitas fagositosis makrofag.
kelompok perlakuan sehingga diperoleh dosis yang optimal untuk meningkatkan kapasitas fagositosis makrofag secara maksimal.
41
BAB V
KESIMPULAN DAN SARAN
A.Kesimpulan
Pemberian madu hutan berpengaruh terhadap aktivitas dan kapasitas fagositosis makrofag pada hewan uji, yaitu berupa peningkatan aktivitas dan kapasitas fagositosis makrofag yang signifikan dibanding kontrol negatif.
B.Saran
1. Perlu dilakukan penelitian lebih lanjut mengenai dosis madu hutan yang memberikan respon peningkatan aktivitas dan kapasitas fagositosis makrofag secara maksimal untuk lebih mengetahui pengaruhnya terhadap respon imun. 2. Perlu penelitian lebih lanjut untuk mengidentifikasi senyawa dalam madu
42
DAFTAR PUSTAKA
Abbas, A. K., Lichtman, A. H., and Pober J. S., 2000, Cellular and Molecular
Immunology, 4th ed, WB Saunders Co, Philadelphia.
Abbas, A. K., and Lichtman, A. H., 2005, Cellular and Mollecular Imunology, 5th ed., Elsevier Publisher, Philadelphia. Inflicted Wounds: An Animal Model, MJIAS, 13 (3),125-132.
Arsani, R. B., 2010, Pengaruh Pemberian Ekstrak Etanolik Daun Kersen
(Muntingia calabura L.) terhadap Peningkatan Titer Imunoglobulin G
(IgG) dan Fagositosis Makrofag pada Tikus yang Diinduksi Vaksin Hepatitis B, Skripsi, Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta.
Baratawidjaja, K. G., D.I. Rengganis, 2010, Imunologi Dasar, edisi ke-9, hal. 29, 38, 39, 61-64, 69,71, Fakultas Kedokteran Universitas Indonesia, Jakarta. Basuki, P.S., 2005, Infeksi Bakteri Intraseluler pada Anak, Fakultas Kedoketeran
Universitas Airlangga, Surabaya.
Cahanar, P. dan Irwan S., 2006, Makan Sehat dan Hidup Sehat, hal. 81, Penerbit Buku KOMPAS, Jakarta.
Efendi, Z., 2003, Daya Fagositosis Makrofag pada Jaringan Ikat Longgar Tubuh, Bagian Histologi Fakultas Kedokteran Universitas Sumatera Utara, Sumatera Utara.
Febrita, D., 2011, Karakterisasi dan Uji Aktivitas Antioksidan Madu Hutan Lhoknga, Montasik dan Sare Kabupaten Aceh Besar secara
SpektrofotometriVisibel, http://repository.usu.ac.id/handle/123456789/29569,
diiakses tanggal 10 Mei 2012.
Hariyati, L.F., 2010, Aktivitas Antibakteri Berbagai Jenis Madu terhadap Mikroba Pembusuk (Pseudomonas fluorescens FNCC 0071 dan Pseudomonas
putida FNCC 0070), Skripsi, 3, 8, Fakultas Pertanian, Universitas
Hasanah, N., 2005, Pengaruh Pemberian Ekstrak Metanol Pasak Bumi (Eucycoma
longifolia Jack) pada Respon Imun Seluler terhadap Infeksi Listeria
monocytogenes: Kajian Aktivitas Fagositosis dan Sekresi Nitric Oxide
(NO) Makrofag Peritoneal Mencit, Tesis, Program Pascasarjana Universitas Gadjah Mada, Yogyakarta.
Haviva, 2011, Dahsyatnya Mukjizat Madu, hal. 12-14, DIVA Press (Anggota IKAPI), Yogyakarta.
Krell, R., 1996, Value-Added Product From Beekeeping, FAO Agricultural
Services Bulletine, 124, Food and Agriculture Organization of the United
Nations Rome, www.fao.org/docrep/w0076e/w0076e00.HTM, diakses tanggal 24 Juli 2011.
Kresno, S. B., 2010, IMUNOLOGI : Diagnosis dan Prosedur Laboratorium, edisi ke-5, 71, Badan Penerbit Fakultas Kedokteran Universitas Indonesia, Jakarta.
Kusmardi, S. Kumala, E. E. Triana, 2007, Efek Imunomodulator Ekstrak Daun Ketepeng Cina (Cassia alata L.) terhadap Aktivitas dan Kapasitas Fagositosis Makrofag, MAKARA KESEHATAN, 11 (2), 50-53.
Mardilah, Zakaria, F.R., dan Asydhad, L.A., 2006, Makanan Antikanker, 25, Kawan Pustaka, Jakarta
Mansooq, S., Singh P., Samoon M.H, and Balange A.K., 2010, Effect of Dietary Chitosan on Non-specific Immune Response and Growth of Cyprinus
carpio challenged with Aeromonas hydrophilic, Int Aquast Res, 2, 80.
Mulu, A., B. Tessema, and F. Derby, 2004. In vitro Assesment of The Antimicrobial Potential of Honey on Common Human Pathogen, Ethiop.
J. Health Dev., 18, 2.
Munawaroh, F., 2008, Pengaruh Pemberian Ekstrak Etanolik 30 % Daun Sembung (Blumea balsamifera {L.} DC.) terhadap Fagositosis Makrofag pada Mencit Jantan yang Diinfeksi dengan Listeria monocytogenes,
Skripsi, Fakultas Farmasi Universitas Gadjah Mada, Yogyakarta.
Ngatidjan, 1991, Petunjuk Laboratorium Metode Laboratorium dalam
Toksikologi, hal. 94, Pusat Antar Universitas Bioteknologi Universitas
Gadjah Mada, Yogyakarta.
Roitt, I.M., 2002, Imunologi (EssensialImunology), diterjemahkan oleh Haraha A., edisi VIII, Widya Medika, Jakarta.
Rosanti, T.I., 2005, Pengaruh Infeksi Brugia malayi dan Imunisasi Protein Ekskretori-sekretori Brugia malayi terhadap Aktivasi Makrofag dan Proriferasi Limfosit T (Meriones unguiculatus): Kajian pada Mencit Balb/c dan Gerbil (Meriones unguiculatus), Tesis, Program Pascasarjana Univesitas Gadjah Mada, Yogyakarta.
Sambodo, N.W., 2009, Uji Efek Tonik Madu Rambutan pada Mencit Putih Jantan dengan Metode Natatory Exhaustion, Skripsi, 5, Universitas Muhammadiyah, Surakarta.
Sheehan, C., 1997, Clinical Immunology : Principles and Laboratory Diagnosis, 2nd edition, 130-131, Lippincontt-Raven Publishers, Philadelphia, New York.
Sriningsih, Wibowo, A.H., 2006, Efek Protektif Pemberian Ekstrak Etanol Herba Meniran (Phyllanthus niruri L.) terhadap Aktivitas dan Kapasitas Fagositosis Makrofag Peritoneum Tikus, Artocarpus, 6, 95.
Sumoprastowo, R.M., dan Suprapto, A.G., 1980, Beternak Lebah Madu Modern, Bhratara Karya Aksara, Jakarta.
Suranto, A., 2007, Terapi Lebah, hal. 27-28, 30-32, 49, Penebar Plus, Jakarta. Tan, B.K.H. and Vanitha, J., 2004, Immunomodulatory and Antimicrobial Effects
of Some Traditional Chinese Medicinal Herbs, CMC, 11 (11), 1423-1430.
Vanani, A.H., 2011, Pengaruh Sediaan Madu Propolis terhadap Kemampuan Fagositosis Makrofag pada Peritonium Mencit yang Diinfeksi
Plasmodium berghei, Skripsi, Fakultas Kedokteran, Universitas Gadjah
Mada, Yogyakarta.
Wagner, H., and K. Jurcic, 1991, Assay for Immunomodulation and Effect on Mediators og Inflammation, In: Methods in Plants Biochemestry : Assay
for Bioactivity, Ed. VI., PM Dey and JB Harborne (Eds.) Academic
Press, London.
Widianto, M.B., 1987, Imunomodulator, Cermin Dunia Kedokteran, 44, 43
World Health Organization, 1993, Research Guidelines for Evaluating the Safety
and Efficacy of Herbal Medicines, World Health Organization Regional
Lampiran 3. Foto Perbandingan Warna antara Madu Hutan dengan Madu Ternak
(a) (b)
Lampiran 4. Komposisi Media Tumbuh Makrofag
1. Medium RPMI
RPMI : 10,4 g NaHCO3 : 2 g
Hepes : 2,6 g Aquades add 1000 mL
2. Medium Komplit
Medium RPMI : 100 mL
FBS : 10 mL
Lampiran 5. Perhitungan Dosis Pemberian Madu Hutan pada Hewan Uji Tahap Orientasi Dosis
1. Dosis madu hutan
Madu hutan 1 sendok makan = 15 mL
Faktor konversi manusia (70 kg) ke tikus (200g) = 0,018 Dosis madu hutan untuk tikus 200 g
= 0,018 x 15 mL
= 0,27 mL/200 g BB tikus
Larutan madu dibuat dengan melakukan pengenceran : 20 mL madu hutan + aquadest 100 mL larutan madu
Jadi, dalam 1 mL larutan madu mengandung 0,2 mL madu hutan. 2. Perhitungan dosis kelompok perlakuan madu hutan
a. Dosis 1 = 0,27 mL/200 g BB tikus
b. Dosis 2 = 1,5 x 0,27 mL/200 g BB tikus = 0,405 mL/200 g BB tikus c. Dosis 3 = 2 x 0,27 mL/200 g BB tikus = 0,54 mL/200 g BB tikus 3. Perhitungan volume pemberian madu hutan
Dosis madu hutan hasil konversi adalah 0,27 mL/200 g BB tikus, sehingga volume pemberian larutan madu adalah 1,35 mL/200 g BB tikus.
a. Volume pemberian dosis 1 = 1,35 mL/200 g BB tikus b. Volume pemberian dosis 2 = 1,5 x 1,35 mL/200 g BB tikus
= 2,03 mL/200 g BB tikus c. Volume pemberian dosis 3 = 2 x 1,35 mL/200 g BB tikus
= 2,7 mL/200 g BB tikus 4. Tabel volume pemberian larutan madu pada hewan uji
(volume pemberian x berat badan tikus)
Kelompok perlakuan Orientasi (mL)
Akuades (2,5 mL/200 g BB)
2,3
1,8
1,8
Madu Hutan (1,35 mL/200 g BB tikus)
0,9
0,8
1,05
Madu Hutan (2,03 mL/200 g BB tikus)
1,7
1,5
1,6
Madu Hutan (2,7 mL/200 g BB tikus)
2,3
1,9
Lampiran 6. Data Aktivitas Fagositosis Makrofag Tahap Orientasi Dosis
Kelompok Perlakuan Replikasi Aktivitas fagositosis (%)
Akuades (2,5 mL/200 g BB)
1 13
2 48
3 20
Madu Hutan (1,35 mL/200 g BB tikus)
1 75
2 74
3 56
Madu Hutan (2,03 mL/200 g BB tikus)
1 64
2 75
3 80
Madu Hutan (2,7 mL/200 g BB tikus)
1 68
2 81
Lampiran 7. Data Kapasitas Fagositosis Makrofag Tahap Orientasi Dosis
Kelompok Perlakuan Replikasi Kapasitas fagositosis
Akuades (2,5 mL/200 g BB)
1 14
2 79
3 24
Madu Hutan (1,35 mL/200 g BB tikus)
1 112
2 106
3 88
Madu Hutan (2,03 mL/200 g BB tikus)
1 90
2 111
3 71
Madu Hutan (2,7 mL/200 g BB tikus)
1 102
2 129
Lampiran 8. Hasil Analisis Aktivitas Fagositosis Makrofag Tahap
Normal Parametersa Mean 57.7500 Std. Deviation 23.19140 Most Extreme Differences Absolute .190
Positive .158
Negative -.190
Kolmogorov-Smirnov Z .657
Asymp. Sig. (2-tailed) .782
a. Test distribution is Normal.
One way
Descriptives Makrofag
N Mean Std. Deviation Std. Error
95% Confidence Interval for Mean
Minimum Maximum Lower Bound Upper Bound
1 3 27.0000 18.52026 10.69268 -19.0069 73.0069 13.00 48.00 2 3 68.3333 10.69268 6.17342 41.7713 94.8954 56.00 75.00 3 3 73.0000 8.18535 4.72582 52.6665 93.3335 64.00 80.00 4 3 62.6667 21.50194 12.41415 9.2529 116.0804 39.00 81.00 Total 12 57.7500 23.19140 6.69478 43.0149 72.4851 13.00 81.00
Test of Homogeneity of Variances
Post Hoc Tests
*. The mean difference is significant at the 0.05 level.
Lampiran 9. Hasil Analisis Kapasitas Fagositosis Makrofag Tahap
Normal Parametersa Mean 83.0833 Std. Deviation 34.70776 Most Extreme Differences Absolute .197
Positive .122
Negative -.197
Kolmogorov-Smirnov Z .683
Asymp. Sig. (2-tailed) .739
a. Test distribution is Normal.
Oneway
Descriptives Makrofag
N Mean Std. Deviation Std. Error
95% Confidence Interval for Mean
Minimum Maximum Lower Bound Upper Bound
Lampiran 10. Perhitungan Dosis Pemberian Madu Hutan pada Hewan Uji Tahap Percobaan
1. Dosis madu hutan = 0,27 mL/200 g BB tikus
2. Perhitungan dosis kelompok perlakuan madu hutan (faktor pengali = 2) a. Dosis 1 = 0,27 mL/200 g BB tikus
b. Dosis 2 = 2 x 0,27 mL/200 g BB tikus = 0,54 mL/200 g BB tikus c. Dosis 3 = 4 x 0,27 mL/200 g BB tikus = 1,08 mL/200 g BB tikus 3. Perhitungan volume pemberian madu hutan
Larutan madu dibuat dengan melakukan pengenceran : 40 mL madu hutan + aquadest 100 mL larutan madu
Jadi, dalam 1 mL larutan madu mengandung 0,4 mL madu hutan.
Dosis madu hutan hasil konversi adalah 0,27 mL/200 g BB tikus, sehingga volume pemberian larutan madu adalah 0,675 mL/200 g BB tikus.
a. Volume pemberian dosis 1 = 0,675 mL/200 g BB tikus b. Volume pemberian dosis 2 = 2 x 0,675 mL/200 g BB tikus
= 1,35 mL/200 g BB tikus c. Volume pemberian dosis 3 = 4 x 0,675 mL/200 g BB tikus
= 2,7 mL/200 g BB tikus 4. Tabel volume pemberian larutan madu pada hewan uji
(volume pemberian x berat badan tikus)
Kelompok perlakuan Perlakuan (mL)
Akuades (2,5 mL/200 g BB)
Madu Hutan (0,27 mL/200 g BB tikus)
0,78
0,89
0,73
0,72
0,68
Madu Hutan (0,54 mL/200 g BB tikus)
1,24
1,54
2,5
2,7
2,5
Madu Hutan (1,08 mL/200 g BB tikus)
2,6
2,9
0,78
0,89
Lampiran 11. Penimbangan Berat Badan Hewan Uji untuk Tahap Percobaan
Kelompok perlakuan Sebelum perlakuan
(g)
Madu Hutan (0,27 mL/200 g BB tikus)
Madu Hutan (0,54 mL/200 g BB tikus)
Lampiran 12. Data Aktivitas Fagositosis Makrofag Tahap Percobaan
Perlakuan Replikasi Aktivitas makrofag
(%)
Madu Hutan (0,27 mL/200 g BB tikus)
1 74
2 67
3 67
4 69
5 75
Madu Hutan (0,54 mL/200 g BB tikus)
1 76
2 78
3 70
4 78
5 71
Madu Hutan (1,08 mL/200 g BB tikus)
1 86
2 80
3 78
4 91
Lampiran 13. Data Kapasitas Fagositosis Makrofag Tahap Percobaan
Perlakuan Replikasi Kapasitas makrofag
Akuades (2,5 mL/200 g BB)
Madu Hutan (0,27 mL/200 g BB tikus)
1 104
2 100
3 185
4 120
5 116
Madu Hutan (0,54 mL/200 g BB tikus)
1 141
2 150
3 173
4 153
5 120
Madu Hutan (1,08 mL/200 g BB tikus)
1 138
2 156
3 140
4 163
Lampiran 14. Hasil Analisis Aktivitas Fagositosis Makrofag Tahap
Normal Parametersa Mean 67.3000 Std. Deviation 16.48955 Most Extreme Differences Absolute .243
Positive .121 Negative -.243 Kolmogorov-Smirnov Z 1.086 Asymp. Sig. (2-tailed) .189
a. Test distribution is Normal.
Oneway
95% Confidence Interval for Mean
Minimum Maximum
Lower Bound Upper Bound
1 5 41.6000 5.68331 2.54165 34.5432 48.6568 36.00 49.00
2 5 70.4000 3.84708 1.72047 65.6232 75.1768 67.00 75.00
3 5 74.6000 3.84708 1.72047 69.8232 79.3768 70.00 78.00
4 5 82.6000 5.72713 2.56125 75.4888 89.7112 78.00 91.00
Total 20 67.3000 16.48955 3.68718 59.5827 75.0173 36.00 91.00
Test of Homogeneity of Variances
Post Hoc Tests
*. The mean difference is significant at the 0.05 level.
Homogeneous Subsets
Lampiran 15. Hasil Analisis Kapasitas Fagositosis Makrofag Tahap
Normal Parametersa Mean 125.8500 Std. Deviation 39.09270 Most Extreme Differences Absolute .122
Positive .065
Negative -.122
Kolmogorov-Smirnov Z .546
Asymp. Sig. (2-tailed) .927
Post Hoc Tests
*. The mean difference is significant at the 0.05 level.
Homogeneous Subsets