1
UJI KEMAMPUAN PIPA PERFORATED ALUMINIUM DAN PIPA TEMBAGA PADA REAKTOR DESALINASI ELEKTROGRAVITASI UNTUK MENURUNKAN
KLORIDA
THE ABILITY OF PERFORATED ALUMINUM PIPE AND COPPER PIPE ON THE ELECTROGRAVITATIONAL DESALINATION REACTOR TO REMOVE CHLORIDE
Rizka Rachmania1) dan Wahyono Hadi
1) Jurusan Teknik Lingkungan FTSP-ITS Surabaya Abstrak
Teknologi desalinasi umumnya membutuhkan energi listrik yang besar dan mahal. Salah satu alternatif teknologi desalinasi yang digunakan tanpa memerlukan energi listrik dalam pengoperasiannya adalah teknologi desalinasi elektrogravitasi. Penelitian ini bertujuan untuk mengetahui kemampuan pipa aluminium berlubang dan pipa tembaga pada reaktor desalinasi elektrogravitasi sehingga dapat diketahui jumlah konsentrasi klorida yang dapat diturunkan dengan menggunakan reaktor ini.
Dilakukan variasi konsentrasi klorida dari larutan garam artifisial dengan konsentrasi klorida 1.000 ppm, 2.500 ppm, dan 5.000 ppm serta variasi waktu kontak 6 jam, 12 jam, dan 24 jam. Pengambilan sampel dilakukan setiap 6 jam sekali setelah melalui waktu kontaknya hingga waktu operasi 36 jam. Parameter yang diuji adalah: konsentrasi klorida, kekeruhan, dan pH.
Hasil Penelitian menunjukkan bahwa semakin rendah konsentrasi klorida dan semakin lama waktu kontak serta operasi, maka efisiensi penurunan yang di dapatkan juga semakin besar. Semakin besar konsentrasi, maka pH dan kekeruhan juga semakin besar. Penurunan tertinggi terjadi dengan waktu kontak 24 jam pada waktu pengambilan sampel pada jam ke 36 dengan efisiensi penurunan sebesar 24,39 %.
Kata kunci : Air payau, Klorida, Desalinasi, Desalinasi elektrogravitasi Abstract
Desalination technology generally need large electrical energy and the cost is expensive. One of alternative desalination technologies without using electrical energy in its operation is electrogravitational desalination technology. This study aims to determine the ability of perforated aluminum pipe and copper pipe on the electrogravitational desalination reactor, to know the amount of chloride concentration that can be removed by using this reactor.
This research use variations of chloride concentration: 1.000 ppm, 2.500 ppm and 5.000 ppm and the variation of contact time : 6 hours, 12 hours, and 24 hours. Sampling was performed every 6 hours after the detention time up to 36 hours operating time. Parameters tested are: the concentration of chloride, turbidity, and pH.
Result shows that the lower concentration of chloride and the longer contact time in operation, increased the removal efficiency of chloride to the highest level. The greater concentration of chloride, the biggest pH and turbidity. The removal of chloride occurred with the highest contact time of 24 hours at the time of sampling at the 36 hours with an efficiency of 24,39%.
2 1. PENDAHULUAN
Teknologi desalinasi secara umum dapat dibagi menjadi dua kategori utama yakni distilasi termal yang meliputi : MSF (multi-stage flash), MED (multiple effect distillation) dan Reverse Osmosis (RO) (AMTA, 2007). MSF dan MED membutuhkan dua energi untuk pengoperasiannya yakni energi termal dan listrik. MSF membutuhkan energi listrik sebesar 3,5–5,0 kWh/m3 sedangkan kebuthan energi listrik untuk MED adalah sebesar 1,5–0,5 kWh/m3
(ESCWA, 2009). Kebutuhan energi listrik RO dalam pengoperasiannya untuk mengolah air laut sebesar 4–8 kWh/m3
dan untuk air payau sebesar 2-3 kWh/m3.
Kedua macam teknologi desalinasi tersebut membutuhkan energi listrik yang besar dan mahal sehingga kurang cocok jika digunakan di negara berkembang seperti Indonesia. Kebutuhan listrik semakin meningkat tetapi pasokan energi listrik masih terbatas sehingga teknologi tersebut kurang cocok jika direncanakan di Indonesia. Listrik telah menjadi kebutuhan masyarakat luas di Indonesia, namun masih tetap meresahkan karena masih banyak terjadi pemadaman bergilir dan ada beberapa daerah yang belum terlayani listrik di Indonesia.
Oleh karena itu, dikembangkan suatu teknologi desalinasi elektrogravitasi sebagai suatu metode sederhana yang dapat menghilangkan garam air laut yang tidak menggunakan energi eksternal (Aul, 1969). Metode ini memanfaatkan beda potensial antarelektroda serta memanfaatkan proses elektrokimia dan gravitasi dengan menggunakan aluminium sebagai anoda dan tembaga sebagai katoda yang dapat menghilangkan konsentrasi garam dari air laut (Putra, 2010). Pada penelitian ini dilakukan penelitian dengan menggunakan pipa aluminium yang
diberi lubang dan pipa tembaga dikarenakan harganya murah dan mudah ditemukan di pasaran. Penelitian ini bertujuan untuk mengetahui kemampuan Al dan Cu dalam menurunkan konsentrasi klorida pada reaktor desalinasi elektrogravitasi.
2. METODE PENELITIAN 2.1 Pembuatan Larutan Stok
Membuat larutan stok garam murni dengan kandungan klorida yang disesuaikan dengan konsentrasi klorida yang digunakan dalam penelitian ini yakni 1.000 ppm, 2.500 ppm, dan 5.000 ppm. Larutan stok yang digunakan mengandung klorida sebesar 100.000 ppm. Sehingga, massa NaCl yang akan digunakan adalah: ArCl l g MrNaClx100 / l g l g x 164,7887 / 5 , 35 / 100 5 , 58
2.2 Pembuatan Reaktor Desalinasi Elektrogravitasi
Reaktor terdiri dari pipa tembaga dan pipa aluminium yang diberi lubang. Diameter pipa tembaga luar 2,857cm dan panjang 195 cm. Pipa aluminium 1,5875 cm dengan panjang 190 cm dan memiliki luas permukaan 0,17 m2. Volume reaktor adalah 1.029 ml. Reaktor dioperasikan secara upflow dengan variasi waktu kontak 6 jam, 12 jam, dan 24 jam. 3. HASIL DAN PEMBAHASAN 3.1 Perubahan Konsentrasi Klorida
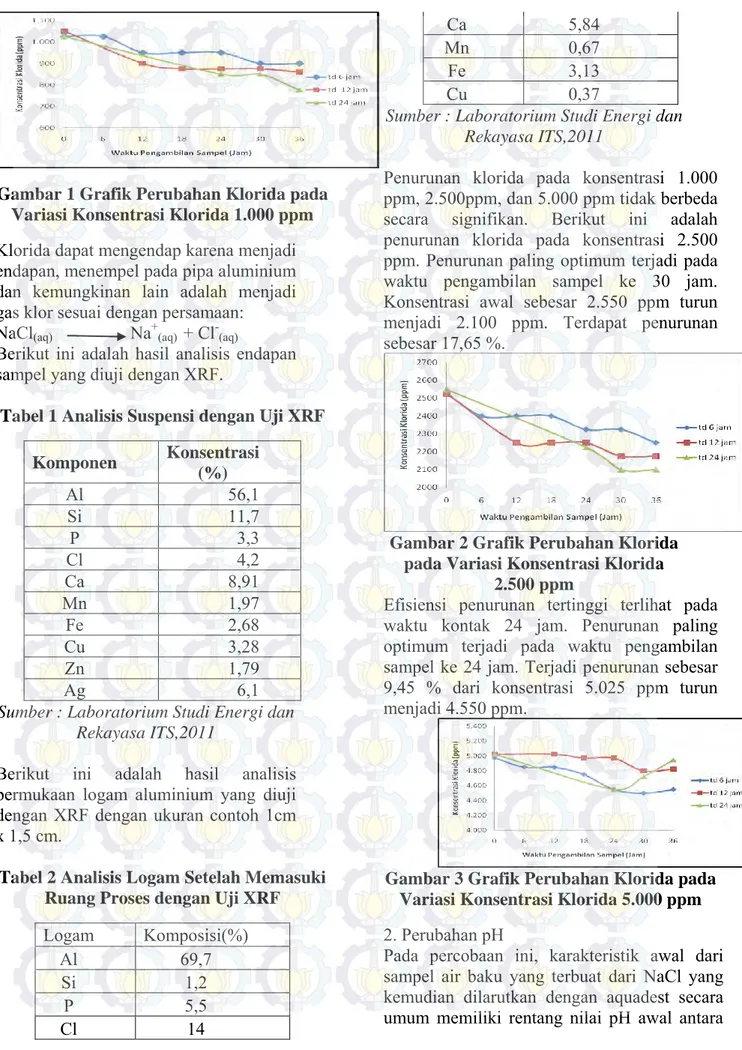
Klorida yang dapat diturunkan dengan menggunakan reaktor ini tertinggi terjadi pada konsentrasi 1.000 ppm dengan penurunan sebesar 24,39%. Penurunan paling optimum terjadi pada waktu pengambilan sampel ke 36 jam dan waktu kontak 24 jam.
3 Gambar 1 Grafik Perubahan Klorida pada
Variasi Konsentrasi Klorida 1.000 ppm Klorida dapat mengendap karena menjadi endapan, menempel pada pipa aluminium dan kemungkinan lain adalah menjadi gas klor sesuai dengan persamaan:
NaCl(aq) Na+(aq) + Cl-(aq)
Berikut ini adalah hasil analisis endapan sampel yang diuji dengan XRF.
Tabel 1 Analisis Suspensi dengan Uji XRF Komponen Konsentrasi (%) Al 56,1 Si 11,7 P 3,3 Cl 4,2 Ca 8,91 Mn 1,97 Fe 2,68 Cu 3,28 Zn 1,79 Ag 6,1
Sumber : Laboratorium Studi Energi dan Rekayasa ITS,2011
Berikut ini adalah hasil analisis permukaan logam aluminium yang diuji dengan XRF dengan ukuran contoh 1cm x 1,5 cm.
Tabel 2 Analisis Logam Setelah Memasuki Ruang Proses dengan Uji XRF Logam Komposisi(%) Al 69,7 Si 1,2 P 5,5 Cl 14 Ca 5,84 Mn 0,67 Fe 3,13 Cu 0,37
Sumber : Laboratorium Studi Energi dan Rekayasa ITS,2011
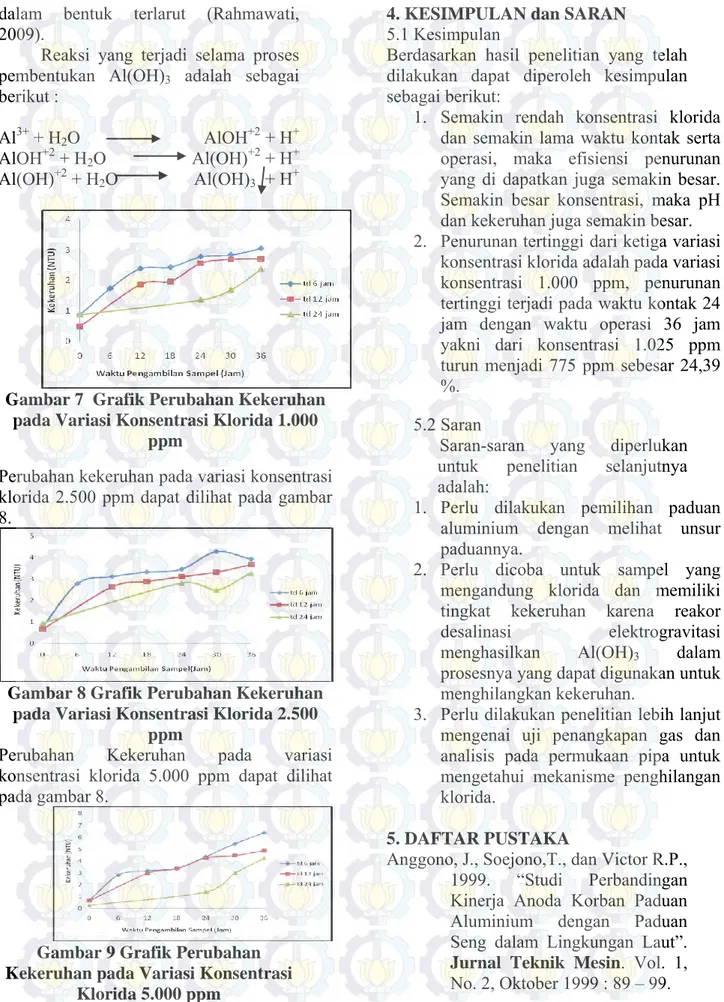
Penurunan klorida pada konsentrasi 1.000 ppm, 2.500ppm, dan 5.000 ppm tidak berbeda secara signifikan. Berikut ini adalah penurunan klorida pada konsentrasi 2.500 ppm. Penurunan paling optimum terjadi pada waktu pengambilan sampel ke 30 jam. Konsentrasi awal sebesar 2.550 ppm turun menjadi 2.100 ppm. Terdapat penurunan sebesar 17,65 %.
Gambar 2 Grafik Perubahan Klorida pada Variasi Konsentrasi Klorida
2.500 ppm
Efisiensi penurunan tertinggi terlihat pada waktu kontak 24 jam. Penurunan paling optimum terjadi pada waktu pengambilan sampel ke 24 jam. Terjadi penurunan sebesar 9,45 % dari konsentrasi 5.025 ppm turun menjadi 4.550 ppm.
Gambar 3 Grafik Perubahan Klorida pada Variasi Konsentrasi Klorida 5.000 ppm 2. Perubahan pH
Pada percobaan ini, karakteristik awal dari sampel air baku yang terbuat dari NaCl yang kemudian dilarutkan dengan aquadest secara umum memiliki rentang nilai pH awal antara
4 6,48 hingga 6,67 . Perubahan pH untuk konsentrasi klorida 1.000 ppm dapat diihat pada gambar 4.
Gambar Error! No text of specified style in document. Grafik Perubahan pH
pada Variasi Konsentrasi Klorida 1.000 ppm
Berdasarkan gambar 4, perlahan lahan pH akan naik kemudian terjadi penurunan nilai pH. Kenaikan pH disebabkan karena terjadi produksi ion OH- yang berlebih di katoda
yang berasal dari reduksi air dari senyawa H2O yang berfungsi sebagai katoda sesuai
dengan persamaan berikut:
2H2O + 2e- → H2 + 2OH-(aq) (Vick et al.,
1984) dan beberapa anion seperti Cl- yang
hadir dalam elektrolit akan bertukar sebagian dengan OH- di Al(OH)
3 untuk membebaskan
OH- yang dapat menyebabkan kenaikan pH
(Chen et al, 2000). Sedangkan penurunan pH disebabkan karena adanya reaksi hidrolisis Al yang akan membebaskan ion H+ sehingga dapat menekan nilai pH. Hal tersebut menandakan bahwa alkalinitas dalam air rendah. Pada dasarnya alkalinitas akan bereaksi dengan ion H+ untuk menjaga nilai
pH tetap stabil. Namun, apabila alkalinitas air rendah dan tidak ada penambahan buffer maka ion H+ dari reaksi hidrolisis akan
menyebabkan penurunan nilai pH (Hendricks, 2005). Semakin lama waktu kontak, maka kenaikan pH juga akan semakin tinggi hal ini dikarenakan waktu kontak memberikan waktu yang cukup untuk membentuk ion OH- dalam
larutan. Semakin cepat waktu kontak, maka produksi ion OH- sedikit sehingga akan
menyebabkan penurunan nilai pH.
Berikut ini adalah perubahan pH pada variasi konsentrasi 2.500 ppm dan 5.000 ppm.
Gambar 5 Grafik Perubahan pH pada Variasi Konsentrasi Klorida
2.500 ppm
3. Perubahan Kekeruhan Pada reaktor desalinasi elektrogravitasi ini terjadi oksidasi Al menjadi Al3+ pada anoda dan pada katoda
akan menghasilkan ion OH- hasil dari proses reduksi air sesuai dengan persamaan berikut ini :
Anoda
Al Al3+ + 3e-
Proses anodik mengakibatkan terlarutnya logam aluminium menjadi ion Al3+. Ion Al3+ yang terbentuk dalam
larutan akan mengalamai reduksi hidrolisis yang tidak dapat lagi larut dalam air (Nugroho, 2008).
Katoda
2H2O(l) +2e- H2(g)+2OH-
Ion Al3+ dari aluminium akan
bergabung dengan ion OH- dari reduksi air membentuk produk Al(OH)3.
Al(OH)3 yang bewarna putih ini
menyebabkan kekeruhan pada ruang proses dan pada sampel hasil olahan. Al(OH)3 merupakan koagulan yang
biasanya digunakan untuk menurunkan kekeruhan air yang mengandung koloid. Pembentukan Al(OH)3 terjadi pada
rentang pH 4,5 – 8,0. Pada pH < 4,5 dan pH > 8,0 sebagian besar aluminum hadir
Gambar 6 Grafik Perubahan pH pada Variasi Konsentrasi Klorida 5.000 ppm
5 dalam bentuk terlarut (Rahmawati, 2009).
Reaksi yang terjadi selama proses pembentukan Al(OH)3 adalah sebagai
berikut : Al3+ + H 2O AlOH+2 + H+ AlOH+2 + H 2O Al(OH)+2 + H+ Al(OH)+2 + H2O Al(OH)3 + H+
Gambar 7 Grafik Perubahan Kekeruhan pada Variasi Konsentrasi Klorida 1.000
ppm
Perubahan kekeruhan pada variasi konsentrasi klorida 2.500 ppm dapat dilihat pada gambar 8.
Gambar 8 Grafik Perubahan Kekeruhan pada Variasi Konsentrasi Klorida 2.500
ppm
Perubahan Kekeruhan pada variasi konsentrasi klorida 5.000 ppm dapat dilihat pada gambar 8.
Gambar 9 Grafik Perubahan Kekeruhan pada Variasi Konsentrasi
Klorida 5.000 ppm
4. KESIMPULAN dan SARAN 5.1 Kesimpulan
Berdasarkan hasil penelitian yang telah dilakukan dapat diperoleh kesimpulan sebagai berikut:
1. Semakin rendah konsentrasi klorida dan semakin lama waktu kontak serta operasi, maka efisiensi penurunan yang di dapatkan juga semakin besar. Semakin besar konsentrasi, maka pH dan kekeruhan juga semakin besar. 2. Penurunan tertinggi dari ketiga variasi
konsentrasi klorida adalah pada variasi konsentrasi 1.000 ppm, penurunan tertinggi terjadi pada waktu kontak 24 jam dengan waktu operasi 36 jam yakni dari konsentrasi 1.025 ppm turun menjadi 775 ppm sebesar 24,39 %.
5.2 Saran
Saran-saran yang diperlukan untuk penelitian selanjutnya adalah:
1. Perlu dilakukan pemilihan paduan aluminium dengan melihat unsur paduannya.
2. Perlu dicoba untuk sampel yang mengandung klorida dan memiliki tingkat kekeruhan karena reakor desalinasi elektrogravitasi menghasilkan Al(OH)3 dalam
prosesnya yang dapat digunakan untuk menghilangkan kekeruhan.
3. Perlu dilakukan penelitian lebih lanjut mengenai uji penangkapan gas dan analisis pada permukaan pipa untuk mengetahui mekanisme penghilangan klorida.
5. DAFTAR PUSTAKA
Anggono, J., Soejono,T., dan Victor R.P., 1999. “Studi Perbandingan Kinerja Anoda Korban Paduan Aluminium dengan Paduan Seng dalam Lingkungan Laut”. Jurnal Teknik Mesin. Vol. 1, No. 2, Oktober 1999 : 89 – 99.
6 AMTA (America's Authority in
Membrane Treatment). 2007. Improving America's Waters Through Membrane Treatment and Desalting, <URL: http://www. membranesamta.org/amta_medi a/pdfs/8_WaterDesalinationPro cesses.pdf>.
APHA, AWWA, dan, WPCF. 1999. Standards Methods for the Examination of Water and
Wastewater, 21th
ed..Washington: American Public Health Association.
Atkins, P.W. 1999. Kimia Fisika. Jakarta :Erlangga.
Aul, A.H. 1969.Electrogravitational Desalination of Saline Water. U.S. Patent #3,474,014 (Cl. 204-150).
Bardford, A. J. and Faulkner, L. R. 1992. Electrochemical Methods. New York: John Wiley & Sons.,Inc. Chang, R. 1998. Electrochemistry,
Chemistry, 6th Edition. United States of America : McGraw Hill.
Chen,X., Chen.,G dan Yue P.L. 2000. ”Separation of pollutants from restaurant wastewater by electrocoagulation” Separation Purification Technology. 19 : 65–76.
Effendi, H. 2003. Telaah Kualitas Air Bagi Pengelolaan Sumber Daya dan Lingkungan Perairan. Yogyakarta : Kanisius.
ESCWA (Economic and Social Commission for Western Asia). 2009. Role of Desalination in Addressing Water Scarcity,<URL:http://www.esc wa.un.org/information/publicati ons/edit/upload/sdpd-09-4.pdf>. Fontana, M.G. 1987. Corrosion Engineering. Singapore : Mc Graw Hill.
Gregory, J. 2006. Particles in Water. London: Taylor & Francis Group.
Heitmann HG. 1990. Saline Water Processing. New York: VCH Publishing.
Hendayana,S., Rohman,A., Sumarna,AA., dan Supriatna A. 1994. Kimia Analitik Instrumen. Semarang: IKIP Semarang Press.
Hendricks, D.W. 2005. Water Treatment Unit Processes: Physical and Chemical. USA: Taylor and Francis Groups.
Mankoedihardjo,S., dan S. Ganjar. 2010. Fitoteknologi Terapan . Yogyakarta:Graha Ilmu.
Lampean N., dan K.G. Petros. 1994. The Importance of the Solution pH in electrochemical Studies oF Aluminium in Aqueius Media Containing Chloride. Corrosion Science.Vol 36 No 6 : 1011- 1025.
Narmasari A. 2005. Proses Penyulingan Air Payau dengan Metode Desalinasi Sederhana.Tugas Akhir. Surabaya: ITS.
Nugroho,F.A. 2008. ”Pengembangan Model Pengolahan Air Baku
dengan Metode
Elektrokoagulasi”. Jurnal Teknik. Volume VII No 2. Purwoto S. 2006. Desalinasi Air Payau
Secara Penguapan dalam Ruang Kaca. Thesis. Surabaya: Teknik Lingkungan ITS.
Putra,D.G.B.P. 2010. Kapasitas Optimum Pada Reaktor Sistem Kontinu Electro Gravitational Desalination (EGD) Dalam Proses Penyisihan Sodium Klorida. Bandung: Tugas Akhir Teknik Lingkungan ITB.
Rahmawati,S.W., Bambang I.,dan Winarni. 2009. Pengaruh Ph Pada Proses Koagulasi Dengan Koagulan Aluminum Sulfat dan Ferri Klorida. Jurnal Teknologi Lingkungan. Vol. 5. No.2. Desember 2009 : 40-45.
7 Reynold, T.D., dan Richards, P.A. 1996.
Unit Operation and Processes in Environmental Engineering. Brooks/Cole Engineering Division. Monterey. California. Sawyer,C.N, P.L MC Carty, dan G.F.
Parkin. 2003. Chemistry for Environmental Engineering and Science, 5th Edition. New York: Mc Graw Hill.
Sinaga,H.K. 2008. Penyisihan Garam
Menggunakan Reaktor Electro-Gravitational Desalination
(EGD). Bandung : Tugas Akhir
TL ITB.
Siregar,T. 2010. “Laju Korosi Dan Mekanisme Inhibisi Aluminium Murni Menggunakan Kalium dan Kalsium Stearat”. Jurnal Kimia 4: 113-124.
Stuyfzand, P.J. 1986a. "A new hydrochemical classification of water types: principles and application to the coastal dunes aquifer system of the Netherlands". Proc. 9th Salt Water Intrusion Meeting, Delft 12-16 May, Delft Univ. Techn : 641-655.
Sutresna,N. 2007 . Cerdas Belajar Kimia. Jakarta: Grafindo Media Pratama.
Syukri,S. 1999. Kimia Dasar 2. Bandung :Penerbit ITB.
Vik E.A., Carlson D.A., dan Eikum A.S. 1984. ”Electrocoagulation of potable water”. Water
Research 18(11): 1355–1360. Vogel, 1990. Buku Teks Analisis
Anorganik Kualitatif Makro dan Semi Mikro. Jakarta: PT. Kalman Media Pustaka.