ANALISA KECUKUPAN PANAS PADA PROSES
PASTEURISASI SANTAN
Oleh :
RINI INDRIANI PRIHATINI F34104102
2008
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
Rini Indriani P. F34104102. Analisa Kecukupan Panas pada Proses Pasteurisasi Santan. Dibawah Bimbingan Mulyorini Rahayuningsih dan Sulusi Prabawati. 2008.
RINGKASAN
Kelapa adalah salah satu komoditas yang memegang peranan penting dalam kehidupan manusia sehari-hari. Di Indonesia, buah kelapa diusahakan melalui perkebunan besar maupun perkebunan rakyat. Buah kelapa di Indonesia sebagian besar dimanfaatkan untuk pembuatan kopra, kelapa sayur dan pembuatan minyak kelapa. Sebagian besar kelapa sayur digunakan dalam bentuk santan. Santan adalah emulsi minyak dalam air (o/w) yang berwarna putih, yang diperoleh dengan cara memeras daging kelapa segar yang telah diparut atau dihancurkan dengan atau tanpa penambahan air. Santan memiliki kandungan air, lemak dan protein yang cukup tinggi. Tingginya kadar air, lemak dan protein tersebut menyebabkan santan sangat mudah rusak. Oleh karena itu, diperlukan suatu teknologi untuk membuat santan menjadi lebih lama umur simpannya. Salah satu metode pengawetan santan adalah dengan menggunakan metode pasteurisasi. Permasalahannya adalah bahwa selama ini suhu dan waktu pasteurisasi yang digunakan adalah masih mengacu pada produk lain karena belum ada data tentang suhu dan waktu optimal pasteurisasi santan. Oleh karena itu, perlu dilakukan penelitian untuk menghitung kecukupan panasnya. Dengan menghitung nilai kecukupan panas, dapat diperoleh suhu serta waktu terbaik untuk pasteurisasi santan.
Penelitian dilakukan dengan cara memanaskan santan dalam tabung ulir pada suhu 65 oC, 75 oC dan 85oC dengan waktu 0, 5, 10, 15 dan 20 menit. Jumlah mikroba yang terdapat dalam santan dihitung. Ketahanan panas mikroba biasanya dinyatakan dengan istilah waktu reduksi atau waktu yang dibutuhkan pada suhu tertentu untuk menurunkan jumlah sel atau spora sepuluh kali lipat (nilai z). Sebelum menentukan nilai z, terlebih dahulu ditentukan kurva kematian mikroba (nilai D). Setelah itu dilakukan perhitungan kecukupan panas yang dinyatakan dengan nilai pasteurisasi (P). Untuk menghitung proses pemanasan pada pasteurisasi biasanya digunakan konsep 5D atau di bawahnya tergantung jumlah mikroba awalnya (Fellow, 1992). Rancangan percobaan yang dilakukan adalah rancangan acak lengkap faktorial, dengan uji lanjut Duncan. Penentuan kondisi terbaik dilakukan dengan metode pembobotan.
Santan tanpa pemanasan memiliki jumlah mikroba sebesar 3,5 x105 koloni/ml. Sementara itu untuk populasi kapang jumlahnya lebih rendah yaitu 4 x 103 koloni/ml. Populasi kapang bernilai nol pada suhu 65oC pada waktu selama 10 menit. Berdasarkan hasil perhitungan pada populasi bakteri diperoleh nilai D65oC
= 12,89 menit, D 75oC = 10,95 menit, D 85oC = 3,55 menit, nilai z = 35,71 oC.
Berdasarkan hasil perhitungan, bakteri pada santan memiliki ketahanan panas yang lebih tinggi dibandingkan kapang, maka nilai z bakteri digunakan sebagai acuan dalam perhitungan nilai kecukupan panas (nilai P). Hasil perhitungan menunjukkan bahwa nilai kecukupan panas (nilai P) pada santan adalah sebesar 16,3 menit. Dari nilai ini selanjutnya dapat dikembangkan menjadi beberapa kombinasi suhu dan waktu pemanasan. Dari kombinasi suhu dan waktu pemanasan tersebut dipilih enam kombinasi yang akan dianalisa sifat fisiko kimianya untuk melihat nilai nutrisi pada santan. Kombinasi tersebut adalah
adalah 65 oC/59,2 menit, 70 oC/42,9 menit, 75 oC/31,2 menit, 80 oC/22,5 menit, 85
oC/16,3 menit dan 90oC/11,8 menit. Berdasarkan hasil analisa fisiko kimia,
diperoleh kondisi terbaik adalah pada 75 oC /31,2 menit, dengan kondisi mutu
kadar air 63,23 persen, kadar abu 0,49 persen, kadar protein 2,25 persen, kadar lemak 12,71 persen, pH 7,25, viskositas 7, stabilitas emulsi 17,24 persen, derajat putih 47,65, bilangan peroksida 0, bilangan asam 1,58, FFA 0,56 persen, total mikroba 0, nilai kesukaan aroma 3,80, nilai kesukaan warna 4,47, nilai kesukaan penampakan umum 3,93.
Rini Indriani P. F34104102. Analysis of Thermal Sufficiency in Pasteurization Process of Coconut Milk. Supervised by Mulyorini
Rahayuningsih and Sulusi Prabawati. 2008.
SUMMARY
Coconut is a main commodity of human dairy needs. Coconuts in Indonesia are produced in large plantation and small masses plantation. This coconut is exploited as copra, coconut oil and coconut milk. Coconut milk is white colored oil in water emulsion which is obtained from squeezing the fresh grinded coconut with or without water addition. Coconut milk contains a large number of water, fat and protein that makes the coconut milk more perishable. It needs more advance technology that can make the coconut milk more endure. One of the well known and the cheapest preserving methods is pasteurization. The problem is there are no data’s that referring the temperature and the optimal time of pasteurization process of coconut milk. So we have to calculate the thermal sufficiency to get the best condition for coconut milk pasteurization.
This research was done using three kinds of temperature (65oC, 75oC and 85oC) with heating time (0, 5, 10, 15 and 20 minutes). The amount of microbe in pasteurized coconut milk was counted. The thermal resistancy of microbe is determine with reduction time or time that needed to decrease amount of cell or spore ten times (z value). Before determining the z value, it needs to determine the curve of cell mortality first (D value). After that the pasteurization value (P) can be determined. To count the heating process of pasteurization usually using 5D concept or below depending amount of first microbe measured. (Fellow, 1992). The complete random design and Duncan test are used whereas to determine the best process for this research was done using the ranking method.
Unheated coconut milk has amount of microbe 3.5 x 105 colony/ml. Otherwise, the mold population has zero amount at 65oC with heating time 10 minutes. D values can be obtained from counting bacteria population which are D65oC = 12,89 minutes, D75oC = 10,95 minutes, D85oC = 3,55 minutes and z =
35,71oC. According the result of measurement, bacteria in coconut milk has
higher thermal sufficiency than mold, so that the z value of bacteria is using as referential to determine the pasteurization value which is P = 16,3 minutes. From P value can be determined the combination between temperature and heating time. There are six combinations which are 65 oC/59,2 minutes, 70 oC/42,9 minutes, 75
oC/31,2 minutes, 80 oC/22,5 minutes, 85 oC/16,3 minutes and 90oC/11,8 minutes.
The best condition of this research at 75 oC /31,2 minutes with water content 63,23 percents, protein content 2,25 percents, fats content 12,71 percents, pH 7,25, viscocity 7 centipoise, stability of emulsion 17,24 percents, degree of white 47,65, peroxide number 0, acid number 1,58, free fatty acid content 0.56 percents, total microbe 0, aroma hedonic value 3,80, color hedonic value 4,47 and general condition hedonic value 3,93.
PERNYATAAN
Dengan ini saya menyatakan bahwa skripsi yang berjudul Analisa
Kecukupan Panas Pada Proses Pasteurisasi Santan adalah benar-benar karya
saya sendiri dengan bimbingan dosen pembimbing dan belum pernah digunakan sebagai karya ilmiah pada perguruan tinggi atau lembaga manapun. Sumber informasi yang berasal atau dikutip dari karya yang telah diterbitkan dari penulis lain telah disebutkan dalam tulisan dan dicantumkan dalam daftar pustaka di bagian akhir skripsi ini.
Bogor, September 2008
RIWAYAT HIDUP
Penulis dilahirkan di Majalengka pada tanggal 18 Januari 1986 dari pasangan Abdul Rosyid dan Munawaroh. Penulis merupakan anak kedua dari tiga bersaudara.
Penulis menempuh pendidikan formal pertama di TK Al Halim Santi Asromo Majalengka dari tahun 1991 hingga tahun 1992. Selanjutnya pada tahun 1992 penulis melanjutkan pendidikan dasar di SDN Singajaya hingga tahun 1998. Pada tahun yang sama penulis menempuh pendidikan di SLTP Negeri 4 Maja dan lulus tahun 2001. Selanjutnya penulis menempuh pendidikan di SMUN 1 Majalengka hingga tahun 2004.
Penulis diterima sebagai mahasiswa Institut Pertanian Bogor (IPB) pada tahun 2004 melalui jalur Seleksi Penerimaan Mahasiswa Baru (SPMB). Penulis diterima di Departemen Teknologi Industri Pertanian, Fakultas teknologi Pertanian, Institut Pertanian Bogor.
ANALISA KECUKUPAN PANAS PADA PROSES
PASTEURISASI SANTAN
Oleh :
RINI INDRIANI PRIHATINI F34104102
SKRIPSI
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
2008
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
DEPARTEMEN TEKNOLOGI INDUSTRI PERTANIAN FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
ANALISA KECUKUPAN PANAS PADA PROSES
PASTEURISASI SANTAN
SKRIPSI
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar
SARJANA TEKNOLOGI PERTANIAN
Pada Departemen Teknologi Industri Pertanian Fakultas Teknologi Pertanian
Institut Pertanian Bogor
Oleh :
RINI INDRIANI PRIHATINI F34104102
Dilahirkan pada Tanggal 18 Januari 1986 di Majalengka
Tanggal Lulus : September 2008
Bogor, September 2008 Disetujui,
Pembimbing I Pembimbing II
Dr. Ir. Mulyorini Rahayuningsih, MSi Ir. Sulusi Prabawati, MS NIP. 131 788 588 NIP. 080 068 204
KATA PENGANTAR
Alhamdulillah, puji serta syukur yang tak terhingga penulis panjatkan ke hadirat Allah SWT yang telah memberikan berbagai karunia sehingga penulis dapat menyelesaikan penyusunan skripsi ini. Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar sarjana pada Departemen Teknologi Industri Pertanian, Fakultas Teknologi Pertanian, Institut Pertanian Bogor.
Penulis telah banyak mendapat bimbingan, petunjuk serta bantuan dar berbagai pihak. Pada kesempatan ini, penghargaan dan ucapan terima kasih yang sebesar-besarnya penulis haturkan kepada :
1. Bapa, mamah, Aa, Ade tercinta yang telah memberikan motivasi, doa dan kasih sayang kepada penulis.
2. Dr. Ir. Mulyorini Rahayuningsih, MSi. sebagai dosen pembimbing I atas bimbingan yang telah diberikan kepada penulis.
3. Ir. Sulusi Prabawati MS, Sebagai dosen pembimbing II atas bimbingan yang telah diberikan kepada penulis.
4. Drs. Purwoko Msi. sebagai penguji sidang skripsi penulis yang telah memberikan berbagai masukan
5. Ermi Sukasih STP. Msi, Ir. Tatang Hidayat Msi, serta Sari Intan Kailaku STP., atas berbagai bantuan dan bimbingannya kepada penulis.
6. Mang Haris serta seluruh keluarga yang telah memberikan dorongan dan berbagai bantuan kepada penulis.
7. Pa Ato, Bu Ika, Pa Adom, Pa Tri, serta seluruh laboran Balai Besar Pascapanen Pertanian
8. Bu Ega, Pa Gun, Pa Darwan, Bu Sri, Pa Diki, Pa Sugi, Bu Nina, Pa Mul, Bu Teti, Bu Nur serta seluruh staff Departemen TIN atas berbagai benatuan yang telah diberikan.
9. Muhammad Havizh Abdillah atas semua dukungan dan dorongan pada penulis.
10. Sahabat-sahabat tercinta Lala, Ayi, Miranti, Sri, Farikha, Yani, Ina, Fahmi atas berbagai bantuan pada penulis.
11. Rekan-rekan seperjuangan di Laboratorium Balai Besar Pascapanen Pertanian Ami, Jajat, Usuy, Beni, Supardi.
12. Seluruh keluarga Departemen Teknologi Industri Pertanian khususnya angkatan 41.
13. Semua pihak atas bantuan dan kerjasama yang diberikan selama proses penelitian dan penyusunan skripsi.
Kritik dan saran yang membangun, sangat penulis harapkan untuk memperbaiki dan menyempurnakan penulisan skripsi baik untuk saat ini maupun di masa yang akan datang. Semoga skripsi ini dapat memberikan manfaat bagi semua pihak.
Bogor, September 2008
DAFTAR ISI
KATA PENGANTAR ... i
DAFTAR ISI... iii
DAFTAR TABEL... v
DAFTAR GAMBAR ... vi
DAFTAR LAMPIRAN... vii
I. PENDAHULUAN ... 1
A. LATAR BELAKANG... 1
B. TUJUAN ... 3
II. TINJAUAN PUSTAKA... 4
A. KELAPA ... 4 1. Botani Kelapa... 4 2. Buah Kelapa... 5 3. Kegunaan Kelapa ... 6 B. SANTAN KELAPA ... 7 1. Santan... 7
2. Kerusakan santan kelapa ... 8
C. PASTEURISASI SANTAN ... 10
1. Ketahanan Mikroba terhadap Panas... 12
2. Perhitungan Nilai Kecukupan Panas... 13
III. METODOLOGI PENELITIAN ... 15
A. ALAT DAN BAHAN ... 15
B. METODE PENELITIAN ... 15
1. Penelitian Pendahuluan ... 15
2. Penelitian Utama ... 16
3. Rancangan Percobaan ... 17
IV. HASIL DAN PEMBAHASAN... 19
A. JUMLAH MIKROBA AWAL... 19
B. KETAHANAN PANAS M IKROORGANISME... 19
D. PENGARUH PEMANASAN TERHADAP MUTU SANTAN... 24 1. Total Mikroba... 24 2. Stabilitas Emulsi ... 25 3. Viskositas ... 26 4. Derajat Putih ... 27 5. Bilangan Peroksida ... 28 6. Kadar Air... 29 7. Kadar Protein ... 30 8. Kadar Lemak... 32
9. Bilangan Asam dan FFA... 32
10. Nilai pH... 34
11. Organoleptik... 34
E. PENENTUAN KONDISI TERBAIK DENGAN METODE PEMBOBOTAN. ... 37
F. STANDAR MUTU... 38
V. KESIMPULAN DAN SARAN ... 41
A. KESIMPULAN ... 41
B. SARAN ... 42
DAFTAR PUSTAKA ... 43
DAFTAR TABEL
Tabel 1. Data Produksi Kelapa... 1
Tabel 2. Komposisi Buah Kelapa... 6
Tabel 3. Komposisi Santan ... 7
Tabel 4. Data Jumlah Mikroorganisme Awal ... 19
Tabel 5. Hasil perhitungan nilai D dan z populasi bakteri pada santan ... 20
Tabel 6. Nilai Pasteurisasi pada tiap Kombinasi Suhu dan Waktu... 23
Tabel 7. Kombinasi suhu dan waktu pasteurisasi pada nilai P 16,3 ... 24
Tabel 8. Penentuan Kondisi Terbaik Dengan Metode Pembobotan ... 38
Tabel 9. Standar Nasional Indonesia untuk Santan... 39
DAFTAR GAMBAR
Gambar 1. Diagram Alir Pembuatan santan pasteurisasi... 18
Gambar 2. Grafik Penetapan Nilai D dan z pada santan... 21
Gambar 3. Grafik Penetapan Nilai Pasteurisasi pada santan ... 23
Gambar 4. Grafik Perubahan Jumlah Mikroba Setelah Pemanasan ... 25
Gambar 5. Grafik Perubahan Stabilitas Emulsi Setelah Pemanasan... 25
Gambar 6. Grafik Perubahan Viskositas Setelah Pemanasan ... 26
Gambar 7. Grafik Perubahan Derajat Putih Setelah Pemanasan... 27
Gambar 8. Grafik Perubahan Bilangan Peroksida Setelah Pemanasan... 29
Gambar 9. Grafik Perubahan Kadar Air Setelah Pemanasan... 30
Gambar 10. Grafik Perubahan Kadar Protein Setelah Pemanasan ... 31
Gambar 11. Grafik Perubahan Kadar Lemak Setelah Pemanasan... 32
Gambar 12. Grafik Perubahan Bilangan Asam Setelah Pemanasan... 33
Gambar 13. Grafik Perubahan %FFA Setelah Pemanasan ... 33
Gambar 14. Grafik Perubahan Nilai pH Setelah Pemanasan... 34
Gambar 15. Grafik Perubahan Nilai Kesukaan Terhadap Warna Setelah Pemanasan ... 35
Gambar 16. Grafik Perubahan Nilai Kesukaan Terhadap Aroma Setelah Pemanasan ... 36
Gambar 17. Grafik Perubahan Nilai Kesukaan Terhadap Penampakan Umum Setelah Pemanasan ... 36
DAFTAR LAMPIRAN
Lampiran 1. Prosedur Analisis Fisiko Kimia Santan... 46
Lampiran 2. Data Pengamatan Total mikroba ... 51
Lampiran 3. Data Pengamatan dan ANOVA Stabilitas Emulsi... 52
Lampiran 4. Data Pengamatan Viskositas ... 53
Lampiran 5. Data Pengamatan dan ANOVA Derajat Putih... 54
Lampiran 6. Data Pengamatan dan ANOVA Bilangan Peroksida... 55
Lampiran 7. Data Pengamatan dan ANOVA Kadar Air... 56
Lampiran 8. Data Pengamatan dan ANOVA Kadar Protein... 57
Lampiran 9. Data Pengamatan dan ANOVA Kadar Lemak ... 58
Lampiran 10. Data Pengamatan dan ANOVA Bilangan Asam dan FFA ... 59
Lampiran 11. Data Pengamatan dan ANOVA Nilai pH... 60
Lampiran 12. Data Pengamatan dan ANOVA Kadar Abu ... 61
Lampiran 13. Data Pengamatan dan ANOVA Kadar Karbohidrat... 62
Lampiran 14. Data Uji kesukaan dan ANOVA terhadap warna... 63
Lampiran 15 Data Uji Kesukaan dan ANOVA Aroma ... 65
Lampiran 16. Data Uji Kesukaan dan ANOVA Penampakan Umum ... 67 Lampiran 17. Foto santan Sebelum dan Sesudah Pemanasan
I. PENDAHULUAN
A. LATAR BELAKANG
Tanaman kelapa (Cocos nucifera L.) merupakan tanaman yang sangat berguna bagi manusia, karena keseluruhan bagian tanaman kelapa dapat dimanfaatkan untuk berbagai kepentingan pangan maupun non pangan. Tanaman kelapa terdapat hampir di seluruh wilayah Indonesia. Daerah penghasil utama kelapa adalah Riau, Jawa Barat, Jawa Tengah, Jawa Timur, Sulawesi Utara, Sulawesi Tengah, dan Maluku.
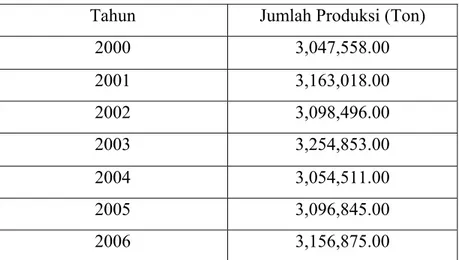
Kelapa adalah salah satu komoditas yang memegang peranan penting dalam kehidupan manusia. Di Indonesia, buah kelapa diusahakan melalui perkebunan besar maupun perkebunan rakyat. Produksi kelapa di Indonesia dapat dilihat pada tabel 1.
Tabel 1. Data Produksi Kelapa
Tahun Jumlah Produksi (Ton)
2000 3,047,558.00 2001 3,163,018.00 2002 3,098,496.00 2003 3,254,853.00 2004 3,054,511.00 2005 3,096,845.00 2006 3,156,875.00 (Departemen Pertanian, 2008)
Buah kelapa di Indonesia sebagian besar dimanfaatkan untuk pembuatan kopra, kelapa sayur dan pembuatan minyak kelapa. Sebagian besar kelapa sayur digunakan dalam bentuk santan. Santan adalah emulsi minyak dalam air yang berwarna putih, yang diperoleh dengan cara memeras daging kelapa segar yang telah diparut atau dihancurkan dengan atau tanpa penambahan air (Hagenmeier, 1973). Santan memiliki kandungan air, lemak dan protein yang cukup tinggi. Tingginya kadar air, lemak dan protein tersebut menyebabkan santan sangat mudah rusak. Oleh karena itu, diperlukan suatu teknologi untuk membuat santan
menjadi lebih lama umur simpannya. Salah satu metode pengawetan santan adalah dengan menggunakan metode pasteurisasi.
Pasteurisasi adalah suatu proses pemanasan pada suhu relatif rendah yaitu dibawah 1000C. Pasteurisasi bertujuan untuk memperpanjang umur simpan suatu produk dengan cara membunuh mikroorganisme pembusuk seperti khamir, kapang serta bakteri yang terdapat dalam produk tetapi tidak merusak produk. Pasteurisasi dapat dilakukan pada suhu yang relatif rendah dalam waktu yang relatif lama yaitu suhu 650C selama 30 menit atau pada suhu tinggi dalam waktu singkat yaitu suhu 720C selama 15 detik. Semakin tinggi suhu pemanasannya,
semakin singkat waktu pemanasannya. Permasalahannya adalah bahwa selama ini suhu dan waktu pasteurisasi yang digunakan masih mengacu pada produk lain misalnya produk susu yang biasanya dipanaskan pada suhu 65oC selama 30 menit. Diaplikasikannya suhu serta waktu produk lain untuk proses pasteurisasi santan dikhawatirkan dapat merusak nilai nutrisi yang terdapat dalam santan akibat suhu terlalu tinggi atau waktu yang terlalu lama. Selain itu, apabila suhu yang digunakan terlalu rendah dikhawatirkan proses pemanasan tidak mampu membunuh mikroorganisme patogen yang terdapat dalam santan. Adanya mikroorganisme dalam santan dapat mengakibatkan santan menjadi sangat mudah rusak sehingga dapat memperpendek umur simpannya. Oleh karena itu, perlu dilakukan penelitian untuk menghitung kecukupan panasnya. Dengan menghitung nilai kecukupan panas pada santan, dapat diperoleh kombinasi suhu dan waktu optimum untuk melakukan pasteurisasi santan.
Pasteurisasi merupakan metode pengawetan yang sangat mudah untuk dilakukan, sederhana serta tidak memerlukan biaya yang mahal. Dengan demikian metode pasteurisasi sangat cocok untuk digunakan di kawasan pedesaan atau pada industri kecil. Penelitian ini bertujuan untuk memperoleh suhu serta waktu terbaik untuk pasteurisasi santan. Dengan demikian santan yang telah dipasteurisasi memiliki umur simpan lebih lama, tetapi kerusakan pada santan akibat pemanasan menjadi lebih sedikit.
B. TUJUAN
1. Menghitung nilai kecukupan panas sehingga dapat diperoleh kombinasi suhu serta waktu terbaik untuk pasteurisasi santan
2. Mengetahui pengaruh kombinasi suhu dan waktu pemanasan terhadap mutu santan
II. TINJAUAN PUSTAKA
A. KELAPA 1. Botani Kelapa
Tanaman kelapa (Cocos nucifera L.) termasuk famili palmae, ordo arecales, dan kelas monokotiledon (Guharja et. al., 1971). Kelapa merupakan satu-satunya spesies dari genus cocos (Santoso et. al., 1982).
Daerah antara 20o lintang utara dan 20o lintang selatan merupakan daerah yang baik untuk berkembang biak tanaman kelapa. Di luar batas ini tidak dapat lagi dijumpai tanaman kelapa. Tanaman kelapa termasuk tanaman dataran rendah, bahkan disebut tanaman pantai. Pada ketinggian sampai 450 m di atas permukaan laut tanaman kelapa tumbuh subur dengan produksi buah yang banyak. Makin rendah tempat tumbuh tanaman kelapa, makin cepat waktu berbuah. Tanaman kelapa masih dapat tumbuh dengan baik pada ketinggian 1000 m di atas permukaan laut. Curah hujan yang dibutuhkan antara 1250-2500 mm per tahun dan distribusinya merata sepanjang tahun. Temperatur rata-ratanya sekitar 27oC merupakan temperatur optimum untuk tanaman kelapa. Tanaman kelapa membutuhkan banyak sinar matahari. Diperkirakan bahwa penyinaran selama 2000 jam per tahun dan 120 jam untuk setiap bulannya merupakan faktor limit dalam pembentukan buah. Tanaman kelapa sangat cocok pada iklim yang panas dan lembab. Udara kering yang berlebihan tidak dikehendaki karena dapat mengakibatkan rontoknya buah-buah muda lebih awal (Santoso et. al., 1982).
Varietas tanaman kelapa banyak sekali, tetapi pada umumnya dibedakan atas dua golongan yaitu kelapa genjah (dwarf coconut) dan kelapa dalam (tall coconut). Kelapa genjah mempunyai sifat morfologi dan biologi yang berbeda dengan kelapa dalam. Jenis kelapa dalam merupakan jenis kelapa yang paling banyak di Indonesia. Berdasarkan warna buahnya, jenis kelapa dalam yang paling banyak tedapat di Indonesia adalah kelapa hijau (var. Viridis), kelapa merah cokelat (var. Rubescens) dan kelapa kelabu cokelat (var. Macrocarps). Kelapa genjah dibagi menjadi tiga jenis berdasarkan warnanya, yaitu kelapa genjah hijau, kuning dan merah (Santoso et. al., 1982).
Batang kelapa dapat mencapai ketinggian 20-25 m pada kelapa dalam dan 10-15 m pada kelapa genjah. Tanaman kelapa merupakan tanaman monokotil sehingga tidak mempunyai lapisan kambium. Diameter batang tanaman dewasa pada ketinggian di atas dua meter dari permukaan tanah rata-rata 30-40 cm pada kelapa dalam. Pada kelapa genjah diameter batangnya lebih kecil daripada kelapa dalam dan bentuknya hampir sama dari bagian bawah sampai ke atas (Santoso et. al., 1982).
Pada tiap tanaman kelapa terdapat bunga jantan dan bunga betina (monocious). Bunga jantan terdapat dalam rangkaian bunga. Kelapa dalam mulai dapat berbunga pada umur 6-7 tahun, sedangkan kelapa genjah pada umur 2-3 tahun. Penyerbukan dapat terjadi oleh angin atau serangga. Tanaman kelapa genjah mulai berproduksi pada umur 3-4 tahun, sedangkan kelapa dalam pada umur 6-8 tahun (Santoso et. al., 1982).
Masa panen buah kelapa berlangsung sepanjang tahun, setiap tahun dapat dipanen satu, dua atau tiga bulan sekali. Kebun kelapa yang dipelihara dengan baik dan dipupuk, setiap pohonnya dapat menghasilkan 80-120 buah per tahun. Kebun kelapa yang hanya dibersihkan dan tidak dipupuk, setiap pohonnya menghasilkan 40-60 buah per tahun (Djatmiko et. al., 1981).
2. Buah Kelapa
Buah kelapa berbentuk bulat memanjang dengan ukuran kurang lebih sebesar kepala manusia. Buah kelapa berdasarkan umurnya dibagi tiga golongan, yaitu kelapa muda, kelapa setengah tua dan kelapa tua. Buah kelapa muda berumur 6-8 bulan, kelapa setengah tua berumur 10-11 bulan dan kelapa tua berumur 11-13 bulan (Nainggolan dan Sitinjak, 1977). Komposisi buah kelapa tua terdiri dari 35 persen sabut, 12 persen tempurung, 28 persen daging buah dan 25 persen air buah (Djatmiko et. al., 1981).
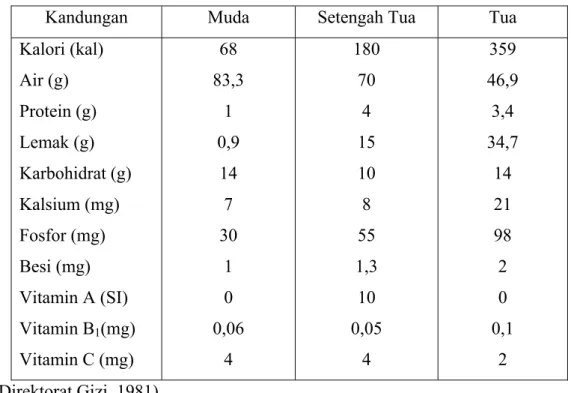
Daging buah kelapa kaya akan lemak dan karbohidrat, serta protein dalam jumlah sedang. Komposisi kimia daging buah kelapa bervariasi menurut tingkat kematangan dan varietas buah kelapa. Kadar lemak tertinggi terdapat pada daging buah kelapa tua. Protein daging buah kelapa mempunyai nilai yang tinggi karena mengandung beberapa asam amino esensial. Adapun komposisi buah kelapa terdapat pada tabel 2.
Tabel 2. Komposisi Buah Kelapa
Kandungan Muda Setengah Tua Tua
Kalori (kal) Air (g) Protein (g) Lemak (g) Karbohidrat (g) Kalsium (mg) Fosfor (mg) Besi (mg) Vitamin A (SI) Vitamin B1(mg) Vitamin C (mg) 68 83,3 1 0,9 14 7 30 1 0 0,06 4 180 70 4 15 10 8 55 1,3 10 0,05 4 359 46,9 3,4 34,7 14 21 98 2 0 0,1 2 (Direktorat Gizi, 1981)
Carey pada tahun 1924 telah mengisolasi rafinosa, sukrosa, fruktosa, galaktosa dan glukosa dari daging buah kelapa. Dalam daging buah kelapa juga terdapat enzim peroksidase, dehidrogenase, ketalase dan phospatase. Pada buah yang sudah dipetik enzim akan mempercepat proses hidrolisis minyak sehingga terbentuk asam lemak bebas dan mempercepat oksidasi pada asam lemak tidak jenuh (Djatmiko et. al.,1981).
3. Kegunaan Kelapa
Tanaman kelapa mempunyai nilai ekonomis yang tinggi karena seluruh bagiannya dapat dimanfaatkan, baik di bidang pangan maupun non-pangan. Sabut kelapa dapat digunakan untuk industri anyaman, tali temali, pembuatan permadani, bahan pengisi tempat duduk dan untuk keperluan rumah tangga. Daun kelapa dapat digunakan untuk atap rumah atau ditenun menjadi topi. Tangkai daun yang tua dapat digunakan menjadi sapu lidi. Batang kelapa bersifat keras, kaku dan awet sehingga dapat digunakan untuk tiang rumah dan keperluan lainnya. Tempurung kelapa dapat dibuat menjadi bahan perhiasan, alat-alat rumah tangga, arang tempurung, arang aktif atau menjadi tepung tempurung kelapa. Air kelapa dapat digunakan sebagai minuman penyegar, bahan pembuat cuka dan nata de coco. Daging buah kelapa dapat dipergunakan untuk membuat santan kelapa,
makanan kecil, kelapa parut kering (desiccated coconut) atau untuk membuat minyak kelapa. Pada umumnya kelapa yang dihasilkan di Indonesia sebagian besar diolah menjadi kopra yang digunakan sebagai bahan baku pembuatan minyak kelapa (Djatmiko dan Ketaren, 1978).
B. SANTAN KELAPA 1. Santan
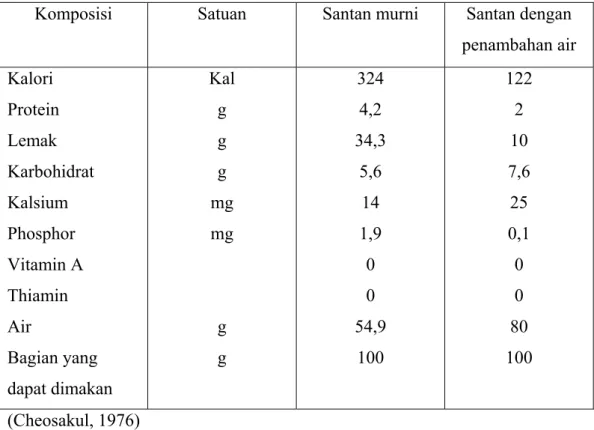
Santan adalah cairan berwarna putih susu yang diperoleh dengan cara pengepresan parutan daging kelapa dengan atau tanpa penambahan air, yang akan mempengaruhi rupa santan terutama komposisi kimia santan. Santan dapat berwarna putih susu karena partikelnya berukuran lebih besar dari satu mikron (Kirk dan Othmer, 1950). Hasil ekstraksi santan dipengaruhi oleh cara pemerasannya. Pemerasan dengan tangan dapat diekstrak santan sebanyak 52,9%, dengan waring blender sebanyak 61%, dengan kempa hidrolik (6000 psi) sebanyak 70,3% serta kombinasi ketiganya dapat diperoleh ekstrak santan sebanyak 72,5% (Dachlan, 1984). Komposisi santan kelapa dapat dilihat pada tabel 3.
Tabel 3. Komposisi Santan
Komposisi Satuan Santan murni Santan dengan penambahan air Kalori Protein Lemak Karbohidrat Kalsium Phosphor Vitamin A Thiamin Air Bagian yang dapat dimakan Kal g g g mg mg g g 324 4,2 34,3 5,6 14 1,9 0 0 54,9 100 122 2 10 7,6 25 0,1 0 0 80 100 (Cheosakul, 1976)
Santan merupakan emulsi lemak dalam air dengan ukuran pertikel lebih besar dari 1 μm sehingga berwarna putih susu (Kirk dan Othmer, 1950). Santan secara alami mengandung emulsifier, Balasubramaniam dan Sihotang (1979) menemukan suatu emulsifier alami pada santan yaitu phospholipid yang jumlahnya 0,27 gram per 100 gram daging buah kelapa. Menurut Grimwood (1975) dan Woodroof (1979), komposisi santan berbeda tergantung dari komposisi daging duah kelapa.
2. Kerusakan santan kelapa
Santan kelapa merupakan produk pangan yang memiliki kadar air, protein dan lemak yang cukup tinggi sehingga mudah ditumbuhi oleh mikroorganisme pembusuk dan santan menjadi mudah rusak. Sementara itu, pengawetan santan dengan metode sterilisasi dapat menyebabkan beberapa kerusakan mutu produk. Kerusakan tersebut antara lain pecahnya emulsi santan, timbulnya aroma tengik dan terjadi perubahan warna menjadi lebih gelap (agak coklat) (Satoto,1999).
Santan sering memberikan beberapa masalah khusus bagi para ahli teknologi pangan, karena santan tidak dapat disterilisasikan dengan pemanasan sebagaimana dilakukan terhadap produk yang lain. Hal ini disebabkan santan mengalami koagulasi jika dipanaskan diatas suhu 80oC, dan aroma (flavor) kelapa yang harum sebagian besar akan hilang (Satoto,1999).
Hasil penelitian Kajs et. al. (1976), menunjukkan bahwa TPC ( Total Plate Count) santan mencapai batas yang menyebabkan kerusakan organoleptik (1,2x106-1,7x108 CFU/ml) hanya dalam waktu 6 jam pada penyimpanan 350C. Selain kerusakan oleh mikroba, santan kelapa sangat rentan terhadap kerusakan kimia (termasuk enzimatis), khususnya melalui oksidasi lemak dan hidrolisis yang menghasilkan bau dan rasa yang tidak enak. Secara fisik santan kelapa tidak stabil dan cenderung terpisah menjadi dua fase. Menurut Tangsuphoom dan Coupland (2005), santan kelapa akan terpisah ke dalam fase kaya minyak (krim) dan fase kaya air (skim) dalam waktu 5-10 jam.
a. Stabilitas Emulsi Santan
Menurut Clemente dan Villacorte (1933), emulsi santan (minyak dalam air) bersifat stabil karena adanya bahan protein dan beberapa jenis ion yang terabsorbsi pada permukaan minyak. Kirk dan Othmer (1950) menyatakan bahwa
stabilitas emulsi tergantung dari ukuran partikel, perbedaan densitas kedua fase (minyak dan air), pemakaian emulsifier dan suhu pengolahan. Menurut Cheosakul (1967) dalam Dachlan (1984), pemanasan suhu sterilisasi (1210C) dalam waktu lama dapat menyebabkan perubahan warna dan pecahnya emulsi.
b. Ketengikan
Santan merupakan salah satu produk pangan berlemak tinggi. Menurut Ketaren (1986) kerusakan bahan pangan berlemak yang sering terjadi adalah kerusakan lemak pada pengolahan maupun saat penyimpanan. Kerusakan lemak yang utama adalah ketengikan yaitu terjadi perubahan bau dan flavor. Winarno (1986) menyatakan kerusakan lemak yang utama adalah timbulnya bau dan rasa tengik yang disebabkan oleh otooksodasi radikal asam lemak tidak jenuh. Menurut Ketaren (1986), faktor-faktor penyebab yang dapat mempercepat terjadinya reaksi otooksidasi antara lain radiasi, misalnya panas dan cahaya, bahan pengoksidasi misalnya peroksida asam nitrat, beberapa senyawa organik nitro dan aldehid aromatik, katalis metal khususnya garam dari beberapa macam logam berat, sistem oksidasi misalnya adanya katalis organik yang labil terhadap panas. Selain itu, ketengikan juga dapat terjadi karena hidrolisis lemak yang kemudian menghasilkan komponen zat berbau tengik yang mengandung asam lemak jenuh rantai pendek. Menurut Djatmiko dan Widjaja (1973), kerusakan karena proses hidrolisis dapat terjadi pada bahan pangan berlemak yang mengandung asam lemak jenuh dalam jumlah cukup besar, dalam hal ini santan kelapa mengandung asam laurat yang cukup banyak. Bau tengik disebabkan oleh asam lemak bebas yang terbentuk selama proses hidrolisis. Proses hidrolisis lemak dapat terjadi karena aktivitas enzim lipase dan mikroba yang dipercepat dengan kondisi kelembaban tinggi, kadar air serta temperatur yang tinggi selama pengolahan. c. Perubahan Warna
Menurut Dachlan (1984), selama pengolahan santan kelapa dengan sterilisasi 1150C selama 60 menit terjadi perubahan derajat putih sebesar 2% sedangkan bila santan disterilisasi selama 75 menit akan mengalami penurunan derajat putih sebesar 6%.
C. PASTEURISASI SANTAN
Pengawetan bahan pangan dapat dilakukan dengan beberapa cara seperti pengolahan dengan panas, pengurangan kandungan air bebas, penambahan pengawet, pengawetan dengan pendinginan dan iradiasi bahan pangan (Desrosier, 1983).
Proses termal yang diterapkan dalam pengolahan dan pengawetan bahan pangan dimaksudkan untuk mengurangi atau menghilangkan aktivitas biologis yang tidak diinginkan yang terjadi dalam bahan pangan, seperti mikroorganisme untuk tumbuh dan berkembang biak, dan menguraikan komponen-komponen nutrisi produk pangan. Selain itu, pemanasan juga bertujuan untuk memperbaiki cita rasa, aroma, tekstur dan penampakan yang lebih baik, serta sedapat mungkin proses termal ini masih dapat mempertahankan zat nutrisi serta mutu bahan pangan semaksimal mungkin (Fardiaz, 1992 a, Frazier dan Westhoff, 1988). Semakin lama waktu pemanasan maka semakin besar pengaruhnya terhadap kematian mikroba, tetapi pengaruh yang lebih besar dan nyata adalah faktor suhu pemanasan. Pada pemanasan yang lebih tinggi dari 100oC akan menurunkan waktu pemanasan secara nyata untuk membunuh mikroba (Fardiaz, 1992 b).
Faktor suhu sangat mempengaruhi kehidupan mikroba khususnya bakteri. Suhu mempengaruhi perkembangbiakan dan daya tahan hidup bakteri. Suhu rendah pada umumnya memperlambat aktivitas metabolisme sel, sedangkan suhu tinggi sampai batas tertentu akan mempercepat aktivitas sel. Hal ini disebabkan karena adanya pengaruh aktivitas enzim dan denaturasi protein atau kerusakan bagian sel yang lain.
Proses termal yang berupa pasteurisasi dan sterilisasi komersial bertujuan untuk menginaktif atau mematikan mikroba yang terdapat dalam bahan pangan. Pasteurisasi merupakan proses termal yang dilakukan pada suhu kurang dari 100oC, dengan waktu yang bervariasi mulai dari beberapa detik hingga beberapa menit. Hal ini bergantung dari suhu yang digunakan. Pasteurisasi bertujuan untuk menginaktif sel vegetatif dari mikroba patogen, mikroba pembusuk dan mikroba pembentuk toksin. Penggunaan panas yang relatif rendah menyebabkan sedikit perubahan pada karakteristik sensori dan nilai gizinya (Jongen, 2002).
Pasteurisasi adalah salah satu cara pengawetan panas dimana pemanasan dilakukan secara mimimun untuk membunuh semua mikroorganisme patogen (Herro, 1980). Prinsip pasteurisasi adalah pemanasan produk dalam waktu yang singkat sampai mencapai kombinasi suhu dan waktu tertentu yang cukup untuk membunuh semua mikroorganisme patogen, tetapi hanya menyebabkan kerusakan sekecil mungkin terhadap produk akibat panas (Woodroof, 1979).
Pasteurisasi biasanya dilakukan pada produk yang mudah rusak apabila dipanaskan atau tidak dapat disterilisasi secara komersil (Desrosier, 1983). Pasteurisasi membunuh semua mikroorganisme psikrofilik, mesofilik, dan sebagian yang bersifat termofilik. Biasanya pasteurisasi dipadukan dengan teknik penyimpanan pada suhu rendah yang bertujuan untuk mencegah pertumbuhan mikroorganisme termofilik yang suhu pertumbuhan minimumnya cukup tinggi. Produk hasil pasteurisasi bila disimpan pada suhu kamar hanya bertahan 1 sampai 2 hari sedang jika disimpan pada suhu rendah dapat tahan 1 minggu. Pasteurisasi memiliki tujuan:
1. Untuk membunuh bakteri patogen, yaitu bakteri yang berbahaya karena dapat menimbulkan penyakit pada manusia.
2. Untuk memperpanjang daya simpan bahan atau produk 3. Dapat menimbulkan citarasa yang lebih baik pada produk Metode pasteurisasi yang umum digunakan adalah:
1. Pasteurisasi dengan suhu tinggi dan waktu singkat (High Temperature Short Time/HTST), yaitu proses pemanasan susu selama 15 – 16 detik pada suhu 71,7 – 750C dengan alat Plate Heat Exchanger.
2. Pasteurisasi dengan suhu rendah dan waktu lama (Low Temperature Long Time/LTLT) yakni proses pemanasan susu pada suhu 610C selama 30 menit.
3. Pasteurisasi dengan suhu sangat tinggi (Ultra High Temperature) yaitu memanaskan susu pada suhu 1310C selama 0,5 detik. Pemanasan dilakukan dengan tekanan tinggi untuk menghasilkan perputaran dan mencegah terjadinya pembakaran produk pada alat pemanas (Nurhidayat, 2007).
Perlakuan panas merupakan proses yang efektif untuk memperpanjang masa simpan santan kelapa. Menurut Seow dan Gwee (1997), pengawetan santan jangka pendek dapat dicapai melalui proses pasteurisasi pada suhu 750C selama 20 menit, sedangkan untuk penyimpanan jangka panjang dapat dicapai dengan proses strerilisasi yang menggunakan rezim panas lebih tinggi (suhu 109-1210C) pada kemasan kaleng atau botol gelas. Namun pada pemanasan santan dengan suhu tinggi (800C atau lebih) protein mengalami denaturasi yang menyebabkan ketidakstabilan emulsi santan (Peamprasart dan Chiewchan, 2006).
Tejada (1973) dalam Djatmiko (1983) melaporkan bahwa santan mempunyai titik awal koagulasi pada suhu 80,9oC dan sama sekali menggumpal pada suhu 85oC. Oleh karena itu pasteurisasi santan dilakukan dibawah titik koagulasi. Santan memerlukan pasteurisasi pada suhu 60oC selama satu jam (Hagenmaier et. al., 1975).
1. Ketahanan Mikroba terhadap Panas
Ketahanan panas mikroorganisme bergantung pada sifat genetis (galur dan spesies) dan faktor-faktor lingkungan seperti medium (substrat) yang digunakan (Santoso, et.al., 1982). Pada umumnya suhu ketahanan panas mikroba juga dipengaruhi oleh suhu optimum pertumbuhannya (Fardiaz, 1992).
Beberapa faktor yang mempengaruhi ketahanan panas mikroba selain galur dan spesies adalah jumlah sel mikroba, umur sel, suhu pertumbuhan, umur sel, kandungan air, lemak, garam, karbohidrat, nilai pH, kandungan protein, adanya senyawa anti mikroba, dan faktor hubungan suhu dan pemanasan (Fardiaz, 1990 a). Faktor-faktor yang meningkatkan ketahanan mikroba terhadap panas yaitu adanya komponen lemak, protein dan jumlah awal sel yang tinggi (identik dengan kandungan protein yang tinggi). Adapun faktor-faktor yang menyebabkan penurunan ketahanan panas mikroba antara lain kandungan air yang tinggi, perubahan pH diluar pH normal (7,0) dan adanya senyawa anti mikroba.
Pengujian ketahanan panas (nilai D dan z) spora bakteri memerlukan beberapa data dan pengukuran melalui percobaan. Salah satu perhitungan yang penting dalam proses termal bakteri adalah kurva TDT (Thermal Death Time), yaitu waktu yang diperlukan untuk membunuh sejumlah mikroorganisme pada suhu tertentu. Untuk mendapatkan kurva TDT (nilai z), sebelumnya ditetapkan
kurva kecepatan kematian mikroba (nilai D) dengan cara melakukan percobaan pemanasan sejumlah suspensi spora bakteri di dalam medium pemanasan dan pada suhu konstan tertentu, serta interval pemanasan yang ditetapkan dengan menggunakan metode tabung (Yamazaki et.al.,1997).
Menurut Fardiaz (1992 a), simbol D menunjukkan waktu reduksi desimal, yaitu pemanasan pada suhu tertentu yang dapat menyebabkan kematian mikroba hingga 90 persen. Nilai D menunjukkan waktu dimana kurva kecepatan kematian menurun satu logaritmik. Dari kurva kematian dapat dikembangkan persamaan berikut:
t D =
log No- log N atau
N = No.10-t/D(T)
No = jumlah spora bakteri awal (koloni/ml) T = lama pemanasan (menit) setelah koreksi T = suhu pemanasan konstan
D(T) = waktu reduksi desimal pada suhu T
N = jumlah spora yang masih hidup setelah pemanasan
Sudut kemiringan (slope) pada kurva TDT disebut nilai z, yaitu interval suhu dalam derajat fahrenheit yang dibutuhkan oleh kurva TDT untuk melewati satu logaritmik dengan persamaan sebagai berikut :
(T2 - T1)
z =
log D1 - log D2
D1 = nilai D pada suhu T1
D2 = nilai D pada suhu T2
T = suhu dalam oC atau oF, dimana T2 lebih besar dari T1
2. Perhitungan Nilai Kecukupan Panas
Parameter kunci dari kecukupan panas pada proses pasteurisasi adalah
telah membunuh mikroba target sebanyak 5D. Maksud dari 5D adalah proses pasteurisasi yang diberikan harus mampu membunuh mikroba target sebanyak 5 siklus logaritma. Artinya mikroba yang terbunuh atau berkurang sebanyak
99.999% dari jumlah awal (Hariyadi, 2006). Nilai kecukupan panas santan dihitung pada setiap kombinasi suhu dan waktu. Nilai kecukupan panas santan dihitung dengan persamaan:
P = [10 (T-Tref)/z]t Dimana :
P : nilai pasteurisasi (menit) T : suhu produk (0C)
Tref : Suhu referen pada nilai DT z : faktor kinetik
III. METODOLOGI PENELITIAN
A. ALAT DAN BAHAN
Bahan untuk penelitian ini terdiri atas bahan baku (buah kelapa tanpa sabut dan tempurung), air, PCA, PDA, NA, bahan kimia yang terdiri dari toluene, etanol netral 95 persen, indikator PP, KOH o,1 N, heksan, katalis selen, H2SO4 pekat,
NaOH 30 persen, asam borat 2 persen, indikator mengsel, HCl 0.02 N, Asam tartarat 10 persen, , asam asetat glasial dan kloroform (3:2), KI jenuh, Na2S2O3 0,1
N, indikator kanji, kertas saring, NaOH 1,25 N, H2SO4 0,325 N, aseton. Adapun
peralatan yang digunakan adalah pisau, mesin pemarut, kempa hidrolik, kain saring, wadah plastik, cawan petri, mikropipet, tabung ulir, waterbath, clean bench, timbangan analitik, autoklaf, kompor, panci, alat aufhauser, tanur, cawan porselen, erlenmeyer, buret, sudip, gelas selai, cawan alumunium, oven, desikator, gelas piala, soxhlet, pompa vakum, alat destilasi, colorimeter, pH meter, viscosimeter brookfield, sentrifuge, jangka sorong,
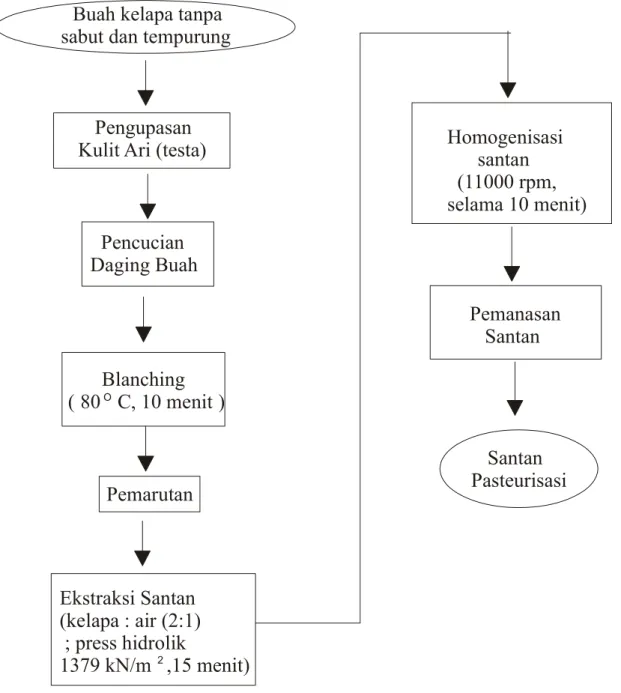
B. METODE PENELITIAN 1. Penelitian Pendahuluan a. Ekstraksi Santan
Tahapan ekstraksi santan dilakukan dengan cara mengupas testa kelapa
tanpa sabut maupun tempurung. Kemudian, daging kelapa dicuci hingga bersih lalu lakukan blanching dengan menggunakan air pada suhu 80oC selama 10 menit. Setelah itu kelapa diparut kemudian dilakukan ekstraksi santan dengan menggunakan kempa hidrolik 1379 kN/m2 selama 15 menit. Perbandingan kelapa dan air yang digunakan adalah 2:1.
b. Homogenisasi Santan
Santan yang telah diekstrak kemudian dihomogenisasi pada kecepatan 11.000 rpm selama 10 menit.
2. Penelitian Utama
a. Uji Ketahanan Panas Populasi Mikroba pada Santan
Uji ketahanan panas dilakukan terhadap populasi mikroba, kapang dan khamir. Kombinasi suhu dan waktu yang digunakan adalah 65, 75 dan 85oC dan waktu 0, 5, 10, 15, dan 20 menit.
Santan yang telah diekstrak dan dihomogenisasi dimasukkan ke dalam tabung reaksi bertutup steril. Kemudian dipanaskan dengan perlakuan kombinasi suhu dan waktu pemanasan 65, 75, dan 85oC dan waktu 0, 5, 10, 15, dan 20 menit. Setelah itu, santan didinginkan di air es. Kemudian dilakukan plating pada media NA dan APDA dengan menggunakan metode tuang. Jumlah pengenceran yang dilakukan adalah 10-1-10-3 untuk kapang dan khamir dan 10-1-10-5 untuk bakteri. Kemudian diinkubasikan pada suhu 370C untuk bakteri dan pada suhu kamar untuk kapang dan khamir selama dua hari. Setelah itu, dilakukan penghitungan jumlah koloninya.
Setelah jumlah koloni diketahui, maka nilai D pada masing-masing suhu pemanasan dihitung. Nilai D adalah waktu yang diperlukan untuk mereduksi mikroba sebesar satu siklus log pada suhu tertentu. Nilai D ditentukan dengan membuat plot antara waktu pemanasan (t) sebagai sumbu X dan log jumlah mikroba setelah pemanasan sebagai sumbu Y, dimana nilai D adalah |1/slope|. Setelah diperoleh nilai D, dihitung nilai z. Nilai z adalah perubahan suhu yang menyebabkan reduksi mikroba sebesar satu nilai D. Nilai z ditentukan dengan membuat plot anatara suhu pemanasan (T) sebagai sumbu X dan nilai D sebagai sumbu Y, dimana nilai z adalah |1/slope|.
b. Nilai Kecukupan Panas
Nilai kecukupan panas santan dihitung pada setiap kombinasi suhu dan waktu. Nilai kecukupan panas santan dihitung dengan persamaan:
P = [10 (T-Tref)/z]t
T merupakan suhu pemanasan santan, Tref merupakan suhu referensi suhu pasteurisasi yaitu 85oC. Selanjutnya dibuat grafik ketahanan panas populasi mikroba dengan membuat plot antara nilai P sebagai sumbu X dan jumlah populasi mikroba setelah pemanasan sebagai sumbu Y. Setelah itu, ditetapkan nilai P yang sesuai dengan target jumlah mikroba yang akan diinaktivasi.
Misalnya jumlah mikroba awal santan adalah 106 CFU akan diinkatifkan menjadi 101. Hal tersebut dilakukan dengan cara menarik garis horizontal pada sumbu Y yang mempunyai nilai 101 sampai memotong kurva dan ditarik garis vertikal sampai memotong sumbu X. Titik potong sumbu X adalah nilai P yang dinyatakan dalam menit. Dari nilai P tersebut dibuat enam kombinasi suhu dan waktu pemanasan yang selanjutnya diberi kode K1, K2, K3, K4, K5, K6. Selanjutnya, dilakukan uji mutu santan yang meliputi uji kadar air, kadar lemak, bilangan asam dan kadar asam lemak bebas, uji bilangan peroksida, pH, kadar abu, kadar karbohidrat, analisis mikroorganisme (TPC), stabilitas emulsi, viskositas, kadar protein, derajat putih serta uji organoleptik. Dari keenam kombinasi tersebut akan dipilih satu kombinasi terbaik. Adapun prosedur analisis fisiko kimia terdapat pada lampiran 1.
3. Rancangan Percobaan
Rancangan percobaan yang digunakan adalah rancangan acak lengkap dengan satu perlakuan.
τ = μ + Ai + εij μ = rata-rata
Ai = pengaruh perlakuan waktu dan suhu pemanasan (i = 1, 2, 3, 4, 5, 6)
εij = galat perlakuan (i) pada ulangan ke-j A = 65oC/59.2 menit 70oC/42.9 menit 75oC/31.2 menit 80oC/22.5 menit 85oC/16.3 menit 90oC/11.8 menit
Pengupasan
Kulit Ari (testa)
Pencucian
Daging Buah
Blanching
( 80 C, 10 menit )
OEkstraksi Santan
(kelapa : air (2:1)
; press hidrolik
1379 kN/m ,15 menit
2Pemanasan
Santan
Santan
Pasteurisasi
Homogenisasi
santan
(11000 rpm,
selama 10 menit)
Buah kelapa tanpa
sabut dan tempurung
Pemarutan
)
IV. HASIL DAN PEMBAHASAN
A. JUMLAH MIKROBA AWAL
Pada tahap proses pembuatan santan, tidak terlepas dari kontaminasi mikroba. Sumber pencemaran pada santan diduga berasal dari bahan baku, pengolahan dan kondisi lingkungan kerja. Jumlah mikroorganisme pada santan tanpa pemanasan terdapat pada tabel 4.
Tabel 4. Data Jumlah Mikroorganisme Awal Jenis Mikroorganisme Jumlah
Mikroorganisme
Bakteri 3,5 x105 koloni/ml
Kapang/Khamir 4,0 x 103 koloni/ml
Tingginya jumlah mikroba yang tedapat dalam santan disuga berasal dari bahan baku, proses pengolahan, serta kondisi dan lingkungan kerja. Kontaminasi mikroba sudah terjadi sejak awal kelapa dikupas. Kelapa yang digunakan untuk membuat santan pada penelitian ini adalah kelapa yang telah dihilangkan sabut dan tempurungnya yang berasal dari pasar di Bogor. Kondisi kelapa tanpa adanya sabut dan tempurung menjadikan kelapa lebih mudah tercemar oleh mikroorganisme. Selain itu, keadaan tempat pembelian kelapa sangat jauh dari kondisi aseptis sehingga semakin mudah dan semakin banyak jenis mikroorganisme yang dapat mencemari kelapa. Penggunaan air dalam proses pembuatan santan dapat menjadi salah satu penyebab sumber mikroorganisme. Air yang digunakan dalam proses ekstraksi santan adalah air matang yang bersuhu ruang sekitar 25-27oC. Selain itu, ditambah pula dengan kontaknya kelapa dengan alat-alat yang digunakan yang tidak terbebas dari mikroorganisme. Dengan demikian semakin banyak sumber pencemar pada proses pembuatan santan.
B. KETAHANAN PANAS MIKROBA
Berdasarkan tabel 4, jumlah rata-rata mikroba yang tumbuh pada santan yang belum dipanaskan adalah sebesar 3,5 x105 koloni/ml, sementara itu untuk
populasi kapang jumlahnya lebih rendah yaitu 4,0 x 103 koloni/ml. Jumlah awal populasi bakteri lebih besar dibanding jumlah populasi kapang. Hal tersebut disebabkan santan merupakan produk yang memiliki nilai aw yang sangat tinggi.
Aw (aktivitas air) adalah ketersediaan air dalam suatu bahan yang dapat digunakan
oleh mikroorganisme. Nilai aw yang sangat tinggi merupakan media yang cocok
bagi pertumbuhan bakteri. Bakteri umumnya dapat tumbuh optimal pada nilai aw minimal 0,91, sedangkan khamir pada 0,88 dan kapang pada 0,98.
Dalam proses pemanasan pada beberapa kombinasi perlakuan menunjukkan bahwa populasi bakteri lebih tahan pemanasan dibandingkan dengan populasi kapang dan khamir. Pada pemanasan suhu 65oC selama 10 menit populasi kapang menunjukkan angka nol. Kondisi tersebut disebabkan oleh adanya perbedaan struktur sel antara bakteri, kapang/khamir. Baik bakteri, kapang maupun khamir memiliki alat perlindungan untuk menghadapi kondisi lingkungan yang kurang menguntungkan. Namun, kemampuan untuk menghadapi kondisi lingkungan yang kurang menguntungkan berbeda-beda.
Ketahanan panas mikroba adalah kemampuan suatu mikroba untuk tetap bertahan pada saat memperoleh perlakuan panas yang dinyatakan dengan besarnya nilai D dan nilai z. Makin besar nilai z suatu mikroba makin besar pula ketahanan panasnya.
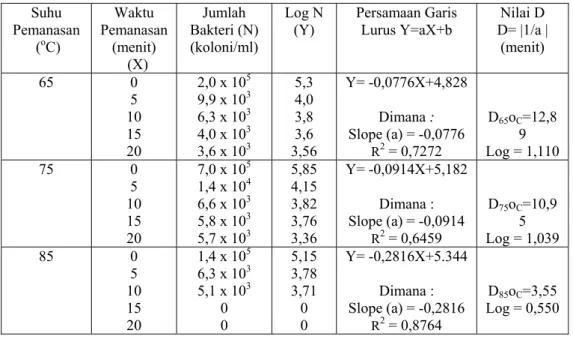
Tabel 5. Hasil perhitungan nilai D serta nilai z populasi bakteri pada santan
Suhu Pemanasan (oC) Waktu Pemanasan (menit) (X) Jumlah Bakteri (N) (koloni/ml) Log N
(Y) Persamaan Garis Lurus Y=aX+b D= |1/a | Nilai D (menit) 65 0 5 10 15 20 2,0 x 105 9,9 x 103 6,3 x 103 4,0 x 103 3,6 x 103 5,3 4,0 3,8 3,6 3,56 Y= -0,0776X+4,828 Dimana : Slope (a) = -0,0776 R2 = 0,7272 D65oC=12,8 9 Log = 1,110 75 0 5 10 15 20 7,0 x 105 1,4 x 104 6,6 x 103 5,8 x 103 5,7 x 103 5,85 4,15 3,82 3,76 3,36 Y= -0,0914X+5,182 Dimana : Slope (a) = -0,0914 R2 = 0,6459 D75oC=10,9 5 Log = 1,039 85 0 5 10 15 20 1,4 x 105 6,3 x 103 5,1 x 103 0 0 5,15 3,78 3,71 0 0 Y= -0,2816X+5.344 Dimana : Slope (a) = -0,2816 R2 = 0,8764 D85oC=3,55 Log = 0,550
Kurva Penetapan Nilai D pada Suhu 75 y = -0.0914x + 5.182 R2 = 0.6459 0 2 4 6 8 0 10 20 3
w aktu pem anasan (m enit)
lo g ju m lah mi k rob a 0
Kurva Penetapan Nilai D pada Suhu 85
y = -0.2816x + 5.344 R2 = 0.8764 -2 0 2 4 6 0 5 10 15 20 25
w aktu pem anasan (m enit)
lo g ju m la h m ikr o b a Nilai z y = -0.028x + 3.0001 R2 = 0.8432 0 0.2 0.4 0.6 0.8 1 1.2 1.4 0 20 40 60 80 10 Suhu 0 (a) (c) (d) antan
Nilai z p uat grafik antara
tiga suh
,028X+3,0001 dengan nilai R2= 0,8432, Slope (a) = -0,028
Berdasarkan Tabel anasan maka makin kecil
nilai D
hu tersebut dapat diperoleh nilai z popula
Kurva Penetapan Nilai D pada Suhu 65
y = -0.0776x + 4.828 R2 = 0.7272 0 2 4 6 0 5 10 15 20 25
w aktu pem anasan (m enit)
log j u m la h mi k roba (b)
Gambar 2. Grafik Penetapan Nilai D dan z pada s (a). D 65oC, (b). D 75oC, (c). D 85oC , (d). Nilai z
opulasi bakteri santan dihitung dengan memb
u pemanasan (65, 75 dan 85oC) sebagai sumbu X dan nilai log D (1,110; 1,039; 0,550) sebagai sumbu Y, maka diperoleh persamaan kurva TDT (thermal death time):
Y= -0
Nilai z = |1/a | = 35,71oC 5, makin tinggi suhu pem
nya. Nilai D adalah waktu yang diperlukan untuk mereduksi mikroba sebesar satu siklus log pada suhu tertentu, sehingga makin tinggi suhu pemanasan maka makin singkat waktu yang diperlukan untuk inaktivasi mikroba. Nilai D tertinggi dicapai pada pemanasan suhu 65oC yaitu 12,89 menit disusul oleh pemanasan suhu 75oC yaitu 10,95 menit dan pemanasan suhu 85oC sebesar 3,55 menit.
Berdasarkan nilai D dari ketiga su
si bakteri yaitu 35,71oC. Nilai z adalah interval suhu yang dibutuhkan untuk menurunkan jumlah mikroba. Bakteri pada santan memiliki ketahanan panas yang lebih tinggi dibandingkan populasi kapang, maka nilai z populasi
bakteri digunakan sebagai referen dalam perhitungan nilai kecukupan panas atau yang dikenal dengan nilai pasteurisasi (nilai P).
Hampir semua bakteri mempunyai struktur dan organisasi dasar yang sama
khamir memiliki kapsul namun amir
C. PERHITUNGAN NILAI KECUKUPAN PANAS
Perhitungan kecukupan panas bertujuan untuk mengetahui jumlah panas yang d
walaupun bentuknya berbeda. Selain itu, beberapa bakteri memiliki struktur tambahan lain seperti cambuk (flagella), kapsul dan endospora. Beberapa sel bakteri pada bagian luarnya dikelilingi oleh lapisan berlendir yang dihasilkan oleh bakteri itu sendiri. Bahan ini dapat melekat pada sel atau berdifusi ke dalam media. Lapisan luar ini disebut kapsul dan dapat terdiri dari gugus kompleks polisakarida atau polipeptida. Adanya kapsul ini dapat mengakibatkan sel lebih tahan terhadap tekanan lingkungannya seperti panas dan bahan-bahan kimia anti mikroba, serta dapat membantu melekat pada bahan pangan atau alat-alat pengolahan bahan pangan. Selain itu, beberapa bakteri memiliki kemampuan memproduksi sel internal yaitu endospora. Endospora berfungsi untuk melindungi sel dari keadaan lingkungan yang kurang baik. Spora-spora ini tahan terhadap fisik atau kimiawi ekstrim seperti suhu, kekeringan, bahan-bahan kimia pembasmi kuman dan dapat bertahan dalam keadaan tidur untuk beberapa tahun. Pada saat kondisi pertumbuhan memungkinkan, spora-spora tersebut tumbuh menjadi sel-sel vegetatif yang normal (Buckle, et.al.,1987).
Seperti halnya bakteri, beberapa jenis
kh tidak memiliki spora aseksual yang tahan panas seperti yang dihasilkan oleh beberapa bakteri. Begitu pula halnya dengan kapang yang menghasilkan spora aseksual yang tahan terhadap perubahan cuaca. Namun, ketahanan yang dimiliki kapang tidak setahan endospora bakteri yang tahan terhadap berbagai kondisi lingkungan (Fardiaz, 1989).
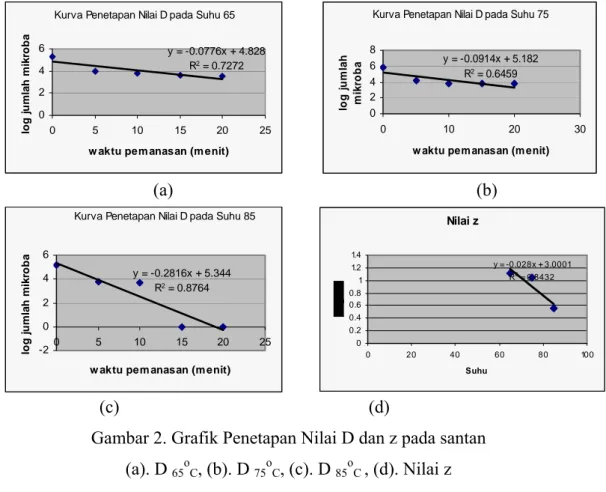
iberikan pada bahan agar bahan yang dipanaskan memiliki jumlah mikroorganisme kecil namun kerusakan akibat pemanasan dapat diminimalisir. Kecukupan panas dapat disebut nilai pasteurisasi (nilai P) yaitu waktu yang dibutuhkan untuk mencapai nilai pasteurisasi pada suhu tertentu. Untuk memperoleh nilai P, diperlukan data log jumlah mikroorganisme serta nilai P pada
setiap suhu dan waktu pemanasan. Tabel 6 menyajikan data log jumlah mikroorganisme serta nilai pasteurisasi pada setiap kombinasi suhu dan waktu pemanasan. Tabel 6. Nila y = -0,2512x + 5,122 R2 = 0,811 0 1 2 3 4 5 6 0 1 2 3 4 5 6 7 8 9 7 11 12 13 14 15 16 17 18 19 20 21 N i P L o g p o p u lasi b akter i 10 ila
i Pasteurisasi pada tiap Kombinasi Suhu dan Waktu
Gambar 3. Penetapan nilai P sesuai standar 5D pada pasteurisasi santan
erdasarkan gambar 3, nilai kecukupan panas (nilai P) pada santan adalah sebesar Pe n pe n Log Mikroorganisme Nilai P Suhu Waktu manasa (oC) manasa (menit) (menit) 65 0 5,3 0 5 4 1,38 10 3 ,8 2,75 15 3,6 4,13 20 3,56 5,51 75 0 5,85 0 5 4,15 2,62 10 3,82 5,25 15 3,76 7,87 20 3,76 10,50 85 0 5,15 0 5 3,78 5,00 10 3,71 10,00 15 0 15,00 20 0 20,00 Nilai P = 16,3 B
16,3 menit. Nilai tersebut diartikan bahwa proses pasteurisasi santan dapat dilakukan pada kombinasi suhu dan waktu yang memiliki nilai pasteurisasi
sebesar 16,3 menit. Berdasarkan nilai p ini, selanjutnya dapat dikembangkan menjadi beberapa kombinasi suhu dan waktu pemanasan seperti disajikan pada tabel 7.
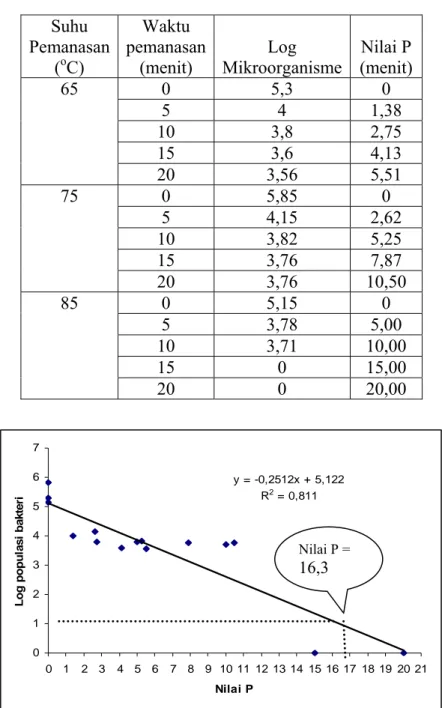
Tabel 7. Kombinasi suhu dan waktu pasteurisasi santan pada nilai Pasteurisasi
hu (oC) Waktu (menit) sebesar 16,3 Su 6 0 81,7 65 59,2 70 42,9 75 31,1 80 22,5 85 16,3 90 11,8 95 8,6 100 6,2 105 4,5
nya dari beberapa kombinasi suhu dan waktu tersebut akan dipilih
D. PENGARUH PEMANASAN TERHADAP MUTU SANTAN 1. Total Mikroba
n jumlah mikroba sangat penting untuk dilakukan terutama Selanjut
sebanyak enam kombinasi untuk dilakukan optimasi untuk mengetahui faktor nutrisi dan kandungan gizi santannya dengan pemanasan tersebut. Enam kombinasi suhu dan waktu yang dipilih adalah 65 oC/59,2 menit, 70 oC/42,9 menit, 75 oC /31,2 menit, 80 oC/22,5 menit, 85 oC/16,3 menit dan 90oC/11,8 menit. Pemilihan enam kombinasi tersebut didasarkan pada literatur yang menyebutkan bahwa proses pasteurisasi berkisar pada suhu 70-90oC (Tangsuphoom dan Coupland, 2005).
Penghitunga
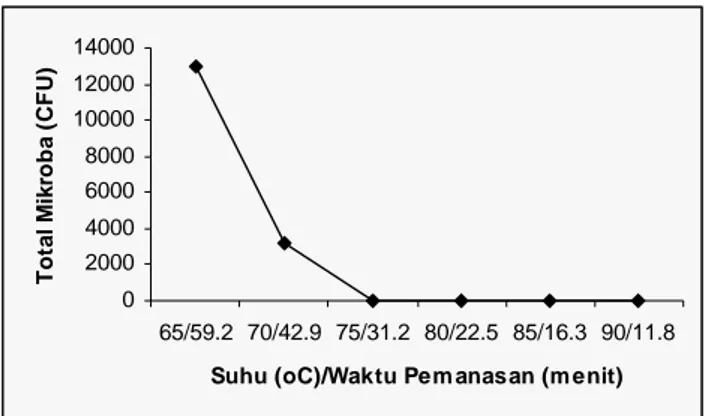
untuk produk pasteurisasi untuk mengetahui efektivitas dari proses pasteurisasi terhadap total mikroba. Data hasil penghitungan total mikroba dapat dilihat pada lampiran 2. Gambar 4 menyajikan grafik perubahan total mikroba setelah pemanasan.
0 2000 4000 6000 8000 10000 12000 14000 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8
Suhu (oC)/Waktu Pem anasan (m enit)
To ta l M ik roba ( C FU ) 0.00 5.00 10.00 15.00 20.00 25.00 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8
Suhu (oC)/Waktu Pem anasan (m enit)
S tab ilit as E m u ls i ( % )
Gambar 4. Grafik Perubahan Jum ah Mikroba Setelah Pemanasan
Berdasarkan gambar 4 dapat dilihat bahwa jumlah mikroba selama mana
2. Stabilitas Emulsi
Stabilitas emulsi merupakan salah satu parameter penting dalam enent
Gambar 5. Grafik Perubahan Stabilitas Emulsi Setelah Pemanasan l
pe san berkurang. Jumlah mikroba pada santan tanpa pemanasan adalah 1,6 x 105. Setelah pemanasan pada suhu 65oC masih terdapat jumlah mikroba sebesar 1,3 x 104, pada suhu 70oC jumlah mikroba sebesar 3,2 x 103. Pada pemanasan suhu 75, 80, 85 dan 90oC, jumlah mikroba yang terdapat dalam santan adalah nol. Berkurangnya jumlah mikroba yang terdapat di dalam santan disebabkan oleh telah tercukupinya panas yang diberikan pada santan sehingga dapat merusak ketahanan mikroba terhadap panas. Semakin kecil jumlah mikroba, maka mutu santan akan semakin baik. Hal tersebut berkaitan dengan umur simpan produk. Semakin kecil jumlah mikroba, maka akan semakin lama umur simpan produk.
m ukan mutu suatu produk emulsi. Adapun data perhitungan stabilitas emulsi sebelum dan setelah pemanasan dapat dilihat pada lampiran 3a. Pada gambar 5 disajikan grafik perubahan stabilitas emulsi selama pemanasan.
Berdasarkan gambar 5, stabilitas emulsi santan mengalami penurunan. Stabilitas emulsi pada santan yang belum dipanaskan adalah 22,09 persen. Setelah mengalami pemanasan, stabilitas emulsi berada pada rentang 15,57-20,47 persen. Hasil analisa ragam dan uji lanjut Duncan (lampiran 3b) menunjukkan bahwa akibat pemanasan stabilitas emulsi pada pemanasan 65oC/59,2 menit, 70oC/42,9 menit, dan 90oC/11,8 menit berbeda nyata dengan stabilitas emulsi pada semua perlakuan lainnya. Stabilitas emulsi pada pemanasan 75 oC /31,2 menit, 80 oC/22,5 menit, 85 oC/16,3 menit tidak berbeda nyata satu sama lain namun berbeda nyata dengan pemanasan pada 65 oC/59,2 menit, 70 oC/42,9 menit, dan 90oC/11,8 menit.
Pemanasan menyebabkan sebagian protein yang terabsorpsi dalam minyak yang pada suhu semakin tinggi dapat menyebabkan perubahan fisik maupun kimia yang mengakibatkan kerusakan sistem emulsi. Denaturasi protein dapat menjadi penyebab rusaknya sistem emulsi. Protein merupakan agen pengemulsi karena memiliki gugus hidrofilik maupun hidrofobik. Ketika protein terdenaturasi, kelarutan protein menjadi berkurang karena lapisan protein bagian dalam yang bersifat hidrofobik berbalik keluar sedangkan bagian hidrofilik yang tadinya di bagian luar terlipat ke dalam (Winarno, 2002). Pemanasan suatu sistem emulsi akan menyebabkan zat hidrofilik memperbesar ukuran globula. Semakin rendah stabilitas emulsi santan, maka semakin rendah mutu santan.
3. Viskositas
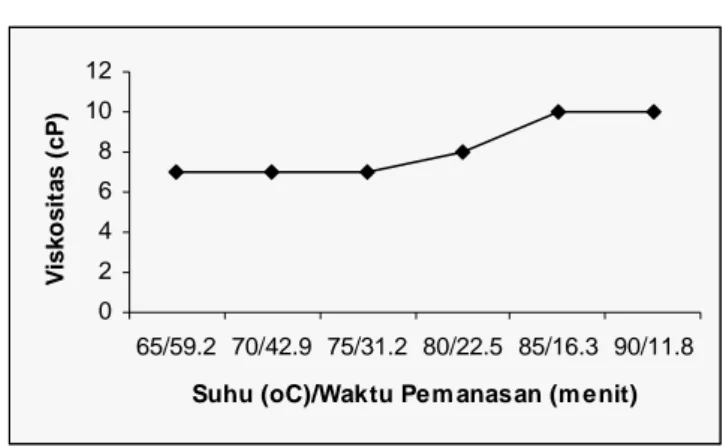
Pemanasan memberikan pengaruh terhadap viskositas santan. Adapun data perhitungan viskositas sebelum dan setelah pemanasan dapat dilihat pada lampiran 4. Pada gambar 6 disajikan grafik perubahan viskositas selama pemanasan. 0 2 4 6 8 10 12 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8 Suhu (oC)/Waktu Pem anasan (m enit)
V is ko si tas ( cP )
Berdasarkan gambar 6, viskositas santan memiliki kecenderungan meningkat. Santan tanpa pemanasan memiliki viskositas sebesar 7 cP. Setelah pemanasan pada suhu 65-75oC, santan memiliki viskositas yang sama dengan santan tanpa pemanasan yaitu 7 cP. Setelah pemanasan pada suhu 80-90oC, viskositas santan berada pada rentang 8-10 cP.
Peningkatan viskositas santan disebabkan oleh adanya penguapan kadar air selama proses pemanasan. Selama pemanasan, kadar air dalam santan menguap sehingga menyebabkan total padatan menjadi meningkat. Selain itu, peningkatan viskositas disebabkan oleh adanya protein yang terdenaturasi. Peningkatan viskositas terjadi pada pemanasan 80 oC/22,5 menit, yaitu pada suhu terjadinya denaturasi protein. Protein yang terdenaturasi akan menyebabkan molekul menjadi mengembang. Komponen karbohidrat utama dalam santan adalah sukrosa dan pati (Anon., 1984). Pemanasan dapat menyebabkan terserapnya air ke dalam granula pati. Jumlah gugus hidroksil yang besar pada pati menyebabkan air yang pada awalnya berada di luar granula pati dan bebas bergerak terserap ke dalam granula pati dan tidak dapat bergerak bebas lagi.
4. Derajat Putih
Pemanasan memberikan pengaruh terhadap derajat putih. Data hasil pengukuran derajat putih dapat dilihat pada lampiran 5. Gambar 7 menyajikan grafik perubahan derajat putih setelah pemanasan.
0.00 10.00 20.00 30.00 40.00 50.00 60.00 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8 Suhu (oC)/Waktu Pem anasan (m enit)
D e ra ja t P uti h
Gambar 7. Grafik Perubahan Derajat Putih Setelah Pemanasan
Berdasarkan gambar 7, dapat dilihat bahwa pemanasan menyebabkan derajat putih pada santan semakin menurun. Berdasarkan hasil analisa ragam dan uji lanjut Duncan, diperoleh bahwa akibat pemanasan derajat putih pada
pemanasan 65 oC/59,2 menit, 80 oC/22,5 menit, 85 oC/16,3 menit dan 90oC/11,8 menit berbeda nyata dengan derajat putih pada semua perlakuan lainnya. Derajat putih pada pemanasan 70 oC/42,9 menit, 75 oC /31,2 menit, tidak berbeda nyata satu sama lain namun berbeda nyata dengan pemanasan pada 65 oC/59,2 menit, 80oC/22,5 menit, 85 oC/16,3 menit dan 90oC/11,8 menit. Santan tanpa pemanasan memiliki derajat putih sebesar 51,06. Setelah pemanasan, derajat putih berada pada rentang 33,81-49,81.
Penurunan derajat putih tersebut disebabkan oleh adanya kandungan protein dan karbohidrat yang terdapat dalam santan. Pada pemanasan suhu yang semakin tinggi, dapat menyebabkan timbulnya reaksi antara karbohidrat dan asam amino yang menyebabkan timbulnya warna kecoklatan. Reaksi tersebut dikenal dengan reaksi Maillard. Menurut Winarno (2002), reaksi Maillard berlangsung melalui tahap-tahap berikut:
1. Suatu aldosa berekasi bolak-balik dengan asam amino sehingga menghasilkan basa Schiff
2. Perubahan terjadi menurut reaksi Amadori sehingga menjadi amino ketosa 3. Dehidrasi dari hasil reaksi Amadori membentuk turunan-turunan
furfuraldehida, misalnya dari heksosa menjadi hidroksi metil furfural 4. Proses dehidrasi selanjutnya menghasilkan hasil antara metil α-dikarbonil
yang diikuti penguraian menghasilkan reduktor-reduktor dan α-dikarboksil seperti metilglioksal, asetol dan diasetil
5. Aldehid-aldehid aktif dari 3 dan 4 terpolimerisasi tanpa mengikutsertakan gugus asam amino atau dengan gugus asam amino membentuk senyawa yang berwarna coklat yang disebut melanoidin
Semakin putih warna santan, maka semakin baik mutunya. Hal tersebut berhubungan dengan nilai kesukaan konsumen terhadap penampilan santan secara fisik.
5. Bilangan Peroksida
Pengukuran bilangan peroksida berkaitan dengan tingkat ketengikan suatu produk. Data hasil pengukuran bilangan peroksida dapat dilihat pada lampiran 6. Gambar 8 menyajikan grafik perubahan bilangan peroksida setelah pemanasan.
0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8 Suhu (oC)/Waktu Pem anasan (m enit)
B il a nga n P e ro k s ida
Gambar 8. Grafik Perubahan Bilangan Peroksida Setelah Pemanasan
Berdasarkan gambar 8, kecenderungan bilangan peroksida pada pemanasan suhu 80-90oC adalah meningkat. Berdasarkan hasil analisa ragam dan uji lanjut Duncan, diperoleh bahwa akibat pemanasan bilangan peroksida pada pemanasan 80 oC/22,5 menit, 85 oC/16,3 menit dan 90oC/11,8 menit berbeda nyata dengan bilangan peroksida pada semua perlakuan lainnya. Bilangan peroksida pada pemanasan 65 oC/59,2 menit, 70 oC/42,9 menit, 75 oC /31,2 menit, tidak berbeda nyata satu sama lain namun berbeda nyata dengan pemanasan pada 80oC/22,5 menit, 85 oC/16,3 menit dan 90oC/11,8 menit. Santan tanpa pemanasan memiliki bilangan peroksida 0. Pada pemanasan suhu 80-90oC, bilangan peroksida berada pada rentang 2,98-6,27.
Meningkatnya bilangan peroksida disebabkan karena adanya reaksi oksidasi pada asam lemak tidak jenuh akibat proses pemanasan. Ikatan rangkap pada asam lemak tidak jenuh mengikat oksigen sehingga membentuk peroksida. Asam lemak tidak jenuh yang terdapat dalam kelapa adalah asam lemak palmitat, oleat dan linoleat. Semakin tinggi suhu yang digunakan akan mempercepat terjadinya proses oksidasi. Semakin tinggi nilai bilangan peroksida, maka semakin kurang baik mutu santan yang dihasilkan.
6. Kadar Air
Kadar air merupakan salah satu penentu keawetan suatu produk. Hal tersebut terkait dengan ketersediaan air yang terdapat dalam produk untuk dapat digunakan oleh mikroorganisme. Adapun data perhitungan kadar air sebelum dan setelah pemanasan dapat dilihat pada lampiran 7. Pada gambar 9 disajikan grafik perubahan kadar air selama pemanasan.
61.50 62.00 62.50 63.00 63.50 64.00 64.50 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8
Suhu (oC)/Waktu Pem anasan (m enit)
K a d a r A ir ( % )
Gambar 9. Grafik Perubahan Kadar Air Setelah Pemanasan
Berdasarkan gambar 9 dapat dilihat bahwa kadar air santan setelah pemanasan memiliki kecenderungan menurun seiring dengan kenaikan suhu. Berdasarkan hasil analisa ragam dan uji lanjut Duncan, diperoleh bahwa akibat pemanasan kadar air pada pemanasan 65 oC/59,2 menit, 70 oC/42,9 menit, dan 90oC/11,8 menit berbeda nyata dengan kadar air pada semua perlakuan lainnya. Kadar air pada perlakuan pemanasan pada 75 oC /31,2 menit, 80 oC/22,5 menit, 85
oC/16,3 menit tidak berbeda nyata satu sama lain namun berbeda nyata dengan
perlakuan 65 oC/59,2 menit, 70 oC/42,9 menit, dan 90oC/11,8 menit. Kadar air santan sebelum pemanasan adalah 64,01 persen. Setelah pemanasan kadar air berkisar antara 62,65-63,50 persen.
Penurunan kadar air disebabkan adanya sebagian air yang menguap selama pemanasan. Semakin banyak air yang menguap, maka semakin sedikit kadar air yang terdapat dalam santan. Semakin kecil kadar air yang terdapat dalam santan, maka semakin baik pula mutu santan. Kadar air yang tinggi menyebabkan stabilitas emulsi santan semakin rendah. Selain itu, bahan yang memiliki kadar air yang tinggi biasanya memiliki nilai aw yang tinggi pula, tingginya nilai aw
merupakan kondisi yang cocok bagi pertumbuhan mikroorganisme terutama bakteri.
7. Kadar Protein
Kadar protein berkaitan erat dengan nilai nutrisi yang terdapat dalam santan. Adapun data perhitungan kadar protein sebelum dan setelah pemanasan dapat dilihat pada lampiran 8. Pada gambar 10 disajikan grafik perubahan kadar protein selama pemanasan.
0.00 0.50 1.00 1.50 2.00 2.50 3.00 65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8
Suhu (oC)/Waktu Pem anasan (m enit)
K a da r P rot e in ( % )
Gambar 10. Grafik Perubahan Kadar Protein Setelah Pemanasan
Berdasarkan gambar 10, kadar protein memiliki kecenderungan menurun seiring dengan semakin tingginya suhu pemanasan. Berdasarkan hasil analisa ragam dan uji lanjut Duncan, diperoleh bahwa akibat pemanasan kadar protein pada pemanasan 65 oC/59,2 menit, 85 oC/16,3 menit dan 90oC/11,8 menit berbeda nyata dengan kadar protein pada semua perlakuan lainnya. Kadar protein pada pemanasan 70 oC/42,9 menit, 75 oC /31,2 menit, 80 oC/22,5 menit, tidak berbeda nyata satu sama lain namun berbeda nyata dengan pemanasan pada 65 oC/59,2 menit, 85 oC/16,3 menit dan 90oC/11,8 menit. Pada santan yang tidak dipanaskan, terdapat kadar protein sebesar 2,76 persen. Setelah pemanasan kadar protein berada pada rentang 1,17-2,76 persen.
Penurunan kadar protein disebabkan oleh adanya denaturasi protein pada suhu yang semakin tinggi. Denaturasi merupakan peristiwa berubahnya ruang atau rantai polipeptida suatu molekul protein. Ikatan-ikatan yang membentuk konfigurasi molekul akan rusak, molekul akan mengembang. Pengembangan molekul protein akan menyebabkan terbukanya gugus reaktif rantai polipeptida. Denaturasi protein menyebabkan ikatan antar asam amino menjadi terputus. Ikatan yang terputus tersebut kemudian bereaksi dengan ikatan pada karbohidrat membentuk senyawa melanoidin yang menyebabkan warna santan menjadi agak kecoklatan. Kondisi tersebut didukung oleh data derajat putih yang semakin menurun akibat pemanasan. Semakin rendah kadar proteinnya, maka semakin rendah pula mutu santan.
8. Kadar Lemak
Lemak merupakan salah satu komponen penting dalam santan. Lemak yang terdapat dalam santan akan mempengaruhi parameter mutu santan lainnya seperti stabilitas emulsi, bilangan peroksida, %FFA dan bilangan asam. Data hasil pengukuran kadar lemak dapat dilihat pada lampiran 9. Gambar 11 menyajikan grafik kadar lemak setelah pemanasan.
11.70 12.60 13.50
65/59.2 70/42.9 75/31.2 80/22.5 85/16.3 90/11.8
Suhu (oC)/Waktu Pem anasan (m enit)
Gambar 11. Grafik Kadar Lemak Setelah Pemanasan
Berdasarkan hasil analisa ragam dan uji lanjut Duncan, diperoleh bahwa faktor suhu dan waktu pemanasan tidak berpengaruh nyata terhadap kadar lemak pada setiap perlakuan kombinasi suhu dan waktu pemanasan. Kadar lemak pada santan yang belum dipanaskan adalah sebesar 13,05 persen. Setelah pemanasan kadar lemak barada pada rentang12,32-12,93 persen. Selama pemanasan, kadar lemak menurun namun penurunan yang terjadi pada setiap perlakuan suhu dan waktu pemanasan tidak signifikan. Berkurangnya kadar lemak dalam santan setelah pemanasan akibat adanya hidrolisis lemak menjadi asam lemak bebas.
9. Bilangan Asam dan FFA
Bilangan asam dan FFA merupakan salah satu parameter mutu minyak dan lemak. Data hasil pengukuran bilangan asam dan FFA dapat dilihat pada lampiran 10. Gambar 12 menyajikan grafik bilangan asam dan gambar 13 menyajikan grafik persen FFA setelah pemanasan.