METODE ANALISIS LABORATORIUM GENETIKA
MOLEKULER SAMPEL HIU PAUS (Rhincodon typus)
SEKOLAH PASCASARJANA INSTITUT PERTANIAN BOGOR
BOGOR 2016
Teknik dan Tahapan Analisis Molekuler Sampel Hiu Paus (Rhincodon typus): Proses Ekstraksi, PCR (Polymerase Chain Reaction) dan Elektroforesis
Technique and Molecular Analysis Stage from Whale Shark (Rhincodon typus) samples: Process of Extraction, PCR (Polymerase Chain Reaction) and Electrophoresis
Samsul Bahri1, Khajar Imaniar1, Mahardika Rizki Himawan1, Hawis Madduppa2
1Program Magister Ilmu Kelautan IPB
2Fakultas Kelautan dan Perikanan IPB
Abstrak
Hiu paus (Rhincodon typus) merupakan spesies terbesar di dunia. Hiu paus tersebar di seluruh perairan Indonesia dan menjadikan Indonesia sebagai habitat dan jalur migrasinya. Praktikum terhadap sampel hiu paus yang telah dilakukan menggunakan metode ekstraksi chelex dan dilanjutkan dengan kegiatan PCR (polymerasi Chain Reaction) dan elektroforesis. Hasil yang diperoleh menunjukkan 8 sampel yang dianalisis mengandung DNA dengan munculnya band positif pada hasil elektroforesis. Hasil dari analisis sampel hiu paus selanjutnya dapat digunakan untuk proses analisis visual DNA.
Kata kunci: Hiu paus (Rhincodon typus), Metode Chelex, DNA
Abstract
Whale shark (Rhincodon typus) is a biggest species in the world. Whale shark are spreading around Indonesia and render Indonesia as their habitat and migration way. The practicum for whale shark samples have been done by chelex extraction method and runned with PCR (polymerasi Chain Reaction) and electrophoresis process. Analysed results by 8 samples showed the samples are contained DNA with positive band showed in electrophoresis. The whale shark DNA samples can be running for further DNA visual analysis.
Key word: Whale shark (Rhincodon typus), chelex method, DNA
Pendahuluan
Hiu paus (Rhincodon typus) dapat ditemukan di hampir semua wilayah Indonesia seperti di perairan Sabang, Pantai Utara Jawa Timur, Bali, Nusa Tenggara, Alor, Flores, Kalimantan, Sulawesi, Maluku, dan Papua. Oleh karena itu, peluang bagi masyarakat untuk bertemu ikan terbesar di
dunia ini cukup besar dan dapat
dimanfaatkan untuk penelitian. Hiu paus merupakan satwa yang dilindungi di Indonesia, sesuai dengan KEPMEN KP No.
18 Tahun 2013 Tentang Penetapan Status Perlindungan Penuh Ikan Hiu Paus.
Hiu paus (Rhincodon typus) merupakan spesies ikan terbesar di dunia. Ukurannya dapat mencapai 20 meter dan bobot 34 ton (Norman 2007). Daerah penyebarannya luas meliputi perairan tropis hingga subtropis hangat yaitu antara 30°LU dan 35°LS dengan kisaran suhu 21°– 30°C (KKJI 2014). Menurut Motta et al. (2010) ikan ini merupakan pemakan zooplankton yang cenderung jinak. Hal ini berbeda dari hiu
pada umumnya yang merupakan karnivora dan buas. Penelitian mengenai beberapa aspek kehidupan hiu paus yang meliputi aspek biologi dan ekologi hingga saat ini cukup banyak dilakukan, seperti di Ninggalo Reef Australia (Steven et al. 2001), Afrika Timur (Stewart 2009), Belize (Heyman et al. 2001), California (Nelson et al. 2007), dan Mexico (Motta et al. 2010). Selain itu, di
Indonesia penelitian mengenai
penyebarannya sudah dilakukan di Taman Nasional Teluk Cendrawasih (Himawan 2014).
Perairan Indonesia yang terletak di wilayah tropis merupakan salah satu jalur migrasi dan habitat hiu paus. Terbukti dari sering munculnya ikan ini hampir di sepanjang tahun maupun menetap secara musiman di perairan tertentu (WWF 2013).
Penelitian terkait genetika populasi hiu paus (Rhincodon typus) penting untuk dilakukan guna melihat struktur populasi, keragaman genetik dan kekerabatan hiu paus
(Rhincodon typus) yang terdapat di
Indonesia bahkan di Asia tenggara. Pada praktikum kali ini akan diajarkan metode analisis laboratorium pada studi kasus menggunakan sampel hiu paus (Rhincodon
typus).
Metode
Metode yang digunakan pada praktikum
ini adalah metode ekstraksi dengan
menggunakan Chelex. Chelex merupakan suatu senyawa ekstraksi yang terdiri dari Resin dan molecular grade water. Chelex yang digunakan pada praktikum ini adalah chelex 100. Sampel yang digunakan pada praktikum adalah sampel daging hiu paus
(Rhincodon typus). Sampel jaringan yang
diperoleh telah ditransport sesuai dengan prosedur standar yang direkomendasikan oleh Eckert et al. (1999). Sampel disimpan dalam tube berukuran 10 ml yang berisi
larutan ethanol 96% guna menjaga kualitas sampel dan diganti ketika lautan ethanol mulai mengalami perubahan warna. Sampel yang telah diperoleh kemudian dibawa ke
laboratorium untuk dilakukan uji
laboratorium lebih lanjut.
2.1 Waktu dan tempat
Praktikum dilakukan di Laboratorium
Marine Biodiversity and Biosystematics
Departemen Ilmu dan Teknologi Kelautan Fakultas Perikanan dan Ilmu Kelautan
Institut Pertanian Bogor. Praktikum
dilaksanakan pada tanggal 12 April 2016 dimulai pada pukul 19.00 WIB hingga selesai.
2.2 Alat dan Bahan
Alat dan bahan yang digunakan tersedia di Laboratorium Marine Biodiversity and
Biosystematics. Alat yang digunakan pada
praktikum meliputi:
Tabel: Alat dan bahan yang digunakan pada praktikum
No Alat Kegunaan
1. Thermocycle Mesin PCR
2. Pinset Penjepit Sampel
3. Centrifuge Pemutar Sampel
4. Vortex Pengaduk Sampel
5. Micro
Pipet Pipeting
6. Heating Block Pemanas Sampel
7. Mesin UV Melihat Genom
Elektro
8. Microwave Pemanas Gel
9. Electro Champber Analisis Genom
10. Glove Pelindung
Tangan
11. Masker Mencegah
Kontaminasi
12. Bunsen Pensteril Alat
13. Tisu Handuk Pembersih
14. Glove Elektroforesis Pelindung
15. Microtube 1.5 Ml Tempat Sampel
16. Tube 2.0 Ml Tempat Sampel
No Bahan Kegunaan
1. Chelex 100% Reagent Ekstraksi
2. Master Mix Reagent
3. Primer LTEi9 Primer Depan
4. Primer H950 Primer Belakang
5. ddH2O Reagent
6. Aquades Mencuci Sampel
7. Ethanol 96% Pengawet
2.3 Langkah Kerja Ekstraksi
Metode ekstraksi yang digunakan pada praktikum ini adalah metode dengan menggunakan chelex. Proses ekstraksi DNA menggunakan metode Chelex 10% dengan komposisi air molekuler dan resin 100%. Jaringan yang diambil merupakan jaringan otot yang banyak mengandung mitokondria, hal ini dikarenakan DNA target yang akan diambil berasal dari DNA mitokondria. Langkah kerja dari metode ini sendiri akan diuraikan dalam bentuk grafik skema dibawah ini.
Gambar: Tahapan proses ekstraksi dengan menggunakan metode chelex
PCR (polymerasi Chain Reaction)
Amplikasi sampel produk esktraksi
dilakukan menggunakan teknik PCR
(Polymerase Chain Reaction) secara in vitro dengan menggunakan primer depan Fish F1 [5’-TCA ACC AAC CAC AAA GAC ATT GGC AC-3’] dan primer belakang Fish R1 [5’-TAG ACT TCT GGG TGG CCA AAG AAT CA-3’] yang direkomendasikan oleh Alberto Abreu-Grobois et al. (2006). PCR dilakukan dalam kondisi 2 µl template
DNA, 9 µl ddH2O, 1,25 µl Primer depan dan
belakang (10 mM), dan 12,5 µl KAPPA ready mix. Proses teknik PCR dilakukan dengan menggunakan mesin PCR (thermo
cycler) dengan total siklus yaitu 38 siklus.
Setiap siklusnya terdiri atas denaturation pada suhu 94°C selama 30 detik, annealling pada suhu 50°C selama 30 detik, dan
extention pada suhu 72°C selama 45 detik.
Kemudian dilanjutkan dengan final
elongated pada suhu 72°C selama 5 detik.
Elektroforesis
Elektroforesis merupakan suatu metode pemisahan senyawa kimia yang berprinsip pada laju pergerakan molekul dalam aliran
listrik (Maduppa 2014). Proses
elektroforesis dilakukan bertujuan untuk melihat komponen DNA yang terdapat pada sampel tukik. Elektroforesis dilakukan pada gel agarose 0.5% yang telah diisi etidium bromide dengan konsentrasi 25 µg/ml dengan marker 100 bp DNA Ladder menggunakan tegangan 100V selama 25 menit. visualisasi DNA dilakukan dengan menggunakan UV dan didokumentasikan
dengan alat geldocs yang dapat
memperlihatkan band DNA memalui layar komputer.
Hasil dan Pembahasan
Berdasarkan praktikum yang telah
dilakukan maka diperoleh hasil
elektroforesis dari beberapa sampel yang telah dilakukan. Hasil elektroforesis dari semua sampel menunjukkan band yang positif. Hal tersebut dapat dilihat pada
Siapkan tabung Chelex 10%
Lakukan pelabelan pada tabung chelex
Gunakan penjepit steril untuk mengambil daging sampel Masukkan daging sampel kedalam chelex Lakukan langkah 3
dan 4 pada semua sampel Lakukan vortex dan
spinning pada
sampel yang telah di ekstraksi
panaskan sampel pada suhu 90o
selama 45 menit
Lakukan kembali vortex dan spinning
pada sampel yang telah dipanaskan
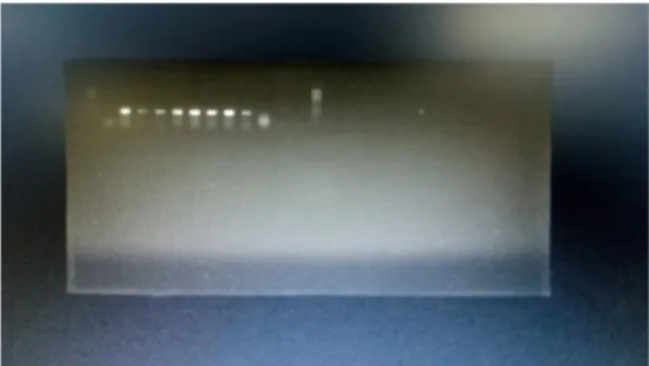
gambar hasil elektroforesis yang ditujukkan dibawah ini.
Gambar: Hasil elektoforesis dari sampel hiu paus (Rhincodon typus)
Gambar diatas menunjukkan sampel dengan band yang positif. Band positif mengindikasikan bahwa semua sampel yang telah diekstraksi dengan menggunakan metode chelex dan PCR (Polymerase Chain
Reaction) yang berjumlah 8 buah mengandung DNA dari sampel hiu paus yang telah dilakukan. Dari hasil yang diperoleh maka produk PCR yang telah diperoleh dapat dilakukan ketahap proses selanjutnya untuk mendapatkan produk
sekuens dalam bentuk visual
(chromatogram). Data ini selanjutnya akan dianalisis menggunakan software Mega Analysis untuk dapat dibaca data sekuens yang telah diperoleh.
Daftar Pustaka
Abreu-Grobois A, Horrocks J, Formia A, Dutton P, LeRoux R, VélezZuazo X, Soares L, Meylan P. 2006. New mtDNA dloop primers which work for a variety of marine turtle species may increase the resolution of mixed stock analyses. Di dalam: International Sea
Turtle Society. 26th Annual
Symposium on Sea Turtle Biology and Conservation; 2006 April 3-8; Island
of Crete, Greece: International Sea Turtle Society. Hal 179. 1601.
Eckert KL, Bjorndal KA, Abreu-Grobois FA, Donnelly M, Editors. 1999.
Research and Management Techniques for the Conservation of Se a Turtles.
Washington (2-8317-0364-6):
IUCN/SSC Marine Turtle Specialist Group.
Heyman WD, Rachel TG, Bjorn k, Robert EJ. 2001. Whale Shark Rhincodon typus aggregate to feed on fish spawn in Belize. Marine Ecology Progress Series. 215: 275-282.
Himawan MR. 2014. Komposisi Hiu Paus
Berdasarkan Jenis Kelamin dan
Ukuran serta Perilaku Kemunculannya di Kawasan Taman Nasional Teluk Cendrawasih [Skripsi]. Program Studi Ilmu dan Teknologi Kelautan. Fakultas Perikanan dan Ilmu Kelautan. Bogor (ID): Institut Pertanian Bogor.
Madduppa H. 2014. Bioekologi dan
Biosistematika Ikan Terumbu. Bogor (ID): IPB Press.
Motta PJ, Maslanka M, Heuter RE, Davis RL, Parra R, Mulvany SL, Habegger Ml, Strother JA, Mara KR, Ganrdiner JM, Tyminsky JP, Zeigler LD. 2010. Feeding anatomy, filter-feeding rate, and diet of whale sharks (Rhincodon typus) during surface ram filter feeding off the Yucatan Peninsula, Mexico. Fisheries Research. 113: 199-212. Nelson JD, Eckert SA. 2007. Foraging
Ecology of Whale Shark (Rhincodon typus) Within Bahia de Los Angeles,
Baja California Norte, Mexico.
Fisheries Research. 84: 47-64.
Norman BM, John DS. 2007. Size and maturity status of the whale shark (Rhincodon typus) at Ningaloo Reef in
Western Australia. Fisheries Research. 84: 81-86.
Steven GW, Taylor JG, Pearce AF. 2001. The seasonal aggregation of whale sharks at Ningaloo Reef, Western Australia: currents, migrations and the El Ni˜no/ Southern Oscillation. Environmental Biology of Fishes. 61: 1–11.
Stewart BS. 2009. Movements and habitats of whale sharks of East Africa: Results
of tagging studies in 2007 & 2008. HSWRI Technical Report. 368: 1-61.
Lampiran: Dokumentasi
Alat dan
digunakan pada praktikum
Asisten sedang memberikan pengarahan
Asisten menjelaskan cara penggunaan alat
Kegiatan ekstraksi sampel hiu paus
Proses vorteks
sampel yang
telah di
ekstraksi
Spinning sampel agar terendam bersama chelex
Sampel dipanaskan (heating) agar terjadi proses lisis pada sampel