OPTIMASI NATRIUM BIKARBONAT DAN CAMPURAN ASAM TARTRAT-ASAM FUMARAT
SEBAGAI EKSIPIEN DALAM PEMBUATAN GRANUL EFFERVESCENT EKSTRAK RIMPANG TEMULAWAK (Curcuma xanthorrhiza Roxb.)
SECARA GRANULASI BASAH DENGAN METODE DESAIN FAKTORIAL
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S. Farm)
Program Studi Ilmu Farmasi
Diajukan oleh: Made Dwi Rantiasih
NIM : 038114120
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
2007
ii
iii
Hidup adalah perjuangan... berjuanglah
Hidup adalah roh/atma... sadarilah
Hidup adalah teka-teki... pecahkanlah
(Sabda Gita tentang Hidup)
KARYA INI KUPERSEMBAHKAN UNTUK:
Ida Sang Hyang Widhi Wasa
yang senantiasa melimpahkan rahmatnya untukku Ayah- Ibuku, keluargaku tercinta
Sebagai ungkapan rasa hormat dan baktiku Adex atas cinta dan kasih sayangnya selama ini
Sahabat-sahabatku selama berjuang... Serta almamaterku...
iii i
v
KATA PENGANTAR
Puji syukur penulis persembahkan kepada Ida Sang Hyang Widhi Wasa, Tuhan Yang Maha Esa karena atas bimbingan dan berkat-Nyalah skripsi yang berjudul “Optimasi Natrium Bikarbonat dan Campuran Asam Tartrat-Asam Fumarat sebagai Eksipien Dalam Pembuatan Granul Effervescent Ekstrak Rimpang Temulawak (Curcuma xanthorrhiza Roxb.) secara Granulasi Basah dengan Metode Desain Faktorial” ini dapat diselesaikan. Skripsi ini dipersembahkan dalam rangka memenuhi syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Dalam kesempatan ini penulis ingin mengucapkan rasa terma kasih kepada segenap pihak yang telah membantu baik secara langsung maupun tidak langsung, terutama kepada :
1. Ibu Rita Suhadi, M.Si.,Apt, selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Sri Hartati Yuliani, M.Si.,Apt., selaku Pembimbing yang telah membantu membimbing serta memberikan masukan kepada penulis dalam menyelesaikan skripsi ini.
3. Ibu Agatha Budi Susiana Lestari, S.Si.,Apt., selaku pemimpin proyek penelitian yang telah membantu, membimbing serta memberikan masukan kepada penulis dalam menyelesaikan skripsi ini.
4. Ibu Rini Dwiastuti, S.Farm., Apt., selaku Penguji yang telah meluangkan waktunya serta memberikan masukan bagi penulis dalam menyelesaikan skripsi ini.
5. Ibu Christine Patramurti, M.Si., Apt., selaku Penguji yang telah
meluangkan waktunya serta memberikan masukan bagi penulis dalam menyelesaikan skripsi ini.
6. Bapak Prof. Dr. Sudibyo Martono, M.Si., Apt., atas sumbangan kurkumin síntesis yang digunakan dalam penelitian ini serta masukan-masukan yang telah diberikan kepada penulis.
7. Bapak Ign. Kristio Budiasmoro, M.Si., dan Bapak Yohanes Dwiatmaka, M.Si., yang telah meluangkan waktu untuk memberi pengarahan kepada penulis untuk kesempurnaan skripsi ini.
8. Bapak dan Ibuku yang tercinta, seluruh keluargaku yang selalu memberikan semangat, motivasi dan kasih sayang serta doanya
9. Tyas Ayu Puspita dan Lucia Esti Purwandari, teman-teman yang selalu berjuang bersama dalam suka dan duka, semangat kalian menjadi motivasi bagi penulis
10. Mas Wagiran, Pak Musrifin, Mas Otok, Mas Agung, yang telah membantu dalam menyelesaikan penelitian di Laboratorium
11. Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah membantu penulis dalam menyelesaikan penelitian ini
Penulis menyadari bahwa masih banyak terdapat kekurangan dalam skripsi ini. Oleh karena itu penulis mengharapkan saran dan kritik yang bersifat membangun.
Penulis
INTISARI
Telah dilakukan penelitian tentang optimasi natrium bikarbonat dan campuran asam tartrat-asam fumarat sebagai eksipien dalam formula granul effervescent ekstrak rimpang temulawak. Penelitian ini bertujuan untuk mengetahui besarnya efek faktor natrium bikarbonat dan campuran asam tartrat-asam fumarat serta interaksi keduanya, yang bersifat dominan terhadap sifat fisik granul effervescent, serta mengetahui area komposisi optimum natrium bikarbonat dan campuran asam tartrat-asam fumarat sebagai eksipien untuk menghasilkan granul effervescent yang sesuai dengan persyaratan.
Penelitian ini merupakan rancangan eksperimental murni menggunakan metode desain faktorial dengan dua faktor (natrium bikarbonat dan campuran asam tartrat-asam fumarat) dan dua level (level rendah dan level tinggi) untuk menentukan efek dari beberapa faktor dan interaksinya yang signifikan. Respon yang dikehendaki yaitu kecepatan alir, waktu larut dan kandungan lembab granul. Dari hasil yang diperoleh kemudian dibuat contour plot sifat fisik granul yang dikehendaki.
Dari hasil penelitian dapat diketahui bahwa efek interaksi natrium bikarbonat dan campuran asam tartrat-asam fumarat diprediksi dominan berpengaruh terhadap kecepatan alir dan waktu larut. Efek campuran asam tartrat-asam fumarat diprediksi dominan berpengaruh terhadap kandungan lembab granul. Dari contour plot super imposed yang terbentuk diperoleh area komposisi optimum natrium bikarbonat dan campuran asam tartrat-asam fumarat terbatas pada level yang diteliti.
Kata kunci: natrium bikarbonat, asam tartrat, asam fumarat, granul effervescent, ekstrak rimpang temulawak (Curcuma xanthorrhiza Roxb.), desain faktorial
ABSTRACT
Have been done research about the optimization between sodium bicarbonate and tartaric acid-fumaric acid combination as excipients in effervescent granules formulation of Tumeric (Curcuma xanthorrhiza Roxb.) extract. This research represent to know the effect of the factor of sodium bicarbonate and tartaric acid-fumaric acid combination or their interaction that dominant to influence physical properties of granules, and also to know the optimal composition area of sodium bicarbonate and tartaric acid-fumaric acid combination as excipients which can be make the physical properties of effervescent granules desired.
This research represent the pure research experimental use designed factorial, with two factor (sodium bicarbonate and tartaric acid-fumaric acid combination) and two level (low level and high level) to specify effect from several significant factor and interaction. Categorize repon desired that is flow rate, disintegration time, and moisture content of granules. Then make the contour plot of the physical properties of granules desired.
From the result of the research known that interaction effect between sodium bicarbonate and tartaric acid-fumaric acid combination dominantly predicted in determine flow rate and disintegration time of granules. Tartaric acid-fumaric acid combination effect dominantly predicted in determine moisture content of granules. From contour plot super imposed formed obtained a optimum composition of sodium bicarbonate and tartaric acid-fumaric acid combination finite at level which have been determined.
Keyword : sodium bicarbonate, tartaric acid, fumaric acid, effervescent granules, Tumeric (Curcuma xanthorrhiza Roxb.) extract, design factorial
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
KATA PENGANTAR... vi
INTISARI ... viii
ABSTRACT ... ix
DAFTAR ISI ... x
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvii
DAFTAR LAMPIRAN ... xix
BAB I. PENGANTAR... 1
A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian Penelitian ... 3
3. Manfaat Penelitian ... 3
B. Tujuan Penelitian... 4
BAB II. PENELAAHAN PUSTAKA... 5
A. Temulawak ………... 5
1. Klasifikasi ...……….. 5
2. Nama daerah ...………... 5
3. Ciri-ciri morfologi ...………... 5
4. Kandungan kimia ...………... 6
5. Khasiat temulawak ...………. 6
B. Kurkumin ...………... 7
C. Kromatografi Lapis Tipis (KLT) Densitometri ... 8
D. Maserasi ...…………... 10
E. Ekstrak ...………... 12
F. Granul Effervescent ...………... 13
G. Metode Pembuatan Granul Effervescent ...……….. 13
1. Metode granulasi basah ……….. 14
2. Metode granulasi kering ...……… 15
H. Uji Sifat Fisik Granul ... 15
1. Sifat alir ...……….. 15
2. Kandungan lembab ...………... 16
3. Waktu larut ………... 16
I. Bahan-Bahan Pembuatan Granul Effervescent………... 16
1. Sumber karbonat ...………... 17
2. Sumber asam ...………... 17
3. Bahan pengisi ...………... 18
4. Bahan pengikat ....………... 18
5. Bahan tambahan .………... 19
J. Pemerian Bahan ...………...……… 19
1. Natrium bikarbonat anhidrat ... 19
2. Asam tartrat anhidrat ... 20
3. Asam fumarat anhidrat ... 20
4. Laktosa ... 20
5. Polivinilpirolidon (PVP) ... 21
6. Aspartam ... 21
K. Desain Faktorial ...………... 22
L. Landasan Teori ...………... 24
M. Hipotesis ...…………... 27
BAB III. METODOLOGI PENELITIAN ……… 28
A. Jenis dan Rancangan Penelitian ……...………... 28
B. Variabel Penelitian dan Definisi Operasional ……….. 28
1. Variabel penelitian ………. 28
2. Definisi operasional ………... 29
C. Bahan dan Alat Penelitian ……… 31
D. Skema Kerja Penelitian ……… 33
E. Tata Cara Penelitian ………. 34
1. Determinasi tanaman temulawak ………..…… 34
2. Penyiapan simplisia dan pembuatan serbuk rimpang temulawak ……… 34
3. Pembuatan ekstrak rimpang temulawak ……… 35
4. Standarisasi ekstrak rimpang temulawak ………... 35
5. Penetapan dosis ekstrak rimpang temulawak …...………. 38
6. Penentuan level natrium bikarbonat dan campuran asam tartrat-asam fumarat ………..……… 38
7. Pembuatan granul effervescent……….. ……….. 40
8. Uji kualitas granul effervescent ………. 41
9. Penentuan efek ………... 42
1 0 . P e n e n t u a n p r o f i l s i f a t f i s i k g r a n u l d a n a r e a optimum ………..…… 42
F. Analisis Hasil ……… 42
BAB IV. HASIL PENELITIAN DAN PEMBAHASAN………. 43
A. Hasil Determinasi Rimpang Temulwak ……….. 43
B. Penyiapan Simplisia dan Pembuatan serbuk Rimpang Temulwak ……… 43
C. Pembuatan ekstrak rimpang temulawak ... 45
D. Hasil Standarisasi Ekstrak Rimpang Temulawak ...……… 46
1. Uji organoleptik ...………. 46
2. Uji daya lekat ...………. 46
3. Uji viskositas ...………... 47
4.Uji kandungan lembab ...………... 48
5. Uji kualitatif ekstrak rimpang temulawak ……….. 49
6. Uji kuantitatif ekstrak rimpang temulawak ……....……… 52
E. Penetapan Dosis Ekstrak Rimpang Temulawak ... 53
F. Formulasi Granul Effervescent Ekstrak Rimpang Temulawak ... 54
G. Hasil Uji Sifat Fisik Granul Effervescent Ekstrak
Rimpang Temulawak ... 55
1. Kecepatan alir ... 55
2. Waktu larut ... 58
3. Kandungan lembab ... 61
H. Prediksi Formula Optimum Granul ... 64
BAB V. KESIMPULAN DAN SARAN ... 69
A. Kesimpulan ... 69
B. Saran ... 69
DAFTAR PUSTAKA ... 70
LAMPIRAN ...………… 74
BIOGRAFI PENULIS ………. 104
DAFTAR TABEL
Halaman
Tabel I. Notasi formula desain faktorial……….. 23
Tabel II. Formula granul effervescent……….. ... 40
Tabel III. Hasil uji sifat fisik ekstrak rimpang temulawak ...…... 46
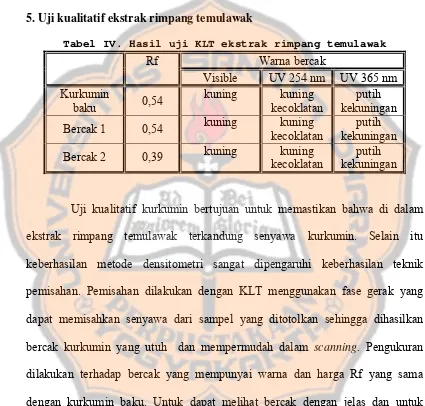
Tabel IV. Hasil uji KLT ekstrak rimpang temulwak …………... 49
Tabel V. Hubungan kadar kurkumin baku dengan AUC ....……... 52
Tabel VI. Penetapan Recovery dan nilai CV ... 53
Tabel VII. Hasil uji sifat fisik granul………. 55
Tabel VIII. Efek natrium bikarbonat, efek campuran asam tartrat- asam fumarat terhadap sifat fisik granul……… 55
Tabel IX. Data recovery 0, 12 µg/µl ……… 75
Tabel X. Data recovery 0, 14 µg/µl ...……… 75
Tabel XI. Data recovery 0, 18 µg/µl ….……… 76
Tabel XII. Data recovery 0, 23 µg/µl ....……… 76
Tabel XIII. Data recovery 0, 35 µg/µl ……….. 77
Tabel XIV. Penetapan kadar kurkumin dalam ekstrak rimpang temulawak ………... 78
Tabel XV. Uji daya lekat ekstrak rimpang temulawak ... 80
Tabel XVI. Uji viskositas ekstrak rimpang temulawak ... 80
Tabel XVII.Uji kandungan lembab ekstrak rimpang temulawak ……… 81
Tabel XVIII. Nilai Rf kurkumin standar, bercak 1, dan bercak 2... 82
Tabel XIX. Uji kecepatan alir granul ... 87
Tabel XX. Uji waktu larut granul ... 87
Tabel XXI. Uji kandungan lembab granul ... 88
Tabel XXII. Nilai efek kecepatan alir granul ... 89
Tabel XXIII. Nilai efek waktu larut granul ... 91
Tabel XXIV. Nilai efek kandungan lembab granul ... 94
Tabel XXV.Pengaruh natrium bikarbonat terhadap kecepatan alir granul ... 97
Tabel XXVI. Pengaruh campuran asam tartrat-asam fumarat terhadap kecepatan alir granul .……… 97
Tabel XXVII. Pengaruh natrium bikarbonat terhadap waktu larut granul ... 98
Tabel XXVIII. Pengaruh campuran asam tartrat-asam fumarat terhadap waktu larut granul ... 98
Tabel XXIX. Pengaruh natrium bikarbonat terhadap kandungan lembab granul ... 99
Tabel XXX. Pengaruh campuran asam tartrat-asam fumarat terhadap kandungan lembab granul ... 99
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur kurkumin……….. 7
Gambar 2. Skema kerja penelitian……… 33
Gambar 3a. Foto uji KLT UV 254 nm………... 50
Gambar 3b. Foto uji KLT UV 365 nm………... 51
Gambar 4. Kurva baku hubungan antara kadar kurkumin standar dengan AUC ... 52
Gambar 5a. Pengaruh natrium bikarbonat terhadap kecepatan alir…….. 56
Gambar 5b. Pengaruh campuran asam tartrat-asam fumarat terhadap kecepatan alir………... 56
Gambar 6a. Pengaruh natrium bikarbonat terhadap waktu larut...….... 59
Gambar 6b. Pengaruh campuran asam tartrat-asam fumarat terhadap waktu larut……….... 59
Gambar 7a. Pengaruh natrium bikarbonat terhadap kandungan lembab…... 62
Gambar 7b. Pengaruh campuran asam tartrat-asam fumarat terhadap kandungan lembab……….. 62
Gambar 8. Contour plot kecepatan alir granul………. 65
Gambar 9. Contour plot waktu hancur granul………..… 66
Gambar 10. Contour plot kandungan lembab granul……… 67
Gambar 11. Contour Plot Super Imposed...………. 68
Gambar 12. Kromatogram kurva baku ……… 74
Gambar 13. Kromatogram sampel ………... 78 Gambar 14. Tanaman temulawak ……….... 101 Gambar 15. Rimpang temulawak ……… 101 Gambar 16. Ekstrak rimpang temulawak untuk granul effervescent …... 101 Gambar 17. Granul effervescent ekstrak rimpang temulawak …………. 102 Gambar 18. Larutan dan granul effervescent ………... 102
DAFTAR LAMPIRAN
Halaman Lampiran 1. Hubungan antara kadar kurkumin standar dengan
area kromatogram untuk pembuatan kurva baku ... ... 74
Lampiran 2. Data recovery ... 75
Lampiran 3. Penetapan kadar kurkumin dalam ekstrak rimpang Temulawak ..……… 78
Lampiran 4. Perhitungan dosis ekstrak rimpang temulawak …... 79
Lampiran 5. Standarisasi ekstrak rimpang temulawak ..…….…………. 80
Lampiran 6. Perhitungan level tinggi dan level rendah campuran asam tartrat-asam fumarat ………... 83
Lampiran 7. Perhitungan level tinggi dan level rendah natrium bikarbonat ……… 84
Lampiran 8. Uji sifat fisik granul effervescent ……… 87
Lampiran 9. Perhitungan desain faktorial ..………... 89
Lampiran 10. Perhitungan kecuraman kurva ………... 97
Lampiran 11. Temulawak (Curcuma xanthorrhiza Roxb.) ………. 101
Lampiran 12. Larutan dan granul effervescent ekstrak rimpang temulawak ……… 102
Lampiran 13. Surat determinasi tanaman temulawak …………. ……… 103
BAB I PENGANTAR A. Latar Belakang
Temulawak merupakan salah satu bahan obat tradisional yang sudah sering digunakan untuk pengobatan karena memiliki banyak khasiat. Penelitian mengenai manfaat temulawak sebagai obat tradisional serta pengembangan bentuk sediaan yang berasal dari temulawak telah banyak dilakukan. Termasuk penelitian yang dilakukan oleh Chrystyani (2005), yang berjudul Optimasi Campuran Asam Tartrat dan Asam Fumarat sebagai Eksipien pada Pembuatan Granul Effervescent Ekstrak Rimpang Temulawak Secara Granulasi Basah Aplikasi Desain Faktorial. Dalam penelitian tersebut dikembangkan bentuk sediaan granul effervescent dari ekstrak rimpang temulawak, dengan melakukan optimasi pada campuran asam tartrat dan asam fumarat sebagai sumber asam.
Keuntungan dari pemilihan bentuk sediaan berupa granul effervescent dibandingkan dengan bentuk sediaan yang lain adalah proses penyajian yang cepat dengan dosis yang tepat, serta adanya gas CO2 yang dihasilkan dari reaksi asam dan basa akan memberikan sensasi menyegarkan saat digunakan. Selain itu keberadaan gas CO2 dapat menutupi rasa pahit dan pedas dari temulawak hal tersebut dapat menambah kenyamanan konsumen saat menggunakan sediaan obat. Penelitian Chrystyani (2005), menghasilkan campuran optimum asam tartrat dan asam fumarat, penggunaan campuran asam lebih dipilih dibandingkan dengan menggunakan asam tunggal karena pada penggunaan asam tunggal akan menimbulkan kesukaran yaitu akan menghasilkan granul yang menggumpal
(Ansel,1989). Kemudian dicoba dilakukan penelitian lebih lanjut tentang optimasi antara natrium bikarbonat dan campuran asam tartrat-asam fumarat sebagai sumber basa dan sumber asam dalam sediaan granul effervescent. Campuran asam dan basa perlu dioptimasi karena campuran asam dan basa inilah yang jika bereaksi dengan adanya air akan melepaskan gas CO2, yang berfungsi sebagai penghancur dalam granul effervescent.
Untuk mendapatkan perbandingan jumlah natrium bikarbonat dan campuran asam tartrat-asam fumarat yang tepat sehingga dapat menghasilkan sediaan granul effervescent yang berkualitas, maka penulis merasa perlu untuk melakukan optimasi formula granul effervescent berikut kontrol kualitasnya yaitu uji sifat fisik meliputi kecepatan alir, waktu larut, dan kandungan lembab granul effervescent. Optimasi formula dalam penelitian ini menggunakan metode desain
faktorial. Dipilih metode optimasi desain faktorial karena metode ini lebih sederhana dibandingkan metode optimasi yang lain, selain itu metode ini juga dapat menggambarkan model hubungan antara variabel respon dengan satu atau lebih variabel bebas. Persamaan umumnya: Y= bo + b1(A) + b2 (B) + b12 (A)(B).
1. Permasalahan
Rumusan masalah dari penelitian ini adalah sebagai berikut:
1. manakah efek yang diprediksi memberikan pengaruh dominan terhadap sifat-sifat fisik granul effervescent ekstrak rimpang temulawak, natrium bikarbonat, campuran asam tartrat-asam fumarat, atau interaksi?
2. apakah dapat ditemukan area komposisi optimum natrium bikarbonat dan
campuran asam tartrat-asam fumarat yang dikehendaki dalam contour plot super imposed pada pembuatan granul effervescent ekstrak rimpang temulawak?
2. Keaslian Penelitian
Berdasarkan sumber informasi yang diperoleh, penelitian ilmiah tentang ekstrak rimpang temulawak dan formulasi granul effervescent ekstrak rimpang temulawak sudah pernah dilakukan. Namun penelitian tentang optimasi natrium bikarbonat dan campuran asam tartrat-asam fumarat sebagai eksipien dalam pembuatan granul effervescent ekstrak rimpang temulawak secara granulasi basah dengan metode desain faktorial belum pernah dilakukan sebelumnya.
3. Manfaat Penelitian
Manfaat penelitian ini adalah sebagai berikut: 1. Manfaat Teoritis
tartrat-asam fumarat sebagai eksipien dalam formula pembuatan granul effervescent ekstrak rimpang temulawak.
2. Manfaat Praktis.
Memperkenalkan kepada masyarakat sediaan granul effervescent ekstrak rimpang temulawak yang dapat dikonsumsi dengan aman, manjur, dan nyaman, serta dapat diterima oleh masyarakat.
B. Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui tentang :
1. pengaruh natrium bikarbonat, campuran asam tartrat-asam fumarat serta interaksi keduanya dalam menentukan kecepatan alir, waktu larut, dan kandungan lembab granul effervescent ekstrak rimpang temulawak.
BAB II
PENELAAHAAN PUSTAKA
A. Temulawak (Curcuma xanthorrhiza Roxb.) 1. Klasifikasi :
Suku : zingiberaceae (Dalimartha, 2000). 2. Nama daerah
Sumatera: temulawak. Jawa: koneng gede, temu raya, temu besar, aci koneng, koneng tegel, temulawak. Madura: temolabak. Bali: tommo. Sulawesi Selatan: tommon. Ternate: karbanga (Dalimartha, 2000)
3. Ciri-ciri morfologi
temulawak belum pernah dilaporkan menghasilkan buah atau biji. Rimpang dibedakan atas rimpang induk (empu) dan rimpang cabang. Rimpang induk bentuknya jorong atau gelendong, berwarna kuning tua atau coklat kemerahan, bagian dalam berwarna jingga coklat. Rimpang cabang keluar dari rimpang induk, ukurannya lebih kecil, tumbuh ke arah samping, bentuknya bermacam-macam, dan warnanya lebih muda. Akar-akar di bagian ujung membengkak, membentuk umbi yang kecil. Rimpang temulawak termasuk yang paling besar diantara semua rimpang marga Curcuma (Dalimartha, 2000).
4. Kandungan kimia
Rimpang temulawak mengandung 48-64% zat tepung, 1,6-2,2% kurkumin dan 1,48-1,63% minyak atsiri (Karden, 2003). Fraksi pati merupakan kandungan terbesar, jumlah bervariasi antara 48-54% tergantung dari ketinggian tempat tumbuh. Makin tinggi tempat tumbuh maka kadar pati makin rendah dan kadar minyak atsiri makin tinggi (Dalimartha, 2000).
5. Khasiat temulawak
(hiperkolesterolemia), haid tidak lancar, flek hitam di muka, jerawat, wasir, dan produksi ASI yang sedikit (Dalimartha, 2000).
B. Kurkumin
O O
HO
H3CO OCH3
OH
(Kurkumin)
1,7-Bis-(4-hydroxy-3-methoxy-phenyl)-hepta-1,6-diene-3,5-dione
Gambar 1. Struktur kurkumin
Kurkumin (C21H20O6), titik didih 184-185°C diisolasi pertama kali pada tahun 1815. Pada tahun 1910 Daube telah berhasil menemukan bentuk kristal dari kurkumin (Majeed, Badmaev, Shivakumar, and Rajendran, 1995).
Kurkumin merupakan zat warna kuning utama (0,5-6%) yang terdapat dalam beberapa spesies Curcuma seperti Curcuma longa L atau Curcuma domestica Val. Kurkumin beserta turunan demetoksinya yaitu demetoksi
kurkumin dan bis demetoksi kurkumin dikenal dengan nama kurkuminoid (Martono, 1996).
Henegouwen, Gerard, and Karlsen, 1986). Kurkumin adalah senyawa yang sukar larut air dengan kelarutan 0,1 mg/ml (Anonim, 2006), larut dalam etanol dan aseton. (Tonnesen and Karlsen, 1985). Kurkuminoid di dalam rimpang temulawak merupakan campuran dari kurkumin dan demetoksikurkumin (Paris and Moyse, 1981).
Kurkumin dan analognya mempunyai aktivitas biologi antara lain sebagai antiinflamasi, antioksidan dan kolagen. Di samping itu kurkumin mempunyai aktivitas biologi spektrum luas yaitu sebagai hipokolesteremik, antiinflamasi, antireumatik, antibakteri, antihepatotoksik, menurunkan glukosa darah dan hipotensif (Tonnesen and Karlsen, 1985).
C. Kromatografi Lapis Tipis (KLT) Densitometri
Pemakaian kurkumin sebagai bahan obat atau campuran obat harus diberikan dengan dosis yang tepat, untuk itu harus diketahui kadar kurkumin dalam sediaan yang diberikan. Untuk mengetahui kadar dengan tepat, diperlukan metode analisis yang tepat, mengingat kurkumin dalam sediaan obat atau makanan umumnya bukan kurkumin murni, namun sebagai kurkuminoid. Apabila kurkumin merupakan zat aktif utama dalam sediaan maka harus dipilih metode penetapan yang dapat memisahkan kurkumin dari turunan demetoksinya (Martono, 1996).
baik lazimnya digunakan adsorben siap pakai yang telah mengalami pra pencucian (Gritter, Bobit, dan Schwarting, 1991).
Menurut Hardjono (1985), penetapan suatu kadar dengan metode densitometri dilakukan dengan mengukur kerapatan bercak senyawa yang dipisahkan dengan cara KLT. Pada umumnya pengukuran kerapatan bercak tersebut dibandingkan dengan kerapatan bercak senyawa standar yang dielusi secara bersama-sama.
Ada dua cara penetapan kadar dengan alat densitometri. Pertama, setiap kali ditotolkan sediaan baku dari senyawa yang bersangkutan dan dielusi bersama-sama dalam satu lempeng, kemudian Area Under Curve (AUC) sampel dibandingkan dengan harga AUC baku. Yang kedua, dengan membuat kurva baku hubungan jumlah zat baku dengan AUC. Kurva baku diperoleh dengan membuat totolan zat baku pada KLT dengan bermacam-macam konsentrasi (minimal tiga macam konsentrasi). Bercak yang diperoleh dicari nilai AUC nya dengan alat densitometer. Dari kurva baku diperoleh persamaan Y = bX + a, X adalah banyaknya zat yang ditotolkan dan Y adalah AUC (Supardjan, 1987).
sebanding dengan jumlah zat pada bercak yang terkena sinar tersebut (Wardani, 2003).
Penelusuran bercak dapat pula dilakukan secara horisontal maupun vertikal (scanning horizontal atau scanning vertical). Penelusuran bercak secara horisontal dapat dilakukan satu per satu atau apabila bercak yang diperoleh pada pelat segaris, dapat dilakukan penelusuran semua bercak sekaligus (Wardani, 2003).
Berdasarkan jalannya sinar, penelusuran dapat dilakukan dengan dua cara, yaitu penelusuran lurus dan zig-zag (naik turun). Pada penelusuran lurus, sinar yang mengenai bercak berjalan lurus dari kiri ke kanan. Sedangkan pada penelusuran zig-zag, sinar mengenai bercak berjalan zig-zag dari kiri ke kanan. Penelusuran bercak akan mendapatkan hasil yang baik apabila dilakukan pada panjang gelombang maksimum (Wardani, 2003).
D. Maserasi
cairan penyari. Cairan penyari akan menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif. Zat aktif ini akan terlarut karena adanya perbedaan konsentrasi antara larutan di dalam dan di luar sel, maka larutan encer akan masuk ke dalam sel. Peristiwa ini terjadi berulang-ulang sampai terjadi keseimbangan antara konsentrasi di dalam dengan konsentrasi di luar sel (Anonim,1986).
Maserasi digunakan untuk penyarian simplisia yang mengandung zat aktif yang mudah larut dalam cairan penyari. Cairan penyari yang digunakan dapat berupa air, etanol, air-etanol, atau pelarut lain. Bila cairan penyari digunakan air, maka untuk mencegah timbulnya kapang dapat ditambahkan bahan pengawet, yang diberikan pada awal penyarian. Keuntungan cara penyarian dengan maserasi adalah cara pengerjaan dan peralatan yang digunakan sederhana (Anonim, 1986). Dibandingkan dengan proses perkolasi pada maserasi tidak memerlukan keahlian tertentu dalam pengoperasiannya, perkolasi juga lebih mahal karena memerlukan peralatan yang khusus dan menghabiskan lebih banyak waktu (Ansel, 1989).
E. Ekstrak
Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya matahari langsung. Sebagai cairan penyari digunakan air, eter atau campuran etanol dan air (Anonim, 1979).
Menurut Voigt (1994), pada ekstrak tumbuhan (umumnya konsentrasi etanolnya berbeda-beda), jika bahan pengekstraksinya diuapkan sebagian atau seluruhnya, maka diperoleh ekstrak yang dikelompokkan menurut sifat-sifatnya menjadi :
1. ekstrak cair (extractum fluidum), merupakan suatu ekstrak yang dibuat sedemikian rupa sehingga satu bagian simplisia sebanding dengan dua (kadang – kadang lebih) bagian ekstrak cair.
2. ekstrak encer (extractum tenue), sediaan seperti itu memiliki konsistensi madu dan dapat dituang.
3. ekstrak kental (extractum spissum), sediaan ini liat dalam keadaan dingin dan tidak dapat dituang. Kandungan airnya berjumlah sampai 30%. Tingginya kandungan air menyebabkan suatu instabilitas sediaan obat (kontaminasi bakteri) dan bahkan instabilitas bahan aktifnya (penguraian secara kimia). Selain itu, ekstrak kental sulit untuk ditakar (penimbangan dan sebagainya) . 4. ekstrak kering (extractum siccum), ekstrak ini memiliki konsistensi kering dan
F. Granul Effervescent
Granul effervescent adalah granul atau serbuk kasar sampai kasar sekali dan mengandung unsur obat dalam campuran kering, biasanya terdiri dari unsur asam (asam sitrat, asam tartrat, asam fumarat) dan unsur basa (natrium karbonat, natrium bikarbonat) bila ditambahkan dengan air, asam dan basanya bereaksi membebaskan karbondioksida sehingga menghasilkan buih (Ansel, 1989).
Keuntungan granul effervescent sebagai bentuk sediaan adalah penyiapan larutan dalam waktu yang cepat dan mengandung dosis obat yang tepat. Menghasilkan rasa yang enak karena adanya karbonat yang membantu memperbaiki rasa obat tertentu, mudah dan nyaman untuk digunakan oleh konsumen (Lindberg, et al., 1992). Kerugian dari granul effervescent adalah harganya yang relatif mahal, hal ini disebabkan karena jumlah yang besar dari eksipien yang harganya mahal dan fasilitas produk yang khusus (Lindberg, et al., 1992). Menurut Lachman dan Liebermann (1989), untuk menjaga kualitas granul effervescent pada penyimpanan perlu pengemasan secara khusus ke dalam
kantong lembaran aluminium kedap udara.
G. Metode Pembuatan Granul Effervescent
1. Metode granulasi basah
Menurut Mohrle (1980), pada prinsipnya proses granulasi untuk granul effervescent memiliki dasar yang sama dengan granulasi pada granul
konvensional. Teknik-teknik granulasi basah melibatkan pencampuran bahan-bahan kering dengan cairan penggranul untuk membuat massa (adonan) yang dapat dibentuk. Granulasi basah pada effervescent dapat dilakukan dengan tiga metode, yaitu dengan penggunaan panas, dengan cairan non reaktif, dan cairan reaktif.
a. Penggunaan panas. Metode ini meliputi pelepasan air dari bahan-bahan hidrat dalam formulasi pada suhu tinggi membentuk massa yang dapat dibentuk. Proses ini sulit untuk dikontrol agar mendapatkan hasil yang reprodusibel (Mohrle, 1980). Pengulangan pengadukan diperlukan untuk menghasilkan keseragaman komponen dalam formulasi (Lindberg, et al., 1992).
c. Dengan cairan reaktif. Cairan atau pelarut yang sering digunakan dalam metode ini adalah air. Proses ini sulit dikendalikan saat massa granul yang terbentuk harus dengan cepat dikeringkan guna menghentikan reaksi effervescent yang terjadi (Mohrle, 1980).
2. Metode granulasi kering
Granulasi dengan metode slugging atau dengan mengkompresi masa tablet yang berukuran besar menggunakan heavy-duty mesin atau roller compactor cocok digunakan untuk bahan-bahan yang tidak dapat diproses secara
granulasi basah. Slug dan bahan dari roller compactor akan mengalami pengurangan ukuran. Bahan pelicin sangat diperlukan selama proses slugging, komponen asam dan basa dapat digranulasi secara terpisah ataupun secara bersama-sama (Lindberg, et al., 1992).
H. Uji Sifat Fisik Granul 1. Sifat alir
2. Kandungan lembab
Kandungan lembab dapat mempengaruhi sifat fisika kimia sediaan padat. Keseimbangan kandungan lembab dapat mempengaruhi aliran dan karakteristik kompresi serbuk, kekerasan granul, serta stabilitas obat (Lachman dan Liebermann, 1989). Kandungan lembab granul effervescent perlu diketahui untuk melihat apakah ada reaksi effervescent yang prematur sehingga dapat mengakibatkan jumlah gas karbondioksida yang dihasilkan berkurang sehingga berpengaruh terhadap kenyamanan orang yang mengkonsumsi sediaan granul effervescent. Menurut Dash (2000), persyaratan kandungan lembab untuk granul
effervescent antara 0,4%-0,7% dan mudah larut dalam air.
3. Waktu larut
Menurut Wehling and Fred (2004), granul effervescent yang baik diharapkan larut dalam waktu kurang dari 2,5 menit (< 150 detik) menggunakan 200 ml air membentuk larutan jernih, dengan kata lain residu yang tidak larut harus seminimal mungkin.
I. Bahan-Bahan Pembuatan Granul Effervescent
ini terjadi setelah pembuatan granul, akan menyebabkan produk menjadi tidak stabil. Oleh karena itu, bahan penyusun granul dipilih dalam bentuk anhidrat yang sedikit atau tidak menyerap lembab atau bentuk hidrat (mengikat air dalam molekulnya) yang stabil dianjurkan untuk dipakai. Kelarutan bahan merupakan sifat lain yang penting dalam pembuatan granul effervescent. Jika bahan tidak larut, maka reaksi effervescent tidak akan terjadi dan granul tidak akan larut secara cepat (Mohrle, 1980).
1. Sumber karbonat
Sumber karbonat digunakan sebagai sumber timbulnya gas karbondioksida pada produk effervescent. Sumber karbonat yang biasa digunakan dalam produk effervescent adalah natrium bikarbonat (NaHCO3) dan natrium karbonat (Na2CO3) (Mohrle, 1980).
2. Sumber asam
Dalam pembuatan sediaan effervescent pada umumnya diolah dengan kombinasi dua jenis sumber asam, mengingat penggunaan asam tunggal dalam sediaan effervescent akan menimbulkan kesukaran, yaitu akan menghasilkan granul yang menggumpal (Ansel, 1989). Menurut Mohrle (1980) asam yang dibutuhkan dalam reaksi effervescent berasal dari 3 jenis sumber asam yaitu food acid (soda kue), asam anhidrat, dan garam-garam asam. Sumber asam yang paling
sering digunakan adalah dari jenis food acid. Yang termasuk food acid antara lain asam tartrat, asam sitrat, asam suksinat, asam malat dan asam fumarat.
menjadi bentuk asamnya, yang kemudian dapat bereaksi dengan sumber karbonat untuk menghasilkan reaksi effervescent (Mohrle, 1980).
3. Bahan pengisi
Pada peracikan obat dalam jumlah yang sangat kecil diperlukan bahan pengisi, untuk memungkinkan suatu pengempaan. Bahan pengisi ini menjamin granul memiliki ukuran atau massa yang dibutuhkan (Voigt, 1994). Pengisi juga dapat ditambah karena alasan yang lain yaitu untuk memperbaiki daya kohesi sehingga dapat dikempa langsung jika ingin dibuat menjadi tablet atau untuk memacu aliran (Banker and Anderson, 1986).
4. Bahan pengikat
Bahan pengikat yaitu bahan yang dapat membantu untuk mengikat bahan-bahan lain menjadi satu biasanya digunakan untuk mengikat serbuk menjadi granul. Kebanyakan bahan pengikat yang digunakan sama untuk pembuatan tablet maupun granul. Penggunaan bahan pengikat pada granul effervescent dibatasi karena dapat menimbulkan reaksi karbonasi. Bahan pengikat
seperti gom selulosa, gelatin dan pasta tidak banyak digunakan karena larutnya lama dan meninggalkan residu. Pengikat kering seperti laktosa, dekstrosa dan manitol sering digunakan tetapi tidak efektif pada konsentrasi rendah.
Sifat bahan pengikat yang digunakan untuk granul effervescent adalah memiliki kelarutan yang baik dalam air (water soluble), contohnya adalah polyvinylpyrrolidone atau polyvinylpyrrolidone-poly (vinyl acetate)-copolymer
5. Bahan tambahan
Dalam tablet effervescent biasanya sering ditambahkan bahan pemanis dan pewarna untuk memperbaiki penampilan dan rasa tablet. Tetapi yang paling penting untuk diperhatikan adalah bahan tersebut harus mudah larut dalam air agar tidak meninggalkan residu (Mohrle, 1980).
J. Pemerian Bahan 1. Natrium bikarbonat anhidrat
Natrium bikarbonat merupakan sumber utama penghasil karbon dioksida pada sistem effervescent. Bersifat mudah larut dalam air, tidak higroskopis, murah, jumlahnya banyak, dan dalam perdagangan terdapat dalam lima tingkatan berdasarkan ukuran partikelnya dari yang berbentuk serbuk halus sampai dengan bentuk granul yang free-flowing. Penggunaan yang lain yaitu sebagai antasida ataupun sebagai salah satu komponen dalam produk antasida. Dalam produksi makanan digunakan sebagai baking soda. Merupakan basa natrium yang paling ringan, memiliki pH 8,3 pada larutan berair dengan konsentrasi 0,85%. Reaksi natrium bikarbonat dengan asam dapat menghasilkan 52% karbon dioksida (Mohrle, 1980).
2. Asam tartrat anhidrat
Asam tartrat merupakan sumber asam yang selalu digunakan dalam pembuatan produk effervescent karena mudah didapatkan di pasaran, lebih mudah larut dibandingkan asam sitrat, dan juga lebih higroskopis dibandingkan asam sitrat. Kekuatan asamnya sama dengan asam sitrat (Mohrle, 1980).
Asam tartrat yang dikeringkan di atas fosfor pentoksida P selama 3 jam mengandung tidak kurang dari 99,7% dan tidak lebih dari 100,5% C4H6O6. Berat molekul dari asam tartrat adalah 150,9. Asam berupa hablur tidak berwarna atau serbuk hablur halus sampai granul, aroma tidak berbau, rasa asam, dan stabil di udara. Kelarutan sangat mudah larut air dan mudah larut etanol (Anonim, 1995). 3. Asam fumarat anhidrat
Kekuatan asam dari asam fumarat sama kuat dengan asam sitrat, hanya saja asam fumarat jarang digunakan dalam pembuatan produk effervescent karena kelarutannya yang rendah dalam air. Asam fumarat bersifat tidak higroskopis dibandingkan sumber asam lain. Kelarutan asam fumarat dapat meningkat jika ditambahkan 0,3% dioctyl sodium sulfosuccinate (Mohrle, 1980).
Asam fumarat berwarna putih, berbau atau sedikit berbau, serbuk kristal, kelarutan dalam air 4,5 g/L, dalam etanol (100%) sebesar 36 g/L pada suhu 20°C (Lindberg, et al., 1992).
4. Laktosa
menyerap bau. Mudah (dan pelan-pelan) larut dalam air dan lebih mudah larut dalam air mendidih, sangat sukar larut dalam etanol, tidak larut dalam klorofom dan dalam eter (Anonim, 1995).
5. Polivinilpirolidon (PVP)
PVP adalah bahan pengikat yang efektif dalam pembuatan granul effervescent. Bahan ini biasa ditambahkan pada serbuk untuk digranulasi basah
yang kemudian dibasahkan dengan cairan penggranul. Penambahan air harus sangat hati-hati dan dikontrol untuk mencegah terjadinya reaksi effervescent dini (Mohrle, 1980).
Polivinilpirolidon (PVP) merupakan polimerisasi dari
1-vinilpirolid-2-on. Bentuknya berupa serbuk putih atau putih kekuningan, berbau lemah atau
tidak berbau dan higroskopis. PVP mudah larut dalam air, etanol (95%), dan dalam kloroform P. Kelarutan tergantung dari bobot rata-rata dan tidak larut dalam ester P (Anonim, 1995).
6. Aspartam
setelah dimakan, akan tetapi stabilitasnya tergantung pada pH dan suhu. Stabil pada pH antara 3,4-5 dan pada suhu pendingin (Allen, 2002).
Berdasarkan Keputusan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia Nomor : HK.00.05.5.1.4547 tentang Persyaratan Penggunaan Bahan Tambahan Pangan Pemanis Buatan dalam Produk Pangan, penggunaan aspartam masih diperbolehkan tetapi wajib mencantumkan peringatan fenilketonuria: mengandung fenilalanin, yang ditulis dan terlihat jelas pada label makanan atau minuman atau sediaan lain yang menggunakan pemanis buatan aspartam (Anonim, 2004). Menurut PerMenKes RI No: 208/Men.Kes/PER/IV/85 tentang Pemanis Buatan, ADI (Acceptable Daily Intake) atau penggunaan aspartam yang diperbolehkan dalam 1 hari adalah 0-40 mg/kg BB (Anonim, 1985). Sejak tahun 1980, WHO dan FDA menyarankan penggunaan aspartam (dibandingkan sakarin dan siklamat) sebagai pengganti sukrosa bagi yang diet kalori (penderita diabetes), dan aspartam tidak menyebabkan kanker (Muchtaridi, 2006).
K. Desain Faktorial
Pada desain faktorial dua level dan dua faktor diperlukan empat percobaan (2n = 4, dengan 2 menunjukkan level dan n menunjukkan jumlah faktor), yaitu (1) A dan B masing-masing pada level rendah, (a) A pada level tinggi dan B pada level rendah, (b) A pada level rendah dan B pada level tinggi, (ab) A dan B masing-masing pada level tinggi.
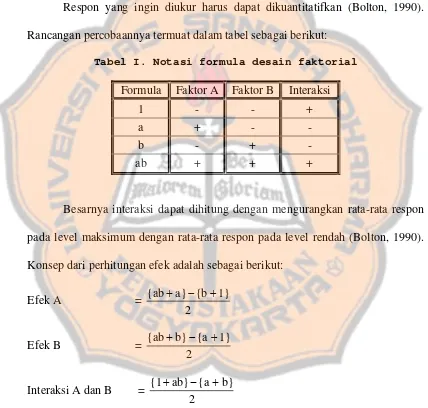
Respon yang ingin diukur harus dapat dikuantitatifkan (Bolton, 1990). Rancangan percobaannya termuat dalam tabel sebagai berikut:
Tabel I. Notasi formula desain faktorial
Formula Faktor A Faktor B Interaksi 1 - - + a + - - b - + - ab + + +
Besarnya interaksi dapat dihitung dengan mengurangkan rata-rata respon pada level maksimum dengan rata-rata respon pada level rendah (Bolton, 1990). Konsep dari perhitungan efek adalah sebagai berikut:
Efek A =
menentukan respon. Jika kurva menunjukkan garis tidak sejajar atau berpotongan, maka dapat dikatakan bahwa ada interaksi antar eksipien dalam menentukan respon.
Persamaan umum dari desain faktorial adalah sebagai berikut : Y = b0 + b1(A) + b2(B) + b12 (A)(B) Y = respon hasil atau sifat yang diamati
(A),(B) = level bagian A dan B, yang nilainya antara -1 sampai +1 b0,b1,b2,b12 = koefisien, dapat dihitung dari hail percobaan
Desain faktorial memiliki beberapa keuntungan, metode ini memiliki efisiensi yang maksimal untuk memperkirakan efek yang dominan dalam menentukan respon. Keuntungan utamanya bahwa metode ini memungkinkan untuk mengidentifikasi efek masing-masing faktor, maupun efek interaksi antar faktor. Metode ini ekonomis dalam arti mampu mengurangi jumlah penelitian jika dibandingkan dengan meneliti 2 efek faktor secara terpisah (Muth, 1999).
L. Landasan Teori
Temulawak merupakan salah satu tanaman berkhasiat yang terdapat di Indonesia. Khasiat temulawak untuk mengobati berbagai macam penyakit mengakibatkan munculnya berbagai jenis sediaan obat yang mengandung
temulawak utamanya kurkumin. Kurkumin pada temulawak berkisar antara 1,6-2,2%.
adalah lebih mudah dalam pengoperasiannya sehingga tidak membutuhkan suatu keahlian khusus, lebih murah karena tidak memerlukan peralatan yang khusus dan dapat menghemat waktu.
Bentuk granul effervescent dari temulawak memiliki beberapa keuntungan yaitu menghasilkan gas CO2 yang memberikan sensasi menyegarkan saat digunakan serta dapat menutupi rasa pahit dan pedas dari temulawak sehingga bentuk sediaan ini menjadi satu pilihan untuk meningkatkan minat konsumen. Kerugian dalam granul effervescent ialah kesulitan untuk menghasilkan produk yang stabil secara kimia karena sistem effervescent tidak stabil dengan adanya lembab. Keberadaan lembab akan menghasilkan reaksi asam dan basa yang terlalu awal sehingga terjadi reaksi effervescent prematur. Untuk mengurangi keberadaan lembab maka semua pekerjaan untuk pembuatan granul effervescent termasuk uji sifat fisik granul dilakukan di dalam ruangan dengan kelembaban relatif maksimal 25% pada suhu ruangan 25°C.
Dalam pembuatan granul effervescent ekstrak rimpang temulawak diperlukan bahan-bahan yang dapat menghasilkan reaksi effervescent. Natrium bikarbonat dan asam tartrat-asam fumarat dipilih sebagai sumber basa dan sumber asam karena diharapkan campuran antara basa dan asam ini jika bereaksi dengan adanya air akan menghasilkan gas CO2 sebagai hasil reaksi effervescent. Gas CO2 ini yang kemudian berfungsi sebagai penghancur dalam granul effervescent.
Campuran asam lebih dipilih dibandingkan dengan menggunakan asam tunggal karena pada penggunaan asam tunggal dalam sediaan effervescent akan menimbulkan kesukaran, yaitu akan menghasilkan granul yang menggumpal sehingga akan mempengaruhi kualitas granul effervescent yang dihasilkan. Asam tartrat bersifat higroskopis, mudah larut dalam air, kekuatan asamnya cukup baik. Dengan sifat asam tartrat yang sangat higroskopis akan menyulitkan dalam pembuatan granul effervescent, sehingga asam tartrat kemudian dikombinasikan dengan asam fumarat yang bersifat kurang higroskopis dibandingkan sumber asam yang lain sehingga jumlah lembab yang masuk ke dalam bahan dapat dikurangi. Untuk bagian basa dipilih natrium bikarbonat karena memiliki sifat mudah larut dalam air serta dapat menghasilkan karbon dioksida dalam jumlah besar yaitu sebanyak 52% dibandingkan dengan sumber basa yang lain.
desain faktorial dapat juga dicari eksipien yang mempunyai pengaruh dominan terhadap sifat fisik granul effervescent serta ada tidaknya interaksi antar eksipien yang mempengaruhi sifat fisik granul effervescent yaitu kecepatan alir, waktu larut, dan kandungan lembab granul.
M. Hipotesis
1. Diduga antara natrium bikarbonat dan campuran asam tartrat-asam fumarat serta interaksinya ada yang merupakan faktor dominan yang menentukan sifat fisik granul effervescent ekstrak rimpang temulawak.
BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian eksperimental murni dengan rancangan penelitian menggunakan desain faktorial.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas :
1). Level tinggi dan level rendah natrium bikarbonat yaitu: i. Level tinggi : 900 mg
ii. Level rendah : 563 mg
2). Level tinggi dan level rendah campuran asam tartrat-asam fumarat yaitu, level tinggi : 800 mg (496 mg asam tartrat dan 304 mg asam fumarat) dan level rendah : 500 mg (310 mg asam tartrat dan 190 mg asam fumarat).
b. Variabel tergantung. Sifat fisik granul yaitu: kecepatan alir, waktu larut granul, dan kandungan lembab granul.
c. Variabel pengacau terkendali. Sifat fisik ekstrak, kadar ekstrak rimpang temulawak, suhu, lama pengeringan, dan kelembaban ruangan penelitian.
2. Definisi operasional
a. Granul effervescent ekstrak rimpang temulawak adalah sediaan padat dalam bentuk granul atau serbuk kasar sampai kasar sekali dan mengandung kurkumin dalam ekstrak rimpang temulawak sebagai bahan obat dengan kombinasi sumber basa (natrium bikarbonat) dan sumber asam (asam tartrat-asam fumarat) sebagai eksipien, bila ditambah dengan air, tartrat-asam dan basanya bereaksi membebaskan CO2 sehingga menghasilkan buih.
b. Ekstrak rimpang temulawak adalah ekstrak yang diperoleh dari maserasi serbuk rimpang temulawak dalam pelarut etanol 96%, yang kemudian dipurifikasi dengan heksan dan diuapkan pada suhu 50-60o C sampai 1/9 berat serbuk kering rimpang temulawak yang digunakan.
c. Eksipien adalah bahan tambahan yang digunakan pada pembuatan granul effervescent ekstrak rimpang temulawak.
d. Komposisi sumber basa dan asam adalah banyaknya natrium bikarbonat dan
campuran asam tartrat-asam fumarat yang digunakan dalam formula granul effervescent ekstrak rimpang temulawak, dapat dinyatakan dalam level rendah
sampai level tinggi.
e. Faktor adalah besaran yang memberikan pengaruh terhadap respon (Voigt, 1994). Dalam penelitian ini digunakan dua faktor yaitu natrium bikarbonat sebagai faktor pertama dan campuran asam tartrat-asam fumarat sebagai faktor kedua.
level rendah natrium bikarbonat sebesar 563 mg dan level tinggi sebesar 900 mg. Level rendah dengan notasi untuk campuran asam tartrat-asam fumarat dinyatakan dalam jumlah bahan 500 mg dan level tinggi dengan notasi sebesar 800 mg.
g. Efek adalah perubahan respon yang disebabkan variasi level dari faktor (Bolton, 1990). Dalam penelitian ini terdapat 3 efek yaitu efek natrium bikarbonat, efek campuran asam tartrat-asam fumarat, dan efek interaksi antara natrium bikarbonat dan campuran asam tartrat-asam fumarat.
h. Interaksi adalah peristiwa berubahnya hasil pengaruh suatu faktor karena keberadaan faktor lain. Nilainya dapat ditentukan oleh perhitungan efek rata-rata atau dapat diamati dengan terjadinya perpotongan garis atau dua garis yang tidak pararel pada grafik hubungan respon-natrium bikarbonat dan grafik hubungan respon-campuran asam tartrat-asam fumarat.
i. Kecepatan alir adalah kecepatan granul effervescent dengan bobot 100 gram
untuk mengalir melewati hopper. Kandungan lembab adalah jumlah lembab yang terdapat dalam granul effervescent. Waktu larut adalah waktu yang dibutuhkan granul effervescent untuk larut atau meninggalkan residu tidak larut seminimal mungkin dalam 200 ml air dengan pengadukan ringan sebanyak 20 kali.
kecepatan alir granul lebih dari 10 gram/detik, kandungan lembab granul antara 0,4% - 0,7%, dan waktu larut granul dengan waktu kurang dari 2,5 menit (< 150 detik).
k. Contour plot : grafik yang memuat nilai respon sifat fisik granul effervescent berdasarkan pada persamaan desain faktorial.
l. Contor plot super imposed : gabungan dari masing-masing contour plot sifat
fisik granul effervescent yang digunakan untuk menentukan area komposisi optimum natrium bikarbonat dan campuran asam tartrat-asam fumarat.
C. Bahan dan Alat Penelitian 1. Bahan penelitian
Serbuk rimpang temulawak, etanol 96% (kualitas teknis), etanol 96% (kualitas pro analisis, E.Merck), aquadest, toluen (kualitas teknis), chloroform (kualitas pro analisis, E.Merck), kurkumin baku (hasil sintesis Fakultas Farmasi Universitas Gajah Mada Yogyakarta), TLC Aluminium sheets precoated silica gel 60 F254 (20x20 cm) dan tebal 0,2 mm (E.Merck), asam tartrat (kualitas farmasetis, Brataco), asam fumarat (kualitas farmasetis, Brataco), natrium bikarbonat (kualitas farmasetis, Brataco), laktosa (kualitas farmasetis, Brataco), aspartam (kualitas farmasetis, Brataco), PVP (kualitas farmasetis, Brataco).
2. Alat penelitian
Alat-alat gelas (Pyrex), neraca analitik (Metler Toledo 603002), stopwatch (Alba), termometer (Celcius), waterbath (Memmert), bejana stainless,
viscosimeter (Type Stromer), alat pengukur waktu alir granul (Modifikasi
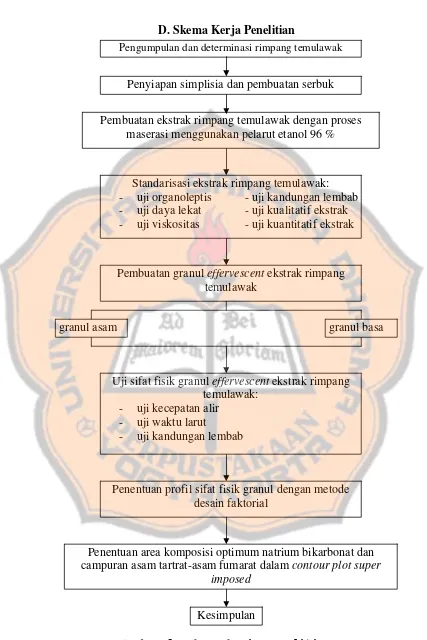
D. Skema Kerja Penelitian
Pengumpulan dan determinasi rimpang temulawak
Penyiapan simplisia dan pembuatan serbuk
Pembuatan ekstrak rimpang temulawak dengan proses maserasi menggunakan pelarut etanol 96 %
Standarisasi ekstrak rimpang temulawak: - uji organoleptis - uji kandungan lembab - uji daya lekat - uji kualitatif ekstrak - uji viskositas - uji kuantitatif ekstrak
Pembuatan granul effervescent ekstrak rimpang temulawak
granul asam granul basa
Uji sifat fisik granul effervescent ekstrak rimpang temulawak:
- uji kecepatan alir - uji waktu larut
- uji kandungan lembab
Penentuan profil sifat fisik granul dengan metode desain faktorial
Penentuan area komposisi optimum natrium bikarbonat dan campuran asam tartrat-asam fumarat dalam contour plot super
imposed
Kesimpulan
E. Tata Cara Penelitian 1. Determinasi tanaman temulawak
Determinasi dilakukan di Laboratorium Farmakognosi Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta menurut buku acuan Atlas Tumbuhan Obat Indonesia (Dalimartha, 2000) untuk memastikan bahwa tanaman yang digunakan dalam penelitian ini adalah benar Curcuma xanthorrhiza Roxb.
2. Penyiapan simplisia dan pembuatan serbuk rimpang temulawak
Rimpang temulawak (Curcuma xanthorrhiza Roxb.) berumur ± 2 tahun sebanyak 200 kg diperoleh dari Samigaluh, Kulon Progo. Rimpang dicuci dengan air mengalir untuk menghilangkan kotoran kemudian dilakukan sortasi basah untuk memisahkan rimpang temulawak dari kemungkinan adanya campuran rimpang lain atau dari bagian tanaman lain. Rimpang dikupas kulitnya lalu diiris
tipis-tipis dengan ketebalan ± 3 mm. Pengeringan dilakukan di bawah sinar
matahari dengan ditutup kain hitam, untuk menyempurnakan pengeringan maka dilakukan pengeringan dengan oven sebelum simplisia diserbuk, menggunakan suhu 50oC sampai simplisia kering ditandai dengan mudah dipatahkan atau hancur bila diremas. Setelah simplisia kering, dilakukan sortasi kering untuk memisahkan kemungkinan pengotor yang masih tertinggal dan simplisia yang rusak.
dengan kertas aluminium foil agar cahaya tidak dapat tembus, serta diberi silica gel sebagai pengawet.
3. Pembuatan ekstrak rimpang temulawak
Perbandingan pelarut dan serbuk yang digunakan adalah 1 bagian serbuk dengan 5 bagian pelarut (Voigt, 1994), menggunakan pelarut etanol 96%. Serbuk yang ditimbang sebanyak 12 kg dilarutkan dengan 60 liter pelarut, lalu dimaserasi selama 4 hari (Ansel, 1989). Setelah 4 hari maserat disaring dengan menggunakan kain penyaring tambahkan etanol pada ekstrak ad 200 ml kemudian didiamkan selama 2 hari lalu didekantasi sehingga diperoleh cairan ekstrak yang terpisah dari endapan hasil pendiaman. Ekstrak yang diperoleh selanjutnya dipurifikasi atau pemurnian ekstrak temulawak dengan metode ekstraksi pelarut menggunakan pelarut heksan. Perbandingan untuk proses purifikasi adalah 1 bagian ekstrak cair dengan 1 bagian heksan diamkan selama 10 menit untuk memaksimalkan pemisahan. Bagian ekstrak (bagian bawah pada corong pisah) diambil lalu diuapkan di atas waterbath pada suhu 50-60oC sampai 1/9 bagian berat serbuk temulawak kering (±1,33 kg), ekstrak yang diperoleh kemudian ditempatkan dalam wadah yang tertutup rapat.
4. Standarisasi ekstrak rimpang temulawak
a. Pemeriksaaan organoleptis. Pemeriksaan ini meliputi warna, bau, rasa, dan konsistensi ekstrak.
dengan gelas objek yang lain dan ditekan dengan beban seberat 1 kg selama 5 menit. Kedua objek gelas yang saling berlekatan itu dipasang pada alat uji dengan beban 80 gram. Dicatat waktu yang diperoleh sampai terpisahnya kedua objek gelas tersebut (Voigt, 1994).
c. Uji viskositas. Uji ini menggunakan viscotester. Ekstrak dimasukkan ke dalam bejana stainless steel dan dipilih rotor yang sesuai dengan konsistensi ekstrak. Rotor dipasang pada alat uji dan diatur sehingga rotor tercelup dalam ekstrak dan alat uji dihidupkan. Dicatat skala yang ditunjukkan oleh jarum sesuai nomor rotor yang dipakai (Voigt, 1994).
d. Uji kandungan lembab. Uji ini menggunakan metode gravimetri, ekstrak rimpang temulawak ditimbang seberat 10 g, dikeringkan dalam oven pada suhu 105º C selama 5 jam. Setiap 60 menit ekstrak rimpang temulawak ditimbang hingga mencapai bobot konstan yakni sampai perbedaan kadar air antara dua penimbangan berturut – turut tidak lebih dari 0,25% (Anonim, 1995).
Berikut rumus kadar air menurut Voigt (!994) :
e. Uji kualitatif ekstrak rimpang temulawak. Uji ini dilakukan dengan menimbang lebih kurang 25,0 mg ekstrak secara seksama kemudian larutkan dalam etanol sampai volume 5,0 ml, ditotolkan sebanyak 1µl pada lempeng silica gel 60 F254 kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhi fase gerak. Setelah dikembangkan segera keluarkan lempeng silica gel, dikeringkan kemudian dideteksi dengan UV 254 nm dan UV 365 nm.
Fase diam : Lempeng silica gel 60 F254
Jarak pengembangan yang digunakan adalah 6,5 cm. (Martono, 1996). Ukur nilai Rf dari sampel kemudian dibandingkan dengan nilai Rf baku.
Rf =
f. Uji kuantitatif ekstrak rimpang temulawak.
1). Pembuatan kurva baku, penetapan recovery dan koefisien variasi (CV)
Timbang kurkumin sintesis lebih kurang 25,0 mg secara seksama, larutkan dalam etanol ad 25,0 ml (larutan induk = 1,0 g/l). Buat pengenceran larutan induk dengan etanol hingga diperoleh seri larutan baku (masing-masing 4
kali) yang mengandung kurkumin 0,12; 0,14; 0,18; 0,23; dan 0,35 μg/μl dengan volume pengambilan sebanyak 1,2 ml; 1,4 ml; 1,8 ml; 2,3 ml; dan 3,5 ml ad etanol sampai 10,0 ml. Semua larutan baku harus terlindung dari cahaya. Larutan
ditotolkan sebanyak 1μl pada lempeng silica-gel 60 F254 kemudian segera dikembangkan dalam bejana kromatografi yang telah dijenuhi dengan campuran kloroform : etanol : aquadest (25:0,96:0,04). Pengembangan dilakukan setinggi 6,5 cm, segera dikeringkan dan secepatnya discanning dengan densitometer pada
sebagai kurva baku. Selanjutnya dihitung nilai perolehan kembali dan koefisien variasinya dari 3 seri larutan baku yang lain.
2). Penetapan kadar kurkumin dalam ekstrak rimpang temulawak
Timbang lebih kurang 25,0 mg ekstrak temulawak secara seksama kemudian larutkan dalam 5,0 ml etanol. Ulangi sebanyak 6 kali, lakukan pemisahan secara kromatografi lapis tipis diikuti scanning densitometri seperti pada larutan baku.
Kadar kurkumin dalam ekstrak temulawak dihitung berdasarkan kromatogram yang memiliki Rf sama dengan Rf kurkumin baku menggunakan persamaan regresi linier dari kurkumin baku. Selanjutnya dihitung kadar rata-rata dan standar deviasinya (SD) (Martono, 1996)
5. Penetapan dosis ekstrak rimpang temulawak
Khasiat yang diharapkan dalam sediaan granul effervescent ekstrak temulawak ini adalah sebagai penciutan volume kandung empedu. Dosis kurkumin sebagai penciutan volume kandung empedu untuk 1 kali minum adalah sebesar 20 mg (Lelo, Rasyid, Zain, 1998). Perhitungan dosis kurkumin berdasarkan kadar kurkumin dalam ekstrak temulawak yang ditetapkan secara KLT-Densitometri. Dosis ekstrak temulawak dihitung sebagai dosis kurkumin dalam ekstrak.
6. Penentuan level natrium bikarbonat dan campuran asam tartrat-asam fumarat
dosis 327 mg (sekali minum) dengan asam tartrat dan asam fumarat sebagai sumber asam dan natrium bikarbonat sebagai sumber basa.
Formula optimum diperoleh berdasarkan penelitian Chrystyani (2005), yang berjudul Optimasi Campuran Asam Tartrat dan Asam Fumarat sebagai Eksipien pada Pembuatan Granul Effervescent Ekstrak Rimpang Temulawak Secara Granulasi Basah Aplikasi Desain Faktorial, didapatkan perbandingan optimum untuk asam tartrat : asam fumarat = 425: 260.
Jumlah asam yang digunakan untuk pembuatan sediaan effervescent berkisar antara 25%-40% (Wehling and Fred, 2004). Asam sejumlah 25% merupakan asam level rendah dan 40% sebagai asam level tinggi.
Jumlah asam level rendah yang digunakan = 500 mg
- asam tartrat = 310 mg - asam fumarat=190 mg
Jumlah asam level tinggi yang digunakan = 800 mg
- asam tartrat = 496 mg - asam fumarat= 304 mg
Perhitungan level rendah dan level tinggi natrium bikarbonat yang digunakan berdasarkan pada jumlah asam yang digunakan melalui perhitungan secara stokiometri.
Jumlah total natrium bikarbonat level rendah= 563 mg
7. Pembuatan granul effervescent
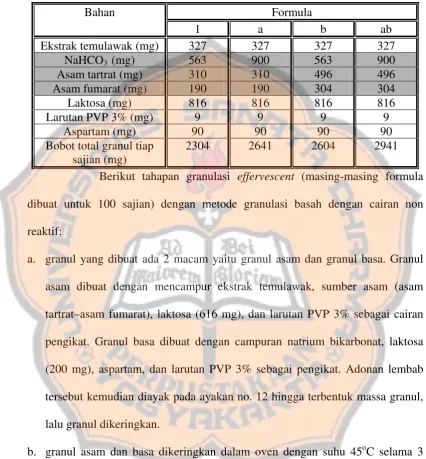
Tabel II. Formula granul effervescent
Bahan Formula
Bobot total granul tiap sajian (mg)
2304 2641 2604 2941
Berikut tahapan granulasi effervescent (masing-masing formula dibuat untuk 100 sajian) dengan metode granulasi basah dengan cairan non reaktif:
a. granul yang dibuat ada 2 macam yaitu granul asam dan granul basa. Granul
asam dibuat dengan mencampur ekstrak temulawak, sumber asam (asam tartrat–asam fumarat), laktosa (616 mg), dan larutan PVP 3% sebagai cairan pengikat. Granul basa dibuat dengan campuran natrium bikarbonat, laktosa (200 mg), aspartam, dan larutan PVP 3% sebagai pengikat. Adonan lembab tersebut kemudian diayak pada ayakan no. 12 hingga terbentuk massa granul, lalu granul dikeringkan.
b. granul asam dan basa dikeringkan dalam oven dengan suhu 45oC selama 3
8. Uji kualitas granul effervescent
a. Kecepatan alir. Granul ditimbang 100 gram kemudian dituang perlahan-lahan ke dalam corong pengukur lewat tepi corong, biarkan granul mengalir keluar. Waktu mengalirnya granul sampai granul berada di corong keluar semua dicatat dengan menggunakan stopwatch (Voigt,1994).
b. Waktu larut. Sejumlah granul (sesuai bobot tiap formula) dilarutkan ke dalam 200 ml air. Dilakukan pengadukan sebanyak 20 kali dengan bantuan stopwatch dicatat waktu yang dibutuhkan oleh granul sampai terbentuk larutan dengan residu tidak larut seminimal mungkin. Menurut Wehling and Fred (2004), syarat waktu larut granul kurang dari 2,5 menit (< 150 detik). Untuk menyempurnakan kelarutan dan mempercepat terjadinya reaksi effervescent terkadang diperlukan suatu pengadukan yang ringan (Mohrle, 1980).
9. Penentuan efek
Penentuan eksipien natrium bikarbonat dan campuran asam tartrat-asam fumarat yang dominan mempengaruhi sifat fisik granul menurut Bolton (1990) dapat dicari dengan menggunakan persamaan:
Efek faktor = rata-rata respon level tinggi – rata-rata respon level rendah 10. Penentuan profil sifat fisik granul dan area optimum
Respon untuk semua kombinasi dapat dihitung dengan persamaan: Y = b0 + b1 (A) + b2 (B) + b12 (AB)
Y = respon hasil atau sifat yang diamati
(A), (B) = level bagian A, bagian B, yang nilainya antara -1 sampai +1 b0,b1, b2, b12= koefisien, dapat dihitung dari hasil percobaan (Bolton,1990)
F. Analisis Hasil
Data yang diperoleh kemudian dianalisis secara matematis menggunakan desain factorial. Dari persamaan didapatkan contour plot dari masing-masing sifat fisik granul. Dari masing-masing contour plot disatukan menjadi contour plot super imposed dan dapat ditentukan area komposisi optimum natrium bikarbonat
BAB IV
HASIL PENELITIAN DAN PEMBAHASAN
A. Hasil Determinasi Rimpang Temulawak
Sebelum menggunakan sediaan herbal sebagai obat, harus dipastikan
bahwa tidak menggunakan bahan tanaman yang salah. Menggunakan sediaan
herbal yang salah dapat menimbulkan efek yang tidak diinginkan atau keracunan.
Oleh karena itulah perlu dilakukan determinasi terhadap tanaman yang akan
digunakan untuk membuat sediaan obat. Determinasi dilakukan di Laboratorium
Farmakognosi Fitokimia Fakultas Farmasi Universitas Sanata Dharma, dengan
cara membuat herbarium basah dari rimpang temulawak kemudian disesuaikan
dengan buku acuan “Atlas Tumbuhan Obat Indonesia” (Dalimartha, 2000). Dari
hasil determinasi dapat dipastikan bahwa tumbuhan yang digunakan dalam
penelitian ini adalah benar-benar tumbuhan temulawak (Curcuma xanthorrhiza
Roxb.).
B. Penyiapan Simplisia dan Pembuatan Serbuk Rimpang Temulawak
Rimpang temulawak (Curcuma xanthorrhiza Roxb.) berumur ± 2 tahun
diperoleh dari Samigaluh, Kulon Progo, yang diambil pada bulan Oktober 2005.
Rimpang temulawak yang digunakan sebanyak 200 kg kemudian rimpang dicuci
dengan air mengalir untuk menghilangkan tanah dan pengotor lainnya yang
masih melekat pada bahan simplisia. Selanjutnya dilakukan sortasi basah untuk
memisahkan rimpang temulawak dari kemungkinan adanya campuran rimpang
lain atau dari bagian tanaman lain.
Perajangan bahan simplisia dilakukan untuk mempermudah proses
pengeringan, pengepakan dan penggilingan. Semakin tipis bahan yang akan
dikeringkan, semakin cepat penguapan airnya sehingga mempercepat waktu
pengeringan. Akan tetapi irisan yang terlalu tipis juga dapat menyebabkan
berkurang atau hilangnya zat berkhasiat yang mudah menguap, sehingga
mempengaruhi komposisi bau dan rasa yang diinginkan. Oleh karena itu bahan
simplisia seperti temulawak dihindari perajangan yang terlalu tipis untuk
mencegah berkurangnya kadar minyak atsiri dan zat aktif lainnya.
Tujuan pengeringan ialah untuk mendapatkan simplisia yang tidak
mudah rusak, sehingga dapat disimpan dalam waktu yang lebih lama. Dengan
mengurangi kandungan lembab dan menghentikan reaksi enzimatik akan
mencegah penurunan mutu atau perusakan simplisia. Setelah simplisia kering,
dilakukan sortasi kering untuk memisahkan kemungkinan pengotor yang masih
tertinggal dan simplisia yang rusak.
Penyerbukan simplisia bertujuan untuk memperkecil ukuran partikel
rimpang temulawak. Ekstraksi akan dipermudah dengan pengecilan ukuran
partikel. Waktu yang dibutuhkan untuk ekstraksi juga dipersingkat dengan
menaikkan luas permukaan kontak antara pelarut dan zat padat karena jarak
C. Pembuatan Ekstrak Rimpang Temulawak
Serbuk rimpang temulawak yang diperoleh dimaserasi dengan
menggunakan pelarut etanol 96 % selama 4 hari. Sifat kurkumin yang kurang
polar serta larut dalam etanol mendasari penggunaan etanol 96% sebagai cairan
penyari. Diharapkan dengan menggunakan etanol 96% kurkumin dapat tersari
secara optimum. Pemilihan metode maserasi dibandingkan dengan metode
ekstraksi yang lain karena metode maserasi dapat menyari bahan dalam jumlah
besar sekaligus. Selain itu proses maserasi dapat untuk menstandarisasi ekstrak
berdasarkan pada prinsip osmolalitas atau kelarutan jenuh. Dengan demikian
diharapkan jumlah kurkumin yang tersari dapat ditentukan sehingga menjamin
reprodusibilitas ekstrak yang dihasilkan.
Ekstrak yang diperoleh didiamkan selama 2 hari dengan tujuan untuk
mengendapkan amilum yang terdapat di dalam ekstrak sehingga diperoleh ekstrak
yang lebih murni (Anonim, 2000). Amilum perlu dihilangkan karena keberadaan
amilum dalam ekstrak akan mempengaruhi waktu larut granul effervescent yang
dihasilkan. Selain itu dengan adanya amilum dalam ekstrak, maka amilum akan
terikut saat menimbang ekstrak yang akan digunakan untuk membuat granul
effervescent. Hal ini tentunya mengakibatkan dosis kurkumin yang digunakan
menjadi tidak seragam.
Untuk menghilangkan resin dan senyawa lain dalam ekstrak yang tidak
dapat dipisahkan melalui pengendapan maka dilakukan proses purifikasi dengan
menggunakan heksan dengan perbandingan 1 bagian ekstrak dipurifikasi dengan 1
menguapkan/memekatkan ekstrak cair sampai diperoleh ekstrak dengan berat 1/9
berat serbuk kering yang digunakan. Pemekatan berarti peningkatan jumlah
parsial solut (senyawa terlarut) melalui proses penguapan pelarut sampai menjadi
kondisi kering atau ekstraknya menjadi lebih kental (Anonim, 2000).
D. Hasil Standarisasi Ekstrak Rimpang Temulawak
Tabel III. Hasil uji sifat fisik ekstrak rimpang temulawak
Uji X ±SD
Daya lekat (detik) 0,34 ± 0,01
Kekentalan (d.Pas) 1,68 ± 0,06
Kandungan lembab (%) 32,88 ± 7,56
Keterangan:
X = Rata-rata dari 6 kali replikasi
SD = Standar Deviasi
1. Uji organoleptik
Konsistensi : cairan agak kental dan lengket
Bau : khas aromatis
Warna : coklat kehitaman
Rasa : pahit
2. Uji daya lekat
Uji daya lekat dilakukan untuk mengkarakterisasi sifat fisik ekstrak
rimpang temulawak agar kualitas bahan yang digunakan seragam. Standarisasi
terhadap daya lekat ekstrak kental rimpang temulawak dilakukan karena daya
lekat dapat mempengaruhi daya ikat terhadap serbuk. Kelengketan ekstrak
rimpang temulawak dalam formulasi dapat berperan sebagai bahan pengikat pada
Daya lekat ekstrak diukur menggunakan parameter waktu lekat. Waktu
lekat adalah waktu yang diperlukan untuk memisahkan 2 gelas objek yang telah
dilekatkan dengan ekstrak rimpang temulawak. Semakin besar waktu lekat maka
daya lekat semakin tinggi, dan kekentalan ekstrak semakin tinggi.
Untuk uji daya lekat berat ekstrak yang digunakan adalah 50 mg, berat
ini dibuat sama untuk tiap kali uji, dengan tujuan agar tidak terjadi variasi hasil
akibat perbedaan berat. Berdasarkan data yang diperoleh seperti yang tertera pada
tabel VI, hasil rata-rata uji daya lekat ekstrak rimpang temulawak sebesar 0,34 ±
0,01 detik, dihitung dari rata-rata yang dibutuhkan untuk melepaskan gelas objek.
3. Uji viskositas
Uji viskositas ini dilakukan untuk mengetahui kekentalan ekstrak yang
diperoleh. Alat yang digunakan adalah viscotester tipe VT-04 dengan mekanisme
kerja berdasarkan hambatan pemutaran rotor, semakin kental bahan yang diuji
hambatan putar rotornya juga semakin besar sehingga rotor yang digunakan
adalah rotor dengan nomor yang semakin besar. Pengujian viskositas ekstrak
rimpang temulawak yang dihasilkan menggunakan rotor nomor 3, berdasarkan
dari hasil uji (tabel VI) didapatkan viskositas ekstrak rimpang temulawak sebesar
1,68 ± 0,06 d.Pas.
Kekentalan ekstrak utamanya berpengaruh terhadap formulasi sediaan
granul effervescent, jika ekstrak yang digunakan terlalu kental maka akan
menyulitkan dalam penuangan ekstrak dan pada saat dicampur dengan
bahan-bahan lain saat granulasi. Jika terlalu encer maka granul yang dihasilkan akan
bahan menjadi granul, sehingga kekentalan ekstrak secara tidak langsung
berpengaruh terhadap waktu larut sediaan.
4. Uji kandungan lembab
Sediaan dari bahan alam perlu diketahui kadar airnya untuk menjaga
stabilitasnya dalam penyimpanan. Kadar air yang tinggi dalam suatu ekstrak dapat
mengaktifkan enzim-enzim dalam bahan alam sehingga bahan tersebut tidak stabil
dalam penyimpanan. Selain itu, keberadaan air didalam ekstrak yang terlalu tinggi
dapat menjadi media pertumbuhan yang baik bagi jamur, bakteri, dan
mikroorganisme lainnya. Salah satu cara untuk menjaga stabilitas bahan alam
adalah dengan cara menghilangkan air atau pelarut sampai kandungan lembab
tertentu melalui proses pemanasan menggunakan suhu di atas 60ºC. Suhu ini
mampu merusak enzim dalam bahan alam secara irreversible, sehingga mampu
menjamin stabilitasnya (Voigt, 1994).
Pengujian kandungan lembab disini bertujuan untuk menstandarisasi
ekstrak rimpang temulawak yang digunakan. Uji kandungan lembab ekstrak
rimpang temulawak dilakukan dengan cara menimbang berak ekstrak rimpang
temulawak sebelum dan sesudah pemanasan 105oC sampai perbedaan bobot dua
kali penimbangan tidak lebih dari 0,25% (Anonim, 1995). Tetapi pada ekstrak
rimpang temulawak yang dihasilkan tidak dapat mencapai bobot konstan dan
perbedaan bobot dua kali penimbangan berturut-turut tidak bisa mencapai 0,25%.
Hal ini disebabkan karena pengaruh pemanasan yang terlalu tinggi mengakibatkan
bahan organik terutama yang mengandung rantai karbon akan terurai menjadi