BAB II
TINJAUAN PUSTAKA
II.1. NEUROPATI DIABETIKA II.1.1. Diabetes Melitus
Diabetes melitus (DM) merupakan penyakit metabolik yang
mempunyai karakteristik ketidakseimbangan metabolisme karbohidrat,
protein dan lemak. Gambaran utamanya adalah peningkatan kadar glukosa
darah (hiperglikemia) yang disebabkan oleh kelainan sekresi insulin, kerja
insulin atau keduanya (PERKENI, 2011)
Hiperglikemia yang menetap dapat mempengaruhi hampir seluruh
jaringan di tubuh dan berhubungan dengan komplikasi berbagai sistem
organ, termasuk mata, saraf, ginjal, dan pembuluh darah. ((Brownlee et al., 2008; Unnikrishnan, et al., 2007)
Prevalensi DM terus meningkat, di Amerika Serikat dari 33 % pada
tahun 1990 menjadi 4.9 % - 6.5 % pada tahun 1998, walaupun peningkatan
ini hasil observasi pada semua umur. Namun pada laporan terakhir
dinyatakan DM dialami sekitar 180 juta penduduk pada tahun 2008, dan
diperkirakan mencapai 360 juta penduduk pada tahun 2030. Diperkirakan 5
-10 % merupakan tipe 1 (yang tergantung insulin) dan 90 % - 95 %
merupakan tipe 2 (tidak tergantung insulin). (Harati, 2002, McGuire KD,
2012 )
Berdasarkan data Badan Pusat Statistik Indonesia pada tahun 2003
Menurut hasil Riset Kesehatan Dasar (Riskesdas) tahun 2007, diabetes di
Indonesia menempati urutan keenam penyakit penyebab kematian (5,8%)
setelah stroke, tuberkulosis, hipertensi, cedera dan perinatal. Diabetes
sebagai penyebab kematian pada kelompok usia 45-54 tahun di daerah
perkotaan menduduki peringkat ke-dua yaitu 14,7%. Dan daerah pedesaan,
diabetes menduduki peringkat ke-enam yaitu 5,8% (PERKENI, 2011)
Klasifikasi DM dibagi berdasarkan etiologinya. Klasifikasi yang di
pakai di Indonesia sesuai dengan klasifikasi menurut American Diabetes Association ( ADA ) 2003 terbagi dalam empat kategori. ( Soegondo, 2004 )
Tabel 1. Klasifikasi Diabetes Melitus
Dikutip dari : Soegondo S. Diagnosis dan klasifikasi diabetes melitus terkini dalam : Sidartawan Soegondo, dkk ( ed ). Penatalaksanaan
II.1.2. Neuropati Diabetika II.1.2.1. Defenisi
Defenisi neuropati diabetika adalah adanya gejala dan / atau tanda
dari disfungsi saraf perifer dari penderita diabetes tanpa ada penyebab lain
selain diabetes. ( Sjahrir, 2006 ; Boulton dkk, 2005 )
II.1.2.2. Epidemiologi
Prevalensi diabetes melitus terus meningkat di Amerika Serikat pada
tahun 1990 sebesar 4 %, meningkat 33 % menjadi 6.5 % pada tahun 1998,
walaupun peningkatan ini hanya berdasarkan observasi pada semua umur,
etnik, jenis kelamin dan tingkat pendidikan. Dan ditemukan angka yang
cukup signifikan yang menunjukkan DM positif pada usia 30 - 39
tahun.(Harati, 2002 )
Neuropati diabetika terjadi hampir 50 % pada pasien DM, dan pada
DM tipe 1 dijumpai lebih cepat sedangkan pada tipe 2 dijumpai lebih lambat.
Neuropati sensorimotor kronik merupakan bentuk yang paling sering dari
polineuropati diabetik dan paling sering didiagnosa pada diabetes tipe 2
sampai 10 %. ( Aring, 2005 ; Boulton, 2005 ).
Laporan dari hasil penelitian di berbagai daerah di Indonesia yang
dilakukan pada dekade 1980 – an menujukkan sebaran prevalensi DM 0.8 %
- 6.1 %. Sedangkan pada rentang tahun 1980 – 2000, menunjukkan
peningkatan prevalensi yang sangat tajam yaitu dari 1.7 % menjadi 5.7 %
penelitian juga ditemukan neuropati diabetika dijumpai pada 50 % pasien
DM. ( Kelompok studi nyeri PERDOSSI, 2011 )
Diperkirakan dari studi epidemiologi prevalensi neuropati pada pasien
DM kira – kira 30 % pada pasien rumah sakit dan 20 % pada pasien di
masyarakat. Di Inggris pada United Kingdom Prospective Diabetes Study (UKPDS), insiden setiap tahun kira – kira 2 % dan pada Diabetes Control and Complication Trial (DCCT), mendapatkan 7 % paien yang didiagnosis dengan DM mengalami neuropati, dan insiden mendekati 50 % pada pasien
yang menderita DM + 25 tahun. (Duby, 2004 )
II.1.2.3. Faktor Resiko
Faktor resiko terjadinya neuropati diabetika adalah : ( Duby, 2004 )
a. Hiperglikemi
b. Lamanya menderita DM
c. Umur
d. Merokok
e. Konsumsi alkohol
f. Hipertensi
g. Hipokolestrolemia
II.1.2.4. Klassifikasi Dan Stadium
Ada beberapa klasifikasi dan stadium dari neuroapti diabetika yaitu
dan American Academy of Neurology ( AAN ). Ada juga yang menurut international Experts In Diabetic Neuropathy. ( Eastman R, Boulton, 2004 )
Pada literatur juga disebutkan stadium beratnya neuropati diabetika
dibuat berdasarkan kecepatan hantaran saraf, quantitative sensory testing (QST ), atau abnormalitas tes otonom. Selain daripada stadium, klinis dari
neuropati diabetika juga dibedakan berdasarkan skala neurologis. ( Boulton,
2004 )
Tabel 2. Klasifikasi Neuropati Diabetika
Tabel 3. Stadium neuropati diabetika
Dikutip dari : Boulton , et al . Diabetic Somatic Neuropathies. Diabetes Care. 2004 : 27 ; 1458 – 1486.
Tabel 4. Stadium beratnya Neuropati Diabetika
II.1.2.5. Patogenesa
Akhir – akhir ini sejumlah patogenesa dibuat untuk melengkapi satu
dengan yang lainnya guna mencapai target pengobatan. Berdasarkan
literatur menunjukan adanya multifaktor yang mendasari patogenesa
neuropati diabetika. ( Duby, 2004 )
Ada tujuh mekanisme yang berpengaruh pada patogenesa neuropati
diabetika yaitu : (i) peningkatan perubahan yang terus menerus jalur poliol
yang didahului oleh penumpukan sorbitol dan fruktosa, pengurangan myio –
inositol dan penurunan aktifitas Na+-K+-ATP-ase, (ii) gangguan metabolisme
asam lemak essensial n – 6 dan prostaglandin yang mengakibatkan
perubahan struktur membran saraf, mikrovaskular dan abnormal hematologi,
(iii) defisit mikrovaskular endoneural mengakibatkan iskemik dan hipoksia
sehingga terjadi oksidatif stress yang disebut dengan hyperglycemic pseudohypoxia, (iv) peningkatan aktivitas protein kinase C β ( PKC β ), (v) penurunan neurotropin yang didahului oleh penurunan ekspresi dan deplesi
Nerve Growth Factor ( NGF ), (vi) penumpukan AGEs pada saraf dan vassa, (vii) proses imunologi yang menyebabkan proses inflamasi. ( Ziegler, 2004 )
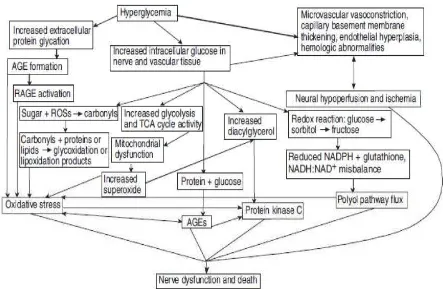
Proses terjadinya neuropati diabetika berawal dari hiperglikemia
berkepanjangan yang mengakibatkan terjadinya peningkatan aktivitas jalur
poliol, sintesis advance glycosilation end products ( AGEs ), pembentukan radikal bebas dan aktivitas protein kinase. Aktivitas berbagai jalur tersebut
berujung pada kurangnya vasodilatasi, sehingga aliran darah ke saraf
menurun dan bersama rendahnya mioinositol dalam sel sehingga terjadilah
Gambar 1. Patogenesa Neuropati Diabetika
Dikutip dari : Duby, et all. Diabetic neuropaty : an intensive review, Am J Health – syst Pharm . 2004 : 61 (12 ); 160 -176
II.1.2.6. Gejala Klinis
Gejala klinis tergantung pada tipe neuropati dan saraf mana yang
terlibat. Pada beberapa orang bisa tidak ditemui gejala. Kesemutan, tingling atau nyeri pada kaki, seringkali merupakan gejala yang utama, bisa juga
nyeri dan kesemutan. Gejala bisa melibatkan sistem saraf sensoris atau
Tabel 5. Gejala khas pada neuropati diabetika
Dikutip dari : Boulton , et al . Diabetic Somatic Neuropathies.
Diabetes Care. 2004 : 27 ; 1458 – 1486.
Berdasarkan waktu, gejala klinis dapat dibagi atas 2 yaitu :
Neuropati sensoris akut
Banyak gejala neuropati sensoris akut dan kronik sama. Perbedaan
yang jelas pada onset, tanda yang menyertai dan prognosis. Pemeriksaan
fisik neuropati sensoris akut relatif normal, dan pada pemeriksaan sensoris
bisa ditemukan alodinia, motorik relatif normal, walaupun terkadang bisa
dijumpai penurunan refleks. ( Aring, 2005 )
Neuropati sensoris kronis
Oleh karena neuropati kronik tergantung pada proses yang panjang,
gejala sensoris paling menonjol adalah pada ektremitas bawah, walaupun
proprioseptik dan kemungkinan abnormal fungsi sensoris otot. ( Boulton,
2005 )
Tabel 6. Gejala Neuropati Diabetika ____________________________________
Symptoms of Diabetic Neuropathy
Sensorimotor neuropathy
Muscular symptoms: muscle weakness (not fatigue), atrophy, balance problems, ataxic gait
Sensory symptoms: pain, paresthesia, numbness, paralysis, cramping, nighttime falls, antalgic gait
Autonomic neuropathy
Cardiovascular symptoms: exercise intolerance, fatigue, sustained heart rate, syncope, dizziness, lightheadedness, balance problems
Gastrointestinal symptoms: dysphagia, bloating, nausea and vomiting, diarrhea, constipation, loss of bowel control
Genitourinary symptoms: loss of bladder control, urinary tract infection, urinary frequency or dribbling, erectile dysfunction, loss of libido, dyspareunia, vaginal dryness, anorgasmia
Sudomotor (sweat glands) symptoms: pruritus, dry skin, limb hair loss, calluses, reddened areas
Endocrine symptoms: hypoglycemic unawareness
Other symptoms: difficulty driving at night, depression, anxiety, sleep disorders, cognitive changes
________________________________________________________ Dikutip dari : Aring, et all. Evaluation an Prevention of Diabetic
Tabel 7. Perbedaan Neuropati Sensoris Akut dan Kronis
Dikutip dari : Boulton , et al . Diabetic Somatic Neuropathies. Diabetes Care. 2004 : 27 ; 1458 – 1486.
II.1.2.7. Diagnosa
a. Anamnesis : ( Kelompok Studi Nyeri PERDOSSI, 2011 )
1. Sensorik : rasa terbakar, ditusuk, ditikam, kesetrum, disobek,
tegang, diikat, alodinia, hiperalgesia, disestasia dapat disertai rasa
baal seperti pakai sarung tangan, hilang keseimbangan, kurang
tangkas, asterogenesis, maupun borok tanpa nyeri. Dan keluhan
akan memberat malam hari.
2. Motorik : Gangguan koordinasi serta paresis distal atau proksimal
antara lain sulit naik tangga, sulit bangkit dari kursi/lantai, terjatuh,
sulit bekerja atau mengangkat lengan ke atas, ibu jari tertekuk,
tersandung, kedua kaki bertabrakan.
3. Otonom : Gangguan berkeringat, sensasi melayang pada posisi
orgasme, sulit menahan BAB/BAK, ngompol, polakisuri, muntah,
diare, konstipasi dan gangguan pupil berupa sulit adaptasi dalam
gelap dan terang.
4. Neuropati diabetika dicurigai pada pasien DM tipe 1 yang lebih dari 5
tahun dan semua DM tipe 2.
b. Pemeriksaan fisik ( Kelompok Studi Nyeri PERDOSSI, 2011 )
Pada inspeksi bisa dijumpai kaki diabetik, neuroartropati dan deformitas
claw toe.
c. Pemeriksaan neurologi ( Kelompok Studi Nyeri PERDOSSI, 2011 }
Pemeriksaan motorik
Pemeriksaan sensorik untuk melihat distribusi lesi saraf.
Pemeriksaan otonom termasuk termasuk evaluasi hipotensi
ortostatik, nadi, tes valsava dan kelenjar keringat.
d. Pemeriksaan penunjang ( Kelompok Studi Nyeri PERDOSSI, 2011 )
Elektroneuromiografi
Test sensoris kuantitatif
e. Laboratorium ( Kelompok Studi Nyeri PERDOSSI, 2011 )
Kadar gula darah atau tes toleransi glukosa, HBA1c.
Laboratorium untuk menyingkirkan diagnosa banding.
Berikut adalah kriteria diagnostik neuropati, di mana diagnostik neuropati
berdasarkan adanya gejala dua atau lebih dari empat kriteria di bawah ini : (Sjahrir,
2006 )
1. Kehadiran satu atau lebih gejala.
2. Ketidakhadiran dua atau lebih reflek ankle.
4. Fungsi otonomik abnormal ( berkurangnya heart rate variability ( HRV ),
postural hypotension dengan turunnya tekanan darah sistolik 20 mmhg
atau lebih, atau kedua – duanya.
Untuk menegakkan diagnosa neuropati diabetika, sekurang –
kurangnya ada dua abnormlitas dari lima pemeriksaan yaitu : gejala, tanda
klinis, elektrofisiologis ( kecepatan hantaran saraf ), quantitative sensory testing ( QST ), dan quantitative autonomic testing ( QAT ). ( Bril, 1999 )
Selain itu juga, penegakkan neuropati diabetika dapat ditegakkan
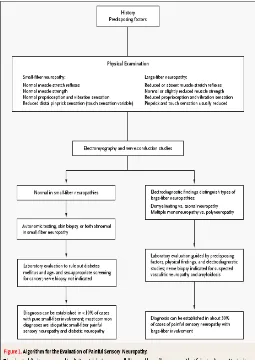
berdasarkan konsensus San Antonio. Pada konsensus tersebut telah direkomendasikan bahwa harus ada 1 dari 5 kriteria yakni : (1) Symptom scoring, (2) Physical examination scoring, (3) Quantitative Sensory Testing, (4) Cardiovascular Autonomic Function Testing (c AFT ), (5) Electrodiagnostic studies ( EDS ). ( Mendel, 2003 )
Pemeriksaan symptom scoring dan physical examination scoring yang telah terbukti memiliki sensitifitas dan spesifisitas tinggi untuk mendiagnosa
neuropati diabetika adalah Diabetic Neuropathy Symptom ( DNS ) dan Diabetic Neuropathy Examination ( DNE ). ( Jan – Willem, 2000 )
DIABETIC NEUROPATHY SYMPTOM ( DNS )
Diabetic Neuropathy Symptom ( DNS ) terdiri dari empat item yang telah divalidasi, dengan angka prediktif yang tinggi untuk skrining
polineuropati pada diabetes. Adanya satu gejala diberi nilai satu poin dengan
nilai maksimum adalah 4 poin, dan jika ada skor yang lebih besar atau sama
Diabetic Neuropathy Symptom ( DNS ) memenuhi kriteria validasi, predictive value, dan practicality untuk tes diagnostik. Skor Diabetic Neuropathy Symptom ( DNS ) cepat dan mudah untuk dilakukan dengan reproducibility yang tinggi. Diabetic Neuropathy Symptom ( DNS ), memiliki spesifisitas 79 % dan sensitivittas 78 %, dengan cut - off point of 0 vs 1 - 4 untuk evaluasi neuropati.(Meijer, 2002)
Asad dkk pada tahun 2010, dalam uji reabilitas, untuk penilaian
neuropati sensorimotor pada pasien tipe 2 mendapatkan skor DNS memiliki
sensitifitas 64.41 % dan spesifisitas 80.95 % , dan menyimpulkan bahwa
DNS adalah paling spesifik pada penilaian neuropati diabetika.(Asad, 2010 )
Dikutip dari : Mendel JR, Sahenk Z. Painful S ensory Neuropathy. N Engl J Med. 2003: 384 ; 1243 -1255
II.1.2.8. Penatalaksanaan
Langkah penatalaksanaan terhadap pasien ND adalah menghentikan
dan memperlambat progresivitas rusaknya serabut saraf dengan kontrol
kadar gula secara baik. Mempertahankan kontrol glukosa darah ketat
mendekati normoglikemi dan kadar HbA1c dibawah 7 %. ( Sjahrir, 2006,
Kelompok Studi PERDOSSI, 2011 )
Pendekatan bisa dilakukan dengan farmakologis dan non
farmakologis. Secara farmakologis dapat diberikan anti konvulsan, NSAID,
analgetik, anti depresan, anti aritmik, dan obat tipikal. Sedangkan terapi
non farmakologis adalah edukasi pasien, dan tindakan bedah. ( Kelompok
Studi Nyeri PERDOSSI, 2011 )
II.2. Disfungsi Otonom
Disfungsi otonom adalah suatu keadaan di mana terjadi kerusakan
pada saraf otonom/ Autonomic Nervus System ( ANS ) yang bisa disebabkan oleh penyakit sistemik. Sistem saraf berfungsi untuk mengontrol sejumlah
fungsi dalam tubuh seperti detak jantung, tekanan darah, saluran
pencernaan dan berkeringat dan lain sebagainya. ( Vinik, 2001)
Sistem saraf otonom berhubungan dengan pengaturan otot jantung,
otot polos pada viseral, dan kelenjar. Sistem saraf otonom membantu
Sistem saraf otonom terdiri dari jaras aferen, eferen dan kumpulan sel saraf
pada otak dan medula spinalis yang mengatur fungsi sistem. Secara
anatomis, sistem saraf otonom dibagi menjadi dua bagian dimana sebagian
besar aktivitas keduanya bekerja secara berlawanan yaitu sistem saraf
simpatis (torakolumbal) dan parasimpatis (kraniosakral). Sistem saraf
otonom juga berhubungan dengan saraf somatik; sebaliknya, kejadian
somatik dapat mempengaruhi fungsi organ otonom. ( Burgos, 2006 )
Pada susunan saraf pusat terdapat beberapa pusat saraf otonom,
seperti medula oblongata terdapat pengatur pernafasan dan tekanan darah.
Hipotalamus dianggap sebagai pusat susunan saraf otonom. Walaupun
demikian masih ada pusat yang lebih tinggi yang dapat mempengaruhinya
yaitu korpus striatum dan korteks serebrum yang dianggap sebagai
Gambar 3. Autonomic Nervus System
Dikutip dari : Burgos AO. Autonomic Function Test. Clinical Application and Examples. Internal Medicine. 2006
II.2.1. Diabetic Autonomic Neuropathy ( DAN ) / Disfungsi Otonom Pada Neuropati Diabetika
II.2.1.1. Defenisi
Diabetic Autonomic Neuropathy (DAN) adalah salah satu komplikasi dari diabetes melitus. Gangguan metabolik pada DM menyebabkan
kerusakan yang luas pada saraf perifer dan saraf otonom. Ketika neuropati
diabetika mempengaruhi saraf otonom, akan menyebabkan kerusakan pada
kardiovaskular, gastrointestinal, urogenital, neurovaskular dan fungsi
Adanya Diabetic Autonomic Neuropathy (DAN) menunjukkan keadaan morbiditas dan cenderung ke arah mortalitas dalam beberapa pasien dengan
diabetes. Manifestasi klinis yang utama adalah resting tachycardia, ortostatik hipertensi, konstipasi, gastroparesis, disfungsi ereksi, disfungsi ereksi,
disfungsi sudomotor, gangguan fungsi neurovaskular, brittle diabetes, dan hypoglycemic autonomic. ( Sjahrir, 2006 )
II.2.1.2. Epidemiologi
Dilaporkan bahwa prevalensi disfungsi otonom pada neuropati
diabetika adalah antara 7.7 – 90 %, dan lebih sering terjadi disfungsi pada
gastrointestinal dan disfungsi ereksi. ( Vinik, 2001 )
II.2.1.3. Anatomi
Sistem saraf otonom adalah bagian dari sistem saraf perifer yang
sebagian besar bertindak independen dari kontrol sadar (sengaja) dan terdiri
dari saraf di otot jantung, otot polos, eksokrin dan kelenjar endokrin. Sistem
saraf otonom bertanggung jawab untuk fungsi-fungsi pemeliharaan
(metabolisme, aktivitas kardiovaskular, pengaturan suhu, pencernaan) yang
memiliki reputasi untuk menjadi di luar kendali sadar. Pembagian utama lain
dari sistem saraf perifer, sistem saraf somatik, terdiri dari tengkorak dan
saraf tulang belakang yang menginervasi jaringan otot rangka dan lebih di
bawah kontrol sengaja. (Anissimov 2006 )
Sistem saraf otonom biasanya dibagi menjadi dua sub sistem utama,
mengimbangi, menawarkan kerja berlawanan dan tetapi efek saling
melengkapi. Sistem simpatis penawaran saraf dengan respon terhadap stres
dan bahaya, melepaskan epinephrines (adrenalin), dan meningkatnya
aktivitas umum dan tingkat metabolisme. Kebalikan sistem saraf
parasimpatis ini, merupakan pusat selama istirahat, tidur, dan mencerna
makanan, secara umum, menurunkan tingkat metabolisme, memperlambat
aktivitas, dan mengembalikan tekanan darah dan detak jantung istirahat, dan
sebagainya. Sebuah subsistem ketiga, sistem saraf enterik, diklasifikasikan
sebagai sebuah divisi dari sistem saraf otonom juga. Subsistem ini memiliki
saraf di sekitar usus, pankreas, dan kandung empedu. (Chamberlain,
2005).
Sistem saraf vertebrata dibagi ke dalam sistem saraf pusat (SSP),
yang terdiri dari otak dan sumsum tulang belakang, dan sistem saraf perifer
(PNS), yang terdiri dari semua saraf dan neuron yang berada atau
perpnajangan di luar sistem saraf pusat, seperti untuk melayani anggota
tubuh dan organ. Sistem saraf perifer, pada gilirannya, biasanya dibagi
menjadi dua sub sistem, sistem saraf somatik dan sistem saraf otonom.
Sistem saraf somatik atau sistem saraf sensorik-somatik melibatkan saraf di
bawah kulit dan berfungsi sebagai koneksi sensorik antara lingkungan luar
dan SSP. Saraf ini berada di bawah kendali kesadaran, namun sebagian
besar memiliki komponen otomatis, seperti yang terlihat dalam kenyataan
bahwa mereka berfungsi bahkan dalam kasus koma (Anissimov 2007).
Sistem saraf otonom biasanya disajikan sebagai yang bagian dari
sengaja dan sadar (refleks), dan untuk memasok otot jantung, kelenjar
endokrin, kelenjar eksokrin, dan otot polos Sebaliknya, sistem saraf somatik
memasok jaringan otot rangka, bukan jaringan halus, jantung, atau kelenjar
(Chamberlin, 2005) .
Sistem saraf otonom dibagi ke dalam sistem saraf simpatik, sistem
saraf parasimpatis, dan sistem saraf enterik. Secara umum, sistem saraf
simpatik meningkatkan aktivitas dan tingkat metabolisme (“respon melawan
atau lari”), sedangkan parasimpatis memperlambat aktivitas dan tingkat
metabolisme, mengembalikan fungsi tubuh ke tingkat normal (“beristirahat
dan keadaan mencerna”) setelah tinggi kegiatan dari stimulasi simpatis
(Chamberlin, 2005)
Sistem saraf enterik melayani daerah sekitar usus, pankreas, dan
kandung empedu, berurusan dengan pencernaan, dan sebagainya. Berbeda
dengan sistem saraf somatik, yang selalu berhubungan dengan jaringan
otot, sistem saraf otonom dapat merangsang atau menghambat jaringan
diinervasi (Chamberlin 2005).
Jaringan yang paling terkait dan organ memiliki saraf dari kedua
simpatik dan sistem saraf parasimpatik. Kedua sistem dapat merangsang
organ target dan jaringan dengan cara yang berlawanan, seperti stimulasi
simpatis meningkatkan denyut jantung dan parasimpatis untuk menurunkan
detak jantung, atau stimulasi simpatis mengakibatkan pelebaran pupil, dan
parasimpatis dalam konstriksi atau penyempitan pupil . (Chamberlin, 2005).
Disfungsi otonom dapat disebabkan berbagai hal, seperti gangguan
auto imun, penyakit sistemik, proses infeksi, toksisitas, drug induced, herediter, gangguan nutrisi dan lain sebagainya seperti tercantum pada
tabel 8. Diabetes melitus adalah penyebab tersering terjadinya disfungsi
otonom. ( Chowdhury D, 2006 )
Tabel 8. Etiologi Neuropati Otonom
Dikutip dari : Chowdhury D. Approach to a Case of Autonomic Peripheral Neuropathy. Japi. 2006 : 54
II.2.1.5. Patofisiologi
Pada penderita diabetes melitus, terjadi metabolisme yang komplek,
di mana gangguan pada pembuluh darah dan faktor hormonal yang
perbaikannya. Dan hal ini juga mempengaruhi serat sensorik dan otonom
bagian distal, sehingga menyebabkan hilangnya sensasi secara progresif.
Diabetes dapat menyebabkan disfungsi dari salah satu atau semua bagian
dari sistem saraf otonom dan menyebabkan berbagai gangguan seperti pada
kardiovaskular, gastrointestinal, urogenital, neurovaskular dan fungsi
metabolisme seperti autoregulasi glukosa. ( Vinik, 2001 )
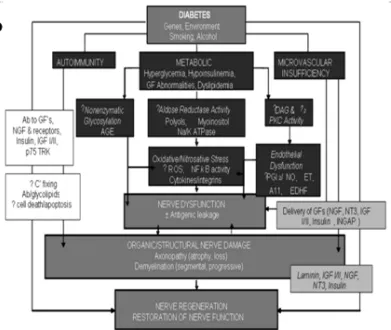
Gambar 4. Patofisiologi Diabetic Autonomic Neuropathy
Dikutip dari : Monica MD, Diabetes Autonomic Neuropathy. IHC SAINT GEORGE UT. 2011
II.2.1.6. Gambaran klinis
Gambaran klinis utama dari disfungsi otonom adalah adanya
perubahan pada diameter pupil, terjadinya hipoglikemic yang episodik
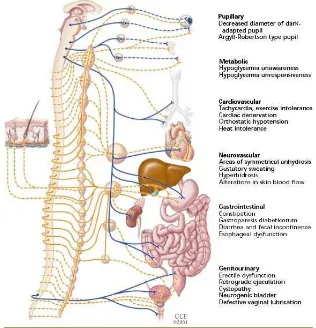
tachycardia, cardiac denervation syndrome; gejala gastrointestinal , seperti dysphagia, nyeri abdominal , nausea, muntah , malabsorbsi, fecal incontinence, diare, konstipasi, gejala neurological seperti symmetrical anhydrotic areas, hyperhidrosis; genito-urinary signs: erectile dysfunction, retrograde ejaculation, neurogenic bladder. ( Laura P, Vinik, 2001 )
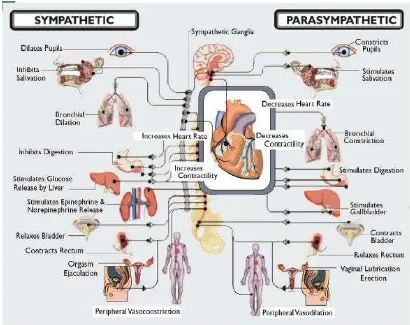
Gambar 5. Manifestasi klinis dari autonomic neuropathy (Sympathetic fibers ditunjukkan dengan orange, parasympathetic ditunjukkan dengan warna biru, preganglionic solid, dan postganglionic ditunjukkan
dengan garis terputus -putus ).
Dikutip dari : Vinik.A. Recognizing and treating diabetic autonomic neuropathy. Cleveland Clinic Journal Of Medicine. .2001 ; 68 II.2.1.7. Diagnosa
Pemeriksaan kulit, selaput lendir, kuku dan pemeriksaan sendi dapat
menunjukkan adanya disfungsi ototnom. Pada pemeriksaan dini, dapat memberi
untuk penyakit kusta, dan adanya angiokeratoma pada tungkai dapat dicurigai
sebagai fabry disease. Terjadinya arthritis dan ruam dapat menunjukkan adanya
gangguan jaringan ikat. ( Chowdhury, 2006 )
Evaluasi neurologi dengan penekanan khusus pada sistem motorik
dan sensoris penting untuk mendeteksi adanya neuropati perifer somatik.
Adanya gejala piramidal, ekstrapiramidal dan serebelum, dapat
mengindikasikan adanya gangguan neurologis pada sistem saraf otonom,
seperti multipel sklerosis. (Chowdhury, 2006 )
Pemeriksaan non invasif, dengan validasi yang baik, tes klinis fungsi
otonom sangat berguna untuk mendiagnosa adanya disfungsi otonom.
(Chowdhury, 2006). Selain itu juga dapat digunakan kuesioner dalam
menilai ada/tidaknya dan berat – ringannya disfungsi otonom seperti
penggunaan Composite Autonomic Symptoms Scale (COMPASS) dan Survey Autonomic Symptoms (SAS). Di mana dinyatakan COMPASS memiliki nilai p < 0.0001 dan SAS memiliki sensitifitas 95 % , spesifisitas 50
%. ( Zilliox, 2011 ; Carla, 2009)
II.2.1.8. Penatalaksanaan
Penatalaksanaan disfungsi otonom pada penderita neuropati diabetika
bertujuan untuk mengobati penyebab spesifik dari otonom neuropati (jika
mungkin ) dan untuk mengontrol gejala neuropati otonom. Kontrol yang
memadai dari kadar glukosa sangat penting dalam neuropati diabetes.
Steroid dan imunoglobulin intravena dapat membantu dalam
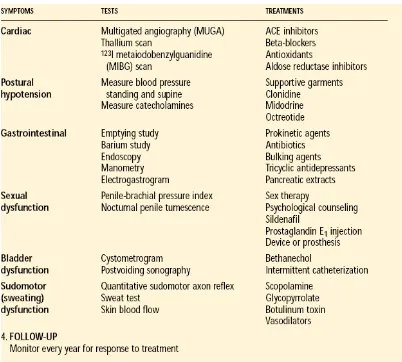
Tabel 9. Penatalaksanaan Neuropati Otonom
Dikutip dari : Vinik. Recognizing and treating diabetic autonomic neuropathy. Cleveland Clinic Journal Of Medicine. 2001 ; 929
II.2.2. Pendekatan Diagnosa Klinis dengan Scoring System
II.2.2.1. Composite Autonomic Symptoms Scale ( COMPASS )
Composite Autonomic Symptoms Scale ( COMPASS ) adalah suatu skor yang memiliki validasi yang cukup baik dalam menilai adanya gangguan
terdiri dari 73 pertanyaan yang menunjukkan simtom dari kelainan fungsi
otonom yaitu : orthostatic (9 items), sudomotor simptoms ( 8 items ), male sexual dysfunction (8 items), urinary (3 items), gastrointestinal temasuk termasuk gastroparesis, diare dan konstipasi (13 items), pupillomotor temasuk gangguan visual (7 items), vasomotor (6 items), refleks sinkop (11 items) dan gangguan tidur (8 items ). (Slettten, 2012 ; Zilliox, 2011 )
II.2.2.2. Survey Autonomic Symptom ( SAS )
Survey Autonomic Symptoms ( SAS ) merupakan suatu skor yang berisi pertanyaan yang dirancang untuk menyediakan sebuah evaluasi yang
singkat tapi jelas tentang gejala otonom pada penderita neuropati.
Pertanyaan diarahkan atau ditujukan untuk mengevaluasi gejala awal dari
disfungsi otonom. Survey tentang gejala otonom digunakan untuk menilai
ada/tidaknya gejala disertai dengan derajat keparahan. Skala ini bermaksud
untuk menegaskan : ( Zilliox, 2011 )
1. Adanya gejala awal disfungsi otonom pada awal neuropati diabetes.
2. Adanya kepastian bahwa penderita dapat memahami dengan jelas
tentang pertanyaan yang diberikan.
3. Skor ini mudah digunakan pada clinical practice.
Skor ini berisi 11 pertanyaan untuk wanita dan 12 untuk pria, di mana
terdiri atas pertanyaan tentang ortostatik, simtom sudomotor, vasomotor,
II.3. Kerangka Teori
DIABETES MELITUS
7 mekanisme pd patogenesa ND :(i) peningkatan terus menerus jalur poliol (ii) gangguan metabolisme asam lemak essensial n – 6 dan prostaglandin, (iii) hyperglycemic pseudohypoxia, (iv) peningkatan aktivitas protein DM dikaitkan dgn banyak sindrom
II.4. Kerangka Konsepsional faktor hormonal yg kemungkinan menggeser keseimbangan antara kerusakan serabut saraf dan perbaikannya. Hal ini juga mempengaruhi serat sensorik dan otonom bagian distal, sehingga menyebabkan hilangnya sensasi secara progresif. ( Vinik, 2001 )