PENINGKATAN KAPASITAS ADSORPSI BATU BARA MUDA MELALUI
PENGAYAAN KADAR OKSIGEN DENGAN MENGGUNAKAN
HIDROGEN PEROKSIDA
SKRIPSI
Diajukan untuk memenuhi sebagian dari syarat memperoleh Gelar Sarjana Sains di Bidang Kimia
IMAS NOVIYANA
0801359
PROGRAM STUDI KIMIA
JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS PENDIDIKAN INDONESIA
PENINGKATAN KAPASITAS ADSORPSI BATU
BARA MUDA MELALUI PENGAYAAN KADAR
OKSIGEN DENGAN MENGGUNAKAN
HIDROGEN PEROKSIDA
Oleh Imas Noviyana
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat memperoleh gelar Sarjana Sains pada Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Imas Noviyana 2013 Universitas Pendidikan Indonesia
Februari 2013
Hak Cipta dilindungi undang-undang.
LEMBAR PENGESAHAN
PENINGKATAN KAPASITAS ADSORPSI BATU BARA MUDA MELALUI
PENGAYAAN KADAR OKSIGEN DENGAN MENGGUNAKAN HIDROGEN
PEROKSIDA
Diajukan Oleh
Imas Noviyana
0801359
Disetujui dan Disahkan Oleh :
Pembimbing I
Dr. Agus Setiabudi, M.Si NIP. 196808031992031002
Pembimbing II
Galuh Yuliani, Ph.D NIP. 198007252001122001
Mengetahui,
Ketua Jurusan Pendidikan Kimia FPMIPA UPI
ABSTRAK
Batu bara muda memiliki nilai kalori pembakaran yang rendah serta kadar sulfur dan air yang tergolong tinggi. Oleh sebab itu, pemanfaatan batu bara muda sebagai bahan bakar dinilai kurang efisien. Telah banyak penelitian yang melaporkan penggunaan batu bara muda sebagai adsorben bagi pencemar logam dan organik. Kapasitas adsorpsi batu bara muda masih lebih rendah dibandingkan adsorben lain terutama arang aktif. Pada penelitian ini telah diupayakan peningkatan kapasitas adsorpsi pada batu bara muda melalui pengayaan kadar oksigen di permukaannya. Umumnya, perlakuan dengan hidrogen peroksida digunakan sebagai penghilang sulfur pada batu bara muda sehingga dapat meningkatkan kualitasnya. Pada penelitian ini hidrogen peroksida digunakan untuk mengoksidasi permukaan batu bara muda, sehingga meningkatkan jumlah gugus karboksilat di permukaan. Gugus karboksilat telah banyak dilaporkan sebagai sisi aktif pada proses adsorpsi senyawa logam dan organik oleh batu bara muda. Batu bara muda yang digunakan berasal dari daerah banten (Indonesia), memiliki nilai kalori 4.955cal/g , 13,11% kadar air, 55,18% karbon, dan 1,4% sulfur. Uji adsorpsi dilakukan menggunakan teknik “batch test” dengan larutan methylene blue sebagai adsorbat dan variasi waktu adsorpsi 1-7 jam. Konsentrasi methylene blue ditentukan menggunakan spektroskopi UV-Vis pada panjang gelombang 665,5nm. Dari hasil uji adsorpsi didapat waktu optimal yaitu selama 5 jam, sehingga untuk tes adsorpsi selanjutnya dilakukan selama 5 jam. Modifikasi menggunakan larutan hidrogen peroksida dilakukan dengan variasi konsentrasi dan waktu pengadukan hidrogen peroksida sebagai berikut : 5% dalam ½ jam, 5% dalam 1 jam, 10% dalam ½ jam dan 20% dalam 10 menit. Kapasitas adsorpsi maksimum ditentukan menggunakan larutan methylene blue dengan model isoterm adsorpsi Freundlich dan Langmuir. Dari plot data eksperimen, diindikasikan bahwa adsorpsi pada batu bara muda dan batu bara muda hasil modifikasi mengikuti model isoterm Langmuir. Kapasitas adsorpsi (qe) batu bara muda dan batu bara muda hasil modifikasi, secara berurutan, mencapai 51,81 mg/g dan 103,09 mg/g. Batu bara muda hasil modifikasi dikarakterisasi dengan menggunakan FTIR, BET adsorption, dan SEM. Data hasil pengujian FTIR batu bara muda hasil modifikasi memberikan puncak serapan baru yang signifikan pada 1700cm-1 yang menandakan adanya gugus C=O (Karboksilat). Luas permukaan batu bara muda setelah modifikasi meningkat menjadi 0,232m2/g dari luas permukaan mula-mula sebesar 0,097m2/g. Gambar-gambar SEM juga mengindikasikan, peningkatan porositas pada permukaan batu bara muda hasil modifikasi. Dari hasil uji adsorpsi dan karakterisasi, disimpulkan bahwa perlakuan menggunakan hidrogen peroksida telah berhasil meningkatkan kemampuan adsorpsi batu bara muda terhadap methylene blue sebesar 100%.
ABSTRACT
Brown coal combustion has a low calori, sulfur and high water. Therefore, the use of brown coal as fuel considered less efficient. There have been many studies reported the use of brown coal as an adsorbent for metals and organic pollutants. Brown coal adsorption capacity is lower than others, especially activated carbon. In this study has been attempted on the adsorption capacity brown coal through the enrichment of oxygen levels in the surface. Generally, treatment with hydrogen peroxide is used as a reliever sulfur in brown coal so as to improve its quality. In this study, hydrogen peroxide is used to oxidize the surface of the brown coal, there by increasing the number of carboxylic groups on the surface. Carboxylate groups has been widely reported as the active site on the metal and the organic compound adsorption by brown coal. Brown coal used comes from Banten (Indonesia), has a calorific value 4.955cal / g, 13.11% water, 55.18% carbon, and 1.4% sulfur. Adsorption test performed using the technique of batch test with a solution of methylene blue as adsorbate and adsorption time variation of 1-7 hours. The concentration of methylene blue were determined using UV-Vis spectroscopy at a wavelength of 665.5 nm. Test results obtained from the adsorption of the optimal time for 5 hours, so for the next adsorption tests carried out for 5 hours. Modifications performed using hydrogen peroxide solution with concentration and stirring time variation of hydrogen peroxide as follows: 5% in ½ hour, 5% in 1 hour, 10% within ½ hours and 20% within 10 minutes. The maximum adsorption capacity was determined using methylene blue solution with the model of Freundlich and Langmuir adsorption isotherms. From the plot of experimental, indicated that the adsorption on brown coal and brown coal modified Langmuir isotherm modeled. Adsorption capacity (qe) brown coal and brown coal modified, respectively, reached 51.81 mg / g and 103.09 mg / g. Brown coal modified characterized using FTIR, BET adsorption, and SEM. Data FTIR test results brown coal modification provides significant new peak at 1700cm-1, which indicates the group C = O (Carboxylic). Surface area after modification increased to 0.232 m2 / g of surface area initially at 0.097 m2 / g. These images also indicate SEM, increased porosity in surface modification. From the test results of adsorption and characterization, it was concluded that the treatment using hydrogen peroxide has been successful in increasing the adsorption capacity brown coal to methylene blue at 100%.
DAFTAR ISI
2.1.2 Komponen-komponen dalam Batu Bara ... 7
2.1.3 Pemanfaatan Batu Bara Muda ... 8
2.2 Adsorpsi ... 9
2.2.1 Jenis Adsorpsi ... 10
2.2.1.1 Adsorpsi Fisika ... 10
2.2.1.2 Adsorpsi Kimia ... 11
2.2.2 Faktor-faktor Yang Mempengaruhi Adsorpsi ... 13
2.2.3 Isoterm Adsorpsi ... 15
2.2.3.1 Isoterm Adsorpsi Langmuir ... 15
2.3 Adsorben ... 18
2.4 Methylene Blue ... 22
2.5 Karakterisasi ... 20
2.5.1 FTIR (Spectrofotometer Fourier Transform Infra Red) .... 23
2.5.2 Spektroskopi UV-Vis ... 23
2.5.3 Scanning Electron Microscopy (SEM) ... 25
BAB III METODOLOGI PENELITIAN ... 27
3.4.3 Uji Kapasitas Adsorpsi pada Karbon Aktif ... 29
3.4.4 Penentuan Waktu Optimum ... 29
3.4.5 Preparasi Batu Bara Muda Modifikasi ... 30
3.4.7 Uji Kapasitas Adsorpsi Batu Bara Muda Modifikasi ... 30
3.4.8 Uji Karakterisasi ... 30
BAB IV HASIL DAN PEMBAHASAN ... 32
4.1 Uji Kapasitas Adsorpsi pada Karbon Aktif ... 32
4.2 Preparasi Batu Bara Muda Modifikasi ... 34
4.3 Uji FTIR ... 38
4.5 Uji Kapasitas Adsorpsi Batu Bara Muda dan
Batu Bara Muda Modifikasi ... 41
4.6 Oksidasi Batu Bara Muda Menggunakan Hidrogen Peroksida 44 4.7 Mekanisme Adsorpsi ... 46
BAB V KESIMPULAN DAN SARAN ... 48
5.1 Kesimpulan ... 48
5.2 Saran ... 49
DAFTAR PUSTAKA ... 50
DAFTAR TABEL
Tabel 2.1 Perbedaan Adsorpsi Kimia dan Fisika ... 12
Tabel 2.2 Spektrum Daerah FTIR ... 23
Tabel 2.3 Spektrum Tampak dan Warna Komplementer ... 25
Tabel 4.1 Hasil Perhitungan Isoterm Adsorpsi Karbon Aktif ... 34
Tabel 4.2 Hasil Perngujian Unsur Batu Bara Muda dan Batu Bara Muda Modifikasi ... 37
Tabel 4.3 Hasil Pengujian BET Batu Bara Muda dan Batu Bara Muda Modifikasi ... 40
DAFTAR GAMBAR
Gambar 2.1 Struktur Batu Bara ... 4
Gambar 2.2 Tingkatan pada Batu Bara ... 6
Gambar 2.3 Ilustrasi Skematik Adsorpsi Adsorbat kedalam Pori ... 11
Gambar 2.4 Persamaan Kapasitas Adsorpsi ... 15
Gambar 2.5 Persamaaan Langmuir ... 16
Gambar 2.6 Kurva Adsorpsi Langmuir ... 17
Gambar 2.7 Persamaan Freundlich ... 17
Gambar 2.8 Kurva Adsorpsi Freundlich ... 18
Gambar 2.9 Struktur Methylene Blue ... 22
Gambar 3.1 Tahapan Umum Penelitian ... 28
Gambar 4.1 Hasil Adsorpsi Karbon Aktif ... 32
Gambar 4.2 Scanning Methylene Blue ... 33
Gambar 4.3 Kurva Isoterm Adsorpsi Langmuir dan Freundlich Karbon Aktif ... 33
Gambar 4.4 Batu Bara Muda DItambahkan Larutan H2O2 ... 35
Gambar 4.5 Batu Bara Muda dan Batu Bara Modifikasi ... 35
Gambar 4.6 Hasil Filtrat dari Batu Bara Muda Modifikasi ... 36
Gambar 4.7 Hasil Scanning Pada Filtrat Batu Bara Muda Modifikasi ... 36
Gambar 4.8 Gabungan Spektra FTIR dari Batu Bara Muda dan Batu Bara Muda Modifikasi ... 38
Gambar 4.9 Gabungan Spektra Sebelum dan Sesudah Adsorpsi pada Batu Bara Muda Modifikasi ... 39
Gambar 4.11 Hasil Adsorpsi Batu Bara Muda ... 41
Gambar 4.12 Kurva Optimasi Waktu Batu Bara Muda ... 41
Gambar 4.13 Kurva Isoterm Adsorpsi Langmuir Batu Bara Muda dan
Batu Bara Muda Modifikasi ... 42
Gambar 4.14 Kurva Isoterm Adsorpsi Freundlich Batu Bara Muda dan
Batu Bara Muda Modifikasi ... 43
DAFTAR LAMPIRAN
Lampiran 1. Lampiran Perhitungan Pembuatan Larutan ... 54
Lampiran 2. Lampiran Kurva Kalibrasi Methylene Blue ... 56
Lampiran 3. Lampiran Hasil Absorbansi ... 57
BAB I
PENDAHULUAN
1.1 Latar Belakang Masalah
Batu bara muda memiliki nilai kalori pembakaran yang rendah, serta kadar
sulfur dan airnya yang tergolong tinggi. Karena itu, pemanfaatan batu bara muda
sebagai bahan bakar tergolong kurang ekonomis. Bila sumber energi ini dibawa
ke lokasi yang jauh dari area tambang, maka biaya transportasinya menjadi mahal.
Ongkos angkut itu sebenarnya dikeluarkan untuk membawa air dan abu yang
nantinya harus dibuang dalam proses pemanfaatan batu bara. Ketika dibakar,
banyak energi yang terbuang untuk menguapkan air, sedangkan nilai kalori yang
diperoleh relatif rendah. Selain itu, kandungan sulfur yang tinggi akan menjadi
gas pencemar. Karenanya diperlukan biaya tambahan untuk mengurangi emisi gas
sulfur. Dengan adanya masalah tersebut, bila terdapat lapisan batu bara muda
dalam penambangan batu bara, maka penambang hanya mengambil lapisan yang
berkualitas tinggi. Sedangkan batu bara muda akan disingkirkan atau ditimbun
kembali di lokasi tambang (Tirasonjaya, 2002).
Berdasarkan penelitian sebelumnya dinyatakan bahwa batu bara muda dari
Victoria Australia, mempunyai luas permukaan yang relatif besar dan dapat
mengadsorpsi zat warna, organik, dan fosfor sehingga dapat dijadikan sebagai
adsorben yang baik (Yuliani, 2012). Batu bara muda pada penelitian tersebut
adalah batu bara muda mentah tanpa perlakuan ataupun tanpa aktivasi lainnya.
2
Dari beberapa literatur, dilaporkan bahwa sisi aktif dari batu bara muda
adalah gugus karboksilat yang dapat mengalami reaksi pertukaran kation dengan
adsorbat (Yuliani, 2012) (Mae, et al., 2006).
Oleh sebab itu, penelitian ini bertujuan untuk meningkatkan kadar
karboksilat (C=O) pada batu bara muda yaitu dengan mereaksikan hidrogen
peroksida sebagai oksidator kuat. Oksidasi dengan menggunakan hidrogen
peroksida sudah dilakukan pada penelitian lain, dengan tujuan untuk
meningkatkan kelarutan dalam pemrosesan batu bara muda menjadi batu bara cair
(Mae, et al, 2006). Namun pada penelitian ini, perlakuan dengan hidrogen
peroksida diharapkan dapat meningkatkan kapasitas adsorpsi dari batu bara muda
tersebut.
1.2 Rumusan Masalah
Berdasarkan uraian yang telah dikemukakan di atas, maka rumusan
masalah dalam penelitian ini adalah:
1. Apakah oksidasi menggunakan hidrogen peroksida dapat meningkatkan
kadar senyawa oksigen (gugus karboksilat) pada batu bara muda?
2. Bagaimana karakter batu bara muda hasil modifikasi dengan hidrogen
peroksida?
3. Termasuk model adsorpsi apakah batu bara muda hasil modifikasi?
4. Seberapa besar peningkatan kapasitas adsorpsi batu bara muda hasil
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah untuk memperkaya kandungan oksigen
(sebagai gugus karboksilat) pada permukaan batu bara muda menggunakan
hidrogen peroksida sebagai oksidator kuat, sehingga meningkatkan kapasitas
adsorpsi batu bara muda terhadap methylene blue.
1.4 Manfaat Penelitian
Melalui penelitian ini diharapkan batu bara muda dengan penambahan
hidrogen peroksida dapat berfungsi sebagai adsorben yang setara dengan arang
aktif. Namun, karena harganya yang jauh di bawah karbon aktif yaitu berkisar $
18,76/ton atau 187.600rb/ton (Indoenergi.com, 2012), sedangkan karbon aktif
mencapai 7.000/kg atau 7jt/ton (Agromarket.com, 2012). Batu bara muda
diharapkan mampu menjadi adsorben alternatif yang murah dan mudah didapat
27
BAB III
METODE PENELITIAN
3.1 Tempat Penelitian
Penelitian ini dilaksanakan di laboratorium Riset (Research Laboratory),
Karakterisasi FTIR dan Karakterisasi UV-Vis dilakukan di laboratorium Kimia
Instrumen, Jurusan Pendidikan Kimia, FPMIPA Univeritas Pendidikan Indonesia
(UPI), Gedung JICA lantai 5, Jl. Dr. Setiabudhi No. 229 Bandung .
3.2 Alat dan Bahan
3.2.1 Alat
Alat-alat yang digunakan adalah : alat-alat gelas, hot plate, shaker,
thermometer, neraca analitik, neraca teknis, penangas, lumping alu dan alat-alat
untuk analisis berupa FTIR Shimadzu 8400, Spektroskopi UV-Vis, SEM, BET
Surface Area dan Analisis Unsur CHONS (Karbon, Hidrogen, Oksigen, Nitrogen,
Sulfur).
3.2.2 Bahan
Bahan-bahan yang digunakan adalah : Batu bara muda, H2O2, aquadest,
kertas saring whatman 40, dan methylene blue.
3.3Desain Penelitian
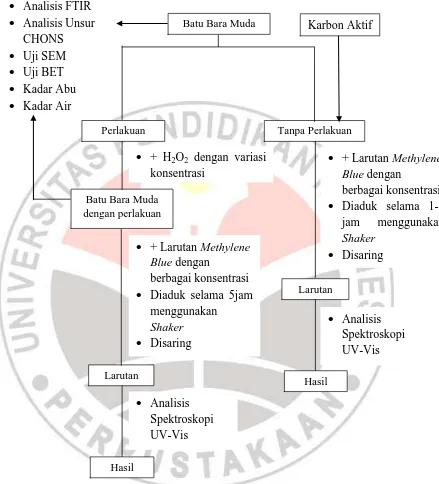
Desain penelitian dilakukan mengikuti alur penelitian seperti ditunjukkan
28
Gambar 3.1 Tahapan umum penelitian.
29
3.4 Prosedur Penelitian
3.4.1 Preparasi Contoh Limbah
Contoh larutan yang digunakan adalah larutan methylene blue. Larutan
induk disiapkan dengan konsentrasi 100ppm. Kurva kalibrasi disiapkan dengan
mengencerkan larutan induk.
3.4.2 Preparasi Adsorben
Adsorben yang digunakan adalah karbon aktif dan batu bara muda.
Adsorben dihaluskan terlebih dahulu menggunakan lumpang dan alu hingga
ukuran partikel dari adsorben halus. Adsorben diayak menggunakan saringan
dengan ukuran 100 mesh. Untuk batu bara muda yang telah dihaluskan diuji
kalori, kadar air, unsur CHONS, FTIR, SEM dan BET.
3.4.3 Uji Kapasitas Adsorpsi Pada Karbon Aktif
Sebanyak 50 mL larutan methylene blue dengan konsentrasi 100ppm
dimasukan pada wadah yang berisi karbon aktif yang telah ditimbang dengan
variasi berat : 0,1g; 0,15g; 0,2 g; 0,25g; 0,3g. Campuran diaduk menggunakan
shaker selama 1jam lalu disaring. Dilakukan berulang-ulang dengan variasi waktu
2jam dan 3jam. Filtrat yang diperoleh dianalisis menggunakan Spektroskopi
UV-Vis pada panjang gelombang 665nm.
3.4.4 Penentuan Waktu Optimum Pengadukan Batu Bara Muda
Sebanyak 50 mL larutan methylene blue dengan konsentrasi 100ppm
dimasukan pada wadah yang berisi batu bara muda yang telah ditimbang dengan
variasi berat : 0,1g; 0,15g; 0,2 g; 0,25g; 0,3g. Campuran diaduk menggunakan
30
2-7 jam. Filtrat yang diperoleh dianalisis menggunakan Spektroskopi UV-Vis
pada panjang gelombang 665nm.
3.4.5 Preparasi Batu Bara Dengan Perlakuan
Seberat 2 gram batu bara muda ditimbang lalu dimasukkan dalam wadah
gelas kimia 100mL. Kedalam gelas kimia ditambahkan aquades terlebih dahulu
(jumlah aquades yang ditambahkan sesuai perbandingan dengan konsentrasi H2O2
yang ditambahkan) diaduk menggunakan stirrer hingga homogen lalu
ditambahkan larutan H2O2 dengan variasi konsentrasi 5%, 10%, dan 20%.
Pengocokan dilakukan selama ½ jam, terkecuali bagi penambahan 5% H2O2
dilakukan ½ jam dan 1jam. Setelah diaduk larutan disaring dan diambil residunya
lalu dikeringkan. Batu bara yang hasil modifikasi diuji kalori, unsur CHONS,
FTIR, SEM dan BET.
3.4.6 Uji Kapasitas Adsorpsi Pada Batu Bara Muda Perlakuan
Sebanyak 50 mL larutan methylene blue dengan konsentrasi 200 ppm
dimasukan pada wadah yang berisi batu bara muda hasil modifikasi yang telah
ditimbang dengan variasi berat : 0,1g; 0,15g; 0,2 g; 0,25g; 0,3g. Campuran diaduk
menggunakan shaker selama 5jam lalu disaring. Filtrat yang diperoleh dianalisis
menggunakan Spektroskopi UV-Vis pada panjang gelombang 665nm. Batu bara
muda hasil modifikasi yang telah diadsorpsi diuji FTIR.
3.4.7 Uji Karakterisasi
a. Uji FTIR
31
dikompa dengan tekanan tinggi. Kemudian diukur persen transmitan dari
bilangan gelombang 400 – 4000 cm.
b. Uji Spektroskopi UV-Vis
Penentuan panjang gelombang maksimum dilakukan pengukuran
absorbat larutan pada rentang panjang gelombang 400-700 nm (jarak
rentang 10 nm, setelah mendekati panjang gelombang maksimum perkecil
rentangnya). Dibuat deret standar methylene blue 0,5 ppm; 1 ppm; 1,5
ppm; 2 ppm dan 2,5 ppm. Pengukuran serapan larutan deret standar dan
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Berdasarkan penelitian yang telah dilakukan, maka dapat disimpulkan
bahwa :
1. Oksidasi menggunakan H2O2 pada batu bara muda dapat meningkatkan
kadar senyawa oksigen dan meningkatkan kapasitas adsorpsi pada
batu bara muda. Hal ini dibuktikan dari FTIR. Dengan adanya puncak
serapan baru yang signifikan 1700 cm-1 yang merupakan serapan
gugus C=O.
2. Hasil SEM dan BET memperlihatkan bahwa adanya peningkatan
porositas pada permukaan batu bara muda hasil modifikasi dan adanya
peningkatan luas permukaan dari batu bara muda modifikasi yaitu dari
0,097 m2/g menjadi 0,232 m2/g.
3. Kesesuaian dengan persamaan Langmuir menunjukan bahwa batu bara
muda dan batu bara muda hasil modifikasi merupakan adsorben
monolayer.
4. Kapasitas maksimum pada batu bara muda meningkat setelah di
5.2 Saran
Dari hasil penelitian yang telah dilakukan, maka penulis dapat
memberikan saran antara lain :
1. Diperlukan adanya peningkatan variasi waktu pada proses oksidasi
larutan H2O2.
2. Diperlukan pengujian pada sistem limbah untuk aplikasi batu bara
DAFTAR PUSTAKA
Aerosol & Particulate Research Lab. Adsorption. [Online]. [Tersedia :
http://files.engineering.com/download.aspx?folder=72dc2393-de04-412e-aac0-0e72014a9c5b&file=adsorption.ppt]. [19 Januari 2013]
Agyei, N.M.; Strydom, C.A. and Potgieter, J.H. (2000). An investigation of
phosphate ion adsorption from aqueous solution by fly ash and slag. Cem.
and Concr. Res., 30(5), 823-826.
Alberty, D. F. dan A. Robert. (1983). Kimia Fisika, Penerjemah Suraida, Jilid
pertama, Edisi kelima, Penerbit Erlangga.
Arnas. (2008). Kapasitas Penyerapan CO2 Pada Karbon Aktif yang Berasal Dari
Batubara Sumatera Selatan Dengan Tekanan Maksimum 2,3 Bar. Skripsi.
Depok : Departemen Teknik Mesin FTUI.
Atkins, P.W. (1999). Kimia Fisika. Jakarta: Erlangga.
Atmoko, Rainudy deswanto. (2012). Pemanfaatan karbon aktif batubara
termodifikasi TiO2 pada proses reduksi gas karbon monoksida (CO) dan
penjernihan asap kebakaran. Skripsi. Depok : Departemen Teknik Kimia
FTUI.
Bendiyasa, Made., Endang Tri Wahyuni dan Iwan Kurniawan. (2008).
Peningkatan Kapasitas Adsorpsi Zeolit Alam Indonesia Terhadap Ion Cd
Dengan Metode Pencucian Sekuensial Memakai Larutan Asam Florida
(HF) dan Disodium Ethylene Diamine Tetra Acetate (Na2EDTA). Media
Teknik. ISSN 0216-3012.
Benefield, L. D., Judkins, J. F., and Weand, B. L., (1982). Process Chemistry For
Water and Wastewater Treatment. New Jersey: Pretice Hall Inc.
Candra. (2009). Briket Batubara. [Online]. [Tersedia :
http://id.scribd.com/doc/17255708/6/Komponen-Komponen-dalam-Batubara]. [20 Februari 2013]
Castellan, G.W. (1982). Physical Chemistry. Third Edition. General Graphic
Servies. New York.
Chodijah, Siti. (2011). Pemanfaatan arang batok kelapa dan batubara sebagai
Chrisman, Anthonyus. (2008). Preparasi Karbon Aktif Sebagai Adsorben Dari
Batubara Sumatera Selatan Dengan Aktivasi CO2. Skripsi. Depok :
Departemen Teknik Mesin FTUI.
Corinne, C.D., and Christopher J.L. (1996). Lignit: A Novel Material For
Low-Cost Removal And Disposal Of Heavy Metals And Radionuclides From
Waste Water. Energei4 Vol. 7, No.2.
Couto, Gabriela Martucci; Anelise Lima de Abreu Dessimoni; Maria Lúcia
Bianchi; Deise Morone Perígolo; and Paulo Fernando Trugilho. (2012).
Use of Sawdust Eucalyptus sp. In The Preparation of Activated Carbons.
Ciênc. agrotec. vol.36 no.1.
Hendra, Ryan. (2008). Pembuatan Karbon Aktif Berbahan Dasar Batubara
Indonesia Dengan Metode Aktivasi Fisika dan Karakteristiknya. Skripsi.
Depok : Departemen Teknik Mesin FTUI.
Ho, Y.S. and McKay, G. (1999a). Competitive sorption of copper and nickel ions
from aqueous solution using peat. Adsorption-Journal of the International
Adsorption Society, 5(4), 409-417.
Krystianty, Kartika. (2008). Adsorpsi Merkuri (II) Oleh Biomassa Enceng Gondok
(Echornia crassipes) Yang Diimobilisasi Pada Matriks Polisilikat
Menggunakan Metode Kolom. Skripsi. Malang : Fakultas Sains dan
Teknologi UINM.
Kumar, K.V., S. Sivanesan. (2006). Equilibrium data, isotherm parameters and
process design for partial and complete isotherm of methylene blue onto
activated carbon. J. Hazard. Mater. 134, 237–244.
Kusuma, E.D., (2002), Kajian Kinetika Adsorpsi Pada Tanah Pertanian Kaolit
Sukamandi Jawa Barat. FMIPA, Yogyakarta.
Landon, J. B. and Maron, S. H., (1974). Fundamental of Physical Chemistry, Mc
Millan Co. Inc., New York.
Larry, D.B., Judkins J.F., and Weant, B.L. (1992). Process Chemistry for Water
and Wastewater. Prentice Hall Inc. New Jersey.
Mae, Kazuhiro; Taisuke Man, Jun Araki, and Kouichi Mura,. (2006).
Peroxide Inconventionally Used Solvents at Room Temberature. Japan :
Department of Chemical Engineering Kyoto University.
Marsh, H., (2001). Activated Carbon Compendium. Elsevier Science, Amsterdam
Moret, A and J. Rubio, (2005). Sulphat Ions Uptake by Chitin-Based Shrimp
Wasted Shells, Departamento de Engenharia de Minas-Laboratorio de
Technologia Minerale Ambiental-Universidade Federal do Rio Grande do
Sul, Av. Osvaldo Aranha 99/512. [Online]. [Tersedia :
http://www.lapes.ufrgs.br/Laboratorios/itm.html]. [11 Januari, 2013]
Mudzakir, Ahmad dkk. (2008). Penuntut Praktikum Kimia Anorganik (KI - 425).
Bandung: Jurusan Pendidikan Kimia FPMIPA UPI.
Mulja, M. dan Suharman. (1995). Analisis Instrumental, Airlangga University
Press, Surabaya.
Orchin, M, Reggel L. (1947). Aromatic Cyclodehydrogenation. J. Am. Chem.
Soc., 69, 505-509.
Oscik, J. (1991). Adsorbtion, Edition Cooper, I.L., John Wiley and Sons, New
York.
Oscik J. (1994). Adsorption. New York: Ellis Horwood.
Palupi, Endang. (2006). Degradasi Methylene Blue Dengan Metode Fotokatalisis
Dan Fotoelektrokatalisis Menggunakan Film TiO2. Bogor : Departemen
Fisika IPB.
Perry, R.H. and Green, D.W., (1984). Perry’s Chemical Engineer’s Handbook.
6ed, pp. 16-4 – 16-14, McGraw-Hill Book Company, Inc., New York.
Sawyer, C.N and Mc Carty, P.L. (1987). Chemistry for Enggineering, 3rd Edition,
Mc Graw-Hill Book Company, New York.
Setiawan, Bambang. (2005). Kebijakan Umum Pemanfaatan Batu Bara dan
Rancangan Undang-undang Mineral dan Batu Bara. Jakarta.
Sholehah, A. (2008). Kimia Permukaan 1, Bahan Ajar Kimia Fisika. Institut
Teknologi Bandung, Bandung.
Singh, B. and Alloway, B.J. (2006). Adsorptive Minerals To Reduce The
Availability Of Cadmium And Arcenic In Contaminated Soils. School of
Tirasonjaya, Fariz. (2002). Batu Bara Muda Untuk Pembangkit Listrik. [Online].
[Tersedia :
http://ilmubatubara.wordpress.com/2002/08/18/batubara-muda-untuk-pembangkit-listrik/]. [16 Februari 2012]
Tong, K. S. ; A. Azraa, and M. Jain Noordin. (2012). Isotherms and Kinetics
Studies on the Removal of Methylene Blue from Aqueous Solution by
Gambir. International Journal of Environmental Science and
Development, Vol. 3, No. 3.
Wang, Haihui; Bogdan Z. Dlugogorski and Eric M. Kennedy. (2003). Coal
oxidation at low temperatures : oxygen consumption, oxidation products,
reaction mechanism and kinetic modeling. Progress in Energy and
Combustion Science. 29, 487–513.
Weber, W.J. (1972). Physicochemical Processes For Water Quality Control.
Wiley Interscience. New York.
Wibowo, Dwi Agus. (2011). Batu Bara. [Online]. [Tersedia :
http://www.scribd.com/doc/69968519/batu]. [20 Februari 2012]
Widhianti, Wahyu Dwi. (2010). Pembuatan Arang Aktif Dari Biji Kapuk (Ceiba
pentandra L.) Sebagai Adsorben Zat Warna Rhodamin B. Skripsi.
Surabaya : Departemen Kimia Universitas Airlangga.
Wiji. Anna Permanasari, dkk. (2010). Penuntun Praktikum Kimia Analitik
Instrumen. Bandung: Jurusan Pendidikan Kimia FPMIA UPI.
World Coal Institute. (2005). Coal-Power For Progress. [Online]. [Tersedia :
www.worldcoal.org]. [20 Februari 2012]
Yuliani, Galuh ; Ying Qi, Andrew F.A. Hoadley, Alan L. Chaffee, and Gil
Garnier. (2012). Lignite clean up of magnesium bisulphite pulp mill
effluent as a proxy for aqueous discharge from a ligno-cellulosic
biorefinery. SciVerse ScienceDirect, Biomass and Bioenergy. 2012, 38,