BAB II
TINJAUAN PUSTAKA
2.1. Pengawetan Buah ( Coater )
Coater merupakan pemberian lapisan tipis pada permukaan buah untuk
menghambat keluarnya gas, uap air dan kontak dengan oksigen, sehingga proses
pemasakan dan reaksi pencoklatan buah dapat diperlambat serta memberikan
perlindungan terhadap kerusakan mekanis buah (Kusuma, 2008).
Proses pengangkutan, untuk pemasaran buah dibutuhkan waktu, pengemasan
dan penanganan pasca panen yang tepat. Pada umumnya, buah dipasarkan dalam
kemasan kotak plastik pada suhu ruang. Cara ini berpengaruh pada kecepatan
penurunan kualitas, ketersediaan dan pemasaran buah. Penurunan kualitas salah
satunya disebabkan oleh aktivitas hidup buah yang terus berlangsung meskipun buah
telah lepas dari tanamannya, contohnya proses respirasi (Swastawati, 2008).
Pada umumnya proses pengangkutan dan penyimpanan masih berlangsung
setelah buah dipanen. Buah terus mengalami proses metabolisme dengan
menggunakan cadangan makanan yang terdapat di dalam buah. Hal itu menyebabkan
cadangan makanan semakin berkurang. Berkurangnya cadangan makanan tersebut
tidak dapat digantikan karena buah sudah terpisah dari pohonnya (Budiman, 2006).
Seiringan dengan itu, metabolisme akan mempercepat proses hilangnya nilai
gizi buah. Tingkat kerusakan buah dipengaruhi oleh difusi gas ke dalam dan luar
buah yang terjadi melalui lentisel yang tersebar di permukaan buah. Secara alami
lilin tersebut dapat berkurang atau hilang akibat pencucian yang dilakukan pada saat
penanganan pasca panen (Rukmana, 1998).
Selama pasca panen akan terjadi beberapa perubahan, yang akhirnya
menyebabkan kerusakan. Kerusakan tersebut dapat diakibatkan terjadinya perubahan
dari segi rasa, bau dan tekstur serta keamanannya untuk dikonsumsi. Kerusakan dapat
pula diakibatkan oleh terjadinya pembusukan karena mikroorganisme.
Mikroorganisme yang sering menyebabkan pembusukan seperti adanya kapang.
Konsep dari mempertahankan umur produk holtikultura adalah dengan
menghambat laju respirasi untuk mencegah degradasi nutrisi-nutrisi di dalamnya.
Maka digunakan pelapisan pada permukaan luar buah. Salah satu cara yang telah
banyak dikenal adalah dengan melakukan coating (Nurrachman, 2007).
2.1.1. Teknik Pengawetan ( Coating )
Menurut Grenner (1994), teknik aplikasi pelapisan pada buah ( coating ), yaitu:
1. Perendaman (dipping)
Teknik ini biasanya digunakan pada produk yang memiliki permukaan yang
kurang nyata. Setelah perendaman, kelebihan bahan coating dibiarkan terbuang.
Produk kemudian dibiarkan dingin sampai edible coating menempel. Teknik ini
2. Penyemprotan (spraying)
Teknik ini dapat menghasilkan produk dengan lapisan yang lebih tipis dan
lebih seragam daripada teknik pencelupan. Teknik ini digunakan untuk produk
yang memiliki dua sisi permukaan, misalnya pizza.
3. Pembungkusan (casting)
Teknik ini digunakan untuk membuat lapisan film yang berdiri sendiri,
terpisah dari produk. Teknik ini diadopsi dari teknik yang dikembangkan untuk
non-coater.
4. Pengolesan (brushing)
Teknik ini dilakukan dengan cara mengoles edible coating pada produk.
Kemampuan coater dalam mengurangi hilangnya air, oksigen, aroma, dan
bahan terlarut pada beberapa produk telah banyak diteliti. Sehingga dapat dijadikan
sebagai salah satu metode paling efektif untuk menjaga kualitas makanan.
Kemampuan ini dapat lebih ditingkatkan lagi dengan menambahkan antioksidan,
antimikroba, pewarna, flavor, fortified nutrient dan rempah.
2.2. Potensi Cangkang Udang Sebagai Pengawet Alami
Sebagai negara maritim, Indonesia mempunyai potensi hasil perikanan laut
yang sangat berlimpah, namun potensi ini masih belum bisa dimanfaatkan secara
optimal. Menurut data Dirjen Perikanan,total potensi ini diperkirakan sebesar 7,2 juta
ton/tahun, dan yang bisa dimanfaatkan baru sekitar 40% atau 2,7 juta ton/tahun
Salah satu potensi ini adalah udang yang saat ini merupakan komoditas
eksport unggulan hasil perikanan, saat ini budi daya udang dengan tambak telah
berkembang dengan pesat, karena udang merupakan komoditi ekspor yang dapat
diandalkan dalam meningkatkan ekspor non-migas dan merupakan salah satu jenis
biota laut yang bernilai ekonomis tinggi. Udang di Indonesia pada umumnya diekspor
dalam bentuk udang beku yang telah dibuang bagian kepala, kulit, dan ekornya
(Kaban, dkk., 2006).
Dalam perkembangannya, Indonesia memasukkan udang vannamei
(Litopenaeus vannnamei ) sebagai salah satu jenis udang budidaya tambak, selain
udang windu (Penaeus monodon) dan udang putih/udang rebung (Penaeus
merguiensis) yang sudah terkenal lebih dahulu ( Amri, 2008). Udang windu saat ini
tidak berkembang lagi karena terserang berbagai macam penyakit udang diantaranya
yang ganas adalah white spot atau virus bintik putih. Petambak udang di Indonesia
saat ini banyak memelihara udang putih ( Pennaeus vannamei) (Purwanti, 2010).
Setelah melalui serangkaian penelitian dan kajian akhirnya melalui SK
Menteri Kelautan dan Perikanan RI No. 41/2001 pemerintah secara resmi melepas
udang vannamei sebagai varietas unggul untuk dibudidayakan petambak di tanah air
pada tanggal 12 Juli 2001 (Amri, 2008).
Berikut tata nama udang vannamei menurut ilmu taksonomi ( Haliman, 2008).
Kingdom : Animalia
Subkingdom : Metazoa
Filum : Arthropoda
Kelas : Malacostraca
Subkelas : Eumalacostraca
Superordo : Eucarida
Ordo : Decapoda
Subordo : Dendrobrachiata
Famili : Penaeidae
Genus : Litopenaeus
Species : Litopenaeus vannamei
Cangkang udang sampai saat ini memang belum banyak mendapat perhatian.
Selama ini orang hanya peduli pada dagingnya saja. Padahal cangkang udang berupa
kulit atau yang juga disebut karapas, yang komposisinya bisa mencapai 50-60 % bisa
dimanfaatkan menjadi berbagai produk. Fungsi cangkang tersebut pada hewan udang
yaitu sebagai pelindung.
Cangkang udang mengandung protein (25% - 40%), kalsium karbonat (45% -
50%), dan chitin (15% - 20%), tetapi besarnya kandungan komponen tersebut
tergantung pada jenis udangnya, sedangkan cangkang kepiting mengandung protein
(15,60% 23,90%), kalsium karbonat (53,70% 78,40%), dan chitin (18,70%
-31,20%), hal ini juga tergantung pada jenis kepiting dan tempat hidupya. Kandungan
chitin dalam cangkang udang lebih sedikit dari cangkang kepiting, tetapi cangkang
udang lebih mudah didapat dan tersedia dalam jumlah yang banyak (Kaban, dkk.,
Meningkatnya jumlah cangkang udang masih merupakan masalah yang perlu
dicarikan upaya pemanfaatannya. Hal ini bukan saja memberikan nilai tambah pada
usaha pengolahan udang, akan tetapi juga dapat menanggulangi masalah pencemaran
lingkungan yang ditimbulkan, terutama masalah bau yang dikeluarkan. Saat ini di
Indonesia sebagian kecil dari cangkang udang sudah dimanfaatkan dalam hal
pembuatan kerupuk udang, petis, terasi, dan bahan pencampur pakan ternak.
Sedangkan di negara maju seperti di Amerika Serikat dan Jepang, cangkang udang
telah dimanfaatkan di dalam industri sebagai bahan dasar pembuatan chtitin dan
chitosan. Manfaatnya di berbagai industri modern banyak sekali seperti industri
farmasi, biokimia, bioteknologi, biomedikal, pangan, kertas, tekstil, pertanian, dan
kesehatan serta pembuatan edible film sebagai pengemas ataupun coating pada
berbagai produk makanan, sayur-sayuran, dan buah-buahan (Restuati, 2008).
Chitin yang belum dimanfaatkan sebesar 56.200 metrik ton/tahun. Menurut
hasil survei Badan Riset Kelautan dan Perikanan (BRKP) menunjukkan bahwa
daerah Jabotabek tersedia sekitar 100 ton/bulan cangkang udang kering setara satu
ton chitin, dikonversikan ke dalam nilai mata uang, maka akan diperoleh devisa
sebesar US$ 65 ribu/bulan atau US$ 780/tahun (Amri, 2008).
Dengan memanfaatkan cangkang udang menjadi chitin dan chitosan dapat
dijadikan sebagai pengawet alami untuk berbagai produk makanan, sayur-sayuran,
dan buah-buahan. Tentu saja ini sangat menguntungkan karena bernilai ekonomi
2.3. Chitosan
2.3.1. Pengertian Chitosan
Gambar 2.1 Serbuk Chitosan
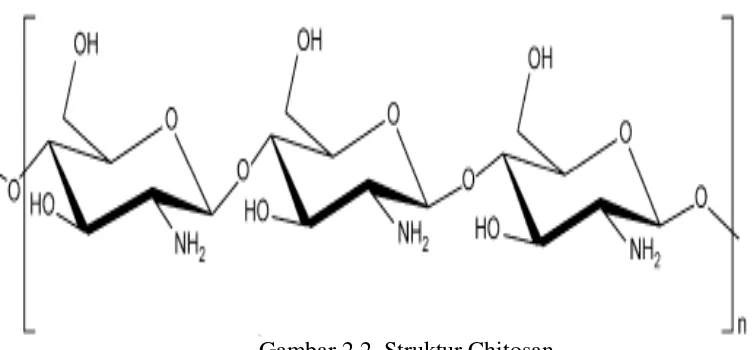
Chitosan yaitu poly-D-glucosamine (tersusun lebih dari 1000 unit glukosamin
dan asetilglukosamin) dengan berat molekul lebih dari satu juta ton, merupakan
dietary fiber (serat yang bisa dimakan) kedua setelah selulosa. Chitosan mempunyai
nama lain selain Chitin yaitu Chitosan Askorbat, NCarboxybutyl Chitosan. Chitosan
diketahui baik untuk kemampuan antimikrobakteri. Volume produksinya di alam
bebas menempati peringkat kedua setelah serat (Swastawati, 2008).
Diketahui bahwa Senyawa ini dapat ditemukan pada cangkang udang,
kepiting, mollusca, serangga, annelida serta beberapa dinding sel jamur dan alga.
Hasil modifikasi chitosan menghasilkan sifat dan manfaat yang spesifik. Secara
komersial telah menghasilkan inovasi diberbagai bidang seperti; industri pangan,
kosmetika, pertanian, farmasi, pengolahan limbah dan penjernihan air (Purwaningsih,
Chitosan merupakan salah satu polisakarida kationik alami yang diperoleh
dari deasetilasi chitin yang banyak terdapat di alam. Chitin dapat diperoleh dari
crustacean atau berbagai fungi. Chitin merupakan bentuk molekul yang hampir sama
dengan selulosa, yaitu suatu bentuk polisakarida yang dibentuk dari molekul-molekul
glukosa sederhana yang identik (Setyasih, 2009).
Marganof (2002) menjelaskan bahwa chitin merupakan polimer linier yang
tersusun oleh 2000-3000 monomer n-asetil D-glukosamin dalam ikatan ß(1-4) atau
2-asetamida-2-deoksi-D-glukopiranol dengan rumus molekul (C8H13NO5)n. Chitin
mudah mengalami degradasi secara biologis, tidak beracun, tidak larut dalam air,
asam anorganik encer, dan asam-asam organik, tetapi larut dalam larutan dimetil
asetamida dan litium klorida.
Gambar 2.2. Struktur Chitosan
2.3.2. Tahapan Pembuatan Chitin dan Chitosan
Reaksi pembentukan chitosan dari chitin merupakan reaksi hidrolisa suatu
amida oleh suatu basa. Chitin bertindak sebagai amida dan NaOH sebagai
basanya.Mula-mula terjadi reaksi adisi, dimana gugus OH- masuk ke dalam gugus
NHCOCH3 kemudian terjadi eliminasi gugus CH3COO- sehingga dihasilkan suatu
amida yaitu chitosan (Swastawati, 2008).
Chitin merupakan poli (2-asetamido-2-deoski-β-(1->4)-D-glukopiranosa)
yang paling melimpah di alam setelah selulosa. Chitin tidak beracun dan bahkan
mudah terurai secara hayati (biodegradable). Bentuk fisiknya merupakan padatan
amorf yang berwarna putih. Keberadaan chitin di alam umumnya terikat dengan
protein, mineral, dan berbagai macam pigmen (Sugita, 2009). Chitin banyak dijumpai
pada jamur, crustacea, insecta, mollusca dan arthropoda. Dalam cangkang udang,
Chitin terdapat sebagai mukopoli sakarida yang berikatan dengan garam-garam
anorganik, terutama kalsium karbonat (CaCO3), protein dan lipida termasuk
pigmen-pigmen (Wardaniati, 2009).
Chitosan adalah senyawa organik turunan chitin, berasal dari biomaterial
chitin yang dapat diperoleh dari deasetilasi chitin. Bentuk fisiknya merupakan
padatan amorf yang berwana putih kekuningan ( Sugita, 2009). Untuk memperoleh
chitin dari cangkang udang melibatkan proses deproteinasi ( penghilangan protein)
dan demineralisasi ( penghilangan mineral). Sedangkan untuk mendapatkan chitosan
dilanjutkan dengan proses deasetilasi ( penghilangan gugus asetil) (Ferdiansyah,
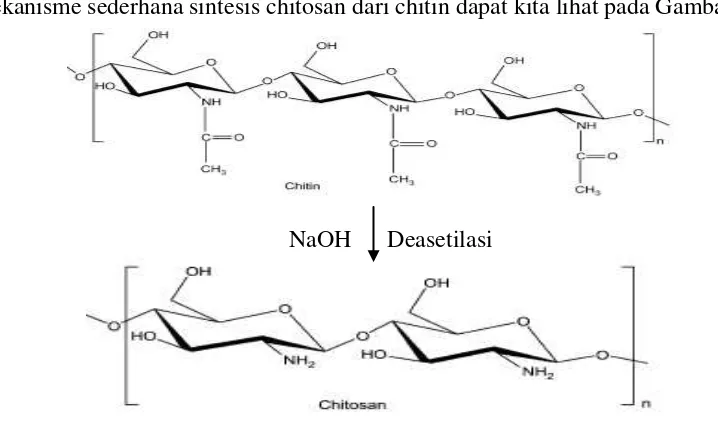
Mekanisme sederhana sintesis chitosan dari chitin dapat kita lihat pada Gambar 2.3.
NaOH Deasetilasi
Gambar 2.3. Mekanisme Sederhana Sintesis Chitosan Dari Chitin
Sumber : Shahidi. (1999). Aplication of Chitin and Chitosan. Trends in Food Science and Technology. vol 10, no 2.
Deproteinasi chitin merupakan reaksi hidrolisi dalam suasana asam dan basa.
Umumnya hidrolisis dilakukan dalam suasana basa dengan menggunakan larutan
NaOH. Demineralisasi secara umum dilakukan dengan larutan HCL atau asam lain
seperti H2SO4 pada kondisi tertentu. Keefektifan HCL dalam melarutkan kalsium
10% lebih tinggi daripada H2SO4. Hal yang terpenting dalam tahap penghilangan
mineral adalah jumlah asam yang digunakan. Secara stoikiometri, perbandingan
antara padatan dan pelarut dapat dibuat sama atau dibuat berlebih pelarutnya agar
reaksinya berjalan sempurna. Urutan deproteinasi dan demineralisasi juga berperan
penting. Deproteinasi sebaiknya dilakukan lebih dahulu jika protein yang terlarut
akan dimanfaatkan lebih lanjut. Deproteinasi pada tahap awal dapat
memaksimumkan hasil dan mutu protein serta mencegah kontaminasi protein pada
NaOH atau KOH. Deasetilasi chitin akan menghilangkan gugus asetil dan
menyisakan gugus amino yang bermuatan positif, sehingga chitosan akan bersifat
polikationik. Semakin banyak gugus asetil yang hilang dari polimer chitin, interaksi
antar ion dan ikatan hidrogen dari chitosan akan semakin kuat (Wardaniati, 2011).
Diagram Alir Pembuatan Chitosan
Cangkang Udang
- Cuci air dingin - Cuci air panas
- Dikeringkan dan dihaluskan
- Direndam dalam larutan NaOH 1M perbandingan 1:5 (g rserbuk/ml NaOH) diaduk 1 jam
- Dipanaskan 90°C selama 1 jam
- Didinginkan dan dicuci dengan air sampai pH netral - Dikeringkan
- Cangkang udang berupa serbuk hasil deproteinasi direndam dalam larutan HCL 1M perbandingan 1:10 (gr serbuk/ml NaOH) diaduk 1 jam
- Dipanaskan 90°C selama 1 jam - Didinginkan dan disaring
- Dicuci dengan air sampai pH netral - Dikeringkan
-2.3.3. Sifat Fisik dan Kimia Chitosan
Sifat dan penampilan produk chitosan dipengaruhi oleh perbedaan kondisi,
seperti jenis pelarut, konsentrasi, waktu, dan suhu proses ekstraksi. Chitosan
berwarna putih kecoklatan. Chitosan dapat diperoleh dengan berbagai macam bentuk
morfologi diantaranya struktur yang tidak teratur, bentuknya kristalin atau
semikristalin. Selain itu dapat juga berbentuk padatan amorf berwarna putih dengan
struktur kristal tetap dari bentuk awal chitin murni (Haliman, 2008).
Chitin memiliki sifat biologi dan mekanik yang tinggi diantaranya adalah
biorenewable, biodegradable, dan biofungsional. Chitosan mempunyai rantai yang
lebih pendek daripada rantai chitin. Kelarutan chitosan dalam larutan asam serta
viscositas larutannya tergantung dari derajat deasetilasi dan derajat degradasi polimer.
Terdapat dua metode untuk memperoleh chitin , chitosan dan oligomernya dengan
berbagai DD, polimerisasi, dan berat molekulnya (BM) yaitu dengan kimia dan
enzimatis (Ramadhan,dkk,2010).
Suatu molekul dikatakan chitin bila mempunyai derajat deasetilasi (DD)
sampai 10% dan kandungan nirogennya kurang dari 7%. Dan dikatakan chitosan bila
nitrogen yang terkandung pada molekulnya lebih besar dari 7% berat dan DD lebih
dari 70% (Zainab, 2010).
Chitosan kering tidak mempunyai titik lebur. Bila disimpan dalam jangka
waktu yang relatif lama pada suhu sekitar 100°F maka sifat keseluruhannya dan
viskositasnya akan berubah. Bila chitosan disimpan lama dalam keadaan terbuka
berkurang. Suatu produk dapat dikatakan chitosan jika memenuhi beberapa standar
seperti tertera pada Tabel 2.1
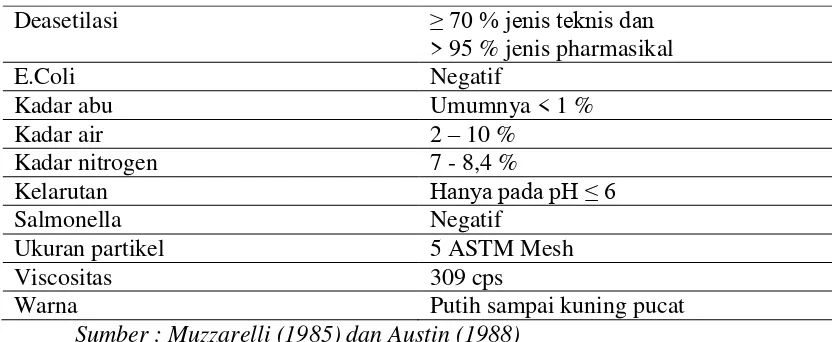
Tabel 2.1. Standard Chitosan
Deasetilasi ≥ 70 % jenis teknis dan
> 95 % jenis pharmasikal
Warna Putih sampai kuning pucat
Sumber : Muzzarelli (1985) dan Austin (1988)
Dua faktor utama yang menjadi ciri dari chitosan adalah viskositas atau berat
molekul dan derajat deasetilasi. Oleh sebab itu, pengendalian kedua parameter
tersebut dalam proses pengolahannya akan menghasilkan chitosan yang bervariasi
dalam penerapannya di berbagai bidang. Misalnya kemampuan chitosan membentuk
gel dalam N-methyl morpholine-N-oxide, belakangan ini telah dimanfaatkan untuk
formulasi obat. Derajat deasetilasi dapat didefinisikan sebagai rasio
2-amino-2-deoxy-D-glucopiranosa dan 2-acetamido-2-deoxy-D-glukopyranose, dan
menunjukkan sejauh mana proses deasetilasi berjalan. Derajat deasetilasi dan berat
molekul berperan penting dalam kelarutan chitosan, sedangkan derajat deasetilasi
sendiri berkaitan dengan kemampuan chitosan untuk membentuk interaksi isoelektrik
Chitosan dapat dapat berinteraksi dengan bahan-bahan yang bermuatan,
seperti protein, polisakarida, anionik, asam lemak, asam empedu dan fosfolipid.
Chitosan larut asam dan larut air mempunyai keunikan membentuk gel yang stabil
dan mempunyai muatan dwi kutub, yaitu muatan negatif pada gugus karboksilat dan
muatan positif pada gugus NH (Rokhati, 2006).
Menurut Wibowo (2006), kelarutan chitosan dipengaruhi oleh tingkat
ionisasinya, dan dalam bentuk terionisasi penuh, kelarutannya dalam air meningkat
karena adanya jumlah gugus yang bermuatan. Sebagai antibakteri, chitosan memiliki
sifat mekanisme penghambatan, dimana chitosan akan berikatan dengan protein
membran sel, yaitu glutamat yang merupakan komponen membran sel. Selain
berikatan dengan protein membraner, chitosan juga berikatan dengan fosfolipid
membraner, terutama fosfatidil kolin (PC), sehingga meningkatkan permeabilitas
inner membran (IM). Naiknya permeabilitas IM akan mempermudah keluarnya
cairan sel. Pada E. coli misalnya, setelah 60 menit, komponen enzim ß galaktosidase
akan terlepas. Hal ini menunjukkan bahwa sitoplasma dapat keluar sambil membawa
metabolit lainnya, atau dengan kata lain mengalami lisis, yang akan menghambat
pembelahan sel (regenerasi). Hal ini akan menyebabkan kematian sel (Fahmi, 1997).
2.3.4. Manfaat Chitosan
Chitosan telah digunakan secara luas di industri makanan, kosmetik,
kesehatan, farmasi dan pertanian serta pada pengolahan air limbah. Di industri
makanan, chitosan dapat digunakan sebagai suspensi padat, pengawet, penstabil
warna, penstabil makanan, bahan pengisi, pembentuk gel, tambahan makanan hewan
Chitosan dan chitin mempunyai potensi yang dapat digunakan baik pada
berbagai jenis industri maupun pada bidang kesehatan. Sebagai contoh, untuk
penjernihan air diperlukan mutu chitin dan chitosan yang tinggi sedangkan untuk
penggunaan di bidang kesehatan diperlukan kemurnian yang tinggi (Sari,2008).
Chitosan dan turunannya telah menarik perhatian sebagai bahan untuk
digunakan dalam bidang obat-obatan dan kesehatan. Chitin dan Chitosan
menunjukkan aktivitas antibakteri, antimetastik, antiurikemik dan antiosteoporotik
menunjukkan potensi yang besar dalam meredakan dan mencegah penyakit atau
memberi kontribusi terhadap kesehatan yang baik. Material yang dapat terurai dan
nontoksik dapat mengaktifkan pasien menahan mencegah infeksi dan mempercepat
penyembuhan luka ( Kaban, 2009).
Di industri makanan, chitosan dapat digunakan sebagai suspensi padat,
pengawet, penstabil warna, penstabil makanan, bahan pengisi, pembentuk gel,
pembentuk tekstur, pengental dan pengemulsi produk olahan pangan , flavor, zat gizi
antimikroba, antijamur dan sebagainya ( Haliman, 2010).
Di dalam pangan chitosan dapat dijadikan sebagai bahan antimikroba untuk
memperpanjang waktu penyimpanan makanan karena chitosan mengandung enzim
lysosim dan gugus aminopolysacharida yang dapat menghambat pertumbuhan
mikroba ( Wardaniati, 2009).
Fungsinya sebagai antimikroba dan antijamur juga diterapkan dibidang
kedokteran. Chitin dan chitosan dapat mencegah pertumbuhan Candida albicans dan
Staphvcoccus aureus. Selain itu, biopolimer tersebut juga berguna sebagai
pembuat lensa kontak, aditif kosmetik, membran dialisis, bahan shampoo dan
kondisioner rambut, zat hemostatik, penstabil liposom, bahan ortopedik, pembalut
luka dan benang bedah yang mudah diserap, serta mempertinggi daya kekebalan
antiinfeksi. Sementara di bidang pertanian chitin dan chitosan digunakan antara lain
untuk pencampur ransum pakan ternak, pestisida, herbisida, virusida tanaman, dan
deasidifikasi buah-buahan, sayuran dan penjernih sari buah ( Sugita, 2009).
Chitosan diketahui dapat menginduksi respons ketahanan tanaman terhadap
infeksi patogen (Hadrami et al. 2010). Selain itu, chitosan dapat digunakan untuk
pelapis buah tomat (Sari, 2008) dan leci (Dong et al. 2004). Chitosan dapat
menginduksi enzim kitinase yang dapat mendegradasi chitin, yang merupakan
penyusun utama dinding sel cendawan sehingga dapat digunakan sebagai fungisida
(Ghaouth et al. 1991). Menurut Pamekas (2009), chitosan mampu menghambat
pertumbuhan Colletotrichum musae melalui penghambatan perkecambahan
konidium, memperkecil lebar hifa, memperpendek ruas hifa, dan menyebabkan hifa
lisis.
Perlakuan chitosan secara umum mampu menekan infeksi C. gloeosporioides
secara in vitro dengan THR yang semakin meningkat seiring dengan meningkatnya
konsentrasi chitosan yang digunakan. Hal ini sejalan dengan hasil penelitian Rogis et
al. (2007) yang menyebutkan bahwa semakin tinggi konsentrasi chitosan yang
digunakan maka semakin besar pula penghambatan terhadap pertumbuhan C. musae.
Secara in vivo, konsentrasi chitosan yang efektif untuk menekan kejadian dan
Chitosan sebagai pelapis pada permukaan buah pepaya dapat menghambat
proses respirasi pada tingkat yang sangat rendah. Respirasi rendah dapat
mengakibatkan pemecahan pati termasuk gula berjalan lambat sehingga semakin
rendah respirasi buah maka proses kematangan buah semakin lambat (Suhardjo,
1992). Daya simpan buah menunjukkan besarnya potensi pemanfaatan kitosan dalam
mendukung peningkatan kualitas dan kuantitas buah-buah yang diekspor dari
Indonesia.
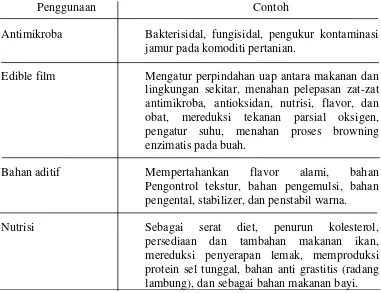
Tabel 2.2. Penggunaan Chitosan dan Turunannya Dalam Industri Pangan
Penggunaan Contoh
Antimikroba Bakterisidal, fungisidal, pengukur kontaminasi jamur pada komoditi pertanian.
Edible film Mengatur perpindahan uap antara makanan dan lingkungan sekitar, menahan pelepasan zat-zat antimikroba, antioksidan, nutrisi, flavor, dan obat, mereduksi tekanan parsial oksigen, pengatur suhu, menahan proses browning enzimatis pada buah.
Bahan aditif Mempertahankan flavor alami, bahan Pengontrol tekstur, bahan pengemulsi, bahan pengental, stabilizer, dan penstabil warna.
2.3.5. Kualitas Chitosan
Chitosan merupakan salah satu biomaterial yang paling menjanjikan untuk
menggantikan bahan sintetis, terutama untuk makanan dan aplikasi kemasan.
Chitosan merupakan polycation yang kepadatan muatan tergantung pada derajat
deasetilasi dan pH. Dengan kualitas chitosan yang baik maka juga akan mendapatkan
chitosan yang memiliki keunggulan dibandingkan biomaterial lain, karena pada
chitosan ini sangat antimikroba. Edible film yang terbuat dari chitosan memiliki daya
tarik yang baik dengan adanya alkilasi. Diketahui bahwa edible film dari chitosan ini
memiliki kecenderungan untuk mengkarakterisasi chitosan sebagai bakteriostatik
daripada bakterisida (Fahmi, 1997).
Kualitas chitosan yang baik memiliki pH rendah dengan pH kurang lebih 6,3.
Keunggulan chitosan ialah antimikroba dan didapatkan dari sifat permeabilitas pada
dinding membran, sehingga terjadi ketidakseimbangan osmotik internal dan
akibatnya menghambat pertumbuhan mikroorganisme. Chitosan edible film
merupakan sifat penghalang yang baik terhadap gas dan lipid tetapi kurang baik
apabila untuk menghalangi uap air. Alkilasi adalah suatu bahan yang dapat
mengurangi rantai dalam dan luar hydrogen, mengelastiskan molekul dan
meningkatkan daya tahan terhadap uap air. Dalam edible film chitosan ini,
mengandung gliserol yang akan menghasilkan edible film dengan kemampuan
rentang yang tinggi dan meningkatkan tingkat permeabilitas (baik oksigen dan air).
Chitosan edible film ini telah terbukti efektif dalam meningkatkan umur simpan dari
2.4. Chitosan Tidak Berbahaya Untuk Dikonsumsi
Chitosan adalah serbuk yang dihasilkan dari deasetilasi chitin, senyawa yang
banyak diperoleh di kerangka luar (eksoskeleteon) hewan Crustacea seperti udang,
kerang, dan kepiting (Rhamnosa, 2006). Serbuk yang telah dilepaskan asetilnya
merupakan zat murni, tinggi sifat basanya, serta mengandung banyak molekul
glukosa. Dalam chitosan terdapat unsur butylosar yang bermanfaat bagi tubuh
manusia. Butylosar yang telah didapatkan itu hanya larut dalam asam encer dan
cairan tubuh manusia. Dengan demikian, butylosar dapat diserap oleh tubuh. Zat itu
merupakan satu-satunya selulosa yang dapat dimakan. Zat ini mempunyai muatan
positif yang kuat, dan dapat mengikat muatan negatif dari senyawa lain. Selain itu,
zat ini mudah mengalami degradasi secara biologis dan tidak beracun ( Purwanti,
2010).
Selain telah memenuhi standard secara mikrobiologi ditinjau dari segi
kimiawi juga aman karena dalam prosesnya chitosan cukup dilarutkan dengan asam
asetat encer (1%) hingga membentuk larutan chitosan homogen yang relatif lebih
aman ( Wardaniati, 2009).
Masalah utama yang dihadapi dalam memproduksi chitin dan chitosan di
Indonesia adalah kualitas produk masih rendah, kontinuitas suplainya belum pasti dan
belum bisa diakses oleh semua kalangan . Selain itu banyak masyarakat yang belum
mengetahui fungsi dari chitin-chitosan ( Swastawati, dkk, 2008).
Jurnal Jonathan Rhodes dan Bob Rastall menyebutkan tentang paten produk di
Rusia yang menggunakan chitosan sebagai pengawet untuk kaviar, yang dinyatakan
2006). Di Indonesia produksi chitosan dalam skala relatif besar mulai diujicobkan CV
Dinar yang berlokasi di sebuah kawasan nelayan di Jl. Raya Dadap, Tangerang
Banten ( Anonimous, 2006).
2.5. Stroberi (Fragaria x ananassa Duch)
2.5.1. Asal Usul Buah Stroberi (Fragaria x ananassa Duch)
Gambar 2.4 Buah Stroberi
Wilhelm dan Sagen (1974) menerangkan pada bukunya bahwa, stroberi
merupakan jenis tanaman berbunga dalam keluarga mawar Rosaceaea, berwarna
merah dan buahnya dapat dikonsumsi, dan dikembang biakkan dengan baik di daerah
Amerika Utara. Dalam bahasa latin buah ini disebut Fragra yang berarti wangi.
Charles Linneans lah orang pertama yang memberikan nama spesies Fragaria untuk
buah ini. Di Perancis, Italia, dan Spanyol buah ini disebut Fraise yang juga memiliki
makna yang sama yaitu wangi, sementara di Amerika Utara disebut buah
Wuttahimheash atau berry hati (Budiman, 2006).
Stroberi pertama kali digambarkan dalam literatur sekitar 1000 AD, dan
terjadi antara 234-149 SM dalam tulisan-tulisan Cato, Senator Romawi. Stroberi
tumbuh liar di Italia sejak 234 SM dan ditemukan di Virginia oleh orang Eropa
pertama ketika kapal mereka mendarat di sana pada 1588. Pada zaman Yunani kuno
buah ini diangkat sebagai lambang dewi cinta (Rukmana, 1998).
Etimologi dari asal-usul nama stroberi, di antaranya dari kata straw(sedotan),
sebagai gambaran dari kegiatan tukang kebun yang menggunakan sedotan untuk
menanam buah ini dan melindunginya dari proses pembusukan, juga dari jaman
Anglo-Saxon dari kata strew (menyebar di sekelilingnya). Deskripsi pertama kali
menggambarkannya untuk penggunaan tanaman obat dan bukan untuk manfaat buah.
Untuk Periode waktu abad ke-12 Saint Hildegard von Binger, seorang kepala
biara, berpendapat bahwa stroberi tidak cocok untuk dimakan, fakta bahwa mereka
tumbuh dekat dengan tanah dan mungkin terkontaminasi oleh hewan ular atau katak.
Bersama dukungan teorinya dan beberapa tokoh politik lokal, banyak orang
menghindari buah ini dan popularitasnya terus menurun ( Budiman, 2006).
Pada awal 1600, koloni pertama Amerika membawa buah ini ke Amerika.
Tanaman Stroberi yang ditemukan di Amerika Utara terkenal lebih unggul dari
varietas Eropa dalam ukuran, rasa, dan keindahan. Stroberi mulai dijual bebas di
pasar London sekitar 1831. Kebanyakan di panen dari ladang terdekat atau hutan, dan
bukan dari area produksi komersil. Di Inggris dan daratan Eropa konsumsi stroberi
menjadi lebih populer. Mulai dari kalangan rakyat biasa hingga aristokrat memiliki
lahan kecil di rumah mereka untuk menanam tumbuhan ini. Sementara Perancis
Setelah 1860 stroberi banyak ditanam dan di budidayakan di California ,dan
sejak 1900 stroberi mulai ditanam diberbagai negara. Hari ini lebih dari 25.000 hektar
stroberi ditanam di Amerika Utara,dan 80 % di Amerika Serikat (Rukmana, 1998).
2.5.2. Klasifikasi Buah Stroberi
Klasifikasi botani tanaman stroberi adalah sebagai berikut (Budiman, 2006) :
Divisi : Spermatophyta Sub divisi : Angiospermae Kelas : Dicotyledonae Keluarga : Rosaceae Genus : Fragaria Spesies : Fragria spp
(Dikutip dari : GRIN Taxonomy Database, 2008).
Varitas stroberi introduksi yang dapat ditanam di Indonesia adalah
Osogrande, ePajero, Selva, Ostara, Tenira, Robunda, Bogota, Elvira, Grella, Red
Gantle, Dorit dan Sweet Charlie.
2.5.3. Anatomi Buah Stroberi
Anatomi dari tanaman stroberi adalah sebagai berikut (Rukmana, 1998) :
1. Akar (Radix)
Struktur akar tanaman stroberi terdiri atas pangkal akar (collum), batang akar
(corpus), ujung akar (apex), bulu akar (pilus radikalis), dan tudung akar (calyptras).
Tanaman stroberi berakar tunggang (radix primaria), akarnya terus tumbuh
tersebut hanya menembus lapisan tanah atas sedalam 15 cm-45 cm tergantung jenis
dan kesuburan tanahnya.
2. Batang (Caulis)
Batang tanaman stroberi beruas-ruas pendek dan berbuku-buku, banyak
mengandung air, serta tertutupi pelepah daun tampak seperti rumpun tanpa batang.
Buku-buku batang yang tertutup oleh sisi daun mempunyai kuncup.
3. Cabang Merayap (Stolon)
Stolon adalah cabang kecil yang tumbuh mendatar atau menjalar di atas
permukaan tanah. Penampakan stolon secara visual mirip dengan sulur. Tunas dan
akar stroberi tumbuh membentuk generasi tanaman baru. Stolon yang tumbuh
mandiri dapat segera dipotong atau dipisahkan dari rumpum induk sebagai bibit.
4. Daun (Folium)
Daun tanaman stroberi tersusun pada tangkai yang berukuran agak panjang,
tangkai daun berbentuk bulat, helai daun bersusun tiga. Bagian tepi daun bergerigi,
berwarna hijau, dan berstruktur tipis. Daun dapat bertahan hidup selama 1-3 bulan,
kemudian daun akan kering dan mati.
5. Bunga (Flos)
Stroberi berbunga sempurna. Struktur bunga terdiri Dari 5 kelopak, 5 daun
mahkota, dan ratusan putik.Setiap mahkota bercabang daun mempunyai empat
macam bunga, yaitu 1 bunga primer, 2 buah bunga sekunder, 4 buah tersier.
6. Buah (Fructus)
Buah stroberi umumnya berbentuk kerucut hingga bulat, buah yang tampak
berubah bentuk menjadi gumpalan daging buah. Buah muda berwarna hijau namun
setelah tua berubah menjadi berwarna merah atau kuning kemerah-merahan.
7. Biji
Biji stroberi berukuran kecil. Biji itu berukuran kecil,terletak dia antara
daging buah .
2.5.4. Spesies Buah Stroberi
Stroberi memiliki lebih dari 20 spesies dan 700 jenis Ada tujuh jenis
kromosom utama yang terdapat di seluruh spesies. Beberapa spesies adalah diploid
yaitu mempunyai dua pasang dari ketujuh kromosom menjadikan jumlahnya 14
kromosom. Yang lainnya merupakan tetraploid yaitu memiliki empat pasang dari
ketujuh kromosom menjadikan jumlahnya 28 kromosom, hexaploid (6 pasang),
oktoploid (8 pasang) atau dekaploid (10 pasang) (Rukmana, 1998).
2.6. Kandungan Buah Stroberi 2.6.1. Senyawa Fitokimia
Sesuai dengan namanya, senyawa fitokimia merupakan senyawa spesifik yang
terdapat pada jenis tanaman tertentu (fito= tanaman) dengan manfaat yang juga
sangat spesifik. Beberapa senyawa fitokimia yang terdapat pada buah stroberi adalah
(Budiman, 2006).
1. Anthocyanin
Anthocyanin tergolong dalam komponen flavonoid. Senyawa ini merupakan
2. Ellagic Acid
Ellagic acid merupakan persenyawaan fenolik alamiah yang ditemukan pada
beberapa famili tanaman, seperti Rosaceae, Fagaceae, Saxifragaceae, Cunomirutceae
dan Myrotharnnaceae. Jenis tanaman yang banyak mengandung ellagic acid di
antaranya stroberi dan apel. Pada stroberi, senyawa tersebut terdapat pada bagian biji,
daun, dan daging buah.
3. Catechin,Quercetin,dan Kaempferol
Selain ellagic acid, senyawa folifenol lain yang memiliki aktivitas sebagai
antioksidan adalah cateehin, quer-cetin, dan kaempferoL.
2.6.2. Antioksidan
Antioksidan dapat didefinisikan sebagai suatu zat yang dapat menghambat /
memperlambat proses oksidasi. Oksidasi adalah jenis reaksi kimia yang melibatkan
pengikatan oksigen, pelepasan hydrogen, atau pelepasan elektron. Proses oksidasi
adalah peristiwa alami yang terjadi di alam dan dapat terjadi dimana-mana tak
terkecuali di dalam tubuh (Sari, 2008).
2.6.3. Vitamin & Mineral
Vitamin dan mineral yang terdapat di dalam buah stroberi ( Budiman, 2006).
1. Vitamin C
Vitamin C adalah salah satu jenis vitamin yang larut dalam air dan memiliki
peranan penting dalam menangkal berbagai penyakit. Vitamin ini juga dikenal
dengan nama kimia dari bentuk utamanya yaitu asam askorbat. Dalam setiap 100 mg
dibandingkan buah jeruk atau orange. Vitamin C sangat bermanfaat sebagai melawan
infeksi.
2. Vitamin A
Vitamin A adalah vitamin yang dibutuhkan oleh retina mata yang mana
molekulnya menyerap cahaya retina, dan mutlak diperlukan untuk melihat
kedua-cahaya (low scotopic visi) dan penglihatan warna. Dalam 100 gram buah stroberi
mengandung 60 Sl vitamin A.
3. Vitamin B1
Vitamin B1, atau tiamina, adalah vitamin yang terlarut dalam air.Tiamina
disintesis dalam bakteri, fungi dan tanaman. Tiamina berperan sangat vital agar otak
dapat bekerja dengan normal. Dalam 100 mg stroberi mengandung 0,03 mg Vitamin
B1.
4. Mineral
Mineral potensial yang ada di dalam 100 gram buah stroberi adalah 28 mg
kalsium, 27 mg fosfor, 0,8 mg zat besi, 10 mg magnesium, 27 mg potassium, dan 0,7
mg selenium.
Buah stroberi mempunyai kandungan gizi yang tinggi dan komposisi gizi
yang cukup lengkap. Kalori sebanyak 37,00 kal, protein 0,80 g, lemak 0,50 g,
karbohidrat 8,30 g, kalsium 28,00 mg, fosfor 27,00 g, zat besi 0,80mg, vitamin A
60,00 SI, vitamin B1 0,03 mg, vitamin C 60,00 mg, air 89,90 g, bagian yang dapat
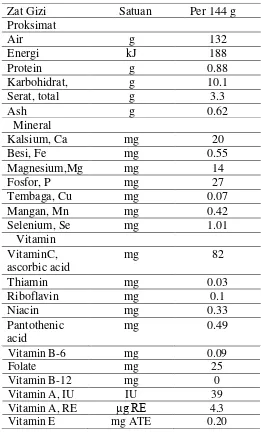
Satu cangkir (144 g) stroberi mengandung sekitar 45 kalori (188 kJ) dan
merupakan sumber vitamin C dan flavonoid yang baik. Berikut ini beberapa
kandungan Gizi dalam satu cangkir (144 g) stroberi dapat dilihat pada tabel 2.3
2.7. Kerusakan pada Buah Stroberi
Kerusakan buah dapat terjadi sejak buah dipanen hingga proses penyimpanan.
Beberapa proses kerusakan yang terjadi pada buah antara lain (Ghaout, 1991).
a. Browning (Pencoklatan)
Proses pencoklatan atau browning sering terjadi pada buah-buahan, seperti
pisang, pir, salak, pala dan apel begitu juga stroberi. Buah stroberi yang memar juga
akan mengalami proses pencoklatan. Pada umumnya, proses pencoklatan dapat
dibagi menjadi dua, yaitu proses pencoklatan enzimatik dan non enzimatik.
Perubahan warna yang utama pada stroberi disebabkan oleh reaksi browning
(pencoklatan). Reaksi pencoklatan terdiri atas pencoklatan enzimatis dan non
enzimatis. Pencoklatan enzimatis disebabkan oleh aktivitas enzim phenolase dan
oliphenolase. Pada buah stroberi utuh, sel-selnya masih utuh, dimana substrat yang
terdiri atas senyawa-senyawa fenol terpisah dari enzim phenolase sehingga tidak
terjadi reaksi browning. Apabila sel pecah akibat terjatuh/memar atau terpotong
(pengupasan, pengirisan) substrat dan enzim akan bertemu pada keadaan aerob
(terdapat oksigen) sehingga terjadi reaksi browning enzimatis.
Pembentukan warna coklat dikarenakan terjadinya oksidasi senyawa-senyawa
fenol dan polifenol oleh enzim fenolase dan polifenolase membentuk quinon, yang
selanjutnya berpolimerisasi membentuk melanin (pigmen berwarna coklat).
b. Loss Mass (Penyusutan Massa)
Susut (losses) kualitas dan kuantitas dapat terjadi sejak pemanenan hingga
saat dikonsumsi. Besarnya susut sangat tergantung pada jenis komoditi dan cara
(1) mengetahui faktor biologis dan lingkungan yang berpengaruh terhadap terjadinya
kerusakan, (2) menguasai teknik penanganan pasca panen yang dapat menunda
kelayuan atau kebusukan dan menjaga kualitas pada tingkatan tertentu yang mungkin
dicapai.
c. Laju Respirasi dan Produksi Etilen yang Tinggi
Respirasi adalah proses pemecahan komponen organik (zat hidrat arang,
lemak dan protein) menjadi produk yang lebih sederhana dan energi. Aktivitas ini
ditujukan untuk memenuhi kebutuhan energi sel agar tetap hidup. Berdasarkan
polanya, proses respirasi dan produksi etilen selama pendewasaan dan pematangan
produk nabati dapat dibedakan menjadi dua, yaitu klimakterik dan non-klimakterik.
Komoditi dengan laju respirasi tinggi akan menunjukkan kecenderungan lebih
cepat rusak. Menurunkan laju respirasi sampai batas minimal pemenuhan kebutuhan
energi sel tanpa menimbulkan fermentasi akan dapat memperpanjang umur ekonomis
produk nabati. Manipulasi faktor ini dapat dilakukan dengan teknik pelapisan
(coating), penyimpanan pada suhu rendah, atau memodifikasi atmosfir ruang
penyimpan.
Setelah dipanen, stroberi masih terus melakukan respirasi dan metabolisme,
karena itulah komoditi tersebut dianggap masih hidup. Selama proses respirasi dan
metabolisme berlangsung, buah akan mengeluarkan CO2 dan air serta etilen, serta
mengkonsumsi oksigen yang ada disekitarnya.
d. Laju Transpirasi yang Tinggi
Transpirasi adalah pengeluaran air dari dalam jaringan produk nabati. Laju
terhadap volume, kerusakan fisik, umur panen) dan faktor eksternal (suhu, RH,
pergerakan udara dan tekanan atmosfir). Transpirasi yang berlebihan akan
menyebabkan produk mengalami pengurangan berat, penurunan daya tarik (karena
layu), nilai tekstur dan nilai gizi. Pengendalian laju transpirasi dilakukan dengan
pelapisan, penyimpanan dingin, atau memodifikasi atmosfir (Ebook Pangan, 2006).
e. Sensitivitas Terhadap Suhu
Pemaparan komoditi pada suhu yang tidak sesuai akan menyebabkan
kerusakan fisiologis pada stroberi yang bisa berupa : (1) freezing injuries, karena
produk disimpan di bawah suhu bekunya; (2) chilling injuries, umum pada produk
tropis yang disimpan di atas suhu beku dan diantara 5 – 15ºC, tergantung sensitivitas
komoditi; (3) heat injuries, terjadi karena paparan sinar matahari atau panas yang
berlebihan. Berdasarkan sensitivitasnya terhadap suhu, dikenal dua golongan produk,
yaitu yang bersifat sensitif dan tidak sensitif terhadap pendinginan. Suhu kritis
stroberi berkisar antara 36 – 38°C jika disimpan melebihi suhu tersebut kerusakan
yang dapat terjadi berupa pencoklatan di bagian dalam, bagian tengah coklat, lembek
dan lepuh.
2.8. Mekanisme Kimia Pengawetan Stroberi Dengan Chitosan
Metode yang digunakan untuk memperpanjang umur simpan buah stroberi
adalah salah satunya dengan pemberian chitosan yang akan membentuk lapisan tipis
atau yang disebut dengan coating. Pemberian lapisan tipis pada permukaan buah
untuk menghambat keluarnya gas, uap air dan menghindari kontak dengan oksigen,
sehingga proses pemasakan dan pencoklatan buah dapat diperlambat, merupakan
buah ini tidak berbahaya dan dapat ikut dikonsumsi bersama buah, salah satunya
adalah menggunakan chitosan. Menurut Ghaouth dkk (1991) dan Ramadhan (2010)
chitosan adalah salah satu bahan yang bisa digunakan untuk pelapisan buah, yang
merupakan polisakarida berasal dari limbah kulit udang, kepiting, dan yang termasuk
ke dalam Crustaceae. Chitosan merupakan suatu senyawa poli (N-amino-2 deoksi β
-D-glukopiranosa) atau glukosamin hasil deasetilasi kitin/poli (N-asetil-2
amino-2-deoksi β- D-glukopiranosa) yang diproduksi dalam jumlah besar di alam. Penggunaan
chitosan sebagai pelapis dalam buah-buahan dapat menghambat difusi oksigen ke
dalam buah sehingga proses respirasi dapat dihambat.
Chitosan sangat berpotensi untuk dijadikan sebagai bahan antimikroba, karena
mengandung enzim lysosimdan gugus aminopolysacharida yang dapat menghambat
pertumbuhan mikroba dan efisiensi daya hambat chitosan terhadap bakteri tergantung
dari konsentrasi pelarutan chitosan. Kemampuan dalam menekan pertumbuhan
bakteridisebabkan chitosan memiliki polikation bermuatan positif yang mampu
menghambat pertumbuhan bakteri dankapang (Zainab, 2010).
Mekanisme yang terjadi dalam pengawetan buah stroberi yaitu molekul
chitosan memiliki kemampuan untuk berinteraksi dengan senyawa pada permukaan
cell bakteri kemudian teradsorbi membentuk semacam layer (lapisan) yang
menghambat saluran transportasi sel sehingga sel mengalami kekurangan substansi
untuk berkembang dan mengakibatkan matinya sel. Sehingga dapat mencegah
hilangnya kelembaban produk, memiliki permeabilitas selektif terhadap gas tertentu,
alami dan bergizi, serta menjadi pembawa bahan aditif seperti pewarna, pengawet dan
penambah aroma yang dapat memperbaiki mutu bahan pangan (Donhowe, 1994).
Selain telah memenuhi standard secara mikrobiologi ditinjau dari segi
kimiawi juga aman karena dalam prosesnya chitosan cukup dilarutkan dengan asam
asetat encer (1%) hingga membentuk larutan chitosan homogen yang relative lebih
aman.Penggunaan coater pada buah segar dapat memperlambat penurunan mutu,
karena metode tersebut dapat digunakan sebagai penahan difusi gas oksigen,
karbondioksida dan uap air serta komponen flavor, sehingga mampu menciptakan
kondisi atmosfir internal yang sesuai dengan kebutuhan produk yang dikemas.
Keuntungan penggunaan coater untuk pelapis buah adalah dapat memperpanjang
umur simpan produk karena coater ini dapat dimakan bersama produk yang
dikemasnya (Rokhati, 2006).
Beberapa penelitian menyebutkan kemampuan film atau coating chitosan
dalam memperpanjang masa simpan dan mengendalikan kerusakan buah dan sayuran
dengan lebih baik, yaitu dengan cara menurunkan kecepatan respirasi, menghambat
pertumbuhan kapang, dan/atau menghambat pematangan dengan mengurangi
produksi etilen dan karbondioksida. Chitosan memiliki kemampuan untuk
membentuk film yang sesuai sebagai pengawet makanan dengan menghambat
patogen psikotrofik membuktikan bahwa coating chitosan (2% chitosan dalam 5%
asam asetat) mampu menghambat penurunan kandungan antosianin dan peningkatan
aktivitas polyphenol oksidase pada penyimpanan leci. Ghaouth dkk (1992) juga
melaporkan bahwa coating chitosan (1% dan 2 % dalam 0.25 N HCl) mengurangi
chitosan akan lebih keras dan lebih sedikit pigmentasi merah jika dibandingkan
dengan sampel kontrol, setelah disimpan selama 4 minggu pada suhu 20°C.
2.9. Kerangka Konsep
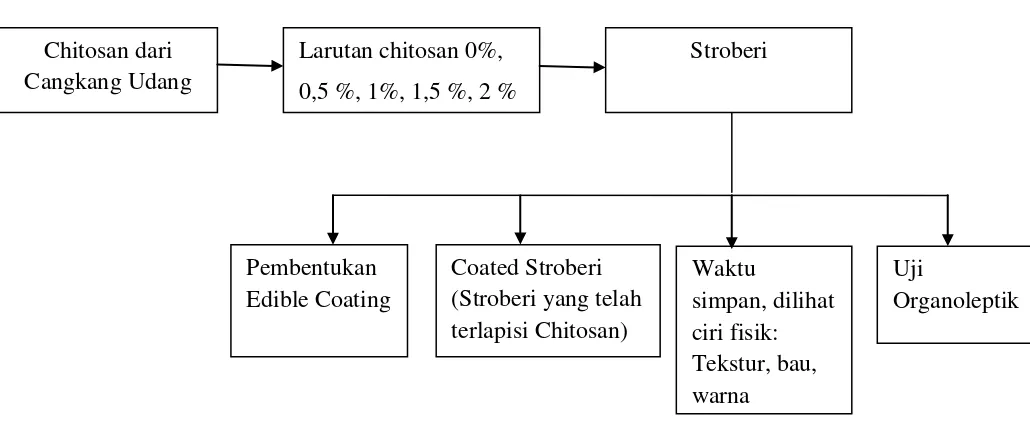
Gambar 2.5. Kerangka Konsep Penggunaan Chitosan Dari Cangkang Udang (Litopenaeus Vannamei) Sebagai Pengawet Alami Untuk Buah Stroberi (Fragaria x ananassa Duch)
Larutan chitosan 0%,
0,5 %, 1%, 1,5 %, 2 %
Stroberi
Pembentukan Edible Coating Chitosan dari
Cangkang Udang
Waktu
simpan, dilihat ciri fisik: Tekstur, bau, warna
Coated Stroberi (Stroberi yang telah terlapisi Chitosan)
Uji