MAKALAH SEMINAR KIMIA
Diajukan Sebagai Syarat dalam Menyelesaikan
Mata Kuliah Seminar Kimia
OLEH :
ARIYESSA DINANTIA
1205113125
PROGRAM STUDI PENDIDIKAN KIMIA
JURUSAN PENDIDIKAN MATEMATIKA DAN
IPA
FAKULTAS KEGURUAN DAN ILMU
PENDIDIKAN
UNIVERSITAS RIAU
PEKANBARU
2016
LEMBAR PENGESAHAN
MAKALAH SEMINAR KIMIA
MEKANISME REAKSI SINTESIS SALISILANILIDA DARI
BAHAN DASAR ASAM SALISILAT
Diajukan Sebagai Syarat dalam Menyelesaikan
Mata Kuliah Seminar Kimia
Oleh:
ARIYESSA DINANTIA
1205113125
Telah diseminarkan pada: 26 April 2016
DISETUJUI OLEH
Dosen Pembimbing/ Penguji I Dosen Pembimbing/ Penguji II
Dr. Susilawati, M.Si Dr. Rasmiwetti, MS
KATA PENGANTAR
Puji syukur kehadirat Allah SWT, yang telah melimpahkan rahmat karunia-Nya sehingga penulis dapat menyelesaikan penulisan makalah ini dengan judul “Mekanisme Reaksi Sintesis Salisilanilida Dari Bahan Dasar Asam Salisilat”. Makalah ini disusun guna menyelesaikan tugas mata kuliah seminar kimia.
Dalam penyusunan makalah ini penulis banyak mendapatkan arahan dan bimbingan serta petunjuk dari berbagai pihak. Untuk itu penulis mengucapkan terimakasih kepada:
1. Ibu Dr. Susilawati, M.Si dan Ibu Dr. Rasmiwetti, MS selaku dosen pembimbing dan dosen penguji yang telah memberikan nasehat dan bimbingan kepada penulis serta arahan dan bantuan dalam penulisan makalah ini.
2. Bapak/Ibu dosen staf pengajar program studi pendidikan kimia.
3. Kedua orang tua dan semua keluarga atas do’a dan motivasi yang telah diberikan.
4. Abang dan kakak senior pendidikan kimia yang selalu menyemangati penulis. 5. Teman-teman seperjuangan Kimia 2012 yang selalu menyemangati penulis. 6. Teman-teman seperjuangan SM Kelas B yang selalu memberikan motivasi.
Penulis menyadari bahwa makalah ini masih jauh dari kesempurnaan, maka dari itu penulis mengharapkan saran dan kritik yang bersifat membangun guna menyempurnakan makalah ini. Semoga makalah ini dapat bermanfaat bagi kita semua.
Penulis
DAFTAR ISI
Kata Pengantar... ...i
Daftar Isi... ...ii
Daftar Gambar...
...iii
Ringkasan... ...iv
BAB I. PENDAHULUAN... ...1
BAB II. TINJAUAN PUSTAKA... 3
2.1 Asam Salisilat... 3
2.2 2-hidroksibenzoil Klorida... 3
2.3 Salisilanilida... 4
2.4 Reaksi Pembentukan Klorida Asam... 5
2.5 Reaksi Substitusi Nukleofilik... 5
2.5.2 Reaksi Substitusi Nukleofilik 2... 9
2.6 Reaksi Substitusi Asil Nukleofilik... 9
BAB III. MEKANISME REAKSI SINTESIS SALISILANILIDA DARI BAHAN DASAR ASAM SALISILAT... ...10
BAB V. KESIMPULAN... 16
DAFTAR PUSTAKA... ...17
DAFTAR GAMBAR
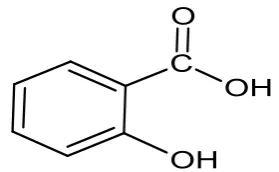
Gambar 2.1 Struktur Asam Salisilat... ...3
Gambar 2.2 Struktur 2-hidroksibenzoil Klorida... ...4
Gambar 2.4 Persamaan Umum Reaksi Pembentukan Klorida Asam... ...6
Gambar 2.5 Reaksi Substitusi Nukleofilik... ...6
Gambar 2.6 Reaksi Substitusi Nukleofilik 1... ...8
Gambar 2.7 Reaksi Substitusi Nukleofilik 2... ...9
Gambar 2.8 Reaksi Substitusi Asil Nukleofilik... 9 Gambar 3.1 Persamaan Reaksi Pembentukan 2-hidrokasibenzoil Klorida.... ...11
Gambar 3.2 Mekanisme Reaksi Pembentukan 2-hidroksibenzoil Klorida.... ...12 Gambar 3.3 Persamaan Reaksi Sintesis Salisilanilida...
...14 Gambar 3.4 Tahap Adisi Nukleofil Pada Gugus Karbonil...
...14 Gambar 3.5 Tahap Pembentukan Senyawa Salisilanilida...
RINGKASAN
Asam salisilat merupakan salah satu jenis dari asam karboksilat yang banyak diperdagangkan di pasaran. Senyawa asam salisilat murni memiliki sifat anti inflamasi, analgesik, dan anti piretik yang cukup rendah. Turunan asam salisilat memiliki sifat analgesik dan antipiretik yang lebih tinggi seperti aspirin dan salisilanilida. Salisilanilida dapat disintesis dari asam salisilat dan anilin. Salisilanilida juga dapat disintesis dengan bahan dasar asam salisilat yang diubah dalam bentuk halida asam berupa 2-hidroksibenzoil klorida melalui reaksi asam salisilat dengan PCl3.
BAB I PENDAHULUAN
1. LATAR BELAKANG
Asam salisilat merupakan salah satu jenis dari asam karboksilat yang banyak diperdagangkan di pasaran. Asam salisilat memiliki fungsi anti inflamasi, analgesik, antipiretik, dan anti jamur. Senyawa asam salisilat murni memiliki sifat anti inflamasi, analgesik, dan anti piretik yang cukup rendah, sehingga diperlukan dosis asam salisilat yang tinggi untuk mengoptimalkan sifat anti inflamasi asam salisilat. Dosis yang terlalu tinggi dapat menyebabkan radang mukosa lambung akibat sifat asam salisilat yang asam, sehingga disintesis turunan asam salisilat untuk meningkatkan sifat anti inflamasi, analgesik, dan antipiretik asam salisilat.
Turunan asam salisilat yang banyak beredar di pasaran adalah asam asetil salisilat (aspirin) dan metil salisilat. Turunan asam salisilat lainnya adalah salisilanilida. Modifikasi struktur pada gugus karboksil dari asam salisilat dengan pensubstitusi senyawa golongan amina telah banyak dilakukan dan menghasilkan senyawa-senyawa amida seperti salisilanilida (Rudyanto dkk, 2005). Salisilanilida merupakan obat anti inflamasi yang berfungsi sebagai analgesik atau antipiretik, dan juga memiliki aktivitas anti jamur. Salisilanilida dapat disintesis dari asam salisilat dan anilin (Parfitt, 1999). Reaksi sintesis salisilanilida dari asam salisilat dan anilin (Kratky dan Vinsova, 2012).
senyawa salisilanilida yang memiliki sifat analgesik dan antipiretik yang lebih baik dari asam salisilat. Salisilanilida memiliki fungsi yang sangat banyak, namun untuk di Indonesia belum dilakukan pengembangan sintesis salisilanilida tersebut.
BAB II
TINJAUAN PUSTAKA
2.1 Asam Salisilat
Asam salisilat adalah salah satu jenis asam karboksilat dengan rumus molekul C7H6O3. Asam salisilat banyak digunakan dalam industri obat-obatan sebagai obat
antijamur (Tjay, 2002)
C O
OH
OH
Gambar 2.1 Struktur Asam Salisilat
Asam salisilat memiliki sifat fisik dan sifat kimia sebagai berikut:
Sifat Fisik Sifat Kimia
- Bentuk : padat - Kelarutan : larut dalam air - Berat molekul : 138,12 gr/mol dan aseton - Titik didih : 211ºC
- Titik leleh : 159 ºC
2.2 2-hidroksibenzoil Klorida
dengan tionil klorida (SOCl2) ataupun dengan fosforus triklorida (PCl3)
(Fessenden dan Fessenden, 1995 B)
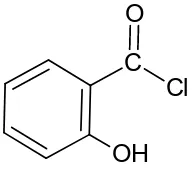
2-hidroksibenzoil klorida adalah salah satu klorida asam yang merupakan turunan dari asam salisilat (asam 2-hidroksibenzoat). Klorida asam memiliki sifat yang paling reaktif diantara semua derivat asam karboksilat. Struktur 2-hidroksibenzoil klorida adalah sebagai berikut:
C O
Cl
OH
Gambar 2.2 Struktur 2-hidroksibenzoil klorida
Asam salisilat memiliki sifat fisik dan sifat kimia sebagai berikut:
Sifat Fisik Sifat Kimia
- Bentuk : padat - Kelarutan : larut dalam air - Berat molekul : 156,566 gr/mol
- Titik didih : 251,4 ºC - Titik leleh : 105,9 ºC
2.3 Senyawa Salisilanilida
C
OH
NH O
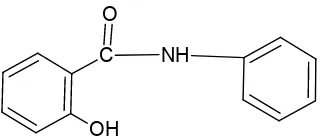
Gambar 2.3 Struktur Salisilanilida
Salisilanilida merupakan obat antiinflamasi yang berfungsi sebagai analgesik dan antipiretik. Salisilanilida juga memiliki aktivitas anti jamur dan anti bakteri serta diindikasikan memiliki fungsi sebagai zat anti kanker (Zhang et al, 2016)
2.4 Reaksi Pembentukan Klorida Asam
Klorida asam merupakan salah satu jenis halida asam yang termasuk ke dalam turunan asam karboksilat. Klorida asam dapat diperoleh melalui reaksi asam karboksilat dengan mensubstitusikan ion klorida untuk menggantikan gugus hidroksida. Gugus hidroksida merupakan gugus pergi yang tidak baik, oleh sebab itu untuk terjadi substitusi gugus hidroksida harus diubah terlebih dahulu menjadi gugus pergi yang baik. Pereaksi yang digunakan dalam reaksi ini yaitu tionil
2.5 Reaksi Substitusi Nukleofilik
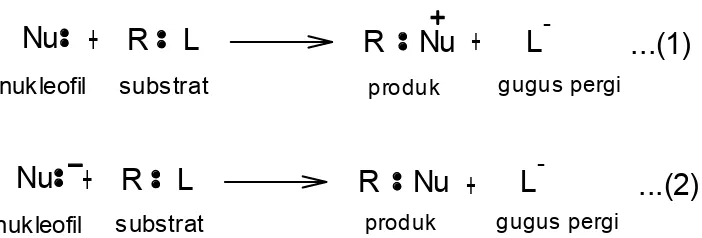
Reaksi substitusi nukleofilik merupakan reaksi dimana terjadi penyerangan secara selektif oleh nukleofil yang kaya akan elektron ke muatan positif dari suatu atom C pada suatu rantai karbon yang mengikat gugus pergi (leaving group) sehingga nukleofil akan menggantikan posisi gugus pergi. Pergantian gugus ini disebabkan karena atom karbon bersifat parsial positif, sehingga mudah diserang oleh anion dan spesi lain yang mempunyai pasangan elektron sunyi (unshared) pada kulit luarnya (Fessenden dan Fessenden, 1995 A)
Nu
+
R L
R Nu
+
L
-Nu
+
R L
R Nu
+
L
-...(1)
...(2)
nukleofil substrat produk gugus pergi
nukleofil substrat produk gugus pergi
Gambar 2.5 Persamaan Umum Reaksi Substitusi Nukleofilik
Berdasarkan persamaan satu, apabila nukleofil dan substrat bersifat netral maka produk reaksi akan bermuatan negatif. Sedangkan bila nukleofil bermuatan negatif dan substrat bersifat netral, maka produk reaksi yang dihasilkan akan bersifat netral juga (dilihat di persamaan dua) (Hart et al, 2003).
Reaksi substitusi nukleofilik ini dipengaruhi oleh beberapa faktor. Ada tiga faktor utama yang mengontrol mekanisme substitusi dan pembentukan hasil sampingan yaitu struktur gugus alkil, sifat gugus pergi dan nukleofil. Nukleofilik dapat bersifat non-basa, seperti ion halida dan basa seperti ion hidroksida (Hardjono Sastrohamidjoyo, 2005).
nukelofilitas. Nukelofilitas merupakan kelajuan penyerangan pada atom karbon elektrofil (Hart et al, 2003)
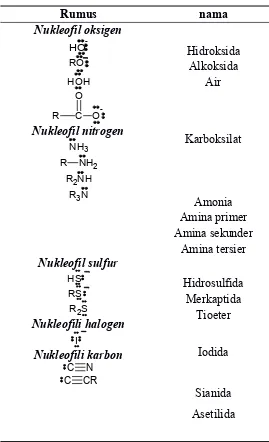
Tabel 2.1 Beberapa jenis nukleofil
Reaksi substitusi nukleofilik terdiri dari dua jenis yaitu SN1 dan SN2. Hal
umum yang membedakan kedua reaksi tersebut adalah pengaruh substrat dan nukleofil terhadap laju reaksi. Pada reaksi SN1 hanya substrat yang mempengaruhi
laju reaksi sehingga reaksi ini mengikuti orde satu dengan persamaan kecepatan reaksi = k [RX] dan produk reaksi berupa campuran rasemik yang tidak optik aktif. Sedangkan pada reaksi SN2 yang mempengaruhi laju reaksi adalah substrat
dan reakstan sehingga reaksi substitusi berlangsung mengikuti orde 2 dengan kecepatan reaksi = k [RX] [Nu-] dimana terjadi reaksi inversi pada atom karbon
pusat (McMurry, 2008)
2.5.1 Reaksi SN1
Reaksi SN1 merupakan substitusi nukleofilik unimolekuler (orde 1). Reaksi
unimolekuler merupakan reaksi yang hanya melibatkan satu molekul dalam keadaan transisi. Reaksi SN1 adalah reaksi ion. Mekanisme reaksi SN1 disebut
Br
+
Brkeadaan transisi 1 zat antara karbokation tak stabil
Tahap 1
Tahap 2
+
nukleofil keadaan transisi 2 produk berproton
Tahap 3
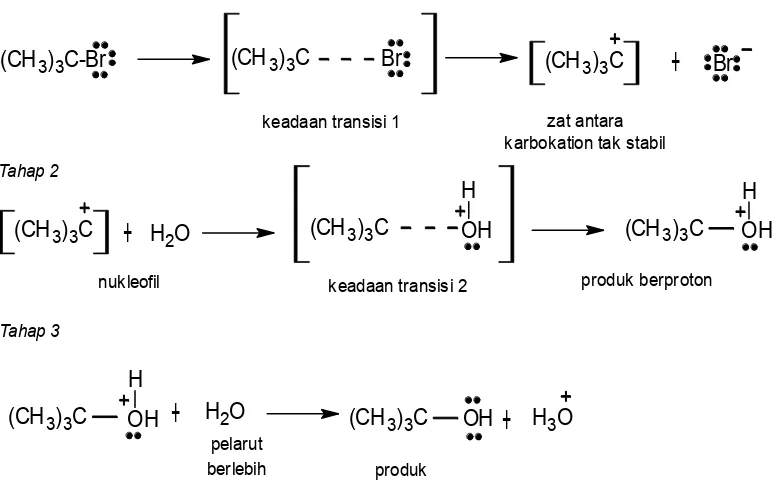
Gambar 2.6 Salah Satu Contoh Reaksi SN1
(Fessenden dan Fessenden,1995 A)
2.5.2 Reaksi SN2
Reaksi SN2 merupakan reaksi nukleofilik bimolekuler (orde 2) yang
berlangsung secara satu tahap melalui tahap transisi (transition state) (Jorapur dan Dae Yoon Chi, 2005). Berikut adalah skema reaksi SN2
R X
+
NuGambar 2.7 Skema Reaksi SN2
2.6 Reaksi Substitusi Nukleofilik Pada Senyawa Karbonil
Reaksi substitusi asil nukleofilik merupakan reaksi substitusi turunan asam karboksilat dengan nukleofil (McMurry, 2008). Klorida asam adalah derivat asam karboksilat yang paling reaktif. Atom klorida yang terikat pada atom C dari gugus karbonil merupakan gugus pergi yang baik. Klorida asam dapat menjalani reaksi substitusi asil nukleofilik dengan nukleofil (Fessenden dan Fessenden, 1995 B)
Reaksi substitusi asil nukleofilik terbagi menjadi 2 tahap, yaitu tahap adisi nukleofil pada gugus karbonil dan tahap eliminasi klorida. Berikut adalah skema reaksi substitusi asil nukleofilik
R C O
Cl
+
Nu R CO
Nu
+
Cl
-Gambar 2.8 Skema Reaksi Asil Nukleofilik
BAB III
MEKANISME REAKSI SINTESIS SALISILANILIDA DARI BAHAN DASAR ASAM SALISILAT
tinggi. Asam salisilat sudah banyak dikembangkan menjadi senyawa lain seperti aspirin (asam asetil salisilat) dan salisilanilida (Rinda Sulistyo dkk, 2015).
Salisilanilida merupakan senyawa turunan asam salisilat yang memiliki banyak fungsi. Salisilanilida dapat digunakan sebagai obat anti inflamasi yang memiliki fungsi analgesik dan antipiretik, selain itu salisilanilida juga memiliki aktivitas anti bakteri dan anti jamur yang baik serta memiliki potensi sebagai zat anti kanker (Wang et al, 2016).
Asam salisilat bila direaksikan dengan anilin akan menghasilkan senyawa salisilanilida. Sintesis salisilanilida dari asam salisilat dan anilin melalui reaksi substitusi nukleofilik terjadi dalam dua tahapan. Tahapan pertama adalah pembentukan klorida asam berupa 2-hidroksibenzoil klorida dan tahapan kedua adalah reaksi substitusi asil nukleofilik 2-hidroksibenzoil klorida dan anilin.
3.1 Pembuatan 2-hidroksibenzoil Klorida
2-hidroksibenzoil klorida adalah salah satu jenis klorida asam yang merupakan turunan dari asam karboksilat. 2-hidroksibenzoil klorida dapat disintesis melalui reaksi antara asam salisilat (asam 2-hidroksibenzoat) dengan zat penghalogen aktif PCl3. Berikut merupakan persamaan reaksi pembentukan
2-hidroksibenzoil klorida
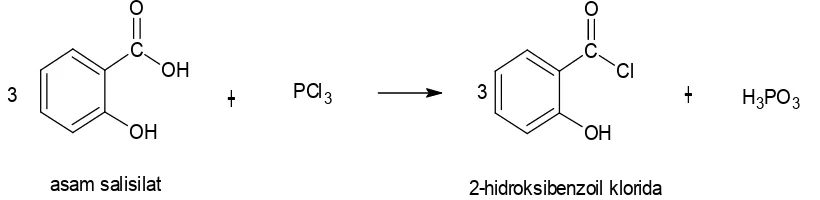
asam salisilat 2-hidroksibenzoil klorida
3 3
Gambar 3.1 Persamaan Reaksi Pembentukan 2-hidroksibenzoil Klorida
Tahapan awal pembentukan 2-hidroksibenzoil klorida yaitu asam salisilat direaksikan dengan PCl3. Elektron sunyi pada atom O dari gugus karbonil
berikatan dengan atom P dan salah satu atom Cl terlepas dari ikatan dengan atom P. Ion Cl- yang terlepas dari ikatan menyerang atom C karbonil sehingga
menyebabkan pemutusan ikatan rangkap antara atom C dengan O . Hal ini
berulang sebanyak tiga kali hingga atom P dari PCl3 berikatan dengan atom O
pada gugus karbonil dari tiga asam salisilat (dapat dilihat pada gambar 3.2).
Tahapan selanjutnya adalah terbentuknya ikatan rangkap antara atom C dengan atom O yang berasal dari gugus hidroksi yang terikat dengan atom C tersebut akibat penyerahan elektron oleh atom H. Terbentuknya ikatan rangkap ini juga menyebabkan ikatan antara masing-masing atom C dan atom O yang terikat dengan atom P terputus sehingga terjadi penyerahan elektron dari ikatan ke atom O. Putusnya ikatan ini menyebabkan gugus PO3 terlepas dan terbentuklah
2-hidroksibenzoil klorida. Ion PO33- berikatan dengan atom H yang terlepas dari
atom C yang membentuk ikatan rangkap dengan atom O sehingga menghasilkan H3PO3 (dapat dilihat pada gambar 3.2).
3.2 Reaksi Sintesis Salisilanilida
Salisilanilida dapat disintesis secara langsung dengan mereaksikan 2-hidroksibenzoil klorida dan anilin dengan pelarut klorobenzen (Kratky dan Vinsova, 2012). Pada tahap ini terjadi reaksi substitusi asil nukleofilik. Reaksi substitusi asil nukleofilik memiliki mekanisme reaksi yang hampir sama dengan reaksi substitusi nukleofilik 2 (SN2), namun pada reaksi substitiusi asil nukleofilik
tidak terjadi pertukaran gugus yang sederhana seperti yang terjadi pada reaksi substitusi nukleofilik 2 (SN2). Reaksi substitusi asil nukleofilik terbagi menjadi 2
tahapan, yaitu tahap adisi nukleofil pada gugus karbonil dan eliminasi ion klorida. 2-hidroksibenzoil klorida adalah salah satu jenis klorida asam, dimana klorida asam merupakan derivat asam karboksilat yang paling reaktif. Atom Cl yang terikat pada atom C karbonil merupakan gugus pergi yang baik dan lebih mudah di substitusikan daripada atom Cl yang terikat dengan alkil (Fessenden & Fessenden, 1995 B). Berikut merupakan persamaan reaksi sintesis salisilanilida:
C
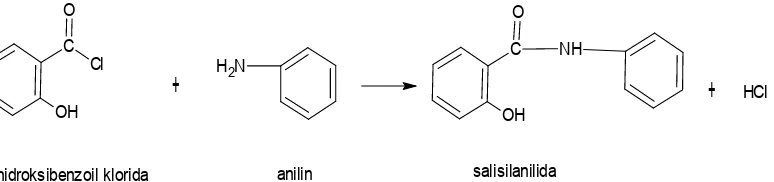
2-hidroksibenzoil klorida anilin salisilanilida
HCl
Gambar 3.3 Reaksi Sintesis Salisilanilida
Sintesis salisilanilida dari 2-hidroksibenzoil klorida melalui reaksi substitusi asil nukleofilik dengan nukleofil anilin berlangsung secara dua tahap. Tahapan reaksi yang terjadi adalah sebagai berikut:
a. Tahap Adisi Nukleofil Pada Gugus Karbonil
C
Gambar 3.4 Tahap Adisi Nukleofil Pada Gugus Karbonil
Elektron sunyi yang terdapat dari atom N pada molekul anilin menyerang atom C karbonil pada molekul 2-hidroksibenzoil klorida. Proses tersebut menyebabkan keterikatan transisi antara anilin dan 2-hidroksibenzoil klorida. Selain itu juga terjadi pemutusan ikatan rangkap antara atom karbon dengan atom O dan penyerahan elektron dari ikatan rangkap ke atom O, sehingga atom O menjadi bermuatan negatif karena kelebihan elektron (dapat dilihat pada gambar 3.4).
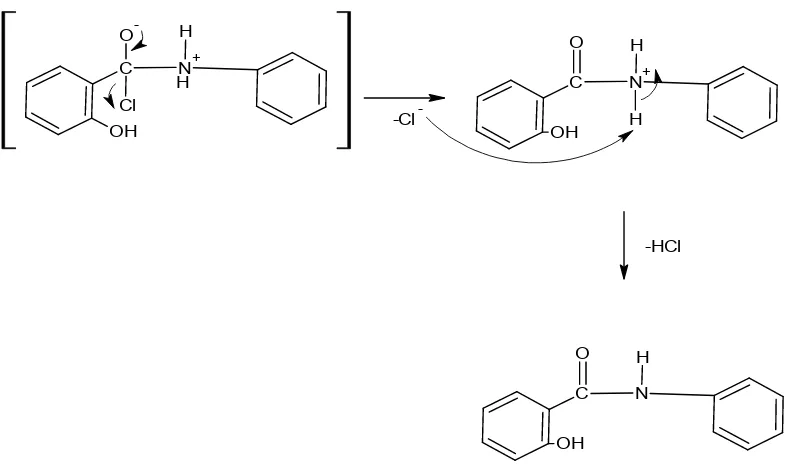
b. Tahap Eliminasi Ion Klorida
Pada tahap ini terjadi pembentukan ikatan rangkap antara gugus O- dengan
atom C. Hal ini dikarenakan atom O yang kelebihan elektron dalam kondisi tidak stabil dan untuk mencapai kestabilan maka terbentuklah ikatan rangkap antara atom O dengan atom C. Selanjutnya terjadi pemutusan ikatan antara atom C dengan atom O dan elektron dari ikatan antara atom C dengan O diserahkan kepada atom O sehingga ion Cl- terlepas dari ikatan. Proses tersebut kemudian
dilanjutkan dengan pelepasan atom H yang terikat pada atom N membentuk gugus amida sehingga terbentuk produk reaksi yaitu salisilanilida. Atom H yang terlepas berikatan dengan ion Cl- menghasilkan asam klorida (dapat dilihat pada gambar
3.5).
C
OH N+ O
-Cl H
H
-Cl
-C
OH
N+ H O
H
-HCl
C
OH N H O
Gambar 3.7 Tahap Pembentukan Senyawa Salisilanilida
BAB IV KESIMPULAN
Berdasarkan pembahasan, dapat disimpulkan hal-hal sebagai berikut:
1. Reaksi sintesis salisilanilida dari bahan dasar asam salisilat melalui reaksi substitusi asil nukleofilik terdiri dari dua tahapan reaksi yaitu, reaksi pembentukan klorida asam dan reaksi substitusi asil nukleofilik.
2. Reaksi pembentukan 2-hidroksibenzoil klorida menggunakan asam salisilat yang direaksikan dengan PCl3.
DAFTAR PUSTAKA
Fessenden, Ralph J. & Joan S. Fessenden. 1995 A. Kimia Organik Edisi Ketiga Jilid 1. Terjemahan Aloysius Hadyana Pudjatmaka. Penerbit Erlangga. Jakarta
Fessenden, Ralph J. & Joan S. Fessenden. 1995 B. Kimia Organik Edisi Ketiga Jilid 2. Terjemahan Aloysius Hadyana Pudjatmaka. Penerbit Erlangga. Jakarta
Hardjono Sastrohamidjoyo. 2005. Kimia Organik. UGM Press. Yogyakarta
Hart, Harold., Leslie E. Craine & David J. Hart. 2003. Kimia Organik Suatu Kuliah Singkat Edisi Kesebelas. Penerbit Erlangga. Jakarta
Jorapur, Yogesh R. & Dae Yoon Chi. 2005. Ionic Liquids: An Environmentally Friendly Media For Nucleophilic Substitution Reaction. Bull Korean Chem Soc
27(3): 345-354. (Online) http://www.journal.kcsnet.or.kr (diakses tanggal 11 April 2016)
Kratky, Martin & J. Vinsova. 2012. Antifungal Activity of Salicylanilides and Their Ester with 4-(triflouromethyl)benzoic Acid. Molecules 17:9426-9442. (Online)
http://www.mdpi.org (diakses tanggal 11 April 2016)
McMurry, J. 2008. Organic Chemistry7th Edition. Thomson Learning Inc. Belmont Parfitt, K. 1999. Martindale The Complete Drugs Reference 32nd Edition.
Pharmaceutical Press. London
Rinda Sulistyo, Suratmo, & Rurini Ekawati. 2015. Sintesis Salisilanilida Dari Komponen Minyak Gandapura. Kimia Student Journal 1(1): 805-811. (Online)
http://www.digilib-unibraw.ac.id (diakses tanggal 18 Januari 2016)
Roth, J.H. & G. Blaschke. 1998. Analisis Farmasi. Terjemahan Kisman. UGM Press. Yogyakarta
Rudianto, Suzana,& G.N. Astika. 2005. Sintesis N-Metilsalisilamida, N,N-Dimetilsalisilamida dan Salisilpiperidida. Akta Kimindo 1(1). (Online)
http://adln.lib.unair.ac.id/go.php?id=gdlhub-gdl-res-2006-rudyantoma-276&PHPSESSID=e99ecec43aeb91a73c0e368ce140cf5f (diakses tanggal 19 April 2016)
Siswandono dan Bambang Soekardjo.1995. Kimia Medisinal. Universitas Airlangga. Surabaya
Vinsova, Jarmila., Amles Imramovsky, Vladimir Buchta, Martina Ceckova, Martin Dolezal, Frantisek Staud, Josef Jampilek, & Jarmila Kaustova. 2007. Salicylanilide Acetates: Synthesis and Bacterial Evaluation. Molecules. 12: 1-12. (Online) http://www.mdpi.org (diakses 11 April 2016)
Wang, Weisi., Zhiqiang Qin, Dan Zhu,Yufen Wei, Shizhu Li, & Liping Duan. 2016. Synthesis, Bioactivity Evaluation, Toxicity Assessment of Novel Salicylinilide Ester Derivatives as Cercarides againts Schistosoma japonicum and Moluscicides againts Oncomelania hupensis. Antimicrobial Agents and Chemotherapy 60(1): 323-331. (Online) http://www.aac.asm.org (diakses tanggal 11 April 2016)
Zang, Li., Li Hou, Wenyan Sun, Zidong Yu, Jibo Wang, Hua Gao, & Guiming Yang. 2016. Synthesisof p-O-Alkyl Salicilanilide Derivatives as Novel EFGR Inhibitors.
Drug Development Research 77: 37-42. (Online)