BAB II
TINJAUAN PUSTAKA
2.1 Pangan
Pangan adalah bahan (biasanya berasal dari hewan dan tumbuhan) yang dimakan/diminum oleh makhluk hidup untuk memberikan tenaga dan nutrisi. Pangan yang dibutuhkan manusia biasanya diperoleh melalui bertani atau berkebun yang meliputi sumber hewan dan tumbuhan. Pada umumnya bahan pangan mengandung air, karbohidrat, protein, lemak, vitamin, enzim, pigmen dan lain-lain. Pangan dari sumber tumbuhan yang sering dikonsumsi manusia yaitu buah, sayuran, biji-bijian, kacang-kacangan dan bumbu, sedangkan pangan dari sumber hewan yaitu daging, produk telur dan susu (Anonimc, 2014).
2.2 Bahan Tambahan Pangan (BTP)
Pengertian bahan tambahan pangan dalam Peraturan Menteri Kesehatan RI No. 772/Menkes/Per/IX/88 dan No. 1168/Menkes/PER/X/1999 secara umum adalah bahan yang biasanya tidak digunakan sebagai makanan dan bukan merupakan komponen khas makanan, mempunyai atau tidak mempunyai nilai gizi, yang dengan sengaja ditambahkan ke dalam makanan untuk maksud teknologi pada pembuatan, pengolahan, penyiapan, perlakuan, pengepakan, pengemasan dan penyimpanan. Tujuan penambahan bahan tambahan pangan adalah dapat meningkatkan atau mempertahankan nilai gizi dan kualitas daya simpan, membuat bahan pangan lebih mudah dihidangkan, serta mempermudah preparasi bahan pangan (Cahyadi, 2009).
Menurut Cahyadi (2009), pada umumnya bahan tambahan terbagi menjadi dua golongan besar, yaitu sebagai berikut:
1. Bahan tambahan pangan yang ditambahkan secara sengaja ke dalam makanan, dengan mengetahui komposisi bahan tersebut dan maksud penambahan itu dapat mempertahankan kesegaran, cita rasa, dan membantu pengolahan, sebagai contoh pengawet, pewarna dan pengeras.
2. Bahan tambahan pangan yang tidak sengaja ditambahkan, yaitu bahan yang tidak mempunyai fungsi dalam makanan tersebut, terdapat secara tidak sengaja, baik dalam jumlah sedikit atau cukup banyak akibat perlakuan selama proses produksi, pengolahan dan pengemasan. Bahan ini dapat pula merupakan residu/kontaminan dari bahan yang sengaja ditambahkan untuk tujuan produksi bahan mentah atau penanganannya yang masih terus terbawa ke dalam makanan yang akan dikonsumsi. Contoh bahan tambahan pangan dalam golongan ini adalah residu pestisida (termasuk insektisida, herbisida, fungisida dan rodentisida) dan antibiotik.
Penggunaan bahan tambahan pangan sebaiknya dengan dosis di bawah ambang batas yang telah ditentukan. Jenis bahan tambahan ada 2, yaitu GRAS (GenerallyRecognized as Safe), zat ini aman dan tidak berefek toksik misalnya gula (glukosa), sedangkan jenis lainnya, yaitu ADI (Acceptable Daily Intake), jenis ini selalu ditetapkan batas penggunaan hariannya (daily intake) demi menjaga/melindungi kesehatan konsumen (Cahyadi, 2009).
Di Indonesia telah disusun peraturan tentang Bahan Tambahan Pangan yang diizinkan ditambahkan dan yang dilarang (disebut Bahan Tambahan Kimia) oleh Departemen Kesehatan diatur dengan Peraturan Menteri Kesehatan Republik Indonesia Nomor 722/Menkes/Per/IX/88, terdiri dari golongan BTP yang diizinkan di antaranya sebagai berikut:
1. Antioksidan (antioxidant) 2. Antikempal (anticaking agent)
3. Pengatur keasaman (acidity regulator) 4. Pemanis buatan (artificial sweeterner)
5. Pemutih dan pematang telur (flour treatment agent)
6. Pengemulsi, pemantap dan pengental (emulsifier, stabilizer, thickener) 7. Pengawet (preservative)
8. Pengeras (firming agent) 9. Pewarna (colour)
10. Penyedap rasa dan aroma, penguat rasa (flavour, flavour enhancer) 11. Sekuestran (sequestrant)
Selain bahan tambahan pangan yang tercantum dalam peraturan tersebut masih ada beberapa bahan tambahan pangan yang biasa digunakan dalam pangan, misalnya enzim, penambah gizi dan humektan. Beberapa bahan tambahan yang dilarang digunakan dalam makanan menurut Permenkes RI No. 722/Menkes/Per/IX/88 yaitu Natrium tetraborat (boraks), Formalin (formaldehyde), P-Phenetilkarbamida (dulcin) dan Asam salisilat, sedangkan menurut Peraturan Menteri Kesehatan RI No. 1168/Menkes/Per/X/1999, selain bahan tambahan di atas masih ada tambahan bahan kimia yang dilarang, seperti Rhodamin B (pewarna merah), Kuning Metanil
(pewarna kuning), Dulsin (pemanis sintetis) dan Kalium bromat (pengeras) (Cahyadi, 2009).
Sejak pertengahan abad ke-20 ini, peranan bahan tambahan pangan menjadi semakin penting sejalan dengan kemajuan teknologi produksi bahan tambahan pangan sintetis. Banyaknya bahan tambahan pangan dalam bentuk murni dan tersedia secara komersil dengan harga yang relatif murah akan mendorong meningkatnya konsumsi bahan tersebut bagi setiap individu. Penggunaan bahan tambahan pangan (BTP) dalam proses produksi pangan perlu diwaspadai bersama, baik oleh produsen maupun oleh konsumen. Dampak penggunaannya dapat berakibat positif maupun negatif bagi masyarakat. Penyimpangan dalam penggunaannya akan membahayakan kita, khususnya generasi muda. Di bidang pangan kita memerlukan sesuatu yang lebih baik untuk masa yang akan datang, yaitu pangan yang aman dikonsumsi, lebih bermutu, bergizi dan lebih mampu bersaing dalam pasar global (Cahyadi, 2009).
Zat aditif pangan juga dapat menyebabkan penyakit jika tidak digunakan sesuai dosis, terutama zat aditif pangan sintetis. Penyakit yang biasa timbul dalam jangka waktu lama setelah pengunaan zat aditif pangan adalah kanker dan kerusakan ginjal (Anonima, 2014).
2.3 Pewarna Bahan Pangan
Penentuan mutu bahan pangan pada umumnya sangat tergantung pada beberapa faktor, seperti cita rasa, tekstur, dan nilai gizinya, juga sifat mikrobiologis tetapi sebelum faktor-faktor lain dipertimbangkan, secara visual faktor warna tampil lebih dahulu dan kadang-kadang sangat menentukan. Selain sebagai faktor
yang menentukan mutu, warna juga dapat digunakan sebagai indikator kesegaran. Baik tidaknya cara pencampuran atau cara pengolahan dapat ditandai dengan adanya warna yang homogen dan merata (Cahyadi, 2009).
Pewarna telah digunakan sejak zaman purbakala. Pewarna biasa diperoleh dari hewan, tumbuhan atau mineral tanpa harus diproses. Umumnya, sumber utama pewarna didapat dari tumbuhan, yaitu dari akar, buah, daun, dan kayu tetapi hanya sedikit yang diperdagangkan. Beberapa pewarna dapat mengendap jika direaksikan dengan garam inert. Secara umum, pewarna terbagi menjadi pewarna alami dan pewarna buatan (sintetis) (Anonimb, 2014).
2.3.1 Pewarna alami
Banyak warna cemerlang yang dijumpai pada hewan dan tumbuhan dapat digunakan sebagai pewarna untuk pangan. Beberapa pewarna alami memberikan nutrisi (karotenoid, riboflavin dan kobalamin), merupakan bumbu (kunir dan paprika) atau pemberi rasa (karamel) ke bahan olahan. Konsumen dewasa ini banyak menginginkan bahan alami dalam diet mereka. Banyak pewarna olahan yang awalnya menggunakan pewarna sintetis berpindah ke pewarna alami. Contohnya penggunaan serbuk beet menggantikan pewarna merah sintetis FD & C No. 2. Beberapa pewarna alami yang berasal dari tumbuhan dan hewan diantaranya klorofil, mioglobin dan hemoglobin, antosianin, flavonoid, tanin, betalain, quinon dan xanthon, serta karotenoid (Cahyadi, 2009).
2.3.2 Pewarna buatan (sintetis)
Di negara maju, suatu zat pewarna buatan harus melalui berbagai prosedur pengujian sebelum dapat digunakan sebagai pewarna pangan. Zat pewarna yang diizinkan penggunaannya dalam pangan disebut permitted color atau certified
color. Zat warna yang akan digunakan harus menjalani pengujian dan prosedur
penggunaannya, yang disebut proses sertifikasi. Proses sertifikasi ini meliputi pengujian kimia, biokimia dan toksikologi terhadap zat tersebut (Yuliarti, 2007).
Di Indonesia, peraturan mengenai penggunaan zat pewarna yang diizinkan dan dilarang untuk pangan diatur melalui SK Menteri Kesehatan RI Nomor 722/Menkes/Per/IX/88 mengenai bahan tambahan pangan. Beberapa contoh zat pewarna yang diizinkan yaitu Biru berlian, Eritosin, Hijau FCF, Indigotin dan Tartrazine. Sedangkan contoh pewarna yang dilarang yaitu Rhodamin B, Kuning metanil dan Amaran. Akan tetapi, seringkali terjadi penyalahgunaan pemakaian zat pewarna untuk pangan, misalnya zat pewarna untuk tekstil dan kulit dipakai untuk mewarnai bahan pangan. Hal ini jelas berbahaya bagi kesehatan karena adanya residu logam berat pada zat pewarna tersebut. Timbulnya penyalahgunaan tersebut antara lain disebabkan oleh ketidaktahuan masyarakat mengenai zat pewarna untuk pangan, dan di samping itu harga zat pewarna untuk industri jauh lebih murah dibandingkan dengan harga zat pewarna untuk pangan juga warna dari zat pewarna tekstil lebih menarik (Cahyadi, 2009).
2.4 Kuning Metanil (Methanyl Yellow)
Kuning metanil adalah zat warna sintetis berbentuk serbuk berwarna kuning kecoklatan (tawny), larut dalam air, agak larut dalam benzen, eter dan sedikit larut dalam aseton. Umumnya digunakan sebagai pewarna tekstil dan cat. Zat tersebut merupakan senyawa kimia azo amin aromatik yang dapat menimbulkan tumor di berbagai jaringan hati, kandung kemih, saluran pencernaan atau jaringan kulit (Yuliarti, 2007).
Demi perlindungan terhadap kesehatan dan keselamatan konsumen, Balai POM meminta produsen pangan tidak menggunakan bahan kimia yang dilarang untuk pangan. Demikian juga, Balai POM meminta toko pengencer bahan kimia untuk tidak menjual bahan kimia yang dilarang kepada konsumen. Menurut Yuliarti (2007), monografi dari kuning metanil adalah sebagai berikut:
Kuning Metanil (Methanyl Yellow)
Gambar 2.1 Rumus bangun kuning metanil
Nama Kimia : 3-(4-Anilinophenylazo)benzenesulfonic acid sodium salt Nama Lazim : Methanyl Yellow; Acid Yellow 36; C.I. 13065
Rumus Kimia : C18H14N3NaO3S
BM : 375,38
Pemerian : Serbuk kuning kecoklatan
Kelarutan : Larut dalam air, agak larut dalam benzen, eter dan sedikit larut dalam aseton .
Penggunaan : Sebagai pewarna tekstil dan cat.
2.5 Spektrofotometri
Spektrofotometri adalah pengukuran absorbsi energi cahaya oleh suatu sistem kimia pada suatu panjang gelombang tertentu. Sinar ultraviolet mempunyai panjang gelombang antara 200-400 nm, sementara sinar tampak mempunyai
panjang gelombang 400-750 nm. Menurut Gandjar dan Rohman (2007), hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan dan berbanding terbalik dengan transmitan. Hukum tersebut dituliskan dengan : A = abc = log 1/T Keterangan : A = absorbans a = koefisien ekstingsi b = tebal sel (cm) c = konsentrasi analit.
Penyerapan radiasi sinar ultraviolet dan sinar tampak oleh spesies atom atau molekul (M) dapat dipertimbangkan sebagai proses 2 langkah; yang pertama adalah melibatkan eksitasi sebagaimana ditunjukkan oleh persamaan berikut:
M + hv M*
Hasil reaksi antara M dengan foton (hv) merupakan partikel yang tereksitasi secara elektronik yang disimbolkan dengan M*. Waktu hidup M* sangat pendek (10-8 – 10-9 detik), dan keberadaannya dapat diakhiri dengan berbagai macam proses relaksasi. Kebanyakan tipe relaksasi melibatkan konversi energi eksitasi menjadi panas, sesuai dengan persamaan berikut:
M* M + panas
Relaksasi juga dapat terjadi dengan terdekomposisinya M* membentuk spesies baru, sebagaimana suatu proses yang disebut dengan reaksi fotokimia. Alternatifnya, relaksasi juga melibatkan emisi radiasi kembali yang dikenal dengan fluorosensi dan fosforesensi (Gandjar dan Rohman, 2007).
Penyerapan (absorpsi) sinar ultraviolet dan sinar tampak pada umumnya dihasilkan oleh eksitasi elektron-elektron ikatan, akibatnya panjang gelombang pita yang mengabsorpsi dapat dihubungkan dengan ikatan yang mungkin ada dalam suatu molekul. Terdapat tiga macam proses penyerapan energi ultraviolet dan sinar
tampak yaitu penyerapan oleh transisi elektron ikatan dan elektron anti ikatan, penyerapan oleh transisi elektron d dan f dari molekul kompleks serta penyerapan oleh perpindahan muatan (Gandjar dan Rohman, 2007).
Menurut Gandjar dan Rohman (2007), terdapat beberapa hal yang harus diperhatikan dalam analisis dengan spektrofotometri ultraviolet dan cahaya tampak terutama untuk senyawa yang tidak berwarna yang akan dianalisis yaitu:
1. Pembentukan molekul yang dapat menyerap sinar UV-Vis
Cara yang digunakan adalah dengan merubahnya menjadi senyawa lain atau direaksikan dengan pereaksi tertentu sehingga dapat menyerap sinar UV-Vis 2. Waktu kerja (operating time)
Tujuannya ialah untuk mengetahui waktu pengukuran yang stabil. Waktu kerja ditentukan dengan mengukur hubungan antara waktu pengukuran dengan absorbansi larutan.
3. Pemilihan panjang gelombang
Panjang gelombang yang digunakan untuk analisis kuantitatif adalah panjang gelombang yang mempunyai absorbansi maksimal.
4. Pembuatan kurva baku
Dilakukan dengan membuat seri larutan baku dalam berbagai konsentrasi kemudian absorbansi tiap konsentrasi diukur lalu dibuat kurva yang merupakan hubungan antara absorbansi dengan konsentrasi.
5. Pembacaan absorbansi sampel
Absorbansi yang terbaca pada spektrofotometer hendaknya terletak antara 0,2 sampai 0,6.
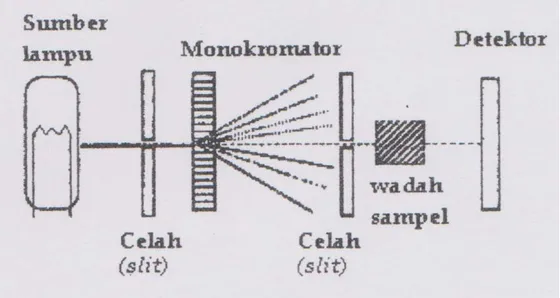
Instrumentasi untuk Spektrofotometri
Gambar 2.2 Diagram skematis spektrofotometer UV-Vis (Sumber : Gandjar dan Rohman, 2007)
Menurut Gandjar dan Rohman (2007), komponen spektrofotometer ultraviolet/sinar tampak terdiri dari:
a. Sumber Cahaya
Sumber energi radiasi yang biasa untuk daerah ultraviolet dan daerah cahaya tampak adalah sebuah lampu wolfram ataupun lampu tabung discas hidrogen (atau deutrium).
b. Monokromator
Monokromator berfungsi mengubah cahaya polikromatis menjadi cahaya yang monokromatis. Alatnya dapat berupa berupa prisma atau kisi difraksi.
c. Sel
Sel yang digunakan untuk daerah tampak terbuat dari kaca sedang untuk daerah ultraviolet digunakan sel kuarsa atau kaca silika. Sel tampak dan ultraviolet yang khas mempunyai panjang lintasan 1 cm, namun tersedia juga sel dengan ketebalan kurang dari 1 milimeter, sampai 10 cm bahkan lebih.
d. Detektor
Peranan detektor adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang. Detektor yang paling sederhana dipakai ialah tabung foto. e. Recorder
Recorder digunakan sebagai perekam absorbansi yang dihasilkan dari pengukuran.
2.6 Validasi
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu, berdasarkan percobaan laboratorium, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004). 2.6.1 Perolehan kembali
Uji perolehan kembali dilakukan dengan metode penambahan larutan baku (standard addition method). Dalam metode ini, kadar kuning metanil dalam sampel ditentukan terlebih dahulu, selanjutnya dilakukan penentuan kadar kuning metanil dalam sampel setelah penambahan larutan standar dengan konsentrasi tertentu. Menurut Harmita (2004), persen perolehan kembali dapat dihitung dengan rumus di bawah ini:
% Perolehan Kembali = CF- CA
𝐶𝐶∗A ×100%
Keterangan: CF = Kadar sampel setelah penambahan larutan baku (mcg/g)
CA = Kadar sampel sebelum penambahan larutan baku (mcg/g)
2.6.2 Uji ketelitian
Keseksamaan atau presisi diukur sebagai simpangan baku relatif atau koefisien variasi. Keseksamaan atau presisi merupakan ukuran yang menunjukkan derajat kesesuaian antara hasil uji individual ketika suatu metode dilakukan secara berulang untuk sampel yang homogen. Nilai simpangan baku relatif yang memenuhi persyaratan menunjukkan adanya keseksamaan metode yang dilakukan. Menurut Harmita (2004), simpangan baku relatif dapat dihitung dengan rumus di bawah ini: RSD = ×100% X SD Keterangan : −
X = Kadar rata-rata sampel (mcg/g)
SD = Standar Deviasi (mcg/g)
RSD = Relative Standard Deviation (%)
2.6.3 Penentuan batas deteksi (limit of detection) dan batas kuantitasi (limit of quantitation)
Batas deteksi merupakan jumlah terkecil analit dalam sampel yang dapat dideteksi yang masih memberikan respon signifikan sedangkan batas kuantitasi merupakan kuantitas terkecil analit dalam sampel yang masih dapat memenuhi kriteria cermat dan seksama. Menurut Harmita (2004), batas deteksi dan batas kuantitasi ini dapat dihitung dengan rumus sebagai berikut:
Simpangan Baku (SY X) =
(
)
2 2 − −∑
n Yi YBatas deteksi (LOD) =
slope X SY x
3
Batas kuantitasi (LOQ) =
slope X SY x