SINTESIS POLIMER TERIMPREGNASI TiO
2DENGAN
TEKNIK MOLECULER IMPRINTED POLYMER DAN UJI
AKTIVITAS FOTOKATALISISNYA
SYNTHESIS TiO2 IMPRINTED POLYMER WITH MOLECULER
IMPRINTED POLYMER TECHNIQ AND ITS PHOTOCALYTIC
ACTIVITY TEST
Yusuf Syah(1), Harjana(2), Hamami(1), Ganden Supriyanto(1)
ABSTRACT
Many efforts have been carried out to handle phenolic compound wastes; such as adsorption by active carbon, chemical oxidation, and biodegradation by microorganism. Those ways have not jet given optimal results. Phoyocatalytic degradation by TiO2 and UV lamp process has been
developed. Until this time, the use of TiO2 for photo catalytic degradation as a suspension forms, so difficult to separate from degradation product, and cannot reuse.
Molecular imprinted polymer (MIP) as a technique by mixing a template from a functional group monomer and cross-linker in a certain solvent. This technique is done by impregnated TiO2 as a template to the polymer, which
produced from the mixture of 4-vinylpiridin as a monomer, and styrene - divinylbenzena as cross-linkers. The polymer without TiO2 as a control
polymer was made too. The purposes of this research are (1) to synthesize TiO2 impregnated polymer from 4- vinylpiridine as monomer and styrene
and divinylpiridine as cross-linker, (2) to test the mechanic property, analyze molecule structure, and to examine the photo catalytic degradation capability of polymer to standard PCP solution.
The results of these research are: it is has a coordinative bound between TiO2 and 4-vinylpiridine in the TiO2 polymer molecule, compression
force of TiO2 impregnated polymer is greater than control polymer, and TiO2
impregnated polymer able to degradates PCP standard solution 66,74% at sixth hour.
Keyword: Molecular imprinted polymer (MIP), TiO2, 4-vinilpiridin, cross-linker
Styrene, PCP, Photo catalytic degradation
(1) Departemen Kimia Fakultas Sains dan Teknologi - Universitas Airlangga (2) Fakultas Farmasi Universitas Airlangga
PENDAHULUAN
Perkembangan industri dapat memberikan keuntungan, tetapi juga dapat memberikan dampak yang merugikan bagi manusia dan lingkungan. Keuntungan yang diperoleh dari perkembangan industri di antaranya adalah terbukanya lapangan kerja baru, berjalannya roda perekonomian dn akhirnya akan meningkatkan kesejahteraan masya-rakat, Sedangkan kerugian yang ditimbulkan akibat adanya perkembangan industri adalah pen-cemaran lingkungan yang diakibatkan limbah industri yang terbuang ke lingkungan. Beberapa limbah industri hádala senyawa- senyawa fenol dan turunannya, antara lían pentaklorofenol (PCP). Senyawa fenol dan turunannya di satu sisi me-nguntungkan manusia karena dapat digunakan sebagai disinfektan, di sisi lain merugikan karena sifatnya yang toksik dan karsinogenik sehingga menyebabkan kerusakan lingkungan perairan dan gangguan kesehatan manusia. (Chen dan Ray, 1993).
Berbagai usaha telah dilakukan untuk menanggulangi limbah senyawa fenol dan turunannya, antara lain dengan cara adsorpsi menggunakan karbon aktif, oksidasi kimiawi, dan biodegradasi oleh mikro-orgnisme. Namun cara-cara tersebut belum memberikan hasil yang optimal. Degradasi limbah dengan metode fotokatalisis menggunakan
TiO2 dan lampu ultra violet (UV) telah
dikembangkan. Dalam proses degradasi fotokatalitik dihasilkan radikal bebas OH yang sangat reaktif untuk mendegradasi senyawa-senyawa organik menjadi produk akhir yang tidak berbahaya. Pada proses ini, semikonduktor diiradiasi dengan sinar ultraviolet. Elektron yang dilepaskan dipromosikan dari pita valensi (valence band) ke pita konduksi (conduction band) yang
menghasilkan pasangan elektron e
-dan lubang h+. Pasangan ini berperan
dalam reaksi oksidasi dan reduksi yang menjadi prinsip dari degradasi fotokatalisis (Hoffman, 1995). Selama
ini TiO2 sebagai fotokatalisator untuk
mendegradasi limbah digunakan dalam bentuk suspensi, sehingga sulit dipisahkan dari hasil degradasi dan tidak dapat digunakan secara berulang (reuse).
Gladis dan Rao (2003) telah mensintesis suatu molecular imprinted
polymer (MIP) dengan cara
mereaksikan UO22+ dengan
5,7-diklorokuinolin-8-ol dan 4-vinilpiridin sebagai monomer fungsional dan stirena-divinilbenzena sebagai
cross-linker. Matilda et al. (2004)
melaporkan pembentukan molecular
imprinted polymer yang digunakan
untuk prekonsentrasi UO22+. Menurut
Tanaka et al. (1993) TiO2 akan
bermuatan negatif pada pH tinggi (basa) dan bermuatan positif pada pH
rendah (asam). Dengan demikian TiO2
pada pH asam diduga mempunyai sifat kemiripan secara kimiawi dengan
UO22+. Dengan menganalogkan TiO2
dengan UO22+ maka dimungkinkan
untuk mengimpregnasi TiO2 pada
suatu polimer.
Senyawa TiO2 telah secara luas
digunakan dalam proses degradasi
fotokatalisis. Penggunaan TiO2 dalam
bentuk senyawa terimpregnasi akan memberikan banyak keuntungan, dia antaranya dapat dipisah dengan mudaah dari hasil degradasi, dapat dipakai berulang kali, mengurangi biaya operasional dan mengurangi
limbah oleh padatan TiO2 yang
terbuang ke lingkungan. Penelitian ini bertujuan untuk: (1) mensintesis
polimer yang terimpregnasi TiO2
menggunakan monomer 4-vinilpiridin dan cross-linker stiren dan divinilpiridin, (2) menguji sifat-sifat polimer yang dihasilkan meliputi: kekuatan gaya tekan, struktutr ikatan dalam molekul, serta kemampuan aktivitas degradasi fotokatalisis
polimernya terhadap larutan standar pentaklorofenol (PCP). Hasil penelitian ini diharapkan diperoleh bahan yang dapat digunakan untuk mendegradasi limbah secara berulang-ulang.
METODE PENELITIAN
Bahan-bahan kimia yang
digunakan adalah 4-vinilpiridin, TiO2,
HNO3 4 N 2-metoksi etanol, stirena,
divinilbenzena, hidrogen peroksida, gas nitrogen, laruta-larutan
4-aminoantipiridin 2%, K3[Fe(CN)6] 8%,
NH4Cl 5%, NH4OH 25%, dan
pentaklorofenol (PCP).
Alat yang diperlukan dalam penelitian ini adalah reaktor yang berupa kotak kayu 20 x 20 x 15 cm yang dilengkapi dengan lampu UV 10 watt; Spektrofotometer UV-Vis, spek-troskopi IR dan Autograph AG-10TE Shimadzu, serta peralatan gelas yang biasa dipakai di laboratorium kimia.
Pembentukan polimer terimpregnasi TiO2 (Ladis dan Rao, 2003)
Ke dalam gelas beker 100 ml
dicampurkan 160 mg TiO2, 1 ml
4-vinilpiridin, 20 ml 2-metoksi etanol,
dan 10 ml HNO3 4 M. Campuran
diaduk dengan dengan kecepatan 500 rpm selama 2 jam. Ke dalam campuran ditambahkan 1,50 ml stiren, 2,50 ml divinil benzena dan 3
ml H2O2, lalu diaduk selama 10 menit.
Campuran didinginkan pada suhu O0
C selama 15 menit, lalu diliri gas N2
dengan kecepatan alir 20 kg/cm2
selama 5 menit. Gelas beker ditutup lalu diaduk selama enam jam. Polimer yang terjadi dituang di atas cetakan kaca dengan ketebalan sekitar 0,50 mm dan sisa pelarut diuapkan pada suhu kamar. Polimer kontrol dibuat dengan prosedur yang sama, tetapi
tanpa TiO2
Uji kekuatan daya tekan polimer
Polimer terimpregnasi TiO2 dan
polimer kontrol diukur kektatan daya
tekannya dengan alat compression
test dengan menempatkan kedua
polimer yang terbentuk pada alat penekan sampel Autograph 500D yang telah dimodifikasi, lalu diberi tekanan sampai polimer tersebut mengalami keretakan. Diukur besar nilaitegangannya (KN).
Analisis struktur ikatan polimer dengan IR
Polimer terimpregnasi TiO2 dan
polimer kontrol dianalisis strukur ikatannya dengan spektroskopi IR.
Uji aktivitas degradasi fotokatalitik polimer
Dibuat larutan induk PCP 1000 ppm dengan jalan melarutkan 100 mg PCP dalam akuades sampai volume 100 ml. Dari larutan induk dibuat enam macam larutan standar PCP masing-masing dengan konsentrasi akhir 1,0; 1,5; 2,0, 2,5; 3,0; dan 3,5 ppm. Ke dalam enam buah kabu takar 10 ml dipipet larutan induk PCP 1000 ppm masing-masing 0,10; 0,15; 0,20; 0,25; 0,30; dan 0,35 ml. Ke dalam setiap labu takar ditambahkan larutan-larutan perekasi: 0,1 mL 4-aminoantipiridin 2%, 0,1 mL
K3[Fe(CN)6] 8%, 0,25 mL, NH4Cl 5%,
0,1 mL NH4OH 25% dan diencerkan
dengan akades samapai garis batas. Setiap campuran diukur absor-bansinya denga spektrofoto-meter UV-Vis pada panjang gelombang 516 nm menggunakan blangko campuran larutan di atas tanpa adanya PCP. Dari hasil pengukuran abosrbansi tersebut dibuat persamaan kurva standarnya.
Ke dalam dua buah cawan petri masing-masing diletakkan plat kaca yang telah tertempel polimer
terimpregnasi TiO2 dan polimer
kontrol.. Kemudian ke dalam cawan tersebut dimasukkan 10 mL larutan standar PCP 50 ppm . Cawan petri diletakkan di dalam reaktor dan diiradiasi dengan sinar UV selama 6
jam. Setiap interval 1 jam dari masing-masing cawan petri dipipet 0,50 mL larutan yang telah diirradiasi ke dalam labu takar 10 ml lalu ditambahkan larutan-larutan pereaksi seperti di atas, dan diukur absorbansinya pada 516 nm.
Absorbansi hasil pengukuran dari kedua tempat dimasukkan ke dalam persamaan regresi linier yang telah dibuat, diperoleh kadar PCP sisa (ppm). Kadar PCP yang terdegradasi dapat dihitung dari pengurangan kadar PCP mula-mula dengan kadar PCP sisa.
HASIL DAN PEMBAHASAN
Hasil Pembentukan Polimer Terimpregnasi TiO2
Hasil polimer teimpregnasi TiO2
yang terbentuk setelah penguapan pelarut berupa padatan kuning keras
yang halus, dengan lapisan TiO2
berwarna putih yang merata pada
permukaan, dan mudah patah., sedangkan polimer kontrol berwarna kekuningan pada permukaannya.
Hasil Uji Kekuatan Daya Tekan Polimer
Dilakukan uji kekuatan daya tekan terhadap polimer terimpregnasi
TiO2 dan polimer kontrol. Hasil uji
tersebut dinyatakan dalam Tabel 1. Nilai gaya per satuan luas polimer
terimpregnasi TiO2 sebesar 68,3
KN/m2 lebih besar dibandingkan
dengan nilai gaya per satuan luas
polimer kontrol yaitu 32,5 KN/m2. Hal
ini menandakan adanya interaksi
antara TiO2 dengan monomer.
Interaksi yang terbentuk kemungkinan berupa ikatan-ikatan
koordinasi antara TiO2 dan N pada
4-vinilpiridin. Adanya ikatan pada TiO2
ini dapat menambah gaya yang cukup besar sehingga meningkatkan sifat kekakuan dari polimer yang terbentuk.
Tabel 1. Data hasil compression test pada polimer
Sampel Ao (m2) F (KN)
o F A
σ = (KN/ m2)
Polimer terimpregnasi TiO2 0,0007544 0,0515 68,3
Polimer kontrol 0,0006154 0,0200 32,5 Hasil Analisis Polimer dengan IR
Analisis dengan IR bertujuan untuk melihat struktur molekul polimer yang terbentuk, khususnya
kedudukan TiO2 dalam polimer.
Analisis ini dilakukan terhadap
polimer terimpregnasi TiO2 maupun
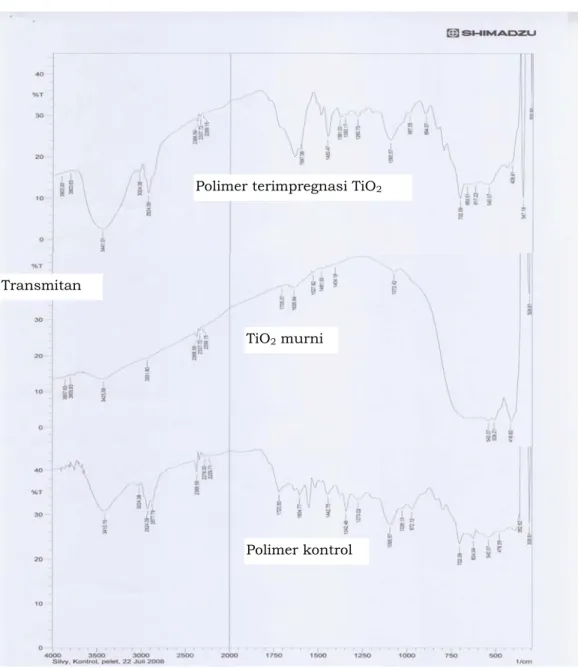
polimer kontrol. Hasil analisis dengan IR ditunjukkan pada Gambar 1.
Dari kedua spektrum polimer
terimpregnasi TiO2 dan polimer
kontrol tampak vibrasi ulur spesifik OH sebagai pita lebar muncul pada
3.425 cm-1, vibrasi ulur C-H (aril)
berkisar antara 3.000-3.300 cm-1,
sedangkan vibrasi C-C (aril) terletak
pada 1.450-1.600 cm-1, kemudian
untuk ikatan C=C dan C=N terletak pada bilangan gelombang antara
1.500-1.900 cm-1, sehingga dapat
diasumsikan struktur molekul polimer kontrol tidak berbeda jauh dengan
polimer terimpregnasi TiO2.
Sedangkan, untuk spektra TiO2
sendiri tampak pita spesifik pada
bilangan gelombang 300-4.000 cm-1.
Pada spektrum polimer terimpregnasi
TiO2 tampak pita spesifik pada
bilangan gelombang 300-350 cm-1
yang ini tidak muncul pada polimer kontrol, tetapi vibrasi ini juga muncul
pada spektrum TiO2. Hal ini diduga
kemungkinan vibrasi tersebut sehingga secara teoritis sebagian
Polimer terimpregnasi TiO2
Transmitan
TiO2 murni
Polimer kontrol
Bilangan gelombang (cm-1
Gambar 1. Hasil analisis IR polimer terimpregnasi TiO2, TiO2 murni dan polimer kontrol
struktur molekul polimer kontrol tidak berbeda jauh dengan polimer
terimpregnasi TiO2.
Namun pada polimer
terimpregnasi TiO2 muncul serapan di
daerah bilangan gelombang 847,97
cm-1, di mana serapan ini tidak
muncul pada polimer terimpregnasi
TiO2 maupun pada TiO2 murni. Dalam
hal ini diduga serapan tersebut ialah serapan milik Ti-N atau Ti-O yang
secara teoritis hanya terbentuk pada
polimer terimpregnasi TiO2.
Sedangkan, untuk keberadaan TiO2
sendiri tampak pada spektrum di daerah bilangan gelombang
3500-4000 cm-1. Hal ini menunjukkan
bahwa keberadaan TiO2 yang bersifat
seperti TiO2 murni masih ada yang
ditunjukkan dengan spektrum yang yang identik. Melalui hasil spektra inframerah ini diduga struktur
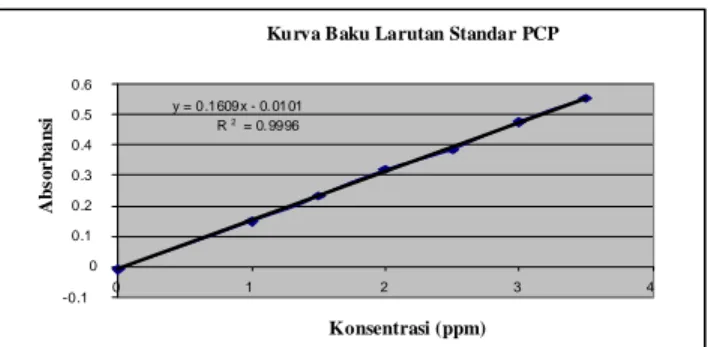
Gambar 2. Kurva standar PCP
Kurva Baku Larutan Standar PCP
y = 0.1609x - 0. 0101 R2= 0.9996 -0.1 0 0.1 0.2 0.3 0.4 0.5 0.6 0 1 2 3 4 Konsentrasi (ppm) Ab s o r b a n si
polimer terimpregnasi TiO2 yang
diharapkan telah dapat terbentuk. Dari kedua spektrum polimer
terimpregnasi TiO2 dan polimer
kontrol tampak vibrasi ulur spesifik OH sebagai pita lebar muncul pada
3.425 cm-1, vibrasi ulur C-H (aril)
berkisar antara 3.000-3.300 cm-1,
sedangkan vibrasi C-C (aril) terletak
pada 1.450-1.600 cm-1, kemudian
untuk ikatan C=C dan C=N terletak pada bilangan gelombang antara
1.500-1.900 cm-1, sehingga dapat
diasumsikan struktur molekul polimer kontrol tidak berbeda jauh dengan
polimer terimpregnasi TiO2.
Sedangkan, untuk spektra TiO2
sendiri tampak pita spesifik pada
bilangan gelombang 300-4.000 cm-1.
Pada spektrum polimer terimpregnasi
TiO2 tampak pita spesifik pada
bilangan gelombang 300-350 cm-1
yang ini tidak muncul pada polimer kontrol, tetapi vibrasi ini juga muncul
pada spektrum TiO2. Hal ini diduga
kemungkinan vibrasi tersebut sehingga secara teoritis sebagian besar struktur molekul polimer kontrol tidak berbeda jauh dengan
polimer terimpregnasi TiO2.
Namun pada polimer
ter-impregnasi TiO2 muncul serapan di
daerah bilangan gelombang 847,97
cm-1, di mana serapan ini tidak
muncul pada polimer terimpregnasi
TiO2 maupun pada TiO2 murni. Dalam
hal ini diduga serapan tersebut ialah serapan milik Ti-N atau Ti-O yang secara teoritis hanya terbentuk pada polimer ter-impregnasi
TiO2. Sedangkan, untuk
kebera-daan TiO2 sendiri
tampak pada spektrum di daerah bilangan gelombang
3500-4000 cm-1. Hal ini
menunjukkan bahwa
keberadaan TiO2 yang
bersifat seperti TiO2 murni
masih ada yang ditunjukkan dengan spektrum yang yang
identik. Melalui hasil spektra inframerah ini diduga struktur
polimer terimpregnasi TiO2 yang
diharapkan telah dapat terbentuk.
Sedangkan, untuk spektra TiO2
sendiri tampak pada bilangan
gelombang 300-4.000 cm-1. Pada
spektrum polimer terimpregnasi TiO2
tampak pita spesifik pada bilangan
gelombang 300-350 cm-1 yang mana
vibrasi ini tidak muncul pada polimer kontrol, tetapi vibrasi ini juga muncul
pada spektrum TiO2. Hal ini diduga
kemungkinan vibrasi tersebut menandakan adanya ikatan
koor-dinasi antara TiO2 dan 4-vinilpiridin,
sehingga dapat dikatakan bahwa TiO2
telah terimpregnasi ke dalam polimer dengan mengikat pada 4-vinilpiridin.
Hasil Uji Aktivitas Degradasi Fotokatalitik Polimer
Hasil pengukuran terhadap enam macam larutan standar PCP untuk menentukan persamaan kurva standarnya disajikan dalam Gambar 2.
Persamaan kurva standar yang didapatkan adalah y = 0, 0861 x –
0,0130 dengan nilai R2 = 0,9985.
Hasil uji aktivitas degradasi fotokatalitik polimer terimpregnasi
TiO2 dan polmier kontrol terhadap
larutan PCP disampaikan dalam tabel dan grafik berikut.
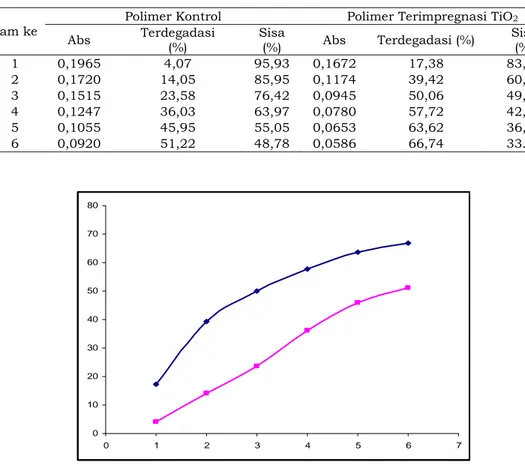
Tabel 2. Hasil Uji Aktivitas Degradasi Fotokatalitik Polimer Terhadap Larutan Standar PCP 50 ppm
Polimer Kontrol Polimer Terimpregnasi TiO2
Jam ke Abs Terdegadasi
(%) Sisa (%) Abs Terdegadasi (%) Sisa (%) 1 0,1965 4,07 95,93 0,1672 17,38 83,72 2 0,1720 14,05 85,95 0,1174 39,42 60,58 3 0,1515 23,58 76,42 0,0945 50,06 49,94 4 0,1247 36,03 63,97 0,0780 57,72 42,28 5 0,1055 45,95 55,05 0,0653 63,62 36,38 6 0,0920 51,22 48,78 0,0586 66,74 33.26 0 10 20 30 40 50 60 70 80 0 1 2 3 4 5 6 7
Gambar 3. Grafik degradasi fotokatalitik polimer terimpregnasi TiO2 dan polimer kontrol
pada larutan standar PCP
Dari hasil uji aktivitas degradasi fotokatalisis polimer di atas terlihat bahwa baik polimer kontrol maupun
polimer terimpregnasi TiO2 dapat
mendegradasi larutan PCP. Sinar UV dapat mendegradasi PCP walaupun
tanpa adanya TiO2. Adanya TiO2
sebagai katalis menaikkan kemampuan degradasi sinar UV dari 4,07% hingga 17,38% pada jam pertama dan dari 51,22% menjadi 66,74% pada jam keenam. Rendahnya kemampuan degradasi fotokatalitik
polimer terimpregnasi TiO2 dalam
hasil penelitian ini kemungkinan disebabkan kurang homogennya
sebaran TiO2 dalam polimer, kondisi
reaksi pembentukan polimer yang tidak optimal.
SIMPULAN DAN SARAN Simpulan
Dari hasil penelitian yang telah dilakukan dapat disimpulkan (1) Telah dapat dibentuk polimer
terimpregnasi TiO2 dari monomer
4-vinil piridin dan stiren dan di4-vinil benzena sebagai cross-linker; (2)
Polimer terimpregnasi TiO2
mempunyai kemampuan degradasi fotokatalisis; dan (3) sampai 66,74% pada jam keenam.
Saran
Disarankan untuk (1) menentukan kondisi optimum percampuran zat-zat agar distribusi
TiO2 lebih homogen, sehingga dapat
fotokatalisisnya; dan (2) menentukan proses degradasi fotokatalisis dalam jangka waktu yang lebih lama dari enam jam untuk mengetahui kemampuan optimalnya.
DAFTAR PUSTAKA
Chen, D and Ray, A.K., 1993.
Photocatalytic Kinetic of Phenol its Derivates over UV Irradiated TiO2,
Applied Catalysis B. Environmental, vol. 23, p.143-157
Gladis, J.M., Rao, T.P., 2003. Synthesis
and Analitical Application of Uranil Ion
Imprinted Polymer Particles, Anal
Letter, vol.36, p. 2107
Hoffman, M.R., Maretin, S.T., Choi, W., Bahnemon, D.W., 1995. Enviromental
Application of Semiconductor Photocatalysis, Chemical Review, vol.
95
Tanaka, K., Hisanaga, T., Rivera, A.P., 1993. Effect of Crystal Form of TiO2 on
The Photocataytic Degradations of Pollutants, Photocatalytic Purification