SINTESIS DAN KARAKTERISASI SERTA UJI PENDAHULUAN AKTIVITAS ANTIKANKER BEBERAPA SENYAWA
ORGANOTIMAH(IV) 2-NITROBENZOAT TERHADAP SEL LEUKIMIA L-1210
Oleh Khoirul Umam
Skripsi
Sebagai Salah Satu Syarat untuk Memperoleh Gelar SARJANA SAINS
Pada Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuan Alam
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
SINTESIS DAN KARAKTERISASI SERTA UJI PENDAHULUAN AKTIVITAS ANTIKAKER BEBERAPA SENYAWA
ORGANOTIMAH(IV) 2-NITROBENZOAT TERHADAP SEL LEUKIMIA L-1210
Oleh
Khoirul Umam
SINTHESIS, CHARACTHERIZATION, AND PRELIMINARY SCREENING ANTICANCER ACTIVITY OF SOME ORGANOTIN(IV)
2-NITROBENZOATE COMPOUNDS AGAINTS LEUKEMIA L-1210 By
Khoirul Umam
DAFTAR ISI
Halaman
PENGESAHAN... i
ABSTRAK... ii
DAFTAR ISI……… ... iii
DAFTAR GAMBAR ... iv
DAFTAR TABEL ... v
I. PENDAHULUAN A. Latar Belakang ... 1
B. Tujuan Penelitian ... 3
C. Manfaat Penelitian ... 3
II. TINJAUAN PUSTAKA A. Timah ... 4
B. Asam 2-nitrobenzoat ... 5
C. Senyawa Organologam ... 6
D. Senyawa Organotimah ... 8
1. Senyawa organotimah halida ... . 10
2. Senyawa organotimah hidroksida dan oksida ... . 11
3. Senyawa organotimah karboksilat ... . 11
E. Aplikasi Senyawa Organotimah ... ….. 12
F. Analisis Senyawa Organotimah ... 14
1. Analisis senyawa organotimah dengan spektroskopi IR ... 14
2. Analisis senyawa organotimah dengan spektroskopi UV-Vis ... . 16
3. Analisis unsur dengan menggunakan microelemental analyzer ... . 18
G. Kanker ... . 18
H. Darah ... .. 19
I. Uji Pendahuluan Aktivitas Antikanker Senyawa Organotimah Terhadap Sel Leukimia L-1210.. ... . 20
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian ... 22 B. Alat dan Bahan ... 22 C. Metode Penelitian... 23
1. Sintesis senyawa dibutiltimah(IV) oksida dan dibutiltimah(IV) di-2-nitrobenzoat ... 23 2. Sintesis senyawa difeniltimah(IV) dihidroksida dan
difeniltimah(IV) di-2-nitrobenzoat... 25 3. Sintesis senyawa trifeniltimah(IV) hidroksida dan
trifeniltimah(IV) 2-nitrobenzoat... 27 4. Pengujian aktivitas antikanker Terhadap Sel Leukimia L-1210 ... 28 5. Analisis probit ... 30
IV. HASIL DAN PEMBAHASAN
A. Sintesis……… 32
1. Sintesis senyawa dibutiltimah(IV) oksida [(C4H9)2SnO] dan
dibutiltimah(IV) di-2-nitrobenzoat [(C4H9)2Sn(C6H4(HO2C)NO2)2]. 32 2. Sintesis senyawa difeniltimah(IV) dihidroksida [(C6H5)2Sn(OH)2] dan difeniltimah(IV) di-2-nitrobenzoat[(C6H5)2Sn(C6H4(HO2C)NO2)2].. 34 3. Sintesis senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH] dan
trifeniltimah(IV) 2-nitrobenzoat [(C6H5)3Sn(C6H4HOOCNO2)]….. 36 B. Karakterisasi Menggunakan Spektrofotometer IR………. 37 1. Senyawa asam 2-nitrobenzoat ((C6H5)OCOHNO2)……….. 37 2. Senyawa dibutiltimah(IV) oksida [(C4H9)2SnO] dan dibutiltimah(IV)
di-2-nitrobenzoat [(C4H9)2Sn(C6H4(HO2C)NO2)2]……… 38 3. Senyawa difeniltimah(IV) dihidroksida [(C6H5)2Sn(OH)2] dan
difeniltimah(IV) di-2-nitrobenzoat[(C6H5)2Sn(C6H4(HO2C)NO2)2].. 40 4. Senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH] dan
trifeniltimah(IV) 2-nitrobenzoat [(C6H5)3Sn(C6H4HOOCNO2)]...… 41 C. Karakterisasi dengan Spektrofotometer UV-Vis……….43 1. Senyawa asam 2-nitrobenzoat……… 43 2. Senyawa dibutiltimah(IV) oksida [(C4H9)2SnO] dan dibutiltimah(IV)
di-2-nitrobenzoat [(C4H9)2Sn(C6H4(HO2C)NO2)2]……… 44 3. Senyawa difeniltimah(IV) dihidroksida [(C6H5)2Sn(OH)2] dan
difeniltimah(IV) di-2-nitrobenzoat[(C6H5)2Sn(C6H4(HO2C)NO2)2].. 45 4. Senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH] dan
trifeniltimah(IV) 2-nitrobenzoat [(C6H5)3Sn(C6H4HOOCNO2)]….. 47 D. Analisis Unsur Menggunakan Microelemental Analyzer………. 48 E. Uji Aktivitas Antikanker Terhadap Sel Leukemia L-1210……… 49
V. SIMPULAN DAN SARAN
A. Simpulan ………...………. 56
B. Saran………... 58
I. PENDAHULUAN
A. Latar Belakang
Dewasa ini, pencarian agen antikanker sedang berkembang. Salah satunya yaitu dengan menggunakan senyawa organotimah. Senyawa organotimah merupakan senyawa dimana atom-atom karbon dari gugus organik terikat pada logam timah.
Senyawa organotimah dapat berbentuk mono, di, tri dan tetraorganotimah bergantung pada gugus alkil (R) atau aril (Ar) yang terikat pada Sn. Senyawa
organotimah(IV) merupakan senyawa yang dikenal memiliki berbagai aktivitas biologis. Sebagian besar senyawa organotimah(IV) bersifat sangat toksik, bahkan pada konsentrasi yang sangat rendah sekalipun (Pellerito and Nagy, 2002).
Senyawa organotimah(IV) ini mempunyai aplikasi yang luas diantaranya sebagai katalis, antifouling agents, biopestisida pertanian dan antitumor.
Senyawa organotimah(IV) 2-nitrobenzoat dipilih dalam penelitian ini berdasarkan aktivitas biologisnya berdasarkan gugus aktif yang diikat logam pusatnya. Dari penelitian sebelumnya, (Aini, 2010; Elianasari, 2012; Sulistriani, 2012),
organotimah(IV) dengan asam hidroksibenzoat sebagai asam karboksilat, mempunyai aktivitas biologis yaitu sebagai antikanker. Pada penelitian kali ini,
Penelitian ini dilakukan untuk mensintesis senyawa dibutiltimah(IV)
di-nitrobenzoat, difeniltimah(IV) di-nitrobenzoat dan trifeniltimah(IV) 2-nitrobenzoat.
Sel Leukimia L-1210 pada penelitian ini dikembangkan dalam media RPMI-1640, yang mengandung L-Glutamin. Sel leukimia L-1210 direaksikan dengan kristal
organotimah(IV) dalam pelarut metanol. Sel hidup dihitung menggunakan haemocytometer Neubauer improved, di bawah mikroskrop. Jika IC50 dari
senyawa ini adalah ≤ 50 µg/mL, maka kemungkinan, senyawa organotimah(IV)
2-nitrobenzoat berpotensi menjadi senyawa antikanker (Mans et al, 2000). Penelitian sebelumnya (Aini, 2010) menggunakan asam salisilat sebagai asam
karboksilatnya, dan diperoleh IC50 3,86 g/mL. Pada penelitian selanjutnya (Sari, 2011) aktivitas antikanker senyawa organotimah(IV) benzoat diperoleh nilai IC50 5,32 g/mL dan pada penelitian lain (Sulistriani, 2012) aktivitas antikanker
senyawa organotimah(IV) 3-hidroksibenzoat diperoleh nilai IC50 3,10 g/mL. Pada penelitian ini diharapkan IC50 yang diperoleh dapat lebih kecil dari penelitian sebelumnya.
Bila telah diketahui dan diperoleh data aktivitas awalnya, maka untuk penelitian selanjutnya akan lebih mudah pengembangannya sebagai new metal-based drugs
B. Tujuan Penelitian
Tujuan dari penelitian ini adalah sebagai berikut:
1. Mensintesis senyawa dibutiltimah(IV) di-2-nitrobenzoat, difeniltimah(IV) di-2-nitrobenzoat dan trifeniltimah(IV) 2-nitrobenzoat.
2. Mengkarakterisasi senyawa dibutiltimah(IV) di-2-nitrobenzoat,
difeniltimah(IV) di-2-nitrobenzoat dan trifeniltimah(IV) 2-nitrobenzoat.
Sebagai perbandingan, bahan baku pembuatan senyawa ini seperti dibutiltimah(IV) diklorida, difeniltimah(IV) diklorida, dan
trifeniltimah(IV) klorida serta senyawa yang dihasilkan seperti
dibutiltimah(IV) oksida, difeniltimah(IV) dihidroksida dan trifeniltimah(IV) hidroksida, juga dikarakterisasi.
3. Menguji dan membandingkan aktivitas antikanker dari senyawa
dibutiltimah(IV) di-2-nitrobenzoat, difeniltimah(IV) di-2-nitrobenzoat dan trifeniltimah(IV) 2-nitrobenzoat terhadap sel leukemia L-1210.
C. Manfaat Penelitian
Hasil penelitian ini diharapkan dapat memberikan sumbangan terhadap
II. TINJAUAN PUSTAKA
A. Timah (Sn)
Timah merupakan unsur golongan IVA (grup 14) dalam tabel periodik, bersama dengan karbon, silikon, germanium, dan timbal. Timah menunjukkan kesamaan sifat kimia dengan Ge dan Pb seperti pembentukan keadaan oksidasi +2 dan +4.
Sebagai anggota dalam golongan IVA, struktur geometri SnCl4 yang telah dikarakterisasi ialah tetrahedral seperti CCl4. Pada suhu ruang, keduanya cairan
tidak berwarna dengan titik didih masing-masing 114°C dan 77°C (pada tekanan atmosfer). Di luar keadaan tersebut, keduanya menunjukkan karakter yang cukup berbeda. Perbedaan tersebut dapat dijelaskan karena ukuran atom Sn yang lebih
besar dibandingkan atom C dan dimilikinya orbital 5d pada atom Sn. Kedua faktor tersebut, membuat Sn memungkinkan untuk “berikatan lebih” (ekstra koordinasi) dengan ligan-ligannya. Dalam hal tersebut, timah memiliki
fleksibilitas valensi yang lebih besar, yaitu memiliki bilangan koordinasi yang dapat lebih dari empat (Purnomo, 2008).
Timah memiliki tiga bentuk alotrop, yaitu timah abu-abu (α), timah putih ( ), dan timah rombik ( ). Pada suhu ruang, timah lebih stabil sebagai logam timah putih
ini terjadi cepat karena timah membentuk oksida film. Peristiwa ini dikenal
sebagai plak timah atau timah plague.
Timah dalam bentuk senyawaannya memiliki tingkat oksidasi +2 dan +4, tingkat
oksidasi +4 lebih stabil dari pada +2. Pada tingkat oksidasi +4, timah
menggunakan seluruh elektron valensinya, yaitu 5s2 5p2 dalam ikatan, sedangkan
pada tingkat oksidasi +2, timah hanya menggunakan elektron valensi 5p2 saja. Tetapi perbedaan energi antara kedua tingkat ini rendah (Cotton dan Wilkinson, 1989).
Akan tetapi jika timah dalam bentuk kompleksnya, seperti organotimah, ternyata timah menjadi bermanfaat, karena diketahui organotimah, khususnya
organotimah(IV) mempunyai berbagai macam aktivitas biologis , seperti
antimikroba (Bonire et al., 1998; Mahmood et al.,2003), antitumor (de Vos et al., 1998; Hadi, S. & Rilyanti, M., 2010; Gielen, 2003),dan antijamur (Ruzika et al., 2002; Mahmood et al., 2003; Hadi et al.,2007; Hadi et al., 2008).
B. Asam 2-Nitrobenzoat
organotimah(IV) dengan asam 2-nitrobenzoat juga mempunyai aktivitas biologis yaitu sebagai senyawa antikanker. Struktur asam 2-nitrobenzoat dapat dilihat
Gambar 1. Struktur asam-2-nitrobenzoat
Asam-2-nitrobenzoat memiliki rumus kimia C7H5NO4. Selain asam nitrobenzoat, biasa juga disebut dengan o-nitrobenzoic acid dan juga
2-nitrobenzoic acid. Asam ini berbentuk bubuk berwarna putih, dan memiliki titik
lebur 146-148C. Asam ini memiliki stabilitas yang cukup baik. Kompatibel
dengan oksidator kuat, kuat basa, dan memiliki berat molekul: 167.1189 g/mol
(Caslab, 2013).
C. Senyawa Organologam
Senyawa organologam merupakan senyawa dimana minimal terdapat satu atom karbon dari gugus organik yang berikatan langsung dengan logam. Istilah
organologam biasanya didefinisikan agak longgar, dan senyawa yang
mengandung ikatan karbon dengan fosfor, arsen, silikon, ataupun boron termasuk
dalam kategori ini. Tetapi untuk senyawa yang mengandung ikatan antara atom logam dengan oksigen, belerang, nitrogen ataupun dengan suatu halogen tidak termasuk sebagai senyawa organologam. Sebagai contoh suatu alkoksida seperti
(C3H7O4)Ti tidaklah termasuk senyawa organologam, karena gugus organiknya terikat pada Ti melalui atom oksigen. Sedangkan senyawa (C6H5)Ti(OC3H7)3
C dari gugus fenil dengan logam Ti. Dari bentuk ikatan pada senyawa
organologam, senyawa ini dapat dikatakan sebagai jembatan antara kimia organik dan anorganik (Cotton dan Wilkinson, 1989).
Berdasarkan keelektronegatifannya, pada umumnya jika unsur-unsur yang berikatan dengan dengan karbon berada pada bilangan oksidasi negatif, turunan
organiknya sebagai senyawaan organik. Turunan senyawa organik dimana unsur-unsur yang berikatan dengan karbon berada pada oksidasi positif, termasuk senyawaan organologam (Tayer, 1988).
Berdasarkan ikatannya, senyawa organologam dapat dikelompokkan menjadi tiga golongan:
A. Senyawa ionik dari logam elektropositif
Senyawa ini terbentuk bila suatu radikal organik terikat pada logam dengan keelektropositifan yang sangat tinggi, misalnya logam alkali atau alkali tanah.
Senyawa-senyawa ini tidak stabil di udara, mudah terhidrolisis dalam air dan tidak larut dalam pelarut hidrokarbon. Kestabilannya bergantung pada kestabilan radikal organiknya.
B. Senyawa organologam dengan ikatan σ (sigma)
Senyawa ini memiliki ikatan σ dua pusat dua elektron yang terbentuk antara
gugus organik dan atom logam dengan keelektropositifan rendah. Pada umumnya, senyawa organologam dengan ikatan ini memiliki ikatan utama kovalen dan sifat kimianya adalah dari kimiawi karbon yang disebabkan
a. Kemungkinan penggunaan orbital d yang lebih tinggi, seperti pada SiR4
yang tidak tampak dalam CR4.
b. Kemampuan donor alkil atau aril dengan pasangan elektron menyendiri.
c. Keasaman Lewis sehubungan dengan kulit valensi yang tidak penuh seperti pada BR2 atau koordinasi tak jenuh seperti ZnR2.
d. Pengaruh perbedaan keelektronegatifan antara ikatan logam-karbon (M-C)
atau karbon-karbon (C-C).
C. Senyawa organologam dengan ikatan nonklasik
Dalam senyawa organologam dengan ikatan nonklasik ini terdapat jenis ikatan antara logam dengan karbon yang tidak dapat dijelaskan secara ikatan ionik
atau pasangan elektron. Senyawa ini terbagi menjadi dua golongan: a. Senyawa organologam yang terbentuk antara logam-logam transisi
dengan alkena, alkuna, benzene, dan senyawa organik tak jenuh lainnya.
b. Senyawa organologam yang memiliki gugus-gugus alkil berjembatan. (Cotton dan Wilkinson, 1989).
D. Senyawa Organotimah
Senyawa organotimah adalah senyawa-senyawa yang mengandung sedikitnya satu ikatan kovalen C-Sn. Sebagian besar senyawa organotimah dapat dianggap sebagi
turunan dari RnSnX4-n (n = 1-4) dan diklasifikasikan sebagai mono-, di-, tri-, dan tetra- organotimah (IV), tergantung pada jumlah gugus alkil (R) atau aril (Ar)
Sn-X memiliki derajat ion tertentu bergantung pada anion (X) dan alkil (R).
Sebagai contoh, titik leleh dari (CH3)3SnX bervariasi untuk: fluorida (300C) > klorida (37C) > bromida (27C) > iodida (3,4C) (Tayer, 1988). Pemanfaatan
senyawa organotimah diantaranya sebagai penstabil dalam produksi plastik, pestisida dalam pertanian, katalis, pelapis kaca, stabilizer poliviniklorida,
antikanker dan antitumor (Gielen, 2003), antifouling agents pada cat (Blunden and Hill, 1990), antimikroba dan antifungi (Bonire et al., 1998).
Kecenderungan terhidrolisis dari senyawa organotimah lebih lemah dibandingkan senyawa Si atau Ge yang terkait dan ikatan Sn-O dapat bereaksi dengan larutan
asam. Senyawa organotimah tahan terhadap hidrolisis atau oksidasi pada kondisi normal walaupun dibakar menjadi SnO2, CO2, dan H2O. Kemudahan putusnya ikatan Sn-C oleh halogen atau reagen lainnya bervariasi berdasarkan gugus
organiknya dan urutannya meningkat dengan urutan: Bu (paling stabil) < Pr < et < me < vinil < Ph < Bz < alil < CH2CN < CH2CO2R (paling tidak stabil).
Penggabungan SnR4 melalui gugus alkil tidak teramati sama sekali. Senyawa-senyawa dengan rumus R3SnX atau R2SnX2 tergabung secara luas melalui jembatan X sehingga meningkatkan bilangan koordinasi Sn menjadi lima, enam
atau bahkan tujuh. Dalam hal ini, F lebih efektif dibandingkan unsur-unsur halogen lainnya. Sebagai contoh Me3SnF memiliki struktur trigonal bipiramida, Me2SnF2 memiliki struktur oktahedral sedangkan jembatan Cl yang lebih lemah
memiliki struktur terdistorsi.
Kereaktifan dari senyawa organotimah(II) tinggi seperti dialkil timah dan diaril
pada senyawa organotimah yang memilki kestabilan divalen (a) kemungkinan
besar pada senyawa organik, (b) bentuk adduct dengan basa Lewis atau (c) pasangan menyendiri Sn terkoordinasi. Pada asam Lewis yang sesuai perbedaan
bilangan koordinasi dan geometri juga mungkin terjadi pada senyawa
organotimah(II) pada penggunaan orbital 5d, yaitu trigonal planar (hibridisasi sp2), tetrahedral (sp3), trigonal bipiramida (sp3d), dan oktahedral (sp3d2) (Van der
Weij, 1981).
1. Senyawa organotimah halida
Senyawa organotimah halida dengan rumus umum RnSnX4-n (n = 1-3; X = Cl, Br, I) pada umumnya merupakan padatan kristalin dan sangat reaktif. Organotimah
halida ini dapat disintesis secara langsung melalui logam timah, Sn(II) atau Sn(IV) dengan alkil halida yang reaktif. Metode ini secara luas digunakan untuk pembuatan dialkiltimah dihalida. Sintesis langsung ini ditinjau ulang oleh
Murphy dan Poller melalui persamaan reaksi:
2 EtI + Sn Et2Sn + I2
Metode lain yang sering digunakan untuk pembuatan organotimah halida adalah
reaksi disproporsionasi tetraalkiltimah dangan timah(IV) klorida. Caranya adalah dengan mengubah perbandingan material awal, seperti ditunjukkan pada
persamaan reaksi berikut:
3 R4Sn + SnCl4 4 R3SnCl
Senyawa organotimah klorida digunakan sebagai kloridanya dengan memakai
logam halida lain yang sesuai seperti ditunjukkan pada persamaan reaksi berikut: R4SnCl4-n + (4-n) MX R4SnX4-n + (4-n) MCl
(X = F, Br atau I; M = K, Na, NH4) (Cotton danWilkinson, 1989).
2. Senyawa organotimah hidroksida dan oksida
Produk kompleks yang diperoleh melalui hidrolisis dari trialkiltimah halida dan senyawa yang berikatan R3SnX, merupakan rute utama pada trialkiltimah oksida
dan trialkiltimah hidroksida.
Prinsip tahapan intermediet ditunjukkan pada reaksi di bawah ini:
OH
R3SnX R3Sn XR3SnOSnR3X XR3SnOSnR3OH R2SnO
X atau
R3SnOH
(Cotton dan Wilkinson, 1989).
3. Senyawa organotimah karboksilat
Senyawa organotimah karboksilat pada umumnya dapat disintesis melalui dua
cara yaitu dari organotimah oksida atau organotimah hidroksidanya dengan asam karboksilat, dan dari organotimah halidanya dengan garam karboksilat. Metode
yang biasa digunakan untuk sintesis organotimah karboksilat adalah dengan menggunakan organotimah halida sebagai material awal. Organotimah halida direaksikan dengan garam karboksilat dalam pelarut yang sesuai, biasanya aseton
Reaksinya adalah sebagai berikut:
RnSnCl4-n + (4-n) MOCOR RnSn(OCOR)4-n + (4-n) MCl Reaksi esterifikasi dari asam karboksilat dengan organotimah oksida atau
hidroksida dilakukan melalui dehidrasi azeotropik dari reaktan dalam toluena, seperti ditunjukkan pada reaksi berikut:
R2SnO + β R’COOH R2Sn(OCOR’)2 + H2O R3SnOH + R’COOH R3SnOCOR’ + H2O
(Cotton dan Wilkinson, 1989).
E. Aplikasi Senyawa Organotimah
Senyawa organotimah memiliki aplikasi yang luas dalam kehidupan sehari-hari.
Aplikasi senyawa organotimah dalam industri antara lain sebagai senyawa
stabilizer polivinilklorida, pestisida nonsistematik, katalis antioksidan, antifouling
agents dalam cat, stabilizer pada plastik dan karet sintetik, stabilizer untuk parfum
dan berbagai macam peralatan yang berhubungan dengan medis dan gigi. Untuk penggunaan tersebut, kurang lebih 25.000 ton timah dipergunakan per tahun (Pellerito and Nagy, 2002).
Mono dan diorganotimah digunakan secara luas sebagai stabilizer polivinilklorida untuk mengurangi degradasi polimer polivinilklorida tersebut. Empat tipe utama
penstabil timah berdasarkan gugus alkilnya yaitu: oktil, butil, fenil, dan metil. Dimana oktiltimah memiliki kandungan timah paling sedikit, paling kurang
yang paling umum digunakan sebagai katalis dalam sintesis kimia yaitu katalis
mono dan diorganotimah. Senyawa organotimah merupakan katalis yang bersifat homogen yang baik untuk pembuatan polisilikon, poliuretan dan untuk sintesis
poliester.
Senyawa organotimah ditemukan berikutnya antara lain sebagai biocide (senyawa
yang mudah terdegradasi), sebagai pestisida yang pertama kali diperkenalkan di Jerman yaitu dari senyawa trifeniltimah asetat pada akhir 1950-an. Kegunaan yang utama dari agrokimia senyawa organotimah karena senyawa ini relatif
memiliki fitotoksisitas (daya racun pada tanaman) yang rendah dan terdegradasi dengan cepat sehingga residunya tidak berbahaya terhadap lingkungan (Cotton
dan Wilkinson, 1989).
Senyawa organotimah(IV) telah diketahui memiliki aktivitas biologi yang kuat. Sebagian besar senyawa organotimah(IV) bersifat toksik walaupun pada
konsentrasi rendah. Aktivitas biologi ini ditentukan oleh jumlah gugus organik yang terikat pada pusat atom Sn. Senyawa organotimah karboksilat diberikan perhatian khusus dikarenakan senyawa ini memiliki kemampuan biologi yang
kuat dibandingkan senyawa organotimah lainnya (Mahmood et al., 2003; Pellerito and Nagy, 2002).
Dalam beberapa penelitian, diketahui senyawa organotimah(IV) karboksilat yang menunjukkan sifat sebagai antimikroorganisme sehingga dapat berfungsi sebagai antifungi dan antimikroba (Bonire et al., 1998). Diketahui bahwa kompleks di-
sebagai fungisida dalam pertanian, bakterisida, dan agen antitumor (Jain et al.,
2003).
F. Analisis Senyawa Organotimah
Senyawa organotimah karboksilat dapat diidentifikasi dengan menggunakan spektroskopi Inframerah (IR), UV-VIS, (Pellerito and Nagy, 2002), dan analisis
unsur C, H, N, dan S dalam suatu senyawa dengan menggunakan alat microelemental analyzer.
1. Analisis senyawa organotimah dengan spektroskopi IR
Pada spektroskopi IR, radiasi infra merah dengan rentangan panjang gelombang
dan intensitas tertentu dilewatkan terhadap sampel. Molekul-molekul senyawa pada sampel akan menyerap seluruh atau sebagian radiasi itu. Penyerapan ini berhubungan dengan adanya sejumlah vibrasi yang terkuantisasi dari atom-atom
yang berikatan secara kovalen pada molekul-molekul itu.
Spektra IR memberikan absorpsi yang bersifat aditif atau bisa juga sebaliknya. Sifat aditif disebabkan karena overtone dari vibrasi-vibrasinya. Penurunan
absorpsi disebabkan karena kesimetrian molekul, sensitifitas alat, dan aturan seleksi. Aturan seleksi yang mempengaruhi intensitas serapan IR ialah perubahan
momen dipol selama vibrasi yang dapat menyebabkan molekul menyerap radiasi IR. Dengan demikian, jenis ikatan yang berlainan (C-H, C-C, atau O-H)
menyerap radiasi IR pada panjang gelombang yang berlainan. Suatu ikatan dalam
Puncak-puncak yang muncul pada daerah 4000-1450 cm-1biasanya berhubungan dengan
energi untuk vibrasi uluran diatomik. Daerahnya dikenal dengan group frequency region.
Tabel 1. Serapan inframerah gugus fungsional senyawa organik.
Bilangan gelombang (cm-1)
Tipe
ikatan Keterangan
3200-3600 -O-H Ikatan hidrogen dapat memperlebar absorpsi. Ikatan hidrogen internal yang sangat kuat dapat menutupi serapan C-H alifatik dan aromatik.
3350-3500 N-H Untuk amina primer memberikan dua puncak, amina sekunder memberikan satu puncak, amina tersier tidak memberikan serapan.
3310-3320 C-H asetilenik
Terdapat pada semua molekul organik, karenanya kegunaannya untuk analisis gugus fungsi terbatas. 3000-3100 C-H aromatik dan etilenik 2850-2950 C-H
alkana
2500-3600 -COOH
Serapan gugus karboksilat sangat lebar, kuat. Puncak tajam dekat 3500 cm-1 menunjukkan vibrasi O-H bebas (yang tidak berikatan hidrogen).
1680-1700 R-CON<
Vibrasi gugus karbonil amida sekunder muncul dengan satu puncak, sedangkan untuk amida tersier tidak muncul puncak.
Secara umum, spektrum serapan IR dapat dibagi menjadi tiga daerah:
b. Inframerah sedang, dengan bilangan gelombang antara 4.000 hingga
650 cm-1. Fenomena yang terjadi ialah vibrasi dan rotasi.
c. Inframerah jauh, dengan bilangan gelombang 650 hingga 200 cm-1. Fenomena
yang terjadi ialah penyerapan oleh ligan atau spesi lainnya yang berenergi rendah.
2. Analisis senyawa organotimah dengan spektroskopi UV-Vis
Spektroskopi sinar UV-Vis akan mengalami transisi elektronik sebagai akibat
penyerapan radiasi sinar UV-Vis dan sinar tampak oleh senyawa yang dianalisis. Transisi tersebut pada umumnya antara orbital ikatan atau pasangan bebas dan
orbital bukan ikatan atau orbital anti ikatan. Panjang gelombang serapan merupakan ukuran perbedaan tingkat-tingkat energi dari orbital-orbital yang bersangkutan. Agar elektron dalam ikatan sigma tereksitasi maka diperlukan
energi paling tinggi dan akan memberikan serapan pada 120-200 nm (1 nm =10-7 cm =10Ǻ ). Daerah ini dikenal sebagai daerah ultraviolet hampa, karena pada
pengukuran tidak boleh ada udara, sehingga sukar dilakukan dan relatif tidak
banyak memberikan keterangan untuk penentuan struktur.
Di atas 200 nm merupakan daerah eksitasi elektron dari orbital p, orbital d, dan orbital π terutama sistem π terkonjugasi mudah pengukurannya dan spektrumnya
memberikan banyak keterangan. Kegunaan spektrofotometer UV-Vis ini terletak pada kemampuannya mengukur jumlah ikatan rangkap atau konjugasi aromatik di
sebgainya. Letak serapan dapat dipengaruhi oleh substituen dan terutama yang
berhubungan dengan substituen yang menimbulkan pergeseran dalam diena terkonjugasi dan senyawa karbonil.
Pada spektroskopi UV-Vis, spektrum tampak (vis) terentang dari sekitar 400 nm (ungu) sampai 750 (merah), sedangkan spektrum ultraviolet (UV) terentang dari
200-400 nm. Informasi yang diperoleh dari spektroskopi ini adalah adanya ikatan rangkap atau ikatan terkonjugasi dan gugus kromofor yang terikat pada ausokrom. Semua molekul dapat menyerap radiasi dalam daerah UV-Vis karena mereka
mengandung elektron, baik sekutu maupun menyendiri, yang dapat dieksitasikan ke tingkat energi yang lebih tinggi. Panjang gelombang terjadinya adsorpsi
tergantung pada kekuatan elektron terikat dengan kuat dan diperlukan radiasi berenergi tinggi atau panjang gelombang yang pendek atau eksitasinya. Hal ini berarti suatu elektron dalam orbital (bonding) dieksitasikan ke orbital
antibonding.
Identifikasi kualitatif senyawaan organik dalam daerah ini jauh lebih terbatas daripada dalam daerah inframerah, dikarenakan pita serapan pada daerah UV-Vis
terlalu lebar dan kurang terperinci. Tetapi gugus-gugus fungsional tertentu seperti karbonil, nitro, dan sistem tergabung menunjukan puncak karakteristik dan dapat
3. Analisis unsur dengan microelemental analyzer
Mikroanalisis adalah penentuan kandungan unsur penyusun suatu senyawa yang dilakukan dengan menggunakan microelemental analyzer. Unsur yang umum
ditentukan adalah karbon (C), hidrogen (H), nitrogen (N), sulfur (S).
Sehingga alat yang biasanya digunakan untuk tujuan mikroanalisis ini dikenal sebagai CHNS microelemental analyzer. Hasil yang diperoleh dari mikroanalisis
ini dibandingkan dengan perhitungan secara teori. Walaupun seringnya hasil yang diperoleh berbeda, perbedaan biasanya antara 1–5%, namun analisis ini tetap
sangat bermanfaat untuk mengetahui kemurnian suatu sampel (Costecsh Analytical Technologies, 2011).
G. Kanker
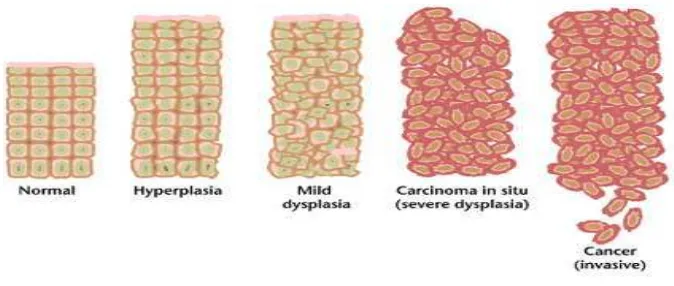
Berdasarkan National Institute of Health (2006), kanker adalah penyakit yang disebabkan oleh pertumbuhan sel-sel jaringan tubuh yang tidak terkontrol, invasi sel ke jaringan lain yang berpotensi untuk melakukan metastasis, akibat dari
akumulasi mutasi genetik yang terjadi dalam tubuh manusia yang menyebabkan perubahan sifat dari sel-sel normal. Pada sel normal, jumlah antara sel yang lahir
dengan sel yang mati akan seimbang untuk memelihara kestabilan dalam tubuh, namun pada induk kanker perbandingan antara sel yang lahir jauh lebih besar dibandingkan sel yang mati. Sel induk kanker memiliki kemampuan dalam
Gambar 2. Perkembangan sel normal menjadi sel kanker (Anand and Kunnumakkara, 2008).
Kanker terjadi karena adanya perubahan mendasar dalam fisiologi sel yang akhirnya tumbuh menjadi malignan serta mempunyai ciri-ciri umum sebagai berikut: (1) mandiri dalam signal pertumbuhan, (2) tidak peka terhadap signal
antipertumbuhan, (3) menghindari apoptosis, (4) memiliki potensi replikasi yang tidak terbatas, (5) angiogenesis, (6) invasi, dan metastase ke jaringan lain
(Manahan and Wienberg, 2002).
H. Darah
Darah adalah suatu suspensi partikel dalam suatu larutan koloid cair yang
mengandung elektrolit. Darah berperan sebagai medium pertukaran antara sel yang terfiksasi dalam tubuh dan lingkungan luar, serta memiliki sifat protektif terhadap organisme dan khususnya terhadap darah sendiri. Komponen cair darah
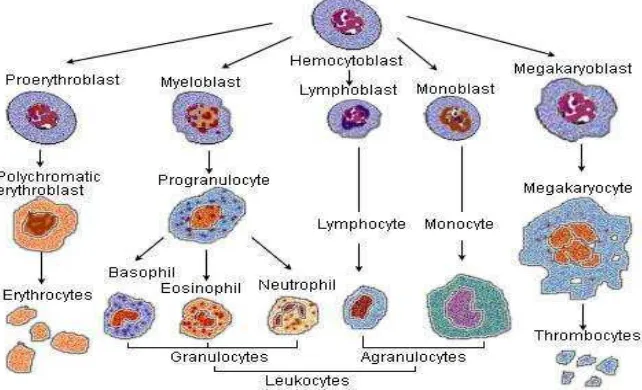
Unsur sel darah (Gambar 3) terdiri dari:
1. Sel darah merah (eritrosit)
2. Beberapa jenis sel darah putih (leukosit) 3. Fragmen sel yang disebut trombosit
Eritrosit berfungsi sebagai transpor atau pertukaran oksigen dan karbondioksida, leukosit berfungsi untuk mengatasi infeksi, dan trombosit untuk hemostatis.
Gambar 3. Unsur sel darah
Sel-sel ini mempunyai umur yang terbatasl, sehingga diperlukan pembentukan optimal yang konstan untuk mempertahankan jumlah yang diperlukan untuk memenuhi kebutuhan jaringan (Price dan Wilson, 2005).
I. Uji Pendahuluan Aktivitas Antikanker Senyawa Organotimah Terhadap Sel Leukemia L-1210
antikanker ini adalah sel leukemia yang diperoleh dari sel limfosit tikus putih
betina jenis DBA (Dilute Brown Non-Agouti Mouse) yang berumur 8 bulan. Sel leukemia ini diambil dari The Institute of Physical and Chemical Research, Japan
yang secara rutin telah digunakan untuk uji senyawa antikanker, baik in vitro maupun in vivo (Hoshino et al., 1966). Ekstrak kasar dari suatu bahan alam atau aktivitas isolat (kristal) dapat diuji secara langsung dalam biakan sel leukemia
L-1210. Sebagai ukuran aktivitas sitotoksik ditentukan nilai IC50 dari ekstrak kasar tersebut. Aktivitas isolat (kristal) dikatakan aktif sebagai anti kanker bila nilai
IC50 ≤ 50 µg/mL (Mans et al., 2000).
J. Analisis Probit
Analisis probit adalah model regresi khusus yang digunakan untuk menganalisis variabel respon binomial. Ide analisis probit pada mulanya dipublikasikan dalam
majalah Science oleh Cester Ittner Bliss pada tahun 1934 yang digunakan untuk mengetahui efektivitas suatu pestisida dengan memplotkan kurva hubungan antara dosis dan respon pada berbagai konsenterasi, dan diperoleh kurva berbentuk
sigmoid (Bliss, 1934). Bliss mengembangkan ide untuk mengubah kurva sigmoid tersebut ke dalam persamaan garis lurus. Pada tahun 1952 seorang profesor
statistik dari Edinburgh yang bernama David Finney menggunakan ide Bliss dan menulis buku yang berjudul Analisis Probit. Sampai saat ini analisis probit masih digunakan untuk mengetahui hubungan antara dosis dan respon (Cochran and
III. METODOLOGI PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilakukan pada bulan April sampai Juni 2013 di Laboratorium Kimia Anorganik FMIPA Universitas Lampung. Analisis senyawa menggunakan spektrofotometer IR dilakukan di Laboratorium Instrumentasi FMIPA Universitas
Islam Indonesia dan analisis dengan spektrofotometer UV-Vis dilakukan di
Laboratorium Kimia Anorganik dan Fisik FMIPA Universitas Lampung. Analisis
unsur dengan menggunakan microelemental analyzer dilakukan di School of Chemical and Food Technology, Universiti Kebangsaan Malaysia. Sedangkan uji aktivitas antikanker dilakukan di BATAN, Jakarta Selatan.
B. Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah: gelas piala, gelas ukur, pipet
tetes, batang pengaduk, corong, satu set alat refluks, hot plate stirrer, kertas saring Whatman No. 42, botol sampel, desikator, spektrofotometer IR (karakterisasi),
spektrofotometer UV-Vis (karakterisasi), microelemental analyzer (analisis unsur)
Bahan-bahan yang digunakan dalam penelitian ini adalah dibutiltimah(IV)
diklorida, difeniltimah(IV) diklorida, trifeniltimah(IV) klorida, NaOH, metanol p.a, akuabides, asam 2-nitrobenzoat, toluena, dan isolat sel leukimia L-1210
BATAN, Jakarta Selatan.
C. Metode Penelitian
Prosedur untuk sintesis senyawa organotimah(IV) karboksilat pada penelitian ini diadopsi dari prosedur yang dilakukan oleh Szorscik et al. (2002); Hadi et al. (2008); dan Hadi et al. (2009); serta pemurnian yang dilakukan oleh Bonire et al.
(1998).
1. Sintesis senyawa dibutiltimah(IV) oksida [(C4H9)2SnO] dan
dibutiltimah(IV) di-2-nitrobenzoat [(C4H9)2Sn(C6H4(HO2C)NO2)2]
Dibutiltimah(IV) diklorida [(C4H9)2SnCl2] sebanyak 0,045 mol (13,68 gram)
direaksikan dengan 0,09 mol (3,6 gram) NaOH untuk mengganti ligan klor dengan oksida dalam 50 mL pelarut metanol p.a dengan distirer ± 1 jam dan suhu 60oC. Selanjutnya endapan yang dihasilkan disaring dengan menggunakan kertas
saring Whatman No. 42, lalu dicuci dengan akuabides dan metanol p.a. kemudian didiamkan di dalam desikator vakum untuk menghasilkan (C4H9)2SnO. Kristal
(C4H9)2SnCl2 dan (C4H9)2SnO dikarakterisasi dengan spektrofotometer IR, spektrofotometer UV-Vis.
perbandingan mol 1:2 dalam 30 mL pelarut metanol p.a dan direfluks dengan
variasi waktu 3, 4, dan 5 jam dengan pemanas pada suhu 60℃. Setelah reaksi
sempurna, metanol diuapkan dan dikeringkan di dalam desikator vakum sampai diperoleh kristal kering. Kristal kering tersebut dilarutkan dengan toluena dengan
dibantu pemanasan hingga larut, lalu didinginkan dengan es dalam keadaan masih panas, senyawa murni akan mengendap, kemudian dipisahkan dari pelarutnya.
Setelah itu, dilakukan pengeringan kembali dengan desikator hingga diperoleh kristal dengan berat konstan. Kristal hasil senyawa dengan rendemen tertinggi dari variasi waktu refluks tersebut siap untuk dikarakterisasi dengan
spektrofotometer IR, spektrofotometer UV-Vis, analisis kandungan unsur C dan H dengan alat microelemental analyzer, dan diuji sifat antikankernya terhadap sel
leukimia L-1210. Sebagai perbandingan, asam 2-nitrobenzoat juga dikarakterisasi dengan spektrofotometer IR, spektrofotometer UV-Vis, dan dianalisis kandungan unsur C dan H dengan alat microelemental analyzer. Skema reaksi dari sintesis ini
Gambar 4. Skema reaksi sintesis senyawa dibutiltimah(IV) oksida [(C4H9)2SnO] dan dibutiltimah(IV) di-2-nitrobenzoat [(C4H9)2Sn(C6H4(HO2C)NO2)2].
2. Sintesis senyawa difeniltimah(IV) dihidroksida [(C6H5)2Sn(OH)2] dan difeniltimah(IV) di-2-nitrobenzoat[(C6H5)2Sn(C6H4(HO2C)NO2)2]
Difeniltimah(IV) diklorida [(C6H5)2SnCl2] sebanyak 0,045 mol (13,68 gram) direaksikan dengan 0,09 mol (3,6 gram) NaOH untuk mengganti ligan klor dengan hidroksida dalam 50 mL pelarut metanol p.a. , selanjutnya endapan yang
dihasilkan disaring dengan kertas saring Whatman No. 42, lalu dicuci dengan akuabides dan metanol p.a. kemudian didiamkan di dalam desikator untuk
menghasilkan senyawa difeniltimah(IV) dihidroksida. Kristal difeniltimah(IV) diklorida dan difeniltimah(IV) dihidroksida dikarakterisasi dengan menggunakan spektrofotometer IR,dan spektrofotometer UV-Vis.
Kemudian senyawa difeniltimah(IV) di-2-nitrobenzoat disintesis dari senyawa
difeniltimah(IV) dihidroksida (C6H5)2Sn(OH)2 sebanyak 0,921 gram direaksikan dibutiltimah(IV) diklorida
dibutiltimah(IV) di-2-nitrobenzoat
dengan asam 2-nitrobenzoat (C6H4(N02)2COOH) sebanyak 1,002 gram dengan
perbandingan mol 1:2 dalam 30 ml pelarut metanol p.a. dan direfluks dengan
variasi waktu 3, 4, dan 5 jam dengan pemanas pada suhu 60℃. Setelah reaksi sempurna, metanol p.a. diuapkan dan dikeringkan di dalam desikator sampai
diperoleh kristal kering. Kristal kering tersebut dilarutkan dengan toluena dengan dibantu pemanasan hingga larut, lalu didinginkan dengan es dalam keadaan masih
panas, senyawa murni akan mengendap, kemudian dipisahkan dari pelarutnya. Setelah itu, dilakukan pengeringan kembali dengan desikator hingga diperoleh kristal dengan berat konstan. Kristal hasil senyawa dengan rendemen tinggi dari
variasi waktu refluks tersebut siap untuk dikarakterisasi dengan spektrofotometer IR, spektroskopi UV-Vis, analisis kandungan unsur C dan H dengan alat
microelemental analyzer, dan diuji sifat antikankernya terhadap sel leukimia
L-1210. Skema reaksi dari sintesis ini dapat dilihat pada Gambar 5.
Gambar 5. Sintesis senyawa difeniltimah(IV) dihidroksida [(C6H5)2Sn(OH)2] dan difeniltimah(IV) di-2-nitrobenzoat[(C6H5)2Sn(C6H4(HO2C)NO2)2]. difeniltimah(IV) di-klorida
difeniltimah(IV) di-2-nitrobenzoat
3. Sintesis senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH] dan trifeniltimah(IV) 2-nitrobenzoat [(C6H5)3Sn(C6H4HOOCNO2)]
Trifeniltimah(IV) klorida [(C6H5)3SnCl] sebanyak 0,045 mol (17,34 gram) direaksikan dengan 0,045 mol (1,8 gram ) NaOH untuk menggantikan ligan klor dengan hidroksida dalam 50 mL pelarut metanol p.a. ,selanjutnya endapan yang
dihasilkan disaring dengan menggunakan kertas saring Whatmann No. 42, lalu dicuci dengan akuabides dan metanol p.a. kemudian didiamkan di dalam desikator
untuk menghasilkan senyawa trifeniltimah(IV) hidroksida (C6H5)3SnOH. Kristal (C6H5)3SnCl dan (C6H5)3SnOH dikarakterisasi dengan menggunakan
spektrofotometer IR,dan spektrofotometer UV-Vis.
Kemudian senyawa trifeniltimah(IV) 2-nitrobenzoat disintesis dari senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH] sebanyak 1,101 gram direaksikan dengan asam 2-nitrobenzoat C6H4(NO2)2COOH sebanyak 0,501 gram dengan perbandingan mol 1:1 dalam 30 ml pelarut metanol p.a. dan direfluks dengan
variasi waktu 3, 4, dan 5 jam dengan pemanas pada suhu 60℃. Setelah reaksi sempurna, metanol p.a. diuapkan dan dikeringkan di dalam desikator sampai
diperoleh kristal kering. Kristal kering tersebut dilarutkan dengan toluena dengan dibantu pemanasan hingga larut, lalu didinginkan dengan es dalam keadaan masih
panas, senyawa murni akan mengendap, kemudian dipisahkan dari pelarutnya. Setelah itu, dilakukan pengeringan kembali dengan desikator hingga diperoleh kristal dengan berat konstan. Kristal hasil senyawa dengan rendemen tertinggi
dari variasi waktu refluks tersebut siap untuk dikarakterisasi dengan
dengan alat microelemental analyzer, dan diuji sifat antikankernya terhadap sel
leukimia L-1210. Skema reaksi sintesis ini dapat dilihat pada Gambar 6.
Gambar 6. Skema sintesis senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH] dan trifeniltimah(IV) 2-nitrobenzoat [(C6H5)3Sn(C6H4HOOCNO2)].
4. Pengujian aktivitas antikanker terhadap sel leukimia L-1210
Prosedur untuk pengujian aktivitas antikanker pada penelitian ini diadopsi dari prosedur yang dilakukan oleh Katrin dan Winarno (2008).
Pembuatan media RPMI-1640 seberat 10,4 g yang mengandung L-glutamin dilarutkan dalam 1 L air steril (A). Kemudian 1,3 g NaHCO3 dilarutkan dalam 50
mL air steril (larutan B). Sebanyak 25 mL larutan B ditambahkan ke dalam 475 mL larutan A, maka diperoleh 500 mL media (C). Untuk keperluan uji, 15 mL calf bovine serum ditambahkan ke dalam 85 mL larutan C. Semua pekerjaan
dilakukan di ruang steril.
trifeniltimah(IV) klorida trifeniltimah(IV) hidroksida
Sel leukimia L-1210 yang menjadi target uji aktivitas antikanker ini adalah sel
leukimia yang diperoleh dari sel limfosit tikus putih betina jenis DBA (Dilute Brown Non-Agouti Mouse) yang berumur 8 bulan. Sel leukimia ini diperoleh dari
The Institute of Physical and Chemical Research, Japan. Sel leukimia
disuspensikan ke dalam media yang telah mengandung calf bovine serum sehingga jumlah sel sekitar 2 x 106 sel/mL.
Pengujian aktivitas dilakukan terhadap sampel uji yang dilarutkan dalam metanol. Pengujian aktivitas sitotoksik sampel uji dilakukan dengan 5 variasi dosis yaitu 1,
2, 4, 8, dan 16 µg/mL. Pengujian dilakukan dengan menggunakan 5 variasi dosis, yaitu 0,02; 0,04; 0,08; 0,16; 0,32 µg/mL. Media yang telah mengandung suspensi
sel leukimia L-1210 (2 x 106 sel/mL) dimasukkan ke dalam multi well plate
tissue’s culture sebanyak 1 mL dalam setiap sumuran. Sebagai kontrol digunakan
10 µL metanol yang telah ditambahkan 990 µL suspensi sel. Percobaan dilakukan
triplo, selanjutnya suspensi sel yang telah diisi zat uji diinkubasi selama 48 jam pada suhu 37°C dalam inkubator 5% CO2.
Perhitungan sel dilakukan menggunakan haemocytometer Neubauer improved.
Untuk membedakan antara sel hidup dengan sel mati maka sebelum dilakukan penghitungan, 90 µL suspensi dimasukkan ke dalam sero cluster plate (96
sumuran) dan ditambah 10 µL larutan 1% larutan tryphan blue dan
dihomogenkan. Campuran sampel uji yang telah diwarnai tryphan blue sebanyak 10 µL larutan dialirkan ke dalam haemocytometer Neubauer improved.
Haemocytometer Neubauer improved merupakan sebuah alat yang digunakan
sebuah Haemocytometer terdapat sebuah ruang yang digunakan untuk menghitung
sel tersebut. Suspensi sel dimasukan dalam ruang tersebut, dan suspense harus cukup encer agar sel atau partikel lain tidak tumpang tindih di grid dan harus
[image:37.595.188.459.234.361.2]merata. Alat Haemocytometer Neubauer improved dapat dilihat pada Gambar 4 berikut.
Gambar 7. Haemocytometer Neubauer improved
Setelah itu, jumlah sel yang masih hidup dihitung di bawah mikroskop. Sel hidup
terlihat sebagai bulatan bening dengan bintik biru inti sel di tengah bulatan, sedangkan sel mati terlihat sebagai bercak biru pekat yang bentuknya tidak
teratur.
Persentase penghambatan zat uji terhadap pertumbuhan sel leukimia L-1210 dihitung sebagai berikut:
% inhibisi = 1− x 100%
A: jumlah sel hidup dalam media yang mengandung zat uji
B: jumlah sel hidup dalam media yang tidak mengandung zat uji (kontrol).
5. Analisis probit
Selanjutnya data persentase inhibisi diplotkan ke Tabel probit untuk memperoleh
sehingga diperoleh persamaan regresi linier y = a + bx. Dengan memasukkan
nilai y = 5 (probit dari 50%), maka diperoleh nilai x (log konsentrasi), nilai IC50 dengan mengkonversikan nilai log konsentrasi ke bentuk anti log. IC50 yaitu
V. SIMPULAN DAN SARAN
A. SIMPULAN
Dari penelitian yang telah dilakukan, dapat ditarik simpulan sebagai berikut:
1. Hasil sintesis senyawa dibutiltimah(IV) di-2-nitrobenzoat,
difeniltimah(IV) di-2-nitrobenzoat, dan trifeniltimah(IV) 2-nitrobenzoat
dengan rendemen tertinggi (refluks empat jam) masing-masing sebesar 1,4275 gram (84,22%), 1,4863 gram (81,89%), dan 1,3262 gram (85,67%).
2. Pada karakterisasi senyawa dibutiltimah(IV) di-2-nitrobenzoat, adanya serapan OH pada daerah 3460,41 cm-1 menandakan bahwa dalam senyawa ini terdapat gugus hidroksil yang berasal dari ligan yaitu asam
2-nitrobenzoat. Selain itu terdapat serapan Sn-O pada 730,76 cm-1 yang menandakan bahwa atom pusat Sn berikatan dengan ligan (asam
2-nitrobenzoat) melalui gugus O dan serapan vibrasi ulur Sn-O-C terlihat pada daerah 1165,16 cm-1, serapan NO2 pada daerah 1533,76 cm-1 dan 1360,69 serta serapan CO2 asimetri pada daerah 1440,62 cm-1.
3. Pada karakterisasi senyawa difeniltimah(IV) di-2-nitrobenzoat, adanya serapan C=O pada daerah 1680,65 cm-1 menandakan bahwa dalam
2-nitrobenzoat. Selain itu terdapat serapan Sn-O pada 730,66 cm-1 yang
menandakan bahwa atom pusat Sn berikatan dengan ligan (asam 2-nitrobenzoat) melalui gugus O dan serapan vibrasi ulur Sn-O-C terlihat
pada daerah 1292,01 cm-1. Serapan OH pada senyawa ini terlihat pada daerah 3462,91 cm-1, serapan NO2 pada daerah 1531,95 cm-1 dan serapan CO2 asimetri pada daerah 1487,95 cm-1.
4. Pada karakterisasi senyawa trifeniltimah(IV) 2-nitrobenzoat, adanya serapan Sn-O pada 731,40 cm-1 yang menandakan bahwa atom pusat Sn
berikatan dengan ligan (asam 2-nitrobenzoat) melalui gugus O dan serapan untuk Sn-O-C terletak pada daerah 1150,72 cm-1. Serapan OH pada
senyawa ini terlihat pada daerah 3438,36 cm-1, serapan C=O pada daerah 1679,55 cm-1, serapan CO2 asimetri terlihat pada 1482,54 cm-1, serapan
NO2 pada 1530,53 cm-1.
5. Hasil karakterisasi dengan menggunakan spektrofotometer UV terdapat transisi elektron π-π* untuk senyawa dibutiltimah(IV) di-2-nitrobenzoat,
difeniltimah(IV) di-2-nitrobenzoat dan trifeniltimah(IV) 2-nitrobenzoat
masing-masing pada max 211 nm, 208 nm, dan 204 nm.
6. Berdasarkan data mikroanalisis dengan menggunakan microelemental analyzer dapat dinyatakan senyawa hasil sintesis telah murni, karena
perbedaan hasil dari mikroanalisis dibandingkan dengan perhitungan secara teori masih dalam kisaran 1-5%.
7. Berdasarkan data IC50 yang diperoleh, trifeniltimah(IV) 2-nitrobenzoat
dibutiltimah(IV) 2-nitrobenzoat (24,66) dan difeniltimah(IV)
di-2-nitrobenzoat (9,87).
B. SARAN
Pada penelitian selanjutnya disarankan untuk menggunakan ligan dengan posisi
DAFTAR PUSTAKA
Aini, N.Q. 2010. Sintesis dan Karakterisasi serta Uji Pendahuluan Aktivitas Antikanker Beberapa Senyawa Organotimah(IV) Salisilat Terhadap Sel Leukimia L-1210. [Skripsi]. Universitas Lampung. Bandar Lampung. Halaman 56.
Anand, P. and A.B. Kunnumakkara. 2008. Canseris a Preventable Disease that Requires Major Lifestyle Changes. Pharm Research. 25 (9): 2097-2116.
Apantaku, L. M. 2002. Breast-conserving surgery for breast cancer. Am. Fam. Physician. 66 (12): 2271-2278.
Bliss, C.I. 1934. The method of probits. Science. 79: 2038.
Blunden, S.J. and R. Hill. 1990. Bis(tributyltin) oxide as a wood preservative: its conversion to tributyltin carboxylates in Pinus sylvestris. Appl
Organometal. Chem. 4: 63-68.
Bonire, J.J., G.A. Ayoko, P.F. Olurinola, J.O. Ehinmidu, N.S.N. Jalil, and A.A. Omachi. 1998. Synthesis and antifungal activity of some organotin(IV) carboxylates. Metal-Based Drugs. 5 (4): 233-236.
Cochran, W.G. and D.J. Finney. 1979. Chester Ittner Bliss, 1899-1979. Biometrics. 35 (4): 715-717..
Cotton, F.A. dan G. Wilkinson. 1989. Kimia Anorganik Dasar. Terjemahan oleh S. Suharto. Penerbit UI Press. Jakarta. Halaman 311-632.
Costech Analytical Technologies. 2011. Elemental Combiustion System CHNS. http://costech analytical.com/. Diakses pada 10 Februari 2013.
Day, R.A. dan A.L. Underwood. 1998. Analisis Kimia Kuantitatif Edisi Keenam. Terjemahan oleh A.H. Pudjaatmaka. Erlangga. Jakarta. Halaman 382-428.
Fessenden, R.J. dan J.S. Fessenden,. 1996. Kimia Organik Dasar. Jilid 2. Terjemahan oleh A.H. Pudjaatmaka. Erlangga. Jakarta. Halaman 64-464. Gielen, M. 2003. An overview of forty years organotin chemistry developed at
the free Universities of Brussels ULB and VUB. J. Braz. Chem. Soc. 14 (6): 870-877.
Gleeson B., Claffey J., Ertler D., Hogan M., Müller-Bunz H., Paradisi F., Wallis D., Tacke M. 2008. Novel organotin antibacterial and anticancer drugs. Elsevier:Polyhedron 27.3619–3624.
Hadi, S., B. Irawan and Efri. 2008. The antifungal activity test of some organotin(IV) carboxylates. J. Appl. Sci. Res.4 (11).1521-1525.
Hadi, S., M. Rilyanti, and Nurhasanah. 2009. Comparative study on the antifungal activity of some Di and Tributyltin(IV) carboxylate compounds. Modern Appl. Sci. 3 (1): 12-17.
Hadi, S. & Rilyanti, M. 2010. Synthesis and in vitro anticancer activity of some organotin(IV) benzoate compounds, Oriental Journal of Chemistry, 26 (3): 775-779.
Halimah. 2011. Sintesis, Karakterisasi serta Uji Pendahuluan Aktivitas Antikanker Beberapa Senyawa Organotimah(IV) ftalat Terhadap Sel Leukimia L-1210. [Skripsi]. Universitas Lampung. Bandar Lampung. Halaman 58.
Hawariah, A.L.P. 1998. Memahami Kanser. Universiti Putra Malaysia. Serdang. Hoshino, A., A.M. Albrecht., J.L. Biedler and D.J. Hutchison. 1966.
Amethopterin resistance in clonal lines of l1210 mouse leukemia : some associated biologic and biochemical alterations. Cancer Res. 26 : 1397-1407.
Jain, M.G., K. Agarwal, and R.V. Singh. 2003. Studies on Nematicidal, Fungicidal and Bacterial Activities of Organotin(IV) Complexes with Heterocyclic Sulphonamide Azomethine. Chemistry : An Indian Journal. 1: 378-391.
Katrin, E. dan H. Winarno. 2008. Aktifitas sitotoksik fraksi-fraksi ekstrak etil asetat kulit batang mahkota dewa (Phaleria macrocarpa (Scheff) Boerl) terhadap sel kanker manusia. Majalah Tanaman Obat Tradisional. 13 (45): 120-125.
Li Y., Li Y., Niu Y., Jie L., Shang X., Guo J., Li, Q. 2008. Synthesis and antitumor activity of a new mixed-ligand complex di-n-butyl-(4-chlorobenzohydroxamato)tin(IV) chloride. Journal of Inorganic Biochemistry 102. 1731–1735.
Mahmood, S., S. Ali, M.H. Bhatti, M. Mazhar, and R. Iqbal. 2003. Synthesis, Characterization, and Biological Applications of Organotin(IV) Derivates of 2-(2-Fluoro-4-biphenyl) Propanoid Acid. Turk J. Chem. 27: 657-666. Manahan, D. and R.A. Wienberg. 2002. The Hallmarks of Cancer. Cell.
100: 57 -70.
Mans, D.R.A., da Rocha, A.B. & Schwartsmann, G. 2000. Anti-Cancer Drug Discovery and Development in Brazil: Targeted Plant Collection as a Rational Strategy to Acquire Candidate Anti- Cancer Compounds, The Oncologist, 5 (3): 185-198.
Pellerito, L. and L. Nagy. 2002. Organotin (IV)n+ Complexes formed with biologically active ligands: equilibrium and structural studies and some biological aspect. Coord. Chem. Rev. 224: 111 – 150.
Price, A.S. dan L.M. Wilson. 2005. Patofisiologi: Konsep Klinis Proses-Proses Penyakit. Penerbit Buku Kedokteran. EGC: Mc Graw Hill. Jakarta.
Pucell, K.F., and F. Keith. 1980. An Introduction to Inorganic Chemistry. Souders College. Phladelphia. P 52-59.
Purnomo, W.F. 2008. Sintesis dan Karakterisasi Senyawa Organotimah(IV) Karboksilat: Trimetiltimah N-maleoilglisinat. (Skripsi). Universitas Indonesia. Depok. Halaman 29-48
Ruzika, A., L. Dostal, R. Jambor, V. Butcha, J. Brus, I. Cisarova, M. Holcapek, and J. Holecek. 2002. Structure and In Vitro Antifungal Activity of [2,6-bis(dimethyl-minomethyl)phenyl]diphenyltin(IV) Compounds. Applied Organometallic Chem. 16 (6): 315-322.
Sari, F.S. 2011. Sintesis, Karakterisasi serta Uji Pendahuluan Aktivitas Antikanker Beberapa Senyawa Organotimah(IV) benzoat Terhadap Sel Leukimia L-1210. [Skripsi]. Universitas Lampung. Bandar Lampung. Halaman 54.
Sudjadi. 1985. Penentuan Struktur Senyawa Organik. Ghalia Indonesia. Jakarta. Halaman 175-232.
Sukarjo.1992. Kimia Koordinasi. P.T. Bina Aksara. Jakarta. Halaman 101-111.
Terhadap Sel Leukimia L-1210. [Skripsi]. Universitas Lampung. Bandar Lampung. Halaman 62.
Szorcsik, A., L. Nagy, L. Pellerito, T. Yamaguchi, and K. Yoshida. 2002. preparation and structural studies of organotin(IV) complexes formed with organic carboxylic acids. J. Radioanal. Nucl. Chem. 256 (1): 3-10.
Tayer, J. 1988. Organometallic Chemistry and Overview. VCH Publisher Inc/ United State. P 7-14.
Van Der Weij, F.W. 1981. Kinetics and mechanism of urethane formation catalysed by organotin compound. J. Poly. Sci. Polym Chem. 19 (2): 381-388.