24
KARAKTERISASI KATALIS ZEOLIT-Ni REGENERASI DAN TANPA REGENERASI
DALAM REAKSI PERENGKAHAN KATALITIK
Astro Tadeus1*, Imelda H. Silalahi1, Endah Sayekti1, Aladin Sianipar2 1
Program Studi Kimia, Fakultas MIPA, Universitas Tanjungpura Pontianak, Jl. Prof. Dr. H. Hadari Nawawi, 2
Pusat Survei Geologi, Bandung, *email: astro_chemistry@yahoo.co.id
ABSTRAK
Karakterisasi katalis zeolit-Ni dengan perlakuan regenerasi dan tanpa regenerasi dalam reaksi perengkahan katalitik telah dilakukan. Tahapan-tahapan preparasi zeolit meliputi demineralisasi, dealuminasi, dan aktivasi. Tahapan selanjutnya yaitu impregnasi zeolit dengan logam Ni, kalsinasi, dan uji aktivitas katalis zeolit-Ni dengan menggunakan kembali katalis sebanyak tiga kali reaksi perengkahan tanpa perlakuan regenerasi katalis (disebut A) dan menggunakan katalis yang diregenerasi (disebut B). Perengkahan terhadap minyak jelantah sebagai umpan dilakukan pada suhu 310 – 320 0C dengan rasio O/C (oil/catalyst)=4 selama 6 jam. Hasil analisis XRD (X-Ray Diffraction) menunjukkan bahwa kuarsa dan mordenit tidak mengalami perubahan struktur dan masih merupakan penyusun utama katalis zeolit-Ni fresh, katalis bekas perengkahan ketiga tanpa perlakuan regenerasi (A-3), dan katalis bekas dengan perlakuan regenerasi (B-3). Keasaman katalis A-3 menurun hingga 98,85 % dan katalis bekas B-3 menurun hingga 84,35 %. Selanjutnya, luas permukaan spesifik katalis mengalami penurunan hingga 43,14 % (A-3) dan 15,97 % (B-3). Namun, rerata jari pori meningkat dari 1,579 nm pada katalis zeolit-Ni baru (fresh) menjadi 4,499 nm (A-3) dan 1,688 nm (B-3). Volume total pori katalis sebesar 9,181 x 10-2 cc/g (zeolit-Ni fresh); 1,487 x 10-1 cc/g (A-3); dan 8,247 x 10-2 cc/g (B-3).
Kata kunci: Karakterisasi, regenerasi, perengkahan, katalis PENDAHULUAN
Perengkahan berkatalis (catalytic cracking) adalah suatu cara yang digunakan untuk
memecah hidrokarbon kompleks menjadi
molekul yang lebih sederhana (Buchori dan Widayat, 2009). Perengkahan berkatalis ini dilakukan dengan menggunakan katalis pada
kondisi temperatur tertentu. Katalis yang
digunakan dalam proses perengkahan pada umumnya adalah katalis logam yang dimodifikasi dengan suatu bahan pengemban. Salah satu bahan pengemban yang sering digunakan yaitu zeolit. Adanya logam aktif pada zeolit (sistem pengemban-logam) akan memperbesar luas permukaan dan meningkatkan keasaman katalis (Suyati dkk., 2009).
Zeolit merupakan suatu mineral dengan struktur kristal aluminosilikat yang berbentuk kerangka (framework) tiga dimensi. Zeolit memiliki pori-pori, saluran dan mengandung
ion-ion logam seperti Na+, K+, Mg2+, dan Ca2+ serta
molekul air (Setiadi dan Pertiwi, 2007). Zeolit sebagai katalis memiliki ukuran pori tertentu.
Selektivitas zeolit terhadap suatu reaksi
disebabkan oleh ukuran pori zeolit yang hanya dapat dimasuki oleh molekul tertentu yang spesifik, yang disebut sebagai shape-selective
catalysis (Tatsumi, 2004
).
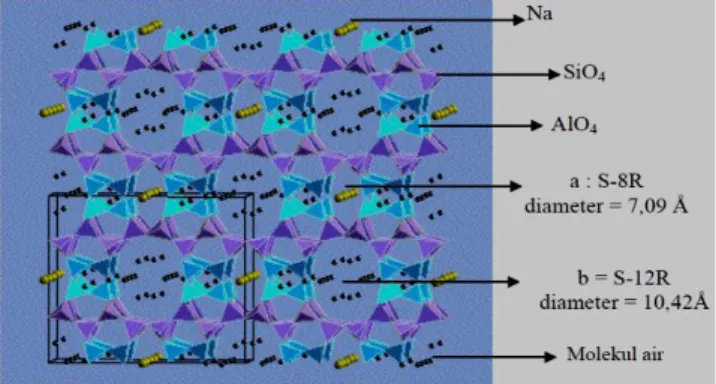
Salah satu jenis zeolit yaitu mordenit. Mordenit memiliki sistem kristal ortorombik dengan simetri grup ruang Cmcm(a = 18.13; b = 20.5; c = 7.52 Å) (Oprea et.al., 2008). Struktur mordenit merupakan struktur sangkar jenis Secondary Building Unit (SBU) 5-1 dengan dua saluran utama yaitu, saluran pertama yang dibatasi oleh 8 Oksigen (S-8R) dan saluran kedua yang dibatasi oleh 12 Oksigen (S-12R) yang ditunjukkan pada Gambar 1.
Gambar 1. Struktur mordenit a) rongga pertama S-8R
ditempati oleh logam alkali dan b) rongga kedua S-12R lebih besar ditempati oleh molekul air (Suminta dan Las, 2006).
Penelitian tentang modifikasi suatu katalis dalam sistem pengemban-logam telah banyak dilakukan guna meningkatkan aktivitas katalis. Septiansyah (2011) telah melakukan modifikasi katalis dengan metode impregnasi terhadap logam Nikel (Ni) ke dalam zeolit jenis mordenit sebagai pengemban, dan diperoleh kesimpulan bahwa persentase Ni terbesar yang terserap ke dalam zeolit terjadi pada zeolit-Ni 0,2 M.
25 Penggunaan katalis dalam waktu tertentu
akan menyebabkan penurunan aktivitas.
Penurunan aktivitas katalis terjadi karena katalis mengalami deaktivasi. Deaktivasi ini diakibatkan oleh pengotor (fouling), yaitu pembentukan karbon atau kokas dalam proses perengkahan (Trisunaryanti dkk., 2002). Kokas/residu karbon mendeaktivasi katalis dengan meracuni situs-situs aktif dan/atau mem-block pori-pori katalis. Kokas yang terbentuk dapat dihilangkan dengan
pembakaran pada 600 0C (Chen and Manos,
2004).
Hasil penelitian Trisunaryanti dan
Emmanuel (2009) menyatakan bahwa deposit kokas pada permukaan katalis CoO-MoO/ZnO-zeolit alam aktif mengalami peningkatan seiring
dengan bertambahnya waktu penggunaan
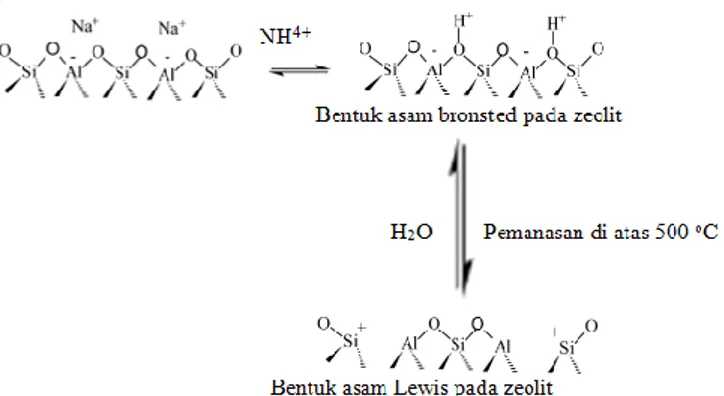
sehingga menyebabkan menurunnya aktivitas katalis. Salah satu faktor penyebab terbentuknya kokas yaitu keasaman total katalis. keasaman total katalis merupakan gabungan dari asam Bronsted dan asan Lewis. Semakin tinggi keasaman katalis maka pembentukan kokas semakin cepat (Wang, 2007). Pembentukan asam Bronsted dan asam Lewis dapat dilihat pada Gambar 2.
Gambar 2. Situs asam Bronsted dan asam Lewis pada
zeolit (Tatsumi, 2004).
Trisunaryanti dkk. (2002) menyatakan bahwa katalis Cr-zeolit alam aktif yang telah terdeaktivasi mengalami peningkatan keasaman total katalis, volume total pori (VTP) dan luas permukaan spesifik (LPS) tetapi rerata jejari pori
(RJP) menurun setelah katalis tersebut
diregenerasi. Hasil konversi metil isobutil keton (MIBK) meningkat dari 0,53 % pada katalis terdeaktivasi menjadi 4,61 % pada katalis teregenerasi.
Penelitian ini bertujuan untuk mengetahui karakteristik zeolit-Ni regenerasi dan tanpa
regenerasi yang dikaji dalam proses
perengkahan minyak jelantah.
METODE PENELITIAN Alat dan Bahan
Alat-alat yang digunakan pada penelitian ini adalah sebagai berikut : Gas Sorption
Analyzer (GSA) Quantachrome version 2.0,
neraca analitik, oven, pH universal, piknometer,
seperangkat alat gelas kimia standar,
seperangkat alat refluks, tanur, viskometer Ostwald kapiler nomor 300, X-Ray
Fluoroscence (XRF) Sequetial Analysis W-XRF Uniquant Thermoelectron Scientific, dan X-Ray Difraction (XRD) PANalytical Philips.
Bahan-bahan kimia yang digunakan adalah
ammonium klorida (NH4Cl) 1 M, asam nitrat
(HNO3) 8 M, natrium etilen diamin tetra asetat
(Na2EDTA), natrium hidroksida (NaOH), dan
nikel klorida (NiCl2). Sampel yang digunakan
adalah batuan zeolit alam asal Bandung Selatan-Jawa Barat dan minyak jelantah.
Prosedur Kerja
Preparasi Sampel (Silalahi dkk., 2012)
Sampel dihancurkan hingga halus dan diayak dengan ayakan 200 mesh. Sampel kemudian dicuci dengan akuabides hingga mencapai pH pencuci (pH=6). Dikeringkan di
oven hingga kering pada suhu 110 0C selama 4
jam. Sampel yang telah kering kemudian ditimbang. Sampel tersebut kemudian dianalisis dengan X-Ray Fluoroscence (XRF).
Demineralisasi dengan EDTA 1M (Silalahi dkk., 2012)
Sampel hasil pencucian kemudian dicuci kembali dengan larutan EDTA 1 M. Pencucian dilakukan dengan proses refluks pada suhu
80-90 0C selama 24 jam. Setelah direfluks, sampel
kemudian dicuci dengan akuabides hingga mencapai pH pencuci (pH=5). Dikeringkan di
oven pada suhu 110 0C selama 4 jam, setelah
kering sampel kemudian ditimbang.
Dealuminasi dengan Asam Nitrat (HNO3) (Silalahi dkk., 2012)
Sampel yang telah dicuci dengan EDTA
1 M kemudian di-leaching dengan HNO3 8 M.
Proses ini juga merupakan proses dealuminasi zeolit. Sampel zeolit ditimbang dan kemudian
direfluks pada suhu 80-90 0C selama 24 jam.
Setelah proses refluks selesai, sampel kemudian dicuci dengan akuabides hingga mencapai pH pencuci (pH=5). Dikeringkan di oven pada suhu
26 Aktivasi dengan Amonium Klorida (NH4Cl) (Silalahi dkk., 2012)
Sampel hasil dealuminasi diaktivasi
dengan menggunakan amonium klorida 1 M. Aktivasi dilakukan dengan cara direfluks pada
suhu 80-90 0C selama 24 jam. Setelah proses
refluks selesai, sampel kemudian dicuci dengan akuabides hingga mencapai pH pencuci (pH=5).
Dikeringkan di oven pada suhu 110 0C selama 4
jam, setelah kering sampel kemudian ditimbang. Sampel hasil pencucian ini dianalisis dengan
X-Ray Fluoroscence (XRF).
Pembuatan Katalis Zeolit-Ni (Silalahi dkk., 2012)
Katalis zeolit-Ni diperoleh dari impregnasi
antara nikel korida (NiCl2) dengan zeolit dalam
media cair. Sampel zeolit ditimbang sebanyak 45 g dimasukkan ke dalam labu alas bulat yang
berisikan 100 mL larutan NiCl2 0,2 M kemudian
direfluks pada suhu 80-90 0C selama 24 jam.
Setelah proses refluks selesai, sampel kemudian dicuci dengan akuabides hingga mencapai pH pencuci (pH=5). Dikeringkan di oven pada suhu
110 0C selama 4 jam, setelah sampel kering
kemudian sampel ditimbang untuk proses berikutnya.
Kalsinasi Katalis (Silalahi dkk., 2012)
Proses kalsinasi dilakukan dengan
memasukkan katalis ke dalam cawan porselen. Kemudian dipanaskan di dalam tanur pada suhu
500-600 0C selama 2-3 jam. Waktu kalsinasi
dihitung setelah mencapai suhu konstan. Sampel hasil kalsinasi ini selanjutnya dianalisis dengan
X-Ray Difraction (XRD), X-Ray Fluoroscence
(XRF) dan metode fisisorpsi.
Uji Deaktivasi dan Regenerasi Katalis Zeolit-Ni
Minyak jelantah sebanyak 40 g bersama
dengan katalis zeolit-Ni sebanyak 10 g
dicampurkan dalam suatu labu destilasi
selanjutnya dipanaskan pada temperatur
310-320 0C dalam labu destilasi yang telah
dihubungkan dengan kondensor. Uap minyak jelantah yang telah direngkahkan oleh zeolit-Ni kemudian didinginkan melewati kondensor, sehingga uap tersebut terkondensasi. Reaksi dihentikan ketika komposisi minyak dalam labu pemanas sudah habis atau sudah tidak mengeluarkan uap cair.
Perengkahan katalitik minyak jelantah
menggunakan katalis zeolit-Ni dibagi menjadi 2, yaitu perengkahan tanpa perlakuan regenerasi katalis (disebut A) dan perengkahan dengan perlakuan regenerasi (disebut B). Perengkahan
A dan B masing-masing dilakukan 3 kali perengkahan. Pada perengkahan A, setelah perengkahan pertama (A-1) selesai, katalis bekas diambil dan dikeringkan pada suhu
300-400 0C selama 4 jam kemudian ditimbang.
Pada perengkahan ketiga (A-3) dilakukan prosedur yang sama seperti perengkahan sebelumnya. Sedangkan pada perengkahan B, setelah perengkahan pertama (B-1) selesai, katalis bekas diambil dan dipanaskan pada suhu
600 0C selama 4 jam (proses regenerasi). Pada
perengkahan ketiga (B-3) dilakukan prosedur yang sama seperti perengkahan sebelumnya. Selanjutnya, katalis bekas pada perengkahan A-3 dan B-3 ditimbang dan dianalisis dengan
XRD (X-Ray Difraction), XRF (X-Ray
Fluoroscence), dan metode fisisorpsi.
HASIL DAN PEMBAHASAN
Hasil analisis XRD memperlihatkan bahwa
mineral kuarsa dan mordenit merupakan
penyusun utama katalis zeolit-Ni 0,2 M. Hal ini dapat ditunjukkan oleh puncak-puncak yaitu,
antara lain pada kuarsa 2θ = 20,82 (d = 4,26 Å)
dengan intensitas sebesar 310,44 dan
2θ = 26,60 (d = 3,35 Å) dengan intensitas yang
sangat tinggi yaitu sebesar 2495,29. Sedangkan pada mordenit ditunjukkan oleh puncak dengan 2θ = 9,73 (d = 9,07 Å) dengan intensitas sebesar
76,08 dan 2θ = 27,72 (d = 3,21 Å) dengan
intensitas sebesar 477,04.
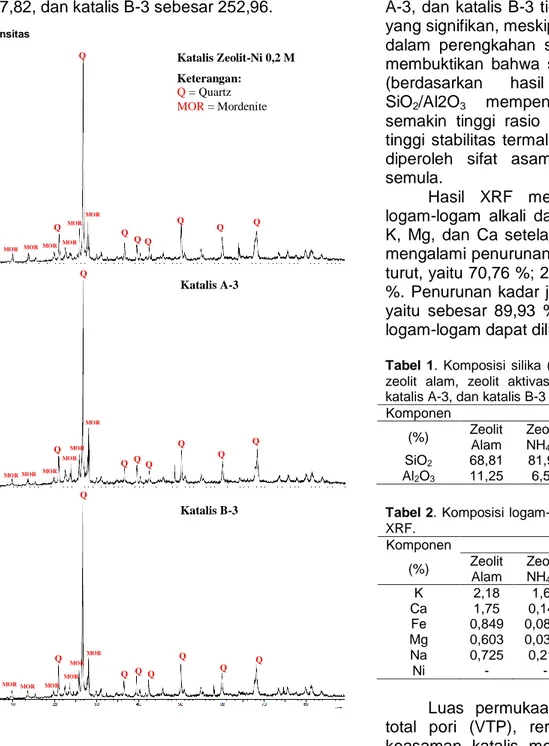
Gambar 3 menunjukkan bahwa kuarsa dan mordenit tidak mengalami perubahan yang signifikan dan masih merupakan penyusun utama katalis zeolit-Ni 0,2 M meskipun telah mengalami perlakuan 3 kali perengkahan, baik katalis A-3 maupun katalis B-3. Struktur ketiga katalis tidak mengalami perubahan struktur mineral kuarsa. Hal ini dapat dilihat dari jarak dasar (d-spacing) untuk mineral kuarsa yang tidak mengalami perubahan. Perubahan yang terjadi hanya terlihat pada intensitas puncak. Intensitas tertinggi pada masing-masing d = 3,34 Å puncak mineral kuarsa pada katalis zeolit-Ni 0,2 M, katalis B-3, dan katalis A-3 berturut-turut yaitu sebesar 2495,29; 2426,74; dan 2399,05. Hal ini dapat terjadi karena pada katalis A-3, pembentukan kokas yang terjadi selama proses
perengkahan berlangsung terdispersi
dipermukaan maupun di dalam pori-pori zeolit sehingga katalis mengalami deaktivasi dan menurunkan intensitas relatif puncak-puncak dari zeolit, tetapi tidak menyebabkan perubahan struktur zeolit sebagai katalis perengkahan.
27 Intensitas difraksi sinar-X menunjukkan kesempurnaan kristal dan keteraturan susunan atom dalam kristal. Intensitas puncak mordenit di
2θ = 27,72 dengan d511 untuk zeolit-Ni 0,2 M,
katalis B-3, dan katalis A-3 mengalami
perubahan intensitas, yaitu untuk katalis zeolit-Ni 0,2 M sebesar 477,04, katalis A-3 sebesar 307,82, dan katalis B-3 sebesar 252,96.
Intensitas
2θ
Gambar 3. Difraktogram katalis Ni-zeolit 0,2 M; katalis A-3;
dan katalis B-3
Berdasarkan hasil X-Ray Fluoroscense (XRF) pada Tabel 1, rasio silika alumina
(SiO2/Al2O3) dari keempat sampel tersebut
masing-masing yaitu, untuk zeolit alam = 6,12;
zeolit-NH4Cl = 12,44; zeolit-Ni 0,2 M = 12,52;
katalis A-3 = 11,99; dan katalis B-3 = 12,02.
Data pada Tabel 1 juga menunjukkan bahwa tahapan-tahapan dari preparasi zeolit dengan demineralisasi, dealuminasi hingga
aktivasi dapat meningkatkan rasio SiO2/Al2O3
dari 6,12 (rasio SiO2/Al2O3 pada zeolit alam)
menjadi 12,44 (setelah diaktivasi dengan NH4Cl).
Rasio SiO2/Al2O3 katalis zeolit-Ni 0,2 M, katalis
A-3, dan katalis B-3 tidak mengalami perubahan yang signifikan, meskipun katalis telah digunakan dalam perengkahan sebanyak tiga kali. Hal ini membuktikan bahwa struktur katalis tidak rusak
(berdasarkan hasil XRD). Perbandingan
SiO2/Al2O3 mempengaruhi aktivitas katalis,
semakin tinggi rasio SiO2/Al2O3 maka semakin
tinggi stabilitas termal dan kekuatan asam serta diperoleh sifat asam yang lebih besar dari semula.
Hasil XRF menunjukkan bahwa kadar logam-logam alkali dan alkali tanah seperti Na,
K, Mg, dan Ca setelah diaktivasi dengan NH4Cl
mengalami penurunan secara signifikan berturut-turut, yaitu 70,76 %; 26,15 %; 94,5 %; dan 91,94 %. Penurunan kadar juga terjadi pada logam Fe yaitu sebesar 89,93 %. Adapun data komposisi logam-logam dapat dilihat pada Tabel 2.
Tabel 1. Komposisi silika (SiO2) dan alumina (Al2O3) pada
zeolit alam, zeolit aktivasi zeolit-NH4Cl, zeolit-Ni 0,2 M,
katalis A-3, dan katalis B-3 hasil analisis XRF.
Tabel 2. Komposisi logam-logam pada katalis hasil analisis
XRF.
Luas permukaan spesifik (LPS), volume total pori (VTP), rerata jari pori (RJP), dan keasaman katalis memegang peranan penting pada zeolit sebagai katalis perengkahan. Luas permukaan spesifik (LPS), volume total pori (VTP), dan rerata jari pori (RJP) dapat dianalisa
dengan uji adsorpsi-desorpsi gas N2
menggunakan persamaan Brunaurer, Emmet dan Teller (BET). Adapun hasil analisa GSA untuk katalis zeolit-Ni 0,2 M, katalis A-3, dan katalis B-3 dapat dilihat pada Tabel 3.
Komponen Sampel (%) Zeolit Alam Zeolit-NH4Cl Zeolit-Ni 0,2M A-3 B-3 SiO2 68,81 81,98 83,98 73,61 84,40 Al2O3 11,25 6,59 6,71 6,14 7,02 Komponen Sampel (%) Zeolit Alam Zeolit-NH4Cl Zeolit-Ni 0,2M A-3 B-3 K 2,18 1,61 1,32 1,25 1,40 Ca 1,75 0,141 0,152 0,231 0,250 Fe 0,849 0,0855 0,0202 0,0706 0,105 Mg 0,603 0,0332 0,0615 0,139 - Na 0,725 0,212 0,182 2,04 - Ni - - 0,045 0,061 0,268 Q
MOR MORMORMOR MOR MOR Q Q QQ Q Q Q Katalis Zeolit-Ni 0,2 M Keterangan: Q = Quartz MOR =Mordenite
MORMOR MOR MOR MOR MOR Q Q QQ Q Q Q Q Q Q Q Q Q Q Q Q MORMOR MOR
MOR MOR
Katalis A-3
Katalis B-3
28
Tabel 3. Hasil pengukuran Luas Permukaan Spesifik (LPS),
Volume Total Pori (VTP), dan Rerata Jari Pori (RJP) pada Katalis zeolit-Ni 0,2 M, Katalis A-3, dan Katalis B-3.
Katalis LPS (m2/g) VTP (10-02cc/g) RJP (nm) Zeolit-Ni 0,2 M 116,233 9,181 1,579 A-3 66,089 14,87 4,499 B-3 97,676 8,247 1,688
Berdasarkan Tabel 3 terlihat bahwa LPS tertinggi terjadi pada katalis zeolit-Ni 0,2 M
sebesar 116,233 m2/g. Setelah katalis digunakan
dan menjadi katalis bekas tanpa regenerasi (A-3), katalis tersebut mengalami penurunan LPS
menjadi 66,089 m2/g. Sedangkan katalis bekas
yang telah diregenerasi (B-3) memiliki LPS
sebesar 97,676 m2/g. Penurunan LPS pada
katalis A-3 terjadi akibat pembentukan kokas dan terdispersi kepermukaan katalis. Terdispersinya kokas ini mengakibatkan situs-situs aktif katalis dan pori-pori yang kecil tertutup sehingga katalis
mengalami deaktivasi (Trisunaryanti dan
Emmanuel, 2009).
Data pada Tabel 3 memperlihatkan bahwa rerata jari pori (RJP) katalis A-3 lebih besar dibandingkan dengan katalis B-3 dan katalis zeolit-Ni 0,2 M. Data RJP ini dapat menjelaskan bahwa selektifitas katalis menurun seiring bertambahnya RJP. Oleh karena itu, katalis zeolit-Ni 0,2 M fresh lebih selektif dari katalis A-3 dan katalis B-3.
Keasaman total merupakan jumlah dari situs asam Lewis dan situs asam Bronsted pada katalis. Keasaman total katalis juga memegang peranan penting dari suatu katalis perengkahan. Katalis yang memiliki keasaman yang besar memberikan kontribusi yang besar juga pada pembentukan produk perengkahan. Situs asam Bronsted maupun situs asam Lewis pada katalis berperan dalam proses hidrogenasi (adanya pemutusan ikatan rangkap dari reaktan) dan
terbentuknya karbokation yang reaktif.
Keasaman total katalis dapat dianalisis dengan FTIR-adsorpsi basa Piridin. Keasaman total ketiga katalis ini dapat dilihat pada Tabel 4.
Tabel 4. Keasaman total katalis zeolit-Ni 0,2 M, katalis A-3,
dan katalis B-3. No Katalis Asam Lewis Asam Bronsted Total (mmol/g) 1 Zeolit-Ni 0,2M 0,139 0,123 0,262 2 A-3 0,002 0,001 0,003 3 B-3 0,026 0,0015 0,041
Tabel 4 memperlihatkan adanya
penurunan keasaman total katalis setelah
digunakan dalam perengkahan katalitik.
Keasaman total katalis A-3 jauh lebih kecil 87 kali lipat katalis zeolit-Ni 0,2 M. Hal ini terjadi karena
katalis A-3 mengalami deaktivasi akibat
terbentuknya kokas yang menutupi situs-situs asam aktif dipermukaan maupun di dalam pori-pori zeolit. Katalis B-3 memiliki keasaman total lebih kecil 6 kali lipat katalis zeolit-Ni 0,2 M. Penurunan keasaman dari zeolit-Ni ke katalis B-3 lebih kecil jika dibandingkan dengan penurunan keasaman dari zeolit-Ni ke katalis A-3. Hal ini
terjadi karena proses regenerasi katalis
(penghilangan kokas) pada katalis B-3. Secara visual, pembentukan kokas dapat dilihat dari perubahan warna katalis fresh dari warna putih menjadi hitam setelah reaksi perengkahan. SIMPULAN
Berdasarkan hasil penelitian dapat
disimpulkan bahwa mordenit dan kuarsa yang merupakan penyusun utama katalis zeolit-Ni baru (fresh), katalis regenerasi (B-3), dan tanpa regenerasi (A-3) tidak mengalami perubahan struktur. Keasaman katalis setelah digunakan
sebanyak 3 kali perengkahan mengalami
penurunan sebesar 98,85 % (A-3) dan 84,35 % (B-3), luas permukaan spesifik katalis menurun hingga 43,14 % (A-3) dan 15,97 % (B-3). Namun, rerata jari pori meningkat dari 1,579 nm pada katalis zeolit-Ni baru (fresh) menjadi 4,499 nm (A-3) dan 1,688 nm (B-3). Volume total pori
pada zeolit-Ni baru (fresh) sebesar 9,181 x 10-2
cc/g, katalis A-3 sebesar 1,487 x 10-1 cc/g, dan
pada katalis B-3 sebesar 8,247 x 10-2 cc/g.
UCAPAN TERIMA KASIH
Terima kasih kepada pihak DIT.
LITABMAS, DIKTI yang telah menyediakan dana penelitian ini.
DAFTAR PUSTAKA
Buchori, L dan Widayat., 2009, Pembuatan Biodiesel dari Minyak Goreng Bekas
dengan Proses Catalytic Cracking,
Prosiding Seminar Nasional Teknik Kimia 2009, Jurusan Kimia Fakultas Teknik
UNDIP, Semarang.
Chen, S and Manos, G., 2004, Study of Coke and Coke Precursors During Catalytic Cracking of n-hexane and 1-hexene Over Ultrastable Y Zeolite, Catalysis Letters, 96:195.
Septiansyah, I., 2011, Preparasi, karakterisasi dan Uji Performa Katalis Zeolit-Ni dalam Perengkahan Katalitik Minyak Jelantah,
Universitas Tanjungpura, Pontianak,
29 Oprea, C., Popcescu, V., and Birghila, S., 2008,
New Studies About the Modified
Mordenites, Romania Journal Physics, 53(1-2):231-239.
Setiadi dan Pertiwi, A., 2007, Preparasi dan Karakterisasi Zeolit Alam untuk Konversi
Senyawa ABE menjadi Hidrokarbon,
Prosiding Konggres dan Simposium Nasional Kedua MKICS 2007 ISSN: 0216-4183, Departemen Teknik Kimia, Fakultas
Teknik Universitas Indonesia, Jakarta. Silalahi, I.H., Sianipar, A., Sayekti, E., dan
Septiansyah, S. I., 2012, Pengaruh
Distribusi Pori Katalis Zeolit-Ni Terhadap Selektivitas Perengkahan Katalitik Minyak Jelantah, Prosiding Semirata BKS PTN B
MIPA, ISBN 978-602-9115-28-4 :69-73.
Suminta, S., dan Las, T., 2006, Penghalusan struktur Sangkar Kristal Mordenit dan Klinoptilolit Alam dengan Metode Rietveld,
Indonesian Journal of Materials Science,
7(2):73-78.
Suyati, L., Nuryanto, R., dan Sulistyorini, H., 2009, Perengkahan Produk Cair Hasil
Pirolisis Sabut Kelapa dengan
Menggunakan Katalis Zeolit Alam dan
Ni/Zeolit pada Suhu 400 oC, Seminar
Nasional Kimia dan Pendidikan Kimia, Laboratorium Kimia Fisik, Jurusan Kimia FMIPA, Universitas Diponegoro.
Tatsumi, T., 2004, Zeolites: Catalysis,
Encyclopedia of Supramolecular
Chemistry, 1: 1, 1610-1616, Yokohama National University, Yokohama, Japan. Trisunaryanti, W and Emmanuel, I., 2009,
Preparation, Characterization, Activity,
Deactivation, and Regeneration Tests of
CoO-MoO/ZnO and
CoO-MoO/ZnO-Activated Zeolite Catalysts for the
Hydrogen Production from Fusel Oil,
Indonesian Journal Chemistry,
9(3):361-368.
Trisunaryanti, W., Triyono., dan Taufiyanti, F., 2002, Deaktivasi dan Regenerasi Katalis Cr/Zeolit Alam Aktif untuk Proses Konversi Metil Isobutil Keton, Gama Sains IV (2). Wang, B., 2007, Zeolite Deactivation During
Hydrocarbon Reactions: Characterisation of Coke Precursors and Acidity, Product Distribution, a Thesis Submitted for the Degree of Doctor of Philosophy of the University College London, London.