AKTIVITAS ANTIMIKROBA FRAKSI PETROLEUM ETER, KLOROFORM, ETANOL BUNGA PULU (Chartamus tinctorius L.) TERHADAP Staphylococcus
aureus, Escherichia coli, dan Candida albicans
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Hermawan Deny Prasetyo NIM : 098114036
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
AKTIVITAS ANTIMIKROBA FRAKSI PETROLEUM ETER, KLOROFORM, ETANOL BUNGA PULU (Chartamus tinctorius L.) TERHADAP Staphylococcus
aureus, Escherichia coli, dan Candida albicans
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh
Hermawan Deny Prasetyo NIM : 098114036
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iii
iv
v
LEMBAR PERNYATAAN KEASLIAN KARYA
Saya menyatakan dengan sesungguhnya bahwa skripsi yang saya tulis ini tidak memuat karya orang lain, kecuali yang telah disebutkan dalam kutipan dan daftar pustaka, sebagaimana layaknya karya ilmiah.
Yogyakarta, 11 Maret 2013 Penulis,
vi
LEMBAR PERNYATAAN PERSETUJUAN
PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS Yang bertanda tangan dibawah ini, saya mahasiswa Universitas Sanata Dharma:
nama : Hermawan Deny Prasetyo nomor mahasiswa : 098114036
Demi pengembangan ilmu pengetahuan, saya memberikan kepada Perpustakaan Universitas Sanata Dharma karya ilmiah saya yang berjudul:
AKTIVITAS ANTIMIKROBA FRAKSI PETROLEUM ETER, KLOROFORM, ETANOL BUNGA PULU (Chartamus tinctorius L.) TERHADAP Staphylococcus aureus, Escherichia coli, dan Candida albicans.
beserta perangkat yang diperlukan (bila ada). Dengan demikian saya memberikan kepada Perpustakaan Universitas Sanata Dharma hak untuk menyimpan, mengalihkan dalam bentuk media lain, mengelolanya dalam bentuk pangkalan data, mendistribusikannya secara terbatas, dan mempublikasikannya di internet atau media lain untuk kepentingan akademis tanpa perlu meminta izin kepada saya maupun memberikan royalti kepada saya selama tetap mencantumkan nama saya sebagai penulis.
Demikian pernyataan ini saya buat dengan sebenarnya.
Dibuat di Yogyakarta Pada tanggal : 23 Mei 2013 Yang Menyatakan
vii
KATA PENGANTAR
Puji syukur kehadirat Allah atas rahmat dan hidayahNya sehingga pada akhirnya penulis dapat menyelesaikan penyusunan skripsi dengan judul “Aktivitas Antimikroba Fraksi Petroleum Eter, Kloroform, Etanol Bunga Pulu (Chartamus tinctorius L.) terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans”.
Penyusunan skripsi ini sebagai syarat untuk memperoleh gelar Sarjana Farmasi Program Studi Farmasi Universitas Sanata Dharma. Perjuangan panjang dalam penyusunan skripsi ini tentunya tidak lepas dari bantuan dan kerja sama berbagai pihak. Oleh karena itu, penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada:
1. Bapak dan Ibu tercinta, Harya Adi Setiawan dan Sumarsih atas kesabaran dan kepercayaan, tulusnya doa dan kasih sayang, dukungan moral dan materi, serta semangat yang selali mengiringi langkahku.
2. Bapak Ipang Djunarko, M.Sc., Apt. Selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
3. Ibu Agustina Setiawati M.Sc., Apt. selaku Dosen Pembimbing yang telah meluangkan waktunya untuk memberikan bimbingan, dukungan moril, pengarahan, evaluasi dan saran mulai penyusunan proposal hingga skripsi ini selesai.
viii
5. Ibu Rini Dwiastuti selaku dosen pembimbing akademik yang telah begitu perhatian, terima kasih atas saran, masukan dan petuah yang sangat berarti baik itu menunjang akademik maupun kepribadian saya.
6. Ibu Maria Dwi Jumpowati, S.Si yang telah bersedia meluangkan waktu untuk berdiskusi, memberi semangat serta masukan kepada penulis.
7. Teman-teman IA1 SMAN I Kolaka yang telah banyak mengisi cerita hidup. 8. Teman-teman seperjuanganku : Wanda Indriani W., Johanes Putra W.,
Bernadeta Arum W., terimaksih untuk doa, kerjasama, dan dukungannya. 9. Seluruh laboran dari lantai satu sampai empat, terutama Mas Wagiran, Mas
Sigit, Pak Mukmin yang telah banyak membantu selama penelitian sampai skripsi dapat diselesaikan.
10.Teman-teman kelas A FSM 2009 untuk kebersamaan dan dukungannya.
11.Teman-teman KKN Kelompok 20 XLIV: Victor, Evy Feny Veronika, Maria Sukma, Agustin Nugroho, Fenny, Elsa Ridho terimakasih untuk pelajaran hidup yang berharga, canda tawa dan kebersamaan kita.
12.Semua pihak yang telah membantu dan mendukung penulis dari awal sampai skripsi ini selesai yang tidak dapat disebutkan satu persatu.
Penulis menyadari bahwa penelitian dan penyusunan skripsi ini jauh dari kesempurnaan dan masih memerlukan kritik dan saran yang membangun dari segi manapun. Akhir kata, penulis berharap hasil penelitian ini bermanfaat dikemudian hari.
ix
LEMBAR PERNYATAAN KEASLIAN KARYA
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS
KATA PENGANTAR
x
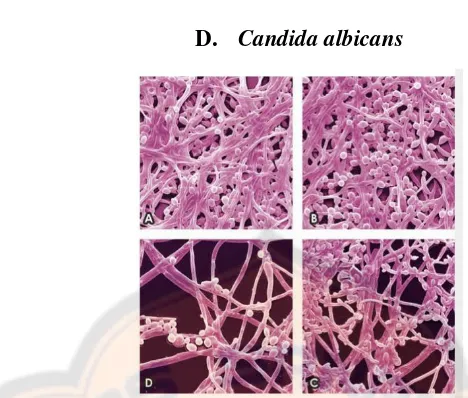
2. Patogenesis dan tanda klinis D. Candida albicans
J. Metode Pengujian Aktivitas Antimikroba 1. Metode dilusi
2. Metode difusi K. Landasan Teori L. Hipotesis
BAB III. METODOLOGI PENELITIAN A. Jenis dan Rancangan Penelitian B. Variabel dan Definisi Operasional
1. Variabel penelitian 2. Definisi operasional C. Bahan dan Alat Penelitian
1. Bahan 2. Alat
D. Tata Cara Penelitian
1. Determinasi bunga pulu
xi 2. Pengumpulan bahan
3. Pengeringan dan pembuatan serbuk 4. Ekstraksi bertingkat serbuk bunga pulu 5. Pengujian potensi antimikroba
6. Identifikasi kandungan senyawa bunga pulu dengan uji tabung E. Kromatografi Lapis Tipis (Uji Penegasan Flavonoid)
F. Kromatografi Lapis Tipis (Uji Penegasan Minyak Atsiri) G. Analisis Hasil
BAB IV. HASIL DAN PEMBAHASAN A. Determinasi Tanaman
B. Hasil Pengumpulan dan Pembersihan C. Hasil Pengeringan
D. Hasil Penyarian Serbuk
E. Uji Aktivitas Antimikroba Fraksi Petroleum Eter, Kloroform, Etanol Bunga Pulu terhadap Staphylococcus aureus, Escherechia coli, dan Candida albicans dengan Metode Difusi
F. Skrining Fitokimia 1. Uji tabung
2. Uji kualitatif secara kromatografi lapis tipis BAB V. KESIMPULAN DAN SARAN
xii
DAFTAR TABEL
Tabel I. Pembuatan variasi konsentrasi uji Tabel II. Hasil maserasi serbuk bunga pulu Tabel III. Kepolaran relatif pelarut organik
Tabel IV. Diameter zona hambat fraksi petroleum eter bunga pulu (Carthamus tinctorius L.) terhadap Staphylococcus aureus,Escherechia coli dan Candida albicans
Tabel V. Diameter Zona Hambat fraksi kloroform bunga pulu (Carthamus tinctorius L.) terhadap Staphylococcus aureus,Escherechia coli dan Candida albicans
Tabel VI. Diameter zona hambat fraksi etanol bunga pulu (Carthamus
tinctorius L.) terhadap Staphylococcus aureus,Escherechia coli dan Candida albicans
Tabel VII. Hasil Pengamatan uji tabung terhadap serbuk bunga pulu
Tabel VIII. Nilai Rf dan warna bercak pada uji KLT dengan fase diam selulosa dan fase gerak n-butanol - asam asetat glasial - air (4:1:5)v/
v dan
pembanding rutin 0,05% untuk analisis flavonoid
Tabel IX. Nilai Rf dan warna bercak pada uji KLT dengan fase diam silika gel dan fase gerak toluen - etil asetat (93:7) v/v dan pembanding terpenoid
untuk analisis minyak atsiri
xiii
DAFTAR GAMBAR
Gambar 1. Bunga Pulu... Gambar 2. Staphylococcus aureus... Gambar 3. Escherecia coli pada media LA, Inkubasi 370C... Gambar 4. Mikrograf Fluoresensi Candida albicans dewasa... Gambar 5. Rumus Bangun Carvacrol... Gambar 6. Rumus Bangun Flavon... Gambar 7. Reaksi antara NaCl dengan senyawa fenolik... Gambar 8. Reaksi antara senyawa fenolik dengan FeCl3...
Gambar 9. Interaksi Flavonoid dengan CaSO4 membentuk kompleks khelat
Gambar 10. Hasil Uji KLT Flavonoid... Gambar 11. Reaksi Flavonoid dengan NH3...
Gambar 12. Hasil Uji KLT Minyak Atsiri...
xiv
DAFTAR LAMPIRAN
Lampiran 1. Surat Keterangan Selesai Melakukan Determinasi Lampiran 2. Sertifikat Hasil Uji Staphylococcus aureus ATCC 25923 Lampiran 3. Sertifikat Hasil Uji Escherichia coli ATCC 32518 Lampiran 4. Sertifikat Hasil Uji Candida albicans ATCC 10231
Lampiran 5. Foto Tanaman Bunga Pulu (Carthamus tinctorius L.) dan Serbuk Bunga Pulu
Lampiran 6. Foto Maserasi, Penguapan Menggunakan Rotaevaporator, Variasi Konsentrasi Fraksi Etanol, Fraksi Kloroform, Fraksi Petroleum eter Lampiran 7. Foto Hasil Uji Pendahuluan Serbuk Bunga Pulu (Carthamus tinctorius
L.) dengan uji tabung
Lampiran 8. Foto Hasil Uji Alkaloid Serbuk Bunga Pulu (Carthamus tinctorius L.) dengan Uji Tabung
Lampiran 9. Foto Hasil Uji Antrakinon Serbuk Bunga Pulu (Carthamus tinctorius L.) dengan Uji Tabung
Lampiran 10. Foto Hasil Uji Polifenol Serbuk Bunga Pulu (Carthamus tinctorius L.) dengan Uji Tabung
Lampiran 11. Foto Hasil Uji Tanin Serbuk Bunga Pulu (Carthamus tinctorius L.) dengan Uji Tabung
Lampiran 12. Foto Hasil Uji Saponin Serbuk Bunga Pulu (Carthamus tinctorius L.) dengan Uji Tabung
Lampiran 13. Foto Hasil KLT Fraksi Metanol Bunga Pulu (Carthamus tinctorius L.) dengan Deteksi UV 254, UV 365, dan Uap Amonia pada Analisis Flavonoid
xv
Lampiran 15. Foto Hasil Uji Potensi Antibakteri Fraksi Petroleum Eter terhadap Staphylococcus aureus ATCC 25923 dengan Metode Difusi Sumuran Lampiran 16. Foto Hasil Uji Potensi Antibakteri Fraksi Kloroform terhadap
Staphylococcus aureus ATCC 25923 dengan Metode Difusi Sumuran Lampiran 17. Foto Hasil Uji Potensi Antibakteri Fraksi Etanol terhadap Staphylococcus
aureus ATCC 25923 dengan Metode Difusi Sumuran
Lampiran 18. Foto Hasil Uji Potensi Antibakteri Fraksi Petroleum Eter terhadap Escherichia coli ATCC 32518 dengan Metode Difusi Sumuran
Lampiran 19. Foto Hasil Uji Potensi Antibakteri Fraksi Kloroform terhadap Escherichia coli ATCC 32518 dengan Metode Difusi Sumuran
Lampiran 20. Foto Hasil Uji Potensi Antibakteri Fraksi Etanol terhadap Escherichia coli ATCC 32518 dengan Metode Difusi Sumuran
Lampiran 21. Foto Hasil Uji Potensi Antibakteri Fraksi Petroleum Eter terhadap Candida albicans ATCC 10231 dengan Metode Difusi Sumuran
Lampiran 22. Foto Hasil Uji Potensi Antibakteri Fraksi Kloroform terhadap Candida albicans ATCC 10231 dengan Metode Difusi Sumuran
Lampiran 23. Foto Hasil Uji Potensi Antibakteri Fraksi Etanol terhadap Candida albicans ATCC 10231 dengan Metode Difusi Sumuran Lampiran 24. Foto Kontrol Media dan Pertumbuhan Staphylococcus aureus,
Escherichia coli, dan Candida albicans Lampiran 25. Foto Kemampuan Difusi Fraksi Petroleum Eter, Kloroform, Etanol
Bunga Pulu (Carthamus tinctorius L.) pada Media Agar
xvi INTISARI
Bunga pulu (Carthamus tinctorius L.) merupakan tanaman obat yang secara empiris digunakan untuk mengatasi kolesterol tinggi, angina pectoris, dan berbagai penyakit lainnya. Kandungan dari Carthamus tinctorius L.ialah flavonoid yang terdiri dari chalcones, carthamin, carthamone, lignin, linalool, carvacrol,dan thymol. Profil resistensi antibiotik terus berkembang terhadap Staphylococcus aureus, Escherechia coli, dan Candida albicans. Perlu dilakukan eksplorasi aktivitas antimikroba dari bunga pulu terhadap bakteri atau fungi tersebut untuk menemukan agen antimikroba alternatif yang lebih poten.
Penelitian ini termasuk penelitian eksperimental murni rancangan acak lengkap pola satu arah. Ekstraksi bertingkat bunga pulu dilakukan menggunakan pelarut petroleum eter, kloroform, dan etanol menggunakan metode maserasi. Uji aktivitas antimikroba menggunakan metode difusi sumuran, dilanjutkan metode dilusi padat untuk mengetahui Kadar Hambat Minimal (KHM) dan Kadar Bunuh Minimum (KBM). Serbuk bunga pulu kemudian diuji secara kualitatif untuk mengidentifikasi kandungan senyawanya. Data zona hambat yang diperoleh kemudian dianalisis secara deskriptif komparatif.
Hasil penelitian menunjukkan fraksi petroleum eter, kloroform, etanol tidak memiliki aktivitas antimikroba terhadap Staphylococcus aureus, Escherechia coli, Candida albicans. Kandungan senyawa aktif hasil uji KLT diperkirakan adalah flavonoid, senyawa fenolik dan minyak atsiri.
xvii ABSTRACT
Pulu flower (Carthamus tinctorius L.) is a medicinal plant, that is empirically used to treat high cholesterol, angina pectoris, and other disease. Constituents of Carthamus tinctorius L. is flavonoid such as chalcones, carthamin, carthamone, lignin, linalool, carvacrol,and thymol Profil of antibiotic resistance is growing among Staphylococcus aureus, Escherechia coli, and Candida albicans. Need some exploration of antimicrobial activity Pulu flower towards bacterial or fungi, to discover alternative antimicrobial agents are potently.
This research is purely experimental, completely randomized design. Terraced extraction pulu flower perfomed using petroleum ether, chloroform, and ethanol using material method. Antimcrobial activity test using diffusion method, followed by dense dilution method to determine the Minimal Inhibitory Concentration (MIC) and Minimal Bactericidal Concentration (MBC). The data then tested qualitatively to identify the content of the active compound. The result was analysed using comparative-descriptive analysing method.
The result showed petroleum ether, chloroform, and ethanol extract does not have antimicrobial activity againts Staphylococcus aureus, Escherechia coli, and Candida albicans. The content of active compound predicted with TLC assay are flavonoids and essential oil (Carvacrol).
1 BAB I PENGANTAR A.Latar Belakang
Penyakit infeksi merupakan salah satu masalah dalam bidang kesehatan yang dari waktu ke waktu dan terus berkembang dan pada tahun 2002, sebanyak 14,9 juta manusia meninggal akibat penyakit infeksi. Penyakit infeksi kulit, demam, dan sakit perut merupakan penyakit yang banyak dijumpai dimasyarakat. Penyakit tersebut antara lain disebabkan oleh bakteri Staphylococcus aureus (10.460 kasus), Escherichia coli (7.632 kasus) dan jamur. Jamur yang paling menginfeksi manusia
adalah jamur oportunistik. Salah satu agen jamur yang ditemui dengan frekuensi terbesar adalah Candida albicans dengan jumlah 7.808 kasus di Amerika Serikat (Madigan, Martinko, Dunlap, Clark, 2009).
Bunga pulu atau kasumba turatea (Carthamus tinctorius L.) dalam bahasa Bugis digunakan secara empiris untuk menurunkan kolesterol tinggi, mengatasi angina pectoris, tromboangitis, hipertensi, kanker, nyeri haid, dan sakit perut setelah melahirkan (Wijayakusama, 2008). Analisis kimia dari ekstrak bunga pulu mengungkapkan senyawa utama ialah chartamin, chartamone, neo-chartamin, nona-cosane, zat warna kuning saflawer, safflomin A, dipalmitin, adenosid, beta-sitosterol, dan polisakarida (Wijayakusuma, 2008a). Analisis minyak atsiri bunga pulu ditemukan thymol, carvacrol, linalool, dan eugenol (Ziarati, Asgarpanah, Klanifard, 2012). Beberapa senyawa tersebut berpotensi mempunyai aktivitas antimikroba (Nostro dan Papalia, 2012); (Akroum, Satta, Lalaoui, 2009).
1. Permasalahan
a. Apakah fraksi petroleum eter, kloroform, dan etanol bunga pulu memiliki aktivitas antimikroba terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans?
b. Berapa Kadar Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) dari fraksi petroleum eter, kloroform, dan etanol bunga pulu terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans?
c. Golongan senyawa apakah yang terkandung didalam bunga pulu?
2. Keaslian penelitian
3. Manfaat penelitian a. Manfaat teoritis
Penelitian ini diharapkan dapat mengembangkan khasanah ilmu pengetahuan khususnya di bidang kesehatan tentang penggunaan bunga pulu (Carthamus tinctorius L.) yang berkhasiat sebagai antimikroba.
b. Manfaat praktis
Penelitian ini diharapkan dapat memberikan informasi tentang manfaat bunga pulu sebagai pengobatan alternatif bagi masyarakat terutama untuk mengobati penyakit yang disebabkan oleh infeksi bakteri dan jamur.
B.Tujuan Penelitian 1. Tujuan umum
Tujuan umum dari penelitian ini adalah untuk mengetahui aktivitas antimikroba fraksi petroleum eter, kloroform, dan etanol bunga pulu terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans.
2. Tujuan khusus
a. Mengetahui aktivitas antimikroba fraksi petroleum eter, kloroform, dan etanol bunga pulu terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans.
b. Mengetahui Kadar Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) dari fraksi petroleum eter, kloroform, dan etanol bunga pulu terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans.
5
BAB II
PENELAAHAN PUSTAKA
A.Bunga Pulu
1. Klasifikasi (Birla Institute of Scientific Research, 2010). Kingdom : Plantae (Tumbuhan)
Divisio : Magnoliophyta (Tumbuhan berbunga)
Sub Divisio : Spermatophyta (Tumbuhan berbiji)
Classis : Dicotyledoneae (Tumbuhan berkeping dua)
Ordo : Asterales
Famili : Asteraceae
Genus : Carthamus
Spesies : Carthamus tinctorius Linn.
Gambar 1. Bunga Pulu (Nagaraj dkk., 2012)
2. Uraian tanaman
Bunga pulu merupakan herba tahunan, tanaman bercabang yang tingginya
dapat mencapai 0,3 -1,5 m. Tanaman ini memiliki sistem akar yang luas dengan akar
30 cm kedalam tanah. Batang yang licin, berkayu, silinder dan berwarna kehijauan di
dekat pangkalan. Daun diatur dalam roset dari dasar, panjang 4-20 cm dan luas 1-5 cm,
hijau tua mengkilap, daun atas menanggung banyak duri tajam. Setiap batang beruang
perbungaan terminal. Ini adalah kapitulum bulat, 1,3 -3,5 cm, mengandung 20-80
tabung oranye-merah, bunga menjadi merah tua saat berbunga. Bunga masing-masing
menghasilkan satu buah. Buah safflower adalah achenes, biasanya disebut biji,
dikelilingi oleh lambung fibrosa tebal yang halus, mengkilap dan runcing sekitar 6-9
mm, berwarna putih atau kecoklatan dan putih dengan abu-abu, cokelat atau garis-garis
hitam (Heuze dan Tran, 2011).
3. Kandungan kimia
Kandungan dari Carthamus tinctorius L. ialah flavonoid yang terdiri dari
chalcones, carthamin, carthamone, dan lignin (Cai, Luo, Sun, Corke, 2003). Analisis kimia dari ekstrak bunga pulu mengungkapkan konstituen utama ialah chartamin, chartamone, neo-chartamin, nona-cosane, zat warna kuning saflower, safflomin A, dipalmitin, adenosid, beta-sitosterol, dan polisakarida (Wijayakusuma, 2008a). 4. Sifat kimiawi dan aktivitas farmakologi
B. Staphylococcus aureus
Gambar 2. Staphylococcus aureus (Stierman, 2012)
Staphylococcus aureus merupakan bakteri Gram positif, anaerob fakultatif
yang tidak membentuk spora, tidak bergerak dinding selnya mengandung
peptidoglikan dan asam teikoat. Selnya berbentuk bola dengan diameter kira-kira 1 µm
tersusun berkelompok menyerupai buah anggur. Tumbuh paling cepat pada suhu 37
0
C. Staphylococcus aureus relatif tahan terhadap panas (500C selama 30 menit) dan
tahan terhadap natrium klorida 9%, tetapi dapat dihambat zat kimia tertentu (Jawetz,
Melnick, Adelberg, 2005). Sifat patogenesis dapat diamati terhadap kemampuan
memfermentasi materi secara aerob, kemampuan memecah gelatin, dan menghemolisis
darah (Todar, 2012). Staphylococcus aureus membentuk koloni abu-abu hinga kuning
emas, karakteristik pertumbuhan dengan menghasilkan katalase, yang membedakan
dengan streptokokus, bakteri ini memfermentasi karbohidrat, menghasilkan asam laktat
dan tidak menghasilkan gas. Aktifitas proteolitik bervariasi dari satu galur ke galur lain,
menyebabkan penyakit pada hampir semua jaringan tubuh yang terutama adalah abses.
Bakteri ini merupakan flora normal pada rongga hidung bagian depan, perineum,
saluran pencernaan, atau kulit (Jawetz, Melnick, dan Adelberg, 2005).
Staphylococcus aureus dapat menyebabkan penyakit berkat kemampuannya
beberapa bahan ekstraseluler. Beberapa bahan tersebut adalah enzim, yang lain dapat
berupa toksin, meskipun fungsinya adalah sebagai enzim. Beberapa toksin berada
dibawah kontrol genetik plasmid, beberapa dibawah kontrol kromosom dan yang lain
mekanisme kontrol genetiknya belum ditemukan (Jawetz, Melnick, dan Adelberg,
2005).
1. Struktur antigen
Staphylococcus mengandung antigen polisakarida dan protein seperti zat lain
yang penting dalam struktur dinding sel. Peptidoglikan, suatu polimer polisakarida
yang mengandung subunit-subunit yang bergabung memberikan eksoskeleton yang
kaku dari dinding sel. Peptidoglikan dirusak oleh asam kuat atau paparan terhadap
lisozim. Infeksi akan merangsang pembentukan interleukin (pirogen endogen) dan
antibodi opsonin oleh monosit; dan ini dapat menjadi penarik kimiawi bagi leukosit
polimorfonuklear, mempunyai aktivitas seperti endotoksin dan mengaktivasi
komplemen (Jawetz, Melnick, dan Adelberg, 2005).
Protein A merupakan komponen dinding sel kebanyakan galur
Staphylococcus aureus yang bisa mengikat ke bagian Fc molekul IgG kecuali IgG3.
Meskipun IgG terikat pada protein A, namun fragmen Fab tetap bisa bebas berikatan
dengan antigen spesifik. Protein A telah menjadi reagen yang penting dalam imunologi
dan teknologi laboratorium diagnostik. Beberapa galur Staphylococcus aureus
mempunyai kapsul yang menghambat fagositosis oleh lekosit polimorfonuklear kecuali
jika terdapat antibodi spesifik. Sebagian besar galur Staphylococcus aureus
mempunyai koagulase atau faktor penggumpalan pada permukaan dinding sel, ikatan
koagulase secara non enzimatik pada fibrinogen, menyebabkan agregasi pada bakteri
2. Toksin dan enzim
Staphylococcus aureus menghasilkan katalase, yang mengubah hidrogen
peroksida menjadi air dan oksigen; koagulase, protein yang menyerupai enzim yang
mampu menggumpalkan plasma yang ditambah dengan oksalat atau sitrat dengan
adanya suatu faktor yang terdapat dalam serum. Faktor serum bereaksi dengan
koagulase untuk membentuk esterase dan aktivitas penggumpalan, dengan cara yang
sama ini untuk mengaktivasi protrombin menjadi trombin. Cara kerja koagulase adalah
dalam lingkup kaskade penggumpalan plasma normal. Koagulase dapat membentuk
fibrin pada permukaan Staphylococcus, ini bisa mengubah ingestinya oleh sel fagositik
atau pengrusakannya dalam sel fagosit; eksotoksin, ini meliputi beberapa toksin yang
bersifat letal jika disuntikkan pada binatang, menyebabkan nekrosis pada kulit, dan
berisi larutan hemolisis yang dapat dipisahkan dengan elektroforesis. Aflatoksin
(hemolisin) adalah protein heterogen yang dapat melisiskan eritrosit dan merusak
platelet serta dimungkinkan sama dengan faktor dermonekrotik dari eksotoksin;
Lekosidin, toksin Staphylococcus aureus ini dapat membunuh sel darah putih pada
berbagai binatang. Peran toksin dalam patogenesis tidak jelas, karena Staphylococcus
aureus yang patogenik tidak dapat membunuh sel darah putih dan dapat difagositosis
efektif seperti yang nonpatogenik; enterotoksin, ada sedikitnya enam (A-F) toksin larut
yang dihasilkan oleh hampir 50 % galur Staphylococcus aureus. Seperti TSST-1,
enteroktoksin adalah superantigen yang berikatan dengan molekul MHC kelas II,
menimbulkan stimulasi sel T, entertoksin stabil terhadap panas dan resisten terhadap
3. Patogenesis dan patologi
Staphylococcus aureus yang patogenik dan bersifat invasif menghasilkan
koagulase dan cenderung untuk menghasilkan pigmen kuning dan menjadi hemolitik.
Kemampuan patogenik Staphylococcus aureus adalah pengaruh gabungan antara
faktor ektraseluer dan toksin bersama dengan daya sebar invasif (Jawetz, Melnick, dan
Adelberg, 2005).
Staphylococcus aureus menetap di folikel rambut menyebabkan nekrosis
jaringan (faktor dermonekrotik). Koagulase dihasilkan dan mengkoagulasi fibrin di
sekitar lesi dan di dalam limfatik, membentuk dinding yang menghambat proses
penyebaran dan diperkuat lagi oleh akumulasi sel inflamasi dan kemudian jaringan
fibrosa. Di dalam pusat lesi, terjadi likuefaksi dan nekrosis jaringan (dipacu oleh
hipersensitivitas tipe lambat) pada bagian abses yang lemah. Drainase cairan pusat
jaringan nekrotik diikuti dengan pengisian secara kavitas oleh jaringan granulasi dan
akhirnya terjadilah penyembuhan (Jawetz, Melnick, dan Adelberg, 2005).
Supurasi fokal (abses) adalah khas untuk infeksi stafilokokus. Dari tiap fokus
manapun, organisme dapat menyebar melalui aliran limfatik dan aliran darah ke bagian
lain dalam tubuh. Supurasi yang terjadi dalam pembuluh darah vena, yang berhubungan
dengan trombosis, merupakan gambaran umum proses penyebaran tersebut. Pada
osteomielitis, fokus primer pertumbuhan Staphylococcus aureus adalah khas di
pembuluh darah tepi dari metafisis menyebabkan pneumonia, meningitis, empiema,
endokarditis atau sepsis dengan supurasi di tiap organ. Staphylococcus aureus
mempunyai kemampuan invasi yang rendah, terlibat dalam banyak infeksi kulit
C.Escherichia coli
Gambar 3. Eschericia coli pada SEM (Rogers, 2011)
Escherichia coli merupakan bakteri Gram negatif yang banyak
ditemukan pada ileum caudal, berbentuk batang pendek, dan dapat begerak. Pada
lingkungan yang kurang baik dapat membentuk spora, dan merupakan kuman
aerob fakultatif. Escherichia coli menghasilkan tes positif terhadap indole, lisin
dekarboksilase, dan memfermentasi manitol dan menghasilkan gas dari glukosa.
Bakteri ini merupakan bagian terbesar dari flora usus dan dianggap sebagai
bakteri yang tidak patogen dalam saluran pencernaan. Escherichia coli akan
bersifat patogen apabila berada terdapat di luar saluran pencernaan dan pada saat
kondisi tubuh manusia menurun (Jawetz, Melnick, dan Adelberg, 2005). 1. Struktur antigen
a. Antigen O merupakan bagian terluar dinding sel lipopolisakarida dan terdiri dari unit berulang polisakarida. Beberapa polisakarida spesifik O mengandung gula unik. Antigen O tahan terhadap panas dan alkohol biasanya dideteksi dengan cara aglutinasi bakteri.
dapat berpengaruh pada reaksi aglutinasi dengan antisera O. Antigen K menyebabkan perlekatan bakteri pada sel epitelial yang memungkinkan invasi ke sistem gastrointestinal atau saluran air kemih.
c. Antigen H terletak pada flagella dan didenaturasi oleh panas atau alkohol. Antigen H mengadakan aglutinasi dengan antibodi H, biasanya IgG
(Jawetz, Melnick, dan Adelberg, 2005).
2. Patogenesis dan tanda klinis
Manifestasi klinis infeksi Escherechia coli tergantung pada tempat infeksi, dan tidak dapat dibedakan dengan gejala atau tanda dari proses-proses yang disebabkan oleh bakteri lain. Berikut beberapa penyakit yang berhubungan dengan Escherechia coli:
a. Infeksi sistem saluran kencing, Escherechia coli merupakan penyebab paling banyak dari infeksi sistem saluran kencing dari jumlah untuk infeksi saluran kencing. Nefropatogenik Escherechia coli secara khas memproduksi hemolisin. Kebanyakan infeksi disebabkan oleh Escherechia coli dari sejumlah antigen O. Antigen K menjadi penting
dalam patogenesis infeksi sistem saluran bagian atas.
b. Escherechia coli yang berhubungan dengan penyakit diare. Escherechia coli yang umumnya menyebabkan diare ini diklasifikasikan berdasarkan sifat karakteristik dari virulensinya dan tiap kelompok menyebabkan penyakit dengan mekanisme yang berbeda.
berhubungan dengan kromosom mendukung pelekatan yang erat. Terjadi kehilangan microvili (affecement), pembentukan filamentasi actin atau struktur seperti cangkir, dan biasanya masuk ke dalam sel mukosa.
2) Enteroxigenic E. coli (ETEC) merupakan penyebab umum diare pada musafir. Strain ETEC memproduksi sebuah eksotoksin yang sifatnya labil terhadap panas (LT) dibawah kontrol plasmid. Sub unit B melekat dengan Gml gangliosida pada sisi sel epitel dari usus kecil dan memberikan fasilitas sebuah pemasukan dari subunit A ke dalam sel, dimana mengaktivasi adenylyl cyclase. Hal ini ditandai dengan adanya peningkatan konsentrasi lokal dari cyclic adenosine monophosfat (cAMP), yang menghasilkan hiperekskresi yang sering dan lama dari air dan klorid serta menghambat penyerapan natrium. Lumen usus digelembungkan dengan cairan hipermotility dan diare terjadi.
3) Enterohemorhagic E. coli (EHEC) memproduksi verotoksin, dan dinamakan berdasarkan efek sitotoksik pada sel vero, merupakan biakan sel ginjal dari monyet hijau Afrika. Terdapat sedikitnya dua bentuk antigenik dari toksin. EHEC berhubungan dengan kolitis hemoragik, bentuk diare yang berat dan dengan sindroma uremia hemolitik, suatu penyakit akibat gagal ginjal akut, anemia hemolitik mikroangiopatik, dan trombositopenia.
berkembang dan dalam perjalanan ke negara tersebut. Strain EIEC memfermentasi laktosa dengan lambat atau tidak memfermentasi laktosa dan tidak motil. EIEC menyebabkan penyakit dengan menyerang sel epithelial mukosa usus.
5) Enteroagregative E. coli (EAEC) menyebabkan diare akut dan kronis. Patogenesis EAEC penyebab diare tidak begitu dipahami dengan baik, meskipun demikian dinyatakan bahwa EAEC melekat pada mukosa intestinal dan menghasilkan enterotoksin dan sitotoksin. Akibatnya adalah kerusakan mukosa, pengeluaran sejumlah besar mukus, dan terjadi diare.
c. Sepsis bila pertahanan inang normal tidak mencukupi. Escherechia coli dapat memasuki aliran darah dan menyebabkan sepsis. Bayi yang baru lahir dapat sangat rentan terhadap sepsis Escherechia coli karena tidak memiliki antibodi IgM. Sepsis dapat terjadi akibat infeksi saluran kemih. d. Meningitis pada bayi, salah satunya disebabkan oleh Escherechia coli
D. Candida albicans
Gambar 4. Mikrograf fluoresensi Candida albicans dewasa. A) sebelum diinkubasi dengan thymol, biofilm sangat banyak pada jaringan multi-layer sel fungi dan berbentuk serabut. B) setelah diinkubasi dengan Thymol ½x dari MIC selama 24 jam, terdapat sedikit perubahan terlihat dibandingkan dengan kontrol. C) setelah diinkubasi dengan Thymol 1x dari MIC terjadi perubahan struktur biofilm. D) setelah diinkubasi dengan Thymol 2x dari MIC jelas menghambat semua unsur dan merusak struktur filamen (Braga, Sasso, Culici, Alfieri, 2008)
Candida albicans termasuk organisme eukariotik dengan bentuk lonjong dan
bertunas, yang menghasilkan pseudomiselium yang terdiri atas pseudohifa yang
membetuk blastokonidia pada nodus-nodus dan kadang-kadang klamidokonidia pada
ujung-ujungnya baik dalam biakan maupun dalam jaringan. Pada agar sabouraud yang
diinkubasi pada suhu kamar atau 37 0C selama 24 jam, spesies Candida menghasilkan
koloni-koloni halus berwarna krem yang mempunyai bau seperti ragi. Pertumbuhan
permukaan terdiri atas sel-sel bertunas lonjong. Candida adalah anggota flora normal
selaput lendir saluran pernafasan, saluran pencernaan, dan genitalia wanita. Pada
tempat ini Candida albicans menjadi dominan dan cenderung patogen. Candida
albicans patogen dapat menimbulkan infeksi dalam aliran darah, endokardiosis, atau
infeksi pada mata dan organ lain (Simatupang, 2009).
Candida dapat eksis dalam rongga mulut sebagai saprofit tanpa menyebabkan
sebagai faktor penyebab paling umum kandidiasis oral. Candida albicans dapat
ditemukan dalam rongga mulut yang sehat pada konsentrasi rendah (20 sel/cc saliva).
Dalam konsentrasi ini, organisme tidak bisa terdeteksi di bawah mikroskop, tetapi
hanya dapat dideteksi melalui kultur dalam media tertentu seperti pada Dextrose
Sabouroud Agar dalam bentuk koloni. Keseimbangan flora rongga mulut dapat
berubah menimbulkan suatu keadaan patologis atau penyakit karena beberapa faktor
seperti kesehatan mulut yang buruk, obat immunosupresan, penyakit sistemik yang
menurunkan daya tahan lokal tubuh (Tanjong cit., Sudiono, 2006).
1. Struktur fisik
2. Patogenesis
Infeksi Candida albicans berkaitan dengan perubahan bentuk sel-sel Candida albicans dari bentuk yeast menjadi bentuk mycelium. Mycelium berbentuk panjang dengan struktur seperti akar yang disebut rhizoid. Rhizoid dapat menembus mukosa, dan dapat juga masuk melalui sel-sel epitel di saluran cerna, invasi ini dapat berlanjut hingga ke pembuluh darah dan menyebabkan septikemia (Riskillah cit., Kayser, Bienz, Eckert, Zinkernage, 2005).
Menempelnya mikroorganisme dalam jaringan sel host menjadi syarat mutlak untuk berkembangnya infeksi. Secara umum diketahui bahwa interaksi antar mikroorganisme dan sel pejamu diperantarai oleh komponen spesifik dari dinding sel mikroorganisme, adhesin dan reseptor. Makanan dan manoprotein merupakan molekul-moleku Candida albicans yang mempunyai aktifitas adhesif. Khitin, komponen kecil yang terdapat pada dinding sel Candida albicans juga berperan dalam aktifitas adhesif. Setelah terjadi proses penempelan, Candida albicans berpenetrasi ke dalam sel mukosa. Dalam hal ini enzim yang berperan adalah aminopeptidase dan asam fosfatase. Setelah proses penetrasi, semua tergantung dari keadaan imun dari host (Tjampaksari, 2006).
E. Ekstraksi Bertingkat
Ekstraksi adalah teknik pemisahan suatu senyawa berdasarkan perbedaan
distribusi zat diantara dua pelarut yang saling bercampur. Pada umumnya zat terlarut
yang diekstrak bersifat tidak larut atau sedikit larut dalam suatu pelarut tetapi mudah
larut dengan pelarut lain. Metode ekstraksi yang tepat ditemukan oleh tekstur
kandungan air bahan-bahan yang akan diekstrak dan senyawa-senyawa yang akan
diisolasi (Harbone,1996). Telah dikembangkan suatu teknik ekstraksi dengan ekstraksi
bertingkat menggunakan pelarut yang berbeda tingkat polaritasnya. Metode ekstraksi
bertingkat memiliki keuntungan karena semua senyawa aktif yang berbeda polaritasnya
dapat diekstraksi sesuai dengan tingkat polaritasnya terhadap pelarut (Damayanti dan
Suparjana, 2007).
F. Maserasi
Maserasi merupakan cara penyarian yang sederhana, maserasi dilakukan
dengan merendam serbuk atau daun segar dalam cairan penyari. Cairan penyari akan
menembus dinding sel dan masuk ke dalam rongga sel yang mengandung zat aktif. Zat
aktif larut dan karena adanya perbedaan konsentrasi antara larutan didalam dengan
diluar sel, maka larutan yang terpekat akan terdesak ke luar. Peristiwa tersebut berulang
sehingga terjadi kesetimbangan konsentrasi antara di luar dan di dalam sel (Departemen
Kesehatan RI, 1986).
Maserasi digunakan untuk penyarian simplisia yang mengandung zat aktif
yang mudah larut dalam cairan penyari, tidak mengandung zat yang mudah
mengembang dalam cairan penyari, tidak mengandung benzoin, stirak dan lain-lain
menggunakan pelarut tertentu sesuai dengan sifat senyawa yang akan dipisahkan.
Pemisahan pelarut berdasarkan kaidah like dissolved like artinya suatu senyawa polar
akan larut dalam pelarut polar. Ekstraksi dapat dilakukan dengan bermacam-macam
metode, tergantung dari tujuan ekstraksi, jenis pelarut yang digunakan dan senyawa
yang diinginkan (Pratiwi, 2008).
Keuntungan cara penyarian dengan maserasi adalah cara pengerjaan,
peralatan sederhana, dan mudah dilakukan. Adapun kerugian cara maserasi adalah
waktu pengerjaan yang lama dan penyarian kurang sempurna. Cara maserasi ini dapat
dipercepat dengan menggunakan mesin pengaduk yang terus-menerus berputar
sehingga mempersingkat waktu maserasi menjadi 6 – 24 jam (Departemen Kesehatan
RI, 1986).
G. Kromatografi Lapis Tipis
Kromatografi Lapis Tipis (KLT) ialah metode pemisahan fisikakimia. Pada
KLT ini menggunakan dua macam fase yaitu fase diam dan fase gerak. Fase diam
merupakan lapisan berpori dan akan menghasilkan pemisahan pada plat. Fase gerak
atau pelarut pengembang ialah media angkut dan terdiri atas satu atau beberapa pelarut,
yang bergerak didalam fase diam karena adanya gaya kapiler (Rohman dan Gandjar,
2007).
Prinsip kerja KLT berupa lapisan yang memisahkan terdiri atas bahan berbutir
atau fase diam ditempatkan pada penyangga berupa plat gelas, logam atau lapisan yang
cocok. Campuran yang akan dipisah berupa larutan dan ditotolkan berupa bercak atau
pita. Setelah plat ditaruh di dalam bejana tertutup rapat yang berisi larutan pengembang
pengembangan, selanjutnya senyawa yang tidak berwarna harus ditampakkan atau
dideteksi dengan lampu ultraviolet atau dengan pereaksi semprot (Rohman dan
Gandjar, 2007). Pada kromatogram KLT dikenal istilah faktor retardasi (Rf) yang
didefinisikan
𝑅𝑓 =𝐽𝑎𝑟𝑎𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑚𝑝𝑢ℎ 𝑓𝑎𝑠𝑒 𝑔𝑒𝑟𝑎𝑘𝐽𝑎𝑟𝑎𝑘 𝑦𝑎𝑛𝑔 𝑑𝑖𝑡𝑒𝑚𝑝𝑢ℎ 𝑠𝑜𝑙𝑢𝑡
(Rohman dan Gandjar, 2007).
H. Minyak Atsiri
Minyak atsiri (disebut juga minyak menguap atau minyak etheral) adalah
cairan berwujud minyak yang beraroma yang berasal dari berbagai bagian tumbuhan
(bunga, kuncup, biji, daun, ranting, kulit, batan, dan rempa, kayu, buah, dan akar)(Di
Pasqua, De Feo, Villani, Mauriello cit. Burt., 2004). Minyak atsiri yang bagian
utamanya terpenoid, biasanya terdapat pada fraksi yang tersuling. Zat inilah penyebab
wangi, harum, atau bau yang khas pada banyak tumbuhan minyak atsiri larut alkohol,
eter, dan pelarut lipid lainnya praktis tidak larut air (Kokate, Purohit, Gokhale, 2009).
Zat pengawet alami salah satunya adalah komponen-komponen minyak atsiri dari
ekstrak tumbuhan seperti rempah-rempah, tanaman tahunan, dan rumput-rumputan
(Ardiansyah, 2007).
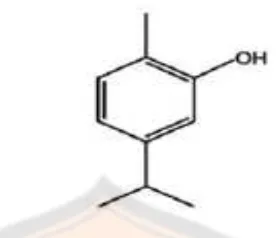
Carvacrol, thymol dan eugenol adalah komponen minyak atsiri yang
diketahui memilik aktivitas antibakteri yang tinggi. Ketiga senyawa ini masuk dalam
Gambar 5. Rumus bangun carvacrol (Nostro dan Papalia, 2012)
Carvacrol atau 2-metil- 5-(1 Metiletil)- fenol adalah monoterpen fenol.
Dibiosintesis dari -terpinen melewati p-cimen. Aktivitas antibakteri carvacrol telah
dikaitkan dengan efek yang cukup besar terhadap struktur dan fungsi dari membran
sitoplasma (Nostro dan Papalia, 2012).
Carvacrol berinteraksi dengan lipid bilayer dari membran sitoplasma
menyebabkan perluasan dan destabilisasi struktur membran dan meningkatkan fluiditas
dan permeabilitas membran. Pada konsentrasi subletal carvacrol mengubah komposisi
asam lemak dari sitoplasma yang mengarah terhadap perubahan struktur permukaan sel
membentuk saluran membran untuk ion, materi seluler, asam nukleat, dan ATP
meninggalkan sitoplasma, menyebabkan kerusakan pada kolam ATP intrasel, baik
dengan pengurangan sintesis ATP atau peningkatan hidrolisis ATP (Nostro dan
Papalia, 2012).
I. Flavonoid
Senyawa flavonoid diturunkan dari unit C6–C3 (fenil-propana) yang
bersumber dari asam sikimat (via fenilalanin) dari unit C6 yang diturunkan dari jalur
poliketida. Fragmen poliketida ini disusun dari tiga molekul malonil-KoA, yang
triketida. Oleh karena itu, flavonoid berasal dari biosintesis gabungan terdiri atas
unit-unit yang diturunkan dari asam sikimat dan jalur poliketida (Heinrich, Barnes, Gibbons,
Williamson, 2010).
Unit awal triketida mengalami siklisasi oleh enzim kalkon sintase untuk
membentuk gugus kalkon pada flavonoid. Kemudian terjadi siklisasi untuk
menghasilkan cincin piranon yang mengandung inti flavonon, yang memiliki ikatan
C2-C3 teroksidasi (tak jenuh) untuk menghasilkan gugus flavonol pada flavonoid.
Senyawa flavonoid berperan dalam memberikan warna di alam terutama mahkota
kuning dan jingga, bahkan flavonoid yang tidak berwarna mengabsorbsi cahaya pada
spektrum UV (karena banyak gugus kromofor) (Heinrich, Barnes, Gibbons,
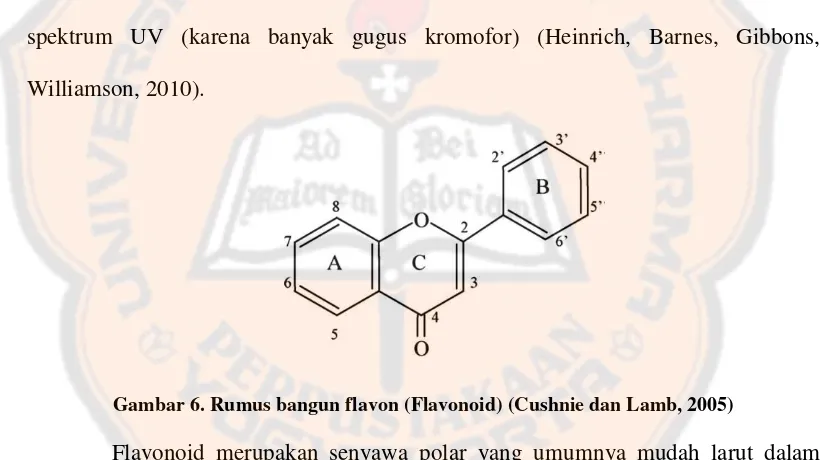
Williamson, 2010).
Gambar 6. Rumus bangun flavon (Flavonoid) (Cushnie dan Lamb, 2005)
Flavonoid merupakan senyawa polar yang umumnya mudah larut dalam
pelarut polar seperti etanol, metanol, butanol, dan aseton. Flavonoid merupakan
golongan terbesar dari senyawa fenol, senyawa fenol mempunyai sifat efektif
menghambat pertumbuhan virus, bakteri dan jamur (Khunaifi, 2010).
Mekanisme flavonoid menghambat pertumbuhan bakteri, yaitu dengan
menyebabkan terjadinya kerusakan permeabilitas dinding sel, mikrosom, dan lisosom.
komponen organik dan transpor nutrisi yang akhirnya akan mengakibatkan timbulnya
efek toksik bagi bakteri (Sabir, 2008).
J. Metode Pengujian Aktivitas Antimikroba
Pengujian ini bertujuan untuk mengetahui kemampuan suatu larutan uji dalam
menghambat atau membunuh mikroba. Metode pengujian antimikroba dapat
dibedakan menjadi dua yaitu:
1. Metode dilusi
Metode dilusi, pada prinsipnya antibiotik diencerkan sehingga diperoleh
beberapa macam kadar. Pada dilusi cair, tiap-tiap kadar sampel obat ditambahkan pada
suspensi bakteri pada media. Pada dilusi padat setiap kadar obat dicampur dengan
media agar kemudian ditanami bakteri. Pengamatannya adalah ada tidaknya
pertumbuhan bakteri atau bila mungkin tingkat kesuburan bakteri. Metode dilusi ini
dapat digunakan untuk menentukan KHM dan KBM (Jawetz, Melnick, dan Adelberg,
2005).
2. Metode difusi
Metode difusi merupakan metode yamg digunakan untuk mengukur potensi
antibakteri berdasarkan pengamatan luas zona jernih yang terbentuk disekitar tempat
penginokulasian obat karena berdifusinya obat (Jawetz, Melnick, dan Adelberg, 2005).
Dilakukan dengan cara menempatkan senyawa uji pada media padat yang lebih
ditanami dengan biakan bakteri. Metode difusi terdapat beberapa cara salah satunya
ialah metode sumuran, metode ini dilakukan dengan membuat lubang pada agar padat
yang telah diinokulasi dengan bakteri. Jumlah dan letak lubang disesuaikan dengan
Setelah dilakukan inkubasi, pertumbuhan bakteri diamati untuk melihat ada tidaknya
daerah hambatan di sekeliling lubang (Kusmayanti dan Agustini, 2007).
Prinsip metode pengenceran adalah senyawa antibakteri diencerkan hingga
diperoleh beberapa macam konsentrasi, kemudian masing-masing konsentrasi
ditambahkan suspensi bakteri uji dalam media cair. Perlakuan tersebut akan diinkubasi
dan diamati ada atau tidaknya pertumbuhan bakteri, yang ditandai dengan terjadinya
kekeruhan. Larutan uji senyawa antibakteri pada kadar terkecil yang terlihat jernih
tanpa adanya pertumbuhan bakteri uji, ditetapkan sebagai Kadar Hambat Minimum
(KHM) atau Minimal Inhibitory Concentration (MIC). Larutan yang ditetapkan KHM
selanjutnya dikultur ulang pada media cair tanpa pertumbuhan bakteri uji ataupun
senyawa antibakteri, dan diinkubasi selama 18-24 jam. Media cair yang tetap terlihat
jernih setelah inkubasi ditetapkan sebagai Kadar Bunuh Minimum (KBM) atau
Minimal Bactericidal Concentration (MBC) (Pratiwi, 2008).
K. Landasan Teori
Penyakit infeksi terus berkembang disertai dengan profil resistensi antibiotik
yang meningkat oleh beberapa bakteri dan fungi oportunistik diantaranya
Staphylococcus aureus, Escherichia coli, dan Candida albicans. Sehubungan dengan
itu perlu dilakukan eksplorasi bahan alam yang mempunyai aktivitas antimikroba yang
memiliki efek samping lebih kecil dan tersedia terus menerus.
Salah satu senyawa yang terkandung di dalam bunga pulu adalah flavonoid
(Cai, Luo, Sun, Corke, 2003). Flavonoid dapat tersari dalam etanol dan memiliki
aktivitas sebagai antibakteri (Akroum, Satta, Lalaoui, 2009). Penelitian Ziarati, Asgarpanah, Kianifard (2012) menyebutkan bahwa terdapat 29 konstituen yang dapat diidentifikasi pada minyak atsiri Carthamus tintorius. Dua puluh sembilan konstituen tersebut sebagian besar mempunyai aktivitas antibakteri terhadap bakteri patogen (Sokovic, Glamoclija, Marin, Brkic, van Griensven, 2010).
Aktivitas antimikroba fraksi petroleum eter, kloroform, etanol bunga pulu dilakukan dengan metode difusi sumuran yang ditunjukan dengan diameter zona hambat (zona jernih) yang dihasilkan dan metode dilusi untuk menentukan nilai KHM dan KBM. Prinsip metode difusi, yaitu pengamatan luas zona jernih pertumbuhan bakteri karena berdifusinya senyawa uji ke sekitar daerah penginokulasian. Penelitian mengenai adanya aktivitas antimikroba fraksi petroleum eter, kloroform, etanol bunga pulu terhadap Staphylococcus aureus, Escherechia coli, dan Candia albicans diharapkan dapat memberikan informasi kepada masyarakat dan perkembangan ilmu pengetahuan mengenai manfaat bunga pulu sebagai salah satu terapi alternatif penyakit infeksi yang disebabkan oleh mikroba di atas.
L. Hipotesis
Fraksi petroleum eter, kloroform, etanol bunga pulu (Carthamus tinctorius)
26 BAB III
METODOLOGI PENELITIAN A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk jenis penelitian rancangan eksperimental murni, dengan rancangan penelitian acak lengkap pola satu arah. Penelitian ini dilakukan di Laboratorium Farmakognosi-Fitokimia, Laboratorium Mikrobiologi, Fakultas Farmasi Universitas Sanata Dharma, Yogyakarta, dan Laboratorium Mikrobiologi, Balai Laboratorium Kesehatan Yogyakarta.
B. Variabel dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas : Fraksi petroleum eter, kloroform, etanol dengan konsentrasi 50 %(b/v) ; 25 %(b/v) ; 12,5 %(b/v) ; 6,25 %(b/v) dan 3,125 %(b/v). b. Variabel tergantung : Diameter zona hambat, Rf.
c. Variabel terkendali : Waktu inkubasi (24 jam), suhu inkubasi (37 0C), jenis bakteri uji, volume suspensi bakteri uji yang di inokulasikan dalam media (50 µL), konsentrasi suspensi mikroba uji setara dengan larutan standar Mc. Farland II (6 x 108 CFU/mL), tempat tumbuh tanaman, suhu pengeringan ± 450C.
2. Definisi operasional
a. Aktivitas antimikroba adalah kemampuan fraksi petroleum eter, kloroform, etanol bunga pulu untuk menghambat atau membunuh mikroba uji Staphylococcus aureus ATCC 25923, Escherichia coli ATCC 32518, dan Candida albicans ATCC 10231.
b. Sampel bunga pulu adalah kumpulan bunga-bunga yang terkumpul dalam satu karangan atau satuan bunga yang menyusun bunga majemuk tanpa daun pelindung.
c. Zona hambat adalah zona jernih pada media agar yang telah ditanami bakteri uji, yang terbentuk disekitar lubang sumuran.
C.Bahan dan Alat Penelitian 1. Bahan
a. Bunga pulu (Carthamus tintorius L.) diperoleh dari petani (Bapak Mubarak) pada tanggal 15 Agustus 2012, Kabupaten Bone, Sulawesi Selatan.
b. Bakteri Staphylococcus aureus, Escherichia coli, dan Candida albicans diperoleh dari Laboratorium Mikrobiologi Balai Laboratorium Kesehatan Yogyakarta.
96% (Brataco®), Petroleum eter teknis (Brataco®), Ketoconazole (Indofarma®), Amoksisillin (Hexpharm Jaya®).
2. Alat
Alat-alat yang digunakan adalah alat-alat gelas, yaitu Erlenmeyer, tabung reaksi, corong, labu ukur, pipet tetes, pH meter, cawan petri, batang pengaduk, gelas ukur, sendok, pelubang sumuran, Platform Shaker (InnovaTM 2100), autoclave (Model
KT-40, ALP Co. Ltd Hamurasi Tokyo Japan), oven (memmert), rotary evaporator (Janke dan Kunkel, Ika-labotechnik, RV 05-ST), inkubator (Mammert tipe BE 400, GmbH + CoKG-D91126, Swahaban FRG Germany microbiological safety cabinet), neraca analitik (Scaltec Instruments Heiligen stadt Germany), densicheck (Vitek®), bunsen, jarum ose, flakon, tempat pengembangan (Chamber) KLT, mikrokapiler, penyangga lempeng kaca, kertas saring, lempeng kromatografi lapis tipis.
D.Tata Cara Penelitian 1. Determinasi bunga pulu
2. Pengumpulan bahan
Bunga pulu didapat dari Kabupaten Bone, Sulawesi Selatan. Bagian yang diambil adalah bagian dasar bunga hingga pucuk bunga. Bunga diambil pada sore hari, kemudian dicuci dengan air mengalir untuk menghilangkan pengotor kemudian ditiriskan untuk menghilangkan sisa-sisa air cucian.
3. Pengeringan dan pembuatan serbuk
Pengeringan dilakukan dengan memasukkan bunga ke dalam oven ± 3 hari dengan suhu 450C. Pengeringan dilakukan hingga bunga tersebut mudah dipatahkan. Daun diserbuk dengan menggunakan mesin penyerbuk, serbuk yang diperoleh, diayak dengan mengunakan pengayak no. 40 sehingga diperoleh serbuk dengan ukuran partikel yang homogen.
4. Ekstraksi bertingkat serbuk bunga pulu
dengan rotary evaporator dan dipekatkan diatas penangas air hingga didapatkan fraksi kental kloroform. Ampas II dimaserasi dengan etanol 96% kurang lebih 3 hari dengan shaker dan ditutup dengan alumunium foil. Saring dengan corong Buchner hingga didapat filtrat etanol dan ampas III (disisihkan). Filtrat etanol diuapkan dengan rotary evaporator dan dipekatkan di atas penangas air hingga didapatkan fraksi etanol.
5. Pengujian potensi antimikroba a. Penyiapan stok mikroba uji
Diambil dari kultur mikroba simpanan menggunakan jarum ose steril sebanyak 1 hingga 2 koloni tunggal. Diinokulasikan pada 5 mL Nutrien Agar miring dan diinkubasi selama 24 jam dan pada suhu 37 0C.
b. Pembuatan suspensi mikroba uji
Pembuatan suspensi mikroba dilakukan dengan mengambil 1-2 ose mikroba dari stok yang telah dibuat sebelumnya, diinokulasikan pada 5 mL media Nutrien Broth, suspensi tersebut diinkubasi selama 24 jam pada suhu 37 0C, kemudian divortex, diambil 1 mL suspensi tersebut ditambah NB dan disetarakan kekeruhannya dengan larutan standar Mc. Farland II (6 x108 CFU/mL)
menggunakan alat Densicheck.
c. Pembuatan variasi konsentrasi larutan uji
masing-masing dibuat dalam berbagai variasi konsentrasi 50 %(b/v) ; 25 %(b/v) ; 12,5 %(b/v) ; 6,25 %(b/v) dan 3,125 %(b/v).
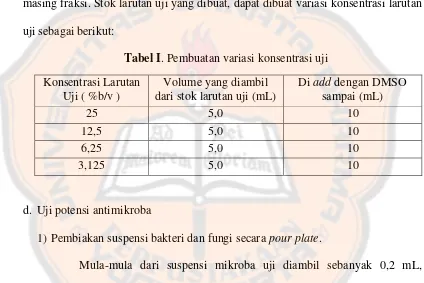
Pembuatan masing-masing fraksi dengan konsentrasi 50 % (stok larutan uji) dibuat dengan cara ekstrak kental (hasil penyarian) yang diperoleh ditimbang sejumlah 5 g yang kemudian dilarutkan ke dalam 10 mL DMSO untuk masing-masing fraksi. Stok larutan uji yang dibuat, dapat dibuat variasi konsentrasi larutan uji sebagai berikut:
Tabel I. Pembuatan variasi konsentrasi uji
d. Uji potensi antimikroba
1) Pembiakan suspensi bakteri dan fungi secara pour plate.
Mula-mula dari suspensi mikroba uji diambil sebanyak 0,2 mL, diinokulasikan kedalam 20 mL media NA dalam tabung reaksi dan divortex. NA yang telah bercampur dengan suspensi tersebut dituang kedalam petri steril kemudian digoyang-goyang dan biarkan memadat.
2) Uji potensi antimikroba dilakukan dengan metode difusi sumuran
Larutan uji dibuat variasi konsentrasi 50% (b/v); 25%(b/v); 12,5%(b/v); 6,25%(b/v) dan 3,125%(b/v). Setelah pembiakan suspensi bakteri secara pour
Konsentrasi Larutan Uji ( %b/v )
Volume yang diambil dari stok larutan uji (mL)
plate, dibuat sumuran dengan menggunakan pelubang sumuran no.4 (berdiameter 8 mm) sebanyak 7 sumuran. Tiap lubang sumuran masing-masing ditambal dengan 50 µL setelah memadat kemudian diisi 50 µL dengan fraksi petroleum eter, kloroform, dan etanol yang berkonsentrasi 50 %(b/v); 25 %(b/v); 12,5 %(b/v); 6,25 %(b/v) dan 3,125 %(b/v). Amoksisilin 0,0005 mg/mL sebagai kontrol positif untuk Staphylococcus aureus, Escherechia coli dan Ketoconazole 0,1 g/mL untuk Candida albicans. DMSO sebagai kontrol negatif dari fraksi petroleum, kloroform dan etanol. Petri-petri tersebut diinkubasi selama 24 jam pada suhu 37 0C kemudian diamati ada tidaknya zona hambat disekitar sumuran. Zona hambat yang terbentuk diukur dengan penggaris. Pada uji potensi antimikroba ini direplikasi sebanyak 3 kali untuk masing-masing fraksi.
e. Pengukuran KHM dengan metode dilusi padat
cawan petri dan diinkubasi selama 24 jam pada suhu 37 0C. Diamati banyak sedikit atau ada tidaknya pertumbuhan bakteri uji pada berbagai variasi konsentrasi dengan ditandai suatu notasi tertentu. Larutan uji untuk fraksi petroleum eter, kloroform, dan etanol dibuat masing-masing dengan cara yang sama.
6. Identifikasi kandungan senyawa bunga pulu dengan uji tabung. a. Uji pendahuluan
Dua gram serbuk bunga pulu dipanaskan dengan 10 mL air selama 30 menit diatas air mendidih. Larutan yang diperoleh disaring menggunakan kapas. Jika larutan menjadi berwarna kuning sampai merah dan bila pada saat penambahan KOH warna larutan menjadi lebih intensif berarti menunjukkan adanya senyawa yang mengandung kromofor dengan gugus hidrofilik.
b. Uji alkaloid
c. Uji tanin
Dua gram serbuk bunga pulu dipanaskan dengan 10 mL air selama 30 menit diatas penangas air. Disaring 5 mL filtrat ditambah 1 mL larutan NaCl 2%, bila terjadi suspensi atau endapan, disaring melalui kertas saring. Filtrat ditambah 5 mL larutan gelatin 1%. Bila terbentuk endapan berarti menunjukan adanya tanin atau zat samak.
d. Uji antrakinon
Tiga ratus mg serbuk bunga pulu didihkan 2 menit dengan 10 mL kalium hidroksida 0,5 N dan 1 mL larutan hidrogen peroksida. Setelah dingin suspensi disaring menggunakan kapas. Lima mL filtrat ditambah 10 tetes asam asetat sampai pH 5. Ditambahkan 10 mL toluene. Lima mL lapisan atas dipisahkan dengan dipipet dan dimasukkan dalam tabung reaksi. Ditambah kalium hidroksida 0,5 N, bila didapatkan warna merah pada lapisan air berarti menunjukan adanya senyawa antrakinon.
e. Uji polifenol
f. Uji saponin
Seratus mg serbuk bunga pulu ditambahkan 10 mL air suling kedalam tabung reaksi, ditutup dan dikocok kuat-kuat selama 30 detik. Tabung dibiarkan dalam posisi tegak selama 30 menit. Apabila terbentuk buih setinggi kurang lebih 3 cm dari permukaan cairan, maka menunjukan adanya saponin, uji lain dilakukan dengan menggunakan pipet kapiler (diameter 1 mm, panjang 12,5 cm). Larutan hasil pemanasan 2 g serbuk bunga pulu dengan 10 mL air dipanaskan selama 30 menit diatas penangas air. Setelah disaring filtrat dimasukkan kedalam pipa kapiler penuh-penuh. Kapiler diletakkan dalam posisi tegak (vertikal), lalu cairan dibiarkan mengalir bebas. Tinggi air suling yang diperlukan sama. Bila didapatkan tinggi cairan yang diuji setengah atau kurang dari tinggi air suling maka menunjukkan adanya saponin.
g. Uji minyak atsiri
Sebanyak 10 g serbuk ditambah 20 mL eter, dikocok kemudian disaring, filtrat yang didapat dikeringuapkan. Bila sedikit berbau aromatik, larutan residu ditambahkan dengan sedikit etanol, uapkan lagi sampai kering. Bila terjadi bau aromatik spesifik menunjukan adanya minyak atsiri.
h. Uji flavonoid
E. Kromatografi Lapis Tipis (Uji Penegasan Flavonoid)
Sejumlah 1 gram serbuk diekstrak menggunakan 10 mL metanol, dipanaskan diatas water bath (± 60 0C) disaring, kemudian filtrat ditotolkan sebanyak 25 - 30 µL pada plat KLT. Standar rutin dilarutkan dalam metanol 0,05% dan 10 µL ditotolkan pada plat KLT. Fase diam yang digunakan adalah selulosa dengan fase gerak n-butanol : asam asetat glasial : air ( 40:10:50) v/v. Spot dideteksi pada panjang gelombang 254 nm, 366 nm, dan pereaksi uap amonia.
F. Kromatografi Lapis Tipis (Uji Penegasan Minyak Atsiri)
Sejumlah 1 g serbuk diekstrak menggunakan 10 mL heksana, divortex selama 2 menit, kemudian disentrifugasi selama 3 menit. Standar terpenoid dan sampel ditotolkan sebanyak 10 µL pada plat KLT, fase diam yang digunakan adalah silika gel 60 F254 dengan fase gerak toluena : etil asetat (93:7) v/v. Spot dideteksi pada panjang
gelombang 254 nm, 366 nm, dan pereaksi vanillin asam sulfat.
G. Analisis Hasil
38 BAB IV
HASIL DAN PEMBAHASAN A.Determinasi Tanaman
Determinasi tanaman dilakukan di Laboratorium Botani Farmasi, Fakultas Farmasi, Universitas Sanata Dharma yang diidentifikasi menurut acuan Idtools (2003). Identifikasi tanaman ini bertujuan untuk memastikan bahwa tanaman yang digunakan adalah bunga pulu atau kasumba turate. Hasil determinasi menunjukkan bahwa bunga pulu yang digunakan dalam penelitian ini memiliki nama ilmiah Carthamus tinctorius L. dengan variasi daun dengan tepi berduri, warna bunga pada saat muda kuning – jingga (didominasi oleh jingga), dan warna bunga pada saat tua berwarna jingga.
B. Hasil Pengumpulan dan Pembersihan
Sampel berupa bunga pulu diambil dari daerah Soppeng, Sulawesi Selatan. Bunga yang diambil adalah bunga yang sudah tua yang berwarna merah karena diharapkan kandungan senyawa yang terkandung berada dalam jumlah yang maksimal. Waktu pengambilan dilakukan pada sore hari, dengan asumsi bahwa pada sore hari, hasil dari metabolisme suatu tanaman mencapai puncaknya, sehingga didapatkan hasil yang maksimal.
C.Hasil Pengeringan
tanaman dari pencemaran jamur, kapang, atau mikroba. Pengeringan juga berfungsi untuk menginaktifkan enzim-enzim dalam tumbuhan sehingga menekan terjadinya peruraian senyawa kimia dalam bunga atau herba oleh enzim-enzim tersebut. Pengeringan pada penelitian ini dilakukan dengan menggunakan oven pada suhu 45 0C sampai didapatkan herba yang dapat dihancurkan dengan tangan. Hasil pengeringan bunga tersebut berwarna jingga. Setelah kering dan dapat dihancurkan dengan tangan, bunga diserbuk dan diayak menggunakan pengayak dengan nomor mesh 40 untuk memperkecil ukuran partikel, sehingga proses penyarian lebih efektif dan optimal, dengan memperkecil ukuran partikel (dalam batas optimal) luas partikel yang kontak dengan pelarut semakin besar. Kandungan zat aktif yang didapatkan akan larut lebih cepat dan lebih banyak.
Tabel II. Hasil maserasi serbuk bunga pulu
Pelarut Volume filtrat Rendemen
Etanol 2100 mL 5,30 g
Kloroform 2100 mL 6,61 g
Petroleum eter 2100 mL 11,93 g
D.Hasil Penyarian Serbuk
Penyarian dilakukan dengan menggunakan pelarut petroleum eter, kloroform, dan etanol. Petroleum eter merupakan pelarut organik yang mampu menarik senyawa nonpolar. Penggunaan kloroform dimaksudkan untuk menarik senyawa yang bersifat non polar sampai semi polar. Etanol digunakan untuk menarik senyawa yang bersifat semi polar sampai polar, sehingga diharapkan zat aktif yang terkandung di dalam tanaman tersebut tersari maksimal sesuai dengan sifat polaritasnya.
Tabel III. Kepolaran relatif pelarut organik
Pelarut Formula Kepolaran Relatif
Petroleum eter C6H14 0,009
Kloroform CHCl3 0,259
Etanol C2H6O 0,654
Air H2O 1
(Murov, 2002).
Metode penyarian maserasi digunakan dalam penelitian ini karena tidak memerlukan pemanasan sehingga zat aktif yang terkandung di dalam bahan tidak mudah rusak. Selain itu, maserasi merupakan metode penyarian yang sederhana, mudah dikerjakan, menggunakan peralatan yang sederhana.
efisiensi dalam mengekstraksi dan untuk mencapai keseimbangan konsentrasi antara cairan di dalam sel dengan cairan di luar sel, dan untuk menarik zat-zat yang diperkirakan masih ada. Pengadukan dimaksudkan untuk meratakan konsentrasi di luar butir simplisia sehingga derajat perbedaan konsentrasi di dalam dan di luar sel tetap terjaga. Hasil maserasi (maserat) kemudian disaring dan diuapkan dengan menggunakan rotary evaporator, agar hasil maserat lebih pekat, maka harus diuapkan lagi di atas waterbath.
E.Uji Aktivitas Antimikroba Fraksi Petroleum Eter, Kloroform, Etanol Bunga Pulu (Carthamus tinctorius L.) terhadap Staphylococcus aureus,
Escherichia coli, dan Candida albicans dengan Metode Difusi
Pengujian aktivitas antimikroba dilakukan secara difusi menggunakan metode sumuran. Prinsip metode difusi yaitu senyawa uji ditempatkan dalam media padat yang sebelumnya telah diinokulasikan bakteri uji. Senyawa uji akan berdifusi ke dalam media dan menghambat pertumbuhan bakteri uji.
sampai pada konsentrasi 50%. DMSO digunakan sebagai kontrol pelarut bertujuan untuk mengetahui apakah pelarut yang digunakan memiliki pengaruh terhadap zona hambat yang terbentuk.
Dalam penelitian ini digunakan amoksisilin dan ketokonazol sebagai kontrol positif. Amoksisilin merupakan suatu antibiotik golongan beta laktam derivat penisilin dengan spektrum luas. Amoksisilin mempunyai aktivitas bakterisida terhadap bakteri Gram negatif maupun Gram positif dengan mekanisme menghambat pembentukan atau sintesis dinding sel mikroba (Todar, 2012). Ketokonazol merupakan turunan imidazol yang mempunyai aktivitas antifungi, turunan azol bekerja dengan menghambat sintesa ergosterol. Ergosterol adalah komponen lipid pada membran plasma fungi, sehingga permeabilitas membran meningkat, isi sitoplasma keluar, dan sel lisis (Hidayah, 2010). DMSO merupakan pelarut yang bersifat nonpolar tetapi diindikasikan tidak mempunyai daya hambat terhadap pertumbuhan bakteri.
Volume fraksi, kontrol positif, dan kontrol negatif yang dimasukkan dalam sumuran adalah 50 L. Setelah diinkubasi selama 24 jam, maka senyawa uji
Tabel IV. Diameter zona hambat fraksi petroleum eter bunga pulu (Carthamus tinctorius L.) terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans
Senyawa
Diameter zona hambat (mm) terhadap
Staphylococcus aureus Escherichia coli Candida albicans
I II III I II III I II III
Hasil yang diperoleh untuk fraksi petroleum eter terhadap Staphylococcus aureus, Escherechia coli, dan Candida albicans yaitu kontrol negatif tidak menunjukan zona hambat, kontrol positif menunjukan adanya zona jernih disekitar sumuran dengan rata-rata diameternya dari tiga replikasi yaitu 11,3 mm, 11,6 mm untuk amoksisilin dan 8,3 untuk ketokenazol. Hasil uji variasi konsentrasi fraksi tidak menunjukkan adanya zona hambat. Hal ini menunjukan tidak adanya penghambatan terhadap pertumbuhan bakteri uji yaitu Staphylococcus aureus, Escherechia coli, dan Candida albicans. Dalam penelitian ini fraksi tidak menunjukkan aktivitas antimikroba.
Tabel V. Diameter zona hambat fraksi kloroform bunga pulu (Carthamus tinctorius L.) terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans
Senyawa
Diameter zona hambat (mm) terhadap
Staphylococcus aureus Escherichia coli Candida albicans
Senyawa
Diameter zona hambat (mm) terhadap
Staphylococcus aureus Escherichia coli Candida albicans
I II III I II III I II III
Konsentrasi 6,25% 0 0 0 0 0 0 0 0 0
Konsentrasi 3,125% 0 0 0 0 0 0 0 0 0
Hasil yang diperoleh untuk fraksi kloroform terhadap Staphylococcus aureus, Escherechia coli, dan Candida albicans yaitu kontrol negatif tidak menunjukan zona hambat, kontrol positif menunjukan adanya zona jernih disekitar sumuran dengan rata-rata diameternya dari tiga replikasi yaitu 13 mm, 11,6 mm untuk amoksisilin dan 8,3 mm untuk ketokenazol. Hasil uji variasi konsentrasi fraksi tidak menunjukkan adanya zona hambat. Hal ini menunjukan tidak adanya penghambatan terhadap pertumbuhan bakteri uji yaitu Staphylococcus aureus, Escherechia coli, dan Candida albicans. Dalam penelitian ini fraksi tidak menunjukkan aktivitas antimikroba.
Tabel VI. Diameter zona hambat fraksi etanol bunga pulu (Carthamus tinctorius L.) terhadap Staphylococcus aureus, Escherichia coli, dan Candida albicans
Senyawa Diameter zona hambat (mm) terhadap
Staphylococcus aureus Escherichia coli Candida albicans
I II III I II III I II III
dengan rata-rata diameternya dari tiga replikasi yaitu 12,3 mm, 10,6 mm untuk amoksisilin dan 6,3 untuk ketokonazol. Hasil uji variasi konsentrasi fraksi tidak menunjukkan adanya zona hambat. Hal ini menunjukan tidak adanya penghambatan terhadap pertumbuhan bakteri uji yaitu Staphylococcus aureus, Escherechia coli, dan Candida albicans. Dalam penelitian ini fraksi tidak menunjukkan aktivitas antimikroba.
Analisis data keseluruhan menunjukkan bahwa variasi konsentrasi uji fraksi petroleum eter, kloroform, etanol bunga pulu (Carthamus tinctorius L.) hingga konsentrasi 50% tidak mempunyai kemampuan sebagai antimikroba terhadap Staphylococcus aureus, Escherechia coli, dan Candida albicans.
F. Skrining Fitokimia
1. Uji tabung
Uji tabung bertujuan untuk mengetahui kandungan kimia bunga pulu, yang kemudian dipertegas dengan KLT. Uji tabung meliputi uji pendahuluan, uji alkaloid, uji antrakinon, uji polifenol, uji tanin, uji saponin, dan uji minyak atsiri.
Tabel VII. Hasil pengamatan uji tabung terhadap serbuk bunga pulu
No Pengujian Pengamatan Hasil
1. Uji Pendahuluan
Filtrat + KOH 0,5 N Lapisan atas(air) bening
_ 4 Uji Polifenol
Filtrat + FeCl3 Larutan berwarna hijau biru +
5 Uji Tanin
Filtrat + NaCl 2% + Gelatin 1%
Tidak terdapat endapan _ 6 Uji Saponin
Pembentukan buih ≥3 cm
dari tinggi larutan Kurang dari 3 cm
_